А суставы болят при кори
Обновлено: 24.04.2024
В статье рассматриваются особенности течения суставных проявлений при хронических воспалительных заболеваниях кишечника, а также приводится клинический пример течения болезни Крона с дебютом с внекишечных проявлений в виде суставного синдрома.
Изучение хронических воспалительных заболеваний кишечника (ХВЗК) является актуальной проблемой не только детской гастроэнтерологии, но и детской ревматологии вследствие частого дебюта этих патологических состояний именно с суставных проявлений и дальнейшего течения клинически взаимосвязанных кишечного и суставного синдромов.
Распространенность ХВЗК среди детского населения составляет 2,2–6,8 на 100 тыс. детей [1, 2]. С наибольшей частотой в детском возрасте диагностируются такие заболевания этой группы, как болезнь Крона и язвенный колит. Отмечено, что язвенный колит чаще встречается у мальчиков, а болезнь Крона — у мальчиков и девочек с примерно с одинаковой частотой [2].
Болезнь Крона (регионарный энтерит, гранулематозный илеит) — воспалительное заболевание с вовлечением в процесс всех слоев кишечной стенки; характеризуется прерывистым (сегментарным) характером поражения различных разделов желудочно-кишечного тракта. Для него характерна диарея с примесью слизи и крови, боли в животе (часто в правой подвздошной области), потеря массы тела, лихорадка.
Язвенный колит (неспецифический язвенный колит, идиопатический колит) — язвенно-деструктивное поражение слизистой оболочки толстой кишки, которое локализуется преимущественно в ее дистальных отделах. В клинической картине характерны: кровотечения из прямой кишки, учащенное опорожнение кишечника, тенезмы; боли в животе менее интенсивны, чем при болезни Крона, локализуются чаще всего в левой подвздошной области. Примерно у 30% пациентов юношеского возраста язвенный колит начинается внезапно с появления болей в животе и диареи с примесью крови.
По данных разных авторов, внекишечные проявления ХВЗК отмечаются в 5–25% случаев. Наибольшая их доля приходится на тотальные формы неспецифического язвенного колита (87,5%) и болезни Крона с вовлечением в процесс толстой (29%) или толстой и тонкой кишки (58,1%) [3]. Системные проявления ХВЗК по патогенетическому принципу разделяют на три группы. К первой группе относят проявления, возникающие вследствие системной гиперсенсибилизации, — поражения суставов, глаз, кожи, слизистой оболочки рта; ко второй — обусловленные бактериемией и антигенемией в портальной системе — поражения печени и билиарного тракта. Выделяют также явления, развивающиеся вторично при длительно существующих нарушениях в толстой кишке, — анемии, электролитные расстройства.
Патогенез суставных проявлений остается неясным. Обсуждается значение повышенной проницаемости стенки кишечника, отмечающейся у больных язвенным колитом и болезнью Крона, в результате чего в кровь в большом количестве попадают компоненты оболочки стенок бактерий. Эти компоненты выступают в качестве пептидных антигенов, способных приводить к развитию артритов. Связываясь с молекулами комплексов гистосовместимости и активируя в дальнейшем Т-лимфоциты, пептиды приводят к возникновению воспаления суставов [3].
С точки зрения ревматолога суставные проявления ХВЗК относят к т. н. серонегативным спондилоартропатиям. Это большая гетерогенная группа клинически пересекающихся, хронических воспалительных ревматических заболеваний [4]. Помимо артритов, связанных с воспалительными заболеваниями кишечника, в эту группу включают такие ревматические заболевания детского возраста, как ювенильный спондилоартрит, ювенильный реактивный артрит, ювенильный псориатический артрит, а также недифференцированные спондилоартропатии (дактилит, увеит, сакроилеит в отсутствии полного набора критериев). Несмотря на гетерогенность заболеваний данной группы, клинически серонегативные спондилоартропатии имеют общие признаки и характеризуются:
- патологическими изменениями в крестцово-подвздошном отделе и/или других суставах позвоночника;
- синдромом периферической воспалительной артропатии, проявляющейся асимметричным артритом преимущественно нижних конечностей;
- энтезопатическим синдромом;
- ассоциацией с антигеном гистосовместимости HLA-B27;
- тенденцией к накоплению этих заболеваний в семьях;
- частым наличием внесуставных симптомов (поражение глаз, клапанов аорты, кожи) [5, 6]. В МКБ-10 поражения суставов при рассматриваемых нами заболеваниях кодируются следующим образом: М07.4 Артропатия при болезни Крона (К50); М07.5 Артропатия при язвенном колите (К51).
Поражения суставов при ХВЗК встречаются в 20–40% случаев и протекают в виде артритов (периферической артропатии), сакроилеита и/или анкилозирующего спондилита [3].
Артриты
Артриты относятся к наиболее частым суставным проявлениям хронических воспалительных заболеваний кишечника. Нередко они сочетаются с поражением кожи в виде узловатой эритемы. Частота возникновения артритов, распространенность поражения толстой кишки коррелируют с воспалительной активностью основного заболевания. В некоторых случаях артриты могут предшествовать кишечным проявлениям за много месяцев и даже лет, а также сохраняться в фазу ремиссии [7].
Клиническая картина артритов при болезни Крона и язвенном колите идентична. Характерно ассиметричное, мигрирующее поражение суставов чаще нижних конечностей. Преимущественно страдают коленные и голеностопные суставы, далее следуют локтевые, тазобедренные, межфаланговые и плюснефаланговые суставы. Число пораженных суставов обычно не превышает пяти. Суставной синдром течет с чередованием периодов обострений, длительность которых не превышает 3–4 месяцев, и ремиссий. Могут выявляться энтезопатии, талалгии. Артриты, как правило, начинаются остро. Однако нередко больные предъявляют жалобы только на артралгии, и при объективном обследовании изменения не обнаруживаются. Со временем обострения артритов становятся реже. У большинства больных артриты не приводят к деформации или деструкции суставов.
Выделяют два типа поражения периферических суставов. Для первого характерно поражение небольшого количества крупных суставов, ассиметричность суставного синдрома, острое течение. Часто при этом типе суставной синдром предшествует клинической картине основного заболевания, ассоциируется с его обострениями и сочетается с другими внекишечными проявлениями ХВЗК. Второй тип протекает по типу симметричного полиартрита, его обострения не совпадают по времени с обострениями основного процесса в кишечнике и другими системными проявлениями заболевания [7, 8].
Проведение колэктомии у больных язвенным колитом способствует прекращению рецидивирующих артритов [3].
Сакроилеит
По данным рентгенологического исследования, сакроилеит обнаруживается примерно у 50% больных ХВЗК. При этом у 90% он имеет бессимптомное течение. Он не ассоциируется с повышенной частотой выявления у больных HLA-B27. Также наличие сакроилеита не коррелирует с активностью воспалительного заболевания кишечника. Существуя на протяжении нескольких лет, может быть предшественником язвенного колита или болезни Крона. Сакроилеит может быть единственной локализацией изменений со стороны суставов, но часто сочетается с первым типом течения артритов. Необходимо помнить, что сакроилеит может быть ранним симптомом анкилозирующего спондилита. Терапия кишечного синдрома не приводит к изменению клинической картины сакроилеита [7].
Анкилозирующий спондилит
Анкилозирующий спондилит (АС) при ХВЗК клинически, как и сакроилеит, не отличается от идиопатического анкилозирующего спондилита. Чаще встречается у лиц мужского пола. По наблюдениям, у лиц женского пола поражение шейного отдела позвоночника манифестирует в более молодом возрасте и протекает тяжелее. Симптомы АС обычно предшествуют манифестации болезни Крона или язвенного колита и не коррелируют с активностью воспаления в кишечнике. Отмечаются боли в позвоночнике, чувство утренней скованности, нарастает ограничение подвижности в шейном, грудном, поясничном отделах позвоночника. Активная терапия основного заболевания не приводит к изменению клинической картины спондилита [3, 7, 9, 10].
Клиническое наблюдение
Иллюстрацией к вышеизложенному материалу может служить клиническое наблюдение за течением болезни Крона с внекишечными суставными проявлениями у пациента подросткового возраста.
Клинический диагноз: болезнь Крона (поражение тонкого, толстого кишечника, желудка, пищевода), фаза ремиссии, внекишечные проявления (лихорадка в анамнезе, лимфаденопатия, гепатомегалия, железодефицитная анемия). Осложнения: стеноз устья баугиниевой заслонки, сужение входа в слепую кишку.
Ювенильный спондилоартрит, активность I степени, рентгенологическая стадия I–II, НФ-1.
Из анамнеза жизни следует отметить, что мальчик от 2-й беременности, протекавшей физиологически, от первых срочных родов, осложнившихся слабостью родовой деятельности (акушерское пособие — наложение проходных щипцов). Находился на раннем искусственном вскармливании. На первом году жизни наблюдался неврологом. В дальнейшем редкие ОРВИ. Привит по календарю. Детскими инфекциями не болел. Наследственность отягощена по заболеваниям сердечно-сосудистой системы.
Анамнез заболевания: в сентябре 2008 г. после травмы левого голеностопного суставе у ребенка отмечался отек и болезненность в левом голеностопном сустава. Получал местно мази с нестероидными противовоспалительными препаратами (НПВП). Также применялось физиотерапевтическое лечение, что вызвало ухудшение состояния: появилась субфебрильная лихорадка, усилились артралгии в левом голеностопном суставе, также появилась болезненность в височно-нижнечелюстных суставах с ограничением подвижности в них. За три месяца мальчик похудел на 12 кг. Обследован по месту жительства: в анализе крови скорость оседания эритроцитов (СОЭ) 47–55 мм/ч, лейкоцитоз, в биохимическом анализе повышение аспартатаминотрансферазы (АСТ) до 2 норм, С-реативный белок (СРБ)++. Выявлена кишечная инфекция: титр к S. flexneri 1:400. Проводимая терапия (НПВП, антибиотики — цефазолин, цефтриаксон, амикацин) эффекта не дала. На фоне приема антибиотиков появился неустойчивый, разжиженный стул, боли в околопупочной области. В НИИ фтизиатрии исключен туберкулез. При компьютерной томографии левого голеностопного сустава выявлено: сужение суставной щели, краевая узура в медиальной лодыжке, выпот в полость сустава. Исключена ортопедическая патология. С января 2009 г. наблюдается в Университетской детской клинической больнице (УДКБ) Первого МГМУ им. И. М. Сеченова. При поступлении состояние средней степени тяжести. Бледен, выражены симптомы интоксикации. Дистрофия. Суставной синдром в виде выпота, ограничения подвижности, повышения местной температуры и болезненности в левом голеностопном суставе, ахиллобурсит слева, умеренная атрофия мышц левой голени, походка нарушена. Ригидность грудного отдела позвоночника (+ 1 см), ограничение подвижности в височно-нижнечелюстных суставах. Отмечаются боли в животе, разжиженный стул. Высокая гуморальная активность: СОЭ до 50 мм/ч, лейкоцитоз до 22 000 в 1 мкл с палочкоядерным сдвигом до 24%, анемия — гемоглобин (Hb) 109 г/л, однократно повышения уровней АСТ и аланинаминотрансферазы (АЛТ) до 1,5–2 норм. Обследован на артритогенные инфекции: результат отрицателен. При иммуногенетическом обследование выявлены HLA 1-го класс: А2, В 64 (14), В38 (16). Ребенку выставлен предварительный диагноз: ювенильный спондилоартрит. Использовали пульс-терапию глюкокортикоидами, введение внутривенного иммуноглобулина, НПВП, проведена внутрисуставная пункция левого голеностопного сустава с введением Депо-медрола. В качестве базисного препарата ребенку назначен сульфасалазин 1500 мг/сутки. На фоне проводимой терапии отмечалась положительная динамика, несколько снизилась лабораторная активность, купированы боли в животе, нормализовался стул, возрос объем движений в левом голеностопном суставе, однако сохранялась отечность и утренняя скованность в нем. В марте 2009 г. вновь обострение суставного синдрома, лихорадка до 37,8 °C, боли в животе, неустойчивый стул, появилась отечность правого голеностопного сустава. Ребенок вновь госпитализирован в УДКБ в мае-июне 2009 г.: СОЭ 29 мм/ч, гипохромная анемия, тромбоцитоз, СРБ ++, IgG 2150 мг/дл, в копрограмме эритроциты до 40 в поле зрения однократно. Выполнена ректороманоскопия: сигмоидит, проктит, эндоскопические признаки колита. На эзофагогастродуоденоскопии: эрозивный гастрит, дуоденит, еюнит. Рекомендовано проведение колоноскопии, от проведения которой родители ребенка отказались. Мальчику была повышена доза сульфасалазина до 1750 мг/сутки. Но состояние пациента оставалось нестабильным: сохранялись неустойчивый стул, отечность, болезненность и нарушение функции левого голеностопного сустава. В октябре 2009 г. вновь госпитализирован в УДКБ: СОЭ 34 мм/ч, наросла гипохромная анемия Hb 90 г/л, тромбоцитоз, лейкоцитоз до 16 тыс. в 1 мкл, СРБ ++. Ребенку проведена колоноскопия: болезнь Крона, глубокие язвы в ободочной кишке, язвенный терминальный илеит, проктит, колит, сигмоидит. По данным магнитно-резонасной томографии илеосакральных сочленений — левосторонний сакроилеит. Мальчику проводилась коррекция терапии: сульфасалазин отменен, назначен Салофальк 2000 мг/сутки, продолжал получать НПВП. На фоне терапии состояние с положительным эффектом — купирован кишечный синдром, нормализовался стул. Однако в декабре 2009 г. после ОРВИ вновь обострение основного заболевания: повышение температуры до фебрильных цифр, СОЭ 50 мм/ч, отек голеностопных суставов, скованность в них. С конца декабря 2009 г. отмечаются схваткообразные боли в животе, разжиженный стул. В январе 2010 г. в связи с высокой лабораторной и клинической активностью основного заболевания, неэффективностью традиционной терапии (монотерапии Салофальком), прогрессирующей инвалидизацией пациента начата терапия инфликсимабом. 3.02.2010 г. проведено первое введение, на фоне которого отмечена выраженная положительная динамика, купирован кишечный синдром, возрос объем движений в голеностопных суставах, уменьшилась экссудация в них, снизилась активность лабораторных показателей. 17.02.2010 и 17.03.2010 проведены второе и третье внутривенное введение Ремикейда по 100 мг на 1 введение. На фоне лечения отчетливая положительная динамика, полностью купирован кишечный синдром, прибавил в весе 7 кг, однако сохранялось снижение Hb до 87 г/л. При госпитализации в мае-июле 2010 г. СОЭ 23 мм/ч, Hb 91 г/л. При повторной колоноскопии выявлено сужение поперечной ободочной кишки, не проходимое для эндоскопа. Проведена ирригоскопия: слепая, восходящая, 1/2 поперечной кишок деформированы, с выраженным спазмом, с постстенотическим расширением поперечной и нисходящей ободочной кишки. Продолжилась терапия инфликсимабом, с учетом увеличения веса пациента доза повышена. Всего мальчик получил 24 введений инфликсимаба. Состояние его полностью стабилизировалось. Он поправился на 22 кг, вырос на 25 см. Полностью купированы кишечный и суставные синдромы. Полностью нормализовались лабораторные показатели СОЭ 5–14 мм/час. Hb 151 г/л. Мальчик ведет активный образ жизни.
Литература
- Яблокова Е. А. Клинические особенности и нарушение минерализации костной ткани у детей с воспалительными заболеваниями кишечника. Дисс. канд. мед. наук. М., 2006. 185 с.
- Tourtelier Y., Dabadie A., Tron I., Alexandre J. L., Robaskiewicz M., Cruchant E., Seyrig J. A., Heresbach D., Bretagne J. F. Incidence of inflammatory bowel disease in children in Britani (1994 –1997). Breton association of study and research on digestive system diseases (Abermad) // Arch Pediatr. 2000 Apr; 7 (4): 377–384.
- Гвидо Адлер. Болезнь Крона и язвенный колит. М.: ГЭОТАР-МЕД, 2001.
- Шостак Н. А., Правдюк Н. Г., Абельдяев Д. В. Серонегативные спондилоартропатии — совершенствование подходов к ранней диагностике и лечению // РМЖ. 2013, № 6, 1002–1008.
- Справочник по ревматологии / Хаким А., Клуни Г., Хак И.; пер. с англ. Н. И. Татаркиной. М.: ГЭОТАР-Медиа, 2010. 560 с.
- Dougados M., Hermann K. G., Landewe R. et al. Assess spondyloarthritis to international Society (ASAS) handbook: a guide The Assessment of spondyloArthritis // Ann Rheum Dis. 2009. Vol. 68. Р. 1–44.
- Ревматология. Национальное руководство под ред. Е. Л. Насонова, В. А. Насоновой. М.: ГЭОТАР-Медиа, 2008. 720 с.
- D’Incà R., Podswiadek M., Ferronato A., Punzi L., Salvagnini M., Sturniolo G. C. Articular manifestation in inflammatory bowel disease patients. A prospective study // Dig Liver Dis. 2009, Mar 9.
- Rodriguez V. E., Costas P. J., Vazquez M., Alvarez G., Perez-Kraft G., Climent C., Nazario C. M. Prevalence of spondyloarthropathy in Puerto Rican patients with inflammatory bowel disease/Ethn Dis. 2008, Spring; 18 (2 Suppl 2): S2–225–9.
- Руководство по детской ревматологии / под ред. Н. А. Геппе, Н. С. Подчерняевой, Г. А. Лыскиной. М.: ГЕОТАР-Медиа, 2012. 720 с.
А. В. Мелешкина 1 , кандидат медицинских наук
С. Н. Чебышева, кандидат медицинских наук
Е. С. Жолобова, доктор медицинских наук, профессор
М. Н. Николаева
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
Abstract. The article covers specifics of development of articular manifestations under chronic inflammatory bowel diseases and provides clinical example of crohn’s disease development starting with un-bowel manifestations in forn of articular syndrome.
Что такое корь? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Корь (Measles) — острое инфекционное заболевание, вызываемое вирусом кори, который поражает эпителий верхних дыхательных путей и кожные покровы. Клинически характеризуется выраженным синдромом общей инфекционной интоксикации, патогномоничной энантемой, макуло-папулёзной сыпью, конъюнктивитом и синдромом поражения респираторного тракта (дыхательных путей).
Этиология
вид — возбудитель кори (Polinosa morbillarum)
Синдромально заболевание было описано в 1890 году доктором Бельским (Псков), в 1895 году детским доктором Филатовым и в 1898 году доктором Копликом (США).
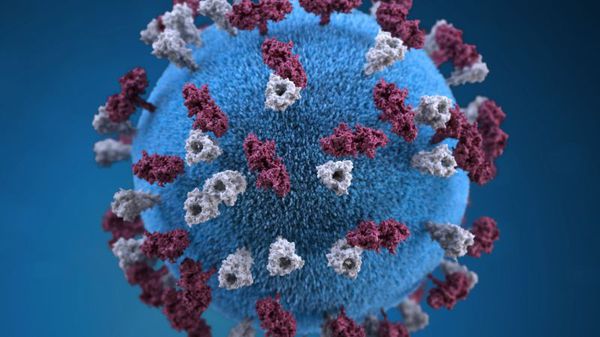
Оболочка вируса имеет 3 слоя: белковую мембрану, липидный слой и наружные гликопротеидные комплексы, образующие своеобразные выступы. Штаммы вирусов идентичны в антигенном отношении, обладают комплементсвязывающими, гемагглютинирующими, гемолизирующими свойствами и симпластообразующей активностью. СД-46 является рецептором у человека к вирусу кори.
Вирус неустойчив во внешней среде – чувствителен к ультрафиолету, в каплях слюны погибает за 30 минут, при высыхании и действии дезинфицирующих средств — мгновенно. Хорошо переносит пониженные температуры. Вирус можно выделить из различных сред организма (кровь, моча, кал, смывы со слизистых ротоглотки, конъюнктив, цереброспинальной жидкости). [2] [5]
Эпидемиология
Антропоноз. Источник заболевания – исключительно заражённый человек, также с атипичной формой заболевания кори. Инфицированный заразен с последних 2-х дней инкубации и до 4-го дня с момента появления высыпаний включительно — с 5 дня заразность пропадает.
Передача заболевания
Механизм передачи: воздушно-капельный (путь аэрозольный), редко трансплацентарный (при заболевании женщины в конце беременности). Теоретически возможно заражение от недавно привитых (но на практике такое случается чрезвычайно редко).
Существует весенне-зимняя сезонность. После перенесённой инфекции, полного курса вакцинации развивается стойкий пожизненный иммунитет.
Корь — одна из основных причин смерти среди детей раннего возраста.
В 2015 году в глобальных масштабах произошло 134 200 случаев смерти от кори. [1] [3]
Кто подвергается риску
Заразиться корью может любой человек, не имеющий иммунитета — тот, кто не был вакцинирован или тот, у кого не выработался иммунитет после вакцинации.
Самому высокому риску заболевания корью и развития осложнений, включая смертельный исход, подвергаются невакцинированные дети раннего возраста. Корь — одна из основных причин смерти среди них.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы кори
Инкубационный период
Инкубационный период при типичной форме — от 9 до 11 суток (в некоторых случая до 13).
Симптомы кори у взрослых
Начало заболевания подострое (т.е. основной синдром появляется на 2-3 сутки от начала заболевания), однако при должной подготовке врача (выявлении патогномоничной энантемы — сыпи на слизистых оболочках) можно определить острое начало (в течении первых суток). Во взрослом возрасте из-за особенностей иммунной системы эти критерии могут не соблюдаться.
- синдром выраженной общей инфекционной интоксикации;
- синдром патогномоничной энантемы (пятна Бельского-Филатова-Коплика);
- синдром макуло-папулёзной экзантемы;
- синдром конъюнктивита (выраженный);
- синдром поражения респираторного тракта (фарингит, трахеобронхит);
- синдром генерализованной лимфаденопатии (ГЛАП);
- гепатолиенальный синдром.
Описана так называемая ранняя диагностика кори, включающая:
- затруднение носового дыхания;
- покраснение правого века;
- субфебрилитет (лихорадка постоянного типа).
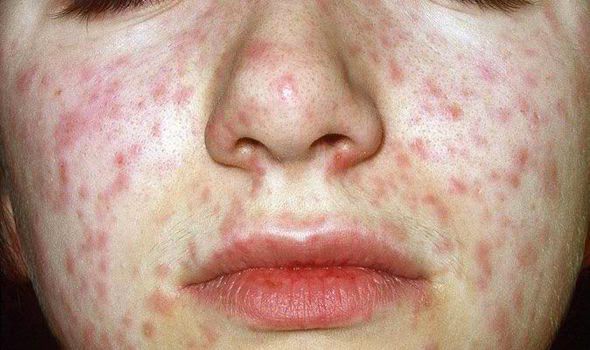
Объективно: можно отметить возникновение макуло-папулёзной сыпи, появляющейся в типичных случаях на 3-4 день болезни, с выраженной этапностью (лицо, шея; после туловище, руки, бёдра; затем олени и стопы, а на лице в этот момент бледнеет). Высыпания представляют собой папулы, окруженные красным пятном, предрасположенные к слиянию (но при наличии чистых участков), иногда появляются петехии. Спустя 3-4 дня сыпь становятся бледной и оставляет после себя бурые пятна и отрубевидное шелушение. Увеличиваются и приобретают чувствительность периферические лимфоузлы (затылочные, заднешейные и подмышечные). Ярко выражен конъюнктивит (конъюнктивы масштабно гиперемированы, отёчны, быстро присоединяется гнойное отделяемое). Характерным является вид больного: одутловатое лицо, красные (как у кролика) глаза, отёчность носа и век, сухие потрескавшиеся губы. При аускультации в лёгких прослушиваются сухие хрипы. Выражена тахикардия, снижение артериального давления. Увеличиваются размеры печени и селезёнки (генерализация инфекции).
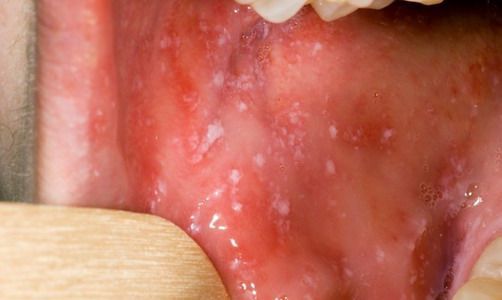
При фарингоскопии в ротоглотке визуализируется гиперемия мягкого нёба, на слизистой поверхности щёк в начале заболевания пятна Бельского — Филатова — Коплика (мелкие белесоватые пятнышки с узкой красноватой каёмкой), которые пропадают при появлении экзантемы. Иногда появляется пятнистая энантема на слизистой мягкого нёба.
Описана митигированная корь (у людей, получивших специфический противокоревой иммуноглобулин в период инкубации), характеризующаяся удлинением инкубационного периода до 21 дня, лёгким течением.
При абортивной форме заболевания характерно типичное начало, но спустя 1-2 суток клинические проявления исчезают.
Существует понятие — реакция на прививку (при первичном введении живой противокоревой вакцины), характеризующееся повышением температуры тела, катаральными явлениями (воспалениями) со стороны верхних дыхательных путей, скудной малозаметной сыпью (чаще развивается у детей и лиц с иммунодефицитом).
У больных с наличием тяжелого иммунодефицита – СПИДа (ВИЧ, онкологические больные, лица, получающие системные цитостатики после трансплантации органов) — течение заболевания крайне тяжёлое (летальность до 80%). [4] [5]
В статье представлены современные сведения о кори — эпидемиология заболевания, краткие данные о патогенезе, клинике и тактике ведения больного. Представлен клинический пример кори с осложнением у взрослого из семейного очага. В статье отражены современны
Features of the course of measles in adults I. A. Ivanova, Zh. B. Ponezheva, M. S. Kozlova, E. T. Vdovina, N. A. Tsvetkova
The article presents a modern understanding of measles — the epidemiology of the disease, brief data on the tactics of treatment of pathogenesis, clinic and patient management. A clinical example of measles in an adult is presented. The article reflects the modern approaches to the diagnosis and prevention of this highly contagious infection.
Корь — высококонтагиозная антропонозная вирусная инфекция с аспирационным механизмом передачи возбудителя. Характеризуется лихорадочным, интоксикационным и экзантемным синдромами, наличием катаральных явлений, энантемы и нередко протекает с первичными и/или вторичными осложнениями. Возбудителем кори является РНК-геномный вирус, относящийся к семейству парамиксовирусов. Возбудитель нестойкий в окружающей среде, но он может сохраняться живым в течение нескольких часов в аэрозолях. По своей эпидемиологии корь является типичной капельной инфекцией. Источником инфекции служат больные люди. Наибольшую опасность в плане передачи инфекции представляют пациенты в катаральном периоде (в среднем за 4 дня до появления высыпаний и до 5-го дня от появления сыпи). Инкубационный период при кори составляет чаще всего 10–14 дней.
Одной из самых опасных вирусных инфекций для взрослых является корь, индекс контагиозности (заболеваемость после контакта с возбудителем) которой равен 90–95%, и заболевание переносится взрослыми значительно тяжелее, чем детьми. В начале кори доминирует поражение клеток эпителия дыхательных путей с развитием соответствующих клинических проявлений. Вирус кори, находясь в слизистой оболочке верхних дыхательных путей и в носоглоточной слизи, выделяется из организма при кашле, чихании, разговоре и даже дыхании в форме мельчайших капелек аэрозоля. Симптомы кори проявляются не сразу после заражения. Классическое клиническое течение кори разделяется на периоды: инкубационный (от 7 до 21 дня), катаральный (появляются первые симптомы кори: повышается температура тела, кашель, насморк) и периоды высыпаний, пигментации и выздоровления (реконвалесценции) [3].
Первыми проявлениями кори (продромальная стадия) являются неспецифические симптомы: лихорадка, кашель, насморк, конъюнктивит. В конце продромального периода на слизистой щек появляются пятна Бельского–Филатова–Коплика, являющиеся специфичными для кори. Они имеют вид серо-белых крупинок, окруженных гиперемией, расположенных на уровне вторых моляров. Эти элементы сыпи сохраняются в течение нескольких дней, они начинают исчезать при появлении высыпаний на коже. Для высыпаний при кори характерна этапность: сначала сыпь появляется на лице, за ушами, на волосистой части головы, затем переходит на туловище и руки, после чего распространяется на ноги. Морфологически высыпания имеют эритематозный, пятнисто-папулезный вид. Сыпь сохраняется до 5 дней, затем она угасает, оставляя после себя пигментации, исчезающие в течение 2–3 недель. Одновременно с пигментацией появляется отрубевидное шелушение, наиболее выраженное на лице и туловище.
Корь может иметь типичные или атипичные проявления. К атипичным относят:
- Стертую форму.В этом случае заболевание проходит в очень легкой форме, без выраженных специфических клинических проявлений. Пациенты отмечают небольшое повышение температуры тела, симптомы простуды (першение в горле, кашель, слабость). Иногда стертая форма заболевания возникает после прививки от кори или введения гамма-глобулина.
- Геморрагическую форму, когда заболевание сопровождается множественными кровоизлияниями на кожных покровах, примесью крови в моче и стуле. Вследствие геморрагической формы нередко случается летальный исход из-за большой потери крови. При своевременной госпитализации в стационар и правильном лечении прогноз заболевания благоприятный.
- Гипертоксическую форму, которая возникает на фоне выраженной интоксикации организма и проявляется температурой до 40 °C и выше, симптомами менингоэнцефалита, сердечной и дыхательной недостаточности [3].
Атипичные проявления у взрослых встречаются чаще. Течение кори у взрослых имеет свои особенности: более выражен интоксикационный синдром (слабость, потливость, сонливость, заторможенность); из катаральных явлений (заложенность носа, явления конъюнктивита, кашель, першение и дискомфорт в горле) преобладает чаще сухой кашель и имеет место нарушение этапности высыпаний.
Корь у взрослых диагностируется на основании характерной симптоматики и результатов лабораторных исследований. По клиническим рекомендациям для лабораторной диагностики инфекции используются серологический и молекулярно-биологический методы. Исследование крови проводится иммуноферментным анализом (ИФА), и для определения антител (IgM, IgG) к вирусу кори кровь берется на 5-й день от начала высыпаний [4]. Для идентификации и определения типа вируса используется метод полимеразной цепной реакции (ПЦР). Для проведения исследования забор материала (носоглоточные смывы, моча, ликвор) производится на 1–3 день с момента высыпаний. В некоторых случаях используют особые вирусологические диагностические методы (микроскопия вируса, реакция иммунофлуоресценции).
Общий анализ крови при кори характеризуется уменьшением количества лейкоцитов, повышением показателя скорости оседания эритроцитов. Если присоединяется вторичная бактериальная инфекция, то в результатах исследования отмечают нейтрофильный лейкоцитоз. Рекомендуется выполнить также биохимический анализ крови и общий анализ мочи: они помогут определить наличие и степень тяжести поражения печени и мочевыделительной системы. При ведении пациента с корью обязателен контроль клинических и биохимических анализов крови в динамике. По необходимости проводится дополнительная диагностика — анализ спинномозговой жидкости, рентгенография и компьютерная томография органов грудной клетки, электрокардиография (ЭКГ), консультации ЛОР-врача, невролога и других специалистов по показаниям.
Особенностью взаимодействия вируса кори и иммунной системы организма человека является развитие транзиторного вторичного иммунодефицита [5], что предполагает высокий риск возникновения тяжелых осложнений (бактериальной и/или вирусной этиологии), которые могут носить деструктивный характер. Чаще возникают острые и хронические заболевания ЛОР-органов, наиболее частым из которых является средний отит, встречающийся у 7–9% заболевших; поражения пищеварительной системы (энтероколит, диарея, гепатит, панкреатит) и мочевыделительной системы (пиелонефрит, цистит, гломерулонефрит), а также заболевания центральной нервной системы, чаще протекающие в виде острых инфекционных и постинфекционных энцефалитов с частотой 0,01–0,02%. Наблюдаются осложнения в виде инфекционной патологии нижних дыхательных путей, где пневмонии имеют место у 1–6% пациентов и могут быть как вирусной, так и бактериальной этиологии. Такие симптомы, как постоянная немотивированная слабость, головные боли, наличие сухого кашля, изменения аускультативной картины, длительная лихорадка и повторное повышение температуры позволяют насторожиться в отношении наличия воспаления легких. Объективную картину дает компьютерная томография органов грудной клетки, также следует проводить бактериологическое исследование мокроты (при наличии влажного кашля, с правильным и корректным сбором биоматериала), ПЦР-исследование на респираторные вирусы и бактерии для уточнения этиологии.
Специфического лечения кори не существует, поэтому терапия этого инфекционного заболевания направлена на облегчение состояния больного и борьбу с вторичными инфекциями, осложнениями. Пациенту назначают жаропонижающие лекарственные препараты для снижения температуры, устранения симптомов интоксикации и воспаления. Для этиотропной терапии рекомендуется применять интерфероны (интерферон-альфа) и иммуноглобулин человека нормальный при тяжелых формах инфекции. Для дезинтоксикационной терапии при среднетяжелых и тяжелых формах показаны растворы электролитов, для легкого течения используется оральная регидратация. Симптоматическая терапия направлена на купирование симптомов (деконгестанты, противокашлевые и отхаркивающие средства, жаропонижающие средства, антигистаминная терапия). При развитии осложнений проводится терапия, направленная на их предотвращение, в т. ч. антибактериальная терапия [6]. Такие группы антимикробных препаратов, как макролиды и фторхинолоны III и IV поколений, являются предпочтительными в отношении пневмоний, вызванных микоплазменной и хламидийной инфекциями, в то время как бактериальные пневмонии (стрептококковая, стафилококковая и др.) при кори успешно поддаются лечению бета-лактамными антибиотиками [6, 7].
Больной заболел 16.01.18, когда началось повышение температуры тела до 40 °С. Больной отрицал катаральные симптомы. Принимал жаропонижающие препараты, проводил симптоматическую терапию, название препаратов не помнил. В течение двух дней лихорадка сохранялась, эффекта от приема лекарств не было. 18.10.18 вызвал бригаду СМП, госпитализирован в ГБУЗ ИКБ № 2.
При поступлении пациент в состоянии средней тяжести, лихорадил до 40 °С, по данным объективного осмотра кожные покровы физиологической окраски, влажные, на ощупь горячие, чистые, сыпь отсутствовала. Склеры не инъецированы. Слизистая оболочка ротовой полости не гиперемирована. Миндалины не гиперемированы, не увеличены, без наложений. Язык чистый, влажный. Пальпировались мелкие шейные лимфатические узлы, до 1 см, эластичные, безболезненные при пальпации. Носовое дыхание свободное. В легких дыхание жесткое, проводится во все отделы, хрипы не выслушивались. Тоны сердца ясные, ритмичные, частота сердечных сокращений и пульс составляли 78 ударов в минуту. Артериальное давление 100/60 мм рт. ст. Живот при пальпации мягкий, безболезненный во всех отделах, печень и селезенка не увеличены. Симптом Щеткина–Блюмберга отрицательный. Мочеиспускание свободное, безболезненное, цвет мочи желтый, диурез достаточный. Стул регулярный, оформленный, без патологических примесей. Грубая менингеальная и очаговая симптоматика не выявлена.
Приведенный клинический пример подтверждает, что зачастую у непривитых лиц корь может протекать тяжелее и с осложнениями.
По данным О. В. Цвиркуна [8], очаги кори преимущественно формировались в стационарах (59%), в семьях (40%), реже (1%) по месту жительства или в детских домах, что свидетельствует о необходимости более тщательного соблюдения правил эпидемического надзора, своевременного выявления и изоляции больного, а также тщательного наблюдения за контактными, своевременная иммунопрофилактика [9].
При изоляции больного на дому обязательна ежедневная влажная уборка, по возможности, максимальное ограничение контакта больного с членами семьи, запрет на посещение больного родственниками или знакомыми. Все контактные подлежат медицинскому наблюдению до 21 дня с момента выявления больного [10].
Госпитализация больных проводится в случае тяжелого течения заболевания и по эпидемическим показаниям (лица, проживающие в общежитиях, гостиницах, хостелах и др., декретированные группы лиц). Больные госпитализируются в отдельный бокс и подлежат строгому постельному режиму. Лица, госпитализированные в стационар, подлежат выписке не ранее чем через 5 дней с момента появления сыпи. Медперсонал, контактирующий с больным корью, обязан перед посещением бокса соблюдать все меры безопасности: быть привитыми либо иметь высокий защитный титр антител, обязательно ношение шапочки, перчаток, масок и специальной медицинской одежды.
После выписки из стационара либо лечения в условиях изоляции дома, больные подлежат обязательному диспансерному учету по месту прикрепления к поликлинике сроком на 1 месяц. Кратность обязательных контрольных обследований врачом составляет 1 раз в две недели. Проводятся анализы крови и мочи через 2 и 4 недели соответственно, ЭКГ и другие лабораторные и инструментальные методы исследования по показаниям, как и консультации узких специалистов [10]. Через 1 месяц врачебного контроля при наличии хороших лабораторных показателей, отсутствии осложнений, пациент подлежит снятию с диспансерного учета.
Общеизвестно, что самым важным и эффективным способом профилактики кори является прививка. Главным и единственно правильным методом профилактики заболевания является активная иммунизация. Качественная вакцинация, проведенная по срокам Национального календаря прививок с соблюдением всех норм, и регулярная ревакцинация, нарастание защитных титров антител приводят к невозможности заражения инфекцией, а лица, привитые однократно, как правило, переносят легкую или атипичную форму заболевания [11, 12].
Вакцину прививают детям, не болевшим корью, с 12-месячного возраста. Ревакцинацию проводят однократно в 6 лет, перед поступлением в школу. Иммунизации против кори подлежат также подростки и взрослые до 35 лет, не болевшие, не привитые и привитые однократно, не имеющие сведений о профилактических прививках против кори. Продолжительность поствакцинального иммунитета до 8–10 лет [13]. Рекомендуется проводить каждые 10 лет ревакцинацию пациентам с низким титром защитных антител.
В качестве неспецифических мер профилактики рекомендуется ношение медицинской маски в общественных местах (метро, магазины и торговые центры, префектуры, поликлиники), особенно в эпидемический сезон, ведение здорового образа жизни, сбалансированное питание с высоким содержанием белков и витаминов, соблюдение режима труда и отдыха, закаливание, избегание переохлаждений и сквозняков. Необходимо своевременное лечение хронических заболеваний, которые способствуют ухудшению работы иммунной системы и повышенной восприимчивости к патогенным бактериям и вирусам.
Заключение
Своевременное выявление и изоляция больных, правильная госпитализация по клиническим и эпидпоказаниям, грамотная тактика ведения пациента и контактных лиц позволят остановить рост заболеваемости и передачи инфекции, предупредить риск развития осложнений и летальных исходов, а активная вакцинопрофилактика населения с широким охватом иммунизации приведет к полной элиминации и ликвидации кори.
Литература
И. А. Иванова* , 1
Ж. Б. Понежева*, доктор медицинских наук
М. С. Козлова**
Е. Т. Вдовина**, кандидат медицинских наук
Н. А. Цветкова**, доктор медицинских наук, профессор
* ФБУН ЦНИИЭ Роспотребнадзора, Москва
** ГБУЗ ИКБ № 2 ДЗМ, Москва
Особенности течения кори у взрослых/ И. А. Иванова, Ж. Б. Понежева, М. С. Козлова, Е. Т. Вдовина, Н. А. Цветкова
Для цитирования: Лечащий врач № 11/2018; Номера страниц в выпуске: 36-39
Теги: вирусная инфекция, заражение, взрослые, клинический пример
Корь — антропонозная острая вирусная инфекционная болезнь с аспирационным механизмом передачи возбудителя, для которой характерна цикличность течения, лихорадка, интоксикация, катарально-респираторный синдром, наличие пятен Филатова–Коплика и пятнисто-пап
Корь — антропонозная острая вирусная инфекционная болезнь с аспирационным механизмом передачи возбудителя, для которой характерна цикличность течения, лихорадка, интоксикация, катарально-респираторный синдром, наличие пятен Филатова–Коплика и пятнисто-папулезная сыпь.
История и распространение. Корь известна с древних времен. В IX веке н. э. описана арабским врачом Разесом, который считал ее легкой формой натуральной оспы. Поэтому она получила название morbilli — малая болезнь, в отличие от morbus — оспа (большая болезнь). В XVII веке подробное описание клиники кори в Англии дал Сиденхем (T. Sydenham) и Мортон (Th. Morton) во Франции. Вирусную этиологию кори в 1911 г. доказали Андерсон (T. Anderson) и Голдбергер (J. Goldberger) путем заражения обезьян фильтратом крови и носоглоточной слизи больных людей, но культура возбудителя была выделена только в 1954 г. Эндерсом (J. Enders).
Корь в средние века и в начале XX века была одной из самых распространенных детских инфекционных болезней, которая характеризовалась тяжелым течением и летальностью среди детей до трех лет до 40%. При заносе кори на изолированные территории (Фарерские острова, Фиджи) переболевало до 80% населения. Снижение летальности было достигнуто благодаря разработке метода серопрофилактики в 1916–1921 гг. Николем (Ch. Nikolle), Консейлом (E. Conseil) и Дегквитцем (R. Dedkwitz). Широкое применение противокоревой вакцины привело к резкому снижению заболеваемости и даже ее ликвидации в ряде стран. Однако в последние годы наблюдаются случаи заболевания среди вакцинированных. По данным ВОЗ в мире регистрируется ежегодно до 30 млн случаев кори, из которых около 50 тыс. заканчиваются летально.
В России была разработана программа ликвидации кори к 2010 г. (Приказ № 270 Минздрава России от 19.08.2002).
Основными принципами ликвидации кори являются: достижение и поддержание высокого (95–98%) уровня охвата населения прививками живой коревой вакциной (ЖКВ); осуществление эффективного эпидемиологического надзора за корью, предусматривающего полное и активное выявление всех случаев кори и их лабораторное подтверждение, а также своевременное принятие управленческих решений и контроль их выполнения.
Этиология. Возбудитель кори относится к роду morbillivirus, семейства парамиксовирусов, имеет сферическую форму, диаметр 120–250 нм, одноцепочечную РНК. Вирион окружен двухслойной липопротеиновой оболочкой. Вирус имеет три основных антигена — гемагглютинин, протеин F и нуклеокапсидный белок, причем антитела к гемагглютинину и протеину F обладают цитотоксическим действием в отношении инфицированных вирусом клеток. Возбудитель кори является индуктором интерферона, антигенно однороден. Некоторые варианты вируса способны к длительной персистенции в организме человека. Вирус кори неустойчив во внешней среде и быстро погибает под воздействием солнечного света и УФ-облучения. При низких температурах может сохраняться в течение нескольких недель, при температуре более 60 °C погибает мгновенно. При комнатной температуре вирус сохраняется в течение 3–4 часов.
Патогенез. Возбудитель кори внедряется в организм через слизистые оболочки верхних дыхательных путей, проникает в регионарные лимфоузлы, где происходит его первичная репликация. Начиная с третьего дня инкубационного периода вирус циркулирует в крови и гематогенным путем диссеминирует в организме. При этом важную роль, как факт переноса, играют лейкоциты, в которых размножается вирус. Дальнейшая репродукция и накопление вируса происходит во всех органах ретикулоэндотелиальной системы, лимфатических узлах, миндалинах, лимфоидных элементах всего организма, миелоидной ткани костного мозга. При этом происходит пролиферация лимфоидных и ретикулярных элементов. В инкубационном периоде начинается стимуляция иммунной системы. Клетки, пораженные вирусом, атакуются специфическими антителами, лимфоцитами-киллерами и другими факторами инфекционного иммунитета и неспецифической защиты, в результате чего происходит их повреждение и лизис. Это приводит к ряду патогенетически важных этапов: развивается повторная интенсивная вирусемия, вирус фиксируется эпителиальными клетками, прежде всего верхних дыхательных путей, кожи, а также пищеварительного тракта. Попадая в ЦНС, вирус поражает нервные клетки. Поступающие в кровь обломки вирусных частиц и лизированных клеток сенсибилизируют организм, вызывая аллергические реакции, сопровождающиеся повреждением сосудов. Именно эти элементы патогенеза соответствуют по времени началу болезни и определяют симптоматику болезни. Важное звено патогенеза — развитие иммуносупрессии, которая наряду с повреждением эпителиального покрова способствует развитию бактериальных осложнений.
Массивная продукция интерферона, синтез антител, нарастание клеточных защитных реакций приводят уже к третьему дню периода высыпания к резкому уменьшению и прекращению вирусемии и элиминации вируса из организма. Но в ряде случаев вирус кори может длительно персистировать в организме и приводить к развитию медленной инфекции ЦНС (подострый склерозирующий панэнцефалит).
Клиника. Инкубационный период длится от 9 до 17 дней, а при профилактическом введении иммуноглобулина он может удлиняться до 28 дней. Для кори характерна цикличность в течение болезни. Различают три периода течения кори: катаральный, период высыпания и пигментации. Заболевание начинается остро с симптомов общей интоксикации (повышение температуры, головная боль, слабость, апатия, бессонница, снижение аппетита), одновременно появляются катаральные явления. Интоксикация выражена умеренно. Температура тела от субфебрильной до 38–39 °C, в конце катарального периода обычно снижается до нормы. Детей беспокоит кашель, першение в горле, светобоязнь, заложенность носа. Выделения из носа слизистого характера, умеренные. Дети раздражительны, капризны. Появляется охриплость голоса.
У многих больных наблюдается увеличение и чувствительность при пальпации шейных, затылочных, а иногда и других групп лимфоузлов, нередко увеличение размеров печени и селезенки.
При аускультации легких определяется жесткое дыхание, иногда могут выслушиваться сухие хрипы. Возможно снижение артериального давления, тахикардия или брадикардия, тоны сердца приглушены. При вовлечении в патологический процесс пищеварительной системы могут быть тошнота, рвота, жидкий стул без патологических примесей, обложенный язык, болезненность живота при пальпации. В анализе крови определяется лейкопения, лимфоцитоз, эозинопения. СОЭ нормальная или умеренно повышенная.
Особенность кори у взрослых. У взрослых и подростков корь характеризуется рядом особенностей: заболевание протекает тяжелее, более выражен синдром интоксикации (головная боль, нарушение сна, рвота), катаральный период более длительный, чем у детей, — 4–8 дней, пятна Филатова–Коплика–Бельского очень обильные, часто сохраняются в периоде высыпания, в то же время катаральные явления выражены слабо, сыпь обильная, более резко выражена полиаденопатия, чаще пальпируется селезенка, коревой энцефалит развивается у 2% больных (у детей в 5–10 раз реже), осложнения, вызванные бактериальной флорой, наблюдаются редко.
Митигированная корь
При введении во время инкубационного периода контактным лицам противокоревого иммуноглобулина с профилактической целью развивается митигированная корь, для которой характерен удлиненный до 21–28 дней инкубационный период, короткий катаральный период (1–2 дня) или его отсутствие, катаральные симптомы слабо выражены, пятна Филатова–Коплика–Бельского часто отсутствуют. Сыпь бледная, мелкая, необильная, часто ее нет на конечностях. Нехарактерна этапность появления сыпи. Период высыпания длится 1–2 дня. Пигментация после исчезновения сыпи выражена слабо и быстро исчезает.
Осложнения. У детей возможны осложнения, вызванные бактериальной флорой, — гнойные риниты, синуситы, отиты, бронхиты, пневмонии, особенно часто у детей раннего возраста. Эти осложнения в последние годы регистрируются реже. Могут быть случаи ларингита со стенозом гортани (коревой круп). Тяжелым осложнением является коревой энцефалит или менингоэнцефалит, который чаще выявляется в периоде угасания сыпи, но возможен в более ранние и поздние сроки — от 3 до 20 дней болезни. Начало острое, бурное. Повышается температура, появляются расстройства сознания, генерализованные судороги, больные нередко впадают в кому. Могут быть двигательные расстройства (парезы, параличи), часто пирамидные знаки. У некоторых больных наблюдается менингеальный синдром, в цереброспинальной жидкости отмечается невысокий лимфоцитарный или смешанный плеоцитоз, содержание белка повышено. Больные часто погибают в острый период болезни при явлениях отека мозга и нарушения функции дыхания. У выздоровевших выявляются часто тяжелые и стойкие поражения ЦНС (парезы, гиперкинезы, снижение интеллекта).
Диагностика. Диагноз кори устанавливают на основании клинико-эпидемиологических данных. Если в анамнезе больной раньше болел корью и есть вакцинация против нее, то это полностью исключает диагноз кори. Сведения о контакте с больным корью имеют относительное значение, т. к. случайные контакты часто не выявляются. Выявление у больного ларингита, ринита, конъюнктивита, нарастание этих симптомов в течение 2–3 дней, наличие энантемы позволяет врачу заподозрить корь. Большое диагностическое значение имеет появление пятен Филатова–Коплика–Бельского. В периоде высыпания диагноз основывается на выявлении катарального синдрома, предшествующего появлению сыпи, этапности появления сыпи, характерного вида элементов сыпи на фоне бледной кожи, динамики их превращения. Лабораторные методы (обнаружение гигантских клеток в носовом отделяемом, выделение культуры вируса, иммунофлюоресцентный метод обнаружения вирусного антигена, выявление антител методом реакции торможения гемагглютинации (РТГА), реакции связывания комплимента (РСК) или иммуноферментным анализом (ИФА)) на практике применяются редко. РНК вируса с первого дня болезни может быть обнаружена в крови и мазках из слизистой ротоглотки методом полимеразной цепной реакции (ПЦР).
Лечение. Больных госпитализируют по клиническим (тяжелое течение болезни, осложнения) и эпидемиологическим показаниям. Режим постельный на все время лихорадочного периода. Кровать пациента должна находиться головным концом к окну, чтобы свет не раздражал глаза, искусственное освещение должно быть приглушенным. В рацион больного необходимо включить морсы, фруктовые соки, минеральную воду. Пища должна быть полноценной, богатой витаминами, легко усваиваться. Следует исключить из рациона молочные продукты. Этиотропная терапия не разработана. В большинстве случаев лечение проводится дома и назначается симптоматическая и патогенетическая терапия. Из-за светобоязни помещение, в котором находится больной, должно быть затенено. Проводится обработка полости рта раствором нитрофурана, настоем ромашки. Витаминотерапия: ретинол (100 000 МЕ/мл) детям в возрасте 1–6 месяцев по 50 000 МЕ, 7–12 месяцев по 100 000 МЕ, старше одного года по 200 000 МЕ. Для смягчения мучительного кашля воздух помещения увлажняется с помощью влажных простыней и назначаются противокашлевые средства. Несколько раз в день глаза промывают теплой кипяченой водой. После удаления гноя и гнойных корок в глаза закапывают раствор ретинола в масле по 1–2 капли 3–4 раза в день. Сухие, потрескавшие губы смазывают борным вазелином или жиром. Нос прочищают ватными тампонами, смоченными теплым вазелиновым маслом, если образовались корки, рекомендуется закапывать в нос вазелиновое масло по 1–2 капли 3–4 раза в день. Жаропонижающие средства назначаются в возрастных дозах. В стационаре проводят дезинтоксикационную терапию. Имеются данные об эффективности препаратов интерферона (Лейкинферон). При развитии осложнений терапия проводится согласно принципам лечения данных заболеваний. При развитии пневмонии или среднего отита назначается антибактериальная терапия в соответствии с результатами посева мокроты на чувствительность к антибиотикам. При развитии энцефалита лечение направлено на поддержание жизненно важных функций и борьбу с отеком-набуханием головного мозга (ОНГМ). Ослабленным больным, детям до года по индивидуальным показаниям возможно превентивное назначение антибиотиков широкого спектра действия.
Дополнительные методы лечения. Физиотерапевтические методы лечения кори — массаж органов грудной клетки и дыхательная гимнастика (назначается и контролируется врачом лечебной физкультуры). При развитии крупа, ярко выраженных симптомах ларинготрахеита проводят ингаляции с щелочными растворами, бронхолитиками, муколитиками. При сухом кашле и сухих хрипах в легких показана микроволновая и ультравысокочастотная терапия на область грудной клетки.
Прогноз. При неосложненном течении заболевания прогноз благоприятный. Летальность в настоящее время при кори составляет около 1,5%, раньше летальность достигала 10%. Летальные случаи регистрируются в развивающихся странах и связаны в основном с развитием коревого энцефалита, при котором летальность составляет 20–30%.
Профилактика. Основным методом профилактики кори является вакцинопрофилактика, цель которой — создание невосприимчивости населения к этой инфекции. Прививки ЖКВ проводят в рамках национального календаря профилактических прививок и календаря прививок по эпидемическим показаниям. Плановые прививки включают однократную вакцинация в возрасте 12 месяцев и ревакцинацию в 6 лет. Охват прививками детей декретированных возрастов должен составлять не менее 95%. Поствакцинальный противовирусный иммунитет формируется у 95–97%, срок его защитного действия составляет в среднем 14 лет.
Комплекс противоэпидемических и профилактических мероприятий включает выявление источников инфекции, определение границ эпидемических очагов, контактировавших с больным корью и не защищенных против кори среди них.
В период выполнения программы элиминации кори в России важное значение приобретает полное и активное выявление всех случаев кори, поэтому больных с экзантемными заболеваниями при малейшем подозрении на корь необходимо обследовать серологическими методами для верификации диагноза. О каждом случае заболевания корью, а также при подозрении на заболевание корью врач лечебно-профилактического учреждения или врач, занимающийся частной практикой, направляет в течение 12 часов экстренное извещение в территориальный отдел Роспотребнадзора по месту жительства больного.
Больного корью госпитализируют по клиническим и эпидемиологическим показаниям. Срок изоляции источника инфекции определяет длительность заразного периода — 5 дней с момента появления сыпи, а при наличии пневмонии он увеличивается до 10 дней.
Восприимчивыми к кори считают тех, кто не болел корью и не прививался против нее или привит однократно, а также лиц с неизвестным инфекционным и прививочным анамнезом или тех, у которых при серологическом обследовании не выявлены антитела к вирусу кори в защитных титрах (в РТГА — 1:5, в реакции торможения пассивной гемагглютинации (РТПГА) — 1:10 и выше).
В эпидемическом очаге кори осуществляют проветривание и влажную уборку.
Следует отметить, что достижение устойчивой стабилизации заболеваемости корью на спорадическом уровне возможно только за счет высокого охвата детского населения прививками против кори на каждом педиатрическом участке. Причем уровень охвата прививками не должен снижаться при регистрации на территории низких показателей заболеваемости или при полном отсутствии случаев кори. Необходимо иметь в виду, что уровень охвата прививками не менее 95% декретированных возрастов препятствует распространению возбудителя среди населения в случае его заноса из-за рубежа.
В рамках осуществления эпидемиологического надзора за корью в условиях низкой заболеваемости существенная роль отведена серологическому мониторингу, позволяющему своевременно определять группы и территории риска при выявлении увеличения числа серонегативных к вирусу кори лиц.
Реализация принципов эпидемиологического надзора за корью, включающего слежение за заболеваемостью, состоянием коллективного иммунитета, клиническим течением инфекции, циркуляцией генотипов возбудителя, оценку эффективности профилактических и противоэпидемических мероприятий, принятие оперативных решений и контроль являются основой для достижения целей национальной программы элиминации кори в Российской Федерации и сертификации территорий, свободных от этой инфекции.
Литература
Г. К. Аликеева, кандидат медицинских наук
Н. Д. Ющук, доктор медицинских наук, профессор, академик РАМН
А. В. Сундуков, доктор медицинских наук, профессор
Г. М. Кожевникова, доктор медицинских наук, профессор
Н. Х. Сафиуллина, кандидат медицинских наук
Е. В. Кухтевич, кандидат медицинских наук
Читайте также:

