Абсцесс головного мозга при вич
Обновлено: 24.04.2024
Диагностика приобретенного ВИЧ-энцефалита по КТ, МРТ
а) Определения:
• ВИЧ-1-энцефалит/ВИЧ-1-энцефалопатия (ВИЧЭ)
• Прямое ВИЧ-инфицирование головного мозга:
о Отсутствие оппортунистических инфекционных заболеваний
о Когнитивные, поведенческие и двигательные аномалии в 25-70% случаев
о Наиболее частая неврологическая манифестация ВИЧ-инфекции
• Умеренные когнитивные нарушения, несмотря на хороший вирусологический ответ на терапию
б) Визуализация:
1. Общие характеристики приобретенного ВИЧ-энцефалита:
• Лучший диагностический критерий:
о Атрофия головного мозга + двустороннее диффузное изменение белого вещества (БВ):
- Картина при диагностической визуализации/патологоанато-мическом исследовании варьирует в зависимости от возраста пациента и остроты симптомов заболевания
• Локализация:
о Перивентрикулярное БВ/БВ полуовального центра с двух сторон, базальные ганглии, мозжечок, ствол мозга
• Размеры:
о Вариабельны, часто диффузный характер поражений
• Морфология:
о Распространяется до границы между серым и белым веществом
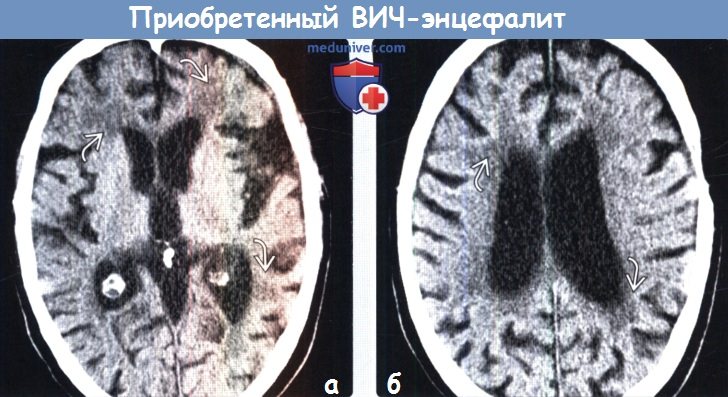
(а) Бесконтрастная КТ, проведенная по поводу снижения когнитивной функции у мужчины 38 лет с длительным анамнезом ВИЧ/СПИД, который получал ВААРТ, аксиальный срез: обратите внимание на выраженную атрофию головного мозга, а также зоны низкой плотности в структуре субкортикального белого вещества.
(б) Бесконтрастная КТ, аксиальный срез: у этого же пациента определяется характерное снижение плотности перивентрикулярного белого вещества в сочетании с диффузным расширением борозд и боковых желудочков.
2. КТ признаки приобретенного ВИЧ-энцефалита:
• Бесконтрастная КТ:
о Дети: атрофия и диффузное снижение плотности белого вещества:
- Внутриутробное инфицирование ВИЧ: характерны двусторонние и симметричные кальцификаты в базальных ганглиях и БВ лобных областей с возможным контрастным усилением
о Взрослые: умеренная атрофия или ее отсутствие, снижение плотности БВ
о Масс-эффект отсутствует
• КТ с контрастированием:
о Отсутствие накопления контрастного вещества
3. МРТ признаки приобретенного ВИЧ-энцефалита:
• Т1-ВИ:
о Изменений в БВ может не наблюдаться
• Т2-ВИ:
о Два визуализационных паттерна:
- фокальные участки гиперинтенсивного сигнала
- Диффузное усиление сигнала от БВ от умеренной до высокой степени выраженности
о Распространенность и протяженность поражения БВ не всегда коррелирует с клинической картиной
• FLAIR:
о Тот же визуализационный паттерн, что и на Т2-ВИ
о Обеспечивает раннее выявление мелких патологических очагов, локализованных в кортикальном/субкортикальном и глубоком БВ
о Большая заметность изменений (по сравнению с Т2-ВИ)
• Постконтратсное Т1-ВИ:
о В вовлеченных областях контрастное усиление отсутствует
• МР-спектроскопия:
о СПИД-дементный комплекс
- ↑ пиков миоинозитола, холина, в белом веществе и базальных ганглиях
- ↓ пика N-ацетиласпартата (NAA) в белом веществе
о Пациенты без симптомов с сохранным сознанием
- Умеренное ↑ пика миоинозитола
• Два основных последствия ВИЧ-инфекции мозговой ткани
о Атрофия мозговой ткани, обусловленная смертью нейронов
о Изменения в глубоком БВ (обычно перивентрикулярные области) → повышение сигнала на Т2-ВИ
• Отношение переноса намагниченности (ОПН):
о ОПН позволяет дифференцировать ВИЧЭ от прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ):
- При ПМЛ наблюдается значительное ↓ ОПН в пораженных областях (по сравнению с таковыми при ВИЧЭ), вероятно обусловленное демиелинизацией
• Диффузионно-тензорная визуализация
о При ВИЧ-ассоциированных когнитивных нарушениях возможно ↓ фракционной анизотропии в раннем периоде заболевания
4. Рекомендации по визуализации:
• Лучший инструмент визуализации:
о МРТ по сравнению с КТ более информативна в обнаружении патологии БВ
о МР-спектроскопия позволяет обнаружить изменения БВ даже на бессимптомной стадии заболевания
• Советы по протоколу исследования:
о КТ исследование должно быть проведено при:
- Впервые возникших судорожном синдроме, головных болях, депрессии или нарушении ориентации
о МРТ исследование должно быть проведено при:
- Обнаружении методом КТ фокального объемного образования
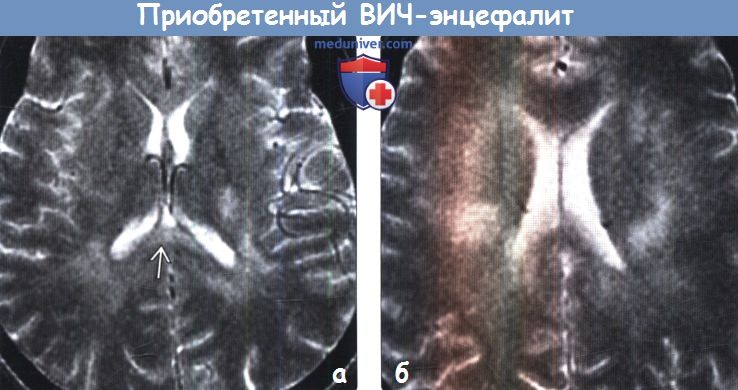
(а) Изменения белого вещества могут появляться в головном мозге пациентов с ВИЧ/СПИД до развития его атрофии и деменции, что и наблюдается у данного ВИЧ-положительного мужчины 34 лет с головными болями. Желудочки имеют нормальный внешний вид, визуализируются двусторонние облаковидные зоны повышения интенсивности сигнала от белого вещества, включая мозолистое тело.
(б) МРТ, Т2-ВИ, аксиальный срез: у этого же пациента неотчетливо определяется мультифокальное двустороннее асимметричное облаковидное повышение сигнала от белого вещества.
в) Дифференциальная диагностика приобретенного ВИЧ-энцефалита:
1. Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ):
• Мультифокальное поражения БВ
о Может быть односторонним, но гораздо чаще имеет двусторонний, асимметричный характер
о Наиболее часто локализуются в теменно-затылочных областях
о Поражение субкортикальных U-волокон (в отличие от ВИЧ-инфекции или ЦМВИ)
• Отсутствие накопления контрастного вещества; при наличии контрастирования предполагайте воспалительный синдром восстановления иммунитета (ВСВИ)
2. ЦМВ-ассоциированное поражение ЦНС:
• Энцефалит (диффузное повышение интенсивности сигнала от БВ на Т2-ВИ)
• Вентрикулит (контрастирование эпендимы)
3. Герпетический энцефалит:
• Вирус простого герпеса (ВПГ), вирус герпеса человека 6 типа (ВГЧ-6): на ранних стадиях зоны поражения локализуются в гиппокампе и медиальных отделах височных областей
4. Токсоплазмоз:
• Объемное образование(я) с кольцевым характером накопления контрастного вещества
• Гиперинтенсивные поражения на T2-ВИ/FLAIR, ДВИ
5. Первичная лимфома ЦНС:
• Одиночные/мультифокальные поражения, локализованы в глубоком > субкортикальном БВ
• Выраженная склонность к поражению базальных ганглиев, полушарий мозжечка, таламуса, ствола мозга, мозолистого тела и субэпендимальных отделов
• КТ с контрастированием: у ВИЧ-положительных пациентов обычно наблюдается краевой характер накопления контрастного вещества
• Положительные результаты ОФЭКТ-исследования с таллием-201
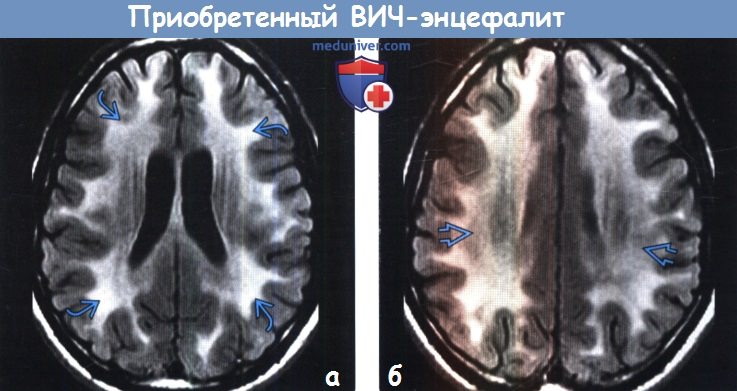
(а) МРТ, FAIR, аксиальный срез: у ВИЧ-позитивного мужчины 25 лет с когнитивными и поведенческими нарушениями определяются протяженные сливные относительно симметричные зоны повышения интенсивности сигнала от белого вещества в сочетании с легкой атрофией.
(б) МРТ, FAIR, аксиальный срез: у этого же пациента определяются схожие диффузные зоны повышения интенсивности сигнала от белого вещества. Данные изменения характерны для ВИЧ-энцефалита. Такие патологические изменения не оказывают масс-эффект на окружающие структуры и не накапливают контрастное вещество. При наличии любого из этих признаков необходимо предполагать иной диагноз.
г) Патология:
1. Общие характеристики приобретенного ВИЧ-энцефалита:
• Этиология:
о При первичной ВИЧ-инфекции вирус проникает в мозг через моноцитарную/макрофагальную систему
о ВИЧ способен вызывать неврологические заболевания, но он не реплицируется в нейронах и клетках глии
о Воспалительные (Т-клеточные) реакции с развитием васкулита, лептоменингита
• Генетика:
о Геномика ВИЧ → более нейровирулентные штаммы
о Деменция развивается лишь у пациентов, инфицированных штаммами ВИЧ, в которых произошли критические мутации
• Ассоциированные аномалии:
о ВИЧЭ может развиваться в сочетании с другими ВИЧ-ассоциированными аномалиями (например, другими инфекциями)
о Прогрессирующая энцефалопатия у детей часто сочетается с миелопатией
• Отличительный признак ВИЧЭ: микроглиальные узелки с гигантскими многоядерными клетками (ГМК)
• Реактивный глиоз, фокальный некроз и демиелинизация
• Умеренная потеря нейронов; минимальные воспалительные изменения
• Проникновение вируса в мозг происходит на самых ранних этапах после системной инфекции
2. Стадирование и классификация приобретенного ВИЧ-энцефалита:
• Три типа нейропатологоанатомических изменений:
о 1 тип: ВИЧ-энцефалит:
- Множественные диссеминированные очаги микроглии, макрофагов и ГМК; если ГМК не обнаружены, необходимо провести исследование на ВИЧ-антиген/нуклеиновые кислоты
о 2 тип: ВИЧ-лейкоэнцефалопатия:
- Диффузное и симметричное поражение БВ (потеря миелина, реактивный астроглиоз, макрофаги и ГМК); если ГМК не обнаружены, необходимо провести исследование на ВИЧ-ан-тиген/нуклеиновые кислоты
о 3 тип: ВИЧ-ассоциированные гигантские клетки:
- PAS(+) одно- или многоядерные макрофаги
• Легкая ВИЧЭ: тип 1 без МГК
• Умеренная ВИЧЭ: тип 1, 2 или 3
• Выраженная ВИЧЭ: атрофия головного мозга + тип 1 или 2
3. Макроскопические и хирургические особенности:
• Ранняя стадия: бледность окраски БВ
• Поздняя стадия: инфицирование неокортекса, атрофия
4. Микроскопия:
• ВИЧЭ:
о Инфицированные клетки: преимущественно макрофаги и микроглия; малая часть астроглии; редко олигодендроциты
о Вторичное повреждение нейронов
о Минимальные воспалительные изменения: периваскулярные макрофагальные инфильтраты и микроглиальные узелки
• Прогрессирующая энцефалопатия у ВИЧ-инфицированных детей:
о Воспалительные инфильтраты с ГМК
о Протяженная кальцифицирующая васкулопатия с преимущественным поражением мелких сосудов базальных ганглиев, а также БВ головного мозга и моста
о Атрофия, обусловленная нарушением созревания миелина или потерей миелина
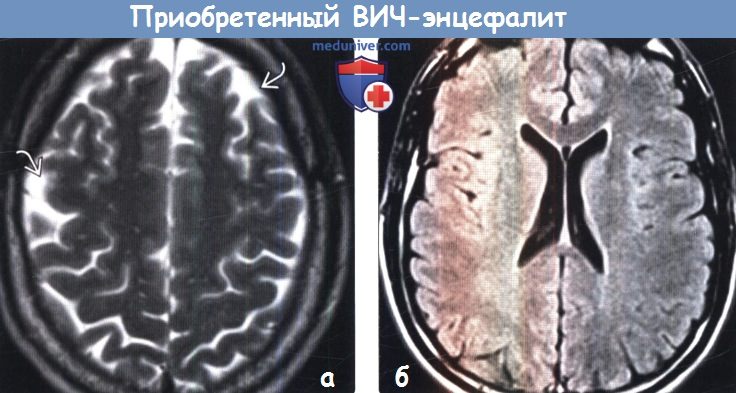
(а) МРТ, Т2-ВИ, аксиальный срез: у ВИЧ-положительного пациента с ранними признаками субкортикальной деменции определяется вариант картины ВИЧ-энцефалита. Атрофические изменения очевидны на уровне верхних отделов полушарий головного мозга, вокруг которых отмечается расширение ликворных пространств ВИЧ-энцефалит при диагностической визуализации наиболее часто проявляется в виде диффузных облако-видных зон поражения белого вещества головного мозга в сочетании с его атрофическими изменениями. Тем не менее, в некоторых случаях (в том числе и здесь) атрофия головного мозга может быть доминирующим признаком.
(б) MPT, FLAIR: у этого же пациента определяется легкая атрофия без значимого изменения белого вещества.
д) Клиническая картина:
1. Проявления приобретенного ВИЧ-энцефалита:
• Наиболее частые признаки/симптомы:
о Субкортикальная деменция с когнитивными, моторными и поведенческими нарушениями
• Клинический профиль:
о ВИЧ-ассоциированный когнитивный синдром: невыраженный или выраженный (деменция)
о Нарушения центральной моторной функции
о Поведенческие нарушения: псевдодеменция (депрессия), делирий и спутанность сознания
о В педиатрической практике: микроцефалия, когнитивные нарушения, слабость, пирамидные знаки, атаксия и судорожные признаки
2. Демография:
• Возраст:
о ВИЧ-положительные пациенты как взрослого, так и детского возраста
• Пол:
о Преобладание патологии у какого-либо пола не выявлено; половая структура распространения ВИЧЭ отражает таковую для ВИЧ инфекции
• Эпидемиология:
о У 33-67% ВИЧ-положительных взрослых и 40-50% ВИЧ- положительных детей развивается ВИЧЭ
о ВИЧЭ развивается до развития оппортунистических инфекций и опухолей; распространенность не связана со стадией заболевания
3. Течение и прогноз:
• Когнитивные нарушения возникают тогда, когда пациент становится иммунокомпрометированным
• Медленно прогрессирующее нарушение контроля мелкой моторики, вербальной беглости и кратковременной памяти
• Через несколько месяцев: выраженное ухудшение и субкортикальная деменция с развитием на поздних стадиях состояний, близких к вегетативному
4. Лечение:
• Высокоактивная антиретровирусная терапия (ВААРТ) не позволяет избежать развития ВИЧЭ, но позволяет ↓ ее выраженность:
о Эра ВААРТ: ↓ частоты встречаемости выраженной ВИЧЭ, но ↑ частоты встречаемости ВИЧЭ легкой-умеренной степени
В Российской Федерации, как и во всем мире, наблюдается рост заболеваемости ВИЧ-инфекцией, что ведет к увеличению числа случаев госпитализаций ВИЧ-инфицированных больных в стационары различного профиля, в том числе неврологические. Это связано, во-первых, с частым и ранним вовлечением нервной системы в патологический процесс, во-вторых, с тяжестью клинических проявлений сочетанного поражения нервной системы при ВИЧ-инфекции, в-третьих, с высоким уровнем смертности и инвалидизации таких больных. Проведен анализ клинического случая абсцесса головного мозга у ВИЧ-инфицированной пациентки. Рассмотрены тактика ведения, основные сложности диагностики и лечения при сочетании поражения нервной системы и ВИЧ-инфекции, а также прокомментированы некоторые проблемы, с которыми сталкиваются врачи при работе с ВИЧ-инфицированными пациентами.

1. Аналитическая справка о деятельности Саратовского областного центра по профилактике и борьбе со СПИД и инфекционными заболеваниями и службы ВИЧ/СПИДа области: аналитическая справка 2012–2013 / ГУЗ Центр-СПИД Саратов. – 2010. – С. 2–18.
2. ВИЧ-инфекция: Информационный бюллетень № 30 ФНМЦ ПБ СПИД Роспотребнадзора / В.В. Покровский, Н.Н. Ладная, Е.В. Соколова и др. – М., 2007. – С. 31.
3. Дмитриенко Е.В., Корнева Е.А. Иммунная система мозга и вирусные инфекции// ВИЧ-инфекция и иммуносупрессии. – 2013. – Т. 5, № 3. – С. 7–17.
4. Леонова О.Н. и др. Поражения нервной системы у больных с ВИЧ-инфекцией на опыте работы отделения паллиативной медицины // ВИЧ-инфекция и иммуносупрессии. – 2011. – Т. 3, № 2. – С. 62–69.
5. Канестри В.Г., Кравченко А.В., Деулина М.О. Влияние антиретровирусной терапии на липидный обмен // Инфекционные болезни. – 2009. – Т. 7, № 3. – С. 25–29.
6. Кравченко А.В. Безопасность и эффективность применения атазанавира в составе современных схем АРВТ // Дальневосточный журнал инфекционной патологии. – 2010. – № 17. – С. 220–235.
7. Станкеева О.Б., Мусатов В.Б., Яковлев А.А. Токсоплазмоз головного мозга у ВИЧ-инфицированных пациентов // ВИЧ-инфекция и иммуносупрессии. – 2013. – Т. 5, № 1 – С. 59–65.
8. Шахгильдян В.И. и др. Спектр, особенности клинического течения, диагностика оппортунистических и сопутствующих заболеваний у ВИЧ-инфицированных больных инфекционного стационара г. Москвы // Терапевтический архив. – 2008. – Т. 80, № 11. – С. 10–18.
10. Eugenin E.A., Berman J.W. Gap junctions mediate human immunodeficiency virus-bystander killing in astrocytes // The Journal of Neuroscience. – 2007, Vol. 27, № 47. – P. 12844–12850.
11. Manfredi R. HIV infection and advanced age: emerging epidemiological, clinical, and management issues // Ageing research reviews. – 2004. – Vol. 3, № 1. – P. 31–54.
12. Palella Jr F. J. et al. Declining morbidity and mortality among patients with advanced human immunodeficiency virus infection // New England Journal of Medicine. – 1998. – Vol. 338, № 13. – P. 853–860.
13. Rotta I., Almeida S.M. Genotypical diversity of HIV clades and central nervous system impairment // Arquivos de neuro-psiquiatria. – 2011. – Vol. 69, № 6. – P. 964–972.
В настоящее время человечество переживает пандемию ВИЧ-инфекции, которая наносит человечеству серьезнейший ущерб. В 2013 г., по данным ВОЗ, в мире проживало более 35 (33,2–37,2) миллионов ВИЧ-инфицированных, с начала эпидемии (1981 г.) свыше 75 (71–87) миллионов человек заразились ВИЧ, из которых 39 (35–43) миллионов умерли [9], при этом в Российской Федерации (РФ) общее количество пациентов с ВИЧ к 2014 г. превысило 800 тыс. человек [1].
ВИЧ поражает все клетки, несущие на своей поверхности CD4 рецепторы, к ним относятся лимфоциты, моноциты, макрофаги, эндотелий кровеносных сосудов, клетки нейроглии и др. [13]. По частоте поражения органов и систем при ВИЧ-инфекции нервная система занимает второе место после иммунной [3]. Доказано, что ВИЧ поступает в центральную нервную систему (НС) уже в ранние сроки после заражения, являясь причиной преимущественно моторных и когнитивных нарушений [10]. ВИЧ-ассоциированное поражение НС наблюдается, по меньшей мере, у 70 % больных, при этом у 10 % инфицированных неврологическая симптоматика является тяжелой [7]. В настоящее время в РФ отмечается существенное увеличение числа ВИЧ-инфицированных, имеющих клинические, в том числе неврологические, проявления заболевания. Это связывают с поздним обращением пациентов за медицинской помощью и, как следствие, несвоевременной диагностикой ВИЧ-инфекции [2, 5]. Такие пациенты нередко нуждаются в стационарном лечении, но, поступая в отделения различного профиля, они зачастую скрывают свой ВИЧ-статус. Инфицированные ВИЧ пациенты, страдающие патологией НС, являются наиболее тяжелыми и диагностически сложными, для них характерна высокая летальность и инвалидизация [4]. В связи с этим изучение различных типов поражения НС при ВИЧ-инфекции представляется весьма актуальным.
Наиболее часто неврологические проявления ВИЧ-инфекции связаны с развитием оппортунистических инфекций (токсоплазмозный энцефалит, криптококковый менингит, прогрессирующая мультифокальная лейкоэнцефалопатия, цитомегаловирусный энцефалит и др.), опухолей (первичная лимфома головного мозга и др.), асептического менингита и энцефалита ВИЧ-этиологии, нервно-мышечной патологии (периферическая полинейропатия, миопатия и др.), цереброваскулярных нарушений [8].
Широкое использование в настоящее время высокоактивной антиретровирусной терапии (ВААРТ) значительно повлияло на естественное течение ВИЧ-инфекции и привело к уменьшению смертности в общей популяции ВИЧ-инфицированных лиц [5, 11, 12]. Имеются данные о том, что в результате применения ВААРТ снизился риск развития и прогрессирования многих ВИЧ-ассоциированных заболеваний НС, например, опухолей головного мозга и др. [6]. Вполне вероятно, что применение ВААРТ, являющейся важным компонентом комплексного лечения больных ВИЧ-инфекцией, позволит снизить уровень летальности и инвалидизации при тяжелом сочетанном поражении НС.
Представляем клинический случай, иллюстрирующий особенности тактики ведения ВИЧ-инфицированных пациентов с сочетанным поражением НС.
Больная Л. 1979 года рождения, поступила в стационар г. Саратова в сентябре 2011 г. с жалобами на головную боль, слабость в правой руке, нарушение речи.
За неделю до госпитализации пациентка обратила внимание на выраженную головную боль, слабость в правой руке, невнятность речи. В связи с этим она обратилась за медицинской помощью в частную амбулаторную клинику, где была консультирована неврологом, выполнена магнитно-резонансная томография (МРТ) головного мозга, при которой выявлены МР-признаки объемного образования в теменно-затылочной области левого полушария. В связи с подозрением на внутримозговую опухоль больная была направлена на стационарное лечение в нейрохирургический стационар. На амбулаторном этапе исследование крови на ВИЧ-инфекцию не проводилось.
В течение 10 лет пациентка состояла на диспансерном учете в Саратовском областном Центре профилактики и борьбы со СПИД (ГУЗ Центр-СПИД), однако о своем ВИЧ-статусе она не сообщила ни врачам частной амбулаторной клиники, ни врачам стационара. Согласно полученной позже информации за 4 месяца до госпитализации больная посещала врача-инфекциониста ГУЗ Центр-СПИД, где при обследовании в крови была выявлена высокая вирусная нагрузка (1,01×105 копий/мл) и низкий уровень CD4-лимфоцитов (327 кл./мл), но от назначения ВААРТ пациентка отказалась.
При поступлении в нейрохирургическое отделение больная была в сознании, вступала в контакт, была ориентирована в месте и времени. Состояние расценено как тяжелое, но стабильное, тяжесть была обусловлена неврологической симптоматикой. При объективном осмотре в неврологическом статусе были выявлены речевые нарушения в виде моторной дисфазии, снижение активности движений в конечностях до степени монопареза в правой руке со снижением силы до 2–3 балла, оживлением карпорадиального и биципитального рефлексов справа. Других очаговых неврологических расстройств, менингеальных знаков выявлено не было.
В день госпитализации у больной развился вторично-генерализованный парциальный судорожный приступ длительностью около 3 минут, после которого больная сразу пришла в сознание. После эпилептического приступа состояние пациентки ухудшилось – усугубилась общемозговая симптоматика, нарос парез в правой руке и моторная афазия, появились признаки поражения VII и XII черепных нервов справа. На следующий день по жизненным показаниям выполнена костно-пластическая трепанация черепа в левой лобно-теменной области с удалением объемного образования.
Больной была проведена массивная антибактериальная, эмпирическая противовирусная, противоотечная и симптоматическая терапия.
В раннем послеоперационном периоде у пациентки сохранялась моторная афазия, парез мышц, иннервируемых VII и XII черепными нервами, справа по центральному типу, правосторонний грубый парез с повышением тонуса и рефлексов, а также субфебрилитет. На фоне комплексного лечения речевые расстройства частично регрессировали, появились движения в правой руке.
На третьи сутки госпитализации был получен положительный результат исследования крови на антитела к ВИЧ методом иммуноферментного анализа (ИФА), который был взят в момент госпитализации в стационар.
При беседе с пациенткой о причинах сокрытия информации о её ВИЧ-статусе, было установлено, что больная умышленно утаила эту информацию от врачей из-за страха отказа в оказании специализированной помощи.
Пациентка выписана из стационара с улучшением на девятые сутки после оперативного вмешательства на амбулаторный этап долечивания под наблюдение невролога по месту жительства и специалистов ГУЗ Центр-СПИД.
Через 1 месяц после начала ВААРТ вирусная нагрузка уменьшилась практически на 2lg, CD4-лимфоциты остались на прежнем уровне. Через 4 месяца вирусная нагрузка в крови составила менее 50 копий/мл, уровень CD4-лимфоцитов вырос в 2 раза. В мае 2012 г. (через 7 месяцев после начала ВААРТ) проведено МР-исследование головного мозга, выявившее признаки вторичных изменений в обеих гемисферах головного мозга, кистозно-глиозные (послеоперационные) изменения в левой лобно-теменной области.
Через 1,5 года после начала терапии вирусная нагрузка в крови не определялась (менее 20 копий/мл), а уровень CD4 лимфоцитов вырос почти в 4,5 раза и составил 243 кл./мл. В ноябре 2014 года иммунный статус находился на стабильном уровне, вирусная нагрузка в крови не определялась.
На фоне проводимого комплексного (оперативного, медикаментозного с использованием специфической антиретровирусной терапии) лечения в состоянии больной отмечена положительная динамика, что проявлялось в улучшении самочувствия, неврологического статуса (уменьшении явлений гемипареза и афазии) и лабораторных показателей (снижения вирусной нагрузки и повышения уровня CD4 лимфоцитов).
Динамика изменений иммунного статуса и вирусной нагрузки у пациентки с ВИЧ-инфекцией на фоне приема ВААРТ
Абсцесс головного мозга — это ограниченное скопление гноя в полости черепа. Различают три вида абсцессов: внутримозговые, субдуральные и эпидуральные. Симптомы абсцесса головного мозга зависят от его месторасположения и размеров. Они не являются специфичными и могут составлять клинику любого объемного образования. Диагностируется абсцесс головного мозга по данным КТ или МРТ головного мозга. При абсцессах небольшого размера подлежат консервативному лечению. Абсцессы, расположенные вблизи желудочков головного мозга, а также вызывающие резкий подъем внутричерепного давления, требуют хирургического вмешательства, при невозможности его проведения - стереотаксической пункции абсцесса.
МКБ-10
Общие сведения
Абсцесс головного мозга — это ограниченное скопление гноя в полости черепа. Различают три вида абсцессов: внутримозговые (скопление гноя в веществе мозга); субдуральные (расположенные под твердой мозговой оболочкой); эпидуральные (локализованные над твердой мозговой оболочкой). Основными путями проникновения инфекции в полость черепа являются: гематогенный; открытая проникающая черепно-мозговая травма; гнойно-воспалительные процессы в придаточных пазухах носа, среднем и внутреннем ухе; инфицирование раны после нейрохирургических вмешательств.

Причины
Среди выделенных возбудителей гематогенных абсцессов головного мозга преобладают стрептококки, часто в ассоциации с бактериотидами (Bacteroides spp.). Для гематогенных и отогенных абсцессов характерны Enterobacteriaceae (в том числе Proteus vulgaris). При открытой проникающей черепно-мозговой травме в патогенезе абсцесса мозга преобладают стафилококки (St. aureus), реже Enterobacteriaceae.
При различных иммунодефицитных состояниях (иммунодепрессивная терапия после трансплантации органов и тканей, ВИЧ-инфекция) из посева содержимого абсцесса головного мозга выделяют Aspergillus fumigatus. Однако идентифицировать возбудителя инфекции в содержимом абсцесса мозга довольно часто не представляется возможным, так как в 25-30 % случаев посевы содержимого абсцесса оказываются стерильными. Болезнь провоцируется следующими патологическими состояниями:
- Воспалительные процессы в легких. Чаще всего причиной образования гематогенных абсцессов головного мозга являются бронхоэктатическая болезнь, эмпиема плевры, хроническая пневмония, абсцесс легкого). Бактериальным эмболом становится фрагмент инфицированного тромба, который попадет в большой круг кровообращения и потоком крови разносится в сосуды мозга, где фиксируется в мелких сосудах (прекапилляре, капилляре или артериоле). Незначительную роль в патогенезе абсцессов могут играть хронический (или острый) бактериальный эндокардит, инфекции ЖКТ и сепсис.
- Черепно-мозговая травма. В случае открытой проникающей ЧМТ абсцесс мозга развивается вследствие прямого попадания инфекции в полость черепа. В мирное время доля таких абсцессов составляет 15-20%. В условиях боевых действий она возрастает в разы (минно-взрывные ранения, огнестрельные ранения).
- ЛОР-патологии. При гнойно-воспалительных процессах в придаточных пазухах носа (синуситы), среднем и внутреннем ухе возможны два пути распространения инфекции: ретроградный — по синусам твердой мозговой оболочки и мозговым венам; и непосредственное проникновение инфекции через твердую оболочку мозга. Во втором случае отграниченный очаг воспаления первоначально формируется в мозговых оболочках, а затем — в прилежащем отделе мозга.
- Послеоперационные осложнения. Абсцессы мозга, формирующиеся на фоне интракраниальных инфекционных осложнений после нейрохирургических вмешательств (вентрикулиты, менингиты), возникают, как правило, у тяжелых, ослабленных больных.
- Другие заболевания. Незначительную роль в патогенезе гематогенных абсцессов могут играть хронический (или острый) бактериальный эндокардит, инфекции ЖКТ и сепсис.
Патогенез
Формирование абсцесса мозга проходит в несколько этапов.
- 1-3 сутки. Развивается ограниченное воспаление мозговой ткани — энцефалит (ранний церебрит). На данном этапе воспалительный процесс обратим. Возможно как спонтанное его разрешение, так и под влиянием антибактериальной терапии.
- 4-9 сутки. В результате недостаточных защитных механизмов или в случае неверного лечения воспалительный процесс прогрессирует, в его центре полость, заполненная гноем, способная к увеличению.
- 10-13 сутки. На этой стадии вокруг гнойного очага формируется защитная капсула из соединительной ткани, которая препятствует распространению гнойного процесса.
- Третья неделя. Капсула окончательно уплотняется, вокруг нее формируется зона глиоза. В дальнейшем развитие ситуации зависит от вирулентности флоры, реактивности организма и адекватности лечебно-диагностических мероприятий. Возможно обратное развитие абсцесса мозга, но чаще увеличение его внутреннего объема или образование новых очагов воспаления по периферии капсулы.
Симптомы абсцесса головного мозга
На сегодняшний день патогномоничная симптоматика не выявлена. Клиническая картина при абсцессах головного мозга схожа с клинической картиной объемного образования, когда клинические симптомы могут варьироваться от головной боли до тяжелейших общемозговых симптомов, сопряженных с угнетением сознания и выраженными очаговыми симптомами поражения головного мозга.
В некоторых случаях первым проявлением болезни становится эпилептиформный припадок. Могут наблюдаться менингеальные симптомы (при субдуральных процессах, эмпиеме). Эпидуральные абсцессы головного мозга зачастую ассоциируются с остеомиелитом костей черепа. Наблюдается прогредиентное нарастание симптоматики.
Диагностика
Для диагностирования абсцесса головного мозга огромное значение имеет тщательный сбор анамнеза (наличие очагов гнойной инфекции, острое инфекционное начало). Наличие воспалительного процесса, сопряженного с появлением и усугублением неврологических симптомов — основание для дополнительного нейровизуализационного обследования.
Точность диагностирования с помощью КТ головного мозга зависит от стадии формирования абсцесса. На ранних стадиях заболевания диагностика затруднена. На этапе раннего энцефалита (1-3 сутки) КТ определяет зону сниженной плотности неправильной формы. Введенное контрастное вещество накапливается неравномерно, преимущественно периферических отделах очага, реже в центре.
На более поздних этапах энцефалита контуры очага приобретают ровные округлые очертания. Контрастное вещество распределяется равномерно, по всей периферии очага; плотность центральной зоны очага при этом не меняется. Однако на повторной КТ (через 30-40 минут) определяется диффузия контраста в центр капсулы, а также наличие его и в периферической зоне, что не характерно для злокачественных новообразований.
Инкапсулированный абсцесс мозга на КТ имеет вид округлого объемного образования с четкими ровными контурами повышенной плотности (фиброзная капсула). В центре капсулы зона пониженной плотности (гной), по периферии видна зона отека. Введенное контрастное вещество накапливается в виде кольца (по контуру фиброзной капсулы) с небольшой прилежащей зоной глиоза.
На повторной КТ (через 30-40 минут) контрастное вещество не определяется. При исследовании результатов компьютерной томографии следует учесть, что противовоспалительные препараты (глюкокортикостероиды, салицилаты) в значительной степени влияют на скопление контраста в энцефалитическом очаге.
МРТ головного мозга — более точный метод диагностирования. При проведении МРТ на первых стадиях формирования абсцесса мозга (1-9 сутки) энцефалитический очаг выглядит: на Т1-взвешенных изображениях — гипоинтенсивным, на Т2-взвешенных изображениях — гиперинтенсивным. МРТ на поздней (капсулированной) стадии абсцесса головного мозга: на Т1-взвешенных изображениях абсцесс выглядит, как зона пониженного сигнала в центре и на периферии (в зоне отека), а по контуру капсулы сигнал гиперинтенсивный. На Т2-взвешенных изображениях центр абсцесса изо- или гипоинтенсивный, в периферической зоне (зоне отека) гиперинтенсивный. Контур капсулы четко очерчен.
Дифференциальная диагностика абсцесса головного мозга должна проводиться с первичными глиальными и метастатическими опухолями полушарий мозга. При сомнениях в диагнозе следует проводить МЗ-спектроскопия. В таком случае дифференциация будет основываться на различном содержании аминокислот и лактата в опухолях и абсцессах головного мозга.
Иные способы диагностики и дифференциальной диагностики абсцесса головного мозга малоинформативны. Увеличение СОЭ, повышенное содержание С-реактивного белка в крови, лейкоцитоз, лихорадка — симптомокомплекс практически любых воспалительных процессов, включая внутричерепные. Бакпосевы крови при абсцессах головного мозга в 80-90% стерильны.
Лечение абсцесса головного мозга
На энцефалитической стадии абсцесса (анамнез – до 2 недель), а также в случае небольшого абсцесса головного мозга (до 3 см в диаметре) рекомендовано консервативное лечение, основой которого должна стать эмпирическая антибактериальная терапия. В некоторых случаях возможно проведение стереотаксической биопсии в целях окончательной верификации диагноза и выделения возбудителя.
Абсцессы, вызывающие дислокацию мозга и повышение внутричерепного давления, а также локализованные в зоне желудочковой системы (попадание гноя в желудочковую систему зачастую приводит к летальным исходам) — абсолютные показания к хирургическому вмешательству. Травматические абсцессы головного мозга, расположенные в зоне инородного тела также подлежат хирургическому лечению, так как данный воспалительный процесс не поддается консервативному лечению. Несмотря на неблагоприятный прогноз, грибковые абсцессы также являются абсолютным показанием к хирургическому вмешательству.
Противопоказанием к хирургическому лечению являются абсцессы мозга, расположенные в жизненно важных и глубинных структурах (зрительный бугор, ствол мозга, подкорковые ядра). В таких случаях возможно проведение стереотаксического метода лечения: пункция абсцесса мозга и его опорожнение с последующим промыванием полости и введением антибактериальных препаратов. Возможно как однократное, так и многократное (через установленный на несколько суток катетер) промывание полости.
Тяжелые соматические заболевания не являются абсолютным противопоказанием к проведению хирургического лечения, так как стереотаксическая операция может проводиться и под местной анестезией. Абсолютным противопоказанием к проведению операции может быть только крайне тяжелое состояние пациента (терминальная кома), так как в таких случаях любое оперативное вмешательство противопоказано.
Медикаментозное лечение
Целью эмпирической (в отсутствии посева или при невозможности выделения возбудителя) антибактериальной терапии является покрытие максимально возможного спектра возбудителей. Рекомендуемые программы лечения:
- При абсцессе головного мозга без ЧМТ или нейрохирургического вмешательства в анамнезе показан следующий алгоритм лечения: ванкомицин; цефалоспорины III поколения (цефотаксим, цефтриаксон, цефиксим); метронидазол. В случае посттравматического абсцесса головного мозга метронидазол заменяют на рифампицин.
- Возбудителем абсцесса головного мозга у пациентов с иммунодефицитными состояниями (кроме ВИЧ) чаще всего является Cryptococcus neoformans, реже Сandida spp или Aspergillius spp. Поэтому в данных случаях назначают амфоретицин В или липосомальный амфоретицин В. После исчезновения абсцесса (по данным нейровиуализационных исследований) применяют флуконазол в течение 10 недель, впоследствии дозу уменьшают вдвое и оставляют в качестве поддерживающей.
- У пациентов с ВИЧ возбудителем абсцесса головного мозга чаще всего является Toxoplasma gondii, поэтому эмпирическое лечение больных должно включать в себя сульфадиазин с пириметамином.
После выделения возбудителя из посева лечение необходимо изменить, учитывая антибиотикограмму. В случае стерильного посева следует продолжить эмпирическую антибактериальную терапию. Продолжительность интенсивной антибактериальной терапии — не менее 6 недель, после этого рекомендуется сменить антибиотики на пероральные и продолжить лечение еще 6 недель.
Назначение глюкокортикоидов оправдано только в случае адекватной антибактериальной терапии, так как только при положительном прогнозе глюкокортикоиды могут вызвать уменьшение выраженности и обратное развитие капсулы абсцесса головного мозга. В иных случаях их применение может вызвать распространение воспалительного процесса за пределы первичного очага.
Хирургическое лечение
Основными методами хирургического лечения внутримозговых абсцессов являются простое или приточно-отточное дренирование. Их суть заключается в установке в полость абсцесса катетера, через который осуществляется эвакуация гноя с последующим введением антибактериальных препаратов. Возможна установка второго катетера меньшего диаметра (на несколько суток), через который проводится инфузия раствора для промывания (чаще всего, 0,9 % раствора хлорида натрия). Дренирование абсцесса необходимо сопровождать антибактериальной терапией (сначала эмпирической, далее — с учетом чувствительности к антибиотикам выделенного патогена).
Стереотаксическая аспирация содержимого абсцесса без установки дренажа — альтернативный метод хирургического лечения абсцесса головного мозга. Главные его преимущества — снисходительные требования к квалификации медперсонала (для контроля над функционированием приточно-отточной системы необходимы пристальное внимание и специальные знания) и меньший риск вторичного инфицирования. Однако в 70% использования данного метода возникает необходимость повторных аспираций.
В случае множественных абсцессов головного мозга необходимо в первую очередь дренировать очаг, наиболее опасный в отношении осложнений (прорыв гноя в желудочковую систему, дислокация мозга), а также наиболее значимый в клинической картине. В случае эмпиемы или субдурального абсцесса головного мозга применяют дренирование, не используя приточно-отточную систему.
Прогноз при абсцессе головного мозга
В прогнозировании абсцессов головного мозга большое значение имеет возможность выделить возбудителя из посева и определить его чувствительность к антибиотикам, только в этом случае возможно проведение адекватной патогенетической терапии. Кроме этого, исход заболевания зависит от количества абсцессов, реактивности организма, адекватности и своевременности лечебных мероприятий. Процент летальных исходов при абсцессах головного мозга — 10%, инвалидизации — 50%. Почти у трети выживших пациентов последствием заболевания становится эпилептический синдром.
При субдуральных эмпиемах прогнозы менее благоприятны из-за отсутствия границ гнойного очага, так это свидетельствует высокой вирулентности возбудителя, либо о минимальной сопротивляемости пациента. Летальность в таких случаях — до 50%. Грибковые эмпиемы в сочетании с иммунодефицитными состояниями в большинстве случаев (до 95%) приводят к летальному исходу.
Эпидуральные эмпиемы и абсцессы головного мозга обычно имеют благоприятный прогноз. Проникновение инфекции через неповрежденную твердую мозговую оболочку практически исключено. Санация остеомиелитического очага позволяет устранить эпидуральную эмпиему. Своевременное и адекватное лечение первичных гнойных процессов, а также полноценная первичная обработка ран при ЧМТ позволяют в значительной степени снизить возможность развития абсцесса головного мозга.
1. Абсцессы головного мозга: диагностика и лечение/ Ырысов К.Б., Арстанбеков Н.А., Мамашарипов К.М.// Наука и новые технологии - 2011 - № 6
2. Современная терапия абсцесса головного мозга/ Амчеславский В.Г. , Шиманский В.Н. , Шатворян Б.Р. // РМЖ (Русский медицинский журнал) - 2000 - №13
3. Диагностика абсцессов головного мозга/Султанов Б.М., Ырысов К.Б., Мамашарипов К.М.// Вестник КГМА им. И.К. Ахунбаева. - 2012 - № 1
Аннотация научной статьи по клинической медицине, автор научной работы — Сотскова В.А., Колоколов О.В., Шульдяков А.А., Макаров Н.С.
Цель: обратить внимание специалистов на редкие случаи патологии нервной системы у ВИЧ-инфицированных пациентов. В работе описано клиническое наблюдение ВИЧ-позитивной пациентки 32 лет с абсцессом головного мозга. На фоне комплексного оперативного и медикаментозного лечения антиретровирусными препаратами удалось добиться хорошего вирусологического ответа и регресса неврологической симптоматики. Представленный клинический случай может быть полезен специалистам при определении тактики лечения абсцесса головного мозга у ВИЧ-инфицированных пациентов.
Похожие темы научных работ по клинической медицине , автор научной работы — Сотскова В.А., Колоколов О.В., Шульдяков А.А., Макаров Н.С.
Инфекционное поражение центральной нервной системы как вторичное проявление ВИЧ-инфекции (клиническое наблюдение)
Rare forms neurological disorders in an HIV-infected patient
The study aims paying the attention of specialists in rare cases of pathology of the nervous system in HIV-infected patients. The clinical case of brain abscess in a 32 year-old HIV-positive patient. Against the background of the surgical and antiretroviral treatment of brain abscess in HIV-positive patients it managed to achieve a virologic response and regression of neurological symptoms. Presented clinical case can be useful for specialists in determining the tactics of treatment of brain abscess in HIV-infected patients.
23. Nemni R, Corbo M, Fazio R, et al. Peripheral neuropathy in hepatitis C virus infection with and without cryoglobulinae-mia. J Neurol Neurosurg Psychiatry 2003; 74: 1267-1271.
24. Ooi WW, Srinivasan J. Leprosy and the peripheral nervous system: basic and clinical aspects. Muscle Nerve 2004; 30: 393-409.
25. Grisold W, Drlicek M. Paraneoplastic neuropathy. Curr Opin Neurol 1999; 12 (5): 617-625.
26. Schneider NA, Kantimirova EA. Paraneoplastic polyneuropathy: definition, etiology and pathogenesis, diagnosis. Siberian Health Review 2010; 1: 12-16. Russian (Шнайдер Н. А.,
Кантимирова Е. А. Паранеопластическая полинейропатия: дефиниция, этиопатогенез, диагностика. Сибирское медицинское обозрение 2010; 1: 12-16).
27. Forman AD. Peripheral neuropathy and cancer. Current oncology reports 2004; 6 (1): 20-25.
29. Smith AG, Singleton JR. The Diagnostic yield of a standardized approachto idiopathic sensory-predominant neuropathy. Arch Intern Med 2004; 164: 1021-1025.
РЕДКИЕ ФОРМЫ ПОРАЖЕНИЯ НЕРВНОЙ СИСТЕМЫ У ВИЧ-ИНФИЦИРОВАННЫХ ПАЦИЕНТОВ
RARE FORMS OF NEUROLOGICAL DISORDERS IN HIV-INFECTED PATIENTS
V. A. Sotskova — Saratov State Medical University n.a. V. I. Razumovsky of Ministry of Health of the Russian Federation, Department of Infectious Diseases, Postgraduate; O. V. Kolokolov — Saratov State Medical University n.a. V. I. Razumovsky^ of Ministry of Health of the Russian Federation, Head of the Department of Neurology n.a. K. N. Tretiakov, Postgraduate Education Faculty, Associate Professor, Doctor of Medical Science; A.A. Shuldyakov — Saratov State Medical University n.a. V.I. Razumovsky of Ministry of Health of the Russian Federation, Head of the Department of Infectious Diseases, Professor, Doctor of Medical Science; N. S. Makarov — Saratov State Medical University n.a. V. I. Razumovsky of Ministry of Health of the Russian Federation, Department of Neurology n.a. K. N. Tretiakov, Postgraduate Education Faculty, Associate Professor, Candidate of Medical Science.
Дата поступления — 01.06.2016 г. Дата принятия в печать — 09.06.2016 г.
Сотскова В. А., Колоколов О. В., Шульдяков А. А., Макаров Н. С. Редкие формы поражения нервной системы у ВИЧ-инфицированных пациентов. Саратовский научно-медицинский журнал 2016; 12 (2): 296-299.
Цель: обратить внимание специалистов на редкие случаи патологии нервной системы у ВИЧ-инфицированных пациентов. В работе описано клиническое наблюдение ВИЧ-позитивной пациентки 32 лет с абсцессом головного мозга. На фоне комплексного оперативного и медикаментозного лечения антиретровирусными препаратами удалось добиться хорошего вирусологического ответа и регресса неврологической симптоматики. Представленный клинический случай может быть полезен специалистам при определении тактики лечения абсцесса головного мозга у ВИЧ-инфицированных пациентов.
Ключевые слова: ВИЧ-инфекция, патология нервной системы, нейрохирургическое лечение, клинический случай.
Sotskova VA, Kolokolov OV, ShuldyakovAA, MakarovNS. Rare forms neurological disorders in an HIV-infected patient. Saratov Journal of Medical Scientific Research 2016; 12 (2): 296-299.
The study aims paying the attention of specialists in rare cases of pathology of the nervous system in HIV-infected patients. The clinical case of brain abscess in a 32 year-old HIV-positive patient. Against the background of the surgical and antiretroviral treatment of brain abscess in HIV-positive patients it managed to achieve a virologic response and regression of neurological symptoms. Presented clinical case can be useful for specialists in determining the tactics of treatment of brain abscess in HIV-infected patients.
Key words: HIV infection, pathology of the nervous system, neurosurgical treatment, clinical case.
Введение. Поражение нервной системы может наблюдаться на любой стадии ВИЧ-инфекции: в субклинической фазе у 20%, в стадии развернутой клинической картины болезни у 40-50%, в более поздних стадиях у 30-90% больных [1]. Причины первичных неврологических осложнений ВИЧ-инфекции различны: прямое повреждающее воздействие вируса на центральную нервную систему (ЦНС), аутоиммунные процессы, нейротоксический эффект, который оказывают как компоненты вируса, так и продукты иммунных реакций. Вторичные осложне-
ния связаны с оппортунистическими инфекциями и опухолями, а также нейротоксическим действием некоторых противовирусных средств. Несмотря на широкую доступность и использование антиретрови-русной терапии (АРВТ), оппортунистические инфекции по-прежнему являются частой причиной заболеваемости и смертности среди лиц, инфицированных ВИЧ [2].
В структуре вторичных (оппортунистических) инфекций, поражающих нервную систему, первое место отводят цитомегаловирусной инфекции (ЦМВ), второе — туберкулезу, третье — токсоплазмозу [3]. Вместе с другими поражениями (лимфома и цере-броваскулярные заболевания) они составляют от
80 до 90% неврологических синдромов при ВИЧ-инфекции [4].
Еще одним примером редкого поражения нервной системы при ВИЧ-инфекции служит метаста-зирование саркомы Капоши (СК) в головной мозг. Данная патология крайне редко встречается у ВИЧ-инфицированных больных, особенно после введения в практику врачей-инфекционистов ВААРТ. К примеру, в работе M. J. Mossakowski, I. B. Zelman приводятся данные результатов патологоанатомического исследования мозга ста больных, умерших от СПИДа в период 1987-1995 гг., среди них был выявлен лишь один случай метастазов саркомы в головной мозг [6].
(ЦСЖ) исследована методом ПЦР, по результатам которого обнаружено высокое содержание вируса JC (45 млн копий в 1 мл), установлен диагноз прогрессирующей мультифокальной лейкоэнцефало-патии (ПМЛ). Через 8 недель после начала ВААРТ вирусная нагрузка ВИЧ в плазме составила менее 75 копий в 1 мл, но уровень CD4-лимфоцитов снизился до 24 клеток в 1 мл. У пациентки развилась тяжелая моторная и сенсорная афазия, правосторонняя го-монимная гемианопсия, правосторонний гемипарез. Через 5 месяцев после начала терапии больная скончалась.
Особый интерес представляют данные, иллюстрирующие сочетанное поражение головного и спинного мозга при ВИЧ-инфекции и сложности дифференциальной диагностики, в частности развитие бокового амиотрофического склероза (БАС; ALS) у больных с ВИЧ-инфекцией.
БАС наиболее часто развивается на шестом десятилетии жизни и приводит к смерти в течение 3-5 лет, с ежегодной всемирной заболеваемостью примерно 2х10-5 [9]. В 5-10% случаев БАС имеет наследственный характер, в то время как остальные случаи являются спорадическими. Несмотря на обширные исследования, этиология БАС остается невыясненной. Мутация гена супероксиддисмутазы (SODv MIM 147450) в локусе 21q22.1 была идентифицирована в 20% семейных случав БАС. Исследовательские группы, занимающиеся поиском причины развития спорадических случаев БАС, ранее обнаружили в сыворотке больных обратную транскриптазу, фермент, являющийся продуктом деятельности ре-тровирусов, в том числе и ВИЧ.
В 2001 г. A. Moulignier et al. [10] сообщили о шести случаях ВИЧ-ассоциированного БАС (HALS). Ученые провели ретроспективное исследование 1700 ВИЧ-инфицированных с патологией нервной системы за 13-летний период. Шесть пациентов с ВИЧ и выраженной иммунодепрессией (средний уровень CD4-лимфоцитов 86,2 в 1 мм3) имели клинические симптомы БАС. Иные, кроме ВИЧ-инфекции, причины развития БАС в этих случаях были исключены. Необычно быстрое развитие болезни и положительный ответ от ВААРТ позволили предположить, что синдром БАС ассоциирован с ВИЧ-инфекцией.
Клинически HALS отличается от БАС (ALS) по нескольким аспектам: более молодым возрастом дебюта заболевания, быстрым прогрессированием, высоким содержанием белка в ЦСЖ и частичным клиническим улучшением на фоне приема АРВТ. В отличие от неизменного прогрессирования БАС, исход HALS на воне применения ВААРТ может быть вариабельным: от летального до благоприятного (описано полное выздоровление). Поэтому из-за потенциальной обратимости БАС у ВИЧ-инфицированных пациентов тестирование на ВИЧ-инфекцию в каждом случае БАС оправдано у всех лиц с высоким риском заражения ВИЧ.
Описание клинического случая. Больная 32 лет поступила в нейрохирургическое отделение многопрофильного стационара г. Саратова с диагнозом: «Подозрение на внутримозговую опухоль лобной и теменной
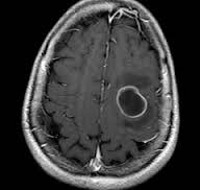
Рис. 1. МРТ головы. Признаки объемного образования (абсцесса головного мозга) у ВИЧ-позитивной пациентки 32 лет
При поступлении состояние больной оценивалось как тяжелое. Пациентка предъявляла жалобы на слабость, головную боль, чувство слабости в правой руке, невнятность речи, которые появились за неделю до госпитализации. При осмотре больная находилась в сознании, полностью ориентирована в месте и времени. Но к своему состоянию некритична. В неврологическом статусе отмечались элементы моторной афазии, нарушение двигательной функции в виде снижения активности движений в конечностях, монопареза в правой руке со снижением мышечной силы до 2-3 баллов, усиление справа карпорадиаль-ного и биципитального рефлексов. Других изменений выявлено не было.
К вечеру у больной развился генерализованный судорожный припадок, продолжительностью около трех минут, после которого ее состояние ухудшилось: усугубилась общемозговая симптоматика, наросли элементы моторной афазии. По экстренным показаниям проведено МР-исследование головного мозга с контрастным усилением во фронтальной, аксиальной и сагиттальной проекциях срезами толщиной 4 мм, шагом 4,5 мм, в режимах Т и Т2. На серии полученных томограмм в левой лобно-теменной области была выявлена зона неоднородного измененного МР-сигнала с наличием конвексиально расположенного объемного образования 15^16x17 мм, кольцевидно накапливающее контрастное вещество, и зоны перифокального отека неправильной формы 56x49x42 мм. Изменения были расценены как МР-признаки опухоли левой лобно-теменной области.
На следующий день по жизненным показаниям была выполнена костно-пластическая трепанация черепа в левой лобно-теменной области с удалением внутримозговой опухоли.
Отсутствие перед операцией результата анализа на ВИЧ-инфекцию способствовало настороженности персонала, и хирургическое вмешательство проводилось с использованием всех необходимых мер предосторожности. Положительный результат исследования крови на антитела к ВИЧ методом иммуно-ферментного анализа (ИФА) был получен уже после оперативного вмешательства.
Рис. 2. МРТ головы. Состояние через 7 месяцев после хирургического удаления абсцесса головного мозга у ВИЧ-позитивной пациентки 32 лет
После оперативного вмешательства в раннем периоде у больной наблюдалась правосторонняя геми-плегия, сенсорная и моторная афазия, парез мышц, иннервируемых VII и XII черепными нервами справа по центральному типу, субфебриллитет.
Помимо хирургического лечения в стационаре пациентка получала антибактериальную (це-фалоспорины 3-го поколения), противовирусную и противоотечную терапию. На фоне проводимого медикаментозного лечения состояние пациентки улучшилось: частично регрессировали расстройства речи, появились движения в правой руке, температура тела нормализовалась.
Уже через месяц после начала АРВТ вирусная нагрузка уменьшилась практически в 2 раза, однако CD4-лимфоциты остались на прежнем уровне. Через 2 месяца вирусная нагрузка в крови составила менее 30 копий/мл, уровень CD4-лимфоцитов начал расти (до 56 в 1 мл).
На МРТ головного мозга, выполненного через 7 месяцев после оперативного лечения и начала ВА-АРТ, ухудшений не обнаружено; выявлены признаки вторичных изменений в обеих гемисферах головного мозга, послеоперационные изменения в левой лоб-но-теменной области (рис. 2).
Через 2 года после начала ВААРТ вирусная нагрузка в крови не определялась (менее 20 копий в 1 мл), а уровень CD4-лимфоцитов вырос почти в 6 раз и составил 294 в 1 мл.
Самочувствие больной улучшилось, явления ге-мипареза и афазии уменьшились.
Заключение. Важной задачей любого практикующего врача является своевременная диагностика
ВИЧ-инфекции и ее неврологических осложнений как на ранних, так и на поздних стадиях инфекционного процесса. Любое неврологическое заболевание, особенно у лиц молодого возраста, характеризующееся быстрым нарастанием неврологического дефицита, может является проявлением ВИЧ-инфекции.
Рост количества ВИЧ-инфицированных, особенно в стадии глубокого иммунодефицита, требует настороженности врачей в отношении ВИЧ-инфекции вследствие высокой возможности появления данной категории пациентов в неврологических и нейрохирургических стационарах.
При лечении подобной группы пациентов следует помнить, что назначение ВААРТ является важным компонентом комплексного лечения сочетанной патологии при ВИЧ-инфекции и позволяет снизить риск летальных исходов.
Конфликт интересов не заявляется.
Авторский вклад: концепция и дизайн исследования — В. А. Сотскова, О. В. Колоколов, А. А. Шуль-дяков; получение данных — В. А. Сотскова; анализ данных — В. А. Сотскова, О. В. Колоколов, А. А. Шуль-дяков; интерпретация результатов — В. А. Сотскова, О. В. Колоколов, А. А. Шульдяков; написание статьи — В. А. Сотскова., О. В. Колоколов, А. А. Шульдяков, Н. С. Макаров; утверждение рукописи для публикации — О. В. Колоколов, А. А. Шульдяков.
1. Yakovlev NA, Zhulev NM, Slyusar TA. NeuroAIDS: Neurological disorders in HIV/AIDS. Moscow: MIA, 2005; 67161 p. Russian (Яковлев Н. А., Жулев Н. М., Слюсарь Т. А. Ней-роспид: Неврологические расстройства при ВИЧ-инфекции/ СПИДе. М.: МИА, 2005; 67-161 с.).
2. Ogbuagu O, Villanueva M. Extensive central nervous system cryptococcal disease presenting as immune reconstitution syndrome in a patient with advanced HIV: report of a case and review of management dilemmas and strategies. Infectious disease reports 2014; 6 (4): 5576.
3. Leonova ON, Stepanova EV, Fomenkova NV. Neurological pathology in HIV patiens as follows form experience gained at palliative care department. HIV Infection and Immunosuppressive Disorders 2011; 3 (2): 62-69. Russian (Леонова О. Н., Степанова Е. В., Фоменкова Н. В. и др. Поражения нервной системы у больных с ВИЧ-инфекцией на опыте работы отделения паллиативной медицины. ВИЧ-инфекция и иммуносупрессии 2011; 3 (2): 62-69).
4. Belyakov nA, Rakhmanova AG. Human immunodeficiency virus — medicine. St. Petersburg: Baltic Medical Educational Center, 2012; 656 p. Russian (Беляков Н. А., Рахманова А. Г. Вирус иммунодефицита человека — медицина. СПб.: Балтийский медицинский образовательный центр, 2012; 656 с.).
5. Marcela C, Phung MK, Ahmed R, et al. A Woman with HIV Infection, Brain Abscesses and Eosinophilia. Clinical infectious diseases 2010; 50 (2): 239-277.
6. Baldin F, Baiocchini A, Schinina V, et al. Brain localization of Kaposi's sarcoma in a patient treated by combination antiretroviral therapy. BMC infectious diseases 2013; 13 (1): 600.
7. Mossakowski MJ, Zelman IB. Neuropathological syndromes in the course of full blown acquired immune deficiency syndrome (AIDS) in adults in Poland (1987-1995). Folia neuropathologica/ Association of Polish Neuropathologists and Medical Research Centre, Polish Academy of Sciences 1996; 35 (3): 133-143.
8. Gheuens S, Cheeseman SH, Koralnik iJ. Hidden in plain view: emergence of Progressive Multifocal Leukoencephalopathy after treatment of CNS Toxoplasmosis. Acta neurologica Belgica 2011; 111 (3): 217-9.
9. Logroscino G, Traynor BJ, Hardiman O, et al. Incidence of amyotrophic lateral sclerosis in Europe. Journal of Neurology, Neurosurgery & Psychiatry 2010; 81 (4): 385-390.
10. Moulignier A, Moulonguet A, Pialoux G, et al. Reversible ALS-like disorder in HIV infection. Neurology 2001; 57 (6): 995-1001.
Читайте также:

