Анаэробная инфекция в хирургии пути передачи
Обновлено: 17.04.2024
Патологические процессы, возникающие в тканях, различных органах в результате проникновения в них болезнетворных возбудителей (микроорганизмов), требующие применения хирургического вмешательства, и послеоперационные осложнения входят в понятие о хирургической инфекции. Воспалительные заболевания, основой которых является инфекционный процесс, составляют третью часть болезней хирургического характера.
Пути заражения
Хирургическая инфекция имеет следующие источники происхождения: внешний (экзогенный) и внутренний (эндогенный).
Заражение извне происходит несколькими путями:
- через воздух,
- имплантационным,
- через контакты,
- капельным.
Контактная инфекция развивается при бытовых травмах, производственных повреждениях кожного покрова и слизистых, при попадании в них микробов, при контакте с инфицированными животными (царапины) или с повреждающим предметом, а также от остатков инородных тел (щепки или осколки). Может произойти контактное заражение инфекцией в области хирургического вмешательства в результате использования инструментов (тампоны, шовный материал) с недостаточной стерилизацией.
Имплантационная хирургическая инфекция может развиться после наложения швов или после установки протезов. Существуют различные состояния организма (переохлаждение, сахарный диабет, ушибы тканей, авитаминоз, переутомление, вирусная инфекция), ослабляющие иммунную систему, которая в таком виде становится дополнительным источником для интенсивного развития воспалительного процесса.
Капельный путь заражения – это попадание микробов на пораженную поверхность с каплями слюны, пота или выделений из носа.
Воздушным путем микробы проникают в рану с частицами пыли в момент проведения операции.
Физические (кровопотеря, низкая или высокая температура, радиационное излучение), химические факторы также способствуют заражению и дальнейшему развитию инфекционного процесса.
Укрепление иммунитета, выявление и ликвидация до начала операции любых очагов внутренней инфекции (например, гнилостные полости или кариозные зубы – эндогенные очаги) являются обязательными условиями для предупреждения возникновения осложнений и развития различного рода инфекций в области хирургического вмешательства.
Классификация хирургической инфекции
Данные инфекции по клиническому течению делятся на острую форму и хроническую.
Острая форма, в свою очередь, имеет несколько разновидностей:
- гнойная (аэробная);
- анаэробная (газовая);
- гнилостная;
- специфическая хирургическая инфекция (дифтерия, язва сибирская, столбняк).
К хронической форме имеют отношение:
- неспецифические хирургические инфекции (серозно-гнойная и гнойная);
- специфическая (например, актиномикоз, сифилис, туберкулез).
По форме распространения:
По виду микробов (возбудителей):
- стрептококковая;
- стафилококковая;
- гонококковая;
- пневмококковая;
- колибациллярная;
- анаэробная (клостридиальная и неспорообразующая).
По количеству микроорганизмов:
- моноинфекция (один возбудитель);
- полиинфекция (смешанная форма).
По месту локализации выделяют следующие воспалительные процессы:
- заражение кожного покрова и подкожной клетчатки (флегмона, карбункул, рожистое воспаление, абсцесс);
- воспаление мозговой оболочки;
- поражение костной ткани, суставов (артрит, остеомиелит);
- воспаление железистых органов (лимфаденит, мастит);
- воспаление органов таза;
- поражения в области брюшной полости;
- воспаление слизистых оболочек (легкие, плевральная полость, грудная клетка).
Острая форма инфекции
Гнойная инфекция острой формы вызывается кишечной, синегнойной палочками и разнообразными кокками. На проникновение данных возбудителей организм проявляет реакции местного и общего видов.
Местный вид реакции
Для данной реакции характерно покраснение кожного покрова, отек, болезненность в области повреждения, повышение температуры тела. При тяжелой форме в очаге заражения происходит прогрессирование гнойного воспаления.
Параллельно с местной реакцией тканей начинается развитие общей. При высокой степени заражения организма, происходящей в результате отравления выделениями микробов, у больного развиваются следующие симптомы: боль в голове, лихорадка, общее недомогание, затемнение в глазах, учащение пульса, потеря сознания, снижение давления, возбуждение или слабость.
При проведении анализов выявляются изменения в составе крови, обнаруживаются сбои в функционировании почек, печени, которые по клинической картине аналогичны с сепсисом и другими патологиями (бруцеллез и тиф).
Сепсис относится к общей гнойной инфекции и является тяжелым заболеванием с такими клиническими проявлениями, как: температура тела от 40 и более градусов, тахикардия, озноб, возникновение галлюцинаций, желтушность кожи, кожная сыпь, увеличение объема селезенки. В качестве осложнения развивается септический шок.
При несвоевременном лечении сепсис может привести к летальному исходу, поэтому при возникновении перечисленных проявлений следует незамедлительно обратиться к специалисту для проведения комплексного терапевтического и хирургического лечения при стационаре.
Эта форма хирургической инфекции развивается при присутствии в зоне заражения различных инородных тел, нарушений оттока отделений из раны. Развитие процесса воспаления имеет вялое начало, но в дальнейшем способствует спаду работоспособности.
Реакция организма на заражение при хронической форме развивающихся инфекционных заболеваний имеет специфический характер для каждого из них, что ускоряет диагностирование. При туберкулезе суставов появляются характерные симптомы: мышцы атрофируются, суставы теряют подвижность, появляются свищи. На заражение актиномикозом указывают изменения кожного покрова и образующиеся свищи, содержащие гной.
Методы диагностики
Помимо внешних симптомов заражения для установления правильного диагноза проводят дополнительные методы исследования:
- Инструментальные (рентгенография и рентгеноскопия, ультразвуковое сканирование и компьютерная томография, диагностические пункции, торакоскопия, лапароскопия) определяют очаг воспаления, его характер, скопление гноя в органах, тканях и внутренних органах;Томография
- Лабораторные (общий, биохимический анализы крови, анализ мочи) позволяют установить глубину нарушений, уровень интоксикации и дают представление о прогнозе развития воспалительного процесса;
- Микробиологические (бактериоскопия мазка, частица ткани, спинномозговая жидкость, моча, мокрота или кровь) идентифицируют возбудителя.
- Иммунологические способы определяют состояние иммунитета пациента.
Диагностика заболеваний инфекционного характера должна проводиться с использованием всех способов исследования в комплексе.
Лечебные методы
Терапия хирургической инфекции проводится с учетом вида возбудителя, фазы воспаления и индивидуальных свойств организма пациента. Лечебные мероприятия состоят из местного, консервативного, физиотерапевтического, комбинированного и оперативного способов лечения.
Оперативное вмешательство играет основную роль в лечении, так как позволяет ликвидировать гнойный очаг, остановить распространение воспаления, снизить интоксикацию организма.
Меры профилактики
Избежать заражения и развития острых форм осложнений помогает профилактика хирургической инфекции, заключающаяся:
- в применении асептики и антисептики;
- в дезинфекции, стерилизации хирургических инструментов, постельного белья, перевязочного материала;
- в содержании в чистоте одежды, в соблюдении тщательной гигиены рук медицинского персонала;
- в систематической санитарной обработке палаты пациента, операционного блока и всего хирургического отделения.
Профилактика хирургической инфекции требует обязательного соблюдения всех правил до, во время и после проведения операции.
Сестринская помощь при хирургической инфекции
Так как хирургическая инфекция, особенно в острой форме, подлежит лечению в специализированных отделениях, то подготовка квалифицированного медицинского персонала имеет большое значение. Сестринская помощь при хирургической инфекции заключается в правильном уходе за пациентом и состоит:
- из введения инъекций, раздачи таблеток, выполнения различных процедур (измерение температуры, постановка клизм, перевязки);
- из контроля над соблюдением режима отделения, правил гигиены и режима питания;
- из стерилизации, дезинфекции хирургических инструментов. Сестринская помощь
Не только квалифицированный уход и лечебные мероприятия входят в обязанности младшего медицинского персонала, но и заполнение специальных документов:
- журнал назначений;
- тетрадь передачи дежурств;
- журнал о проведении перевязок;
- журнал учета дефицитных лекарств;
- журнал списания спирта, расхода перевязочных средств;
- журнал учета инструментария и его обработки;
- журнал кварцевания;
- журнал учета санитарной обработки всех помещений отделения;
- журнал регистрации осложнений и учета прививок от столбняка.
Медицинским сестрам необходимо постоянно повышать уровень своих знаний и навыков. Инфекция в хирургии является серьезной проблемой, поэтому изучение новейших технологий, посещение семинаров, прослушивание лекций обучающего характера являются обязательными условиями для данной специальности.
Прослушивание лекции о принципах медицинской этики необходимо для воспитания нравственного, заботливого, ответственного отношения медицинского работника к пациенту, а также для развития умения устанавливать психологический контакт с больными разных возрастных категорий.
Лекция о возможных ошибках, нарушении обязанностей в профессиональной деятельности медицинской сестры поможет избежать проступков в работе и убережет от уголовной ответственности.
Установлению атмосферы взаимопомощи, доверия, взаимоуважения между членами медицинского коллектива посвящено большое количество лекций на данную тему.
Внутрибольничные инфекции – различные инфекционные заболевания, заражение которыми произошло в условиях лечебного учреждения. В зависимости от степени распространения различают генерализованные (бактериемию, септицемию, септикопиемию, бактериальный шок) и локализованные формы внутрибольничных инфекций (с поражением кожи и подкожной клетчатки, дыхательной, сердечно-сосудистой, урогенитальной системы, костей и суставов, ЦНС и т. д.). Выявление возбудителей внутрибольничных инфекций проводится с помощью методов лабораторной диагностики (микроскопических, микробиологических, серологических, молекулярно-биологических). При лечении внутрибольничных инфекций используются антибиотики, антисептики, иммуностимуляторы, физиотерапия, экстракорпоральная гемокоррекция и т. д.

Общие сведения
Внутрибольничные (госпитальные, нозокомиальные) инфекции - инфекционные заболевания различной этиологии, возникшие у пациента или медицинского сотрудника в связи с пребыванием в лечебно-профилактическом учреждении. Инфекция считается внутрибольничной, если она развилась не ранее 48 часов после поступления больного в стационар. Распространенность внутрибольничных инфекций (ВБИ) в медицинских учреждениях различного профиля составляет 5-12%. Наибольший удельный вес внутрибольничных инфекций приходится на акушерские и хирургические стационары (отделения реанимации, абдоминальной хирургии, травматологии, ожоговой травмы, урологии, гинекологии, отоларингологии, стоматологии, онкологии и др.). Внутрибольничные инфекции представляют собой большую медико-социальную проблему, поскольку утяжеляют течение основного заболевания, увеличивают длительность лечения в 1,5 раза, а количество летальных исходов - в 5 раз.

Этиология и эпидемиология внутрибольничных инфекций
Основными возбудителями внутрибольничных инфекций (85% от общего числа) выступают условно-патогенные микроорганизмы: грамположительные кокки (эпидермальный и золотистый стафилококк, бета-гемолитический стрептококк, пневмококк, энтерококк) и грамотрицательные палочковидные бактерии (клебсиеллы, эшерихии, энтеробактер, протей, псевдомонады и др.). Кроме этого, в этиологии внутрибольничных инфекций велика удельная роль вирусных возбудителей простого герпеса, аденовирусной инфекции, гриппа, парагриппа, цитомегалии, вирусных гепатитов, респираторно-синцитиальной инфекции, а также риновирусов, ротавирусов, энтеровирусов и пр. Также внутрибольничные инфекции могут быть вызваны условно-патогенными и патогенными грибами (дрожжеподобными, плесневыми, лучистыми). Особенностью внутригоспитальных штаммов условно-патогенных микроорганизмов служит их высокая изменчивость, лекарственная резистентность и устойчивость к воздействию факторов среды (ультрафиолета, дезинфектантов и пр.).
Источниками внутрибольничных инфекций в большинстве случаев выступают пациенты или медицинский персонал, являющиеся бактерионосителями или больными стертыми и манифестными формами патологии. Как показывают исследования, роль третьих лиц (в частности, посетителей стационаров) в распространении ВБИ невелика. Передача различных форм госпитальной инфекции реализуется с помощью воздушно-капельного, фекально-орального, контактного, трансмиссивного механизма. Кроме этого, возможен парентеральный путь передачи внутрибольничной инфекции при проведении различных инвазивных медицинских манипуляций: забора крови, инъекций, вакцинации, инструментальных манипуляций, операций, ИВЛ, гемодиализа и пр. Таким образом в медучреждении возможно заразиться гепатитами В, С и D, гнойно-воспалительными заболеваниями, сифилисом, ВИЧ-инфекцией. Известны случаи внутрибольничных вспышек легионеллеза при приеме больными лечебного душа и вихревых ванн.
Факторами, участвующими в распространении внутрибольничной инфекции, могут выступать контаминированные предметы ухода и обстановки, медицинский инструментарий и аппаратура, растворы для инфузионной терапии, спецодежда и руки медперсонала, изделия медицинского назначения многоразового использования (зонды, катетеры, эндоскопы), питьевая вода, постельные принадлежности, шовный и перевязочный материал и мн. др.
Значимость тех или иных видов внутрибольничной инфекции во многом зависит от профиля лечебного учреждения. Так, в ожоговых отделениях преобладает синегнойная инфекция, которая в основном передается через предметы ухода и руки персонала, а главным источником внутрибольничной инфекции являются сами пациенты. В учреждениях родовспоможения основную проблему представляет стафилококковая инфекция, распространяемая медицинским персоналом-носителем золотистого стафилококка. В урологических отделениях доминирует инфекция, вызываемая грамотрицательной флорой: кишечной, синегнойной палочкой и др. В педиатрических стационарах особую значимость имеет проблема распространения детских инфекций – ветряной оспы, эпидемического паротита, краснухи, кори. Возникновению и распространению внутрибольничной инфекции способствуют нарушение санитарно-эпидемиологического режима ЛПУ (несоблюдение личной гигиены, асептики и антисептики, режима дезинфекции и стерилизации, несвоевременное выявление и изоляция лиц-источников инфекции и т. д.).
К группе риска, в наибольшей степени подверженной развитию внутрибольничной инфекции, относятся новорожденные (особенно недоношенные) и дети раннего возраста; пожилые и ослабленные пациенты; лица, страдающие хроническими заболеваниями (сахарным диабетом, болезнями крови, почечной недостаточностью), иммунодефицитом, онкопатологией. Восприимчивость человека к внутрибольничным инфекциям увеличивается при наличии у него открытых ран, полостных дренажей, внутрисосудистых и мочевых катетеров, трахеостомы и других инвазивных устройств. На частоту возникновения и тяжесть течения внутрибольничной инфекции влияет долгое нахождение пациента в стационаре, длительная антибиотикотерапия, иммуносупрессивная терапия.
Классификация внутрибольничных инфекций
По длительности течения внутрибольничные инфекции делятся на острые, подострые и хронические; по тяжести клинических проявлений – на легкие, среднетяжелые и тяжелые формы. В зависимости от степени распространенности инфекционного процесса различают генерализованные и локализованные формы внутрибольничной инфекции. Генерализованные инфекции представлены бактериемией, септицемией, бактериальным шоком. В свою очередь, среди локализованных форм выделяют:
- инфекции кожи, слизистых и подкожной клетчатки, в т. ч. послеоперационных, ожоговых, травматических ран. В частности, к их числу относятся омфалит, абсцессы и флегмоны, пиодермия, рожа, мастит, парапроктит, грибковые инфекции кожи и др.
- инфекции полости рта (стоматит) и ЛОР-органов (ангина, фарингит, ларингит, эпиглоттит, ринит, синусит, отит, мастоидит)
- инфекции бронхолегочной системы (бронхит, пневмония, плеврит, абсцесс легкого, гангрена легкого, эмпиема плевры, медиастинит)
- инфекции пищеварительной системы (гастрит, энтерит, колит, вирусные гепатиты)
- глазные инфекции (блефарит, конъюнктивит, кератит)
- инфекции урогенитального тракта (бактериурия, уретрит, цистит, пиелонефрит, эндометрит, аднексит)
- инфекции костно-суставной системы (бурсит, артрит, остеомиелит)
- инфекции сердца и сосудов (перикардит, миокардит, эндокардит, тромбофлебиты).
- инфекции ЦНС (абсцесс мозга, менингит, миелит и др.).
Диагностика внутрибольничных инфекций
Критериями, позволяющими думать о развитии внутрибольничной инфекции, служат: возникновение клинических признаков заболевания не ранее чем через 48 часов после поступления в стационар; связь с проведением инвазивного вмешательства; установление источника инфекции и фактора передачи. Окончательное суждение о характере инфекционного процесса получают после идентификации штамма возбудителя с помощью лабораторных методов диагностики.
Для исключения или подтверждения бактериемии проводится бактериологический посев крови на стерильность, желательно не менее 2-3-х раз. При локализованных формах внутрибольничной инфекции микробиологическое выделение возбудителя может быть произведено из других биологических сред, в связи с чем выполняется посев мочи, кала, мокроты, отделяемого ран, материала из зева, мазка с конъюнктивы, из половых путей на микрофлору. Дополнительно к культуральному методу выявления возбудителей внутрибольничных инфекций используются микроскопия, серологические реакции (РСК, РА, ИФА, РИА), вирусологический, молекулярно-биологический (ПЦР) методы.
Лечение внутрибольничных инфекций
Сложности лечения внутрибольничной инфекции обусловлены ее развитием в ослабленном организме, на фоне основной патологии, а также резистентностью госпитальных штаммов к традиционной фармакотерапии. Больные с диагностированными инфекционными процессами подлежат изоляции; в отделении проводится тщательная текущая и заключительная дезинфекция. Выбор противомикробного препарата основывается на особенностях антибиотикограммы: при внутрибольничной инфекции, вызванной грамположительной флорой наиболее эффективен ванкомицин; грамотрицательными микроорганизмами – карбапенемы, цефалоспорины IV поколения, аминогликозиды. Возможно дополнительное применение специфических бактериофагов, иммуностимуляторов, интерферона, лейкоцитарной массы, витаминотерапии.
При необходимости проводится чрескожное облучение крови (ВЛОК, УФОК), экстракорпоральная гемокоррекция (гемосорбция, лимфосорбция). Симптоматическая терапия осуществляется с учетом клинической формы внутрибольничной инфекции с участием специалистов соответствующего профиля: хирургов, травматологов, пульмонологов, урологов, гинекологов и др.
Профилактика внутрибольничных инфекций
Основные меры профилактики внутрибольничных инфекций сводятся к соблюдению санитарно-гигиенических и противоэпидемических требований. В первую очередь, это касается режима дезинфекции помещений и предметов ухода, применения современных высокоэффективных антисептиков, проведения качественной предстерилизационной обработки и стерилизации инструментария, безукоснительного следования правилам асептики и антисептики.
Медицинский персонал должен соблюдать меры индивидуальной защиты при проведении инвазивных процедур: работать в резиновых перчатках, защитных очках и маске; осторожно обращаться с медицинским инструментарием. Большое значение в профилактике внутрибольничных инфекций имеет вакцинация медработников от гепатита В, краснухи, гриппа, дифтерии, столбняка и других инфекций. Все сотрудники ЛПУ подлежат регулярному плановому диспансерному обследованию, направленному на выявление носительства патогенов. Предупредить возникновение и распространение внутрибольничных инфекций позволит сокращение сроков госпитализации пациентов, рациональная антибиотикотерапия, обоснованность проведения инвазивных диагностических и лечебных процедур, эпидемиологический контроль в ЛПУ.
Анаэробная инфекция – это инфекционный процесс, вызываемый спорообразующими или неспорообразующими микроорганизмами в условиях, благоприятных для их жизнедеятельности. Характерными клиническими признаками анаэробной инфекции служат преобладание симптомов эндогенной интоксикации над местными проявлениями, гнилостный характер экссудата, газообразующие процессы в ране, быстро прогрессирующий некроз тканей. Анаэробная инфекция распознается на основании клинической картины, подтвержденной результатами микробиологической диагностики, газожидкостной хроматографии, масс-спектрометрии, иммуноэлектрофореза, ПЦР, ИФА и др. Лечение анаэробной инфекции предполагает радикальную хирургическую обработку гнойного очага, интенсивную дезинтоксикационную и антибактериальную терапию.
МКБ-10
Общие сведения
Анаэробная инфекция – патологический процесс, возбудителями которого выступают анаэробные бактерии, развивающиеся в условиях аноксии (отсутствия кислорода) или гипоксии (низкого напряжения кислорода). Анаэробная инфекция представляет собой тяжелую форму инфекционного процесса, сопровождающуюся поражением жизненно важных органов и высоким процентом летальности. В клинической практике с анаэробной инфекцией приходится сталкиваться специалистам в области хирургии, травматологии, педиатрии, нейрохиругии, отоларингологии, стоматологии, пульмонологии, гинекологии и других медицинских направлений. Анаэробная инфекция может возникнуть у пациентов любого возраста. Доля заболеваний, вызываемых анаэробной инфекцией, точно не известна; из гнойных очагов в мягких тканях, костях или суставах анаэробы высеваются примерно в 30% случаев; анаэробная бактериемия подтверждается в 2-5% случаев.

Причины
Анаэробы входят в состав нормальной микрофлоры кожи, слизистых оболочек, желудочно-кишечного тракта, органов мочеполовой системы и по своим вирулентным свойствам являются условно-патогенными. При определенных условиях они становятся возбудителями эндогенной анаэробной инфекции. Экзогенные анаэробы присутствуют в почве и разлагающихся органических массах и вызывают патологический процесс при попадании в рану извне. Анаэробные микроорганизмы делятся на:
- Факультативные. Способны выживать как в отсутствии, так и в присутствии кислорода. К ним принадлежат кишечная палочка, шигеллы, иерсинии, стрептококки, стафилококки и др.
- Облигатные. Их развитие и размножение осуществляется в бескислородной среде. Облигатные возбудители делятся на две группы:
- спорообразующие (клостридии) - являются возбудителями клостридиозов экзогенного происхождения (столбняка, газовой гангрены, ботулизма, пищевых токсикоинфекций и др.);
- неспорообразующие (неклостридиальные) анаэробы (фузобактерии, бактероиды, вейллонеллы, пропионибактерии, пептострептококки и др.). В большинстве случаев вызывают гнойно-воспалительные процессы эндогенной природы (абсцессы внутренних органов, перитонит, пневмонию, флегмоны челюстно-лицевой области, отит, сепсис и др.).
Факторы риска
Условиями, благоприятствующими развитию анаэробной инфекции, являются повреждение анатомических барьеров с проникновением анаэробов в ткани и кровеносное русло, а также снижение окислительно-восстановительного потенциала тканей (ишемия, кровотечение, некроз). Попадание анаэробов в ткани может происходить при оперативных вмешательствах, инвазивных манипуляциях (пункциях, биопсии, экстракции зуба и др.), перфорации внутренних органов, открытых травмах, ранениях, ожогах, укусах животных, синдроме длительного сдавления, криминальных абортах и т. д. Факторами, способствующими возникновению анаэробной инфекции, выступают:
- массивное загрязнение ран землей;
- наличие инородных тел в ране;
- гиповолемический и травматический шок;
- сопутствующие заболевания (коллагенозы, сахарный диабет, опухоли);
- иммунодефицит.
Кроме этого, большое значение имеет нерациональная антибиотикотерапия, направленная на подавление сопутствующей аэробной микрофлоры.
Патогенез
Основными факторами патогенности анаэробных микроорганизмов служат их количество в патологическом очаге, биологические свойства возбудителей, наличие бактерий-ассоциантов. В патогенезе анаэробной инфекции ведущая роль принадлежит продуцируемым микроорганизмами ферментам, эндо- и экзотоксинам, неспецифическим факторам метаболизма. Так, ферменты (гепариназа, гиалуронидаза, коллагеназа, дезоксирибонуклеаза) способны усиливать вирулентность анаэробов, деструкцию мышечной и соединительной тканей.
Эндо- и экзотоксины вызывают повреждение эндотелия сосудов, внутрисосудистый гемолиз и тромбоз. Кроме этого, некоторые клостридиальные токисины обладают нефротропным, нейротропным, кардиотропным действием. Также токсическое влияние на организм оказывают и неспецифические факторы метаболизма анаэробов - индол, жирные кислоты, сероводород, аммиак.
Классификация
В зависимости от локализации различают анаэробную инфекцию:
- центральной нервной системы (абсцесс мозга, менингит, субдуральная эмпиема и др.)
- головы и шеи (пародонтальный абсцесс, ангина Людвига, средний отит, синусит, флегмона шеи и т. д.)
- дыхательных путей и плевры (аспирационная пневмония, абсцесс легкого, эмпиема плевры и пр.)
- женской половой системы (сальпингит, аднексит, эндометрит, пельвиоперитонит)
- брюшной полости (абсцесс брюшной полости, перитонит)
- кожи и мягких тканей (клостридиальный целлюлит, газовая гангрена, некротизирующий фасциит, абсцессы и др.)
- костей и суставов (остеомиелит, гнойный артрит)
- бактериемию.
Течение анаэробной инфекции может быть молниеносным (в течение 1 суток с момента операции или травмы), острым (в течение 3-4 суток), подострым (более 4 суток).
Симптомы анаэробной инфекции
Независимо от вида возбудителя и локализации инфекционного очага, различным клиническим формам свойственны некоторые общие черты. В большинстве случаев анаэробная инфекция имеет острое начало и характеризуется сочетанием местных и общих симптомов. Инкубационный период может составлять от нескольких часов до нескольких суток (в среднем около 3-х дней).
Типичным признаком анаэробной инфекции служит преобладание симптомов общей интоксикации над местными воспалительными явлениями. Резкое ухудшение общего состояния больного обычно наступает еще до возникновения локальных симптомов. Проявлением тяжелого эндотоксикоза служит высокая лихорадка с ознобами, выраженная слабость, тошнота, головная боль, заторможенность. Характерны артериальная гипотония, тахипноэ, тахикардия, гемолитическая анемия, иктеричность кожи и склер, акроцианоз.
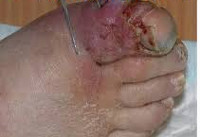
При раневой анаэробной инфекции ранним местным симптомом выступает сильная, нарастающая боль распирающего характера, эмфизема и крепитация мягких тканей, обусловленные газообразующими процессами в ране. К числу постоянных признаков относится зловонный ихорозный запах экссудата, связанный с выделением азота, водорода и метана при анаэробном окислении белкового субстрата. Экссудат имеет жидкую консистенцию, серозно-геморрагический, гнойно-геморрагический или гнойный характер, неоднородную окраску с вкраплениями жира и наличием пузырьков газа. На гнилостный характер воспаления также указывает внешний вид раны, содержащей ткани серо-зеленого или серо-коричневого цвета, иногда струпы черного цвета.
Осложнения
Анаэробная инфекция часто сопровождается развитием полиорганной недостаточности (почечной, печеночной, сердечно-легочной), инфекционно-токсического шока, тяжелого сепсиса, являющихся причиной летального исхода.
Диагностика
Для своевременной диагностики анаэробной инфекции большое значение имеет правильная оценка клинических симптомов, позволяющая своевременно оказать необходимую медицинскую помощь. В зависимости от локализации инфекционного очага диагностикой и лечением анаэробной инфекции могут заниматься клиницисты различных специальностей – общие хирурги, травматологи, нейрохирурги, гинекологи, отоларингологи, челюстно-лицевые и торакальные хирурги. С целью определения патогенного агента и тяжести инфекционного процесса используют:
- Методы детекции возбудителя. Методы экспресс-диагностики анаэробной инфекции включают бактериоскопию раневого отделяемого с окраской мазка по Грамму и газожидкостную хроматографию. В верификации возбудителя ведущая роль принадлежит бактериологическому посеву отделяемого раны или содержимого абсцесса, анализу плевральной жидкости, посеву крови на аэробные и анаэробные бактерии, иммуноферментному анализу, ПЦР.
- Другие анализы. В биохимических показателях крови при анаэробной инфекции обнаруживается снижение концентрации белков, увеличение уровня креатинина, мочевины, билирубина, активности трансаминаз и щелочной фосфатазы.
- Инструментальную диагностику. Наряду с клиническими и лабораторными исследования, выполняется рентгенография, при которой обнаруживается скопление газа в пораженных тканях или полостях.
Анаэробную инфекцию необходимо дифференцировать от рожистого воспаления мягких тканей, полиморфной экссудативной эритемы, тромбоза глубоких вен, пневмоторакса, пневмоперитонеума, перфорации полых органов брюшной полости.
Лечение анаэробной инфекции
Комплексный подход к лечению анаэробной инфекции предполагает проведение радикальной хирургической обработки гнойного очага, интенсивной дезинтоксикационной и антибактериальной терапии. Хирургический этап должен быть выполнен как можно раньше – от этого зависит жизнь больного. Как правило, он заключается в широком рассечении очага поражения с удалением некротизированных тканей, декомпрессии окружающих тканей, открытом дренировании с промыванием полостей и ран растворами антисептиков. Особенности течения анаэробной инфекции нередко требуют проведения повторных некрэктомий, раскрытия гнойных карманов, обработки ран ультразвуком и лазером, озонотерапии и т. д. При обширной деструкции тканей может быть показана ампутация или экзартикуляция конечности.
Важнейшими составляющими лечения анаэробной инфекции являются интенсивная инфузионная терапия и антибиотикотерапия препаратами широкого спектра действия, высокотропными к анаэробам. В рамках комплексного лечения анаэробной инфекции находят свое применение гипербарическая оксигенация, УФОК, экстракорпоральная гемокоррекция (гемосорбция, плазмаферез и др.). При необходимости пациенту вводится антитоксическая противогангренозная сыворотка.
Прогноз и профилактика
Исход анаэробной инфекции во многом зависит от клинической формы патологического процесса, преморбидного фона, своевременности установления диагноза и начала лечения. Уровень летальности при некоторых формах анаэробной инфекции превышает 20%. Профилактика анаэробной инфекции заключается в своевременной и адекватной ПХО ран, удалении инородных тел мягких тканей, соблюдении требований асептики и антисептики при проведении операций. При обширных раневых повреждениях и высоком риске развития анаэробной инфекции необходимо проведение специфической иммунизации и противомикробной профилактики.
В статье приводится краткое описание анаэробной инфекции, профилактика которой должна осуществляться на всех этапах оказания медицинской помощи, учитывая ее опасность и значимость в повседневной клинической практике.
Анаэробная инфекция – это крайне опасный для жизни и здоровья патологический процесс, причинами которого становятся развитие анаэробной микрофлоры в мягких тканях организма.
Особенностями данного вида инфекции является то, что активизация размножения микроорганизмов наступает лишь при попадании их в среду без доступа кислорода.
Такие условия могут формироваться при попадании микробов в ткани при любом виде ранения.
Потенциально любая рана, проникающая в подкожно-жировую клетчатку может привести к развитию этого вида инфекции. Однако наиболее часто причинами развития данного вида инфекции являются размозженные, огнестрельные, колотые ранения, ожоги и обморожения. При создании благоприятных условий скорость развития инфекции становится настолько быстрой, что без немедленной хирургической помощи состояние больного ухудшается в считанные часы и в большинстве случаев приводит к летальному исходу. Развивающаяся в тканях микрофлора оказывает агрессивное разрушительное воздействие на ткани вызывая их гибель (некробиоз), а также начинает вырабатывать токсины, быстро всасывающиеся в кровь и нарушающие обменные процессы во всех органах и тканях (сердце, легкие, печень, почки) и тем самым замыкая порочный круг развития патологического процесса. Даже при своевременно начатом лечении летальность колеблется в пределах 30-50%. Анаэробные микроорганизмы присутствуют в почве, а так же входят в состав нормальной микрофлоры толстой кишки и вызывают патологический процесс при попадании в рану извне, в момент ранения. Однако отсутствия загрязнения раны почвой, как содержащей большое количество данного вида микроорганизмов носит условный характер, так как спорообразующие микроорганизмы могут присутствовать на коже у здоровых людей не вызывая никаких патологических процессов. Попадание анаэробов в ткани может происходить при оперативных вмешательствах, инвазивных манипуляциях (пункциях, биопсии, экстракции зуба и др.) при нарушении асептики, перфорации внутренних органов, открытых травмах, ранениях, ожогах, укусах животных, синдроме длительного сдавления, криминальных абортах .
Анаэробная инфекция может возникнуть у пациентов любого возраста.
Анаэробные микроорганизмы делятся на облигатные и факультативные: развитие и размножение облигатных анаэробов осуществляется в бескислородной среде; факультативные анаэробы способны выживать как в отсутствии, так и в присутствии кислорода.
Облигатные возбудители анаэробной инфекции делятся на две группы: клостридии и неспорообразующие анаэробы (бактероиды, вейллонеллы, пропионибактерии, пептострептококки, фузобактерии и др.). К факультативным анаэробными бактериями принадлежат кишечная палочка, шигеллы, иерсинии, стрептококки, стафилококки и др.
Симптомы анаэробной инфекции. Независимо от вида возбудителя и локализации очага анаэробной инфекции, различным клиническим формам свойственны некоторые общие черты. В большинстве случаев анаэробная инфекция имеет острое начало и характеризуется сочетанием местных и общих симптомов. Инкубационный период может составлять от нескольких часов до нескольких суток (в среднем около 3-х дней).
Течение анаэробной инфекции может быть молниеносным (в течение 1 суток с момента операции или травмы), острым (в течение 3-4 суток), подострым (более 4 суток). Анаэробная инфекция часто сопровождается развитием полиорганной недостаточности (почечной, печеночной, сердечно-легочной), инфекционно-токсического шока, тяжелого сепсиса, являющихся причиной летального исхода.
Первичная диагностика основывается на клинических признаках. В верификации возбудителя ведущая роль принадлежит бактериологическому посеву отделяемого раны или содержимого абсцесса. Наряду с клиническими и лабораторными исследования, выполняется рентгенография, при которой обнаруживается скопление газа в пораженных тканях или полостях.
Особенности течения анаэробной инфекции нередко требуют проведения повторных операций, вскрытия формирующихся гнойных карманов, обработки ран ультразвуком и лазером, озонотерапии и т.д. При обширной деструкции тканей может быть показана ампутация конечности. Важнейшими составляющими лечения анаэробной инфекции являются интенсивная инфузионная терапия и антибиотикотерапия препаратами широкого спектра действия, зачастую назначается комплекс из трех антибактериальных препаратов. В рамках комплексного лечения анаэробной инфекции находят свое применение гипербарическая оксигенация, ультрафиолетовое облучение крови, методы экстракорпоральной детоксикации. При необходимости пациенту вводится антитоксическая противогангренозная сыворотка.
В случае выявления случая анаэробной инфекции в лечебном учреждении, последнее закрывается на карантин с обязательной генеральной дезинфекцией всех помещений с последующим контролем сотрудниками санитарно-эпидемиологической службы.

В настоящее время считается, что возбудители хирургической инфекции в основном попадают в рану из внешней среды. Между тем, в природе широко распространен феномен транслокации бактерий из желудочно-кишечного тракта, который является причиной значительного числа госпитальных инфекций и депрессии иммунитета после травмы.
Транслокация - это прохождение жизнеспособных бактерий из желудочно-кишечного тракта через слизистую оболочку в экстраинтестинальные участки макроорганизма, например, мезентериальные лимфоузлы, печень, селезенку, кровоток.
Обнаружена транслокация бактерий при стрессе, травмах, ожогах, геморрагическом шоке, кишечной непроходимости, полиорганной недостаточности, механической желтухе, остром панкреатите, токсических гепатитах. Хирургическое вмешательство также индуцирует проникновение жизнеспособных бактерий через слизистые оболочки желудочно-кишечного тракта в кровь, лимфу, органы и ткани.
При обследовании 448 больных, подвергнутых лапаротомии, транслокация бактерий в мезентериальные лимфоузлы обнаружена у 15,4% пациентов, причем у 74% из них выделены бактерии кишечника. Транслокация бактерий начинается в течение 15-20 минут и уже через несколько часов наблюдается элиминация их через раневые поверхности, мочевыделительную систему.
Закономерность транслокации микроорганизмов из желудочно-кишечного тракта в экстраинтестинальные участки - видоспецифичность. Не все микробы способны к транслокации. Из аутофлоры наиболее часто транслоцируются кишечная палочка, протей, энтеробактерии, из транзиторных штаммов - сенная палочка. Следующими в ряду идут грам-положительные аэробы. В то же время уровень транслокации облигатных анаэробов очень низкий.
Транслокация одинаково интенсивна на всём протяжении кишечника. Первичной локализацией транслоцированных бактерий являются брыжеечные лимфоузлы. Выход бактерий из лимфатического комплекса, вероятно, может регулироваться макроорганизмом. Любая травма или воспалительный процесс, в том числе и за пределами желудочно-кишечного тракта, меняет характер транслокации. Из лимфатической системы бактерии проникают в кровь, лимфу, достигают очага повреждения, локализуясь в мертвых и жизнеспособных тканях.
Существуют четыре основных пути транслокации микроорганизмов через слизистые оболочки желудочно-кишечного тракта: межклеточный, чрезклеточный, с помощью фагоцитоза и через дефекты эпителия.
Механизмы регуляции бактериальной транслокации изучены недостаточно.
Тотальное парентеральное питание в послеоперационном периоде приводит к нарушению функции кишечного барьера и повышению транслокации. Для решения этой проблемы рекомендовано применять энтеральное питание с обязательным добавлением глютамина (ограничивает проницаемость кишечной слизистой). Наличие в диете неперевариваемой клетчатки также снижает транслокацию бактерий за счет улучшения функции кишечного барьера. Повреждающее влияние на слизистую оболочку могут оказывать эндотоксины грам-отрицательной аутофлоры. При этом повышение проницаемости слизистой для бактерий индуцируется как внутрикишечными, так и плазменными липополисахаридами бактерий. Нарушения мезентериального кровообращения могут менять уровень транслокации. Тканевое парциальное давление кислорода является основным регулятором функции кишечного барьера. При интестинальной ишемии любого генеза (перевязка сосудов брыжейки, шок) происходит выделение цитокинов мононуклеарами, нарушается проницаемость слизистой и увеличивается транслокация.
При геморрагическом шоке за счет ишемического повреждения слизистой (фокальные очаги некроза, субэпителиальный отек) резко увеличивается транслокация индигенной микрофлоры и её метаболитов из ЖКТ, причем выявляется корреляция между длительностью шокового состояния и уровнем транслокации. В течение первых трех суток постреанимационного периода жизнеспособные энтеробактерии проникают в брыжеечные лимфоузлы. Это обусловлено выраженными деструктивными изменениями в слизистой оболочке тонкой кишки. Повреждение слизистой реализуется через фермент ксантин-оксидазу (запускает реакции перекисного окисления). Ингибирование этого фермента аллопуринолом замедляет транслокацию.
Велика роль индигенной микрофлоры в предотвращении чрезмерного размножения микроорганизмов признаётся многими авторами. Механизм, с помощью которого контролируется качественный и количественный состав условно-патогенной микрофлоры, сохраняется динамическое равновесие между микрофлорой, населяющей кишечник, и микрофлорой, поступающей извне, определен как "колонизационная резистентность". Нормальная перистальтическая активность кишечника является эффективной защитной мерой организма против избыточной колонизации тонкого кишечника. Любое замедление пассажа кишечного содержимого приводит к повышенному росту микроорганизмов. Обнаружена обратная зависимость между скоростью кишечного пассажа контраста, уровнем колонизации кишечника и уровнем транслокации.
После перорального введения антибактериальных препаратов мышам (пенициллин G, метронидазол, клиндамицин) и последующего снижения количества анаэробных бактерий в кишечнике наблюдается повышение транслокации грам-отрицательной микрофлоры в мезентериальные лимфоузлы. Применение антибиотиков, снижающих уровень аэробной микрофлоры, напротив, снижает транслокацию.
Транслокация бактерий из просвета кишечника встречается при различной хирургической патологии. Предполагают связь этого феномена с развитием синдрома системной воспалительной реакции, сепсиса и полиорганной недостаточности. Увеличивается количество свидетельств того, что большинство госпитальных инфекций вызваны транслоцировавшимися кишечными микроорганизмами, хотя точную сферу действия транслокации у хирургических пациентов трудно установить.
Шок предшествует транслокации бактерий и эндотоксинов из кишечника в постгипотензивном периоде. Именно бактериальная транслокация и эндотоксинемия определяют неблагоприятный прогноз шока. Повышение внутрибрюшного давления при лапароскопических операциях представляет собой определенную опасность в плане увеличения уровня бактериальной транслокации с последующим развитием сепсиса. Пневмоперитонеум на модели крыс при 15 мм рт.ст. в течение 60 минут способствует интестинальной ишемии, активации перекисного окисления, бактериальной транслокации.
Одни исследователи считают проникновение кишечных бактерий во внутренние среды организма следствием иммунной несостоятельности, но, по мнению других, транслокация - процесс биологически целесообразный (кишечник - важнейший иммунный орган, в котором осуществляется непрерывная антигенная стимуляция). У здоровых животных микроорганизмы проникают в кровь и лимфу из желудочно-кишечного тракта в основном через слизистые оболочки желудка и тонкого кишечника без всякой стимуляции транслокации. В последующем бактерии концентрируются в лимфатических узлах, селезенке, печени, являясь источником антигенов для поддержания уровня нормальных антител. При повреждениях любых видов (механические, термические, воспаление и др.) различной локализации микроорганизмы вновь попадают в кровь и лимфу. С их током бактерии достигают патологического очага, где локализуются в жизнеспособных тканях, в основном, соединительной, костной и вокруг сосудов. В зоне повреждения микробы выделяют широкий набор антибиотиков, протеолитических ферментов, иммуномодуляторов, фактор роста фибробластов, чем способствуют очищению от некроза и ускорению регенерации. Транслокацию возбудителей хирургической инфекции блокируют антибиотики и, еще более эффективно, живые бактериальные препараты споробактерин, бактисубтил, лактобактерин, бифидумбактерин.
Таким образом, явление транслокации бактерий из желудочно-кишечного тракта встречается достаточно часто. На современном этапе существуют две трактовки значения этого феномена. Согласно первой - бактериальная транслокация возникает при резком угнетении иммунитета вследствие стресса, травмы или иного экстремального воздействия и является патогенетическим звеном ряда заболеваний. Вторая - транслокация может быть не только механизмом проникновения возбудителей, но и в определенных условиях является природным защитным механизмом, который надо учитывать и использовать в клинической практике. Феномен транслокации бактерий из желудочно-кишечного тракта еще мало изучен. И дальнейшие исследования как по проблеме хирургической инфекции, так и в других областях позволят сделать много интересных находок.
Читайте также:

