Анаэробной инфекции и в высоких концентрациях бактерицид
Обновлено: 07.05.2024
В статье приводится краткое описание анаэробной инфекции, профилактика которой должна осуществляться на всех этапах оказания медицинской помощи, учитывая ее опасность и значимость в повседневной клинической практике.
Анаэробная инфекция – это крайне опасный для жизни и здоровья патологический процесс, причинами которого становятся развитие анаэробной микрофлоры в мягких тканях организма.
Особенностями данного вида инфекции является то, что активизация размножения микроорганизмов наступает лишь при попадании их в среду без доступа кислорода.
Такие условия могут формироваться при попадании микробов в ткани при любом виде ранения.
Потенциально любая рана, проникающая в подкожно-жировую клетчатку может привести к развитию этого вида инфекции. Однако наиболее часто причинами развития данного вида инфекции являются размозженные, огнестрельные, колотые ранения, ожоги и обморожения. При создании благоприятных условий скорость развития инфекции становится настолько быстрой, что без немедленной хирургической помощи состояние больного ухудшается в считанные часы и в большинстве случаев приводит к летальному исходу. Развивающаяся в тканях микрофлора оказывает агрессивное разрушительное воздействие на ткани вызывая их гибель (некробиоз), а также начинает вырабатывать токсины, быстро всасывающиеся в кровь и нарушающие обменные процессы во всех органах и тканях (сердце, легкие, печень, почки) и тем самым замыкая порочный круг развития патологического процесса. Даже при своевременно начатом лечении летальность колеблется в пределах 30-50%. Анаэробные микроорганизмы присутствуют в почве, а так же входят в состав нормальной микрофлоры толстой кишки и вызывают патологический процесс при попадании в рану извне, в момент ранения. Однако отсутствия загрязнения раны почвой, как содержащей большое количество данного вида микроорганизмов носит условный характер, так как спорообразующие микроорганизмы могут присутствовать на коже у здоровых людей не вызывая никаких патологических процессов. Попадание анаэробов в ткани может происходить при оперативных вмешательствах, инвазивных манипуляциях (пункциях, биопсии, экстракции зуба и др.) при нарушении асептики, перфорации внутренних органов, открытых травмах, ранениях, ожогах, укусах животных, синдроме длительного сдавления, криминальных абортах .
Анаэробная инфекция может возникнуть у пациентов любого возраста.
Анаэробные микроорганизмы делятся на облигатные и факультативные: развитие и размножение облигатных анаэробов осуществляется в бескислородной среде; факультативные анаэробы способны выживать как в отсутствии, так и в присутствии кислорода.
Облигатные возбудители анаэробной инфекции делятся на две группы: клостридии и неспорообразующие анаэробы (бактероиды, вейллонеллы, пропионибактерии, пептострептококки, фузобактерии и др.). К факультативным анаэробными бактериями принадлежат кишечная палочка, шигеллы, иерсинии, стрептококки, стафилококки и др.
Симптомы анаэробной инфекции. Независимо от вида возбудителя и локализации очага анаэробной инфекции, различным клиническим формам свойственны некоторые общие черты. В большинстве случаев анаэробная инфекция имеет острое начало и характеризуется сочетанием местных и общих симптомов. Инкубационный период может составлять от нескольких часов до нескольких суток (в среднем около 3-х дней).
Течение анаэробной инфекции может быть молниеносным (в течение 1 суток с момента операции или травмы), острым (в течение 3-4 суток), подострым (более 4 суток). Анаэробная инфекция часто сопровождается развитием полиорганной недостаточности (почечной, печеночной, сердечно-легочной), инфекционно-токсического шока, тяжелого сепсиса, являющихся причиной летального исхода.
Первичная диагностика основывается на клинических признаках. В верификации возбудителя ведущая роль принадлежит бактериологическому посеву отделяемого раны или содержимого абсцесса. Наряду с клиническими и лабораторными исследования, выполняется рентгенография, при которой обнаруживается скопление газа в пораженных тканях или полостях.
Особенности течения анаэробной инфекции нередко требуют проведения повторных операций, вскрытия формирующихся гнойных карманов, обработки ран ультразвуком и лазером, озонотерапии и т.д. При обширной деструкции тканей может быть показана ампутация конечности. Важнейшими составляющими лечения анаэробной инфекции являются интенсивная инфузионная терапия и антибиотикотерапия препаратами широкого спектра действия, зачастую назначается комплекс из трех антибактериальных препаратов. В рамках комплексного лечения анаэробной инфекции находят свое применение гипербарическая оксигенация, ультрафиолетовое облучение крови, методы экстракорпоральной детоксикации. При необходимости пациенту вводится антитоксическая противогангренозная сыворотка.
В случае выявления случая анаэробной инфекции в лечебном учреждении, последнее закрывается на карантин с обязательной генеральной дезинфекцией всех помещений с последующим контролем сотрудниками санитарно-эпидемиологической службы.
В статье приводится краткое описание анаэробной инфекции, профилактика которой должна осуществляться на всех этапах оказания медицинской помощи, учитывая ее опасность и значимость в повседневной клинической практике.
Анаэробная инфекция – это крайне опасный для жизни и здоровья патологический процесс, причинами которого становятся развитие анаэробной микрофлоры в мягких тканях организма.
Особенностями данного вида инфекции является то, что активизация размножения микроорганизмов наступает лишь при попадании их в среду без доступа кислорода.
Такие условия могут формироваться при попадании микробов в ткани при любом виде ранения.
Потенциально любая рана, проникающая в подкожно-жировую клетчатку может привести к развитию этого вида инфекции. Однако наиболее часто причинами развития данного вида инфекции являются размозженные, огнестрельные, колотые ранения, ожоги и обморожения. При создании благоприятных условий скорость развития инфекции становится настолько быстрой, что без немедленной хирургической помощи состояние больного ухудшается в считанные часы и в большинстве случаев приводит к летальному исходу. Развивающаяся в тканях микрофлора оказывает агрессивное разрушительное воздействие на ткани вызывая их гибель (некробиоз), а также начинает вырабатывать токсины, быстро всасывающиеся в кровь и нарушающие обменные процессы во всех органах и тканях (сердце, легкие, печень, почки) и тем самым замыкая порочный круг развития патологического процесса. Даже при своевременно начатом лечении летальность колеблется в пределах 30-50%. Анаэробные микроорганизмы присутствуют в почве, а так же входят в состав нормальной микрофлоры толстой кишки и вызывают патологический процесс при попадании в рану извне, в момент ранения. Однако отсутствия загрязнения раны почвой, как содержащей большое количество данного вида микроорганизмов носит условный характер, так как спорообразующие микроорганизмы могут присутствовать на коже у здоровых людей не вызывая никаких патологических процессов. Попадание анаэробов в ткани может происходить при оперативных вмешательствах, инвазивных манипуляциях (пункциях, биопсии, экстракции зуба и др.) при нарушении асептики, перфорации внутренних органов, открытых травмах, ранениях, ожогах, укусах животных, синдроме длительного сдавления, криминальных абортах .
Анаэробная инфекция может возникнуть у пациентов любого возраста.
Анаэробные микроорганизмы делятся на облигатные и факультативные: развитие и размножение облигатных анаэробов осуществляется в бескислородной среде; факультативные анаэробы способны выживать как в отсутствии, так и в присутствии кислорода.
Облигатные возбудители анаэробной инфекции делятся на две группы: клостридии и неспорообразующие анаэробы (бактероиды, вейллонеллы, пропионибактерии, пептострептококки, фузобактерии и др.). К факультативным анаэробными бактериями принадлежат кишечная палочка, шигеллы, иерсинии, стрептококки, стафилококки и др.
Симптомы анаэробной инфекции. Независимо от вида возбудителя и локализации очага анаэробной инфекции, различным клиническим формам свойственны некоторые общие черты. В большинстве случаев анаэробная инфекция имеет острое начало и характеризуется сочетанием местных и общих симптомов. Инкубационный период может составлять от нескольких часов до нескольких суток (в среднем около 3-х дней).
Течение анаэробной инфекции может быть молниеносным (в течение 1 суток с момента операции или травмы), острым (в течение 3-4 суток), подострым (более 4 суток). Анаэробная инфекция часто сопровождается развитием полиорганной недостаточности (почечной, печеночной, сердечно-легочной), инфекционно-токсического шока, тяжелого сепсиса, являющихся причиной летального исхода.
Первичная диагностика основывается на клинических признаках. В верификации возбудителя ведущая роль принадлежит бактериологическому посеву отделяемого раны или содержимого абсцесса. Наряду с клиническими и лабораторными исследования, выполняется рентгенография, при которой обнаруживается скопление газа в пораженных тканях или полостях.
Особенности течения анаэробной инфекции нередко требуют проведения повторных операций, вскрытия формирующихся гнойных карманов, обработки ран ультразвуком и лазером, озонотерапии и т.д. При обширной деструкции тканей может быть показана ампутация конечности. Важнейшими составляющими лечения анаэробной инфекции являются интенсивная инфузионная терапия и антибиотикотерапия препаратами широкого спектра действия, зачастую назначается комплекс из трех антибактериальных препаратов. В рамках комплексного лечения анаэробной инфекции находят свое применение гипербарическая оксигенация, ультрафиолетовое облучение крови, методы экстракорпоральной детоксикации. При необходимости пациенту вводится антитоксическая противогангренозная сыворотка.
В случае выявления случая анаэробной инфекции в лечебном учреждении, последнее закрывается на карантин с обязательной генеральной дезинфекцией всех помещений с последующим контролем сотрудниками санитарно-эпидемиологической службы.
По спектру активности антимикробные препараты делятся на: антибактериальные, антигрибковые и антипротозойные. Кроме того, все антимикробные средства делят на препараты узкого и широкого спектра действия.
К препаратам узкого спектра действия преимущественно на грамположительные микроорганизмы относятся, например, природные пенициллины, макролиды, линкомицин, фузидин, оксациллин, ванкомицин, цефалоспорины I поколения. К препаратам узкого спектра действия преимущественно на грамотрицательные палочки относятся полимиксины и монобактамы. К препаратам широкого спектра действия относятся тетрациклины, левомицетин, аминогликозиды, большинство полусинтетических пенициллинов, цефалоспорины начиная со 2 поколения, карбопенемы, фторхинолоны. Узкий спектр имеют антигрибковые препараты нистатин и леворин (только против кандиды), а широкий – клотримазол, миконазол, амфотерицин В.
По типу взаимодействия с микробной клеткой антимикробные препараты делятся на:
· бактерицидные – необратимо нарушают функции микробной клетки либо ее целостность, вызывая немедленную гибель микроорганизма, применяются при тяжелых инфекциях и у ослабленных больных,
· бактериостатические – обратимо блокируют репликацию или деление клетки, применяются при нетяжелых инфекциях у неослабленных больных.
По кислотоустойчивости антимикробные препараты классифицируются на:
· кислотоустойчивые – могут применяться перорально, например, феноксиметилпенициллин,
· кислотонеустойчивые – предназначены только для парентерального применения, например, бензилпенициллин.
В настоящее время используются следующие основные группы антимикробных препаратов для системного применения.
¨ Лактамные антибиотики
Лактамные антибиотики (табл. 9.2) из всех антимикробных препаратов наименее токсичны, так как, нарушая синтез клеточной стенки бактерий, не имеют мишени в организме человека. Их применение при наличии чувствительности к ним возбудителей является предпочтительным. Наиболее широкий спектр действия среди лактамных антибиотиков имеют карбапенемы, они используются как препараты резерва – только при инфекциях, резистентных к пенициллинам и цефалоспоринам, а также при госпитальных и полимикробных инфекциях.
¨ Антибиотики других групп
Антибиотики других групп (табл. 9.3) имеют различные механизмы действия. Бактериостатические препараты нарушают этапы синтеза белка на рибосомах, бактерицидные – нарушают либо целостность цитоплазматической мембраны, либо процесс синтеза ДНК и РНК. В любом случае они имеют мишень в организме человека, поэтому по сравнению с лактамными препаратами более токсичны, и должны использоваться только при невозможности применения последних.
¨ Синтетические антибактериальные препараты
Синтетические антибактериальные препараты (табл. 9.4) также имеют различные механизмы действия: ингибирование ДНК-гиразы, нарушение включения ПАБК в ДГФК и т.д. Также рекомендуются к применению при невозможности использования лактамных антибиотиков.
¨ Побочные эффекты антимикробных препаратов,
их профилактика и лечение
Антимикробные препараты обладают целым рядом разнообразных побочных эффектов, некоторые из которых могут привести к тяжелым осложнениям и даже к летальному исходу.
Аллергические реакции
Аллергические реакции могут иметь место при применении любого антимикробного препарата. Могут развиться аллергический дерматит, бронхоспазм, ринит, артрит, отек Квинке, анафилактический шок, васкулит, нефрит, волчаночноподобный синдром. Чаще всего они наблюдаются при применении пенициллинов и сульфаниламидов. У некоторых пациентов развивается перекрестная аллергия на пенициллины и цефалоспорины. Зачастую отмечаются аллергии на ванкомицин и сульфаниламиды. Очень редко дают аллергические реакции аминогликозиды и левомицетин.
Профилактике способствует тщательный сбор аллергологического анамнеза. Если пациент не может указать, на какие именно антибактериальные препараты в у него наблюдались аллергические реакции, перед введением антибиотиков необходимо выполнение проб. Развитие аллергии независимо от тяжести реакции требует немедленной отмены вызвавшего ее препарата. В последующем введение даже сходных по химической структуре антибиотиков (например, цефалоспоринов при аллергии на пенициллин) допускается только в случаях крайней необходимости. Лечение инфекции должно быть продолжено препаратами других групп. При тяжелых аллергических реакциях требуется внутривенное введение преднизолона и симпатомиметиков, инфузионная терапия. В нетяжелых случаях назначаются антигистаминные препараты.
Раздражающее действие на путях введения
При пероральном применении раздражающее действие может выражаться в диспепсических явлениях, при внутривенном введении – в развитии флебитов. Тромбофлебиты чаще всего вызывают цефалоспорины и гликопептиды.
Суперинфекция, в том числе дисбактериоз
Вероятность дисбактериоза зависит от широты спектра действия препарата. Наиболее часто возникающий кандидомикоз развивается при применении препаратов узкого спектра через неделю, при применении препаратов широкого спектра – уже от одной таблетки. Однако цефалоспорины относительно редко дают грибковую суперинфекцию. На 1 месте по частоте и тяжести вызываемого дисбактериоза находится линкомицин. Нарушения флоры при его применении могут принять характер псевдомембранозного колита – тяжелого заболевания кишечника, вызываемого клостридиями, сопровождающегося диареей, дегидратацией, электролитными нарушениями, и в отдельных случаях осложняющегося перфорацией толстой кишки. Гликопептиды тоже могут вызвать псевдомембранозный колит. Часто вызывают дисбактериоз тетрациклины, фторхинолоны, левомицетин.
Дисбактериоз требует отмены применявшегося препарата и длительного лечения эубиотиками после предварительной антимикробной терапии, которая проводится по результатам чувствительности микроорганизма, вызвавшего воспалительный процесс в кишечнике. Применяемые для лечения дисбактериоза антибиотики не должны оказывать влияния на нормальную кишечную аутофлору – бифидо- и лактобактерии. Однако при лечении псевдомембранозного колита используется метронидазол или, как альтернатива, ванкомицин. Необходима также коррекция водно-электролитных нарушений.
Нарушение толерантности к алкоголю - свойственно всем лактамным антибиотикам, метронидазолу, левомицетину. Проявляется появлением при одновременном употреблении алкоголя тошноты, рвоты, головокружения, тремора, потливости и падения артериального давления. Пациенты должны быть предупреждены о недопустимости приема алкоголя на весь период лечения антимикробным препаратом.
Органоспецифичные побочные эффекты для различных групп препаратов:
· Поражение системы крови и кроветворения – присущи левомицетину, реже линкосомидам, цефалоспоринам 1 поколения, сульфаниламидам, производным нитрофурана, фторхинолонам, гликопептидам. Проявляется апластической анемией, лейкопенией, тромбицитопенией. Необходима отмена препарата, в тяжелых случаях заместительная терапия. Геморрагический синдром может развиться при применении цефалоспоринов 2-3 поколения, нарушающих всасывание витамина К в кишечнике, антисинегнойных пенициллинов, нарушающих функции тромбоцитов, метронидазола, вытесняющего кумариновые антикоагулянты из связей с альбумином. Для лечения и профилактики используются препараты витамина К.
· Поражение печени – присущи тетрациклинам, которые блокируют ферментную систему гепатоцитов, а также оксациллину, азтреонаму, линкозаминам и сульфаниламидам. Холестаз и холестатический гепатит могут вызвать макролиды, цефтриаксон. Клиническими проявлениями служит повышение печеночных ферментов и билирубина в сыворотке крови. При необходимости применения гепатотоксических антимикробных средств более недели необходим лабораторный контроль перечисленных показателей. В случае повышения АСТ, АЛТ, билирубина, щелочной фосфатазы или глутамилтранспептидазы лечение должно быть продолжено препаратами других групп.
· Поражение костей и зубов характерны для тетрациклинов, растущих хрящей – для фторхинолонов.
· Поражение почек присуще аминогликозидам и полимиксинам, которые нарушают функции канальцев, сульфаниламидам, вызывающим кристаллурию, цефалоспоринам поколения, вызывающим альбуминурию, и ванкомицину. Предрасполагающими факторами являются старческий возраст, заболевания почек, гиповолемия и гипотензия. Поэтому при лечении данными препаратами необходима предварительная коррекция гиповолемии, контроль диуреза, подбор доз с учетом функции почек и массы ткла, Курс лечения должен быть коротким.
· Миокардит – побочный эффект левомицетина.
· Диспепсия, не являющаяся следствием дисбактериоза, характерна при применении макролидов, которые обладают прокинетическими свойствами.
· Различные поражения ЦНС развиваются от многих антимикробных препаратов. Наблюдаются:
- психозы при лечении левомицетином,
- парезы и периферические параличи при применении аминогликозидов и полимиксинов за счет их курареподобного действия (поэтому их нельзя применять одновременно с миорелаксантами),
- головная боль и центральная рвота при использовании сульфаниламидов и нитрофуранов,
- судороги и галлюцинации при использовании аминопенициллинов и цефалоспоринов в высоких дозах, являющиеся результатом антагонизма этих препаратов с ГАМК,
- судороги при применении имипенема,
- возбуждение при использовании фторхинолонов,
- менингизм при лечении тетрациклинами из-за увеличения ими продукции ликвора,
- нарушения зрения при лечении азтреонамом и левомицетином,
- периферическая нейропатия при применении изониазида, метронидазола, левомицетина.
· Поражение слуха и вестибулярные расстройства – побочный эффект аминогликозидов, более свойственный 1 поколению. Так как данный эффект связан с накоплением препаратов, длительность их применения не должна превышать 7 дней. Дополнительными факторами риска являются старческий возраст, почечная недостаточность и одновременное применение петлевых диуретиков. Обратимые изменения слуха вызывает ванкомицин. При появлении жалоб на снижение слуха, головокружение, тошноту, неустойчивость при ходьбе необходима замена антибиотика на препараты других групп.
· Поражения кожи в виде дерматита характерны для левомицетина. Тетрациклины и фторхинолоны вызывают фотосенсибилизацию. При лечении этими препаратами не назначаются физиотерапевтические процедуры, и следует избегать нахождения на солнце.
· Гипофункцию щитовидной железы вызывают сульфаниламиды.
· Тератогенность присуща тетрациклинам, фторхинолонам, сульфаниламидам.
· Возможен паралич дыхательной мускулатуры при быстром внутривенном введении линкомицина и кардиодепрессия при быстром внутривенном введении тетрациклинов.
· Электролитные нарушения вызывают антисинегнойные пенициллины. Особо опасно развитие гипокалиемии при наличии заболеваний сердечно-сосудистой системы. При назначении данных препаратов необходим контроль ЭКГ и электролитов крови. При лечении используют инфузионно-корригирующую терапию и диуретики.
Микробиологическая диагностика
Эффективность микробиологической диагностики, абсолютно необходимой для рационального подбора антимикробной терапии, зависит от соблюдения правил забора, транспортировки и хранения исследуемого материала. Правила забора биологического материала включают:
- взятие материала из области, максимально приближенной к очагу инфекции,
- предотвращение контаминации другой микрофлорой.
Транспортировка материала должна с одной стороны обеспечить жизнеспособность бактерий, а с другой - предотвратить их размножение. Желательно, чтобы материал хранился до начала исследования при комнатной температуре и не более 2 часов. В настоящее время для забора и транспортировки материала используются специальные плотно закрывающиеся стерильные контейнеры и транспортные среды.
В не меньшей степени эффективность микробиологической диагностики зависит от грамотной интерпретации результатов. Считается, что выделение патогенных микроорганизмов даже в малых количествах всегда позволяет отнести их к истинным возбудителям заболевания. Условно патогенный микроорганизм считают возбудителем, если он выделяется из стерильных в норме сред организма или в большом количестве из сред, не характерных для его обитания. В противном случае он является представителем нормальной аутофлоры либо контаминирует исследуемый материал в процессе забора или исследования. Выделение малопатогенных бактерий из нехарактерных для их обитания областей в умеренных количествах свидетельствует о транслокации микроорганизмов, однако не позволяет отнести их к истинным возбудителям заболевания.
Гораздо сложнее бывает интерпретировать результаты микробиологического исследования при высевании нескольких видов микроорганизмов. В таких случаях ориентируются на количественное соотношение потенциальных возбудителей. Чаще значимыми в этиологии данного заболевания бывают 1-2 из них. Следует иметь в виду, что вероятность равной этиологической значимости более чем 3 различных видов микроорганизмов незначительна.
В основе лабораторных тестов на выработку грамотрицательными микроорганизмами БЛРС лежит чувствительность БЛРС к ингибиторам бета-лактамаз, таким как клавулановая кислота, сульбактам и тазобактам. При этом, если микроорганизм семейства энтеробактерий оказывается резистентен к цефалоспоринам 3 поколения, а при добавлении к этим препаратам ингибиторов бета-лактамаз демонстрирует чувствительность, то данный штамм идентифицируется как БЛРС-продуцирующий.
Антибиотикотерапия должна быть направлена только на истинный возбудитель инфекции! Однако в большинстве стационаров микробиологические лаборатории не могут установить этиологию инфекции и чувствительность возбудителей к антимикробным препаратам в день поступления больного, поэтому неизбежным является первичное эмпирическое назначение антибиотиков. При этом учитываются особенности этиологии инфекций различных локализаций, характерные для данного лечебного учреждения. В связи с чем необходимы регулярные микробиологические исследования структуры инфекционных заболеваний и чувствительности их возбудителей к антибактериальным препаратам в каждом стационаре. Анализ результатов такого микробиологического мониторинга необходимо проводить ежемесячно.
Анаэробная инфекция – это инфекционный процесс, вызываемый спорообразующими или неспорообразующими микроорганизмами в условиях, благоприятных для их жизнедеятельности. Характерными клиническими признаками анаэробной инфекции служат преобладание симптомов эндогенной интоксикации над местными проявлениями, гнилостный характер экссудата, газообразующие процессы в ране, быстро прогрессирующий некроз тканей. Анаэробная инфекция распознается на основании клинической картины, подтвержденной результатами микробиологической диагностики, газожидкостной хроматографии, масс-спектрометрии, иммуноэлектрофореза, ПЦР, ИФА и др. Лечение анаэробной инфекции предполагает радикальную хирургическую обработку гнойного очага, интенсивную дезинтоксикационную и антибактериальную терапию.
МКБ-10
Общие сведения
Анаэробная инфекция – патологический процесс, возбудителями которого выступают анаэробные бактерии, развивающиеся в условиях аноксии (отсутствия кислорода) или гипоксии (низкого напряжения кислорода). Анаэробная инфекция представляет собой тяжелую форму инфекционного процесса, сопровождающуюся поражением жизненно важных органов и высоким процентом летальности. В клинической практике с анаэробной инфекцией приходится сталкиваться специалистам в области хирургии, травматологии, педиатрии, нейрохиругии, отоларингологии, стоматологии, пульмонологии, гинекологии и других медицинских направлений. Анаэробная инфекция может возникнуть у пациентов любого возраста. Доля заболеваний, вызываемых анаэробной инфекцией, точно не известна; из гнойных очагов в мягких тканях, костях или суставах анаэробы высеваются примерно в 30% случаев; анаэробная бактериемия подтверждается в 2-5% случаев.

Причины
Анаэробы входят в состав нормальной микрофлоры кожи, слизистых оболочек, желудочно-кишечного тракта, органов мочеполовой системы и по своим вирулентным свойствам являются условно-патогенными. При определенных условиях они становятся возбудителями эндогенной анаэробной инфекции. Экзогенные анаэробы присутствуют в почве и разлагающихся органических массах и вызывают патологический процесс при попадании в рану извне. Анаэробные микроорганизмы делятся на:
- Факультативные. Способны выживать как в отсутствии, так и в присутствии кислорода. К ним принадлежат кишечная палочка, шигеллы, иерсинии, стрептококки, стафилококки и др.
- Облигатные. Их развитие и размножение осуществляется в бескислородной среде. Облигатные возбудители делятся на две группы:
- спорообразующие (клостридии) - являются возбудителями клостридиозов экзогенного происхождения (столбняка, газовой гангрены, ботулизма, пищевых токсикоинфекций и др.);
- неспорообразующие (неклостридиальные) анаэробы (фузобактерии, бактероиды, вейллонеллы, пропионибактерии, пептострептококки и др.). В большинстве случаев вызывают гнойно-воспалительные процессы эндогенной природы (абсцессы внутренних органов, перитонит, пневмонию, флегмоны челюстно-лицевой области, отит, сепсис и др.).
Факторы риска
Условиями, благоприятствующими развитию анаэробной инфекции, являются повреждение анатомических барьеров с проникновением анаэробов в ткани и кровеносное русло, а также снижение окислительно-восстановительного потенциала тканей (ишемия, кровотечение, некроз). Попадание анаэробов в ткани может происходить при оперативных вмешательствах, инвазивных манипуляциях (пункциях, биопсии, экстракции зуба и др.), перфорации внутренних органов, открытых травмах, ранениях, ожогах, укусах животных, синдроме длительного сдавления, криминальных абортах и т. д. Факторами, способствующими возникновению анаэробной инфекции, выступают:
- массивное загрязнение ран землей;
- наличие инородных тел в ране;
- гиповолемический и травматический шок;
- сопутствующие заболевания (коллагенозы, сахарный диабет, опухоли);
- иммунодефицит.
Кроме этого, большое значение имеет нерациональная антибиотикотерапия, направленная на подавление сопутствующей аэробной микрофлоры.
Патогенез
Основными факторами патогенности анаэробных микроорганизмов служат их количество в патологическом очаге, биологические свойства возбудителей, наличие бактерий-ассоциантов. В патогенезе анаэробной инфекции ведущая роль принадлежит продуцируемым микроорганизмами ферментам, эндо- и экзотоксинам, неспецифическим факторам метаболизма. Так, ферменты (гепариназа, гиалуронидаза, коллагеназа, дезоксирибонуклеаза) способны усиливать вирулентность анаэробов, деструкцию мышечной и соединительной тканей.
Эндо- и экзотоксины вызывают повреждение эндотелия сосудов, внутрисосудистый гемолиз и тромбоз. Кроме этого, некоторые клостридиальные токисины обладают нефротропным, нейротропным, кардиотропным действием. Также токсическое влияние на организм оказывают и неспецифические факторы метаболизма анаэробов - индол, жирные кислоты, сероводород, аммиак.
Классификация
В зависимости от локализации различают анаэробную инфекцию:
- центральной нервной системы (абсцесс мозга, менингит, субдуральная эмпиема и др.)
- головы и шеи (пародонтальный абсцесс, ангина Людвига, средний отит, синусит, флегмона шеи и т. д.)
- дыхательных путей и плевры (аспирационная пневмония, абсцесс легкого, эмпиема плевры и пр.)
- женской половой системы (сальпингит, аднексит, эндометрит, пельвиоперитонит)
- брюшной полости (абсцесс брюшной полости, перитонит)
- кожи и мягких тканей (клостридиальный целлюлит, газовая гангрена, некротизирующий фасциит, абсцессы и др.)
- костей и суставов (остеомиелит, гнойный артрит)
- бактериемию.
Течение анаэробной инфекции может быть молниеносным (в течение 1 суток с момента операции или травмы), острым (в течение 3-4 суток), подострым (более 4 суток).
Симптомы анаэробной инфекции
Независимо от вида возбудителя и локализации инфекционного очага, различным клиническим формам свойственны некоторые общие черты. В большинстве случаев анаэробная инфекция имеет острое начало и характеризуется сочетанием местных и общих симптомов. Инкубационный период может составлять от нескольких часов до нескольких суток (в среднем около 3-х дней).
Типичным признаком анаэробной инфекции служит преобладание симптомов общей интоксикации над местными воспалительными явлениями. Резкое ухудшение общего состояния больного обычно наступает еще до возникновения локальных симптомов. Проявлением тяжелого эндотоксикоза служит высокая лихорадка с ознобами, выраженная слабость, тошнота, головная боль, заторможенность. Характерны артериальная гипотония, тахипноэ, тахикардия, гемолитическая анемия, иктеричность кожи и склер, акроцианоз.
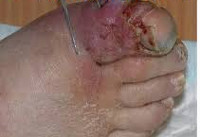
При раневой анаэробной инфекции ранним местным симптомом выступает сильная, нарастающая боль распирающего характера, эмфизема и крепитация мягких тканей, обусловленные газообразующими процессами в ране. К числу постоянных признаков относится зловонный ихорозный запах экссудата, связанный с выделением азота, водорода и метана при анаэробном окислении белкового субстрата. Экссудат имеет жидкую консистенцию, серозно-геморрагический, гнойно-геморрагический или гнойный характер, неоднородную окраску с вкраплениями жира и наличием пузырьков газа. На гнилостный характер воспаления также указывает внешний вид раны, содержащей ткани серо-зеленого или серо-коричневого цвета, иногда струпы черного цвета.
Осложнения
Анаэробная инфекция часто сопровождается развитием полиорганной недостаточности (почечной, печеночной, сердечно-легочной), инфекционно-токсического шока, тяжелого сепсиса, являющихся причиной летального исхода.
Диагностика
Для своевременной диагностики анаэробной инфекции большое значение имеет правильная оценка клинических симптомов, позволяющая своевременно оказать необходимую медицинскую помощь. В зависимости от локализации инфекционного очага диагностикой и лечением анаэробной инфекции могут заниматься клиницисты различных специальностей – общие хирурги, травматологи, нейрохирурги, гинекологи, отоларингологи, челюстно-лицевые и торакальные хирурги. С целью определения патогенного агента и тяжести инфекционного процесса используют:
- Методы детекции возбудителя. Методы экспресс-диагностики анаэробной инфекции включают бактериоскопию раневого отделяемого с окраской мазка по Грамму и газожидкостную хроматографию. В верификации возбудителя ведущая роль принадлежит бактериологическому посеву отделяемого раны или содержимого абсцесса, анализу плевральной жидкости, посеву крови на аэробные и анаэробные бактерии, иммуноферментному анализу, ПЦР.
- Другие анализы. В биохимических показателях крови при анаэробной инфекции обнаруживается снижение концентрации белков, увеличение уровня креатинина, мочевины, билирубина, активности трансаминаз и щелочной фосфатазы.
- Инструментальную диагностику. Наряду с клиническими и лабораторными исследования, выполняется рентгенография, при которой обнаруживается скопление газа в пораженных тканях или полостях.
Анаэробную инфекцию необходимо дифференцировать от рожистого воспаления мягких тканей, полиморфной экссудативной эритемы, тромбоза глубоких вен, пневмоторакса, пневмоперитонеума, перфорации полых органов брюшной полости.
Лечение анаэробной инфекции
Комплексный подход к лечению анаэробной инфекции предполагает проведение радикальной хирургической обработки гнойного очага, интенсивной дезинтоксикационной и антибактериальной терапии. Хирургический этап должен быть выполнен как можно раньше – от этого зависит жизнь больного. Как правило, он заключается в широком рассечении очага поражения с удалением некротизированных тканей, декомпрессии окружающих тканей, открытом дренировании с промыванием полостей и ран растворами антисептиков. Особенности течения анаэробной инфекции нередко требуют проведения повторных некрэктомий, раскрытия гнойных карманов, обработки ран ультразвуком и лазером, озонотерапии и т. д. При обширной деструкции тканей может быть показана ампутация или экзартикуляция конечности.
Важнейшими составляющими лечения анаэробной инфекции являются интенсивная инфузионная терапия и антибиотикотерапия препаратами широкого спектра действия, высокотропными к анаэробам. В рамках комплексного лечения анаэробной инфекции находят свое применение гипербарическая оксигенация, УФОК, экстракорпоральная гемокоррекция (гемосорбция, плазмаферез и др.). При необходимости пациенту вводится антитоксическая противогангренозная сыворотка.
Прогноз и профилактика
Исход анаэробной инфекции во многом зависит от клинической формы патологического процесса, преморбидного фона, своевременности установления диагноза и начала лечения. Уровень летальности при некоторых формах анаэробной инфекции превышает 20%. Профилактика анаэробной инфекции заключается в своевременной и адекватной ПХО ран, удалении инородных тел мягких тканей, соблюдении требований асептики и антисептики при проведении операций. При обширных раневых повреждениях и высоком риске развития анаэробной инфекции необходимо проведение специфической иммунизации и противомикробной профилактики.
В больницах источниками инфекции являются пациенты с газовой гангреной. Поскольку больные с газовой гангреной представляют опасность для других хирургических пациентов, их размещают в отдельных палатах. Кроме того, лечение таких пациентов осуществляют в отдельных операционных-перевязочных с индивидуальной вентиляцией.

Стоит также отметить, что клостридии чрезвычайно устойчивы во внешней среде и способны образовывать споры. Поэтому при борьбе с этой инфекцией необходимо использовать различные методы обеззараживания — дезинфекцию и стерилизацию. При этом дезинфекция при анаэробной инфекции должна осуществляться с применением высокоэффективных дезсредств.
Дезинфекция помещений
Пол и стены в помещениях для больных с анаэробной инфекцией должны быть выполнены из материалов, которые допускают возможность проведения дезинфекции. Помещения также оборудуют УФ-облучателями.
После выписки пациента, используемую им мебель (кровать, тумбочку) в обязательном порядке полностью протирают ветошью, смоченной в дезсредство.
Уборочный инвентарь маркируют и применяют исключительно по назначению. Инвентарь после использования обеззараживают в автоклаве.
Дезинфекция предметов личного обихода
Постельное белье и полотенца следует менять раз в неделю, а при необходимости чаще. Белье собирают в закрывающиеся мешки и относят в прачечную. Непосредственно в прачечной белье сначала подвергают обеззараживанию путем замачивания в дезсредстве. По окончанию экспозиции белье стирают в машинках со стиральным порошком.
Помещения прачечной необходимо содержать в чистоте. Ежедневно поверхности помещения (пол, стены, двери) моют с дезинфицирующими средствами.
Постельные принадлежности (матрацы, одеяла) обеззараживают после выписки пациента. Обеззараживание осуществляют в дезкамерах по режиму для уничтожения споровых форм микробов.
При поступлении в больницу пациенту выдают в индивидуальное пользование предметы ухода, такие как плевательница, судно. Их регулярно моют по мере загрязнения. После выписки использованные предметы личного ухода освобождают от загрязнений, а затем подвергают дезинфекции путем замачивания в дезрастворе.
Обеззараживание медицинских изделий
Медицинские изделия также могут выступать фактором передачи анаэробной инфекции, поэтому их обязательно подвергают обеззараживанию.
Перед входом в перевязочную и операционную медперсонал надевает маски, бахилы, клеенчатые фартуки. После проведенных манипуляций фартуки вытирают ветошью, смоченной в дезсредство.
Отработанный перевязочный материал кладут в биксы и автоклавируют, затем его сжигают.
Использованный инструментарий собирают в емкость, а затем обрабатывают в три этапа:
- Дезинфекция — замачивание в дезрастворе;
- ПСО — чистка щетками в дезсредстве или мыльном растворе;
- Стерилизация — обеззараживание в стерилизаторе.
Читайте также:

