Анализ чего на хламидиоз и токсоплазмоз
Обновлено: 24.04.2024

Хламидиоз – специфическое инфекционное заболевание с половым путем передачи, возбудителем которого служит бактерия Chlamydia trachomatis. Она представляет собой внутриклеточный грамотрицательный микроорганизм, определенные серотипы которого провоцируют поражение разных тканей организма. Урогенитальный хламидиоз достаточно часто встречается в популяции среди всех ЗППП. Среди всех возрастных групп в Беларуси с наибольшей частотой выявляется у людей моложе 25 лет.
Симптомы хламидиоза

Единственным доказанным способом заражения хламидийной инфекцией как для мужчин, так и для женщин является половой контакт в любой форме с человеком, больным хламидиозом. У детей возможно инфицирование при прохождении через родовые пути больной матери.
Чаще всего встречается хламидиоз урогенитальной системы. Помимо этого возможно развитие хламидийной инфекции органов малого таза, аноректальной зоны, хламидийного фарингита и конъюнктивита. Также встречаются специфические бактериальные поражения со стороны других отделов тела: с поражением суставов (артрит), генерализованная хламидийная инфекция в виде пневмонии или перитонита.
Первые признаки хламидиоза, как правило, неспецифичны и дают повод врачу задуматься о различных инфекционных заболеваниях. При урогенитальном процессе ранние симптомы проявляются в виде выделений из половых органов, сопровождающихся зудом и повышенной чувствительностью в области промежности, отмечаются ложные позывы к мочеиспусканию. Как и при всех воспалительных процессах, будет повышена температура тела.
Хламидиоз мочеполовой локализации имеет некоторые различия в симптоматике у мужчин и у женщин. Известно, что более половины женщин не испытывают никаких симптомов хламидиоза. При развитии специфической симптоматики хламидиоза, клиническая картина будет следующая:
- женщина жалуется на слизисто — гнойное отделяемое из половой щели;
- отмечаются кровянистые выделения вне менструального цикла;
- присутствует явная болезненность при половом акте;
- отмечается жжение во время мочеиспускания;
- иногда беспокоит дискомфорт или болевые ощущения внизу живота.
С такими жалобами пациентка с подозрением на хламидиоз обычно приходит к гинекологу. При осмотре зоны промежности врач отмечает классические признаки хламидийной инфекции:
- гиперемия (покраснение) и отек слизистой выстилки уретры со слизисто — гнойным отделяемым;
- отек плюс значительная гиперемия шейки матки, сопровождающаяся также выделениями слизисто — гнойного секрета из шеечного канала.
Симптомы хламидиоза у мужчин можно описать следующим образом:
- наличие скудного слизистого или слизисто — гнойного секрета из уретрального канала;
- жжение и раздражающий зуд вплоть до болезненных ощущений при мочеиспускании;
- постоянный дискомфорт в зоне уретры;
- отмечается болезненность при половом акте;
- увеличивается частота мочеиспусканий;
- могут возникать болевые ощущения в зоне промежности, которые распространяются на область прямой кишки.
Пациент с данными жалобами попадает, как правило, на прием к урологу. При осмотре мужчины с хламидиозом врач отметит: гиперемию и значительный отек слизистой вокруг мочеиспускательного канала, и сопутствующие слизисто — гнойные выделения из уретры.
Диагностика хламидиоза

При предъявлении характерных жалоб и при выявлении специфических признаков, указывающих на развитие хламидиоза, лечащий врач обязательно назначит пациенту проведение лабораторных анализов. Только с помощью специальных тестов можно подтвердить или опровергнуть наличие бактериальной хламидийной инфекции.
В современной практике применяется несколько высоко чувствительных методов:
- тест — системы для идентификации частей ДНК или РНК хламидий;
- способ выделения возбудителя хламидиоза методом клеточного культивирования.
Симптомы урогенитального хламидиоза во многом сходны с проявлениями прочих ЗППП, поэтому перед врачом стоит задача провести дифференциальную диагностику с выявлением истинного возбудителя уретрита или цервицита. Это обусловливает целесообразность забора биоматериала для проведения ряда лабораторных проб для исключения инфицирования другими патогенными микроорганизмами, в частности, гонококком, трихомонадой, микоплазмой. Условно — патогенная флора (кандиды), а также вирусы (например, вирус простого герпеса) могут вызывать сходные с хламидиозом симптомы, и подлежат проверке в лаборатории.
Лечение хламидиоза
Обоснованием для назначения и начала лечения служит обнаружение возбудителя хламидиоза в организме с помощью лабораторных исследований. Причем хорошую антибиотикотерапию должен пройти и половой партнер инфицированного пациента. Такой подход является обязательным и необходим для полного выздоровления от хламидиоза, для предупреждения возникновения осложнений заболевания, для предотвращения распространения бактериальной инфекции и заражения других людей.
Отдельные группы населения имеют свои особенности при проведении лекарственной терапии хламидиоза:
- инфицированные беременные женщины нуждаются в лечении независимо от срока гестации, терапия проводится совместно с акушером — гинекологом, выбор медикаментов осуществляется с учетом их потенциального влияния на плод;
- терапия новорожденных проводится при участии врача неонатолога.
Препаратами выбора при лечении хламидиоза являются: доксициклин, джозамицин, азитромицин. К альтернативным антибактериальным препаратам относят фторхинолоны: левофлоксацин и офлоксацин.
Если эффекта от лечения не наблюдается, то необходимо исключить инфицирование другим видом микроорганизмов или назначить лекарственный препарат из другого фармакологического ряда.
При констатации клинического выздоровления необходимо провести лабораторный контроль через 14 дней после завершения терапии. При отрицательных результатах тестирования пациенты снимаются с диспансерного учета.
В настоящее время разработаны и применяются врачами нашей клиники клинические рекомендации для эффективной терапии ЗППП, в том числе хламидиоза. Следует понимать, что правильное грамотное назначение лечения при хламидиозе позволяет достаточно быстро устранить клинические проявления болезни и не допустить инфицирования партнера.
Что такое токсоплазмоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Токсоплазмоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое простейшими внутриклеточными паразитами — токсоплазмами, которые попадая в организм человека могут при условиях иммунодефицита поражать нервную ткань, среды глаза, сердечно-сосудистую и ретикулоэндотелиальную системы, вызывая поражение организма той или иной степени тяжести. Болезнь относится к группе TORCH-комплекса, т. е. вызывает врождённую патологию.
Этиология
Таксономия:
Вид — Toxoplasma gondii
Токсоплазмы обитают в мире в трёх формах:
- трофозоиты (тахизоиты);
- цисты (брадизоиты);
- ооцисты.
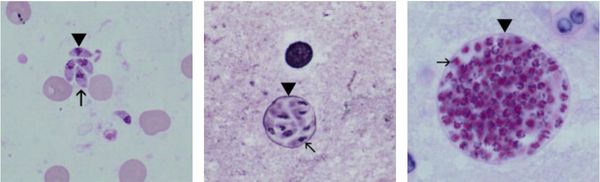
Трофозоиты достигают 4-7 мкм в длину и 2-4 мкм в ширину. Их тело по форме напоминает полумесяц с заострённым передним и закруглённым задним концами, состоит из пелликулы (покровной ткани) и различных органелл. Такие паразиты обитают во всех клетках млекопитающих кроме эритроцитов, размножаются путём деления. Могут создавать движение, активно проникая в клетки хозяина через клеточную мембрану или посредством фагоцитоза (захвата и переваривания клетки). Обнаруживаются в тканях в острой стадии инфекции. Их скопление внутри одной клетки называют псевдоцистой. Трофозоиты неустойчивы вне клетки и во внешней среде, быстро погибают при высушивании, прогревании и применении дезинфицирующих средств. Хорошо окрашиваются по Романовскому. Чувствительны к различным химиопрепаратам (сульфаниламидам, некоторым макролидам и другим).
Цисты размерами до 100 мкм отличаются плотной оболочкой, через которую не могут проникнуть антитела или лекарственные препараты. Внутри оболочки сосредоточено 3000-5000 паразитов, со временем они увеличиваются. Цисты формируются в организме хозяина (в основном в скелетных мышцах, миокарде и ЦНС) и живут там десятки лет. Чрезвычайно устойчивы к воздействиям внешних факторов. При адекватной иммунной системе могут пожизненно находиться в состоянии функционального покоя и не приносить никакого вреда организму человека.
Ооцисты играют основную роль в передаче инфекции. Они представляют собой овальные образования 10-12 мкм в диаметре. Их развитие и формирование длится 3-24 дня и проходит в слизистой оболочке тонкой кишки кошек. Затем в течение 7-20 дней паразиты выделяются с испражнениями, после этого срока новые фекалии кошки уже не заразны. За сутки с испражнениях животного выделяется до 10 миллионов ооцист. Спустя 2-3 дня при температуре 24 °C происходит споруляция ооцист — образование спор. При благоприятных условиях микроорганизмы сохраняются во внешней среде до года и дольше.
Существует множество штаммов токсоплазм, одни из которых отличаются высокой вирулентностью, а другие относительно маловирулентны. [1] [2] [7] [9]
Эпидемиология
Учитывая большое количество латентных форм, заболевание не поддаётся общему исчислению — им может быть заражено не менее 1,5 миллиардов человек. Только ежегодно регистрируется около 200 тысяч случаев внутриутробного инфицирования.
Распространение возбудителя повсеместное — токсоплазма обнаружена на всех материках. После заражения паразиты способны пожизненно сохранятся в организме большинства животных и птиц. Количество случаев приобретённого токсоплазмоза в разных странах колеблется: от 85 % во Франции и Мадагаскаре до 15 % в США и Англии.
- Фекально-оральный:
- водный и пищевой путь — при недостаточной термической обработке, чаще при употреблении сырого мяса и фарша;
- контактно-бытовой путь — при несоблюдении санитарных норм в повседневной жизни, например, при общении с кошками.
- Вертикальный путь (от матери к плоду) — преимущественно при первичном заражении матери во время беременности, часто у ВИЧ-инфицированных в стадии СПИДа.
- Артифициальный путь — при пересадке органов, в которых расположены цисты, пациенту с плохим иммунитету.
- Аэрогенный путь — при попадании инфицированной ооцистами пыли в рот человека.
- Контактный путь — при повреждении целостности кожных покровов. Встречается крайне редко, в основном у работников лабораторий и скотобоен, отмечен лишь в некоторых источниках, явного практического значения не имеет.
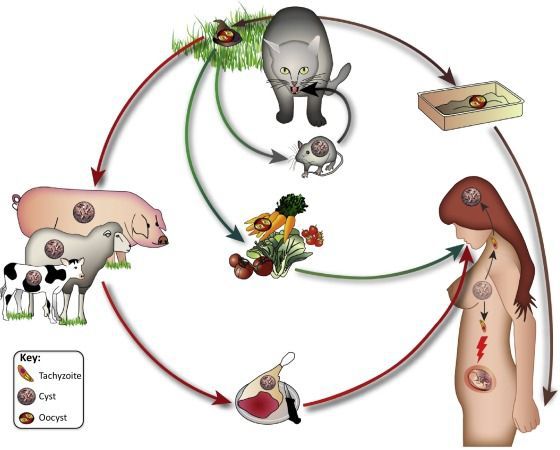
От человека к человеку заболевание не предаётся (кроме случаев каннибализма). Нельзя заразиться посредством укуса насекомых и при половом контакте.
Инфицирование токсоплазмой вызывает устойчивый пожизненный иммунитет к повторному заражению, однако известны случаи рецидива первичной инфекции при заражении другим высоковирулентным штаммом (у беременных, заразившихся при употреблении сырого мяса с другого континента). [1] [3] [5] [8] [9]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы токсоплазмоза
Инкубационный период при манифестных формах (явных проявлениях болезни) длится от двух недель до двух месяцев.
Специфичных симптомов, характерных именно для токсоплазмоза, не существует.
В большинстве случаев приобретённого токсоплазмоза заболевание протекает бессимптомно или со стёртой клиникой, напоминающей нетяжёлое ОРЗ: кратковременная лихорадка, слабость, недомогание, повышение температуры до 38,0 °C, увеличение периферических лимфоузлов, небольшое увеличение печени и селезёнки.
Доказано, что токсоплазма может оказывать влияние на психику человека. Это выражается в учащении рискованных действий, снижении концентрации внимания, повышенной нервозности, у лиц с тяжёлым острым или длительным хроническим активным течением повышен риск развития шизофрении.
Иногда заболевание проявляется изолированной глазной формой — длительно текущие увеиты, иридоциклиты и хориоретиниты. Как правило, эти нарушения являются поздними проявлениями нераспознанного ранее врождённого процесса.
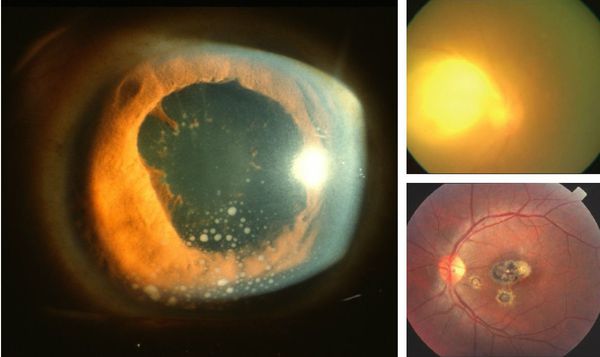
У людей с выраженным иммунодефицитом (ВИЧ, пересадка органов с последующей цитостатической терапией) возможно развитие генерализованного процесса с поражением нескольких органов (головного мозга, сердца, печени, почек, лёгких), нередко очень тяжёлого течения, проявляющегося в виде синдрома полиорганной недостаточности.
Токсоплазмоз у беременных может протекать в различных клинических вариантах и представляет опасность не столько для самой беременной (исключая тяжело протекающие патологии у беременных со СПИДом), сколько для плода.
При первичном заражении беременной токсоплазмозом имеет значение срок гестации:
- При инфицировании в первом триместре передача возбудителя плоду происходит лишь в 4 % случаев (к 13 неделе — в 6 %), но заканчивается, как правило, гибелью плода и выкидышем на ранних сроках. Если первичная инфекция у матери в первом триместре доказано, но выкидыш до 13 недели беременности не произошёл, то крайне высока вероятность, что внутриутробной передачи не было и ребёнок будет здоров.
- При инфицировании во втором триместре (особенно на 24-26 неделях) риск внутриутробной передачи резко возрастает и достигает 30-40 %, причём сопровождается развитием тяжёлых проявлений заболевания — одновременное увеличение селезёнки и печени, воспаление сосудистой оболочки и сетчатки глаза, поражения ЦНС в виде гидроцефалии, кальцификация, сыпь, миокардит, пневмония и другие.
- При заражении матери в третьем триместре передача инфекции ребёнку происходит с частотой до 90 %, однако проявления заболевания являются латентными или субклиническими и могут появиться спустя годы после рождения (отставание в развитии, нарушения зрения). [1][2][4][9]
Патогенез токсоплазмоза
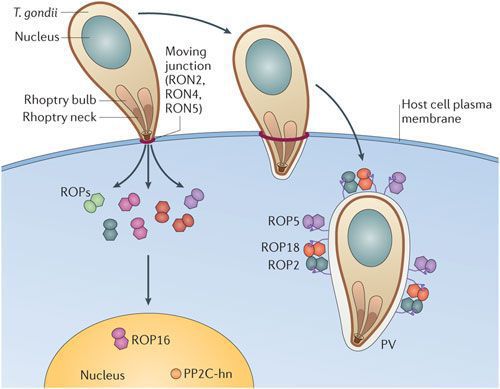
По мере развития и размножения токсоплазм поражённые клетки разрушаются, происходит заражение новых здоровых клеток, и при попадании возбудителя в кровоток паразиты разносятся по всему организму. Образуются некрозы с формированием фиброзной ткани и кальцификацией (отложение солей кальция в организме).
Под воздействием иммунитета безоболочечные трофозоиты превращаются в брадизоиты (оболочечные скопления токсоплазм), т.е. в тканевые цисты, которые сохраняются десятками лет в неактивном состоянии и при значительном снижении иммунитета способны к обратной трансформации с развитием обострения.
При первичной инфекции у беременных возбудитель проникает в ткани плода и вызывает воспалительный процесс, причём в разные периоды развития наблюдается различный характер воспаления: у эмбриона происходит лишь альтерация (дистрофия и некроз ткани без фиброза), в раннем фетальном периоде дополняется повышенным образованием соединительной ткани (фиброзом), а в позднем фетальном периоде присоединяется сосудистый компонент. Отсюда вытекают различные по характеру и тяжести поражения плода, которые зависят от сроков инфицирования матери. [1] [2]
Классификация и стадии развития токсоплазмоза
По течению процесса токсоплазмоз бывает:
- острым — до одного месяца;
- подострым - 1-3 месяц;
- хроническим — более трёх месяцев.
По клиническим признакам выделяют пять форм заболевания:
- Врождённый острый токсоплазмоз:
- манифестная форма (с указанием ведущих проявлений);
- субклиническая форма (с указанием способа верификации диагноза).
- Врождённый хронический токсоплазмоз:
- обострение / ремиссия;
- с резидуальными (остаточными) явлениями / без резидуальных явлений.
- Врождённый латентный токсоплазмоз.
- Приобретённый острый токсоплазмоз.
- Приобретённый хронический токсоплазмоз.
По степени тяжести заболевание бывает:
- лёгким;
- среднетяжёлым;
- тяжёлым (врождённая инфекция, токсоплазмоз при СПИДе).
По наличию осложнений выделяют:
- осложнённый токсоплазмоз;
- неосложнённый токсоплазмоз.
В Международной классификации болезней 10 пересмотра выделены шесть типов заболевания:
- B58.0 Токсоплазмозная окулопатия;
- B58.1 Токсоплазмозный гепатит (K77.0*);
- B58.2 Токсоплазмозный менингоэнцефалит (G05.2*);
- B58.3 Легочный токсоплазмоз (J17.3*);
- B58.8 Токсоплазмоз с поражением других органов;
- B58.9 Токсоплазмоз неуточнённый. [1][2][3]
Осложнения токсоплазмоза
При врождённой форме может возникнуть гидроцефалия, микроцефалия, задержка психомоторного развития и слепота. Эти осложнения сопровождаются увеличением или уменьшением размеров черепа, различными неврологическими расстройствами — косоглазием, судорогами, трудностью с сидением и держанием головы, рвотой и другими.
При глазной форме заболевания развивается слепота, снижение остроты зрения и воспалительные явления всех сред глаза. Причём возможно как рождение с грубыми дефектами зрения, так и появление воспалительных явлений и нарушения зрения спустя много лет после рождения.
Токсоплазмоз у иммунокомпрометированных людей осложняется шизофренией, токсоплазменный энцефалитом и полиорганной недостаточностью — тяжёлой патологией различных органов при выраженном иммунодефиците. При этом свойственна картина тяжёлого энцефалита. Прогноз, как правило, неблагоприятный. [1] [5] [8] [9]
Диагностика токсоплазмоза
Лабораторная диагностика:
- Клинический анализ крови: снижение уровня тромбоцитов, увеличение количества лимфоцитов и эозинофилов.
- Биохимический анализ крови: возможно повышение уровня трансаминаз и билирубина.
- Иммуноферментный анализ (ИФА):
- Выявление специфических антител класса M — острая инфекция или её реактивация. Имеет ряд недостатков — низкая специфичность, длительная циркуляция в организме, иногда до года после острого процесса. В сложных случаях уточнение следует производить при помощи метода "двойной сэндвич" или "иммунозахват" IgM ELISA.
- Выявление специфических антител класса G (клеток памяти) — носительство, инфицированность — появляются в среднем со второй недели заболевания и достигают пика на 1-2 месяце, сохраняются пожизненно, за исключением СПИД-ассоциированных заболеваний.
- Авидность IgG — уточнение давности заболевания. Недостатком является отсутствие стандартизации результатов, что зачастую приводит к различным ошибкам интерпретации. Наибольшее значение имеет высокая авидность, остальные результаты низкой и слабой авидности могут быть ошибочными и не должны трактоваться как недавно перенесённое заболевание при отсутствии других подтверждающих этот факт тестов.
- ПЦР-диагностика: выявление ДНК токсоплазмы в крови, других жидкостях и тканях человеческого организма. Особенно информативна в диагностике генерализованного, глазного и врождённого токсоплазмоза, в т. ч. в антенатальном периоде путём проведения амнио (не ранее 16 недель) и кордоцентеза (с 18 недели беременности).
- УЗИ-диагностика: внутриутробное выявление гидро- и микроцефалии, кальцификатов, гепатоспленомегалии и выраженной задержки развития. [1][2][4][5][6]
Дифференциальная диагностика
Токсоплазмоз — это инфекция с необычайно разнообразными проявлениями, поэтому ввиду неспецифичности проявлений основное место в дифференциальной диагностике отводиться лабораторному обследованию, а именно специфическим серологическим тестам.
Необходимо исключить следующие заболевания:
-
(ВЭБ-инфекцию) — боли в горле, преимущественное увеличение затылочных и заднешейных лимфоузлов, характерные изменения гемограммы (появление большого количества атипичных мононуклеаров и отсутствие столь выраженных изменений при врождённом течении), положительные IgM и ПЦР крови; — лимфоцитарный характер гемограммы, частое поражение слюнных желёз, положительные IgM, ПЦР крови;
- туберкулёз — длительное постепенное начало, лёгкий субфебрилитет (до 38,0 °C), ночная потливость, нездоровый румянец на щеках, кашель, специфические изменения в лёгких, положительные пробы на туберкулёз, выявление бациллы Коха в мокроте;
- лимфопролиферативные заболевания (лимфома Ходжкина, неходжкинские лимфомы) — специфические изменения при биопсии поражённой ткани (лимфоузлов);
- ВИЧ-инфекция — наличие факта возможного заражения, увеличение всех групп лимфоузлов, положительная серология;
- саркоидоз — специфические изменения в лёгких, положительные результаты гистологического исследования. [1][2][5]
Лечение токсоплазмоза
Большинство случаев приобретённого токсоплазмоза протекают в лёгкой или бессимптомной форме, они не регистрируются и, по-видимому, не нуждаются в каком-либо лечении.
Необходимость проведения специфической этиотропной терапии возникает лишь у некоторых групп пациентов:
- беременные с доказанным первичным инфицированием (в ряде случаев при реактивации хронической инфекции);
- дети с врождённой формой токсоплазмоза (при наличии явных клинических и лабораторных проявлений заболевания, субклинических и инаппарантных формах) — сроки и объём терапии зависят от конкретных данных;
- иммунокомпрометированные люди, у которых токсоплазмоз (острый или в фазе реактивации хронического процесса) протекает с выраженными клинико-лабораторными проявлениями. Основное направление воздействия в этом случае должно быть на устранение причины иммунодефицита, повышение уровня СД4 клеток.
Проведение лечения может осуществляться как в стационаре, так и амбулаторно в зависимости от выраженности процесса, реакции пациента на вводимые препараты, необходимости тех или иных вариантов патогенетического и симптоматического обеспечения. [1] [4] [7]
Прогноз. Профилактика
При приобретённом токсоплазмозе у иммунокомпетентных лиц прогноз благоприятный, у иммунокомпрометированных лиц (СПИД) прогноз серьёзен, нередки летальные исходы.
При врождённом токсоплазмозе исход заболевания зависит от сроков инфицирования плода:
- при инфицировании в первом триместре, как правило, происходит выкидыш;
- в более поздние сроки последствия варьируются от тяжёлых до резидуальных форм.
Основным методом профилактики приобретённого и врождённого токсоплазмоза является соблюдение санитарно-гигиенических правил, особенно беременными, не имеющими антител класса G к токсоплазмам:
- ограничение контакта с кошками;
- запрет на употребление сырого мяса, фарша и морепродуктов;
- тщательная промывка зелени, фруктов и овощей;
- мытьё рук перед едой;
- работа на приусадебном участке только в перчатках.
Для беременных особенно важен скрининг антител к токсоплазме, позволяющий выявить активно протекающее заболевание или риск его возникновения, а также вовремя провести медикаментозную профилактику острого токсоплазмоза беременной и снизить риск врождённой инфекции на 60 %. При отсутствии антител класса G в первом триместре необходимо отслеживать антитела IgM и IgG не только в тертьем, но и во втором триместре беременности.
В очаге токсоплазмоза противоэпидемические мероприятия не проводятся, вакцина на разработана. [2] [3]
Токсоплазмоз — это заболевание человека, вызванное микроскопическим одноклеточным паразитом Toxoplasma gondii. Отличается большим разнообразием клинических проявлений, в основном поражает:
- Нервную систему.
- Глаза.
- Скелетные и сердечную мышцы.
- Лимфатическую систему.
Возбудитель очень распространен в природе, его переносят несколько сотен видов животных и птиц, в том числе – домашних. Паразит легко проникает в организм, но часто не приводит к развитию острой инфекции. Заболевание обычно развивается у людей со сниженной иммунной реакцией – больных СПИДом и другими иммунодефицитными состояниями, при приеме иммуносупрессоров.
Возбудители заболевания, его источники
Наиболее опасным является внутриутробное инфицирование, которое нередко заканчивается выкидышем либо тяжелыми врожденными патологиями. По этой причине анализ на токсоплазмоз должен обязательно проводится при подготовке к беременности и вынашиванию ребенка.
По статистическим данным токсоплазма обнаруживается у 25-80% населения планеты. В отдельных регионах степень заражения достигает 95%.

Токсоплазма – внутриклеточный паразитический организм, который способен существовать в трех формах:
- Тахиозоиты. Имеют форму полумесяца и размер 2-4 мкм. Характерная особенность – при специальной окраске (по Романовскому-Гимзе) ядро приобретает красный цвет, а цитоплазма становится серо-голубой. В этой форме паразит проникает в клетки иммунной системы (макрофаги, фагоциты), в которых быстро размножается. После гибели клетки тахиозоиты высвобождаются и заражают здоровых макрофагов.
- Брадиозоиты (псевдоцисты). Это защитная форма токсоплазмы, в которой происходит большая часть жизнедеятельности возбудителя при нормальной иммунной реакции со стороны зараженного организма. Форма клетки брадиозоитов удлиненная, ядро смещено к одному из окончаний. Токсоплазмы в этой форме часто формируют тканевые псевдоцисты состоящие из множества клеток паразиты покрытых общей защитной оболочкой.
- Ооцисты. Эта форма токсоплазмы встречается только в эпителиальных клетках кишечника домашней кошки и ее диких родственников. Образуется в результате полового размножения паразита внутри клеток животного. Затем незрелые ооцисты выделяются в окружающую среду вместе с фекалиями. При достаточной температуре и притоке свежего кислорода ооцисты созревают в течение 2-7 дней. После завершения созревания ооцисты становятся способны заражать промежуточных хозяев токсоплазмы, в том числе – людей.
Основным источником заражения являются представители семейства кошачьих, в подавляющем большинстве – домашняя кошка. Механизм передачи паразита – фекально-оральный. Реализуется за счет:
- Употребления недостаточно термически обработанных мясных продуктов (особенно свинины и баранины).
- Через плохо вымытые овощи, зелень, фрукты.
- Несоблюдение правил личной гигиены (немытые руки).
Изредка возможно прямое заражение токсоплазмой через микроповреждения кожных покровов. От матери к ребенку паразит передается редко. В среднем одно заражение на 2-3,5 тыс. беременных. Наиболее вероятно инфицирование плода токсоплазмой если в процессе вынашивания организм беременной впервые столкнулся с паразитом.
Восприимчивость к токсоплазме крайне высока, для заражения достаточно единичных ооцист. Наиболее восприимчивы молодые люди, у пожилых (после 60 лет) паразит выявляется значительно реже.

Приобретенный токсоплазмоз, симптомы

Явные клинические симптомы у большей части заразившихся отсутствуют, болезнь сразу переходит в латентную фазу носительства. Инкубационный период составляет от 1 до 3 недель.
При проявлении выраженной клинической картины симптоматика нарастает медленно. Обычно болезнь начинается бессимптомно с увеличения региональных лимфатических узлов (паховых, подмышечных, шейных). Лимфоузлы эластичны, безболезненны, больные в этот период не предъявляют никаких жалоб.
После первой недели развития инфекционного процесса происходит увеличение селезенки и печени. Могут возникать ноющие боли в крупных мышечных группах нижних и верхних конечностей. У каждого пятого в этот период развивается хориоретинит проявляющийся в выпадении участков поля зрения.
Начиная со второй недели симптоматика поражения ЖКТ начинает затухать. Уменьшаются и быстро исчезают симптомы энтерита, снижается общая интоксикация организма. Одновременно развивается поражение:
- Опорно-двигательной системы. Усиливается болевой синдром в конечностях, суставах, возможно нарушение подвижности и мелкой моторики.
- Ретикулоэндотелиальной. Проявляется гепатолиенальным синдромом, мезаденитом.
- Сердечно-сосудистой. Нередко развиваются нарушения ритма сердечных сокращений, симптомы миокардита либо перикардита.
На 3-4 неделе заболевание завершается затуханием всех проявлений и переходом токсоплазмоза в бессимптомное носительство. При воздействии негативных факторов, ослабляющих иммунитет возможна манифестация заболевания с развитием вышеописанной клинической картины, которая снова переходит в латентную фазу.
Частые рецидивы острой формы токсоплазмоза, особенно на фоне иммуноподавляющих факторов, могут приводить к серьезным осложнениям. Чаще встречаются:
- Миокардиодистрофия.
- Психоневрологические патологии.
- Снижение интеллекта.
- Атрофия зрительного нерва вплоть до полной слепоты.
- Синдром хронической усталости.
Острый токсоплазмоз у женщин может приводит к нарушению менструального цикла, выкидышам и другим патологиям со стороны половой системы.
Хронический приобретенный токсоплазмоз – достаточно редкое явление, считается СПИД-ассоциированной формой заболевания. Протекает с периодическими обострениями, часто развиваются осложнения со стороны ЦНС в виде энцефалитов и поражения органов зрения.
Наиболее тяжелое следствие хронического токсоплазмоза – генерализованная инфекция в ходе которой быстро развивается полиорганная недостаточность, иногда данное осложнение завершается смертью больного.
Врожденный токсоплазмоз, возникающий при беременности

Возникает при проникновении паразита через плацентарный барьер и заражении плода. В большинстве случаев происходит при первичном заражении во время беременности, реже – при рецидиве токсоплазмоза связанном со снижением иммунитета. Основная группа риска – женщины, которые не были заражены токсоплазмой до наступления беременности. Если в результате контакта с возбудителем произойдет манифестация заболевания в процессе вынашивания плода – достаточно высока вероятность развития врожденного токсоплазмоза.
Процент выживаемости детей при внутриутробном инфицировании зависит от срока, на котором оно произошло:
- При инфицировании на первом триместре шанс на выживание плода – 15%
- На втором – 30%.
- На третьем – 60%
Даже если беременность успешно завершается, сохраняется крайне высокая степень развития врожденных патологий и врожденного токсоплазмоза. Болезнь протекает тяжело, особенно если инфицирование произошло на ранних сроках. Развивается характерная тетрада патологигй:
- Гидроцефалия.
- Двусторонний ретинохороидит.
- Задержка психофизического развития.
- Церебральные кальцификаты.
Прогноз в случае врожденного токсоплазмоза неблагоприятный, в большинстве случаев болезнь завершается смертью новорожденного либо тяжелой инвалидизацией. Даже если после внутриутробного заражения острая клиническая картина не возникла такие дети находятся в группе риска развития:
- Умственной недостаточности.
- Эпилепсии.
Возможно развития многих других патологий, которые проявляются спустя месяцы и годы после рождения. По этой причине острая форма токсоплазмоза, возникшая во время беременности – показание к проведению аборта даже на поздних сроках. При беременности необходимо сдавать массу анализов, которые помогают выявить наличие не только токсоплазмоза, но и ЦМВ-инфекции.
Показания к обследованию
Анализ чаще всего назначают в двух случаях:
- При планировании беременности в составе стандартного пакета лабораторной диагностики TORCH-инфекции.
- При подозрении на токсоплазмоз и определенных симптомах.
Также лабораторная диагностика используется при выявлении симптомов острого токсоплазмоза у взрослых либо детей.
В общей врачебной практике данный анализ назначают в случае проявления у пациентов специфических симптомов (нарушение зрения, судороги) а также ВИЧ-инфицированным.
Дифференциальная диагностика
Проводится с болезнями, симптомы которых схожи с острой и хронической формой токсоплазменной инфекции. В их число входят:
- Инфекционный мононуклеаз.
- Микоплазмоз.
- Хламидиоз.
- Цитомегалия.
- Туберкулез.
Также необходимо исключить онкологические патологии и системные заболевания (ревматизм, лимфогранулематоз). Окончательный диагноз устанавливается после получения результатов специфичных серологических исследований и ПЦР. Существует достаточно много лабораторных методик обнаружения специфических антител к токсоплазме. В их число входят:
- ИФА. Иммуноферментный анализ.
- РНИФ. Реакция непрямой иммунофлюоресценции. Становится позитивной с первой недели заболевания. Высокий титр антител может сохранятся до 15 лет.
- РСК. Реакция связывания комплемента. Становится положительной с 10-14 дня развития болезни, сохраняется на протяжении 2-3 лет.
Материал для исследования

Для обнаружения специфических антител к токсоплазме производится забор крови из вены, особой подготовки процедура не требует. Для проведения ПЦР-реакции подходит любой биологический материал – кровь, слюна, образцы тканей, другие биологические жидкости (ликвор, моча).
Если возникает потребность в диагностике токсоплазмоза у плода возможен забор крови из пупочного канатика. Процедура назначается редко потому что связана с высоким риском осложнений и преждевременного прерывания беременности. Более щадящая методика – взятие на анализ околоплодной жидкости путем пункции. Эти методики применяют в случае, когда результаты специфических анализов беременной с подозрением на токсоплазмоз не дают достаточной ясности диагноза.
Показания к применению различных лабораторных исследований и особенности интерпретации результатов у разных категорий обследуемых
В зависимости от категории пациента (возрастной группы, группы риска) показано применения различных наборов методик диагностики. Особенно важен правильный выбор диагностических методов в случае подозрений на токсоплазмоз у беременных женщин.
Обследование на токсоплазмоз при беременности
Если в процессе беременности у беременной выявлены симптомы которые могут свидетельствовать о развитии острого токсоплазмоза необходимо при помощи серологических методов установить уровень специфических иммуноглобулинов.
Для выявления острой стадии заболевания лучше всего подходит иммуноферментный метод (ИФА). Он наиболее точно показывает концентрацию IgM, повышение уровня которого свидетельствует о протекающем, либо недавно присутствовавшем остром токсоплазмозе.
Определение уровней IgG менее информативно так как эти антитела сохраняются долгое время после перенесенной инфекции и свидетельствуют скорее о носительстве, чем о недавнем заражении либо обострении. Женщины, перенесшие инфицирование токсоплазмой до беременности застрахованы от заражения плода и не входят в группу риска.
Также важно получение иммунологической картины в динамике, для чего специфические тесты проводятся не реже 1 раза в 2 недели. Изучение динамики изменений титров антител позволяют с большей точностью установить диагноз.
Нужно учитывать, что серологическая картина, свидетельствующая об инфицировании токсоплазмой не является 100% показанием для прерывания беременности. В этом случае потребуется проведение дополнительных анализов путем взятия крови плода из пупочного канатика и образцов амниотической жидкости пункционным методом.
Обследование новорожденных детей и детей раннего возраста
Направлено на раннее обнаружение возбудителя, до начала острой фазы врожденного токсоплазмоза и развития тяжелых осложнений. Назначается, когда есть подозрение на инфицирование токсоплазмой, включает в себя следующие тесты:
- Выделение паразита путем внесения материала из плаценты и пупочного канатика в живых мышей.
- Проведение ПЦР-анализа амниотической и люмбальной жидкостей.
- Компьютерная томография либо МРТ головы. Позволяет выявить на ранних стадиях специфические изменения в головном мозге, например, гидроцефалию.
Серологические методики также применяются, но они дают только дополнительную информацию. Иммунная система новорожденного недостаточно активна, часто неспособна выработать достаточно высокий титр специфических антител.
Обследование больных ВИЧ-инфекцией
Диагностика заключается в регулярном отслеживании титров иммуноглобулинов G серологическими методами. Титрование иммуноглобулинов M неинформативно так как у большинства ВИЧ-позитивных уровень антител этой группы крайне вариабелен.
В прямом выявлении возбудителя путем микроскопии образцов ткани либо заражения лабораторных животных как правило необходимости нет. Диагноз достаточно точно можно установить за счет серологической диагностики и наличия специфической клиники токсоплазмоза. У ВИЧ-позитивных больных она более выражена, что значительно упрощает постановку диагноза.
Обследование в Медарт

На базе медицинского центра Медарт выполняется полный комплекс серологических анализов для выявления токсоплазмы в организме пациента. Иммунологическое исследование с целью выявления специфических иммуноглобулинов входит в состав комплексных тестов ЗППП, предназначенных для пар, планирующих рождение ребенка. Возможно выполнения забора крови и других биологических жидкостей для установления наличия токсоплазмы и уточнения клинической картины протекания заболевания.
Высокоточное современное оборудование позволяет в кратчайшие сроки получить точные результаты исследований.
Преимущества медицинского центра Медарт:
- Квалифицированные специалисты.
- Возможность быстро получить точный результат исследования.
- Доступная стоимость.
На базе медцентра предоставляется полный комплекс услуг, от предварительного приема и консультаций до постановки и уточнения диагноза и назначения эффективных схем лечения и профилактики токсоплазмоза и других заболеваний.

Хламидии в человеческом организме — причина хронических и острых инфекций. У 70-80% пациентов, инфицированных хламидиями, выраженные симптомы отсутствуют. Обнаружить источник проблем со здоровьем можно только, сдав анализ на хламидии.
СТОИМОСТЬ ПРИЕМА ГИНЕКОЛОГА, УРОЛОГА (МУЖЧИНЫ, ЖЕНЩИНЫ) — 1000 руб. КОНСУЛЬТАЦИЯ ПО РЕЗУЛЬТАТАМ УЗИ или АНАЛИЗОВ — 500 руб.
Хламидиоз – опасная и очень распространенная инфекция. Согласно статистике, приблизительно 5-10% ведущих активную половую жизнь людей до 35 лет являются ее носителями. Болезнь вызывается хламидиями – внутриклеточными паразитами, в которых объединены признаки патогенных вирусов и бактерий. Исследование в лабораторных условиях – основное средство обнаружения хламидий в организме пациента.

Когда нужно сдать анализ на хламидии
На анализ на хламидии направляет гинеколог или уролог, но пройти его можно и по своей инициативе, без направления.
- Обследование на хламидии обязательно проходить всем супружеским парам, планирующим беременность. Хламидиоз негативно влияет на течение беременности и плод, вызывая выкидыши, задержку развития и внутриутробное заражение плода.
- Проверка на хламидии показана представителям обоих полов в связи с бесплодием, воспалением гениталий, болезнями суставов и дыхательных путей, конъюнктивитом, особенно если при этом присутствуют проблемы с мочеполовой сферой. Часто именно этот возбудитель становится причиной тяжелых заболеваний, но узкопрофильные врачи даже не предполагают такой вариант. В результате назначенное лечение не приносит результатов.
- Исследование на хламидии стоит пройти женщинам, у которых были преждевременные роды, внематочные беременности и самопроизвольная гибель плода.
Какие анализы нужно сдать: плюсы и минусы диагностики
Существуют три варианта анализов на хламидии: бактериальный посев, ИФА и ПЦР. Все они обладают плюсами, минусами и в разной степени точны, поэтому в идеале стоит проходить комплексную проверку.
В обязательном порядке проводится анализ крови на хламидии. Этот анализ считается более достоверным, чем бактериологическое изучение соскобов и мазков. Также проводится ПЦР анализ и ИФА.
ИФА на хламидии — достоверность 60%
ИФА — эффективный иммуноферментный анализ, при котором на предмет антител к хламидиям проверяют кровь пациента. Расшифровка анализа позволяет установить, был ли пациент заражен хламидиями, активна ли инфекция в его организме.
ИФА находит в крови антитела IgM, IgG, IgA к хламидиям. Организм вырабатывает эти иммуноглобулины в ответ на инфицирование. Основное достоинство анализа ИФА — возможность не только определить возбудителя болезни, но и установить стадию развития инфекции – хроническую или острую.
Первые антитела возникают в крови человека уже приблизительно на 10-20 день заболевания. Затем развиваются и другие иммуноглобулины, сообщающие о повторном заражении или хроническом хламидиозе. Основной минус ИФА – вероятность ошибки, так как точность этого анализа на хламидии составляет около 60%.
ПЦР-диагностика — 99%
Этот анализ наиболее эффективный и точный метод обнаружения хламидий. При ПЦР анализе изучается ДНК, приумноженная в несколько раз. Повышенная степень чувствительности реакции дает возможность определить как острый, так и латентный хламидиоз, развивающийся в хронической скрытой форме.
У метода ПЦР как средства выявления хламидий есть масса преимуществ. Анализ позволяет обнаружить бессимптомную инфекцию, характеризуется высокой точностью (99%). Однако ложноположительные результаты все-таки встречаются Поэтому при подозрении на хламидии следует комбинировать этот способ обследования с другими.
Культуральный метод (бактериальный посев) — достоверность 100 или 50%
Посредством этого анализа устанавливают чувствительность инфекции к антибиотикам. Для обнаружения хламидий в лабораторных условиях в специфической среде выращивается биологический материал, взятый у пациента. Исследуются особенности, присущие конкретному возбудителю.
Основные недостатки культурального способа – длительность ожидания результатов и высокая стоимость. В то же время эта методика гарантирует стопроцентную точность положительного результата. К сожалению, это не относится к хроническому хламидиозу. Он устанавливается с помощью культурального посева только в 50% случаях.
Комплекс анализов на хламидии позволит сформировать полную картину заболевания, подобрать индивидуальную программу лечения для конкретного пациента.
Подготовка к анализу на хламидии
Обнаружение хламидий в организме пациента несложная задача при достаточной оснащенности медицинского центра. От больного требуется всего лишь грамотно подготовиться к сдаче материала.
Мазок
Для проведения анализа ПЦР на хламидии у пациентов обоих полов в основном берется мазок. Ниже рассмотрены правила подготовки для мужчин и женщин. Особая подготовка к анализу на хламидии при беременности не требуется.
Подготовка к взятию мазка у мужчин:
- Приблизительно за пару дней до взятия мазка на хламидии мужчина должен начать воздерживаться от половых контактов.
- Вечером перед анализом ПЦР на хламидии нужно провести гигиену половых органов. Мыться в день обследования не нужно.
- Примерно за 2-3 часа перед проведением анализа не рекомендуется мочиться.
- Прием любых лекарственных медикаментов должен быть прекращен приблизительно за 7 дней до обследования. Если это не представляется возможным, нужно обсудить ситуацию с лечащим врачом.
Подготовка к взятию мазка у женщин:
- За пару дней до проведения ПЦР на хламидии отказаться от занятий сексом.
- Прекратить применять любые средства интимной гигиены, проводить спринцевания за 2-3 суток до сдачи мазка.
- Примерно за неделю до анализа стоит отказаться от лекарств в виде таблеток, вагинальных свечей или спреев, если их прием перед исследованием на хламидии не прописан врачом.
- Гигиена половых органов осуществляется вечером, используется только теплая вода. В день обследования она не нужна.
- За 2-3 часа до анализа ПЦР желательно не мочиться.
Правила подготовки к анализу крови ИФА на хламидии
Принципы подготовки к анализу крови ИФА на хламидии, одинаковы для мужчин и женщин.
- Кровь на хламидии рекомендуется сдавать натощак, воздерживаясь от употребления пищи в течение 6-8 часов. Вода может употребляться пациентом в любом количестве, однако сладкие напитки под запретом.
- От жирной пищи нужно отказаться примерно за сутки до анализа, чтобы результаты не искажались.
- Допустимость приема лекарственных препаратов за неделю до проведения ИФА анализа стоит обговорить с лечащим врачом. Если такая возможность есть, лучше воздержаться от этого.
- За день или два до сдачи крови на хламидии нужно отказаться от употребления алкогольных напитков, приблизительно за час до анализа нельзя курить.
Соблюдая эти простые правила, пациент может рассчитывать на получение корректных результатов анализов, их правильную расшифровку.
Расшифровка анализа на хламидии
Расшифровку анализов на хламидиоз проводят гинеколог и уролог. Эти же врачи занимаются лечением инфекции.

Прием гинеколога

Прием уролога
Расшифровка анализа ПЦР. При проведении анализа ПЦР на хламидии возможно два результата: отрицательный и положительный.
- Отрицательный результат ПЦР говорит о том, что следы хламидий не были обнаружены в биологическом материале. Следовательно, инфекция в организме отсутствует.
- Положительный результат анализа ПЦР говорит о том, что хламидии присутствуют в биологическом материале больного.
Метод ПЦР как средство выявления хламидий характеризуется более высокой точностью и надежностью, чем анализ крови ИФА. Поэтому расшифровке его результатов можно доверять, он сдается в обязательном порядке при подозрении на наличие хламидий в организме.
Результаты анализа крови ИФА
Основное преимущество анализа крови ИФА – возможность не только определять или опровергать присутствие хламидий в человеческом организме, но и контролировать динамику развития инфекции. Расшифровка анализа ИФА может дать один из приведенных ниже результатов.
Отсутствие антител IgM, IgG. Если в результате анализа ИФА на хламидии не были диагностированы антитела к ним, можно прийти к выводу, эта инфекция не знакома организму пациента.
Отсутствие антител IgM, наличие антител IgG. Если в крови пациента в результате проведения ИФА выявляются лишь иммуноглобулины IgG к хламидиям, это говорит о том, что заболевание было перенесено им в прошлом, а сейчас оно неактивно.
Наличие антител IgM и IgG. Если расшифровка ИФА говорит о том, что в крови больного присутствуют иммуноглобулины обеих групп, можно сделать два предположения. Первый вариант – хламидии были занесены в организм пациента несколько месяцев назад. Второй вариант – инфекция активизировалась в организме человека повторно.
Точность анализа ИФА на хламидии составляет приблизительно 60%. Следовательно, его следует применять лишь в комплексе с другими исследованиями, но не как самостоятельное средство обнаружения хламидиоза.
Читайте также:

