Анализ на сифилис после сафоцида
Обновлено: 17.04.2024
До настоящего времени инфекции, передающиеся половым путем (ИППП), остаются важнейшей проблемой здравоохранения. Интерес к этой тематике обусловлен произошедшими в нашей стране глубокими социально-экономическими изменениями, приведшими к росту заболеваемости ИППП, которые нередко влекут за собой развитие осложнений со стороны репродуктивной системы мужчин и женщин.
В настоящей статье будут освещены вопросы терапии наиболее значимых урогенитальных инфекционных заболеваний.
Основными препаратами, применяемыми в терапии гонококковой инфекции, являются цефалоспорины III поколения (цефтриаксон, цефотаксим), фторхинолоны (ципрофлоксацин, офлоксацин) и спектиномицин.
До настоящего времени, несмотря на наличие высокоэффективных антимикробных препаратов, во всем мире гонорея остается трудноконтролируемым заболеванием, на эпидемиологию которого значительное влияние оказывают социальные, демографические и поведенческие факторы. Наиболее серьезной проблемой в терапии гонореи являются рост и быстрое распространение резистентности гонококка как к традиционно применяющимся, так и к новейшим антибиотикам.
В последние годы вопросами резистентности гонококка к антибактериальным препаратам занимаются исследователи многих стран мира. В Российской Федерации благодаря внедрению в 2004 г. системы мониторинга антибиотикорезистентности продемонстрирована высокая степень резистентности возбудителя к традиционно применяемым препаратам, а также выявлена тенденция к изменению чувствительности микроорганизма к препаратам, появившимся на фармацевтическом рынке сравнительно недавно. В 2006 г. обнаружены однонаправленные тенденции роста устойчивости гонококков к пенициллинам, тетрациклинам, ципрофлоксацину, а в ряде регионов – к спектиномицину, что позволило внести коррективы в схемы лечения гонореи в зависимости от региональной принадлежности штаммов. В настоящее время ввиду распространенности перекрестной резистентности штаммов гонококков можно прогнозировать возрастание уровня устойчивости как к ципрофлоксацину, так и к другим представителям группы фторхинолонов.
Одним из антибиотиков, обладающих активностью в отношении возбудителя гонококковой инфекции, является азитромицин. Согласно данным проведенных исследований, резистентность N. gonorrhoeae к нему до последнего времени оставалась на низком уровне и составляла в различных регионах от 1 до 3 %. Хотя в настоящее время азитромицин не входит в список препаратов, рекомендуемых международными руководствами для лечения гонореи, в некоторых ситуациях, в частности при непереносимости других лекарственных средств, его применение может быть вполне оправданным.
Следует особо подчеркнуть, что азитромицин является эффективным препаратом и для лечения другой распространенной ИППП – хламидийной инфекции. Урогенитальный хламидиоз довольно часто бывает ассоциирован с гонококковой инфекцией, однако воспалительный процесс, как правило, протекает без клинических симптомов, что в отсутствие своевременной диагностики и лечения может привести к длительному течению заболевания, развитию осложнений, нарушению репродуктивной функции.
Современные схемы лечения хламидийной инфекции основаны на применении одного из антибиотиков следующих фармакологических групп: макролидов (азитромицин, джозамицин, кларитромицин, рокситромицин и др.), фторхинолонов (офлоксацин, левофлоксацин, моксифлоксацин и др.) и тетрациклинов (доксициклин). Доза препарата и длительность лечения зависят от характера течения заболевания и определяются врачом.
Наиболее часто рекомендуется применение азитромицина. Среди макролидов он способен создавать самые высокие концентрации в тканях, характеризуется хорошей переносимостью. Прием пищи несколько снижает биодоступность этого препарата, поэтому желателен его прием натощак. Период полувыведения азитромицина достигает 55 часов, что позволяет однократно применять его при хламидиозе нижних отделов мочеполового тракта. Согласно данным Веселова А.В. и соавт. (2006), азитромицин при однократном применении обладает 96 %-ной эффективностью, что соответствует эффективности доксициклина, назначаемого дважды в день в течение 7 дней.
Азитромицин также является одним из препаратов выбора в терапии урогенитальных инфекционных заболеваний, ассоциированных с генитальными микоплазмами. По материалам публикаций, около 40 % воспалительных заболеваний мочеполовых органов ассоциированы с микоплазмами, три из которых (Ureaplasma urealyticum, Mycoplasma hominis, Mycoplasma genitalium) считаются возбудителями урогенитальных инфекций. Известно, что человек является хозяином 16 видов микоплазм, причем 6 выделяют в урогенитальном тракте: M. hominis, U. urealyticum, M. primatum, M. genitalium, M. spermatophilum и M. penetrans.
Результаты изучения этиологического спектра негонококковых уретритов свидетельствуют о том, что выявление M. genitalium и U. urealyticum является независимым фактором риска развития их хронических форм (Horner P.J., 2003). Что касается острого негонококкового уретрита, то из всех микоплазм только M. genitalium ассоциирована с этим заболеванием, в то время как U. urealyticum ответственна за рецидивирование уретритов после проведенного лечения.
Одним из самых распространенных заболеваний мочеполового тракта на сегодняшний день остается урогенитальный трихомониаз, который занимает ведущее место в структуре ИППП. В мире им страдают около 170 млн человек. Это широкораспространенное паразитарное заболевание, вызываемое Trichomonas vaginalis, одинаково часто поражает как мужчин, так и женщин.
По оценке CDC, 5 % клинических изолятов T. vaginalis показали некоторую степень устойчивости к метронидазолу и тинидазолу, что заставило исследователей заняться поиском альтернативных препаратов для лечения урогенитального трихомониаза. Одним из них является секнидазол с таким же спектром активности, как и другие нитроимидазолы, но, по мнению Videau D. и соавт. (1978), более предпочтителен ввиду длительного поддержания в крови активных концентраций, т. к. его период полувыведения составляет 19 часов (у тинидазола – 12 часов, у орнидазола – 14). По сравнению с метронидазолом секнидазол менее токсичен и лучше переносится пациентами.
Секнидазол широко применяется и в терапии бактериального вагиноза – общего инфекционного невоспалительного синдрома полимикробной этиологии, связанного с дисбиозом влагалищного биотопа, который характеризуется резким увеличением облигатных и факультативных анаэробных условно-патогенных микроорганизмов и снижением или полным исчезновением лактобактерий, особенно перекисьпродуцирующих. Активность секнидазола в отношении анаэробов дает возможность использовать его в лечении этого заболевания.
Наряду с бактериальным вагинозом в клинической практике специалисты нередко сталкиваются с другой причиной вагинальных выделений – урогенитальным кандидозом – инфекционным поражением слизистой оболочки вульвы и влагалища, вызываемым дрожжеподобными грибами рода Candida. Как в России, так и во многих других странах кандидоз занимает одно из ведущих мест в структуре акушерско-гинекологической заболеваемости и является одной из наиболее частых причин обращения женщин за медицинской помощью. Частота кандидозного вульвовагинита за последние 10 лет почти удвоилась и составляет 30–45 % среди инфекционных поражений вульвы и влагалища.
В настоящее время препаратом выбора при лечении кандидаинфекции является флуконазол. Его основным преимуществом перед другими препаратами, применяемыми в терапии урогенитального кандидоза, является отсутствие влияния на гормональный профиль макроорганизма, что значительно снижает частоту побочных реакций. Биодоступность флуконазола достигает 94 %, а длительный период полувыведения (30 часов) позволяет использовать однократный прием препарата при кандидозном вульвовагините. По данным Страчунского Л.С. и соавт. (2000), клинический эффект при длительном наблюдении сохранялся после применения флуконазола у 93 % пациентов, при неэффективности предыдущей терапии – у 98 %, при рецидивирующем кандидозном вульвовагините – у 95 %; в случае терапии заболевания клотримазолом эти показатели составили 84, 85 и 85 % соответственно.
Таким образом, за последние десятилетия возросло количество научных исследований, посвященных диагностике и лечению урогенитальных инфекций, появились новые данные о лекарственных средствах и схемах их применения при ИППП и нарушениях микробиоценоза влагалища (бактериальном вагинозе, кандидозном вульвовагините), что привело к необходимости оптимизации подходов к назначению тех или иных препаратов. Всемирная организация здравоохранения определила ряд критериев, которым должны соответствовать лекарственные средства, используемые при лечении ИППП:
- эффективность не менее 95 %;
- малая токсичность и хорошая переносимость;
- возможность однократного применения;
- пероральный прием;
- возможность назначения во время беременности;
- медленное развитие резистентности микроорганизмов к проводимой терапии;
- обеспечение высокой комплаентности;
- доступная цена.
В настоящее время на фармацевтическом рынке появился уникальный препарат, соответствующий вышеперечисленным критериям, – Сафоцид (содержит в одной блистерной упаковке одну таблетку азитромицина 1 г, две – секнидазола по 1 г и одну – флуконазола 150 мг), удобный для терапии микст-инфекций урогенитальной системы.
Показаниями к назначению Сафоцида являются ИППП (гонорея, трихомониаз, хламидиоз) и неспецифические урогенитальные заболевания (бактериальный вагиноз, в т. ч. в ассоциации с генитальными микоплазмами; урогенитальный кандидоз).
В 2007 г. в ГУ “Центральный научно-исследовательский кожно-венерологический институт” Росздрава проведено исследование, целью которого стало изучение эффективности, безопасности и переносимости препарата Сафоцид, применяемого однократно у больных ИППП (гонорея, урогенитальный трихомониаз, хламидиоз) и неспецифическими урогенитальными инфекционными заболеваниями (бактериальный вагиноз; урогенитальный кандидоз; заболевания урогенитальной системы, ассоциированные с генитальными микоплазмами).
В исследование были включены 40 пациентов обоего пола, разделенные на четыре группы:
- 1-я – 5 пациентов с гонореей в сочетании с другими ИППП и/или вышеуказанными неспецифическими урогенитальными заболеваниями;
- 2-я – 5 пациентов с урогенитальным трихомониазом в сочетании с другими ИППП и/или неспецифическими урогенитальными заболеваниями;
- 3-я – 15 пациентов с хламидиозом в сочетании с другими ИППП и/или неспецифическими урогенитальными заболеваниями;
- 4-я – 15 пациентов с неспецифическими урогенитальными заболеваниями в различных сочетаниях.
Перед включением пациентов в исследование выполнялись следующие процедуры: сбор анамнеза (демографические данные, сведения о сопутствующих заболеваниях и сопутствующей терапии), оценка витальных показателей (частота сердечных сокращений, артериальное давление, температура тела), физикальное обследование (наружный осмотр аногенитальной области, бимануальное гинекологическое исследование, обследование с помощью гинекологического зеркала Куско), тест на беременность, получение клинического материала для лабораторного исследования. Последнее включало: проведение аминотеста и рН-метрию влагалищного экссудата; микроскопическое исследование клинического материала из уретры, боковых и заднего сводов влагалища, цервикального канала и прямой кишки (U, C, R, V); культуральное исследование на N. gonorrhoeae, T. vaginalis, генитальные микоплазмы (M. hominis, U. urealyticum) с их количественным определением; бактериологическое исследование состава вагинального микробиоценоза (аэробные, анаэробные микроорганизмы, грибы Candida); определение чувствительности условно-патогенных микроорганизмов к антибактериальным препаратам; культуральное и/или ПИФ и/или ПЦР исследование на C. trachomatis; ПЦР исследование на M. genitalium; серологическое исследование на сифилис и ВИЧ; клинический анализ крови и мочи; биохимическое исследование крови.
На момент обращения за медицинской помощью длительность заболевания у пациентов составляла от трех дней до месяца.
Основными субъективными проявлениями урогенитальных инфекций были: патологические выделения из половых путей – в 26 (65,0 %) случаях, дизурия – в 18 (45,0 %), диспареуния – в 28 (70,0 %), зуд и/или жжение в области наружных половых органов – в 19 (47,5 %).
При физикальном обследовании клинические признаки уретрита (гиперемия, отек слизистой наружного отверстия уретры, патологические уретральные выделения) выявлены в 15 (37,5 %), вульвовагинита (гиперемия, отек слизистой вульвы и/или влагалища, патологические вагинальные выделения) – в 10 (25,0 %), цервицита (гиперемия, отек, рыхлость слизистой экто- и/или эндоцервикса, патологические выделения из цервикального канала) – в 15 (37,5 %), цистита (дизурические явления, лейкоцитурия) – в 8 (20,0 %) случаях.
У 18 (45,0 %) пациенток 3-й и 4-й групп при проведении аминотеста получены положительные результаты; значение рН вагинального экссудата превышало 4,5.
По результатам лабораторного исследования у пациентов 1-й группы диагностирована гонорея в двух наблюдениях в виде моноинфекции, в одном – в ассоциации с C. trachomatis, в двух – в ассоциации с условно-патогенными микроорганизмами (G. vaginalis, генитальные микоплазмы). У пациентов 2-й группы диагностирован урогенитальный трихомониаз в трех наблюдениях в виде моноинфекции, в двух – в ассоциации с условно-патогенными микроорганизмами (генитальные микоплазмы). У пациентов 3-й группы хламидиоз нижних отделов мочеполового тракта в виде моноинфекции наблюдался в 5 случаях, а его сочетание с условно-патогенными микроорганизмами G. vaginalis, Candida, генитальные микоплазмы) – в 10 наблюдениях. У пациентов 4-й группы урогенитальные инфекции были вызваны условно-патогенными микроорганизмами в различных ассоциациях (G. vaginalis, Candida, генитальные микоплазмы в титрах более 104 КОЕ/мл).
Все включенные в исследование пациенты получали терапию препаратом Сафоцид, назначенным однократно перорально (все 4 таблетки, входящие в блистер) за час до или через 2 часа после еды.
Через 7–10 дней после назначения терапии пациентам 1-й и 2-й групп и через 28 дней – пациентам 3-й и 4-й групп произведена оценка эффективности и безопасности Сафоцида. При этом осуществлялось физикальное обследование, в т. ч. исследование органов малого таза и определение признаков/симптомов по совокупности показателей (табл. 1); оценка витальных показателей; запись любых неблагоприятных явлений с момента последнего визита. Лабораторные исследования включали: микроскопическое исследование (U, C, V, R), культуральное исследование показателей вагинального микроценоза (аэробные и анаэробные микроорганизмы), культуральное исследование на N. gonorrhoeae (в 1-й группе), культуральное исследование на T. vaginalis (во 2-й группе), культуральное и/или ПИФ и/или ПЦР исследование на C. trachomatis (в 3-й группе), культуральное исследование на M. hominis и U. urealyticum (в 4-й группе). Во время контрольного визита дополнительно проводились клинические исследования крови и мочи, биохимическое исследование крови.
Как свидетельствуют представленные в табл. 1 данные, клиническая эффективность терапии достигнута в 80 % наблюдений у пациентов 1-й и 2-й и в 93,3 % – 3-й и
4-й групп. Субъективные симптомы в виде диспареунии у двух пациентов 1-й и 2-й групп расценены как остаточные явления перенесенного воспалительного процесса, т. к. при повторном обследовании через неделю после 2-го визита пациенты не предъявляли жалоб со стороны урогенитальной системы. У одной пациентки 4-й группы при контрольном обследовании выявлены клинические признаки бактериального вагиноза, аналогичные таковым до назначения терапии.
При оценке витальных показателей ни в одном из наблюдений не отмечено отклонений от нормы.
Микробиологическая эффективность проведенной терапии оценивалась через две–четыре недели после приема Сафоцида (в зависимости от этиологического агента). Результаты лабораторных исследований представлены в табл. 2.
Согласно полученным данным, эрадикация возбудителей ИППП (N. gonorrhoeae, T. vaginalis, С. trachomatis) достигнута в 100 % случаев. Во время 2-го визита ни у кого из пациентов 1-й и 2-й групп не наблюдалось отклонений от нормы при микроскопическом и микробиологическом исследованиях. У одной пациентки 3-й группы выявлен лейкоцитоз при микроскопическом исследовании цервикального секрета, что, возможно, связано с наличием у нее эрозии шейки матки. У 13 (86,7 %) пациентов 4-й группы достигнута эрадикация условно-патогенных микроорганизмов, в остальных наблюдениях отмечено снижение титров последних менее 103 КОЕ/мл. У одной пациентки во время 2-го визита отмечены клинические признаки бактериального вагиноза (положительный аминотест, рН > 4,5, “ключевые клетки”).
Следовательно, терапия препаратом Сафоцид позволила достичь эрадикации патогенных возбудителей в 100 %, а условно-патогенных – в 86,7 % наблюдений.
При анализе показателей клинических анализов крови и мочи во время 2-го визита выраженных отклонений от нормы не выявлено. В 2 (5,0 %) случаях отмечено повышение активности печеночных ферментов (АЛТ, АСТ) не более 100 % по сравнению с нормальным исходным уровнем. В остальных наблюдениях клинически значимых изменений биохимических параметров крови не зафиксировано.
Таким образом, по итогам проведенного исследования, Сафоцид продемонстрировал высокую эффективность в терапии урогенитальных инфекционных заболеваний, ассоциированных с патогенными и условно-патогенными микроорганизмами. Клиническая эффективность препарата составила 93,3–100,0 %, микробиологическая – 86,7–100,0 %. Полученные данные дают возможность рекомендовать Сафоцид для терапии урогенитальных инфекций как средство, характеризующееся высокой эффективностью, низкой частотой развития побочных эффектов и удобством применения, а также обеспечивающее высокую комплаентность.
В заключение необходимо еще раз подчеркнуть недопустимость самолечения ИППП, т. к. в подавляющем большинстве случаев только врач может правильно диагностировать заболевание и назначить адекватный курс терапии с учетом индивидуальных особенностей конкретного пациента. При самолечении нередко развивается резистентность возбудителей к тем или иным препаратам, что в дальнейшем ведет к необходимости назначения более длительных курсов терапии.

Анализ на сифилис, экспресс-методы определения заболевания
Если у вас есть малейшее подозрение на заражение сифилисом, вам надо срочно сдать анализы крови на сифилис. Одним из методов обследования пациента на сифилис является экспресс-диагностика на венерические заболевания (инфекции, передающиеся половым путем). Такой анализ можно сделать у нас в клинике в течении 20 минут.
Главное — необходимо понимать, чем скорее будет поставлен диагноз, тем больший процент вероятности вылечиться без серьезных осложнений на внутренние органы и системы.
Подготовка к сдаче анализа на сифилис
Для того, чтобы анализы на сифилис были более точными, к ним следует подготовиться. Для получения точных результатов анализов крайне важно строгое соблюдение пациентами правил подготовки к лабораторным исследованиям.
Требования для сдачи анализа на сифилис.
Требования для сдачи анализа совсем несложные. Кровь для исследования на сифилис берут натощак. Натощак — это через 12 часов после последнего приема пищи, лучше утром. В крайнем случае – не ранее, чем через четыре часа после еды. Можно пить воду. Накануне забора крови пациенту не следует употреблять алкоголь, наркотические и медикаментозные препараты, принимать жирную пищу. При взятии крови в более ранние сроки после приема пищи, в особенности жирной, а также после употребления алкоголя, могут выпадать неспецифические ложноположительные результаты.
Чтобы не получить ложноположительные результаты (ЛПР), не рекомендуется сдавать анализ во время лихорадочных состояний или непосредственно после перенесенных инфекционных заболеваний.
По тем же причинам не следует брать кровь у женщин — во время менструации, у беременных — в последние две недели перед родами и в ближайшие 10 дней после родов, у новорожденных — в первые 10 дней жизни. Нельзя брать кровь у больных с повышенной температурой, у пациентов ранее 24 часов с момента употребления ими спиртных напитков. Кровь не следует сдавать после рентгенографии, ректального исследования или физиотерапевтических процедур.
Венозная кровь – лучший материал для лабораторных исследований. Кровь для анализа берется из вены, в количестве 5-10 мл. Техника получения венозной крови из локтевой вены не отличается от стандарта взятия крови для других исследований в клинико-диагностической лаборатории.
Методы исследования сыворотки и плазмы крови на сифилис
Один из методов определения заболевания – серологические исследования. Они основаны на выявлении в сыворотке (плазме) крови антител, образующихся в организме больного при заражении сифилитической инфекцией. Такие исследования делят на нетрепонемные и трепонемные. При подозрении на наличие сифилиса серологические реакции являются обязательным компонентом обследования пациентов.
Привычный всем анализ на RW (реакция Вассермана) относится к нетрепонемным тестам. Современные интерпретации этого метода - RPR (быстрый плазмореагиновый тест) и VDRL (определение антител к кардиолипиновому антигену).
Экспресс-анализ на сифилис (это нетрепонемный анализ) не дает точного ответа на вопрос о наличии заболевания сифилиса у пациента. Суть метода состоит в следующем: проводится тест на преципитацию или осаждение с кардиолипиновым агентом. Результат экспресс-анализа на сифилис будет готов спустя 20 минут после забора крови. Если тест показывает положительный результат, то это следует рассматривать как причину для проведения более углубленных исследований (ИФА, РПГА,РИФ,антитела IgM и IgG).
Трепонемный анализ на сифилис представляет собой специфический тест, который выявляет только антитела к возбудителю сифилиса. Один существенный недостаток этого метода – антитела остаются в крови человека и после благополучного лечения, в течение всей оставшейся жизни.
Ложноположительные анализы крови возможны при ревматоидном артрите, ревматизме, туберкулезе, мононуклеозе, у беременных, у пожилых старше 60 лет, у людей с онкологическими, эндокринными, язвой желудка и т.д
Результаты диагностики оценивает врач-венеролог. Окончательный диагноз ставиться только врачом при положительных углубленных анализах .
Экспресс анализ на сифилис – доступная стоимость и быстрый результат.

Стоимость анализа на сифилис зависит от того, какой именно анализ вы хотите провести. Экспресс-анализ, проводимый в нашей клинике, имеет стоимость 1000р. Эта процедура является быстрой и эффективной, поэтому при малейшем подозрении (незащищенный секс, случайная половая связь, изнасилование, наличие подозрительных высыпаний) такой анализ сдать необходимо.
Анализ на сифилис после лечения необходим для оценки эффективности терапии.
После окончания лечения сифилиса, пациент еще некоторое время остается под наблюдением венеролога.
Такое наблюдение называется клинико-серологическим контролем.

Длительность наблюдения составляет:
- a) После превентивного лечения сифилиса – полгода;
- b) После лечения первичного серопозитивного и вторичного сифилиса – три года;
- c) После лечения третичного сифилиса – пять лет.
Наблюдение включает в себя осмотры специалистов и регулярные анализы крови.
Какой анализ сдавать после лечения сифилиса?
Основным анализом для контроля лечения сифилиса, является антикардиолипиновый тест, или RPR.
Кроме него может использоваться микрореакция преципитации.
Этот анализ очень похож на RPR и также относится к нетрепонемным тестам.
При постановке антикардиолипиновых тестов к сыворотке крови добавляют кардиолипиновый антиген.
При наличии иммуноглобулинов IgM в сыворотке образуется темный осадок из комплекса антиген-антитело.

Важно! Классическая реакция Вассермана, RW, считается устаревшей и не применяется.
Под этим термином обычно подразумевают антикардиолипиновый RPR-тест.
RPR определяет присутствие в крови антител к липоидным веществами, входящим в состав бледной трепонемы.
Благодаря этому RPR является наиболее надежным способом контроля успешности терапии заболевания.
При снижении количества бактерий в крови, снижается и уровень определяемых антител.
Если титр RPR снизился в 4 раза или больше, терапия считается эффективной.
Анализ сдается до тех пор, пока RPR не станет отрицательной.
Окончательным критерием является два отрицательных теста RPR подряд в течение полугода.
Для исследования используется венозная кровь.
Чтобы анализ дал верные результаты, необходимо соблюдать правила подготовки:
- Анализ сдают утром и строго натощак;
- Накануне следует исключить из рациона алкоголь и жирную пищу;
- Полчаса до анализа не следует курить.
Важно! Результаты анализа могут зависеть от наличия других заболеваний.
Перед выполнением анализа необходимо предупредить врача о состоянии своего здоровья и принимаемых медикаментах.
Самым распространенным венерическим заболеванием является сифилис.
Заражение в подавляющем большинстве случаев происходит при половом контакте (вагинальном, оральном, анальном).
Реже контактно-бытовым путем и при переливании крови.
Возбудитель инфекции также передается внутриутробно через плаценту матери плоду.
Инкубационный период трепонемы составляет 20-30 дней от момента заражения.
Первым симптомом заболевания является возникновение на слизистой половых органов специфического язвенно-эрозивного образования – твердого шанкра.
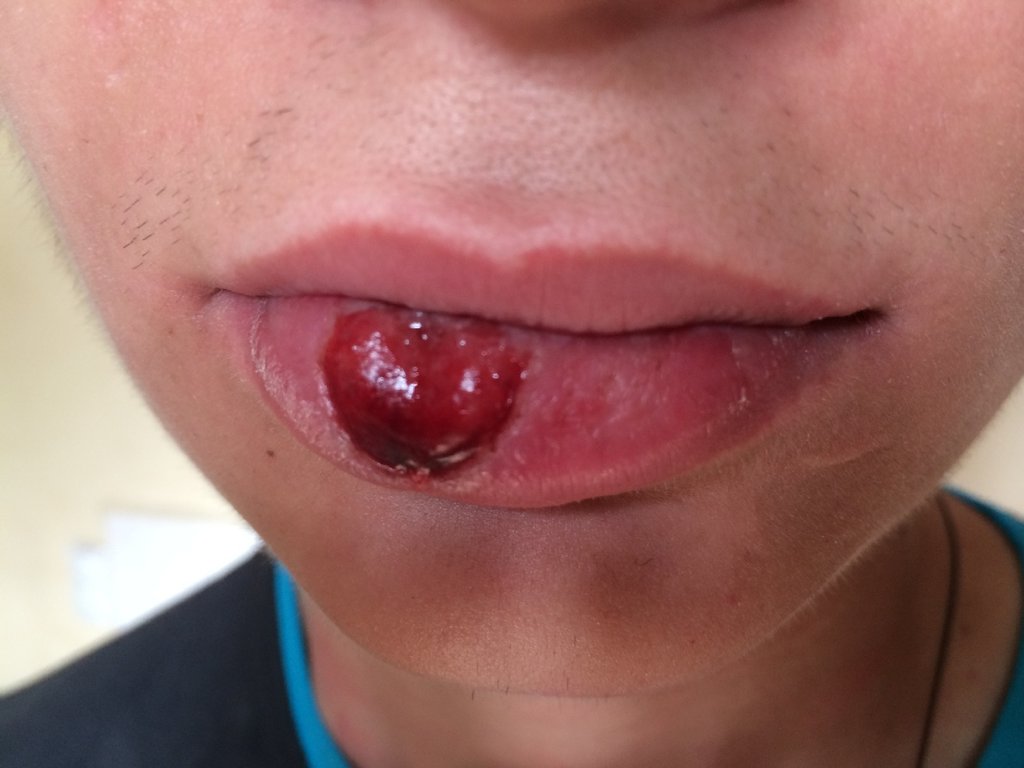
Этот патологический элемент всегда локализуется в месте проникновения в организм возбудителя.
Т.е. в области инфекционных ворот.
Твердый шанкр выглядит в виде небольшой округлой язвы синевато-красного цвета с гладким блестящим дном и неровными краями.
Образование безболезненное и плотное на ощупь, не чешется и не вызывает у больного никакого дискомфорта.
Паховые при локализации язвы на гениталиях, шейные и подчелюстные при оральном заражении.
Через некоторое время шанкр самопроизвольно, без применения каких-либо лечебных мер исчезает.
Через 1,5-2 месяца наступает вторичный период болезни, он знаменуется появлением на теле больных сифилитической сыпи в виде папул красного цвета.
При этом сыпь не чешется и не болит.
При отсутствии лечения во вторичном периоде происходит поражение внутренних органов и систем.
При длительном персистирующем течении инфекции эти изменения тяжелые и необратимые.
Сифилис: особенности диагностики
Диагностика сифилиса осуществляется венерологом.
На основании клинической картины болезни, данных визуального осмотра больного, лабораторных исследований соскобов с сифилитических высыпаний, урогенитального соскоба, крови и т.д.
Основополагающим методом лабораторной диагностики сифилиса является иммунологическое исследование.
Серологические тесты на сифилис делят не специфические и неспецифические.
Неспецифические тесты позволяют выявлять в крови больных антитела к бледной трепонеме.
Следует отметить, что антитела к возбудителю сифилиса обнаруживают, в том числе, в организме уже переболевших в прошлом людей – следы сифилиса в их крови остаются на всю жизнь.
Этот факт всегда учитывается при исследованиях, которые дают ложноположительные результаты.
Несмотря на доступность, а главное – эффективность антибиотиков, полностью уничтожить сифилис не удается.

О том как обнаруживается
след сифилиса в крови
рассказывает подполковник
медицинской службы, врач
Ленкин Сергей Геннадьевич
Содержание данной статьи проверено и подтверждено на соответствие медицинским
стандартам врачем дерматовенерологом, урологом, к.м.н.
Ленкиным Сергеем Геннадьевичем
| Наименование | Срок | Цена |
|---|---|---|
| Прием венеролога | 900.00 руб. | |
| Микрореакция на сифилис качественно (RPR) | 1 д. | 500.00 руб. |
Возможно ли убрать следы сифилиса
Иногда люди, перенесшие инфекцию в прошлом, интересуются, как убрать следы сифилиса из крови.
Однако это сделать невозможно: следы в виде антител останутся в организме на всю жизнь.
И будут выявляться во время анализов даже через много лет после переболевания сифилисом.
В тех случаях, когда анализ на сифилис дает положительный результат, для исключения сомнений и подтверждения диагноза прибегают к помощи специфических тестов.
Они позволяют определить наличие первичного инфицирования, стадию развития заболевания, интенсивность инфекционного процесса.
Это возможно благодаря определению класса обнаруженных иммуноглобулинов (A, M и G), а также их титра.
Для окончательной верификации диагноза может использоваться ПЦР-исследование.
Оно позволяет обнаружить в биологическом материале геном бледной трепонемы.
Лечение сифилиса осуществляют комплексно, главным образом, с помощью системной антибиотикотерапии.

При обнаружении сифилиса у пациента, медикаментозное лечение должно быть проведено у всех его половых партнером.
Во время курса лечения категорически запрещен прием алкоголя и половые отношения.
РПГА: след сифилиса
При помощи этого исследования проверяют количество возбудителя в сыворотки крови больного.
Таким образом проверяют кровь на следы сифилиса.
Данный метод является чувствительным и достаточно точным.
После того как было пройдено лечение, методика исследования может давать слабоположительный ответ.
Такой результат можно наблюдать на протяжении многих лет после выздоровления.
В качестве исключения, анализ методом РПГА, может давать отрицательный ответ при перенесенном заболевании.
Обычно это происходит в том случае, если проводилось своевременное лечение болезни на ранней стадии.
Важно! Реакция пассивной гемагглютинации не является информативной при исследованиях раннего или позднего сифилиса.
Данный метод не применяется в качестве оценки эффективности терапии.
Наличие антител можно обнаружить при наличии системных заболеваний, онкологии.
При ложноположительном ответе, результат может наблюдаться длительный период времени и после этого бесследно исчезать.
Чтобы поставить диагноз и определить остаточное количество спирохет, следует провести дополнительные лабораторные анализы.
Подтвердить следы сифилиса помогут дополнительные методы диагностики.
В этом случае, врач проведет дифференциальную диагностику, чтобы исключить возможность развития дополнительной инфекции.
Предупредить рецидив заболевания поможет обследование партнера на наличие возбудителя сифилиса.
РИБТ и РИФ: следы сифилиса
Реакция иммобилизации бледных трепонем и иммунофлюоресценции применяется для изучения крови человека на наличие сифилиса.
Этот вид теста считается трепонемным.
При помощи методик заболевание выявляется и на начальных стадиях развития.
Кроме этого, их применяют для исследования латентной формы болезни, когда признаки сифилиса не проявляются.
Как проводится исследование?
Данные методы анализа выполняются путем определения антител в крови человека.
Используется венозная кровь человека, в сыворотку добавляют специальные реагенты.
В результате выработки антител, происходит реакция, при которой бактерии склеиваются.
Исследование оценивается путем подсчета количества комплексов.
Следы сифилиса при диагностике РИБТ и РИФ методами можно определить на разных стадиях заболевания.
Иногда они дают слабоположительный ответ.
Если отмечается прогрессирование инфекции, количество антител будет возрастать.
Часто, врач назначает одновременно несколько диагностических исследований.
Это необходимо для точной диагностики и контроля лечения.
Иммуноблот: след сифилиса
Относительно новый вид исследования.
Считается одним из достоверных методов при выявлении бледной трепонемы.
При помощи иммуноблота, определятся уровень антител.
Иммунная система в ответ на наличие возбудителя начинает выделять антитела М и иммуноглобулин сифилиса G.
Позволяет выявить ответ иммунной системы организма на заболевание до и после прохождения лечения.
Метод не применяют в качестве контрольных анализов после лечения.
Иммуноблот – трепонемный тест, для использования этого метода анализа применяют специфические антигены возбудителя сифилиса.
Как интерпретируют результат?
Положительный результат дает две окрашенные полосы.
По их интенсивности судят о развитии болезни.
Четко окрашенные две полоски говорят о положительном результате.
Если полосы отсутствуют, результат можно интерпретировать как отрицательный.
В том случае если ответ получился слабоположительным, необходимо повторить исследование не ранее чем через неделю.
Возможно, что человек, в недавнем времени, переболел сифилисом.
Важно! Диагноз ставит врач венеролог. Не стоит делать самостоятельные выводы по результатам одного анализа.
Обычно рекомендуется сдать анализы на М антитела к другим белкам трепонемы.
Иммуноблот тест, при необходимости, позволяет определить антитела M и G отдельно друг от друга.
Если болезнь имеет скрытое течение, то обнаружить IgM невозможно.
IgG появляется к концу течения болезни, и сохраняется в организме длительный период времени.
Если антитела в крови больного появились повторно, это может свидетельствовать о рецидиве заболевания или не эффективности антибактериального лечения.
Особая подготовка для проведения анализа методом иммуноблот не требуется.
Забор крови должен осуществляться натощак.
Перед исследованием следует отменить прием алкогольных и табачных изделий.
Проводится анализ после отмены лекарственных препаратов.
Следы после сифилиса
Как правило, человек переболевший сифилисом, возвращается в нормальную повседневную жизнь.
Он продолжает жить как люди, которые никогда не болели сифилисом.
Но все же, есть определенные ограничения.
После того как больной выписан из стационара, следует посещать врача венеролога.
После успешно пройденного лечения определенный период времени пациент находится под наблюдением в кожно-венерологическом диспансере.
Человек считается здоровым, если было успешно пройден курс медикаментозной терапии.
Подтверждают выздоровление при помощи:
- Отрицательных серологических исследований
- Отсутствия повреждения слизистых и кожных покровов
- Рентгенологических исследований
Но, несмотря на это, остается след сифилиса в крови человека.
Почему тест на сифилис положительный после лечения?
Это является результатом того что кровь не очищается от антител, даже после выздоровления.
Такой результат называется ложноположительным, он может сопровождать человека на протяжении всей жизни.
Как убрать следы сифилиса из крови?
Чтобы очистить кровь, следует выяснить причину такой реакции.
Наличие положительной реакции может быть признаком сифилиса, которые не вылечен до конца.
На состояние крови влияют следующие факторы:
- 1. Недостаточная дозировка лекарственных препаратов
- 2. Прекращение приема препаратов самостоятельно, раньше указанного срока
- 3. Поздняя диагностика и терапия болезни
- 4. Не восприимчивость трепонемы к антибиотикам пенициллиновой группе
Если трепонема остается в организме в небольшом количестве после лечения, обычно она не способна размножаться.
При таком состоянии возбудителя в организме, он не способен наносить вреда.
Но не стоит игнорировать этот процесс.
При наличии малейших сомнений, проконсультируйтесь с врачом.
Возможно, ли заражение сифилисом при половом контакте, если остались следы сифилиса в крови?
Если произойдет контакт с больным человеком, возможно повторное заражение сифилисом.
Иммунитета к инфекции не формируется.
Обратите внимание! При обнаружении следов сифилиса в крови, следует обязательно выяснить причину и при необходимости повторить лечение.
После того как будет пройдено лечение, видимые признаки исчезают и человек может вернуться к полноценной жизни.
Для контроля приводится периодическое обследование.
У некоторых людей, которые переболели сифилисом, может отмечаться положительный результат.
Убрать следы трепонем из крови человека невозможно.
Иногда, иммуноглобулины исчезают сами.
Способ для очистки крови от остаточных антител не найден.
Когда уйдут следы сифилиса после лечения?
Процесс очищения может занять несколько лет, а в некоторых случаях и всю жизнь.
Для контроля состояния организма после лечения следует проводить не один, а несколько контрольных тестов.
Только комплексное исследование поможет определить состояние здоровья человека.
Для этого применяют специфические тесты.
Они позволяют определить класс иммуноглобулина.
Носителям чаще всего назначается исследование методом ПЦР, количественным способом.
Такое исследование поможет определить наличие или отсутствие ДНК трепонемы.
При необходимости получить консультацию по поводу сифилиса обращайтесь к автору этой статьи – венерологу в Москве с 15 летним опытом работы.
Читайте также:

