Анализ на вич при приеме лекарств
Обновлено: 25.04.2024
У каждого есть ВИЧ-статус, только у одних он положительный, а у других — отрицательный. Однако знать его необходимо, особенно в российских реалиях, когда в стране эпидемия, и уже более одного процента населения живет с вирусом.
Для диагностики вируса иммунодефицита человека существует несколько видов тестов, причем их классификация сложна лишь на первый взгляд, на самом деле она весьма логична. Главное — помнить, что, несмотря на высокую точность анализов, ни один тест не найдет вирус сразу после заражения.
Скрининговые (поисковые) тесты
Они помогают заподозрить инфекцию, но их результаты надо подтверждать другими анализами. Для скрининга используют тесты либо на антитела, либо на антигены/антитела.
ИФА (иммуноферментый анализ).
Этот метод служит не для обнаружения самого вируса, а антител, которые наша иммунная система вырабатывает для борьбы с ним.
Существует несколько поколений ИФА:
- В первом поколении тестов использовался сам вирус, обработанный ультразвуком, при этом определялись антитела только ВИЧ-1. Анализ обладал невысокой чувствительностью и специфичностью.
- ИФА второго поколения научили определять антитела как к ВИЧ-1, так и к ВИЧ-2. Материалом служили синтезированные белки, аналогичные настоящим антигенам вируса. Впрочем, тесты первого и второго поколения давно не используются.
- Следом появились тесты третьего поколения, которые позволяют диагностировать длительно текущую (хроническую) ВИЧ-инфекцию с чувствительностью и специфичностью около 100 %. Однако при острой ВИЧ-инфекции (когда антител мало или совсем нет) их точность считается недостаточной.
За счет своей простоты и дешевизны этот метод используется чаще всего, в том числе на его основе работают экспресс-тесты.
Подтверждающие тесты
Как следует из названия, они позволяют наверняка убедиться в наличии или отсутствии вируса иммунодефицита у человека. Их минус в сложности и дороговизне.
Иммуноблоттинг помогает проверить результаты скрининговых анализов и уточнить, каким видом вируса инфицирован человек: ВИЧ-1, ВИЧ-2 или обоими. Этот метод обладает высокой точностью, чувствительностью, но дорог и сложен в исполнении. Он является комбинацией ИФА и электрофореза, что позволяет определить антитела к специфическим антигенам ВИЧ-1 (gp160, gp120, gp41).
ПЦР (полимеразная цепная реакция). Тест способен находить генетический материал ВИЧ (ДНК/РНК), то есть проверяет, есть ли непосредственно вирус в крови. Нуклеиновые кислоты могут обнаруживаться уже на 7-й день после инфицирования (по данным CDC — c 10 по 33 день).
Кроме того, ПЦР бывает качественным и количественным. В последнем случае можно отслеживать вирусную нагрузку (концентрацию вируса в крови и других биологических жидкостях) у людей с ВИЧ, оценивая эффект терапии.
А я могу сдать сразу иммуноблот или ПЦР, чтобы узнать свой ВИЧ-статус?
Иммуноблот используют специальные лаборатории центров по борьбе со СПИДом. Пробы крови направляются туда для перепроверки уже положительных первичных скрининговых анализов. Сразу сдать его не получится, даже в платных клиниках.
ПЦР, наоборот, можно сдать в любой момент, но только обратившись в коммерческую лабораторию. В СПИД-центрах его делают также для перепроверки ранее положительного теста. Да, ПЦР позволяет максимально быстро (в течение 7—10 дней после инфицирования) обнаружить ВИЧ, но и у него есть недостатки:
- высокая стоимость;
- может обнаружить только ВИЧ-1;
- в редких случаях выявление низких уровней РНК ВИЧ (например,
Этот тест имеет смысл делать если:
- у человека есть подозрение на острую ВИЧ-инфекцию (высокий риск инфицирования) или в период серологического окна;
- донорам крови;
- новорожденным от ВИЧ-положительных матерей
Как тогда правильно проверяться на ВИЧ?
Нужно ли повторно тестироваться, если результат анализа отрицательный?
Универсальной рекомендации, увы, нет. Повторные тесты нужны чтобы застраховаться от попадания в период окна, когда в крови еще нет антител и антигенов ВИЧ, а вирус уже проник в организм.
То же самое и с частотой тестирования — она зависит от разных факторов: количества рисков, приема доконтактной (PrEP) и постконтактной (PEP) профилактики, нахождения в группах риска (инъекционные наркопотребители, секс-работники, мужчины, практикующие секс с мужчинами). Однако эксперты рекомендуют проверяться каждые 6—12 месяцев.
Что может влиять на результат теста на ВИЧ?
Анализ на ВИЧ может дать неправильные результаты в следующих случаях:
- при наличии системных аутоиммунных заболеваний (коллагенозов, васкулитов) и злокачественных опухолей;
- при тестировании в период серологического окна — когда в крови еще не появились антитела к ВИЧ;
- из-за ошибки при проведении теста в лаборатории;
- после вакцинации от гриппа.
У детей, рожденных от ВИЧ-положительных матерей, до восемнадцатимесячного возраста в крови могут сохраняться материнские антитела, что может приводить к ложноположительным результатам.
Кроме того, прием PrEP и PEP могут влиять на точность анализов, так как антиретровирусные препараты уменьшают количество вируса в крови и антител к нему.
В случае с PEP после окончания курса рекомендуется посоветоваться с врачом и подобрать оптимальные сроки проведения анализов. Первый тест обычно проводят через 4—6 недель после контакта с ВИЧ, затем через 3 месяца, при необходимости — через 6 месяцев.
Считается, что крайне важно сдать анализ на ВИЧ перед началом приема PrEP и затем проверяться каждые 3 месяца, уже находясь на PrEP.
На результаты теста не влияют прием пищи и алкоголя или курение. Специальной подготовки перед сдачей анализов на ВИЧ не требуется.
А что с экспресс-тестами?
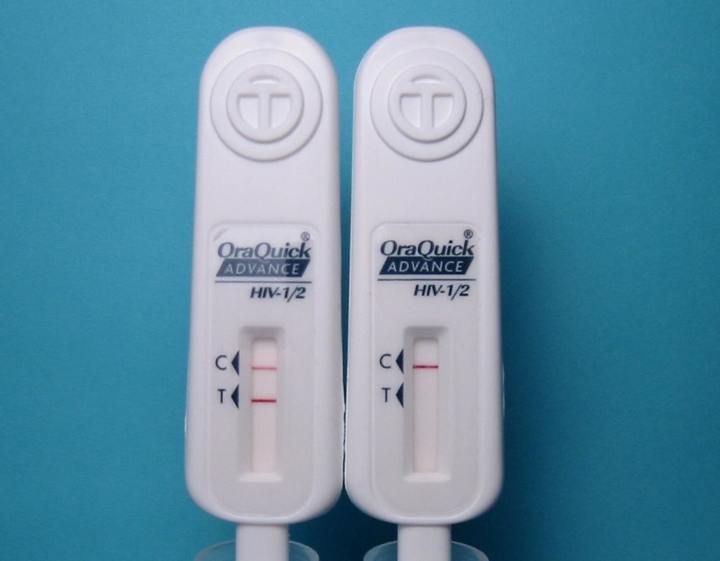
Они позволяют провериться на ВИЧ, не посещая лабораторию или поликлинику. По сути, это тесты ИФА третьего поколения, которые определяют антитела к ВИЧ-1 и ВИЧ-2 в слюне, моче или крови.
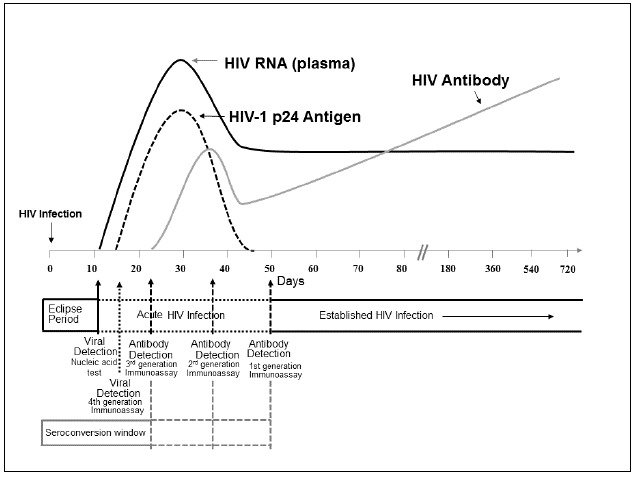
На рисунке показано, как быстро в крови появляются сам вирус (его генетический материал РНК) антитела и антигены, а также какие системы тестирования можно применить.
Точность большинства экспресс-тестов при хронической (длительно текущей) ВИЧ-инфекции достаточно высока (> 99 % чувствительности и специфичности), но все равно чуть ниже лабораторных анализов.
Сегодня среди них наиболее популярны тесты слюны (или околодесневой жидкости) и крови. Их можно либо купить самому, либо получить бесплатно в ВИЧ-сервисных организациях.
Важно помнить! Если такой тест оказался положительным, результат необходимо как можно быстрее перепроверить более точным методом.
Где я могу сделать тест на ВИЧ анонимно и бесплатно?
Анализ на ВИЧ бесплатный и анонимный, прикрепление к поликлинике и регистрация не требуются. После сдачи теста выдается идентификационный номер, по которому можно будет узнать результат.
На сервисе СпросиВрача доступна консультация детского врача аллерголога по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно. Задайте свой вопрос и получите ответ сразу же!

Здравствуйте нет ни что не даёт сбои в диагностике
Таи исследования на конкретно ВИЧ, ни как е другие патонкнытне помеха







Здравствуйте! Нет, стрептококк тут не при чем. Получите консультацию у врача-инфекциониста центра СПИДа.

Анастасия, если у Вас сомнения, сдайте анализы повторно в разных клиниках, чтобы была возможность сравнить, если и на этот раз будут сомнения, обязательно проконсультируйтесь с инфекционистом, приложив все результаты анализов. А стрептококк такой реакции дать не может. У него нет необходимых для этого антител.

Добрыы день. Анализ на антитела к ВИЧ подразумевает постановку 2х реакций- ИФА и иммуноблота. Иммуноблота строго специфичен, соответственно ложным практически не бывает. Стрептококк тут ни при чем, простуда тоже. Не нужно тратить время на бесконечные анализы, посетите СПИД центр и сдайте кровь на ПЦР. Вас так же нужно сдать кровь на антитела к ВИЧ. Здоровья Вам и супругу.
На сервисе СпросиВрача доступна консультация инфекциониста по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!

Здравствуйте.Не очень понятен вопрос.Связи ВИЧ-инфекции с ревматоидным артритом нет, если Вы об этом.
Яна, здравствуйте. Я просто хочу понять у меня +, а у него - мы никогда не предохранялись. Может быть такое.


Если вы на терапии - у вас должна быть низкая вирусная нагрузка.В этом случае партнёра заразить трудно.
Галина, просто хочу понять мы живём 4 года. Терапию я принимаю 2,6 года у меня+у него - такое может быть

Если Вы выполняете ВСЕ рекомендации врача и принимаете терапию, то Вы не передаёте вирус своему партнёру. Стоит Вам пропустить приём и вирусная нагрузка возрастёт.
Галина, я же говорю что мы с ним жили, 4 года я ещё не знала о виче узнала спустя 1,6 года. Я же это время не принимала терапию

Такое может быть, если у Вас была изначально небольшая вирусная нагрузка и Вы её, как узнали, постоянно снижали. Какой анализ он сдавал? Нужно сдать кровь методом ИФА 4 поколения.

Павел, я принимаю терапию 2,6 года до этого я не подозревала что у меня вич. Живём мы 4 года ведь небыло никакой терапии 1,6 года и мы никогда не предохранялись. Разве возможно не заболеть.

Вероятность заболевания определяется многими факторами, можно жить вместе и не заразить. Терапия назначается при выявлении вируса, ошибки быть не могло.

Здравствуйте! Мужчины заражаются значительно реже женщин ВИЧ инфекцией при половом контакте.
Такое может быть, что у Вас есть ВИЧ, а у мужа нет. Возможно также, что у него сейчас период инкубации.
Если у вас низкая вирусная нагрузка, то с секретом половых органов вирус практически не выделяется. Тем более, что при сексе с женщиной мужчины травмируются, чтобы были входные ворота для вируса, значительно реже.
Нина, до начала принятия терапии мы жили и не знали ни о каком вич. После того как я узнала о своём статусе он тоже не сдавал анализы и только сейчас спустя 2,6 года он здал у него отрицательный т. ЕСТЬ ЗА 4 ГОДА ОН НЕ ЗАРАЗИЛСЯ

Такое вполне может быть! Вам надо продолжать антиретровирусную терапию.
Если Вас что то смущает, сделайте повторное обследование крови на ВИЧ методом ИФА 4 поколения и методом ПЦР

Здравствуйте Олеся. Ревматоидный артрит и препараты, принимаемые для его лечения не влияют на анализы на ВИЧ.

Михаил, спасибо. Но все таки 4 года живём вместе. А когда узнала про вич очень много лечилась принимала антибиотиков. И до того как я начала принимать терапию мы жили не предохроняясь 1,6 года

Дело в том, что медицина это не математика. Здесь 2х2 может быть и 3 и 5 и в очень редких случаях 8.
Да, такие случаи как в Вашей семье встречаются. У меня лично есть знакомая пара, которая живет более 10-ти лет вместе, где у женщины ВИЧ, а мужчина здоров. Даже родили здорового ребенка.

Добрый день. К счастью, нередко встречаются дискордантные пары. Есть в моей практике пациенты, жены которых при отсутствии предохранения в течение 6 лет не заразились, причем на начальном этапе не было ВААРВТ. Вот это действительно редкость, поскольку женщине заразиться легче, нежели мужчине. Если у супруга нет воспалительных заболеваний половых органов, то риск заразиться снижается существенно. Проводилось ли Вам эпидрасследование? Или Вы уверены, что инфицировались до замужества? ВИЧ передается не только половым путем.
Наталья, я никогда не принимала норкотиков. Я просто много почитала в интернете и получает то что нас дезинформируют. Всё врачи говорят переспал 1 раз сдавай анализы пол года, а лучше больше. А тут 4 года не защищённого секса и ничего.

Я не о наркотиках. Заражение может происходить при использовании общей бритвы, маникюрных принадлежностей с потенциально инфицированным , при переливании крови. Почему дезинформируют? У меея много пауиентов, имевших лишь всего один подозрительный контакт. Чтобы произошло инфицирование , должны совпасть многие факторы- количество вируса в жидкостях и крови рафинированного, иммунитета самого контактного, интенсивность половых отношений и многое другое.
Наталья, вы как врач я как процент один вопрос и последний почему тогда нас дезинформируют и где искать ответ. Если за один раз можно а за 4 года может и нет
Наталья, я просто хочу понять теперь уже для себя. Врачи интернета пишут что один раз переспали и уже надо задуматься. Мы спали 1,6 года и ничего значит и не так заразно как сифилис например или грипп


Вы в то время на Вич сдавали кровь? Когда не предохранялись? Если Вы говорите с такой уверенностью, то Вы знали о своем ВИЧ статусе и не предохранялись? Мне кажется, нужно на данной площадке закрыть дискуссию. У Вас есть лечащий доктор, который отвечает на любые вопросы своих пациентов, по крайней мере должен.
Испытания лекарств от ВИЧ часто включает в себя аналитическое прерывание лечения, когда пациенты с ВИЧ прекращают прием антиретровирусной терапии (АРТ), чтобы ученые могли понаблюдать, как неконтролируемый вирус реагирует на исследуемые препараты.
Участие в такого рода клинических испытаниях может вызвать страх у человека с ВИЧ, который привык поддерживать неопределяемую вирусную нагрузку. Кроме того, предыдущее исследование, проведенное доктором Лау, показало, что многие люди с ВИЧ не были уверены в том, как работают эти испытания, и многие из них не были готовы к длительным периодам определяемой вирусной нагрузки.
Ученые работают над различными стратегиями излечения ВИЧ-инфекции. Некоторые методы нацелены на сокращение латентных резервуаров ВИЧ — инфицированных иммунных клеток, которые не производят новые вирионы в течение многих месяцев или лет. Другие виды терапии пытаются повысить способность иммунной системы контролировать вирус.
Существуют два типа исследований, основанных на прерывании лечения, которые используются для оценки потенциальной терапии: изучение времени до восстановления вирусной активности (TVR) и изучение контрольных точек. В исследованиях TVR после того, как участники прекращают АРТ, ученые измеряют время, необходимое, чтобы вирусная нагрузка сначала достигла обнаруживаемого уровня (50 копий/мл), а затем время, необходимое для достижения более высокого порога (часто 10 000 копий/мл), после чего участники возобновляют прием АРТ. Если тем, кто получает лечение, требуется больше времени для достижения этих пороговых значений по сравнению с контрольной группой, это указывает на то, что терапия замедляет восстановление вирусной активности. Исследования TVR часто используются для оценки методов терапии, нацеленной на резервуары, обычно они длятся всего несколько недель.
Исследования контрольных точек демонстрируют, насколько эффективно иммунная система участников контролирует ВИЧ самостоятельно. В этих гораздо более длительных исследованиях (до нескольких месяцев) исследователи позволяют вирусным нагрузкам участников достигать высоких уровней, имитируя острую фазу ВИЧ, чтобы проследить, сможет ли их иммунная система в дальнейшем снизить эту нагрузку. Порог для возобновления АРТ обычно устанавливается на высоком уровне (часто 100 000 копий/мл). Когда участники, получающие лечение, способны контролировать ВИЧ при более низких уровнях вирусной нагрузки и в течение более длительного времени, чем участники контрольной группы, это говорит о том, что терапия повышает их иммунитет против вируса.
Несмотря на то, что нет конкретных рекомендаций, определяющих, как планировать исследования с прерыванием лечения, группа ученых, занимающихся исследованием ВИЧ, встретилась в 2018 году, чтобы обсудить этические стороны и выработать методы для снижения риска. Прекращение АРТ во время этих исследований не просто подвергает участников риску длительных периодов определяемой, а в некоторых случаях и высокой вирусной нагрузки. Более высокие вирусные нагрузки также могут подвергать опасности и ВИЧ-отрицательных половых партнеров участников.
До сих пор в большинстве исследований риск снижался за счет небольшого числа участников и отсутствия контрольной группы, которая вместо лечения принимала неактивное плацебо. Включение контрольной группы важно, потому что это позволяет ученым сравнивать тех, кто принимает лекарства, с теми, кто находится на плацебо. Тем не менее научное сообщество обсуждало этичность использования контрольных групп в подобных испытаниях лекарств, потому что они подвергаются длительным периодам повышенной вирусной нагрузки в отсутствие каких-либо препаратов, даже экспериментальных.
Исследование
Доктор Лау и ее коллеги использовали данные предыдущих клинических испытаний для создания математических моделей, позволяющих оценить, как различные их параметры влияют на статистическую мощность испытания.
Статистическая мощность аналогична чувствительности. Например, тест на ВИЧ с чувствительностью 80% успешно идентифицирует вирус у 80% людей, которые на самом деле ВИЧ-положительны, но не выявит у остальных 20% ВИЧ-положительных людей. Когда клиническое испытание, оценивающее лечебную терапию, должно достигнуть статистической мощности в 80% (при условии, что терапия имеет реальную пользу для тех, кто ее принимает), в испытании будет 80-процентная вероятность обнаружить пользу и 20-процентная вероятность ее упустить.
Проще говоря, чем больше данных задействовано в испытании, тем большей статистической мощностью оно будет обладать. Такие факторы, как количество участников, число контрольных параметров, продолжительность испытания и частота анализов крови, влияют на статистическую мощность испытания.
Результаты пробного моделирования TVR
В отношении недавнего исследования TVR с участием 13 человек такая модель показала, что при мощности 80% исследование выявило бы только лечение со значительным снижением реактивации (от 70 до 80%). Чтобы исследование TVR выявило снижение реактивации на 30%, потребуется уже по 120 участников в группе терапии и в контрольной группе. Поскольку в большинстве исследований TVR задействовано малое число участников, они, вероятно, не устанавливают умеренных результатов терапии.
Может показаться нелогичным планирование исследования для выявления меньшего эффекта от лечения, когда конечной целью является поиск максимальной пользы (т. е. терапия, приводящая к 100% снижению реактивации). Тем не менее на начальных этапах поиска лекарства необходимо фиксировать даже умеренные результаты, чтобы решить, требует ли этот метод дальнейшего изучения.
Помимо рекомендации увеличить количество участников, команда предлагает использовать ретроспективные контрольные данные в дополнение к контрольным группам. Данные из предыдущих испытаний, в которых люди прерывали АРТ, могли бы повысить потенциал выявления умеренной пользы от лечения. Они смоделировали гипотетическое исследование TVR, в которое вошли 50 участников и 50 человек из контрольной группы. При мощности 80% эта конструкция может обнаруживать снижение реактивации до 43%. Добавление ретроспективных данных еще 150 участников позволило бы в том же испытании выявить снижение до 36%.
Такое моделирование также не показало практически никакого улучшения способности обнаруживать снижение реактивации при увеличении продолжительности испытаний TVR свыше пяти недель. После этого срока модель предсказала улучшение обнаружения не более чем на 1%. Точно так же они не обнаружили практически никакой пользы от проведения лабораторного мониторинга чаще, чем раз в неделю. Наблюдение за людьми два раза в неделю почти не помогло обнаружить снижение реактивации.
Ученые провели отдельный анализ для оценки максимального риска передачи ВИЧ во время исследований TVR на основе предыдущих данных. Они оценили максимальный риск передачи, предполагая, что участники занимались незащищенным сексом и что доконтактная или другие методы профилактики не использовались. Кроме того, если во время еженедельного мониторинга не сообщать пациенту показатель вирусной нагрузки сразу же, то участник, которому необходимо возобновить АРТ (если его вирусная нагрузка превысила 1000), скорее всего, отложит это до следующего еженедельного визита.
Было подсчитано, что в этом случае во время пятинедельного исследования TVR с порогом вирусной нагрузки 1000 для повторного начала АРТ максимальный риск передачи ВИЧ составил 3,6 на 1000 участников, занимающихся вагинальным сексом. При анальном сексе для вводящих партнеров максимальный риск составлял около 7 на 1000, а для принимающих партнеров — около 70 из 1000. Изменение схемы исследования, включающее экспресс-тестирование на вирусную нагрузку и возобновление АРТ в тот же день, снижает предполагаемый максимальный риск до 0,9, 1,8 и 18 на 1000 соответственно.
Результаты моделирования исследования по контрольным величинам
Исследования контрольных точек должны иметь достаточную статистическую мощность, чтобы отделять преимущества предлагаемой лечебной терапии от контроля после лечения. Используя результаты исследования CHAMP, ученые предположили, что исходный уровень контроллеров после лечения ниже 4%. Если целью исследования было определить увеличение количества контролеров до 20% (это означает, что терапия помогла людям, которые не являются естественными контроллерами, подавить вирус), их модель показала, что 24-недельное исследование со статистической мощностью 80% потребует участия 60 пациентов.
Из-за чрезвычайно высоких вирусных нагрузок в типичных исследованиях контрольных величин (до 100 000) авторы сравнили, как использование более консервативного порогового значения (1000) для возобновления АРТ повлияет на способность этих исследований обнаруживать увеличение числа контроллеров после лечения. CHAMP показало, что у 55% контроллеров после лечения первоначальные всплески вирусной нагрузки не превышали 1000 копий/мл, и в дальнейшем они сохраняли вирусную нагрузку ниже этого порога.
Используя эти данные, Лау и Кромер предположили, что использование порога в 1000 копий маскирует 45% естественных контроллеров после лечения, что может помешать обнаружить, когда терапия усиливает иммунный контроль участников над ВИЧ. Чтобы восстановить статистическую мощность, потребуется больше участников. Как и в приведенном выше примере, при мощности 80% и цели выявления 20-процентного повышение числа контроллеров после лечения свыше базового уровня 4%, более низкий порог вирусной нагрузки потребует увеличить количество участников с 60 до 120 как в лечебных, так и контрольных группах.
Как и в случае исследований TVR, ученые также оценили максимальный риск передачи ВИЧ во время определения контрольных величин, используя те же предположения, что и описанные выше (отсутствие стратегий профилактики и экспресс-тестирования на вирусную нагрузку, незащищенный секс, недельная задержка перед возобновлением АРТ). Из-за гораздо большей продолжительности испытаний и высоких пороговых значений вирусной нагрузки (для этого они сослались на исследование контрольных величин, в котором использовали данные 50 000 человек) они оценили максимальный риск передачи ВИЧ как 13 случаев на 1000 при вагинальных половых контактах, около 25 на 1000 — для вводящего партнера при анальном сексе, 214 на 1000 — крайне высокий — для принимающего партнера при анальном сексе.
Предлагаемая гибридная схема испытаний
Основываясь на собственном моделировании и оценках максимального риска передачи, ученые предлагают использовать гибридную модель для анализа прерывания лечения. В озвученной ими схеме прерывания будут начинаться с пятинедельного исследования TVR. Хотя оно, как правило, применяется, когда терапия нацелена на резервуары ВИЧ, у людей, отвечающих на терапию, направленную на усиление иммунитета, также будет наблюдаться более медленное восстановление вируса (если лечение было эффективным).
Начало испытания для оценки потенциального лечения с помощью исследования TVR подвергнет участников гораздо более коротким перерывам в лечении, что позволит исследователям определить, имела ли эта терапия достаточную эффективность, чтобы перейти к более длительному изучению заданных значений. Если медики согласятся с необходимостью дальнейшего исследования, а пациенты с вирусной нагрузкой ниже 1000 согласятся перейти к следующей фазе, они продолжат тщательное наблюдение в течение 24 недель или до тех пор, пока вирусная нагрузка участников не превысит 1000 копий/мл, после чего они возобновят АРТ.
Ученые рекомендуют провести экспресс-тестирование на вирусную нагрузку и возобновить АРТ в тот же день, чтобы свести к минимуму риск передачи инфекции. По их оценке, ограничение контрольной точки теми, кто уже демонстрирует контроль за вирусом, до вирусной нагрузки ниже 1000, снижение порога вирусной нагрузки для возобновления АРТ до 1000, ограничение продолжительности до 24 недель, а также включение тестирования по месту оказания медицинской помощи и возобновление АРТ в тот же день снижают максимальный риск передачи до 0,2 на 1000 при вагинальном сексе, до 0,35 на 1000 — для вводящего партнера при анальном сексе и до 3,1 на 1000 — для принимающего партнера при анальном сексе. И это значительное улучшение показателей по сравнению с оценкой, полученной в ходе традиционных исследований контрольных величин.
Если первоначальное исследование TVR показывает, что лечение не требует дальнейшего изучения (например, если не обнаружено позитивного эффекта), то ученые смогут избежать затрат на проведение длительного исследования контрольных величин.
Выводы
Ученые пришли к выводу, что в испытаниях лекарств недостаточно участников для обеспечения знаковой статистической мощности при умеренных результатах лечения. Поскольку чаще всего при испытаниях терапии также не используются контрольные группы, количественная оценка пользы лечения чрезвычайно сложна. Специалисты рекомендуют сотрудничать всем заинтересованным структурам для создания ретроспективной контрольной базы данных, которая позволила бы разработать схему испытаний, не полностью полагающуюся на контрольные группы плацебо. Тем не менее они отмечают, что задействование ретроспективных контрольных данных означает включение людей, которые с большей вероятностью начали АРТ во время хронической ВИЧ-инфекции, и тех, кто использует более старые схемы АРТ, которые могут действовать как искажающие факторы.
Тем не менее сокращение числа участников, получающих плацебо, снижение пороговых значений вирусной нагрузки, продолжительности испытаний и рисков передачи ВИЧ могут побудить большее число людей с ВИЧ участвовать в исследованиях с прерыванием лечения.
Читайте также:

