Ангина после ротавирусной инфекции
Обновлено: 19.04.2024
В развитии инфекционного заболевания обычно выделяют четыре периода: латентный (инкубационный), продромальный, разгар болезни и исход. Латентный период продолжается от момента воздействия этиологического фактора до появления первых кли
В развитии инфекционного заболевания обычно выделяют четыре периода: латентный (инкубационный), продромальный, разгар болезни и исход. Латентный период продолжается от момента воздействия этиологического фактора до появления первых клинических признаков болезни. В этот период происходит мобилизация защитных сил организма, направленных на компенсацию возможных нарушений, на уничтожение болезнетворных агентов и удаление их из организма. Продромальный период представляет собой временной интервал от первых симптомов заболевания до полного проявления. Период выраженных проявлений заболевания характеризуется полным развитием клинической картины. При различных инфекционных заболеваниях может страдать нервная система ребенка, что клинически проявляется синдромом нейротоксикоза. Нейротоксикоз — ответная неспецифическая реакция детского организма на воздействие вирусной, бактериальной или вирусно-бактериальной флоры, характеризующаяся преимущественным поражением центральной (ЦНС) и вегетативной нервной системы. С истощением функциональных возможностей органов и систем в результате перенесенного заболевания, особенно нервной системы при ее перенапряжении, а также вследствие аутоинтоксикации или экзогенного токсикоза связывают возникновение астенического синдрома. Это наиболее частое клиническое проявление периода реконвалесценции. Утомление в течение длительного времени, которое не компенсируется полным восстановлением, вызывает синдром перегрузки, следом за которым развивается состояние истощения. Субъективно ощущаемое чувство утомления — прежде всего сигнал о перегрузке центральных регуляторных систем, неудовлетворительном состоянии энергетических ресурсов организма и аутоинтоксикации продуктами метаболизма. Длительное утомление, приводящее к истощению, по сути своей является результатом стрессорного воздействия на организм, вызывающего нарушение функций регуляторных систем — вегетативной, эндокринной и иммунной. Если стрессорные факторы действуют в течение длительного времени, может развиться реакция организма, при которой возможны функциональные изменения в виде вегетативной дисфункции [1, 6]. Синдром вегетативной дисфункции (СВД) включает в себя проявление всех форм нарушения вегетативной регуляции. Наряду с соматическими проявлениями: головокружением, головными болями, сердцебиением, одышкой, жаждой, булимией, рвотой после еды, непереносимостью отдельных видов пищи, субфебрилитетом неясного происхождения, кожными высыпаниями и др., у пациентов с СВД выявляют эмоциональные расстройства разной степени выраженности в виде тревожности, нарушения сна, беспричинного плача, а также расстройства поведения, в частности, импульсивности, повышенной двигательной активности и возбудимости, дефицита внимания, что клинически определяется как астеновегетативный или психовегетативный синдром [Вейн А. М., 1981].
Интерес и сложность проблемы астеновегетативного синдрома заключается в том, что она является комплексной: медицинской, психологической и педагогической. Однако все специалисты сходятся в том, что такое состояние существует, его необходимо диагностировать и правильно корректировать.
Задачи исследования
Данное исследование посвящено изучению динамики состояния вегетативной нервной системы детей с астеновегетативным синдромом после перенесенных инфекционных заболеваний, а также оценке эффективности препарата Тенотен детский при названной патологии.
Тенотен детский содержит сверхмалые дозы антител к мозгоспецифическому белку S-100, создан по особой технологии специально для детского возраста, оказывает успокаивающее, нормализующее настроение и поведение действие, а также выраженное вегетостабилизирующий эффект [3, 5].
Критерии включения больных в исследование:
Критерии исключения больных из исследования:
Наличие декомпенсированных заболеваний или острых состояний, которые могут влиять на проведение исследования.
Применение вегетотропных и ноотропных препаратов в период исследования и в последние две недели перед исследованием.
Участие в других клинических исследованиях в течение четырех недель перед включением в данное исследование.
Материал исследования
Для исследования методом случайной выборки дети были распределены в две группы. В основной группе (30 человек) дети в периоде реконвалесценции наряду с симптоматической витаминотерапией получали Тенотен детский по 1 таблетке 3 раза в день в течение 4 недель в сочетании со стандартной терапией. В контрольную группу (20 человек) вошли дети, получавшие стандартную витаминотерапию и симптоматическую терапию за исключением препаратов, обладающих вегетотропной активностью.
Достоверных различий по половозрастным показателям между основной и контрольной группами детей не было.
По спектру перенесенных заболеваний, их тяжести, характеру осложнений выделенные группы детей также значительно не отличались. Спектр заболеваний включал вирусные и вирусно-бактериальные инфекции дыхательных путей (этиологически подтвержденные формы гриппа и другие респираторные вирусные инфекции, тяжелые формы бронхитов и пневмоний и др.), острые средние отиты, тяжелые и осложненные формы инфекционного мононуклеоза, висцеральные формы ветряной оспы, протекающие с нейротоксикозом и везикулезными высыпаниями на внутренних органах. Данные о заболеваниях приведены в таблице.
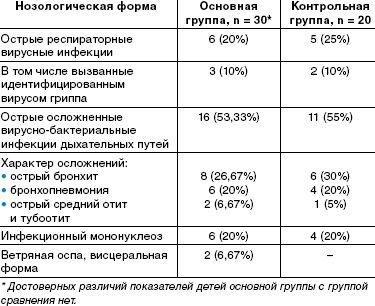
Диагностическое обследование включало в себя клиническую оценку проявлений вегетативной дисфункции, психологическое исследование, неврологическое обследование, электрокардиографию (ЭКГ).
Состояние вегетативной нервной системы определялось по исходному вегетативному тонусу, вегетативной реактивности и вегетативному обеспечению деятельности. Исходный вегетативный тонус, характеризующий направленность функционирования вегетативной нервной системы в состоянии покоя, оценивался по анализу субъективных жалоб и объективных параметров. Оценивалась степень выраженности психопатологических проявлений: утомляемость, тревожность, эмоциональная неустойчивость и др. (модифицированный опросник А. М. Вейна). Определялся внутрисистемный вегетативный тонус по индексу Кердо и межсистемный вегетативный тонус по коэффициенту Хильдебранта. Для оценки вегетативного обеспечения деятельности, отражающего в основном состояние автономной системы регуляции, проводилась клиноортостатическая проба (КОП). Функциональное состояние сердечно-сосудистой системы рассматривалось также на основании данных электрокардиографии.
Уровень внимания оценивался с использованием шкалы SNAP-IV, таблиц Шульте, по результатам модифицированного метода Пьерона–Рузерапо. Выявление расстройств кратковременной и долговременной памяти, косвенно отражающей выраженность астении, проводилось с помощью методики 10 слов и пиктограммы.
Для определения состояния эмоциональной сферы обследуемых (тревоги, депрессии) использовался ахроматический и цветовой тесты Люшера.
После окончания лечения всем детям было проведено повторное комплексное обследование для оценки эффективности терапии. Кроме того, родителям детей предлагалось оценить результаты лечения при помощи десятибалльной аналого-визуальной шкалы, где 0 — это очень плохая оценка, 10 — очень хорошая.
Результаты исследования
Перед началом исследования у всех обследуемых детей (без достоверных различий в обеих группах) с помощью опросника А. М. Вейна определялись умеренно выраженные психопатологические расстройства, в виде неустойчивости эмоционального фона (84%), повышенной тревожности (34%), утомляемости (38%), отвлекаемости (86%), нарушений сна (74%), снижения памяти, а также различные соматические проявления в виде периодических головных болей (52%), головокружения (24%), метеозависимости (12%), снижения аппетита (64%), диспептических нарушений в виде тошноты, рвоты, вздутия живота (44%).
Индекс Кердо позволил определить наличие внутрисистемной дистонии у детей, перенесших тяжелые инфекционные заболевания, он составил в среднем 32,89 ± 0,99 в обеих исследованных группах, что свидетельствовало о превалировании симпатических влияний на организм в покое.
Межсистемный вегетативный тонус, оцениваемый с помощью коэффициента Хильдебранта (средние значения составили 3,98 ± 0,03), имел, в основном, эйтонический характер.
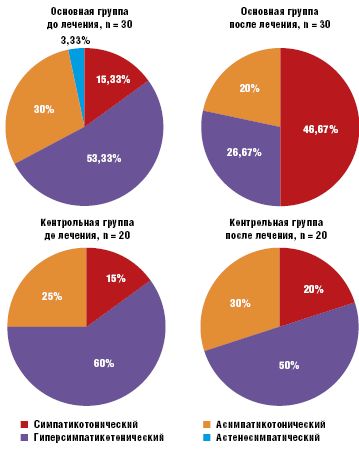
КОП, определяющая вегетативное обеспечение автономной системы регуляции, наряду с нормальным симпатикотоническим вариантом КОП, отражающим устойчивость гемодинамики в ортостазе (14% случаев), выявила и патологические варианты. Гиперсимпатикотонический вариант КОП, характеризующийся резким повышением систолического артериального давления (САД) и диастолического артериального давления (ДАД) и частоты сердечных сокращений (ЧСС) и обусловленный избыточным включением симпатико-адреналовой системы, встречался в преобладающем количестве случаев — у 58% детей. Асимпатикотонический вариант КОП, обусловленный недостаточным подключением симпатического отдела вегетативной нервной системы, при котором САД и ДАД не изменяются или падают, ЧСС остается нормальной или компенсаторно увеличивается, встречался у 28% детей с СВД. Астеносимпатический вариант КОП с падением САД и ДАД и резким увеличением ЧСС в первые минуты ортостаза, с последующей гиперсимпатикотонической реакцией был выявлен в 2% случаев.
Основными психопатологическими проявлениями СВД являлись невнимательность, гиперактивность, импульсивность. Их оценка производилась с помощью шкалы-опросника SNAP-IV (Swanson J., 1992). Показатель невнимательности в двух группах по этой шкале достоверно не отличался и составил в среднем 53,33% (норма (Swanson J., 1992) — 0,40–1,82), средний показатель гиперактивности — 1,96 ± 0,32 (норма (Swanson J., 1992) — 0,27–1,59) и импульсивности 2,13 ± 0,37 (норма (Swanson J., 1992) — 0,26–1,52) (p < 0,05 — достоверность различий по сравнению с возрастными нормами).
Выраженность астении косвенно отражается на интеллектуально-мнестических показателях, в частности на оперативной памяти: чем выше утомляемость ребенка в период после перенесенного инфекционного заболевания, тем больше страдает процесс запоминания. Оценка памяти у детей проводилась с помощью методики запоминания десяти слов. Регистрировались следующие показатели: 1) количество повторений, необходимых для воспроизведения 10 слов; 2) количество слов, воспроизведенных через 1 час.
В большинстве случаев обследуемым обеих групп (достоверных различий показателей детей основной группы с группой сравнения нет) для воспроизведения 10 слов требовалось 3 и более повторений, что свидетельствовало о снижении показателей механического запоминания. В то же время количество воспроизводимых слов через час после начала исследования значительно снизилось, что явилось признаком нарушения динамической памяти у детей с вегетативной дистонией.
В качестве методики для исследования опосредованного запоминания использовалась пиктограмма. Регистрировались следующие показатели: 1) количество воспроизведенных понятий; 2) динамика воспроизведенных понятий через 1 час.
Оценка результатов пиктограмм в целом показала, что у детей с СВД дистонией изображаемые образы часто не соответствовали реальным объектам, что впоследствии затрудняло их интерпретацию. Показатели по критерию адекватности (обоснованности связи между предложенным понятием и его пиктограммой) в среднем составили около 50%.
Проведенное по методике Люшера тестирование отразило статистически значимое отклонение преимущественно выбираемой обследуемыми цветовой гаммы от аутогенной нормы. В то же время величина вегетативного показателя не имела столь значимых различий по сравнению с возрастными нормами. Среднестатистические показатели тревожности и напряжения, определенные с помощью теста Люшера, также не имели значительных отклонений от стандартных показателей (p < 0,05 — достоверность различий по сравнению с возрастными нормами).
Таким образом, проведенное клиническое обследование детей, перенесших инфекционные заболевания, выявило наличие у них различной степени выраженности проявлений СВД. Безусловно, такие психовегетативные нарушения отражались на периоде реконвалесценции, ухудшали качество жизни и требовали их адекватной коррекции.
В качестве альтернативного препарата для коррекции проявлений СВД был использован Тенотен детский с успокаивающим и выраженным вегетостабилизирующим действием (Лобов М. А., 2008). Основная группа детей (30 человек) получала Тенотен в дозе 3 таблетки/сутки курсом 1 месяц в сочетании со стандартной витаминотерапией. Контрольная группа детей (20 человек) получала стандартную терапию с применением лекарственных средств, не обладающих психотропной и вегетотропной активностью. По окончании курса лечения были проведены повторные клинические исследования.
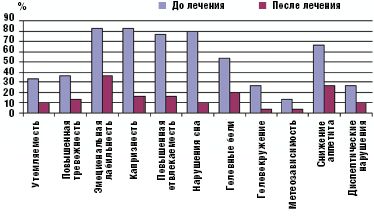
Прием препарата Тенотен детский в течение месяца обеспечил достоверное (в сравнении с контрольной группой) улучшение показателей психовегетативного статуса и снижение частоты соматоневрологических расстройств у детей, принимавших Тенотен детский, тогда как в контрольной группе детей эти показатели оставались практически на прежнем уровне (рис. 1, 2).
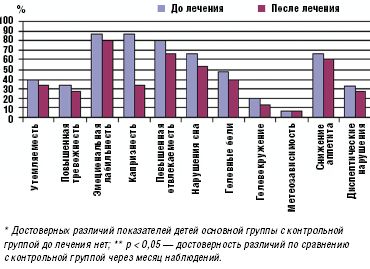
Улучшение показателей вегетативного тонуса отмечалось не только в его психоэмоциональной (утомляемость, тревожность, эмоциональная неустойчивость, отвлекаемость, нарушение сна), но и соматоневрологической (головные боли, головокружение, снижение аппетита, диспептические нарушения) составляющей. Полученные данные отражены на рис. 1.
Качественно изменились результаты КОП. У детей, принимавших Тенотен детский, отмечалась нормализация показателей вегетативного обеспечения (симпатикотонический вариант КОП) с 15,33% детей в начале терапии до 46,67% (p < 0,05), у остальных наметилась четкая тенденция к улучшению. В контрольной группе показатели КОП остались практически на прежнем уровне. Данные отражены на рис. 3.
Была выявлена положительная динамика в отношении патопсихологических проявлений. После курсового применения препарата уменьшение выраженности мнестических и поведенческих симптомов (невнимательность, гиперактивность, импульсивность) отмечалось в среднем у 85% детей. Все показатели шкалы SNAP-IV у детей основной группы после лечения Тенотеном достоверно снизились (p < 0,05). Показатели гиперактивности и невнимательности снизились до нормальных значений, абсолютные показатели импульсивности также значительно уменьшились в наблюдаемой группе.
По данным психометрического исследования у пациентов с СВД основной группы были выявлены достоверные положительные изменения при проведении тестов на память и внимание в сравнении с контрольной группой. Данные тестирования выявили отчетливое улучшение показателей механической и динамической памяти у 30% детей (p < 0,05), а также опосредованной памяти в тестах с пиктограммой — повышение показателя адекватности до 75% (p < 0,05).
Динамическая оценка результатов цветового теста Люшера выявила относительную стабилизацию психоэмоционального состояния у детей основной группы, что отразилось на предпочитаемой цветовой гамме и приближении ее к аутогенной норме (по коэффициенту суммарного отклонения от аутогенной нормы — p < 0,05). У детей контрольной группы определяемые показатели не имели статистически значимых изменений.
По окончании исследования родители оценили результаты лечения при помощи десятибалльной аналого-визуальной шкалы. В среднем успешность лечения в основной группе была оценена на 7–8 баллов, в контрольной — на 4–5 баллов.
Выводы
Проведенное исследование показало, что у детей, перенесших инфекционные заболевания, имеются в различной степени выраженные симптомы астеновегетативного синдрома (СВД) в виде психоэмоциональных (утомляемость, тревожность, эмоциональная неустойчивость, отвлекаемость, нарушение сна) и соматоневрологических (головные боли, головокружение, снижение аппетита, диспепсия) нарушений.
Астеновегетативные нарушения отрицательно влияют на процесс реконвалесценции у детей после перенесенных тяжелых инфекционных заболеваний, удлиняя этот период и ухудшая качество жизни пациентов.
Применение препарата Тенотен детский после перенесенных инфекционных заболеваний в дозе 1 таблетка 3 раза в день приводит к нормализации показателей вегетативного тонуса и обеспечения, уменьшает частоту соматоневрологических проявлений вегетативной дисфункции, что способствует более быстрому завершению периода восстановления.
Тенотен детский устраняет проявления астении, стабилизирует психоэмоциональное состояние детей: улучшает настроение, успокаивает, способствует снижению раздражительности и капризности, облегчает процессы обучения (запоминание, концентрацию внимания, усидчивость).
Препарат Тенотен детский безопасен у пациентов старшего дошкольного и младшего школьного возраста. Побочных эффектов во время применения препарата не было отмечено.
Доказанное успокаивающее, выраженное вегетотропное и антиастеническое действие препарата Тенотен детский позволяет рекомендовать его для применения у детей с различными проявлениями вегетососудистой дисфункции после перенесенных инфекционных заболеваний.
По вопросам литературы обращайтесь в редакцию.
Е. В. Михайлова, доктор медицинских наук, профессор
Т. Ильичева
Cаратовская областная детская инфекционная клиническая больница,
Саратовский государственный медицинский университет, Саратов

Разработчик сайтов, журналист, редактор, дизайнер, программист, копирайтер. Стаж работы — 25 лет. Область интересов: новейшие технологии в медицине, медицинский web-контент, профессиональное фото, видео, web-дизайн. Цели: максимально амбициозные.
- Запись опубликована: 24.01.2022
- Reading time: 4 минут чтения
Норовирусы — распространенная причина пищевых инфекций, проявляющихся рвотой и диареей. Заражение происходит через загрязненные руки и пищу. Распространению вируса способствует несоблюдение элементарных правил гигиены. Каждый третий случай норовирусных инфекций касается детей до 5 лет, однако норовирусы также очень легко передаются взрослым и вызывают те же симптомы.
Вирус легко распространяется в среде, становясь причиной эндемической диареи, например, во время курортного сезона.
Норовирусы – характеристики семейства калицивирусов
Норовирусы относятся к семейству калицивирусов (Calciviridae), включающему в себя различные типы одноцепочечных РНК-вирусов. К ним относятся:
- Норовирусы , вызывающие острый вирусный гастроэнтерит (неправильно называемый желудочным гриппом) у людей всех возрастов;
- Саповирусы , вызывающие острую диарею преимущественно у детей.
Семейство калицивирусов также включает лаговирус и пузырчатый вирус — непатогенные для человека.
Норовирусы и ротавирусы — в чем разница?
Ротавирусы вызывают норовирусоподобные инфекции желудочно-кишечного тракта, но относятся к другому семейству (ротавирусы – семейство Reoviridae) и характеризуются иной структурой (двухцепочечные РНК).
Отличить инфекции можно по следующим факторам:
- Норовирусы вызывают диарею и рвоту у людей разного возраста, а ротавирусы чаще всего являются причиной диареи у младенцев и у маленьких детей.
- Инфекция, вызванная ротавирусами, дает симптомы, похожие на норовирусную инфекцию, однако период инкубации в этом случае длиннее.
- Ротавирус вызывает водянистую диарею и рвоту, лихорадку и боль в животе. Дети во время болезни теряют аппетит, что может очень быстро привести к обезвоживанию. Обезвоживание, если его не лечить должным образом, опасно для жизни.
Так как уже доступны ротавирусные вакцины, эта инфекция во многих странах распространена менее, чем норовирусная, которая сейчас является основной причиной диареи вирусного происхождения.
Симптомы норовирусной инфекции
Случаи норовирусных инфекций возможны в течение всего года, но в умеренном климате они увеличиваются в период с ноября по апрель.
Симптомы обычно появляются внезапно, через 24-48 часов после воздействия норовируса, но также могут возникать в течение 12-72 часов. У большинства пациентов они длятся от 1 до 3 дней, однако могут быть и дольше.
Норовирусы вызывают острый гастроэнтерит. Основные симптомы:
- тошнота, рвота (чаще, чем при гастроэнтерите, вызванном другими вирусами);
- диарея (обычно умеренная – 4-8 раз за 24 часа) без крови и слизи в кале;
- слабость;
- схваткообразные боли в животе;
- реже лихорадка, озноб, мышечные и головные боли.
Симптомы обезвоживания включают в себя:
- снижение частоты мочеиспускания;
- сухость во рту и горле;
- головокружение при вставании.
Симптомы могут проявляться в разной комбинации: у некоторых пациентов, например, наблюдается только диарея, у других только рвота или только боли в животе. У детей обезвоживание проявляется рядом симптомов:
- плач без слез;
- сонливость;
- капризы;
- отсутствие мочеиспускания более 3 часов;
- изменения ритма дыхания — глубокое, ускоренное дыхание;
- сухость слизистых оболочек
Норовирусы называются норуолковскими, так как впервые вспышка острого гастроэнтерита была замечена в школе в Норуолке, штат США. Все люди, заболевшие в то время, имели одинаковые симптомы норовирусной инфекции: диарея, рвота, тошнота, лихорадка. У всех них симптомы исчезали в течение 2 дней.
Как распространяется норовирусная инфекция?
Норовирусом можно заразиться очень легко:
- капельно при контакте с больным человеком;
- с плохо вымытой или загрязненной на этапе приготовления пищей;
- при прикосновении к загрязненным поверхностям и переносе вируса грязными руками в рот (фекально-оральный путь).
Источником заражения также — загрязненные дверные ручки, телефоны, краны. Заражение также может произойти в результате употребления загрязненной норовирусом воды или случайного проглатывания воды из бассейна.
Продукты, обычно связанные с передачей инфекций:
- листовые овощи;
- свежие фрукты;
- ракообразные, особенно устрицы;
- салаты, бутерброды;
- размороженные фрукты и овощи.
Рост заболеваемости норовирусной инфекцией в мире наблюдается сезонно, зимой и летом. В северном полушарии наибольшее число случаев кишечного гриппа, вызванного норовирусом, наблюдается в зимние месяцы, с ноября по апрель, а в странах южного полушария с мая по сентябрь.
Норовирусы распространяются легко и быстро: для заражения достаточно следового количества инфекционного материала – 10-100 вирионов (вирусных частиц). Источник инфекции в первую очередь — больные люди, выделяющие огромное количество вирусных частиц.
От заражения до появления первых симптомов проходит 12-48 часов. Период наибольшей заразности приходится на время появления симптомов норовирусной инфекции, поскольку вирус присутствует в кале и рвотных массах больных людей. Время выведения вируса составляет около двух недель после исчезновения симптомов. У людей с ослабленным иммунитетом и детей вирусная экскреция в стуле может сохраняться гораздо дольше.
Течение болезни обычно слабое, но быстро может произойти обезвоживание организма, особенно у детей и пожилых людей.
Диагностика норовируса
Норовирус обычно диагностируется на основании тщательного анамнеза и обследования пациента. Лабораторные исследования, при характерных симптомах и в единичных случаях инфекции, могут не проводиться. Лабораторные тесты необходимы для выявления эпидемий и мониторинга эффективности мер по прекращению распространения вируса.
Диагностика предполагает исследование образца кала на наличие норовируса. Образец следует брать в острой фазе заболевания, предпочтительно до 72 часов после появления первых симптомов, когда консистенция кала еще полутвердая или жидкая.
В острой фазе заболевания наибольшее количество вирусов можно обнаружить в кале. Вирус может быть обнаружен при обследовании кала также позже, после исчезновения симптомов, до 10 дней после заболевания.
Также положительный результат анализа кала на норовирус наблюдается у некоторых пациентов даже через несколько недель после выздоровления, это называется носительством. Больной выздоровев, может выделять норовирусы с калом, что может способствовать развитию эпидемии.
В случае эпидемии также должна проверяться на норовориус вода.
Норовирусы – лечение
Симптомы норовирусной инфекции сохраняются в течение 1–3 дней и обычно проходят самостоятельно. Противодиарейные препараты и антибиотики в этом случае не применяют. В тяжелых случаях врачи назначают противорвотные средства.
Лечение норовирусной инфекции заключается в обеспечении адекватной гидратации организма. Особенно опасно обезвоживание для маленьких детей. Для обеспечения эффективной гидратации во время диареи рекомендуется гипоосмолярный пероральный регидратационный раствор со сбалансированной концентрацией глюкозы и электролитов. В первые 3-6 часов после каждой рвоты или жидкого стула следует вводить 50 мл приготовленного раствора на килограмм массы тела и дополнительно 5-10 мл/кг массы тела.
Если возникает рвота, регидратационные жидкости вводят часто, но в небольших объемах, например, по 5 мл каждые 5 минут. Если рвота сохраняется, необходимо внутривенное введение. Стационарное лечение для внутривенной регидратации следует проводить, если у пациента наблюдается сильное обезвоживание, нарушение сознания или постоянная рвота, препятствующая пероральной регидратации.
Когда симптомы стихнут, следует продолжить гидратацию и вернуться к питанию. Диета должна быть легкоусвояемой, можно давать рисовую кашу или постные бульоны с белым измельченным мясом. Нельзя пить молоко, колу, фруктовые соки и газированные напитки.
У детей нормальное питание следует возобновить не позднее, чем через 4 часа. В случае младенцев, находящихся на грудном вскармливании и искусственном вскармливании, рекомендуется продолжать текущее кормление. Детям постарше можно давать без ограничений, например, отварной картофель, рис, каши, нежирное мясо и йогурт, фрукты и овощи.
Могут использоваться в качестве дополнения штаммы пробиотиков с документированной эффективностью, т.е. препараты, включающие живые бактерии, сходные с таковыми из физиологической флоры.
Профилактика норовирусной инфекции
Норовирусы относительно устойчивы к температуре (как к замораживанию, так и к термической обработке; температура 60°С инактивирует норовирусы только через 30 минут), хлорной дезинфекции (ниже 6,25 мг/л до 30 минут); норовирус не погибает от алкоголя или стандартных чистящих средств
Основна профилактики против всех кишечных инфекций — гигиена:
- частое мытье рук, особенно после посещения туалета;
- поддержание чистоты в туалетах (сиденье унитаза, дверные ручки, краны);
- поддержание чистоты общих поверхностей в местах, где находится много людей.
Очень важно соблюдать правила гигиены при уходе за больным человеком, так как норовирусы содержатся в кале и рвотных массах инфицированных людей. Необходимо немедленно тщательно очистить и продезинфицировать место, когда больного вырвало, унитаз и раковину после посещения больным туалета.
Пациент должен быть максимально изолирован от других людей, чтобы снизить риск передачи инфекции. При возникновении вспышки норовируса среди людей, пребывающих друг с другом, например, в доме отдыха, необходимо соблюдать правила гигиенического мытья рук.
Правильная гигиена очень важна в местах общественного питания, при обработке продуктов питания и подаче напитков, в том числе напитков, содержащих кубики льда.
Больные люди должны оставаться дома ещё 2 дня после исчезновения симптомов. Во время появления симптомов заболевания и через несколько дней после их исчезновения следует избегать приготовления пищи для окружающих. Пациентам с симптомами норовирусной инфекции не разрешается пользоваться общественными бассейнами во время симптомов и в течение одной недели после того, как они стихли.
Вакцинация — эффективная форма профилактики заболевания, но работа над вакциной против норовирусов все еще продолжается. Работу тормозит частая рекомбинация между штаммами вируса способствующая быстрым изменениям его генетического разнообразия. Многие рекомбинанты столь же заразны и вирулентны, как и прототипы штаммов. Если вакцина будет разработана, то это будет отличный шанс снизить заболеваемость и смертность от диареи среди детей и взрослых во всем мире.
Что такое ангина? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
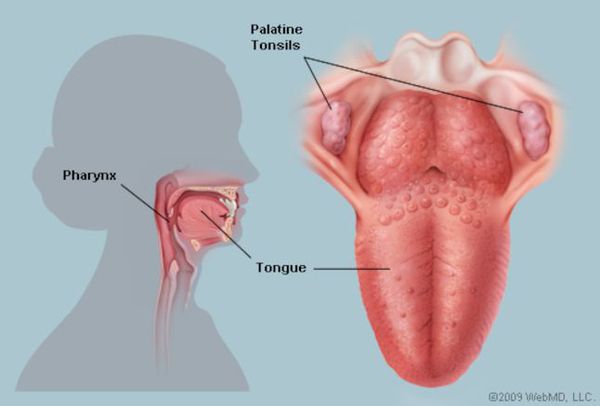
Этиология (причина ангины)
Впервые стрептококк был обнаружен т. Бильротом в 1874 году.
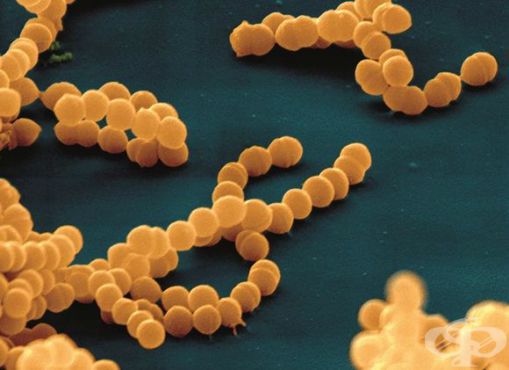
Стрептококки являются неподвижными грамположительными бактериями. Они располагаются парами, цепочками. Их таксономическое деление основано на различиях строения А-липополисахарида (обеспечивает сродство к соединительной ткани).
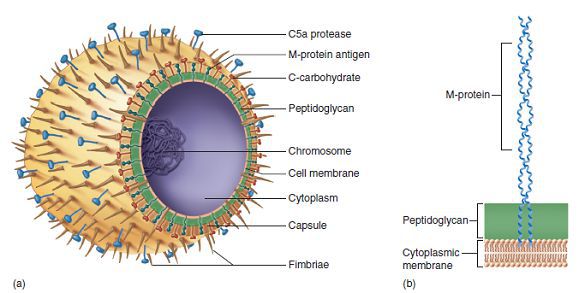
Строение стрептококка:
- Протеины клеточной стенки:
- М — подавляет фагоцитоз, имеет сродство к соединительной ткани сердца;
- Т — фактор типоспецифичности;
- R — нуклеопротеид;
- Протеиназа — вызывает набухание соединительной ткани сердца;
- Стрептокиназа — участвует в переводе плазмина в плазминоген, т. е. вызывает фибринолиз
- Липотейхоевая кислота — обладает сродством к эпителию лимфоидного аппарата глотки, обеспечивает фиксацию стрептококка, т. е. является рецептором;
- Гиалуроновая кислота — входит в состав капсулы, препятствует фагоцитозу возбудителя и расщепляет гликозаминогликаны;
- Стрептолизины:
- S (гемолиз эритроцитов, иммуносупрессия);
- О (кардиотоксичен — воздействует на митохондрии, блокирует тканевое дыхание в сердечной мышце и нарушает проведение сердечных импульсов);
- Эритрогенный экзотоксин — т. н. токсин Дика, вызывающий типичные проявления скарлатины, а в совокупности с другими факторами патогенности поражает капилляры, вызывая точечную сыпь. Первичная инфекция, как правило, протекает по типу скарлатины, а все повторные заражения — по типу ангины, так как к токсину Дика вырабатывается иммунитет. Однако следует помнить, что проявления жизни на Земле весьма обширны и многообразны, и не всегда подчиняются правилам — иногда скарлатина не проявляется, например, при субклинической форме, когда первичное заболевание протекает скрыто, а иммунитет к токсину формируется, или конкретный штамм стрептококка является нетоксигенным, т. е. не вырабатывает токсин, и первая встреча с возбудителем будет типичной ангиной. Также возможна повторная скарлатина, вызванная различными антигенными вариантами стрептококка).
При реакции организма на разные типы стрептококков выделяют однородный иммунитет (стойкий полииммунитет), который защищает от заражения, а также моноиммунитет (обусловленный бактериальными типоспецифичными М-антигенами), который не предохраняет от заболевания другими типами.
Возбудитель чувствителен к высыханию, погибает при нагревании до 60°C за 30 минут, высокочувствителен к антибиотикам пенициллинового и цефалоспоринового рядов. Стрептококки размножаются на кровяном агаре (вызывают гемолиз эритроцитов), могут расти в молочных продуктах, мясном фарше и салатах. [2] [3] [4]
Эпидемиология
Антропоноз. Источник инфекции — больные ангиной, скарлатиной и другими формами стрептококковой инфекции (бета-гемолитический стрептококк группы А) и носители стрептококка.
Механизм передачи: аэрозольный (путь передачи воздушно-капельный), возможен алиментарный (связанный с неполноценным питанием) и контактный пути передачи, особенно у детей раннего возраста.
Восприимчивость к инфекции высокая, сезонность осенне-зимняя. Значительную роль в распространении заболевания имеет повышенная скученность населения. [1] [3] [5]
Факторы риска
Чаще всего ангиной заболевают:
- дети от 5 до 15 лет;
- родители ребёнка школьного возраста;
- взрослые, часто контактирующие с детьми.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы ангины
Инкубационный период — до 2-х суток. Начало острое.
- общей инфекционной интоксикации;
- тонзиллита (острый, гнойный);
- углочелюстного лимфаденита.
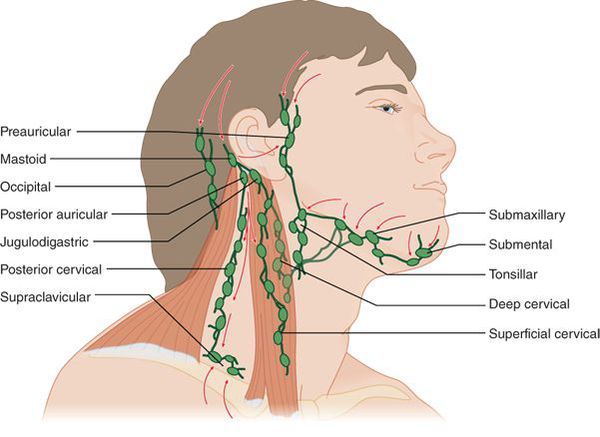
Повышение температуры, озноб и общая утомляемость
Головные боли и ломота в мышцах
При ангине появляется головная боль (тупая, без чёткой локализации) и выраженная ломота в мышцах и суставах.
Боли в горле
В первые сутки заболевания боли в горле проявляются при глотании, затем переходят в постоянное проявление и могут отдавать в ухо.
Увеличение и болезненность лимфатических узлов
Увеличиваются углочелюстные лимфоузлы, становятся очень болезненными, плотноэластической консистенции, не спаяны между собой и окружающими тканями.
Очень характерными являются данные, получаемые при фарингоскопии:
- открывание рта свободное;
- нёбные дужки, язычок, миндалины и мягкое нёбо в первые дни ярко гиперемированы.
Основные проявления тонзиллитов
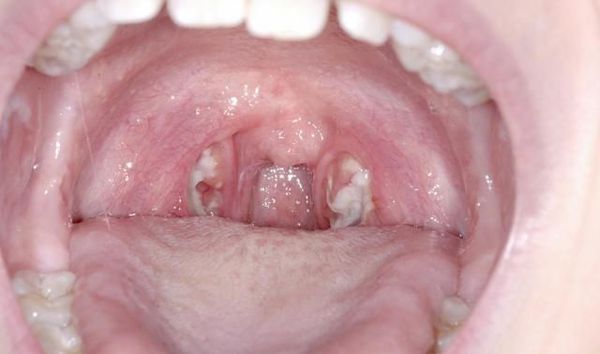
С третьего дня в лакунах появляется отделяемое жёлто-белого цвета (гной) — фолликулярно-лакунарный тонзиллит.
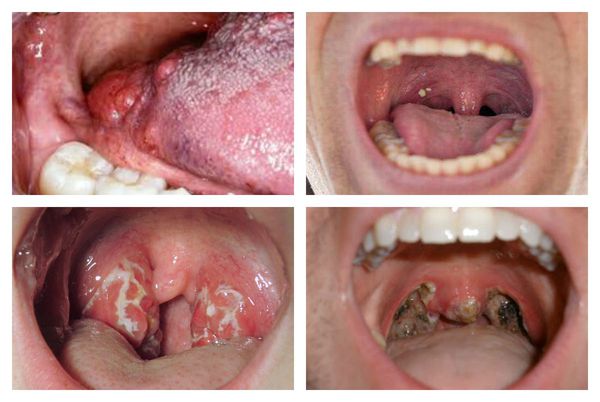
Как выглядит горло при ангине:
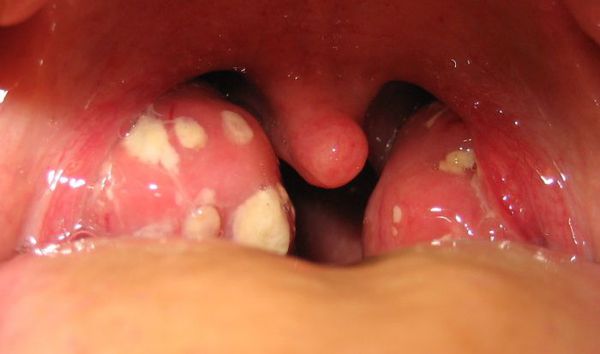
Далее при тяжёлых формах возникает некротический тонзиллит: тёмно-серый цвет миндалин, после отторжения гнойно-некротических масс остаются дефекты ткани.
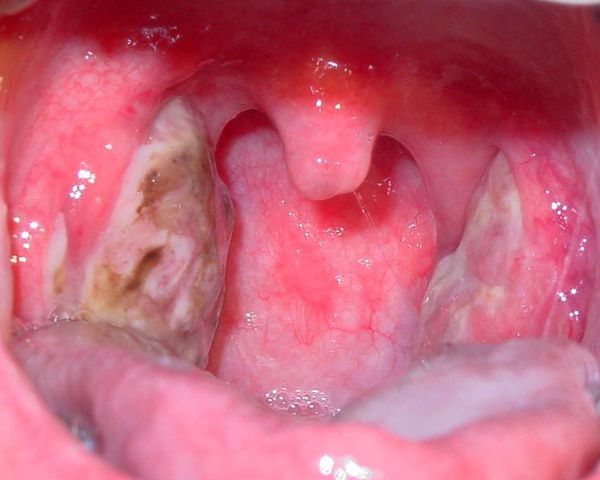
Необходимо помнить, что гнойный налёт при ангине не распространяется за пределы миндалин, легко снимается, не тонет в воде — появление каких-либо других вариантов течения является поводом для сомнения в диагнозе. [2] [3] [5] [6]
Флегмонозный тонзиллит
Флегмонозный тонзиллит — наиболее тяжёлая форма ангины. Характеризуется развитием в ткани миндалин чаще одностороннего гнойного очага без чётких границ. Резко усиливается интоксикация, возникает выраженная болезненность на стороне поражения и отёк, становится сложно открыть рот. Заболевание требует срочного хирургического лечения.
Язвенно-плёнчатая форма тонзиллита
При язвенно-плёнчатой форме ангины возникают изъязвления на поверхности ткани миндалин, сильная болезненность и налёт, который легко снимается шпателем.
Как протекает вирусная и герпесная ангина
"Вирусные ангины" не имеют ничего общего с классической стрептококковой ангиной. Они являются лишь отдельными синдромами при вирусных заболеваниях: аденовирусной, цитомегаловирусной и энтеровирусной (герпангина) инфекции и множестве других. Термин "ангина" применим только к заболеваниям, вызванным бета-гемолитическим стрептококком группы А. Все остальные воспаления ткани миндалины следует называть острым или хроническим тонзиллитом.
По этой причине выделять герпетическую ангину, ангину при дифтерии, гриппе, скарлатине и инфекционном мононуклеозе некорректно.
Как протекает ангина у детей
У детей симптомы ангины более выражены, чем у взрослых. Сильнее интоксикация, ребёнок вялый, отказывается от еды, возможны боли в животе, сильные головные боли, тошнота и рвота.
При каких симптомах ангины стоит бить тревогу
Когда обратиться к врачу:
- при подъёме температуры свыше 37,5 °C;
- сильной и мучительной боли в горле;
- выраженной интоксикации;
- болезненности углочелюстных лимфатических узлов.
Патогенез ангины
Ворота инфекции — лимфоидные образования кольца Пирогова — Лангханса. Происходит проникновение в них стрептококков, воспалительная реакция и дальнейшее распространение возбудителя, его токсинов и продуктов распада бактерий и клеток организма по лимфатическим путям в углочелюстные лимфоузлы (углочелюстной лимфаденит).
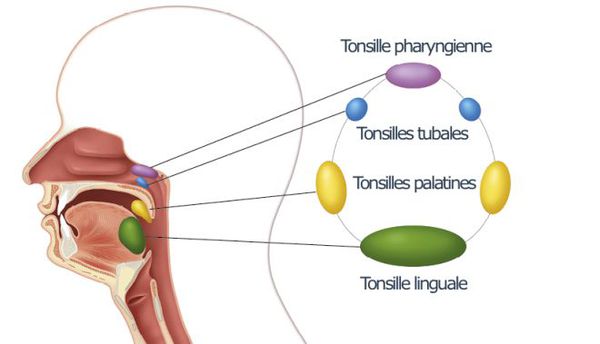
При благоприятном течении этим процесс ограничивается. При барьерной недостаточности стрептококки проникают в околоминдаликовую клетчатку (паратонзиллит, паратонзиллярный абсцесс), вызывают токсическое поражение всего организма. При проходе через слуховую трубу в среднее ухо возбудитель способен вызвать развитие отита и синусита. Достаточно редко при выраженном иммунодефиците развивается сепсис.
В ответ на проникновение бактериальных антигенов в организме больного образуются антитела, которые при взаимодействии с антигенами образуют циркулирующие иммунные комплексы антиген-антитело (АГ-АТ). В норме они разрушаются путём фагоцитоза, комплементом и не вызывают иммунопатологических реакций. Однако бывают ситуации, когда механизмы элиминации не срабатывают.
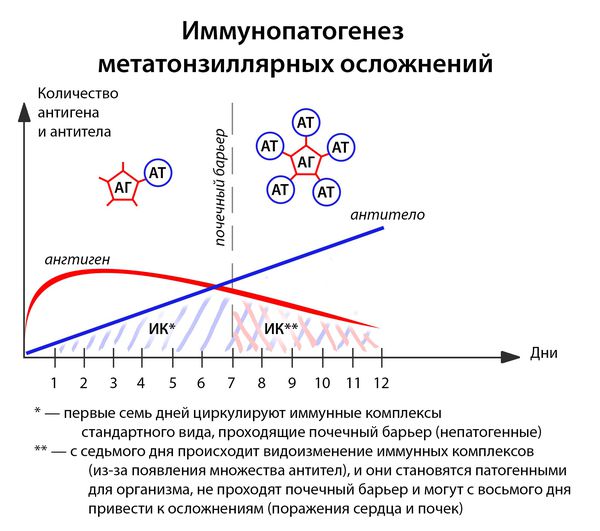
Иммунные комплексы оседают на базальной мембране сосудов (почек) и разрушают её. Далее происходит разрушение подлежащей соединительной ткани. Условиями для этого являются:
- большое количество образующихся иммунных комплексов (при сильном иммунитете, например, у подростков до 17 лет);
- массивная антигенемия (при несвоевременном лечении, высокой вирулентности возбудителя);
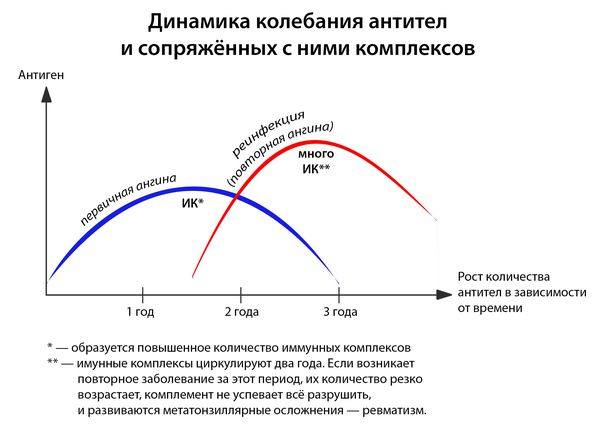
- частые повторные заболевания (2 года после перенесенной ангины — это период повышенного риска).
Иммунитет развивается с третьего дня: макрофаги подготавливают антигены, образуется суперантиген, и лишь затем передают его Т- и В-лимфоцитам, вырабатывающим специфические антитела. [1] [3] [4]
Классификация и стадии развития ангины
По степени тяжести ангина бывает:
- лёгкой;
- среднетяжёлой;
- тяжёлой.
По клинической форме:
- первичная — возникшая впервые или не раньше двух лет после ангины, перенесённой ранее);
- повторная — результат реинфицирования людей с повышенной восприимчивостью в течении двух лет от первичной ангины.
По характеру воспаления миндалин:
- катаральная ангина — покраснение и отёк миндалин;
- фолликулярная ангина — фолликулы белого цвета в ткани миндалин;
- лакунарная ангина — гнойное отделяемое из лакун миндалин;
- некротическая ангина — некроз ткани миндалин;
- гнойно-некротическая ангина — некроз и гнойное расплавление ткани миндалин.
- ангина язычной миндалины;
- ангина гортанных валиков;
- ангина нёбных миндалин;
- комбинированная ангина. [3][4]
Осложнения ангины
Осложнения ангины включают пара и метатонзиллярные процессы.
В острый период могут возникнуть:
- паратонзиллит, паратонзиллярный абсцесс (усиление лихорадки, односторонний характер болей, гиперсаливация, болезненность при открывании рта, асимметрия язычка, односторонний отёк, выраженная гиперемия мягкого нёба);
- инфекционно-токсический миокардит (боли в сердце, перебои в его работе, изменение размеров сердца, появление шумов, одышка, повышение ЛДГ на 1-2 нормы); (воспаление придаточных пазух носа);
- медиастенит (воспаление органов средостения — появление боли за грудиной, одышка);
- заглоточный абсцесс (нагноение лимфатических узлов и клетчатки заглоточного пространства — затруднение глотания, одышка, усиление инотоксикации);
- сепсис (полиорганное заражение, циркуляция возбудителя в крови).
В период выздоровления:
Диагностика ангины
Подготовка к посещению врача
При повышении температуры свыше 37,5 °С, сильной и мучительной боли в горле, болезненности углочелюстных лимфатических узлов и выраженной интоксикации нужно как можно скорее посетить терапевта. Специальная подготовка для этого не требуется.
Лабораторная диагностика
К методам лабораторной диагностики относятся:
- клинический анализ крови (нейтрофильный лейкоцитоз со сдвигом влево, повышение СОЭ);
- общий анализ мочи (мочевой синдром при осложнениях);
- ЭКГ (выполняется в день поступления и при выписке, могут быть признаки гипоксии, нарушения проводимости);
- бактериальный посев с миндалин (мазок) на бета-гемолитический стрептококк (и дифтерию);
- биохимия крови (АСЛО, РФ, СРБ). [3][4]
Дифференциальная диагностика
Боли в горле и повышение температуры тела являются достаточно частыми симптомами множества заболеваний, поэтому вопросы отличия ангины от других патологий являются основополагающими в практике любого врача:
Как отличить ангину от ОРЗ или фарингита
При остром респираторном заболевании поражается не паренхима миндалин, а в основном слизистая оболочка ротоглотки и других отделов респираторного тракта, отсутствует углочелюстной лимфаденит. При фарингите затрагиваются поверхностные слои гортани (слизистая оболочка).
Лечение ангины
Как долго лечится ангина
Режим и диета. Рекомендации и противопоказания для заболевших
Лечение осуществляется в домашних условиях, тяжёлые и осложнённые формы ангины лечатся в стационаре.
Режим палатный, диета — общий стол, при выраженном болевом синдроме показана механически и химически щадящая пища, обильное питьё.
Народные методы терапии. Лечение ангины народными способами и средствами недоказательной медицины недопустимо — это опасно для жизни и здоровья.
Антибиотики — лекарства для лечения ангины
Несмотря на длительное и широкое применение антибактериальных препаратов первого поколения бета-гемолитический стрептококк остаётся высокочувствителен к пенициллиновой и аминопенициллиновой группе антибиотиков, которые и являются препаратами первого выбора терапии — к концу вторых суток применения антибиотиков возбудитель уже погибает. При невозможности использования препаратов данных групп возможна замена на цефалоспориновый или макролидный ряд антибиотиков.
Уход на дому
При лечении ангины на дому первые три дня показано активное ежедневное наблюдение врача в целях своевременного выявления развития осложнений и исключения дифтерии зева.
В качестве патогенетической и симптоматической терапии широко используется:
- антисептические растворы — орошение ротоглотки и миндалин;
- полоскания горла;
- антигистаминные препараты;
- общеукрепляющие средства для повышения иммунитета;
- дезинтоксикационная парентеральная инфузионная терапия — при выраженном синдроме общей инфекционной интоксикации.
Основа лечения ангины — это высокоэффективная антибактериальная терапия. Поэтому применение трав, снимающих боль в горле, и ингаляций при болезни являются лишь вспомогательными. Противогрибковые препараты и компрессы при патологии не используются.
Выписка больных
Выписка пациентов осуществляется не ранее семи дней нормализации температуры тела при условии нормальных анализов крови, мочи и ЭКГ. [2] [3] [6]
Лечение гнойной ангины
В большинстве случаев ангина — это гнойно-воспалительное заболевание, которое требует скорейшего применения антибиотиков и при необходимости нестероидных противовоспалительных и противоаллергических средств.
Лечение простой и хронической ангины
Ангина — это острое заболевание без хронических форм. Однако есть термин "стрептококковое носительство" — отсутствие болезни как таковой, чаще на фоне хронической ЛОР-патологии. В этом случае проводят санирование очага, применяют антибиотики с учётом чувствительности к ним и аппаратно промывают миндалины.
Стоит ли удалять гланды
При ангине не удаляют миндалины. Хирургическое лечение возможно лишь при флегмонозной форме ангины и при редких случаях тяжёлого течения заболевания. При развитии осложнений, например, паратонзиллярного абсцесса производится вскрытие гнойника под местной анестезией и его санация.
Прогноз. Профилактика
Прогноз обычно благоприятный. У людей с тяжёлым иммунодефицитом повышенный риск развития осложнений в острый период болезни.
Поможет ли профилактика
Методы профилактики ангины не разработаны. Основное значение при возникновении очага заболевания имеют:
- изоляция больного и его лечение;
- обследование и санация контактных лиц (бактерионосителей);
- при частых повторных заболеваниях — бициллинопрофилактика, по показаниям — удаление миндалин (решение принимает ЛОР-врач);
- здоровый образ жизни, закаливание, приём витаминов.[reference:] [4]
Кормление грудью при болезни
Грудное вскармливание при ангине можно продолжить. Однако необходимо соблюдать меры профилактики заражения ребёнка:
- не дышать и не кашлять на него;
- чаще мыть руки;
- пользоваться защитной маской, не забывать постоянно менять её;
- регулярно проветривать помещение.
Также следует принимать индивидуально подобранный антибиотик, разрешённый при грудном вскармливании.

Почти каждый человек хоть раз прошел испытание ротавирусом и помнит эти изматывающие симптомы заболевания: слабость, рвоту, боли в кишечнике и диарею. И хотя длится это состояние недолго, следует отнестись к нему серьезно, особенно если болен грудничок и маленький ребенок.
Опасное состояние при этом заболевании состоит в том, что организму грозит обезвоживание.
Источники заражения ротавирусной инфекцией
Источником заражения является заболевший человек, при этом даже спустя десять дней после выздоровления вирус продолжает появляться в фекалиях. Поэтому так важно соблюдать бытовую гигиену.
Заражение происходит следующими способами:
- Через пищу или воду
- Пользуясь бытовыми предметами больного: посудой, полотенцем, игрушками
- При контакте с заболевшим человеком
Вирус можно подцепить в транспорте или магазине, поэтому так важно мыть руки после улицы.
Ротавирус обладает высокой устойчивостью. Попадая в организм человека, возбудитель поражает эпителиальные клетки тонкого кишечника. Вместо пораженных клеток на смену приходят незрелые эпителиоциты, которые являются функционально неполноценными, что влечет ферментативную недостаточность кишечника. В условиях недостатка ферментов желудочно-кишечный тракт не в состоянии расщепить углеводы и особенно лактозу. Поэтому больному назначают специальную диету без молочных продуктов и сдобы. Так непереваренные остатки пищи попадают в толстый кишечник, в нем накапливается жидкость из окружающих тканей и больной страдает от диареи. В результате наступает обезвоживание организма.
Болезнь не проходит, пока эпителий не станет зрелым, и кишечник не восстановится.
Симптомы
Инкубационный период составляет от нескольких часов до трех дней. Спустя некоторое время после заражения больной начинает чувствовать слабость, тошноту, повышается температура. Затем начинается рвота, она может быть как однократной, так и множественной. У детей симптомы выражены сильнее, и они переносят заболевание тяжелее. Затем начинаются боли в животе, которые сопровождаются нарушением стула: сначала он становится кашицеобразным, потом перерастает в диарею. Спустя несколько часов больной чувствует сухость во рту – это первый признак обезвоживания. Больной теряет вес, особенно это выражено у детей до года. От обезвоживания сохнут и трескаются губы и западают глаза. Если у больного спустя 6 часов нет мочеиспускания, то это опасный симптом обезвоживания. Если ребенок тяжело переносит болезнь, то лучше всего его госпитализировать. В условиях стационара больше возможностей вывести ребенка из этого состояния: применяют капельницы, чтобы ликвидировать обезвоживание.
Лечение
Основное лечение – это избавление от токсинов и восполнение жидкости в организме. Поэтому больному врач-терапевт прописывает сорбенты: энтеросгель, активированный уголь, полисорб. Для восполнения потери жидкости используют Регидрон – один пакетик на литр воды. Если обезвоживание ярко выражено, то больного госпитализируют и применяют инфузионную терапию растворами Трисоль или Рингера.
Антибиотики при ротавирусной инфекции бесполезны. Назначают их лишь в одном случае, если заболевание осложнилось кишечной инфекцией. Если диарея затянулась и больной спустя несколько дней не чувствует себя лучше, то выписывают энтерофурил или фуразолидон.
Для восстановления пищеварения назначают мезим или фестал и пробиотики.
Обязательно следует соблюдать безмолочную диету. Пищу лучше готовить на пару или отваривать. Рекомендуется кисель, рисовая каша на воде, печеные яблоки, нежирный мясной бульон, рыбу и нежирное мясо, вареный картофель.
Запрещено все овощи и фрукты, бобовые, молочные продукты, сдоба и газированные напитки. Если аппетита нет, то через силу есть не надо, но пить надо обязательно.
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо). Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гаст
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо).
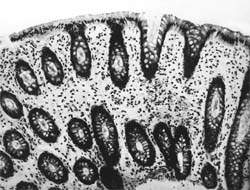 |
| Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимально выраженный катаральный колит. х 100. |
Ротавирусы представляют собой род семейства Reoviridae, который объединяет большое количество сходных по морфологии и антигенной структуре вирусов, вызывающих гастроэнтерит у человека, млекопитающих и птиц. Систематическое изучение ротавирусов человека началось с 1973 года, когда они были обнаружены при электронной микроскопии ультратонких срезов биоптатов слизистой оболочки двенадцатиперстной кишки, полученных от больных острым гастроэнтеритом детей Австралии (Р. Бишоп и соавторы). В том же году Т. Флеветт обнаружил сходный вирус в копрофильтратах больных гастроэнтеритом методом электронной микроскопии при негативном контрастировании препаратов.
Вирусные частицы имеют диаметр от 65 до 75 нм. При проникновении контрастирующего вещества в вирион выявляется электронно-плотный центр диаметром 38 — 40 нм, который представляет собой так называемую сердцевину, окруженную электронно-прозрачным слоем. Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободом, поэтому их стали называть ротавирусами (лат. rota — колесо).
Ротавирусы имеют две белковые оболочки — наружный и внутренний капсиды. Сердцевина содержит внутренние белки и генетический материал, представленный двунитчатой фрагментированной РНК. Геном ротавирусов человека и животных состоит из 11 фрагментов, которые могут быть разделены при электрофорезе в полиакриламидном геле (ПААГ) или агарозе. В составе ротавирусов обнаружено четыре антигена; основной из них — это групповой антиген, обусловленный белком внутреннего капсида. С учетом группоспецифических антигенов все ротавирусы делятся на пять групп: A, B, C, D, E. Ротавирусы одной группы имеют общий групповой антиген, который выявляется иммунологическими реакциями: иммуноферментный анализ, иммунофлюоресценция, иммунная электронная микроскопия и др. Большинство ротавирусов человека и животных относятся к группе A.
| Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями |
Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями. Вирусы в фекалиях заболевших появляются одновременно с развитием клинических симптомов, наибольшая концентрация их в кале (до 109 — 1011 вирусных частиц в 1 г) регистрируется в первые 3 — 5 дней болезни. В эти дни больные представляют наибольшую эпидемиологическую опасность для лиц, контактирующих с ними. Наиболее частым источником заболевания для детей первого года жизни являются инфицированные ротавирусом матери; для взрослых и детей более старшего возраста — дети, в основном из детских коллективов. Возможность заражения человека от животных не доказана.
Патогенез ротавирусной инфекции характеризуется проникновением вируса в эпителиоциты слизистой оболочки желудочно-кишечного тракта, преимущественно тонкой кишки, что приводит к их повреждению и отторжению от ворсинок. Вследствие этого на ворсинках тонкой кишки появляются функционально и структурно незрелые энтроциты с низкой способностью синтезировать пищеварительные ферменты. При ротавирусном гастроэнтерите это проявляется снижением уровня дисахаридаз, развивается вторичная дисахаридазная недостаточность, при которой в просвете тонкой кишки накапливаются нерасщепленные дисахариды, что создает повышенное осмотическое давление и приводит к выводу в просвет кишечника воды и электролитов из тканей организма. Это является основной причиной диареи и дегидратации и определяет основные клинические проявления болезни.
Ротавирусный гастроэнтерит как инфекционное заболевание имеет циклическое течение. Инкубационный период продолжается чаще всего от 12 — 24 часов до двух суток. Клиническая картина ротавирусного гастроэнтерита характеризуется в основном острым началом, однако в ряде случаев может иметь место продромальный период длительности от 12 до 48 — 72 часов. В этот период больные отмечают недомогание, общую слабость, повышенную утомляемость, снижение аппетита, головную боль, познабливание, урчание и неприятные ощущения в животе, умеренно выраженные катаральные явления: заложенность носа, першение в горле, легкий кашель.
В клинической картине ротавирусного гастроэнтерита в период развернутых клинических проявлений ведущими являются синдромы гастроэнтерита и интоксикации. Выраженность диареи и обусловленной ею той или иной степени дегидратации организма, а также токсикоза, продолжительность этих симптомов в значительной мере определяет тяжесть течения заболевания.
Синдром гастроэнтерита характеризуется развитием диареи, снижением аппетита, появлением урчания и болей в животе, тошноты и рвоты. Наиболее типичен для ротавирусного гастроэнтерита обильный водянистый пенистый стул желтого или желто-зеленого цвета. У больных с легким течением заболевания стул может быть кашицеобразным. Как правило, патологические примеси в стуле отсутствуют. Боль локализуется преимущественно в верхней половине живота или является диффузной, она может быть разной интенсивности. Почти всегда она сопровождается громким урчанием в животе.
Синдром интоксикации появляется в самом начале заболевания. Слабость, зачастую резкая, является наиболее частым проявлением этого синдрома; реже отмечается головная боль. При более тяжелом течении имеют место головокружение, обморочное состояние, коллапс. Обращает на себя внимание следующая особенность ротавирусного гастроэнтерита: два ведущих в клинической картине болезни синдрома развиваются в процессе заболевания не всегда однонаправленно; у некоторых больных на фоне сравнительно слабо выраженных диспепсических явлений могут наблюдаться резко выраженные симптомы общей интоксикации, особенно слабость.
Повышение температуры тела не всегда может отмечаться при ротавирусном гастроэнтерите, особенно у взрослых. У некоторых больных может быть озноб без повышения температуры. В то же время нередко в разгар заболевания выраженность лихорадочной реакции варьируется от субфебрильных цифр и выше и может достигать 38 — 39°С как у детей, так и у взрослых.
Важным в диагностическом плане для ротавирусного гастроэнтерита считается сочетание двух ведущих клинических синдромов с симптомами поражения верхних дыхательных путей. Катаральный синдром встречается приблизительно у 50% больных и проявляется в виде гиперемии и зернистости слизистых оболочек мягкого неба, небных дужек, язычка, задней стенки глотки, а также насморка, заложенности носа, кашля, болей в горле. В ряде случаев катаральные симптомы наблюдаются уже в продромальном периоде, до проявления симптомов гастроэнтерита.
В разгар болезни отмечается изменение функционального состояния сердечно-сосудистой системы, чаще у пациентов с более тяжелым течением и при наличии сопутствующих заболеваний органов кровообращения. У большинства пациентов отмечается тенденция к артериальной гипертензии, тахикардия, определяется глухость сердечных тонов при аускультации. У больных с тяжелым течением заболевания, как правило, возникают обмороки и коллапсы из-за выраженных расстройств гемоциркуляции, в генезе которых наряду с токсическими воздействиями существенное значение имеет гиповолемия. Потери жидкости и электролитов вследствие рвоты и диареи могут быть значительными и приводят к развитию дегидратации. Клинические проявления дегидратации зависят от ее степени. При легком и среднетяжелом течении ротавирусного гастроэнтерита отмечается жажда, сухость во рту, слабость, бледность (дегидратация I — II степени), при тяжелом течении наряду с этими симптомами наблюдаются также осиплость голоса, судороги мышц конечностей, акроцианоз, снижение тургора кожи, уменьшение диуреза (дегидратация III степени).
В связи с развитием при ротавирусном гастроэнтерите возможных осложнений, главным образом циркуляторных расстройств, острой сердечно-сосудистой недостаточности, нарушений гомеостаза, выделяют группы больных повышенного риска, в которые включают новорожденных, детей младшего возраста, лиц пожилого возраста, а также больных с тяжелыми сопутствующими заболеваниями. Описанные в литературе и наблюдавшиеся нами случаи ротавирусного заболевания с летальным исходом относятся именно к этим группам.
Выделяются две основные клинические формы ротавирусного заболевания — гастроэнтерическая и энтерическая. Симптомы только острого гастрита (гастритический вариант) встречаются в 3 — 10% случаев. Функциональные и морфологические нарушения со стороны желудочно-кишечного тракта, возникающие при ротавирусном гастроэнтерите в случае наличия у пациентов фоновой гастроэнтерологической патологии, нередко способствуют развитию таких осложнений основного заболевания, как обострение сопутствующих болезней: хронического гастрита, энтероколита, панкреатита, часто в сочетании с выраженными явлениями дисбактериоза кишечника, требующими коррекции при лечении.
Методы диагностики ротавирусной инфекции
При ротавирусном гастроэнтерите гемограмма изменяется следующим образом: в остром периоде заболевания с высокой частотой выявляются лейкоцитоз с нейтрофилезом и повышенная СОЭ. В периоде реконвалесценции картина крови обычно нормализуется полностью. Изменения урограммы у большинства больных имеют кратковременный характер и проявляются чаще всего небольшой протеин-, лейкоцит- и эритроцитурией; в редких случаях в моче появляются гиалиновые цилиндры в незначительном количестве. При тяжелом течении заболевания нарушения функции почек могут быть более выраженными, с повышением уровня мочевины крови, олигоурией или анурией, снижением клубочковой фильтрации. На фоне проводимой терапии указанные изменения быстро исчезают и при повторных обследованиях не отмечаются.
В качестве примера, иллюстрирующего особенности клинического течения ротавирусного гастроэнтерита, приводим выписку из истории болезни.
Лечение: обильное питье солевых растворов, парентеральная регидратационная и дезинтоксикационная терапия — трисоль 1000 мл внутривенное капельное введение, внутрь ферментные препараты: абомин, панкреатин, тансол, карболен. Течение заболевания без осложнений. На третий день болезни — субфебрильная температура, оставалась слабость; боли в животе прекратились. Стул кашицеобразный до пятого дня от начала заболевания. Полное выздоровление наступило на седьмой день болезни.
Дифференциальный диагноз у больных ротавирусным гастроэнтеритом проводят с другими острыми кишечными инфекциями как вирусной так и бактериальной этиологии, прежде всего в тех случаях, когда в клинической картине на первый план выступает синдром гастроэнтерита: с вирусными диареями различной этиологии (аденовирусы, коронавирусы, астровирусы, калицивирусы, вирус Норфолк, энтеровирусы Коксаки и ЕСНО); с гастроинтестинальной формой сальмонеллеза, с гастроэнтеритическим и гастроэнтероколитическим вариантами острой дизентерии, с пищевыми токсикоинфекциями, вызванными условно-патогенными бактериями; с холерой.
Обнаружение специфических антител и нарастание их титра в сыворотке крови больных и переболевших ротавирусным гастроэнтеритом при помощи серологических реакций с целью текущей диагностики на практике в настоящее время широкого распространения не получило и используется в основном для ретроспективного анализа различных эпидемиологических ситуаций.
Методы обнаружения вирусспецифической РНК, которые можно назвать высокочувствительными и специфичными, имеют, однако, ряд недостатков, ограничивающих их практическое применение (необходимость наличия специальной аппаратуры, реактивов, квалифицированного персонала и др.) Наиболее простой метод в этой группе — электрофорез ротавирусной РНК в полиакриламидном геле. Этот метод, позволяющий идентифицировать штаммы вирусов, вызвавшие заболевание, и дать характеристику штаммов, циркулирующих на данной территории, в основном применяется при эпидемиологических исследованиях.
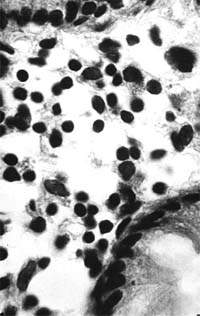 |
| Рисунок 2. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимальное содержание плазматических клеток в собственной пластинке, увеличение в ней числа макрофагов. х 400 |
В клинической практике врач нередко сталкивается с обстоятельствами (сомнительные результаты вирусологических и серологических исследований, случаи микст-инфекций), когда возникает необходимость в применении дополнительных методов для верификации диагноза. С этой целью может быть использован доступный для практического здравоохранения интрументальный метод исследования — ректороманоскопия с аспирационной биопсией слизистой оболочки толстой кишки. При гистологическом, морфометрическом и гистохимическом исследованиях биоптатов при ротавирусном гастроэнтерите выявляются характерные изменения в виде поверхностного минимально выраженного катарального колита с незначительной дистрофией эпителия (рис. 1), снижения числа серотонинсодержащих желудочно-кишечных эндокриноцитов (ЕС-клетки) в эпителиальном пласте кишечных желез, умеренной инфильтрацией собственной пластинки плазматическими клетками и увеличением в ней числа макрофагов (рис. 2). Эти особенности имеют дифференциально-диагностическое значение, поскольку отличаются указанным показателем от других острых кишечных инфекций, что может быть использовано в диагностически сложных случаях.
Здравоохранение в настоящее время не располагает препаратами, обладающими специфическим антиротавирусным действием, поэтому терапия ротавирусного гастроэнтерита является патогенетической. Основные ее цели — борьба с дегидратацией, токсикозом и связанными с ними наиболее часто встречающимися при ротавирусном гастроэнтерите нарушениями функции жизненно важных органов — сердечно-сосудистой системы и органов мочевыделения, степень выраженности которых во многом определяет тяжесть течения заболевания и его прогноз.
Для правильного выбора характера и объема проводимой регидратационной терапии в первую очередь необходимо установить степень дегидратации у того или иного пациента. При эксикозе I — II степени следует ограничиваться пероральной регидратационной терапией (препараты регидрон, глюксолан и др.). При дегидратации III степени целесообразно прибегать к комбинированной парентеральной и пероральной регидратации. Для парентеральной регидратации применяют растворы трисоль, квартасоль, ацесоль и др. С целью дезинтоксикации и улучшения гемодинамики при среднетяжелом и тяжелом течении заболевания показаны коллоидные растворы (гемодез, полиглюкин и др.).
| Для ротавирусной инфекции характерно сочетание гастроэнтерита, интоксикации и симптомов поражения верхних дыхательных путей |
Современными представлениями о патогенезе диарейного синдрома при ротавирусном гастроэнтерите обусловлено и назначение соответствующих средств, способствующих нормализации состояния пищеварительного тракта, а также диеты. Учитывая нарушения активности ряда пищеварительных ферментов, в частности лактазы, рекомендуется исключить в острый период заболевания из пищевого рациона больных молоко и молочные продукты. Кроме того, по этой же причине целесообразно ограничивать и пищу, богатую углеводами. В связи с вышеизложенным, в острый период необходимы энзимные препараты (панзинорм-форте, фестал и др). Кроме того, в остром периоде заболевания могут быть использованы адсорбирующие и вяжущие средства, способствующие ускоренному формированию стула (смекта, карболен и др.) также возможно применение хилака-форте. Высокой частотой дисбактериозов кишечника различной степени выраженности у больных ротавирусным гастроэнтеритом обусловлена необходимость применения в комплексной терапии бактерийных биологических препаратов. Лучшая терапевтическая эффективность при ротавирусном гастроэнтерите отмечена при применении лактосодержащих бактерийных биологических препаратов (ацилакт, лактобактерин и др.), что, по-видимому, связано с заместительным действием бактериальной лактазы, содержащейся в лактобактериях. В последние годы в комплексной терапии ротавирусного гастроэнтерита начал применяться комплексный иммуноглобулиновый препарат (КИП), который разработан и выпускается в МНИИЭМ им. Г. Н. Габричевского. Это первый отечественный иммуноглобулиновый препарат для энтерального применения. КИП характеризуется повышенной концентрацией антител к микроорганизмам, возбудителям острых кишечных инфекций, в том числе ротавирусам, сальмонеллам, шигеллам, эшерихиям и др. Применение КИП в комплексной терапии больных ротавирусным гастроэнтеритом оказывает отчетливый положительный терапевтический эффект, существенно сокращая продолжительность интоксикации и диареи, что открывает новые возможности в лечении этого заболевания.
Литература
1. Букринская А. Г., Грачева Н. М., Васильева В. И. Ротавирусная инфекция. М., 1989.
2. Дроздов С. Г., Покровский В. И., Шекоян Л. А., Машилов В. П. и др. Ротавирусный гастроэнтерит. М., 1982.
3. Новикова А. В. и др. Архив патологии, 1989, №6.
4. Щербаков И. Т. и др. Архив патологии, 2995, №3.
5. Юшук Н. Д., Царегородцев А. Д.. Лекции по инфекционным болезням. М., 1996.
Читайте также:

