Антибиотикотерапия при инфекционных осложнениях
Обновлено: 25.04.2024
New Possibilities of Antibacterial Therapy of Infections in Surgical Practice
A. A. ZAITSEV, 0. I. KARPOV, A. YU. STREKACHEV
Institute of Pharmacology, St.Petersburg I. P. Pavlov State Medical University © Коллектив авторов, 2003
Эмпирический подход к антибиотикотерапии внебольничных инфекций в стационаре является определяющим, по крайней мере на начальном этапе лечения. От грамотного решения врача в выборе средств и методов стартовой терапии зависит самое главное — удастся ли остановить инфекционный процесс на начальной фазе его развития или же допустить его прогрессирование. Правильная врачебная тактика обусловливает возможность борьбы с внебольничной условно-патогенной микрофлорой, тогда как ее недостаточная эффективность приводит к пролонгации пребывания больного в стационаре и, соответственно, повышает риск присоединения внутригоспитальных патогенов, возможности борьбы с которыми более ограничены. Иными словами, эффективная стартовая антибиотикотерапия — это чрезвычайно важный фактор, от которого во многом зависит исход болезни.
Преобладающие микроорганизмы и рекомендуемые антибактериальные средства
Все сказанное имеет прямое отношение к осложненным внебольничным интраабдоминальным инфекциям, требующих не только оперативного лечения, но и назначения антибактериальных средств. Эти инфекции, как правило, имеют полимикробную этиологию, включающую ассоциации грамположительных и грамотрицательных аэробов и анаэробов. Частота встречаемости анаэробов неодинаково оценивается разными авторами, но главное, что эти микроорганизмы единодушно признаются ведущими возбудителями инфекций брюшной полости и, следовательно, антианаэробный компонент в спектре антибиотика является одним из определяющих критериев в его выборе. Немаловажное значение имеют также фармакокинетика антибактериального препарата, его переносимость и фармакоэкономические аспекты лечения. Применение антибиотиков направлено на предупреждение интраабдоминального реинфицирования и формирование экстраабдоминальных очагов. Даже при наличии микробиологических данных существуют сложности их клинической оценки, затрудняющие установление ведущего возбудителя.
Среди аэробных микроорганизмов при внебольничных интраабдоминальных инфекциях преобладают грамположительные кокки — золотистый стафилококк, обычно чувствительный к метициллину, пиогенный и другие стрептококки. Грамотрицательные микроорганизмы представлены бактериями семейства Enterobacteriaceae — прежде всего E.coli, реже другими видами (Klebsiella spp., Proteus spp.). К сожалению, даже внебольничные штаммы энтеробактерий способны продуцировать различные бета-лактамазы, инактивирующие незащищенные пенициллины и цефалоспорины I—II, а иногда и III поколения.
Среди анаэробных возбудителей внебольничных интраабдоминальных инфекций встречаются различные бактероиды, клостридии, фузобактерии, пептострептококки и некоторые другие. Важно еще раз подчеркнуть, что необходимо приостановить инфекционный процесс именно на этом этапе, поскольку его прогрессирование сопровождается риском присоединения госпитальных резистентных штаммов микроорганизмов (например, метициллинорезистентных стафилококков, клебсиеллы, продуцирующих бета-лактамазы расширенного спектра), в том числе новых, не характерных для внебольничных инфекций, таких как Enterobacter spp., Serratia spp., Citrobacterspp. и неферментирующих бактерий — псевдомонад и ацинетобактера, характеризующихся высокой устойчивостью ко многим группам антибактериальных препаратов.
Внебольничные интраабдоминальные инфекции рассматриваются как весьма серьезные заболевания, до сих пор характеризующиеся вариабельной, но высокой летальностью (3—30%). Анализ эффективности различных схем антибиотикотерапии показывает, что при эмпирическом подходе успех стартовой терапии достигается не более чем в 65% случаев [1]. В остальных случаях необходимо назначение антибактериальных препаратов второй линии, иногда — повторное оперативное вмешательство, а часть больных погибает. При неуспехе стартовой терапии значительно удлиняются сроки госпитализации и существенно — в 3—10 раз — возрастает стоимость излечения одного больного (затраты на дополнительные парентеральные антибиотики + новая операция + дополнительные дни пребывания в стационаре).
Клинико-фармакологическая характеристика моксифлоксацина
Заслуженной популярностью при лечении интраабдоминальных инфекций пользуются синтетические противомикробные средства фторхинолоны и, в первую очередь, наиболее активный из них ципрофлоксацин. В целом, по антимикробному спектру ципрофлоксацин сопоставим с аминогликозидами, но не обладает присущей последним нефро— и ототоксичностью. К сожалению, он характеризуются низкой активностью в отношении стрептококков и отсутствием реального эффекта против анаэробов — клостридий и бактероидов.
Учитывая ключевую роль полимикробных ассоциаций в этиологии интраабдоминальных инфекций, большие надежды в их лечении возлагаются на фторхинолоны последнего поколения. Из них в нашей стране разрешены к клиническому применению препараты левофлоксацин (Таваник) и моксифлоксацин (Авелокс). Они обладают повышенной активностью против пневмококков, стрептококков и стафилококков, сопоставимы с ципрофлоксацином по активности против Enterobacteriaceae, а моксифлоксацин характеризуется также высокой антианаэробной активностью.
Моксифлоксацин обладает широким антибактериальным спектром, включающим большинство клинически значимых возбудителей интраабдоминальных инфекций. Среди грамположительных бактерий к нему высокочувствительны стрептококки, пневмококки, стафилококки, причем моксифлоксацин превосходит другие фторхинолоны по активности в отношении пенициллинорезистентных штаммов пневмококков и метициллино-резистентных стафилококков. Для большинства представителей Enterobacteriaceae МПК90 моксифлоксацина составляет < 1 мг/л, хотя он, по сравнению с ципрофлоксацином, менее активен in vitro против Pseudomonas spp. и некоторых штаммов энтеробактера и цитробактера. По действию на анаэробы моксифлоксацин не уступает метронидазолу, ингибитор-защищенным пенициллинам и карбапенемам [2].
Важной фармакодинамической особенностью моксифлоксацина является приблизительно одинаковое сродство к топоизомеразам I и II типов — мишеням фторхинолонов в бактериальной клетке, что в наибольшей степени предотвращает селекцию устойчивых штаммов [3]. Надежность эффекта препарата подтверждается также данными in vitro о том, что его активность лишь незначительно снижается при сдвигах рН среды в диапазоне 5,6—8,4 и практически не изменяется при значениях инокулюма 10 4 —10 6 КОЕ/мл [4].
С этой точки зрения перспективным представляется использование современных фторхинолонов, в частности, моксифлоксацина, для профилактических целей, что нами сделано, например, при гистерэктомии. 30 больных были рандомизированы на 2 равные группы. Больные первой группы получали моксифлоксацин внутрь в дозе 0,4 г за 2 часа до операции, больные второй группы — цефуроксим в дозе 1,5 г и метронидазол в дозе 0,5 г внутривенно за 60 мин до операции. В обеих группах пациенток эффективность периоперационной профилактики составила 100%. Побочные эффекты при профилактике не возникли.
Анализ минимизации стоимости профилактики говорит в пользу моксифлоксацина, поскольку профилактика обходится в среднем в 170 руб./чел., а при использовании цефуроксима с метронидазолом (с учетом расходных материалов) — 207 руб./чел. [7]. По результатам этого исследования нами сделан вывод, что моксифлоксацин эффективен и безопасен в качестве средства периоперационной профилактики при абдоминальной гистерэктомии и имеет фармакоэкономические преимущества перед комбинацией цефуроксим + метронидазол.
ЛИТЕРАТУРА
1. Cattan P., Yin D. D., Satfati E. et al. Cost of care for inpatients with community-acquired intra-abdominal infections. Eur J Clin Microbiol Infect Dis 2002; 21: 787-793.
2. Яковлев С. В., Мохов О. И., Суворова М. П. Моксифлоксацин: антимикробная активность, фармакокинетика и клиническое применение при внебольничных респираторных инфекциях. Клин фармакол тер 2001; 2: 51—56.
3. Сидоренко С. В. Перспективы применения моксифлоксацина для лечения инфекций мочеполовых путей. Антибиотики и химиотер 2002; 1:2-8.
4. Herrington J. A., Federici J. A., Remy J. M. Factors affecting the in vitro activity of moxifloxacin. Moxifloxacin in practice/ Adam D., Finch R. eds. New York 2000; 3: 73-79.
5. Praise A. P., Bass S., Cunningham B. etal. An outbreak of enterococcal infection controlled by encouraging quinolone usage. Clin Microbiol Infect 1999; 5: 3: 309.
6. Карпов О. И., Зайцев А. А., Суисси Р. Фармакоэпидемиология ан-тибиотикопрофилактики. X Национальный конгресс: Человек и лекарство. М.: 2003; 32.
7. Карпов О. И., НиауриД. А., Зайцев А. А. и др. Эффективность моксифлоксацина для профилактики инфекции при абдоминальной гистерэктомии. Там же; 209—210.
8. Sologub Т., Karpov О., ZaytsevA. Susceptibility of problem respiratory pathogens to levofloxacine. Europ Resp J 2002 .20: Suppl.38: 526—527.
Выбор антибиотика при инфекциях. Рекомендации, критерии
Основные принципы антибактериальной терапии — избирательная токсичность в отношении патогенного микроорганизма и относительная безопасность для организма человека. Для их выполнения большое значение имеет использование в качестве мишеней для лекарственных препаратов тех компонентов бактериальной клетки, которые отсутствуют у человека.
Примером такого компонента может быть клеточная стенка, воздействие на которую оказывает слабое влияние на макроорганизм и в то же время губительно для бактерии. Правильно подобранная антибиотикотерапия всегда эффективна и достаточно безопасна.
Несмотря на то, что почти все антибиотики обладают рядом побочных эффектов, серьёзные нарушения возникают достаточно редко. Кроме того, препараты этой группы имеют достаточно высокий терапевтический индекс, а потому побочные эффекты манифестируют только при назначении доз, намного превышающих терапевтическую. Важное исключение — аминогликозиды, наблюдение за концентрацией которых в сыворотке крови имеет первостепенное значение.
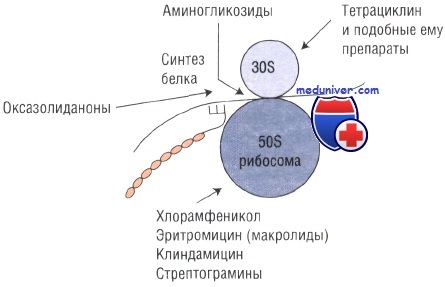
Выбор антибиотика
Выбор антибиотика зависит от локализации очага инфекции, чувствительности микроорганизмов, тяжести заболевания и аллергического анамнеза, вероятности возникновения побочных эффектов, стоимость препарата рассматривают в последнюю очередь. Рациональный выбор терапии зависит от знания локализации возбудителя и профиля его чувствительности к антибиотикам.
Локализация очага инфекции. Способность проникать в ткани (костную, суставную) или спинномозговую жидкость у всех антибактериальных препаратов различна. При абсцессах, а также в тканях с низким кровотоком достаточно трудно достичь высокого уровня антимикробной активности. Кроме того, эффект некоторых антибиотиков (например, аминогликозидов) снижается при низких значениях рН. В связи с этим абсцесс, возникающий внутри костной ткани или в спинномозговом канале, очень тяжело поддаётся лечению.
Чувствительность микроорганизмов. Streptococcus pyogenes высокочувствителен к действию бензилпенициллина, но другие бактерии, например, рода Acinetobacter и Pseudomonas. не восприимчивы к действию большинства антибиотиков, а потому подобрать эффективный препарат бывает достаточно сложно.
Вероятность возникновения аллергических реакций или побочных эффектов. Многие пациенты имеют в анамнезе наличие аллергических реакций к одному или более антибиотикам (наиболее чаще к пенициллину). В таких случаях обычно назначают альтернативное лечение. Возникновение аллергии — основное противопоказание не только к применению препарата, вызвавшего её, но и к назначению других родственных лекарств этой группы.
Противопоказание к использованию аминогликозидов — нарушение функции почек. Применение препаратов цефалоспоринового ряда ограничивается возрастом пациента, так как эти лекарственные средства повышают риск развития суперинфекции (например, в случае С. difficile).

Методы введения антибиотиков в организм при инфекциях
В настоящее время наиболее распространён приём препаратов внутрь (как при амбулаторном, так и при стационарном лечении). Кроме того, антибиотики можно применять местно (при кожных инфекциях), ректально (метронидазол для профилактики осложнений после хирургических операций) или вагинально (в виде пессариев). При тяжёлых инфекционных заболеваниях (септицемия и др.) для обеспечения терапевтического эффекта рекомендовано внутривенное введение антибактериальных препаратов.
Этот метод также показан пациентам, которые не могут принимать лекарства внутрь (например, при повторной рвоте). В педиатрии следует также учитывать вкусовые свойства антибиотиков. Кроме того, для многих пациентов большую роль играет кратность приёма и сложность режима лечения.
Многие пациенты имеют в анамнезе наличие аллергических реакций к одному или более антибиотикам (наиболее чаще к пенициллину).
Контроль антибактериальной терапии инфекции
Для контроля достижения и поддержания терапевтической дозы препарата, а также для снижения риска возникновения токсического эффекта при лечении антибиотиками необходимо наблюдение за состоянием пациентов. Это особенно важно в случаях, когда терапевтическая и токсическая дозы антибиотика отличаются незначительно. Перед внутривенным введением ванкомицина и аминогликозидов, а также по истечении часа после их введения необходимо измерять концентрацию препаратов в сыворотке крови.
Для обеспечения терапевтического эффекта и снижения риска интоксикации полученные результаты анализов должны соответствовать установленным нормам. Например, если концентрация высока, то дозу необходимо уменьшить. Кроме того, понизить уровень препарата в крови помогает снижение частоты его приёма. При приёме пролонгированных форм (когда для обеспечения терапевтического эффекта достаточно однократного приёма в сутки) анализы интерпретируют при помощи нормограммм и сравнивают результаты с общепринятыми нормами.
При лечении инфекций, вызванных частично устойчивыми микроорганизмами, также необходимо измерять концентрацию препаратов в сыворотке крови. Если рост бактерий ингибирует высокая концентрация антибиотика, то важно поддерживать её в сыворотке на постоянном уровне. Если инфекция возникает в труднодоступных местах (например, менингит, вызванный штаммами Pseudomonas), то содержание препарата можно измерить в спинномозговой жидкости.
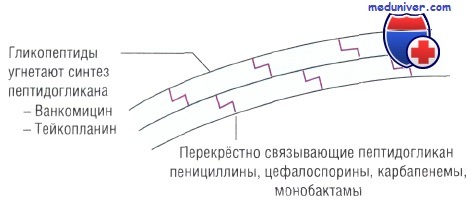
Побочные эффекты антибиотиков
Наиболее распространённый побочный эффект при приёме антибиотиков — незначительные желудочно-кишечные расстройства. В исключительных случаях наблюдают тяжёлые аллергические реакции, приводящие к анафилактическому шоку или сывороточной болезни.
Желудочно-кишечный тракт при антибактериальной терапии. Антибактериальные препараты (особенно бета-лактамы) нарушают баланс нормальной микрофлоры кишечника, вызывая активный рост условно-патогенных микроорганизмов, таких, как род Candida. Таким образом, антибактериальная терапия может привести к острой диарее или более серьёзному осложнению — пневдомембранозному колиту.
Кожа при антибактериальной терапии. Кожные реакции могут быть различны: от лёгкой крапивницы или пятнисто-папулёзной эритематозной сыпи до мультиформной эритемы и крайне опасного синдрома Стивенса— Джонсона. В большинстве своём они не носят угрожающего характера и исчезают при отмене препарата.
Система кроветворения при антибактериальной терапии. У пациентов, принимающих хлорамфеникол или ингибиторы фолиевой кислоты, наблюдают дозозависимое угнетение функции костного мозга. При тяжёлых осложнениях вследствие лечения хлорамфениколом возникает апластическая анемия. Высокие дозы р-лактамных препаратов вызывают гранулоцитопению. Иногда при приёме антибиотиков развивается гемолитическая анемия. Большинство антибактериальных препаратов вызывают обратимую тромбоцитопению или угнетение функции костного мозга.
Мочевыводящая система при антибактериальной терапии. Нефротоксичность аминогликозидов обусловлена их способностью повреждать клетки проксимальных извитых канальцев почек. В группу риска входят пожилые пациенты, лица с заболеваниями почек, а также пациенты, принимающие помимо аминогликозидов другие нефротоксичные препараты (например, антибиотики тетрациклинового ряда).
Печень при антибактериальной терапии. Изониазид и рифампицин могут быть причиной развития гепатита, особенно если у пациентов ещё до приёма этих препаратов были заболевания печени. Другие препараты, связанные с развитием гепатита, — тетрациклины, эритромицин, пиразинамид, этионамид и реже ампициллин или фторхинолоны. Кроме того, при приёме тетрациклинов или высоких доз фузидовой кислоты возникает холестатическая желтуха.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Лечение гнойных и септических осложнений ранений: устранение очага инфекции, антибиотикотерапия
Лечение любого гнойно-септического осложнения является комплексным и включает в себя следующие мероприятия:
1) Устранение первичного очага инфекции хирургическим путем. Хирургическое вмешательство прекращает дальнейшее поступление микроорганизмов. Это может быть ушивание дефекта стенки полого органа, его резекция или удаление. После этого следует санация очага гнойной инфекции, которая заключается в механическом удалении гнойного экссудата, пропитанных гноем некротических тканей из серозных полостей, средостения и забрюшинного пространства. Заключительным этапом хирургического метода лечения является полноценное дренирование гнойного очага.
Наиболее эффективным мы считаем метод активного дренирования с аспирацией и промыванием, принципы и детали которого изложены ниже, в разделах, посвященных специфическим осложнениям ранений.
2) Устранение расстройств внешнего дыхания достигается:
— обогащением кислородом вдыхаемой смеси;
— ИВЛ с положительным давлением в конце выдоха;
— постоянной санацией трахеобронхиального дерева.
Для предупреждения пневмонии применяют аэрозольные ингаляции с антибиотиками, парокислородные ингаляции, муколитики, вибромассаж груди (при отсутствии противопоказаний).
3) Коррекция расстройств системного кровообращения достигается:
— устранением дефицита объема внеклеточной жидкости (кристаллоиды, коллоиды, альбумин, кровь, по показаниям — вазопрессоры);
— снижением вязкости циркулирующей крови.
При проведении инфузионно-трансфузиониой терапии нельзя допускать возникновения легочной артериальной гипертензии.
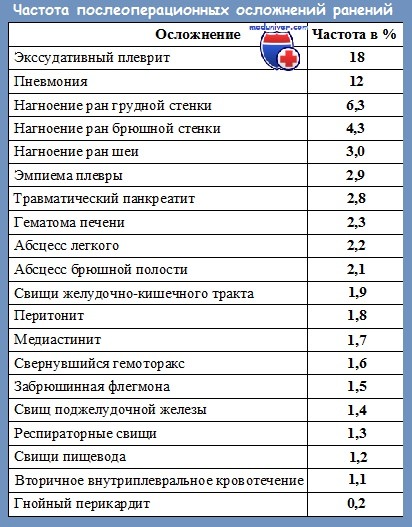
4) Антибактериальная терапия. На протяжении нескольких десятилетий при лечении гнойных осложнений применялась эскалационная (восходящая) методика антибактериальной терапии, когда при неэффективности препаратов первого ряда назначались более мощные антибиотики.
Так, в прошлом достаточно эффективным было применение амоксициллина или ампициллина с сульбактамом, цефалоспоринов второго поколения (цефуроксима, цефокситина), третьего (цефтриаксона, цефоперазона) или четвертого (цефенима) поколений, фторхинолонов (ципрофлоксацина, левофлоксацина).
Эти препараты обычно применяли в комбинации с аминогликозидами, ванкомицином и антиаэробными средствами (метронидазол, линкомицин, клиндамицин).
Такой подход был клинически и экономически оправдан в условиях низкого уровня резистентности микроорганизмов. Однако во второй половине 80-х и в 90-х годах XX в. отмечен повсеместный рост резистентности, обусловленный как неблагоприятными изменениями внешней среды обитания (экология, социальные условия, алкоголизм, наркомания), так и бесконтрольным употреблением антибиотиков.
В настоящее время устойчивость микроорганизмов объявлена угрозой для человечества в целом. В таких условиях для лечения гнойно-септических осложнений приходится применять деэскалационную методику, которая заключается в максимально раннем назначении массивных доз антибиотика, спектр действия которого максимально охватывает всех возможных возбудителей с последующим (при получении результатов микробиологического исследования) переходом па препараты более узкого спектра.
В этом плане наиболее эффективными в настоящее время являются антибиотики из группы карбоненемов. Несмотря на более чем 20-летнее использование, уровень устойчивости к ним клинически значимых возбудителей остается низким, возможно из-за их устойчивости к бета-лактамазам, выделяемым микроорганизмами для разрушения антибиотиков.
5) Интенсивное парентеральное и энтералъное питание. В первую очередь необходимо обеспечить введение аминокислот, вследствие их усиленного потребления для сохранения барьерной функции кишечника и клеток иммунной системы. Наиболее эффективными в этом смысле являются смеси для энтерального введения, содержащие омега-3 жирные кислоты, глютамин, аргинин, а также пектин.
6) Активные методы детоксикации. Среди методов экстракорпоральной детоксикации у пострадавших с множественными и сочетанными ранениями шеи, груди и живота, осложненными сепсисом, самым распространеным и хорошо изученным является плаз-маферез.
Положительный эффект плазмафереза основан на удалении высокомолекулярных белков острой фазы воспаления, а также нормализации реологических свойств крови. Метод позволяет быстро удалять из циркулирующей крови токсины (как водорастворимые, так и связанные с белками), свободный миоглобин, активированные компоненты свертывающей системы крови, С-реактивный белок, цитокины, комплемент, лизосомальные ферменты, аутоантитела, иммунные комплексы и просто обломки разрушенных клеток и клеток в состоянии апоптоза.
Метод существует в двух модификациях: прерывистый и непрерывный. Не останавливаясь на деталях этих модификаций, необходимо подчеркнуть, что у пострадавших в критическом состоянии используют непрерывную технологию, которая меньше оказывает отрицательное влияние на гемодинамику.
7) Торможение образования медиаторов воспалительной реакции. В настоящее время большие надежды возлагаются на восполнение дефицита селена — микроэлемента, входящего в состав фермента (глютатионпероксидазы), отвечающего за антиоксидантную систему защиты клеток. В частности, достаточное количество этого фермента обеспечивает преобразование свободных радикалов в спирты и таким образом сохраняет целость клеточной мембраны.
Препараты селена при лечении гнойно-септических осложнений применяются в виде пентагидрата селенита натрия. К сожалению, в настоящее время пока нет возможности четко определить закономерности в реакциях и взаимодействиях сотен различных медиаторов, а следовательно, и избирательную нейтрализацию активности циркулирующих в крови медиаторов, как воспалительных, так и противовоспалительных.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
М.Н. ЗУБКОВ, доктор медицинских наук, профессор, вице-президент Межрегиональной ассоциации клинической микробиологии и антимикробной химиотерапии (МАКМАХ). ПРОФИЛАКТИКА И ТЕРАПИЯ ХИРУРГИЧЕСКОЙ ИНФЕКЦИИ
Основная роль антибиотикопрофилактики в хирургии заключается в предупреждении инфекций, возникающих вследствие операции или других инвазивных вмешательств либо имеющих прямую связь с ними, а побочная цель - в уменьшении продолжительности и стоимости пребывания больного в стационаре.
Ее суть состоит в достижении эффективных концентраций антибиотика в операционной зоне во время ее микробного загрязнения и поддержании бактерицидного уровня препарата в течение всей операции и первых 3-4 часов после оперативного вмешательства, поскольку этот отрезок времени является решающим для размножения и адгезии на клетках хозяина попавших в рану микробов, что служит пусковым механизмом для начала инфекционно-воспалительного процесса в ране. Антибиотикопрофилактика, начатая по истечении этого периода, является запоздалой, а ее продолжение после окончания операции в большинстве случаев излишним, поскольку профилактическая роль антибиотика в основном заключается в уменьшении пороговой концентрации бактерий в ране и препятствии адгезии возбудителя.
Антибиотикопрофилактика показана там, где особенно высок риск развития послеоперационной инфекции (например, при "условно чистых" операциях на органах брюшной, грудной полости и малого таза, затрагивающих слизистые оболочки, населенные микрофлорой) или если ее последствия могут представлять угрозу здоровью и жизни больного (при некоторых "чистых" операциях, связанных с имплантацией сосудистых шунтов или искусственных протезов, когда немногочисленные и малопатогенные микроорганизмы с поверхности кожи могут проникнуть глубоко в рану и вызвать ее нагноение). Если хирург заранее уверен, что встретится с инфекцией в процессе операции (например, при "условно чистых" или "загрязненных" вмешательствах), в качестве антибактериальной защиты проводят превентивную антибиотикотерапию, которая должна быть ограничена самыми жесткими показаниями: патофизиологическими предпосылками (например, перфорация органов желудочно-кишечного тракта в результате проникающего ранения или имеющая эндогенное происхождение, сопровождающаяся загрязнением кишечной микрофлорой брюшной полости и прилегающих к ней структур); наличием входных ворот инфекции (например, открытые переломы); биологией потенциального возбудителя. Раннее назначение антибиотиков, обычно в течение 12 часов с момента перфорации или травмы, расценивается как профилактика, более позднее, когда развились признаки серьезной инфекции, - как лечение.
В большинстве случаев для профилактики послеоперационной инфекции достаточно одной дозы антибиотика (во время премедикации; вторая доза вводится при 3-часовых и более длительных операциях) либо проводят сверхкраткий курс антибиотикопрофилактики, ограниченный двумя-тремя дозами препарата. Такая тактика, основанная на многочисленных клинических и экспериментальных наблюдениях, вполне эффективна, снижает вероятность побочных действий антибиотика, ограничивает возможность развития устойчивости бактерий к химиопрепаратам, обеспечивает меньшую стоимость лечения. Профилактическое применение антибиотиков задолго до операции или более 48 часов в послеоперационном периоде ведет к нарушению биоценоза желудочно-кишечного тракта и колонизации верхних его отделов микрофлорой толстой кишки с возможным развитием эндогенной инфекции путем бактериальной транслокации условных патогенов через лимфатическую систему тонкого кишечника. Кроме того, возрастает опасность суперинфекции у оперированных больных за счет селекции антибиотикорезистентных штаммов. Поэтому антибиотик следует вводить больному в соответствующей дозе непосредственно перед операцией (за 10-15 мин. внутривенно во время наркоза либо за 40-60 мин. до операции внутримышечно) с последующими повторными инъекциями по показаниям, но не более 24-48 часов.
Для профилактики раневой инфекции чаще всего назначают цефалоспорины 1-го и 2-го поколения (препараты 3-го поколения существенно дороже и используются в основном для лечения), так как они имеют достаточный спектр бактерицидной активности против наиболее распространенных возбудителей послеоперационных осложнений, и прежде всего стафилококков; при парентеральном введении создают высокие концентрации в операционной зоне; отличаются малой токсичностью и частотой побочных действий. К числу недостатков всех цефалоспоринов следует отнести неэффективность при энтерококковой инфекции; плохое проникновение через гематоэнцефалический барьер (кроме цефтазидима и некоторых других препаратов 3-го поколения); возможное увеличение нефротоксичности в комбинации с аминогликозидами.
Помимо цефалоспоринов при высоком риске стафилококковой хирургической инфекции у ортопедических и некоторых других категорий больных применяют ванкомицин. При колоректальных операциях наряду с пероральным промыванием кишечника изотоническим раствором за сутки до операции больному назначают внутрь неомицин, 1 г + эритромицин, 1 г в 13, 14 и 22 ч., а в день операции - цефалоспорины 1-2-го поколения в/в дважды с интервалом 8 ч. При катаральном и флегмонозном аппендиците достаточно однократного применения в/в цефазолина (1 г) или цефуроксима (1,5 г) либо проведения короткого курса (2-3 дозы). При гангренозном аппендиците дополнительно вводят метронидазол, 0,5 г в/в. Если в послеоперационном периоде возникает подозрение на перитонит и/или абсцедирование, продолжают применение антибиотиков в течение 3-5 суток. Схемы профилактики при других видах операций приведены в таблице 1.
Таблица 1
ВАРИАНТЫ АНТИБИОТИКОПРОФИЛАКТИКИ (АП) РАНЕВОЙ ИНФЕКЦИИ ПРИ НЕКОТОРЫХ ВИДАХ ХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВ*
1 Первую дозу цефалоспорина вводят в/в во время вводного наркоза (за 10-15 мин. до разреза); при операциях > 3 ч антибиотик вводят повторно; при реконструктивных операциях на сосудах и нервных окончаниях АП продлевают до 2-3 сут.
2 До 3 дней, по показаниям.
3 В/в капельно в течение 1 часа.
4 Профилактика газовой гангрены.
5 АП не показана при катетеризации сердца.
6 О преимуществах нетилмицино см. в тексте.
7 Цефалоспорины 2-го поколения, активные против анаэробов.
8 При брюшном доступе повторяют по 1 г в/в через 8 ч и 16 ч.
Антибиотикопрофилактику считают неэффективной, если в области первичного операционного разреза возникла послеоперационная инфекция; если появилась необходимость дренирования операционной зоны; если в течение 4-недельного периода после первичной операции понадобилось не находящее объяснений применение антимикробных препаратов.
При уже развившейся хирургической инфекции на начальном этапе лечения назначение антибиотиков носит эмпирический характер до получения результатов бактериологического исследования материалов из раны. При этом выбор тактики химиотерапии зависит от характера хирургической патологии и локализации гнойно-воспалительного процесса, определяющих специфику раневой инфекции. Вполне естественно, что при перитонитах, где превалирует анаэробная флора в ассоциации с энтеробактериями, и при инфекциях костей и мягких тканей, где ведущую роль играют стафилококки, алгоритмы эмпирической антибиотикотерапии будут различными.
При травматических ранах с признаками нагноения назначают комбинированную терапию, учитывая лидирующее положение стафилококков и высокий удельный вес микробных ассоциаций (до 70%) при посттравматических инфекциях. Обычно используют гентамицин (4,5 мг/кг/сут) в сочетании с оксациллином (4-6 г/сут), цефазолином (3 г/сут) или линкомицином (1200-1800 мг/сут) при высоком риске развития анаэробной инфекции.
Состав микрофлоры при перитонитах
Стрептококки - 11%
Энтеробактерии - 24%
Стафилококки - 5%
Псевдомонады - 12%
Анаэробы - 48%
Состав микрофлоры при инфекциях костей и мягких тканей
Стрептококки - 7%
Энтеробактерии - 15%
Стафилококки - 60%
Псевдомонады - 8%
Анаэробы - 10%
Но особенно следует выделить антисинегнойную активность пиперациллина и тазоцина, что позволяет использовать их для лечения внутрибольничных инфекций в виде монотерапии (4 г/0,5 г тазоцина) или в комбинации с нетилмицином (4,5 г/кг/сут).
При острых интраабдоминальных инфекциях (80% из них возникает вне стационара), когда точная локализация неизвестна, лечение направляют против смешанной флоры кишечника, включающей факультативные грамотрицательные бактерии и часто встречающиеся анаэробы (Clostridium spp. и Bacteroides spp.). Одна из применяемых в настоящее время схем противоинфекционной терапии предусматривает комбинацию аминогликозида с антианаэробным препаратом (метронидазол или клиндамицин). Многие хирурги предпочитают добавлять ампициллин для воздействия на энтерококки. Назначение тазоцина по эффективности не уступает комбинированному препарату имипенем-циластатин. Широко используются также комбинации цефалоспоринов 3-го поколения с клиндамицином или метронидазолом. Парентеральную терапию продолжают до исчезновения лихорадки, снижения числа лейкоцитов крови (< 1200 в 1 мкл), восстановления функции кишечника (обычно примерно после недельного курса лечения).
Инфицирование послеоперационных ран относится к разряду внутрибольничных инфекций, где возможны разные варианты эмпирической антибиотикотерапии в зависимости от тяжести течения раневой инфекции и особенностей формирования резистентности бактерий к антибиотикам. При неосложненных инфекциях мягких тканей, как правило, обходятся монотерапией, в то время как осложненные инфекции, требующие повторных оперативных вмешательств и нередко приобретающие системный характер, чаще нуждаются в назначении антибиотиков более широкого спектра действия или проведении комбинированной антибиотикотерапии.
При лечении тяжелых и жизнеугрожающих инфекций препаратами выбора становятся аминогликозиды, спектр действия которых охватывает подавляющее большинство аэробных грам(-) и грам(+) бактерий (за исключением стрептококков и пневмококков), а в комбинации с пенициллином они оказывают синергическое бактерицидное действие на энтерококки. Однако, несмотря на их активность против Staphylococcus spp., аминогликозиды не следует применять в качестве стартовой монотерапии при стафилококковой инфекции. Гентамицин наиболее широко применяется в практике, однако имеется много свидетельств о высоком удельном весе резистентных к нему микробных изолятов от стационарных больных, что снижает эффективность лечения хирургической инфекции. Наиболее активным среди аминогликозидов является нетилмицин (нетромицин), который, по нашим данным, превосходит другие антибиотики этой группы и некоторые цефалоспорины 3-го поколения и сопоставим по антимикробной эффективности лишь с фторхинолонами (см. табл. 2). У него наименее выражен ото- и нефротоксический эффект, что позволяет вводить суточную дозу препарата однократно без увеличения частоты побочных осложнений. Такой режим введения существенно увеличивает ударное антимикробное действие нетилмицина и имеет экономические преимущества. По стоимости он гораздо доступнее амикацина и, по нашему опыту, должен занять первостепенное положение среди аминогликозидов в лечении оппортунистических инфекций.
Таблица 2
АНТИБИОТИКОЧУВСТВИТЕЛЬНОСТЬ ГРАМ(-) БАКТЕРИЙ ПРИ ИНФЕКЦИЯХ КОСТЕЙ И МЯГКИХ ТКАНЕЙ (%)
| Антибиотики | E.col (n=28) | KES* (n=48) | Proteus spp. (n=22) | P.aeruginoza (n=37) | Acinetobacter (n=19) |
| Нетромицин | 100 | 90 | 73 | 74 | 88 |
| Амикацин | 75 | 40 | 57 | 67 | 75 |
| Тобрамицин | 58 | 34 | 22 | 63 | 43 |
| Гентамицин | 50 | 36 | 30 | 58 | 27 |
| Цефтазидим | 83 | 40 | 70 | 57 | 40 |
| Ципрофлоксацин | 100 | 88 | 79 | 83 | 80 |
Нельзя обойти вниманием и фторхинолоны, которые все чаще становятся препаратами выбора при системных инфекциях. Среди них ципрофлоксацин (ципробай, ципринол) занял прочное место в хирургической практике, в то время как другие препараты этой группы чаще используются для лечения больных терапевтического профиля. Наличие инфузионной формы препарата существенно повышает его конкурентоспособность при лечении больных в реанимационных отделениях, а возможность проведения так называемой ступенчатой терапии с переходом на пероральный прием антибиотика (без существенного снижения его концентрации в крови из-за высокой биоусвояемости при всасывании) значительно снижает стоимость курса лечения. Область применения ципрофлоксацина в хирургии с одинаковым успехом распространяется на инфекции костей и мягких тканей, интраабдоминальные инфекции, инфекции органов грудной полости и малого таза и, конечно, при лечении сепсиса.
Таким образом, применение антибиотиков в хирургии с профилактической и лечебной целью имеет свои особенности, а знание спектра возбудителей хирургических инфекций и антимикробного действия химиопрепаратов является основой правильного их применения в клинике.
Читайте также:

