Антитела резус фактор и вич
Обновлено: 18.04.2024
Это выявление антител к специфическому белку, находящемуся на поверхности эритроцитов, – резус-фактору. Данные антитела являются одной из основных причин гемолитической болезни новорождённых.
Синонимы русские
Титр антирезусных антител, непрямая реакция Кумбса.
Синонимы английские
Anti Rh, Rh Typing.
Метод исследования
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Резус-фактор (Rh) передается по наследству, это белок на поверхности эритроцитов. Те люди, у которых он есть (а это большинство, около 85 %), называются резус-положительными. Однако у некоторых, резус-отрицательных, этот белок отсутствует. Отрицательный резус никак не влияет на здоровье самого человека. Однако у матери и ребенка, которого она вынашивает, могут возникнуть проблемы, если у них разные резус-факторы или если у матери развиваются антитела, которые реагируют с факторами клеток крови ребенка. Наиболее распространенный пример: женщина с негативным резус-фактором (Rh-) беременна ребенком с положительным резус-фактором (Rh+). Иммунная система этой женщины может выработать антитела против резус-положительного фактора крови ее ребенка. Несмотря на это первенец довольно редко бывает больным, потому что материнский иммунитет не вступает в контакт с кровью ребенка до самых родов. Однако антитела, выработанные при первой беременности, могут свободно проникать через плаценту при следующих беременностях и таким образом создавать проблемы резус-положительному ребенку.
Для чего используется исследование?
Анализ на антирезусные антитела применяется главным образом для обнаружения антител на резус-фактор. Резус-отрицательная мать и резус-положительный отец могут зачать Rh+ ребенка, при этом есть вероятность, что некоторые эритроциты крови ребенка попадут в кровяное русло матери во время беременности и родов. В ответ на чужеродные эритроциты Rh+ организм матери вырабатывает антирезусные антитела. Они представляют собой угрозу для будущих детей этой матери. Каждая женщина до наступления беременности либо во время нее должна сдать анализ на резус-фактор. Он поможет определить, является ли ее кровь резус-отрицательной, а также выяснить, приобрела ли резус-отрицательная женщина антитела против эритроцитов Rh+. Беременная женщина, организм которой еще не образовал антирезусные антитела, для предотвращения их появления может воспользоваться инъекциями иммуноглобулина. Резус-отрицательной женщине при беременности следует пройти дополнительное лечение иммуноглобулинами сразу после любой ситуации, когда кровь плода могла попасть в ее кровяное русло. Анализ на антирезусные антитела помогает выявлять эти процессы и вовремя назначать и корректировать лечение для предотвращения резус-конфликта.
Когда назначается исследование?
- При необходимости назначить лечение иммуноглобулиновыми инъекциями беременной женщине с отрицательным резус-фактором.
- В случае когда эритроциты плода могли попасть в кровяное русло беременной с резус-отрицательным фактором, если у нее были выкидыши, внематочная беременность, искусственные роды или аборты, пункция плодного пузыря, травмы живота, искусственное изменение положения плода.
- Анализ может быть назначен женщине с отрицательным резус-фактором, родившей ребенка с положительным резусом и прошедшей лечение инъекциями иммуноглобулинов, для того чтобы определить, есть ли у него антитела против эритроцитов Rh+.
Что означают результаты?
Референсные значения: отрицательно.
- Антитела обнаружены, есть вероятность резус-конфликта.
- Антитела не обнаружены, вероятность резус-конфликта низкая.
Правильно проведенное лечение анти-D-гамма-глобулинами препятствует образованию антирезусных антител практически у всех беременных женщин с отрицательным резус-фактором. Однако такая профилактика не действует, если у женщины уже образовались антирезусные антитела.
Кандидат биологических наук А. ЛУШНИКОВА. По материалам "Scientific American".
Вирус иммунодефицита человека (ВИЧ) открыли в 1983 году сразу в двух лабораториях: в Институте Пастера во Франции, под руководством Люка Монтанье, и в Национальном институте рака (США), Роберт Галло и его сотрудники. Сейчас уже ни у кого нет сомнений в том, что ВИЧ вызывает страшную болезнь, "чуму ХХ века" - СПИД (это название расшифровывается как "синдром приобретенного иммунодефицита"). Однако за более чем десятилетнюю историю исследований накопилось немало загадок, связанных с развитием этого заболевания. Например, у некоторых зараженных вирусом иммунодефицита людей признаки болезни появляются спустя несколько лет или не появляются вовсе. Оказалось, что существуют люди, устойчивые к СПИДу. Как много таких людей, какими особенностями они обладают, не есть ли это ключ к лечению страшной болезни? На эти вопросы пытается ответить публикуемая статья.
Так устроен вирус иммунодефицита человека. Внутри него находится наследственный материал - две молекулы РНК, на поверхности - белки оболочки.
У человека с обычным иммунитетом клетки-киллеры, несущие на своей поверхности молекулу-рецептор СD8, выделяют гормоноподобные вещества хемокины.
Если человек имеет нормальный ген ССR5, то под контролем этого гена в клетках-мишенях вырабатывается белок, который совместно с другим белком (СD4) служит "посадочной площадкой" для вируса иммунодефицита на поверхности клетки.
Иголка в стоге сена
Генетикам давно известны гены устойчивости к некоторым вирусам у мышей, например к вирусу лейкоза. Но существуют ли подобные гены у человека, и если да, то какова их роль в защите против СПИДа?
Стивен О'Брайн и Михаэль Дин со своими коллегами из Национального института рака США много лет вели поиск таких генов у человека.
В начале 80-х годов американские ученые исследовали множество людей, которые по тем или иным причинам могли заразиться вирусом иммунодефицита. Они проанализировали тысячи образцов крови и обнаружили, казалось бы, необъяснимое явление: у 10-25% обследованных вирус вообще не выявляется, а около 1% носителей ВИЧ - относительно здоровы, признаки СПИДа у них либо отсутствуют, либо выражены очень слабо, а иммунная система в полном порядке. Неужели существует какая-то устойчивость к вирусу у некоторых людей? И если да, то с чем она связана?
Опыты на лабораторных мышах, крысах, морских свинках и кроликах показали, что устойчивость к различным вирусным инфекциям часто определяется целым набором генов. Оказалось, что сходный механизм определяет и устойчивость к вирусу иммунодефицита человека.
Известно, что многие гены ответственны за выработку определенных белков. Часто бывает, что один и тот же ген существует в нескольких измененных вариантах. Такие "многоликие" гены называются полиморфными, а их варианты могут отвечать за выработку различных белков, которые по-разному ведут себя в клетке.
Сравнив восприимчивость к вирусам у мышей, несущих множество разнообразных наборов генов, и у мышей с небольшим числом генных вариантов, ученые пришли к выводу, что чем разнороднее генетически были животные, тем реже они заражались вирусом. В таком случае можно предположить, что в генетически разнообразных человеческих популяциях генные варианты, определяющие устойчивость к ВИЧ, должны встречаться достаточно часто. Анализ заболеваемости СПИДом среди американцев различных национальностей выявил еще одну особенность: более устойчивы американцы европейского происхождения, у африканцев и азиатов устойчивость близка к нулю. Чем объяснить такие различия?
Ответ на этот вопрос предложил в середине 80-х годов американский вирусолог Джей Леви из Калифорнийского университета в Сан-Франциско. Леви и его коллеги пытались выяснить, какие именно клетки в организме поражает вирус. Они обнаружили, что после того, как вирус заражает иммунные клетки, они легко узнаются иммунными клетками другого типа, так называемыми Т-киллерами (убийцами). Киллеры разрушают зараженные вирусом клетки, препятствуя дальнейшему размножению вируса. Клетки-убийцы несут на своей поверхности особую молекулу - рецептор CD8. Она, как принимающая антенна, "узнает" сигналы от клеток, зараженных вирусом, и клетки-убийцы уничтожают их. Если из крови удалить все клетки, несущие молекулу CD8, то вскоре в организме обнаруживаются многочисленные вирусные частицы, происходит быстрое размножение вируса и разрушение лимфоцитов. Не в этом ли ключ к разгадке?
В 1995 году группа американских ученых под руководством Р. Галло обнаружила вещества, которые вырабатываются в клетках-киллерах, несущих молекулы CD8, и подавляют размножение ВИЧ. Защитные вещества оказались гормоноподобными молекулами, называемыми хемокинами. Это небольшие белки, которые прикрепляются к молекулам-рецепторам на поверхности иммунных клеток, когда клетки направляются к месту воспаления или заражения. Оставалось найти "ворота", сквозь которые проникают в иммунные клетки вирусные частицы, то есть понять, с какими именно рецепторами взаимодействуют хемокины.
Ахиллесова пята иммунных клеток
Вскоре после открытия хемокинов Эдвард Бергер, биохимик из Национального института аллергических и инфекционных болезней в Бетезде, США, обнаружил в иммунных клетках, в первую очередь поражаемых вирусом (их называют клетки-мишени), сложный по строению белок. Этот белок как бы пронизывает мембраны клеток и содействует "посадке" и слиянию вирусных частиц с оболочкой иммунных клеток. Бергер назвал этот белок "фузин", от английского слова fusion - слияние. Оказалось, что фузин родствен белкам-рецепторам хемокинов. Не служит ли этот белок "входными воротами" иммунных клеток, через которые вирус проникает внутрь? В таком случае взаимодействие с фузином какого-нибудь другого вещества закроет доступ вирусным частицам в клетку: представьте, что в скважину замка вставляется ключ, и вирусная "лазейка" исчезает. Казалось бы, все встало на свои места, и взаимосвязь хемокины - фузин - ВИЧ уже не вызывала сомнений. Но верна ли эта схема для всех типов клеток, зараженных вирусом?
Пока молекулярные биологи распутывали сложный клубок событий, происходящих на поверхности клеток, генетики продолжали поиск генов устойчивости к вирусу иммунодефицита у людей. Американские исследователи из Национального института рака получили культуры клеток крови и различных тканей от сотен пациентов, зараженных ВИЧ. Из этих клеток выделили ДНК для поиска генов устойчивости.
Чтобы понять, насколько сложна эта задача, достаточно вспомнить, что в хромосомах человека содержится около 100 тысяч различных генов. Проверка хотя бы сотой доли этих генов потребовала бы нескольких лет напряженной работы. Круг генов-кандидатов заметно сузился, когда ученые сосредоточили свое внимание на клетках, которые прежде всего поражает вирус, - так называемых клетках-мишенях.
Уравнение со многими неизвестными
Одна из особенностей вируса иммунодефицита заключается в том, что его гены внедряются в наследственное вещество зараженной клетки и "затаиваются" там на время. Пока эта клетка растет и размножается, вирусные гены воспроизводятся вместе с собственными генами клетки. Затем они попадают в дочерние клетки и заражают их.
Из множества людей с высоким риском заражения ВИЧ отобрали зараженных вирусом и тех, кто не стал носителем ВИЧ, несмотря на постоянные контакты с больными. Среди зараженных выделили группы относительно здоровых и людей с быстро развивающимися признаками СПИДа, которые страдали сопутствующими заболеваниями: пневмонией, раком кожи и другими. Ученые изучили разные варианты взаимодействия вируса с организмом человека. Различный исход этого взаимодействия, по-видимому, зависел от набора генов у обследованных людей.
Выяснилось, что люди, устойчивые к СПИДу, имеют мутантные, измененные гены рецептора хемокинов - молекулы, к которой прикрепляется вирус, чтобы проникнуть в иммунную клетку. У них контакт иммунной клетки с вирусом невозможен, поскольку нет "принимающего устройства".
В это же время бельгийские ученые Михаэль Симпсон и Марк Парментье выделили ген другого рецептора. Им оказался белок, который также служит рецептором для связывания ВИЧ на поверхности иммунных клеток. Только взаимодействие этих двух молекул-рецепторов на поверхности иммунной клетки создает "посадочную площадку" для вируса.
Итак, основными "виновниками" заражения клеток вирусом иммунодефицита служат молекулы-рецепторы, названные CCR5 и CD4. Возник вопрос: что происходит с этими рецепторами при устойчивости к ВИЧ?
В июле 1996 года американская исследовательница Мэри Керингтон из Института рака сообщила, что нормальный ген рецептора ССR5 обнаруживается лишь у 1/5 обследованных ею пациентов. Дальнейший поиск вариантов этого гена среди двух тысяч больных дал удивительные результаты. Оказалось, что у 3% людей, не заразившихся вирусом, несмотря на контакты с больными, ген рецептора ССR5 измененный, мутантный. Например, при обследовании двух нью-йоркских гомосексуалистов - здоровых, несмотря на контакты с зараженными, выяснилось, что в их клетках образуется мутантный белок CCR5, не способный взаимодействовать с вирусными частицами. Подобные генетические варианты были найдены лишь у американцев европейского происхождения или у выходцев из западной Азии, у американцев же африканского и восточноазиатского происхождения не нашли "защитных" генов.
Оказалось также, что устойчивость некоторых пациентов к инфекции лишь временная, если они получили "спасительную" мутацию только от одного из своих родителей. Через несколько лет после заражения количество иммунных клеток в крови таких пациентов снижалось в 5 раз, и на этом фоне развивались сопутствующие СПИДу осложнения. Таким образом, неуязвимыми для ВИЧ были только носители сразу двух мутантных генов.
Но у обладателей одного мутантного гена признаки СПИДа все же развивались медленнее, чем у носителей двух нормальных генов, и такие больные лучше поддавались лечению.
Продолжение следует
Не так давно исследователи обнаружили разновидности чрезвычайно агрессивных вирусов. Людей, зараженных такими вирусами, не спасает даже присутствие двух мутантных генов, обеспечивающих устойчивость к ВИЧ.
Это заставляет продолжать поиск генов устойчивости к ВИЧ. Недавно американские исследователи О'Брайн и М. Дин с коллегами обнаружили ген, который, присутствуя у людей лишь в одной копии, задерживает развитие СПИДа на 2-3 года и более. Значит ли это, что появилось новое оружие в борьбе с вирусом, вызывающим СПИД? Скорее всего, ученые приоткрыли еще одну завесу над загадками ВИЧ, и это поможет медикам в поисках средств лечения "чумы ХХ века". В многочисленных популяциях американцев афро-азиатского происхождения мутантные гены так и не найдены, но тем не менее есть небольшие группы здоровых людей, контактировавших с зараженными. Это говорит о существовании других генов защиты иммунной системы от страшной инфекции. Пока можно лишь предполагать, что в различных популяциях человека сложились свои системы генетической защиты. По-видимому, и для других инфекционных заболеваний, включая вирусный гепатит, также имеются гены устойчивости к вирусам-возбудителям. Теперь уже никто из генетиков не сомневается в существовании таких генов для вируса иммунодефицита. Исследования последних лет дали надежду найти решение такой, казалось бы, неразрешимой проблемы, как борьба со СПИДом. Кто станет победителем в противоборстве ВИЧ - человек, покажет будущее.
Наука - здравоохранению
КАК ЛЕЧИТЬ СПИД. ПОИСК СТРАТЕГИИ
Результаты исследований последних лет заставили задуматься не только ученых и практических врачей, занимающихся проблемами СПИДа, но и фармацевтов. Раньше основное внимание уделялось комбинированному лечению инфекции, направленному против вируса. Применялись препараты, препятствующие размножению вируса в клетке: невипарин и атевирдин. Это так называемая группа ингибиторов обратной транскриптазы ВИЧ, которые не дают наследственному материалу вируса внедряться в ДНК иммунных клеток. Их сочетают с аналогами нуклеозидов типа зидовудина, диданозина и ставудина, которые облегчают течение болезни. Однако эти средства токсичны и обладают побочными действиями на организм, поэтому их нельзя считать оптимальными. Им на смену все чаще приходят более совершенные средства воздействия на ВИЧ.
В последнее время появилась возможность препятствовать "посадке" вирусных частиц на поверхность клеток. Известно, что этот процесс происходит за счет связывания вирусного белка gр120 с клеточными рецепторами. Искусственное блокирование мест связывания ВИЧ с помощью хемокинов должно защищать клетки от вторжения ВИЧ. Для этого нужно разработать специальные препараты-блокаторы.
Другой путь - получение антител, которые будут связываться с рецепторами ССR5, создающими "посадочную площадку". Такие антитела будут препятствовать взаимодействию этих рецепторов с вирусом, не давая доступа ВИЧ в клетки. Кроме того, можно вводить в организм фрагменты молекул ССR5. В ответ на это иммунная система начнет вырабатывать антитела к данному белку, которые также перекроют доступ к нему вирусных частиц.
Наиболее дорогостоящий способ обезопасить вирусные частицы - ввести в иммунные клетки новые мутантные гены. В результате сборка рецептора для "посадки" вируса на поверхности "оперированных" клеток прекратится, и вирусные частицы не смогут заразить такие клетки. Подобная защищающая терапия, по-видимому, наиболее перспективна при лечении больных СПИДом, хотя и весьма дорого стоит.
При лечении сопровождающих СПИД раковых заболеваний врачи чаще всего прибегают к высоким дозам химических препаратов и к облучению опухолей, что нарушает кроветворение и требует пересадки больным здорового костного мозга. А что, если в качестве донорских кроветворных клеток пересадить больному костный мозг, взятый от людей, генетически устойчивых к инфекции ВИЧ? Можно предположить, что после такой пересадки распространение вируса в организме пациента будет остановлено: ведь донорские клетки устойчивы к инфекции, поскольку не имеют рецепторов, позволяющих вирусу проникнуть через клеточную мембрану. Однако эту привлекательную идею вряд ли удастся воплотить в практику полностью. Дело в том, что иммунологические различия между пациентом и донором, как правило, приводят к отторжению пересаженной ткани, а иногда и к более серьезным последствиям, когда донорские клетки атакуют чужеродные для них клетки реципиента, вызывая их массовую гибель.
Т-киллеры - иммунные клетки, которые уничтожают зараженные вирусом клетки.
Рецепторы клеток - особые молекулы на поверхности, которые служат "опознавательным знаком" для вирусных частиц и других клеток.
Ген рецептора - ген, ответственный за выработку соответствующего белка.
Хемокины - гормоноподобные вещества на поверхности иммунных клеток, которые подавляют размножение вируса в организме.
Культура клеток - клетки, развивающиеся вне организма, в питательной среде пробирки.
Мутантные гены - измененные гены, не способные контролировать выработку нужного белка.
Клетки-мишени - иммунные клетки, которые в первую очередь поражает вирус.
Цифры и факты
- Сегодня в мире 29 миллионов зараженных вирусом иммунодефицита. 1,5 миллиона человек уже умерли от вызванного этим заражением СПИДа.
- Самый неблагополучный по СПИДу регион - Африка. В Европе лидируют Испания, Италия, Франция, Германия. С 1997 года к этим странам присоединилась Россия. На территории бывшего СССР зараженность ВИЧ распределяется так: 70% - Украина, 18,2% - Россия, 5,4% - Беларусь, 1,9% - Молдова, 1,3% - Казахстан, остальные - менее 0,5%.
- В России и странах ближнего зарубежья существует более 80 центров по профилактике и борьбе со СПИДом.
Читайте в любое время
У человека с обычным иммунитетом клетки-киллеры, несущие на своей поверхности молекулу-рецептор СD8, выделяют гормоноподобные вещества хемокины. Хемокины взаимодействуют с другими иммунными клетками-мишенями, которые в первую очередь заражает вирус иммунодефицита. Хемокины связываются с белком фузином на поверхности клеток-мишеней и тем самым закрывают доступ в клетку вирусным частицам. Те же клетки, которые вирус все-таки заразил, уничтожаются киллерами. Если клеток-киллеров с молекулой СD8 у человека не очень много, он все же заражается вирусом.
Если человек имеет нормальный ген ССR5, то под контролем этого гена в клетках-мишенях вырабатывается белок, который совместно с другим белком (СD4) служит "посадочной площадкой" для вируса иммунодефицита на поверхности клетки. Если же ген ССR5 мутантный, то взаимодействия с вирусом не происходит, и, несмотря на контакт с вирусом, человек остается здоровым.
Оформите заявку на сайте, мы свяжемся с вами в ближайшее время и ответим на все интересующие вопросы.
ВИЧ – инфекционное заболевание, при котором поражается иммунная система человека. Патология вызвана вирусом иммунодефицита человека, который разрушает иммунные клетки. В результате снижается способность организма противостоять инфекционным заболеваниям и онкопроцессам.
Вирус в окружающей среде
ВИЧ — вирус нестойкий, он погибает вне среды человеческого организма при высыхании содержащих его жидкостей и практически моментально погибает при температуре выше 56ºС.
При воздействии солнечных лучей.
В щелочной и кислой среде. Женщины, имеющие здоровую микрофлору половых органов с повышенной кислотностью, заражаются реже.
От высоких температур. На поверхности предметов в условиях умеренной температуры ВИЧ может жить до 2 часов. Однако при нагревании свыше 60 градусов погибает за 1-2 минуты. При кипячении – моментально. При дезинфекции.
От действия хлора. То же действие вызывает 6% перекись водорода, убивает патоген и 70% этиловый спирт.
Дольше всего ВИЧ сохраняется в крови человека. Высохшая капля крови содержит в себе активный вирус на протяжении 2-3 суток в нормальных условиях окружающей среды. Другие жидкости на предметах могут сохранять инфекцию 2-3 суток. Чем ниже температура окружающей среды, тем дольше живёт микроорганизм.
Пути инфицирования ВИЧ
Незащищенный проникающий сексуальный контакт – анальный или вагинальный.
Совместное использование нестерильного оборудования для инъекций.
Совместное использование нестерильного оборудования для татуировок и пирсинга.
От ВИЧ-инфицированной матери ребенку (возможно инфицирование во время беременности, родов и при кормлении грудью).
Заболевание не передается бытовым путем, так как вирус не способен передвигаться в окружающей среде и быстро погибает. Также невозможно заразиться через рукопожатие или объятие. Риск передачи вируса через слюну ничтожно мал, для этого два партнёра с ранками на слизистой оболочке рта должны довольно долго целоваться. При этом у носителя должно быть большое количество вируса в крови.
Классификация заболевания
Различают 2 основных типа возбудителя ВИЧ-1 и ВИЧ-2. Оба приводят к постепенному снижению иммунитета, но ВИЧ-2 менее патогенен. Для него характерно меньшее число вирусных частиц на микролитр крови, поэтому передаётся он реже и не так часто приводит к СПИДу.
Основные стадии заболевания
Инкубационная – происходит заражение и последующее размножение вируса в крови. Она длится до шести недель, иногда меньше. Даже будучи зараженным, на этом этапе человек не увидит явных признаков, а анализ крови не покажет, что в крови есть антитела.
Первичная – могут появиться первые признаки инфекции. Длится вторая стадия в течение 3 недель – в это время появляются антитела, вирус определяется лабораторно.
Субклиническая. Появляется первый признак болезни – увеличенные лимфоузлы. Пациент чувствует себя полностью здоровым, на самочувствие не жалуется. Могут появляться вторичные заболевания: от частых простуд до кандидоза и пневмонии.
Терминальная – предполагает быстрое и прогрессирующее истощение, а также последующую смерть больного.
Симптомы развития ВИЧ-инфекции в организме
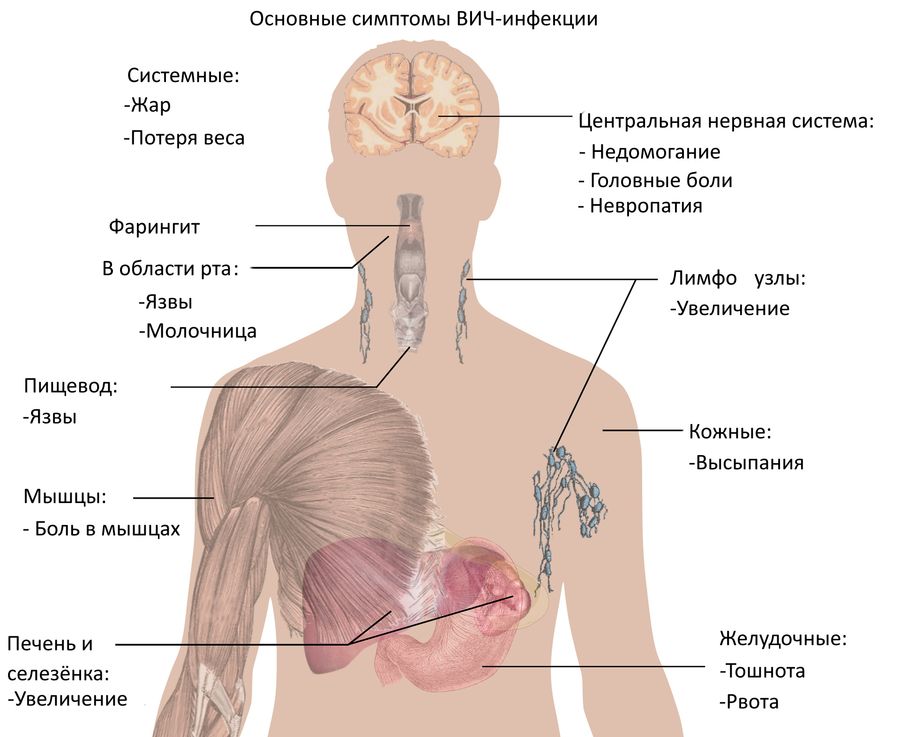
ВИЧ-инфекция течет медленно и почти бессимптомно. В течение многих лет (от 5 до 15 лет) она может никак не тревожить человека. Бывает и так, что первые признаки могут появиться на ранней стадии, а затем исчезнуть и больше не беспокоить носителя инфекции на протяжении длительного времени.
Также первые симптомы ВИЧ легко спутать с признаками других заболеваний, что может вводить в заблуждение.
На первом этапе:
боль в горле, повышение температуры
болезненность кожи, суставов, костей
одновременно увеличиваются шейные лимфоузлы
могут проявляться высыпания на коже разного рода
Новые признаки ВИЧ возвращаются через несколько лет спокойной и здоровой жизни. К ним относятся:
сильная усталость, быстрая утомляемость
увеличение лимфоузлов – не только шейных, а уже нескольких групп
снижение веса. Обычно оно выглядит беспричинным, человек не понимает, в чем дело
лихорадка, озноб, потливость (преимущественно ночная)
проблемы с ЖКТ – обычно проявляются жидким стулом без видимых на то причин
Чем опасна патология?
Болезнь опасна, в первую очередь, для заразившегося. Попадая в кровь, патоген постепенно уничтожает клетки иммунитета. Этот процесс можно замедлить с помощью антиретровирусной терапии, но полностью остановить нельзя. В результате этого организм не может противостоять инфекциям извне.
Чаще всего у пациентов развивается молочница, стоматит, длительная диарея, частые ОРВИ и т. д. Чем меньше иммунных клеток в организме человека, тем в последующем появляются более опасные заболевания, среди которых туберкулёз, онкология, поражения периферической нервной системы, саркома Капоши и другие.
Инфекция может проявлять себя абсолютно на всех органах и системах, часто заболевания совмещаются. При должном лечении эти болезни можно вылечить и поддерживать приемлемый уровень жизни пациента.
Главная опасность – это СПИД – последняя стадия ВИЧ заболевания. Средняя продолжительность жизни на этой стадии – до 9 месяцев. Хотя при положительном психологическом состоянии и должной терапии пациент может прожить ещё до 3 лет.
Методы диагностики патологии
Сегодня применяются специальные высокоточные тесты, которые способны обнаружить оба вируса и антитела к ним, в том числе и в латентном течении.
Наличие ВИЧ в организме человека определяется по присутствию антител в крови. Для этого у пациента берут кровь на ВИЧ из вены. Этот анализ позволяет решить 3 задачи:
определить присутствие вируса в крови и начать лечение на ранних стадиях
выявить стадию болезни и спрогнозировать ее течение
контролировать результативность терапии
Обнаружить заболевание можно с помощью:
Полимеразной цепной реакции (ПЦР) – высокоточный метод молекулярно-генетической диагностики, который позволяет выявить у человека инфекционные и наследственные заболевания.
Диагностика этим методом позволяет найти возбудителя непосредственно в гене, который содержится в исследуемых материалах. Это самый точный анализ на половые инфекции, скрытые инфекции, различные венерические заболевания.
Метод прекрасен тем, что обладает высокой чувствительностью. Возможно выявить возбудителя болезни даже при наличии нескольких молекул его ДНК, то есть на очень ранних стадиях. Что позволяет вовремя вылечить заболевание.
ИФА (иммуноферментный анализ), который определяет антитела к обеим разновидностям вируса (ВИЧ 1 и 2). Достоверность метода составляет до 98%. При положительном результате анализ делают повторно или проводят дополнительный анализ методом иммуноблота.
Ложноположительные результаты возможны при беременности, аутоиммунных заболеваниях, гепатите или даже гриппе.
Как лечится ВИЧ?
Необходимо как можно скорее после обнаружения в организме следов вируса начать антиретровирусную терапию (сокращенно АРВТ или АРТ).
Антиретровирусная терапия — это комбинация из 3-4 препаратов, которые блокируют размножение ВИЧ на разных этапах. Вследствие ее применения вирус иммунодефицита человека перестает размножаться.
Пока АРТ не способна полностью вылечить ВИЧ-инфекцию, однако в состоянии не просто продлить жизнь ВИЧ-инфицированного человека, но и повысить ее качество.
Не менее важен образ жизни пациента, ему показан эмоциональный покой, правильное питание, профилактика инфекционных заболеваний. Также для качественного лечения важно вовремя проходить осмотр и сдавать анализы.
Какие меры профилактики нужно применять?

Так как основной способ передачи вируса – половым путем, следует заниматься только защищенным проникающим сексом. Иначе увеличивается риск заражения ВИЧ.
Кроме того, необходимо:
использовать только личные средства гигиены (зубная щётка, бритва, маникюрные принадлежности и т. д.)
проверять дезинфекцию инструментов в косметическом и медицинском кабинете, тату-салоне и во время других услуг, где можно повредить кожу
парам – совместно сдавать анализы 2 раза в год
зависимым от инъекционных наркотиков – использовать новый шприц или только свой
Комплексное скрининговое экспресс-исследование на гепатиты B и C, ВИЧ-инфекцию 1-го и 2-го типов и сифилис, обязательное для госпитализации, оформления санитарной книжки, постановки на учет по беременности, постановки на воинский учет, получения разрешения на работу и пр.
Синонимы русские
Гепатит С, антитела + гепатит B, антиген, австралийский антиген + ВИЧ 1 и 2, антитела и антиген p24 + сифилис (бледная трепонема), антитела.
Синонимы английские
Anti-HCV + HBsAg, Hepatitis B Surface Antigen + HIV 1,2 Ag/Ab Combo,HIV 1,2 Abs, p24 antigen + Treponema pallidum Abs.
Метод исследования
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Исследование предназначено для скрининга гепатитов B и C, ВИЧ-инфекции 1 и 2 типов и сифилиса. Так как это экспресс-тест, результаты будут получены в кратчайшие сроки.
Для скрининга гепатита B в анализе крови определяют один из антигенов этого вируса – HBsAg. Он входит в состав оболочки вируса и является самым ранним маркером активной инфекции. HBsAg обычно появляется в крови через 2-8 недель после заражения. Этот антиген может быть обнаружен как при остром, так и при хроническом гепатите В. Он не определяется при разрешении острой инфекции гепатита В и после вакцинации. Следует подчеркнуть, что HBsAg также не обнаруживается в период "серологического окна". Более того, в некоторых случаях инфекция гепатита носит латентный характер, при этом вирус сохраняется в ткани печени (о чем свидетельствует положительный результат анализа на ДНК вируса), однако HBsAg в крови не выявляется. Таким образом, HBsAg – это чувствительный, но не абсолютный маркер для исключения гепатита В. Присутствие HBsAg в крови более 6 месяцев служит одним из критериев диагностики хронического гепатита В. При выявлении HBsAg в крови проводят дополнительные, подтверждающие тесты для уточнения диагноза вирусного гепатита В.
Для скрининга гепатита C в анализе крови определяют IgG-антитела к этому вирусу. Anti-HCV могут быть обнаружены как при текущей инфекции (острой или хронической), так и при разрешении острого гепатита C. Таким образом, анализ на Anti-HCV не позволяет дифференцировать острый и хронический гепатит и гепатит C в анамнезе. При выявлении Anti-HCV в крови проводят дополнительные, подтверждающие тесты для уточнения диагноза вирусного гепатита С.
Анализ на ВИЧ (вирус, вызывающий СПИД), или, точнее, скрининг ВИЧ-инфекции 1-го и 2-го типа осуществляется с помощью определения антител к этому вирусу и антигена p24. Анализ на антитела к вирусу характеризуется очень высокой чувствительностью (> 99,5 %). Специфичность такого анализа ниже: ложноположительный результат может наблюдаться при наличии в крови пациента аутоантител, заболеваниях печени, недавней вакцинации против вируса гриппа и при наличии другой острой вирусной инфекции. По этой причине при получении положительного результата проводят дополнительный, подтверждающий анализ. Также для получения более точной информации о ВИЧ-статусе пациента анализ на антитела к ВИЧ дополняют анализом на антиген p24 – один из структурных белков вирусного капсида, являющийся ранним маркером острой ВИЧ-инфекции. Анализ на p24 может быть особенно полезным на ранних стадиях инфекции, когда титр антител к вирусу еще не достиг определяемого уровня. Следует отметить, что при выработке достаточного количества антител к ВИЧ (в том числе и к p24) этот антиген может больше не определяться. Специфичность анализа на p24 достигает 100 %, а его чувствительность – 30-50 %. Комбинация двух тестов для определения ВИЧ (антитела и антиген p24) позволяет достичь 100 % чувствительности и специфичности.
При анализе крови на сифилис (скрининге сифилиса) определяют IgM- и IgG-антитела к бледной трепонеме (Treponema pallidum). Анализ характеризуется очень высокой чувствительностью. При следующих факторах могут наблюдаться ложноположительные результаты: наличие в крови аутоантител (например, антиядерных антител), наличии ОРВИ, мононуклеоза, кори и других вирусных инфекций, узелкового периартериита, ревматоидного артрита, склеродермии и других заболеваний соединительной ткани, других спирохетозов (болезнь Лайма, лептоспироз) и других трепонематозов. По этой причине при получении положительного результата анализа на сифилис проводят дополнительные, подтверждающие тесты для уточнения диагноза. Серологические тесты имеют наибольшую информативность во вторичном периоде и при латентном сифилисе.
Так как в исследовании определяются антитела к возбудителям заболеваний, при интерпретации результата следует учитывать состояние иммунной системы пациента. Ложноотрицательные результаты могут наблюдаться у пациентов с иммуносупрессией (прием глюкокортикоидов и других иммуносупрессантов) и у пожилых людей. Также большое значение имеют анамнестические данные: принадлежность пациента к группе риска по этим заболеваниям (использование инъекционных наркотических средств, многократные переливания крови), наличие аутоиммунных и инфекционных заболеваний, физиологическое состояние организма (беременность, пожилой возраст).
Для чего используется это исследование?
- Для скрининга гепатитов B и C, ВИЧ-инфекции 1-го и 2-го типов и сифилиса.
Когда назначается исследование?
- При госпитализации в стационар;
- при оформлении санитарной книжки;
- при постановке на учет по беременности;
- при постановке на воинский учет;
- при получении разрешения на работу.
Что означают результаты?
Референсные значения (норма анализов на гепатиты В и С, анализа на ВИЧ, анализа на сифилис): отрицательно – для всех 4 показателей.
Исследование специфических антител и антигена p24 вируса иммунодефицита человека.
Синонимы русские
Антитела к ВИЧ 1, 2, антитела к вирусу иммунодефицита человека, ВИЧ-1 p24, ВИЧ-1-антиген, p24-антиген.
Синонимы английские
Anti-HIV, HIV antibodies, human immunodeficiency virus antibodies, HIV-1 p24, HIV-1 Ag, p24-antigen.
Метод исследования
Электрохемилюминесцентный иммуноанализ (ECLIA).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исследование на наличие ВИЧ-инфекции может проводиться анонимно и конфиденциально. При конфиденциальном обследовании в обязательном порядке необходимо предъявление паспорта.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
ВИЧ (вирус иммунодефицита человека) – вирус семейства ретровирусов, который поражает клетки иммунной системы человека (CD4, Т-хелперы). Вызывает СПИД.
ВИЧ-1 – наиболее распространенный тип вируса, чаще всего встречающийся в России, США, Европе, Японии и Австралии (как правило, субтип В).
ВИЧ-2 – редкий тип, распространен в Западной Африке.
Для диагностики вируса иммунодефицита человека используется комбинированная тест-система четвертого поколения, способная определять ВИЧ-инфекцию уже через 2 недели после попадания вируса в кровь, тогда как тест-системы первого поколения делают это только через 6-12 недель с момента инфицирования.
Преимуществом этого комбинированного ВИЧ-анализа является выявление, благодаря использованию антител к ВИЧ-1 p24 в качестве реагентов, специфического антигена p24 (белка вирусного капсида), который может быть обнаружен данным тестом уже через 1-4 недели с момента инфицирования, т. е. еще до сероконверсии, что значительно сокращает "период окна".
Кроме того, такой анализ на ВИЧ выявляет в крови антитела к ВИЧ-1 и ВИЧ-2 (с использованием реакции антиген-антитело), которые вырабатываются в достаточном количестве для определения тест-системой через 2-8 недель с момента заражения.
После сероконверсии антитела начинают связываться с антигеном p24, в результате чего тест на антитела к ВИЧ будет положительным, а тест на p24 – отрицательным. Однако спустя некоторое время в крови будут определяться и антитела, и антиген одновременно. На терминальной стадии СПИД-тест на антитела к ВИЧ может давать отрицательный результат, так как нарушается механизм выработки антител.
- Инкубационный период, или "период серонегативного окна", – время с момента заражения до выработки в крови защитных антител к вирусу, когда тесты на антитела к ВИЧ отрицательны, но человек уже может передавать вирус другим людям. Продолжительность данного периода – от 2 недель до 6 месяцев.
- Период острой ВИЧ инфекции наступает в среднем через 2-4 недели с момента инфицирования и длится примерно 2-3 недели. На данном этапе у некоторых людей могут развиться неспецифические симптомы, схожие с симптомами гриппа, что связано с активной репликацией вируса.
- Латентная стадия протекает бессимптомно, но в течение нее происходит постепенное снижение иммунитета и увеличение количества вируса в крови.
- СПИД (синдром приобретенного иммунодефицита) является конечной стадией развития ВИЧ-инфекции, которая характеризуется сильным угнетением иммунной системы, а также сопутствующими заболеваниями, энцефалопатией или онкологическими заболеваниями.
Несмотря на то что ВИЧ-инфекция неизлечима, сегодня существует высокоактивная антиретровирусная терапия (АРВТ), которая может значительно продлить жизнь ВИЧ-инфицированного и улучшить ее качество.
Данный тест имеет особенно высокую диагностическую ценность, если инфицирование ВИЧ произошло незадолго до момента тестирования (за 2-4 недели).
Для чего используется исследование?
Анализ используется для ранней диагностики ВИЧ, что позволяет предотвратить дальнейшую передачу вируса другим людям, а также своевременно начать антиретровирусную терапию и лечение заболеваний, способствующих прогрессированию ВИЧ-инфекции.
Читайте также:

