Аскариды у попугаев симптомы
Обновлено: 18.04.2024
В чем заключаются трудности диагностики гельминтозов? Какова терапия гельминтозов? На фоне глобальных экологических изменений, широкого применения иммунных, антибактериальных и прочих лекарственных препаратов, частых нарушений адаптационных процессов
В чем заключаются трудности диагностики гельминтозов?
Какова терапия гельминтозов?
На фоне глобальных экологических изменений, широкого применения иммунных, антибактериальных и прочих лекарственных препаратов, частых нарушений адаптационных процессов (болезни адаптации), постоянного стресса, повышения уровня образованности и культуры населения многие давно известные заболевания человека изменили свою клиническую картину. Некоторые симптомы практически перестали встречаться, другие, наоборот, стали выходить на первый план. Это относится и к заболеваниям, вызываемым гельминтами, в частности, круглыми паразитическими червями (нематодами). В умеренном поясе наиболее широко распространенные нематоды — аскарида и острицы.
Гельминты могут вызывать нарушения функции желудочно-кишечного тракта (ЖКТ), быть причиной аллергических (или псевдоаллергических) реакций или усугублять их, вызывать интоксикацию, а также быть фактором, ослабляющим иммунитет [2]. В настоящее время редко встречаются случаи массивной инвазии, когда диагностика не вызывает затруднений, а клубки гельминтов вызывают обтурации кишечника, — значительно чаще гельминты стали являться причиной развития аллергических проблем. При этом гельминтозы относятся к тем заболеваниям, которые трудно диагностировать в связи с объективными и субъективными трудностями (длительные периоды отсутствия яйцекладки, возможность отсутствия среди паразитирующих особей самок, вероятность технических ошибок). Поэтому важно знать клиническую картину данных заболеваний, чтобы иметь возможность назначать углубленное обследование или эффективную терапию по совокупности косвенных признаков, даже не имея прямых доказательств наличия гельминтоза.
С целью оценить клиническую картину при нематодозах проанализированы жалобы, анамнез и результаты осмотра 150 детей, у которых были обнаружены аскариды (116 детей), острицы (27 детей), аскариды и острицы (7 детей). Гельминты выявлены стандартными методами: обнаружение яиц аскарид в фекалиях методом мазка или яиц остриц в соскобе на энтеробиоз, а также визуальное обнаружение аскарид или остриц в фекалиях, рвотных массах или при оперативном или эндоскопическом вмешательстве в брюшной полости или в области прямой кишки [3].
Среди детей было 67 мальчиков, 83 девочки. Распределение по возрасту представлено в табл. 1. Преобладали дети младшего дошкольного возраста (от одного до трех лет), их количество составило 63%. Именно в этом возрасте — наибольшие эпидемиологические предпосылки появления нематодозов.
У 150 детей с доказанными инвазиями аскаридами и/или острицами отмечались следующие клинические проявления.
У 107 детей (71,3%) были аллергические проблемы: кожные высыпания, диатез, атопический дерматит, нейродермит — у 99 (66%), из них у 18 эти проблемы носили периодический характер, у двух детей, кроме кожных высыпаний, отмечались конъюнктивиты; у десяти (6,7%) отмечалась доказанная пищевая аллергия на какие-то продукты с высоким уровнем специфических IgE в сыворотке крови; у шести детей (4%) отмечался астматический компонент или был установлен диагноз бронхиальная астма.
Бруксизм (скрежетание зубами) — симптом, который часто связывается с глистными инвазиями, но фактически является неспецифическим признаком интоксикации центральной нервной системы и может сопровождать любые хронические интоксикации — отмечался у 25 детей (16,7%).
Нарушения ночного сна отмечались у 81 ребенка (54%): беспокойство к вечеру, затруднения засыпания — у 15 детей (10%); беспокойный ночной сон (вскрикивания, постанывания, метания во сне, пробуждения, плач, бессонница, кошмарные сновидения) — у 76 (50,7%). Некоторые родители старших детей затруднялись охарактеризовать ночной сон ребенка, т. к. ребенок спит в другой комнате. Проблемы с засыпанием и ночным сном — важный симптом глистных инвазий, т. к. известно, что кишечные нематоды (в том числе аскариды и острицы) часто активизируются именно ночью.
У 54 детей (36%) отмечались зуд и/или покраснения в области заднего прохода (анальная эскориация) — у 43 детей (28,7%); зуд — у 38 (25,3%); оба симптома — у 27 (18%). Анальная эскориация и зуд считаются симптомами энтеробиоза (острицы), но при этом из 54 детей, у которых отмечались данные симптомы, энтеробиоз был доказан у 17 детей (31,5% от числа детей с этими симптомами). У других 37 детей (68,5% от числа детей с данными симптомами) было доказано наличие аскаридоза, но ни визуально, ни в анализах не были обнаружены острицы. Это может свидетельствовать либо о том, что в данных случаях присутствовали острицы, которые не были диагностированы, т. е. гельминтоз был смешанным, либо о том, что анальная эскориация и зуд — симптомы, характерные не только для энтеробиоза, но и аскаридоза.
У 29 детей (19,3%) отмечались признаки общего ослабления иммунитета: часто или длительно болеющие дети (по общепринятой классификации Monto J. et al., 87) — 18 детей (12%); рецидивирующие стоматиты, гингивиты отмечались у 13 детей (8,7%); кариес зубов — у шести (4%); рецидивирующие гнойные заболевания кожи или слизистых — у трех (2%).
У 15 детей (10%) имелись результаты исследования иммунного статуса по крови: у 13 детей было снижено количество Т-клеток; у всех 15 детей было снижено количество Т-хелперов, причем у шести из них — существенно; у 12 детей было снижено хелперно-супрессорное соотношение; у семи детей отмечалось снижение уровня IgA (секреторный иммуноглобулин), в том числе у трех — существенное, у остальных же восьми детей уровень IgA в сыворотке крови был либо нормальным, либо повышенным; у шести детей отмечалось снижение количества лимфоцитов, в том числе у одного ребенка была выраженная лимфо- и нейтропения. Эти результаты подтверждают известные данные о том, что аскариды и острицы угнетающе влияют на функции иммунитета, а также что у людей с ослабленным иммунитетом большая вероятность появления гельминтоза [1].
У большинства детей отмечалось более одного симптома. Обобщенные данные по клинической картине представлены в табл. 2.
Терапия во всех случаях состояла из двух этапов: сначала — антигельминтная терапия, причем назначались два разных препарата (декарис и вермокс) с интервалом три — пять дней между ними, чтобы максимально охватить различные стадии жизни гельминтов; через некоторое время после антигельминтной терапии — препараты для микробиологической и функциональной коррекции. Соответственно оценивались результаты противоглистной терапии, результаты всего лечения, а также катамнез в течение шести месяцев после терапии. В большинстве случаев улучшение наступало быстро в процессе лечения. У 36 детей только после антигельминтной терапии существенно уменьшились или полностью исчезли аллергические проявления, у 39 детей после первого этапа терапии нормализовалась работа ЖКТ, у 41 ребенка сразу прекратились боли в животе, по остальным симптомам также наступало улучшение после противоглистных препаратов. Это подтверждает то, что симптомы были вызваны наличием гельминтов.
У 92 детей после всего лечения не было никаких жалоб; о 37 нет данных об изменениях состояния в процессе и после лечения; у 16 детей эффект был неполным, т. е. какие-то симптомы сохранялись и после окончания лечения; у четырех детей эффект от терапии оказался нестойким, поскольку возникли рецидивы после окончания лечения; у трех детей эффекта от терапии не было.
Глисты у попугаев, содержащихся в неволе, встречаются довольно часто.
Большинство владельцев птиц ошибочно полагает, что у попугая, купленного в зоомагазине или у заводчика, глистов быть не должно, и потому не подозревает о высокой степени важности противопаразитарных обработок. Следует отметить, что попугай может заразиться глистами даже, если его кормят только качественным зерновым кормом из вакуумной упаковки, что само по себе неправильно, но здесь это мнение приведено в качестве примера из жизни.
Где и как попугай заражается глистами?

Попугаи монахи или калита (Myiopsitta monachus), как и большинство других видов попугаев ( волнистые попугаи, кореллы, какаду, ара, неразлучники, розеллы, ожереловые попугаи) — проводят очень много времени, копаясь в земле, выкапывая корешки и почвенных насекомых. Однако, исследования попугаев, живущих как в природе, так и в городах, — не обнаруживают кишечных гельминтов. И напротив, эти же попугаи, содержащиеся в неволе в домашних условиях и в зоопарках, — страдают от большого количества кишечных глистов.
Существует два типа гельминтов: одним (для заражения птицы) необходимы промежуточные хозяева (обычно это членистоногие, моллюски (улитки, слизни), дождевые черви), вторым такие сложности не нужны — попугай может неоднократно перезаражать сам себя даже в том случае, если он сидит в клетке одни и не получает ничего кроме зерна.
Яйца гельминтов очень хорошо сохраняются в помете, в пыли, на кормушках и поилках. Они могут сохранять способность заражать много месяцев и даже лет. Раз уж я упомянул о зерновых кормах, то следует сказать, что какими бы качественными не были зерновые смеси, но технология обработки зерна не исключает полностью контакта зерна с помётом голубей, других птиц и животных. Яйца аскарид и других глистов с прямым циклом развития хорошо сохраняются на зерне, на которое попал помёт, на стадии сбора урожая, в процессе транспортировки на завод, где делают корма для домашних пернатых, а также на элеваторах, где зерно хранят.
Промежуточные хозяева гельминтов поедаются попугаями случайно или специально (многие попугаи едят улиток или насекомых). Заразившись, попугай может носить в себе такого паразита несколько лет. Чаще всего это безопасно для птицы, но при большом количестве паразитов в кишечнике или в печени они сильно истощают птицу и могут привести ее к гибели, не говоря уже о том, что большинство попугаев в неволе содержатся в условиях гиподинамии (недостаточной подвижности) и на бедных рационах, что само по себе сильно ослабляет пернатых.
Передаются ли паразитозы от больных родительских птиц птенцам?
Какие признаки наличия глистов у попугаев?
Могут ли паразитозы протекать бессимптомно?
Может ли взрослый человек или ребенок заразиться гельминтами от попугаев?
На данный момент не известны гельминты, которыми человек может заразиться, контактируя с попугаем. Также неизвестно о гельминтах, которыми попугай может заразиться от человека. Другими словами, общих для человека и попугая гельминтов — не выявлено.
Может ли попугай заразиться гельминтами через ветки с лишайником или глину, которые принесены с улицы?
Может, так же как и от любого другого продукта, который вы приносите в дом. Подробно о том, как собирать глину написано в статье о глине в рационах птиц.
Надо ли ошпаривать ветки, сосновые шишки, овощи и фрукты, чтобы устранить гельминтов, перед тем, как давать эти корма попугаю?

На фото попугай ара макао или красный ара (Ara macao) в природе кормится незрелыми орехами индийского миндаля (Terminalia Catappa). Кожура этих орехов содержит большое количество танинов.
Может ли попугай заразиться от других домашних питомцев: грызунов, собак, кошек и т.д ?
От собак и кошек попугаи могут заразиться, например, токсокарами (круглые черви), но попугаи являются промежуточными хозяевами этих паразитов. Т.е. личинки паразитов инкапсулируются в организме птицы и сохраняют свою жизнеспособность несколько месяцев. Если при развитии личинок токсокар не затронуты жизненно важные органы птицы то, обычно никаких последствий такого заражения не последует. Однако существует вероятность поражения центральной нервной системы — эта ситуация очень опасна для попугая. Подробнее об этом написано ниже, в разделе о цереброспинальных паразитах. Попугаи не могут заразить глистами кошек или собак. Но если кошка или собака съест зараженного личинками токсокар попугая, то у них разовьются половозрелые стадии паразитов. Отсюда вывод: глистов надо прогонять всем животным в доме регулярно и не допускать поедания попугаев собаками и кошками.
Когда нужно бить тревогу? На что нужно обратить внимание? Как часто нужно сдавать анализы / проверяться?
Тревогу бить не надо. Достаточно раз в год проводить диспансеризацию попугая у птичьего доктора, сдавать все нужные анализы, и регулярно 2 раза в год проводить курс глистогонных препаратов. Обращать внимание нужно на любые настораживающие признаки в поведении попугая, а для этого владельцу птицы важно знать как выглядит и как ведет себя здоровый попугай. Для этого надо смотреть фильмы о попугаях в дикой природе, так как обилие материалов в социальных сетях с участием больных попугаев приводит к тому, что владельцы попугаев, в конечном итоге, не знают как же выглядят здоровые птицы.
Как часто надо проводить профилактическую терапию против паразитов попугаю?
Глистогонные препараты попугаям рекомендуется давать 2 раза в год: поздней весной и поздней осенью/в начале зимы. Дозировка препаратов рассчитывается птичьим врачом на основании массы тела попугая. Для профилактической регулярной обработки против гельминтов применяют препараты фенбендазола (панакур), левомизола, пирантела, празиквантела, ивермектина и других глистогонных препаратов. Применяются и комбинированные препараты для лечения от нескольких типов глистов сразу (от нематод, трематод и цестод).
Можно ли применять для попугаев глистогонные препараты для кошек, собак, лошадей, людей?
В этом видео, я подробнее рассказываю о глистогонных препаратах, витаминах и антибиотиках для попугаев.
Помогают ли тыквенные семечки, пижма, полынь и другие народные средства от глистов?

Все попугаи в природе питаются большим количеством растений, содержащих такие биологические активные вещества как танины, сапонины, алкалоиды, эфирные масла и пр. Все эти соединения являются ествественными стимуляторами имунной системы попугаев и губительно действуют на большинство паразитов птиц. На фото бледноголовая розелла (Platycercus adscitus) кормится цветками чайного дерева.
Если попугай живет один в клетке и не ест ничего кроме зерна из пачки — надо ли ему прогонять глистов?

В исследовании, проведенном в Австралии, единственным видом попугаев в природе, у которых были обнаружены гельминты, были улетевшие домашние неразлучники. У диких волнистых попугайчиков, корелл, какаду, лорикетов — глистов не было обнаружено ни разу.
Это токсично? Надо ли как-то поддерживать печень попугая во время глистогонки?
При условии правильного расчета дозировки сами по себе глистогонные препараты малотоксичны для организма попугая. Чаще всего при регулярной дегельминтизации никаких дополнительных препаратов, поддерживающих печень, давать нет необходимости. Но в случае, если у попугая очень большое количество гельминтов, то в случае массовой гибели паразитов может развиться интоксикация или/и аллергическая реакция, и в этом случае состояние птицы может ухудшиться, может начаться тошнота, рвота, понос, развиться вялость или хромота. При появлении любых настораживающих признаков нужно сразу же связаться с ветеринарным врачом, курирующим вашу птицу.
Надо ли делать анализы на паразитов перед тем, как давать глистогонные препараты?
Как собирать помёт попугая для паразитологического анализа?
Почему паразитологический анализ помёта может не выявить никаких глистов и других паразитов в одной лаборатории, а в другой лаборатории их находят?
Лаборатории же сами решают каким методом исследовать помет — Как же быть?
Либо выбирать лаборатории, которые делают анализ на все группы паразитов, либо обращаться к птичьим врачам, которые сами делают паразитологические анализы с учетом специфики работы с птицами. Кроме того, некоторые виды паразитов выделяют яйца не постоянно, поэтому возможны ложноотрицательные результаты анализа, и имеет смысл пересдавать помет на анализ через некоторое время.
На всякий случай поясню — ложноотрицательным анализ может быть по причинам указанным выше, а ложноположительным результ анализа помета на глистов быть не может! Если яйца гельминтов обнаружены, нет смысла пересдавать помет, надеясь, что это ошибка лаборатории и глистов нет.
А если купить микроскоп и самим смотреть помёт попугая? Будет ли это полезно?
Это зависит от вашей способности к постижению нового и освоения новых профессий. Большинство методик по диагностике гельминтозов птиц технически легко выполнимы в обычной квартире, пару лет опыта и можно будет научиться определять паразитов самостоятельно.
Может ли развиться самоощипывание попугая от глистов?
Самоощипывание всегда связано с болевой реакцией и воспалительным процессом, поэтому если у птицы большое количество гельминтов, теоретически, это может стать причиной самоощипа попугая, но при такой степени заглистованности всегда развиваются инфекции, вызванные бактериями или грибками, жизнедеятельность которых чаще приводит к самоощипыванию. Само по себе наличие большого количества глистов говорит о том, что у пернатого, скорее всего, есть и другие инфекционные проблемы и надо продолжать обследование.
Что такое лямблиоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Лямблиоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое кишечными лямблиями, которые колонизируют слизистую оболочку преимущественно тонкого кишечника, нарушают процессы пристеночного пищеварения и способствуют развитию и усугублению поражения желудочно-кишечного тракта и других заболеваний.
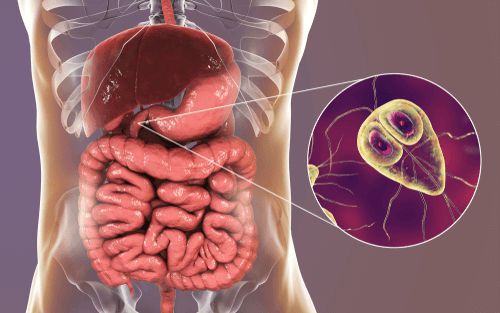
Этиология
Возбудитель — лямблия. Данный род паразитов включает в себя шесть типов, но заболевание человека вызывает только один тип — кишечная лямблия (Giardia duodenalis, Giardia lamblia, Giardia intestinalis). Это жгутиковое микроскопическое простейшее, впервые описанное чешским медиком-анатомом Д.Ф. Лямблем в 1859 году. Оно имеет до восьми генетических подтипов, но для человека патогенны только А и В (также имеют подтипы).
Вид — Giardia lamblia
Возбудитель лямблиоза (кишечная лямблия) существует в виде двух жизненных форм:
- вегетативная (трофозоиты) — стадия активного размножения внутри организма;
- цистная — образуется при неблагоприятных условиях среды.
Трофозоиты — это анаэробные, грушевидные микроорганизмы размерами 9-18 мкм. Они обитают в верхних отделах тонкого кишечника. Подвижны (имеют характерное движение в виде вращения вокруг продольной оси — боковое движение), тело спереди расширено и закруглено, сзади сужено и заострено. Имеют в составе два ядра (между ними пролегают опорные нити — аксостили) и парные органоиды — четыре жгутика и два медиальных тела.
Трофозоиты не имеют цитостома — органа заглатывания пищи и пищеварительной вакуоли, поэтому они всасывают пищу, переваренную хозяином (в основном, углеводы), всей поверхностью тела. Это называется осмотическим питанием.
Как выглядят лямблии:
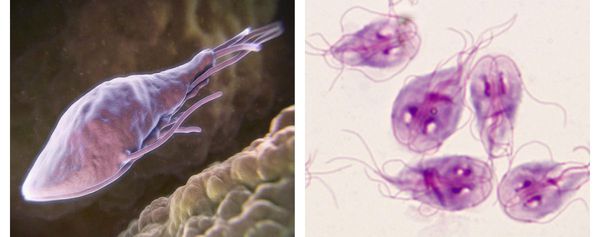
В передней их трети тела расположен присасывательный диск в виде специального углубления. С его помощью лямблии прикрепляются к ворсинкам слизистой оболочки тонкого кишечника. Цитоплазматическая мембрана задней поверхности имеет по краям булавовидные выросты, что также создаёт дополнительную прикрепляющую составляющую.
Размножаются путём продольного деления. Слабо устойчивы в условиях окружающей среды при покидании организма хозяина: при комнатной температуре даже в отсутствии агрессивных факторов быстро погибают.
Цистная форма неподвижна. Паразиты имеют овальную форму, лишены свободных жгутиков (сложно свёрнутые), их размеры достигают 10-14 мкм, окружены толстой, несколько отделённой от тела оболочкой (данная особенность имеет значение при распознавании вида).
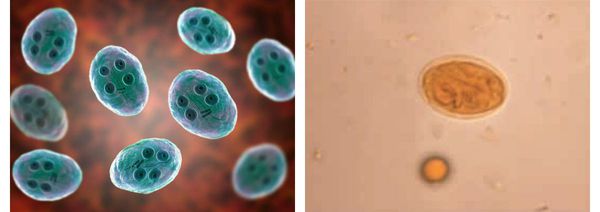
Зрелые цисты внутри имеют четыре ядра, незрелые — два ядра. Образуются в нижних отделах кишечника в процессе выхода из организма с фекалиями. Очень устойчивы во внешней среде: могут сохраняться месяцами в воде при температуре 4-20°C, при хорошей влажности способны сохраняться на контаминированных (обсеменённых) продуктах питания до недели. При кипячении цисты погибают мгновенно, а при высушивании и низкой влажности гибель наступает в течении суток. Устойчивы к бытовому хлорированию воды, действию щелочей и кислот, ультрафиолетовому излучению. Низкие температуры переносит относительно хорошо, но при этом снижая свою жизнеспособность. [1] [3] [6] [9]
Эпидемиология
Распространение заболевания повсеместное, преимущественно в странах с влажным тёплым климатом. Только официально выявляемые случаи в России приближаются к 150 тысячам в год.
Сезонность выражена неярко, некоторый всплеск заболеваемости отмечается в тёплое время года. Возрастной состав больных склоняется в сторону детей.
Источник заражения — люди (больные различными формами лямблиоза и паразитоносители), причём наибольшая заразность наблюдается в подостром периоде заболевания, когда в 1 г фекалий может содержаться до нескольких десятков миллионов цист. Лямблии животных (нечеловеческие типы паразитов) не имеют доказательной базы в плане распространения и заражения человека.
Факторами передачи паразитов выступает загрязнённая цистами термически не обработанная питьевая вода, пища, грязные руки (возможна прямая передача от человека к человеку). Определённую роль в передаче лямблий играют насекомые (тараканы, мухи) и животные (собаки, кошки) — они являются механическими переносчиками (паразиты располагаются на их теле, шерсти, лапках, транзитом в кишечнике).
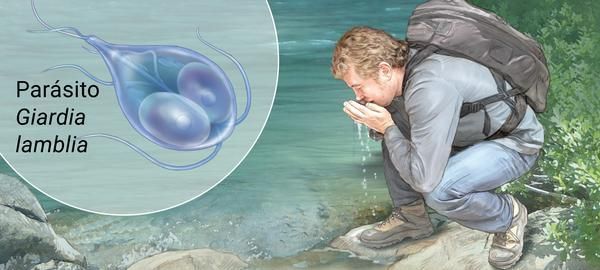
Механизм передачи — фекально-оральный (водный, пищевой и контактно-бытовой пути). Наиболее часто передача осуществляется:
- через водопроводную воду;
- при употреблении плохо промытых зелени и овощей (или промытых под водопроводной водой без последующей термической обработки);
- при нарушении правил санитарной гигиены, особенно в детских коллективах.
Доза заражения — от 10 до 100 цист (в зависимости от индивидуальных свойств иммунной реактивности кишечника). Возможны случаи невосприимчивости к паразитам: цисты лямблий, встречая агрессивно настроенную среду кишечника, проходят транзитом и выделяются в окружающую среду в неизменённом виде.
Иммунитет после лямблиоза нестойкий и ненапряжёный, возможно повторное заражение. Повышенный риск заболевания имеют лица с патологией иммунитета кишечника и дефицитом IgA. [2] [3] [5] [8] [10]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы лямблиоза
Инкубационный период длится от нескольких дней до месяца и более. Чаще всего при заболевании не наблюдается вообще никаких клинических проявлений, особенно у взрослых.
К основным возможным симптомам лямблиоза относятся:
- Симптомы интоксикации и вегетативных изменений — повышенная утомляемость, плаксивость, раздражительность, нарушение ритма сна, головокружения, аритмии, субфебриллитет и другие.
- Симптомы поражения ЖКТ — дискомфорт и боли различной интенсивности и характера в различных отделах живота, тошнота, снижение аппетита, появление чувства горечи во рту, нарушения стула (запоры и поносы), налёт на языке и неприятный запах изо рта, снижение массы тела и другое.
- Симптомы поражения кожи — аллергические высыпания различного характера и локализации, атопический дерматит, бледность и шероховатость кожи, повышенная сухость покровов, хейлит (воспалительные изменения кожи губ и их слизистой), заеды (трещинки в уголках рта), нетипичное/неконтролируемое течение хронических патологий кожи.
- Усиление развития и обострения заболеваний, прямо не связанных с лямблиозом — бронхиальная астма, псевдоаллергические явления, гастриты, язвы желудка и двенадцатиперстной кишки, холецистит, неспецифический язвенный колит, артриты и другое.
- Симптомы мальабсорбции (потери питательных веществ) — авитаминозы, отставание в физическом и умственном развитии, дистрофия (эти проявления более характерны для детей).
Лямблиоз у детей
Как правило, у детей первыми симптомами лямблиоза становится появление субфебрильной или фебрильной температуры (37,1–38,0°C или 38,0–39,0°C), болей в животе, тошноты, иногда рвоты, метеоризма, жидкого стула. Живот при этом болезнен, вздут, урчит по ходу кишечника. Грудные дети становятся беспокойными, кричат, нарушается сон, симптомы лямблиоза усиливаются во время и после кормления, возможно появление аллергодерматозов и опрелостей. В динамике при отсутствии лечения это может приводить к нарушению роста и психоэмоционального развития, частым простудным или аллергическим заболеваниям, развитию хронических проблем органов ЖКТ.
У детей более позднего возраста и взрослых яркие симптомы лямблиоза наблюдаются редко — на первый план выходит постепенное развитие диспепсических явлений со стороны ЖКТ умеренного характера:
- метеоризм;
- дискомфорт и боли в животе преимущественно в околопупочной области и правом подреберье;
- нарушения стула в различных сочетаниях;
- появление налёта на языке;
- иногда горечь во рту и кожные проявления (усиление выраженности угревой сыпи, хронических полиэтиологических заболеваний, например, псориаза и дерматитов);
- возможны вегетативные расстройства, головные боли, головокружения, неустойчивость артериального давления, повышения температуры тела, чувствительность лимфоузлов.
Лямблиоз у беременных
Лямблиоз у беременных не имеет каких-либо специфичных отличий от лямблиоза у остальных людей, но может приводить к повышению риска развития у беременной В-12 дефицитной анемии и снижению веса плода (гипотрофии). [1] [3] [5] [7] [10]
Патогенез лямблиоза
Характерен так называемый "симптом манной крупы" — белёсые полусферические выбухания слизистой оболочки двенадцатиперстной кишки, представляющие собой зоны очагового отёка со скоплением увеличенного количества лейкоцитов.
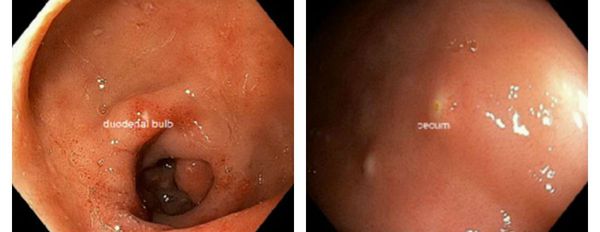
Посредством механического раздражения и выделения паразитами продуктов жизнедеятельности (токсическое влияние) происходит стимуляция образования слизи, повышение регенераторной функции кишечника, нарушение выработки факторов нейрогуморальной регуляции пищеварения (холецистоцикин и других) и двигательной активности гепатогастродуоденальной области. Это ведёт к дезорганизации висцеро-висцеральных связей области двенадцатиперстной кишки, поджелудочной железы и желчевыводящей системы, а также к нарушению функционирования органов ЖКТ, нарушению микробиоценоза кишечника, активизации анаэробной флоры, расстройствам расщепления и всасывания белков, жиров, углеводов, витаминов и микроэлементов.
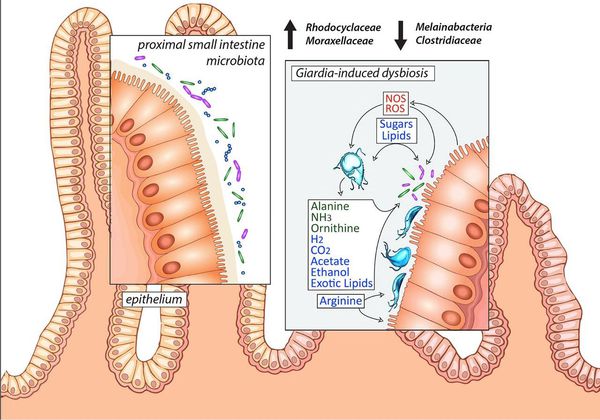
Возникает воспаление слизистой кишечника по типу реакций гиперчувствительности замедленного типа, происходит воздействие на иммунорегуляторные белки (мимикрия), снижение выработки иммуноглобулинов (в частности IgA) из-за нарушения всасывания белков и снижение фагоцитарной активности. Всё это в совокупности со всасываемыми продуктами жизнедеятельности лямблий становится причиной истощения иммунной системы (как кишечника, так и общего иммунитета), развития хронического поражения кишечника, провоцирует длительное обострение имеющихся хронических заболеваний и усугубление ряда аллергозависимых дерматозов. [1] [4] [7] [8]
Классификация и стадии развития лямблиоза
По клинической форме лямблиоз бывает:
- бессимптомным (носительство);
- кишечным — преимущественно симптомы кишечной формы, но можгут быть и гастритические проявления (дискомфорт в животе, неустойчивый стул, тошнота);
- билиарно-панкреатическим (рефлекторный) — дискомфорт в эпигастрии и правом подреберье, привкус горечи во рту, повышенная частота развития плохо контролируемых гастродуоденитов и панкреатитов;
- астено-невротическим — слабость, вялость, повышенная утомляемость, раздражительность, эмоциональная неустойчивость;
- токсико-аллергическим — периодические высыпания на теле, обострение хронических кожных заболеваний и бронхиальной астмы, эозинофилия;
- смешанным.
Течение лямблиоза бывает трёх типов:
- острым — до одного месяца;
- подострым — 1-3 месяца;
- хроническим — более трёх месяцев.
По наличию осложнений лямблиоз бывает:
Выделяют три степени заболевания:
Осложнения лямблиоза
Возможны специфические и неспецифические осложнения лямблиоза.
К специфическим относятся:
-
— зудящие обширные высыпания на теле;
- отёк Квинке — выраженный отёк подкожной клетчатки, иногда сопровождающийся зудоим и чувством удушья;
- офтальмопатия — нарушения восприятия органом зрения;
- артрит — дискомфорт и боли в суставах;
- гипокалиемическая миопатия — слабость определённых групп мышц.
К неспецифическим осложнениям относятся:
- наслоение интеркуррентных заболеваний (вторичная флора);
- белково энергетическая недостаточность (гипо- и авитаминоз, снижение веса, анемия и другие). [1][2][8][10]
Диагностика лямблиоза
Лабораторная диагностика лямблиоза включает в себя:
- Клинический анализ крови — в остром периоде наблюдается эозинофилия, базофилия и повышение СОЭ; в последующие периоды — умеренная эозинофилия или нормальное значение эозинофилов, иногда незначительная базофилия.
- Биохимический анализ крови — иногда отмечается повышение уровня общего билирубина и амилазы.
- Копроовоскопическое исследование кала — "золотой стандарт" диагностики. Оно позволяет выявить цисты (наиболее часто) и вегетативные формы лямблий (в редких случаях). В виду прерывистого цистообразования показано неоднократное исследование с некоторым интервалом (семь дней). Существует широко распространённое заблуждение о том, что кал нужно сдавать "тёплым" (свежим). На самом деле, в этом нет никакой необходимости. Так как данное исследование предполагает обнаружение цист лямблий, которые очень устойчивы во внешней среде, период от дефекации до исследования никоим образом не влияет на информативность результата анализа.
- Иммунохроматографический метод и ПЦР-диагностика кала (выявление антигенов и нуклеиновых кислот паразита) — имеет хорошую информативность и вполне может применяться в комплексе с другими методами исследований.
- ИФА-диагностика — малоинформативное исследование, так как локализация лямблий в просвете кишечника не создаёт условий для полноценного иммунного ответа, который наблюдается в основном у детей при остром заболевании, что создаёт значительное число ошибочных результатов как гипо-, так и гирпедиагностики.
- Дуоденальное зондирование (выявление вегетативных форм лямблий в двенадцатиперстной кишке) — может применяться в сложных диагностических случаях и при подозрении на коинвазирование (например, описторхами при описторхозе).
- УЗИ органов брюшной полости и ФГДС — позволяют выявить признаки нарушения моторики гепатобилиарной области. [2][3][5][6][9]
Дифференциальная диагностика предполагает исключение следующих заболеваний:
- паразитарные заболевания другой этиологии (как кишечной, так и внекишечной локализации);
- хронический гастродуоденит (симптомосходная симптоматика);
- кишечные инфекции (сальмонеллёз, дизентерия, ротавирус и другие);
- дисбиоз кишечника (сборное понятие, характеризующееся неустойчивостью стула, дискомфортом в животе различного характера, снижением веса и другими симптомами). [1][5][9]
Лечение лямблиоза
Лечение острой формы лямблиоза, которая возникает в основном у детей, должно осуществляться в стационаре и включать в первую очередь дезинтоксикационную и дегидратационную терапию, а также щадящее питание.
Медикаментозная терапия
При подтверждении диагноза проводится этиотропное лечение одним из противолямблиозных препаратов (нитрогруппа) в сочетании с желчегонными средствами, и лекарствами, улучшающими микрофлору кишечника.
При длительном хроническом течении в виду персистирующей колонизации лямблиями слизистой оболочки тонкого кишечника и местным иммунодефицитом курс лечения должен быть комплексным, включающим:
- диета (потреблять меньше углеводов);
- средства этиотропного воздействия (химиопрепарат);
- приём желчегонных препаратов;
- иммунотерапию (усиление фагоцитоза и восполнение дефицита IgA);
- устранение дисбиоза кишечника (пробиотики).
К сожалению, в последнее время всё чаще встречаются штаммы лямблий, устойчивых к различным видам противопаразитарной терапии, поэтому средняя вероятность успешной эрадикационного лечения не превышает 85%.
Гигиена при лечении лямблиоза
Лямблиоз редко передаётся между членами семьи, если соблюдать простейшие гигиенические правила: мыть руки после посещения уборной, перед едой и после контакта с животными.
Лечение народными средствами
Эффективность и безопасность методов народной медицины научно не доказана. Без адекватного лечения лямблиоз может привести к различным осложнениям: крапивнице, отёку Квинке, нарушениям зрения, артриту и слабости мышц.
Лечение лямблиоза у детей
Новорождённых от лямблиоза, как правило, не лечат, так как нет подходящих препаратов. В основном рекомендуется улучшать микрофлору и работу кишечника.
Детей старшего возраста лечат так же, как и взрослых, но подбирают необходимую дозировку и форму препарата.
Лечение лямблиоза у беременных
Беременным лечение, как правило, противопоказано (потенциальный вред препаратов превышает пользу от лечения), в основном предпочтение отдаётся улучшению флоры и работы кишечника.
Контроль излеченности
После курса лечения проводится паразитологический контроль методом копроовоскопии или ПЦР не ранее двух недель после завершения курса лечения длительностью в три месяца со сдачей анализа раз в месяц. [1] [3] [4] [5]
Прогноз. Профилактика
При назначении адекватного лечения прогноз благоприятен, осложнения редки.
Специфической профилактики не разработано. Основной упор следует делать на меры соблюдения санитарных норм:
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
- Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
- Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
Рассмотрены факторы риска паразитозов у детей, действие паразитов на организм ребенка, подходы к диагностике паразитарной инвазии и принципы комплексного лечения паразитозов с тем чтобы предотвратить дальнейшее развитие функциональных нарушений с формиров
Risk factors of parasitosis in children was considered, as well as the influence of parasites on a child's body, approaches to the diagnostics of parasitic invasions and principles of integrated treatment of parasitic diseases in order to prevent the further development of functional disorders of the formation of organic pathology.
.jpg)
Паразитарное заболевание — развитие болезненных симптомов в результате жизнедеятельности гельминта или простейших в организме человека [1]. Основной фактор выживания и распространения паразитов — их необычайно высокая репродуктивная способность, а также постоянно совершенствующиеся механизмы приспособления к обитанию в теле человека. К сожалению, настороженность медицинских работников в отношении паразитарных заболеваний у населения в настоящее время чрезвычайно низка, а профилактика гельминтозов сведена к лечению выявленных инвазированных пациентов [12, 13]. Вместе с тем многие исследователи отмечают связь широкой распространенности паразитозов у детского населения с развитием функциональной патологии органов пищеварения на фоне нарушений регуляции и высокий риск формирования хронических заболеваний даже при условии естественной санации ребенка с течением времени.
Самые распространенные и изученные заболевания — аскаридоз, энтеробиоз (рис. 1) и лямблиоз — регистрируются повсеместно. В России ежегодно выявляется более 2 млн больных нематодозами. При оценке территориального распределения лямблиоза по России установлено, что самый высокий средний уровень показателей заболеваемости в течение многих лет отмечен в Санкт-Петербурге, причем пораженность детей, посещающих детские учреждения, составляет 35% [2].
Каждый человек в течение жизни неоднократно переносит различные паразитарные заболевания [9]. В детском возрасте паразитозы встречаются чаще. У детей раннего возраста (до 5 лет) этому способствует широкая распространенность репродуктивного материала паразитов (цисты, яйца, личинки (рис. 2)) в окружающей среде и недостаточное развитие гигиенических навыков.
.jpg)
Значимость определенных факторов риска меняется в соответствии с возрастом ребенка. Доказано, что для детей младшего возраста более значимы санитарно-гигиенические условия проживания, а для подростков при сборе анамнеза необходимо уделить внимание социально-экономическим и географическим факторам (пребывание в лагере, туристическая поездка, наличие младшего брата или сестры) (рис. 3).
.jpg)
Транзиторное снижение противоинфекционного иммунитета как фактор риска возникновения паразитоза у детей регистрируется также в период реконвалесценции после вирусных заболеваний, вызываемых вирусами герпетической группы (цитомегаловирус, вирус простого герпеса I и II, вирус Эпштейна–Барр), может возникать в результате ятрогении (применение иммуносупрессивной терапии при аллергических и аутоиммунных заболеваниях). В настоящее время значимая доля детей находится в состоянии дезадаптации, которое также сопровождается снижением иммунной защиты.
Иммунную защиту желудочно-кишечного тракта (ЖКТ) ребенка можно условно разделить на специфическую и неспецифическую. К неспецифической защите относят комплекс условий нормального пищеварения: зрелость ферментативных систем, обеспечение кислотно-щелочного градиента в различных отделах ЖКТ, деятельность нормальной микрофлоры, адекватную моторику.
Отдельно необходимо отметить, что для такого заболевания, как лямблиоз, предрасполагающим фактором инвазии является нерегулярное и недостаточное отделение желчи в кишечник при аномалиях развития желчного пузыря (перетяжки, перегибы). Лямблиоз, выявленный у пациентов педиатрического отделения МОНИКИ, в 100% случаев сопровождался дисфункцией билиарного тракта.
.jpg)
У детей в восстановительном периоде после острых кишечных инфекций, после массивной антибиотикотерапии, а также у пациентов с хронической патологией органов пищеварения сопутствующие нарушения ферментного обеспечения, нормофлоры и моторики кишечника также делают ЖКТ более уязвимым для паразитов (рис. 4).
Специфическая защита слизистой оболочки органов пищеварения зависит от возраста ребенка и его зрелости. Механизм специфической иммунной защиты является одной из наиболее древних систем организма, так как гельминтозы сопровождают человечество в течение многих тысячелетий. Этот механизм представлен прежде всего эозинофилами крови и иммуноглобулином Е.
Классический развернутый антипаразитарный ответ может быть сформирован у ребенка не ранее достижения им 4 лет и тесно связан с качеством и количеством IgE, созревающего к этому возрасту. При контакте организма с паразитом в первую очередь выделяются медиаторы воспаления: интерлейкин, лейкотриен С4, D4, простагландины, тромбоксаны. Увеличивается количество лимфоцитов, продуцирующих IgM и IgG. В клиническом анализе крови отмечается рост уровня эозинофилов и базофилов, связанный с увеличением содержания этих клеток в тканях инвазированного органа. Встречаясь с личинками паразита, тканевые базофилы выделяют гепарин и гистамин, которые в сочетании с лейкотриенами и другими медиаторами воспаления вызывают общие проявления: зуд, реактивный отек, гиперемию, а также могут спровоцировать общие проявления: бронхоспазм, проявления крапивницы или диарею. Аллергическое воспаление при паразитозах развивается по классическому пути и призвано создать условия, приводящие к гибели и/или элиминации паразита [5].
Вместе с тем эозинофилы обладают выраженным цитотоксическим потенциалом, превышающим возможности других клеток крови, что объясняет первостепенное значение эозинофилов в антипаразитарных реакциях и их повреждающую роль при аллергии. Основное действие эозинофилы оказывают в барьерных тканях. В очаге инвазии они дегранулируют, оказывая гельминтотоксическое и цитотоксическое действие. Белки эозинофильных гранул (большой основной протеин, эозинофильная пероксидаза, эозинофильный катионный протеин, эозинофил-производный нейротоксин) токсичны не только для паразита, но и для клеток организма ребенка. Еще одной из важных причин системных и органных поражений, сопутствующих паразитозам, является образование иммунных комплексов [9, 10].
Действие паразитов на организм ребенка осуществляется с вовлечением многих систем. Практически все их виды могут вызывать сдвиг соотношения Th1/Th2 клеток в направлении, благоприятном для их выживания. Описаны случаи, когда продукты выделения паразита оказывали гормоноподобное действие на организм хозяина [5].
Местное влияние паразиты осуществляют, вызывая контактное воспаление слизистой оболочки и стимулируя вегетативные реакции. При этом нарушаются процессы кишечного всасывания, адекватная моторика ЖКТ и его микробиоценоз.
Системное влияние оказывается за счет использования паразитом энергетического и пластического потенциала пищи в ущерб организму ребенка, индукции аллергии и аутоиммунных процессов, целенаправленной иммуносупрессии и эндогенной интоксикации. Проведенными исследованиями показано, что аллергический синдром сопутствует аскаридозу и энтеробиозу в 71,3% случаев. Среди детей с атопическим дерматитом паразитозы выявляются у 69,1%, при этом лямблиоз из числа всех инвазий составляет 78,5% [4].
Особенно узнаваемую клиническую картину формирует токсокароз (рис. 5). Клиническими маркерами этой инвазии являются лейкемоидная реакция эозинофилов (от 20% и выше эозинофилов в формуле крови), сопровождающая ярко и упорно протекающий аллергический синдром в виде атопического дерматита с выраженным зудом и резистентностью к традиционной терапии или тяжелую бронхиальную астму с частыми приступами.
В 75,3% случаев паразитозы сопровождаются разнообразными функциональными нарушениями со стороны ЖКТ. Рядом работ доказано, что паразитарная инвазия способна вызывать нарушения углеводного обмена, а также дисахаридазную недостаточность за счет снижения уровня лактазы [7, 9].
У большинства детей нарушения адаптации являются одним из важных звеньев патогенетического процесса при паразитозе. Следует отметить, что состояние дезадаптации затрагивает в первую очередь лимфоцитарное звено иммуногенеза, что не может не сказываться на созревании и дифференцировке специфического иммунитета.
Диагностика паразитозов
До настоящего времени ведется поиск простого, доступного и надежного метода диагностики паразитозов. Разработанные методики прямого визуального обнаружения требуют минимальной экспозиции диагностического материала, многократных повторных исследований. Известные способы диагностики глистных инвазий и протозоозов, такие как метод толстого мазка фекалий по Като, метод формалин-эфирного осаждения, перианальный соскоб, микроскопия пузырной и печеночной желчи, имеют ряд недостатков, связанных как с особенностями развития паразита, так и с состоянием макроорганизма и его реактивностью.
Непрямые методы исследования (определение специфических антител) обладают недостаточной специфичностью и достоверностью. Известно, например, что, проходя сложный цикл развития от яйца до взрослого состояния, гельминты меняют свой антигенный состав. Антитела в организме хозяина вырабатываются в основном в ответ на поступление экскретов и секретов гельминта, тогда как в иммунодиагностических реакциях используются соматические антитела. Возникающая неспецифическая сенсибилизация организма, общность некоторых антигенов трематод, простейших и человека создают высокий удельный вес ложноположительных серологических реакций в титрах ниже достоверно диагностических. Таким образом, исследование методом иммуноферментного анализа (ИФА) на гельминты является высокочувствительным, но низкоспецифичным методом. Определение паразитов методом полимеразной цепной реакции (ПЦР) является высокоспецифичным и высокочувствительным методом, но из-за дороговизны и сложности не может быть скрининговым, когда, например, нужно обследовать группу детей из детского учреждения.
Не теряет своей актуальности клинический осмотр ребенка и внимательный учет косвенных признаков паразитоза. Важно отметить возможность течения паразитоза при аллергическом и астеническом синдроме, полилимфаденопатии неясного генеза, при нарушениях кишечного всасывания, углеводного обмена, при затяжном и хроническом течении болезней пищеварительного тракта, гепатоспленомегалии неясного генеза. Течение паразитарной инвазии имеет клинические особенности: обычно признаки поражения минимизированы, заболевание носит стертый характер, обострения полиморфны и неярки. Особенностью обострений заболеваний данной группы является их цикличность с периодом в 11–15 дней.
Косвенными лабораторными признаками паразитоза могут быть анемия, базофилия, эозинофилия, увеличение уровня аспартатаминотранферазы (АСТ).
Кроме того, признаки возможной паразитарной инвазии следует учитывать при оценке результатов инструментального исследования. При ультразвуковом исследовании органов брюшной полости у ребенка старше 3 лет косвенными признаками паразитоза являются гепатоспленомегалия, неравномерность паренхимы печени и селезенки за счет мелких гиперэхогенных сигналов, увеличенные лимфатические узлы в воротах селезенки.
Лечение гельминтозов
Лечение гельминтозов должно начинаться с применения специфических антигельминтных препаратов. Современный арсенал лекарственных средств, используемых для лечения кишечных паразитозов, включает значительное количество препаратов различных химических классов [11]. Они применяются как в клинической практике для лечения выявленных больных, так и с целью массовой профилактики.
Определяя препарат для специфической противопаразитарной терапии, следует понимать, что спектр действия этих препаратов не особенно широк. Практически все препараты этой группы применяются многие десятки лет и целесообразно предположить, что паразиты выработали системы приспособления и заболевание может быть резистентным к проводимой терапии. По данным Г. В. Кадочниковой (2004), эффективность такого традиционного препарата, как Декарис, в современных условиях не достигает 57%. Кроме того, эта группа противопаразитарных средств, к сожалению, имеет ряд побочных эффектов: тошноту, рвоту, абдоминальный синдром.
Таким образом, в современных условиях следует отдавать предпочтение более современным препаратам, которые, во-первых, являются универсальными для лечения как нематодозов, так и смешанных глистных инвазий и активны в отношении такого распространенного паразита, как лямблия. Во-вторых, использование одного противопаразитарного препарата, а не их комбинации, ощутимо снижает риск неприятных побочных эффектов. На сегодняшний день единственный представитель этой группы в нашей стране — альбендазол (Немозол).
Для лечения аскаридоза у детей старшего возраста или при рецидивировании заболевания в настоящее время под наблюдением врача может быть применен комбинированный прием антигельминтных средств (например, альбендазол в течение трех дней, затем — Вермокс в течение трех дней). Непременным условием успешной дегельминтизации больных энтеробиозом являются одновременное лечение всех членов семьи (коллектива) и строгое соблюдение гигиенического режима для исключения реинвазии. Следует отметить, что важное значение имеет ежедневная влажная уборка, так как были описаны казуистические случаи распространения репродуктивного материала остриц на частичках пыли на высоту до 1,5 метра.
В педиатрической клинике МОНИКИ разработаны принципы терапии паразитозов, учитывающие особенности патогенеза инвазии и позволяющие качественно и надежно вылечить данную группу заболеваний. Благодаря применению разработанной схемы терапии удается эффективно предотвратить реинвазию и развитие функциональных нарушений органов пищеварения у детей.
Принципы терапии больных паразитозами
1. Прием антипаразитарных препаратов проводится с учетом вида возбудителя инвазии.
Препараты, применяемые в лечениии аскаридоза:
- Вермокс (мебендазол) (для детей с 2 лет) — по 100 мг 2 раза в сутки в течение 3 дней;
- Пирантел — 10 мг/кг однократно;
- Немозол (альбендазол) (для детей с 2 лет) — 400 мг однократно.
Препараты, применяемые в лечении энтеробиоза:
- Вермокс (мебендазол) (для детей с 2 лет) — 100 мг однократно;
- Пирантел — 10 мг/кг однократно;
- Немозол (альбендазол) (для детей с 2 лет) — 400 мг однократно.
Препараты, применяемые в лечении лямблиоза:
- орнидазол 25–30 мг/кг (если масса тела больше 35 кг — 1000 мг) в два приема в течение 5 дней, 1 день — 1/2 дозы, повторный курс через 7 дней;
- Макмирор (нифурател) — по 15 мг/кг 2 раза в сутки в течение 7 дней;
- Немозол (альбендазол) — по 15 мг/кг однократно в течение 5–7 дней.
2. Лечение паразитоза предусматривает измененные в результате жизнедеятельности паразитов свойства пищеварительного тракта ребенка (функциональные нарушения органов пищеварения, ферментопатия, изменение микробиоценоза) и их коррекцию курсами ферментных препаратов и синбиотиков (табл. 1).
3. Обязательное применение энтеросорбентов и комплекса поливитаминов с микроэлементами (табл. 2 и 3).
Таким образом, разработанные в клинике педиатрии МОНИКИ принципы комплексной терапии паразитозов у детей предусматривают поэтапное восстановление функционального состояния ЖКТ, нарушенного в результате местного и системного влияния паразитов. Применение комплексной терапии позволяет предотвратить дальнейшее развитие функциональных нарушений с формированием органической патологии, а также избежать реинвазии.
Литература
Л. И. Васечкина 1 , кандидат медицинских наук
Т. К. Тюрина, кандидат медицинских наук
Л. П. Пелепец, кандидат биологических наук
А. В. Акинфиев, кандидат медицинских наук
Читайте также:

