Астровирус что это такое у взрослых
Обновлено: 18.04.2024
Инфекции вызванные риновирусом, норовирусом, астровирусом: клиника, диагностика
Риновирус — возбудитель респираторной инфекции — насчитывает свыше ста серотипов. В течение короткого инкубационного периода (2—4 дня) происходит поражение слизистой и подслизистой оболочек верхних дыхательных путей. Максимальное вирусовыделение происходит при появлении первых симптомов заболевания.
Путь передачи — воздушно-капельный (при тесном контакте с больным). Основные симптомы — головная боль, заложенность носа, признаки воспаления верхних дыхательных путей, лихорадка. Как правило, присоединяется вторичная бактериальная инфекция (средний отит, синусит). Заболевание распространено во всём мире и чаще всего возникает в осенне-зимний период.
В связи с огромным разнообразием серотипов после выздоровления формируется слабый иммунитет. В клинических исследованиях применение назальных спреев, содержащих рупринтривир, способствовало уменьшению длительности заболевания. Вакцины против вируса в настоящее время не существует.
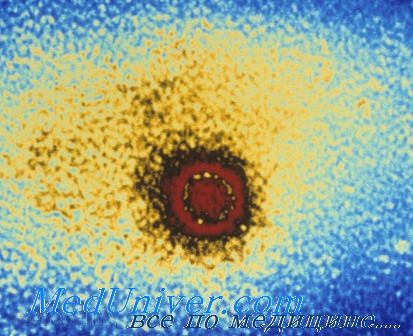
Риновирус
Инфекции вызванные норовирусом и астровирусом
Норовирус относят к группе калицивирусов — возбудителей острой диареи и рвоты в больницах, пансионатах, на круизных лайнерах и в других закрытых общественных местах. Известны три основные генетические группы норовирусов. Астровирусы — мелкие сферические частицы. Насчитывают более пяти серотипов возбудителя.
Репликация вирусов происходит в слизистой оболочке и эпителии тонкой кишки, при этом происходит расширение и выравнивание ворсинок и гиперплазия железистых клеток.
Возбудители обычно вызывают лёгкую саморазрешающуюся острую диарею или внезапную неукротимую рвоту и диарею. Механизм передачи инфекции — фекально-оральный. Первые симптомы возникают после короткого инкубационного периода (24—48 ч). Лечебное учреждение, в котором возникла вспышка норовирусной инфекции, рекомендовано закрывать на карантин, так как при поступлении новых пациентов могут возникнуть определённые трудности в борьбе с инфекцией.
В диагностике предпочтение отдают молекулярно-генетическому методу с применением обратной транскриптазы, так как ИФА и электронная микроскопия менее чувствительны. Для эпидемиологических исследований проводят молекулярно-генетические исследования вирусов, вызвавших заболевание.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо). Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гаст
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо).
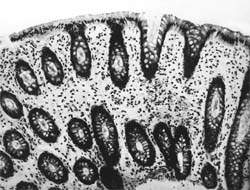 |
| Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимально выраженный катаральный колит. х 100. |
Ротавирусы представляют собой род семейства Reoviridae, который объединяет большое количество сходных по морфологии и антигенной структуре вирусов, вызывающих гастроэнтерит у человека, млекопитающих и птиц. Систематическое изучение ротавирусов человека началось с 1973 года, когда они были обнаружены при электронной микроскопии ультратонких срезов биоптатов слизистой оболочки двенадцатиперстной кишки, полученных от больных острым гастроэнтеритом детей Австралии (Р. Бишоп и соавторы). В том же году Т. Флеветт обнаружил сходный вирус в копрофильтратах больных гастроэнтеритом методом электронной микроскопии при негативном контрастировании препаратов.
Вирусные частицы имеют диаметр от 65 до 75 нм. При проникновении контрастирующего вещества в вирион выявляется электронно-плотный центр диаметром 38 — 40 нм, который представляет собой так называемую сердцевину, окруженную электронно-прозрачным слоем. Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободом, поэтому их стали называть ротавирусами (лат. rota — колесо).
Ротавирусы имеют две белковые оболочки — наружный и внутренний капсиды. Сердцевина содержит внутренние белки и генетический материал, представленный двунитчатой фрагментированной РНК. Геном ротавирусов человека и животных состоит из 11 фрагментов, которые могут быть разделены при электрофорезе в полиакриламидном геле (ПААГ) или агарозе. В составе ротавирусов обнаружено четыре антигена; основной из них — это групповой антиген, обусловленный белком внутреннего капсида. С учетом группоспецифических антигенов все ротавирусы делятся на пять групп: A, B, C, D, E. Ротавирусы одной группы имеют общий групповой антиген, который выявляется иммунологическими реакциями: иммуноферментный анализ, иммунофлюоресценция, иммунная электронная микроскопия и др. Большинство ротавирусов человека и животных относятся к группе A.
| Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями |
Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями. Вирусы в фекалиях заболевших появляются одновременно с развитием клинических симптомов, наибольшая концентрация их в кале (до 109 — 1011 вирусных частиц в 1 г) регистрируется в первые 3 — 5 дней болезни. В эти дни больные представляют наибольшую эпидемиологическую опасность для лиц, контактирующих с ними. Наиболее частым источником заболевания для детей первого года жизни являются инфицированные ротавирусом матери; для взрослых и детей более старшего возраста — дети, в основном из детских коллективов. Возможность заражения человека от животных не доказана.
Патогенез ротавирусной инфекции характеризуется проникновением вируса в эпителиоциты слизистой оболочки желудочно-кишечного тракта, преимущественно тонкой кишки, что приводит к их повреждению и отторжению от ворсинок. Вследствие этого на ворсинках тонкой кишки появляются функционально и структурно незрелые энтроциты с низкой способностью синтезировать пищеварительные ферменты. При ротавирусном гастроэнтерите это проявляется снижением уровня дисахаридаз, развивается вторичная дисахаридазная недостаточность, при которой в просвете тонкой кишки накапливаются нерасщепленные дисахариды, что создает повышенное осмотическое давление и приводит к выводу в просвет кишечника воды и электролитов из тканей организма. Это является основной причиной диареи и дегидратации и определяет основные клинические проявления болезни.
Ротавирусный гастроэнтерит как инфекционное заболевание имеет циклическое течение. Инкубационный период продолжается чаще всего от 12 — 24 часов до двух суток. Клиническая картина ротавирусного гастроэнтерита характеризуется в основном острым началом, однако в ряде случаев может иметь место продромальный период длительности от 12 до 48 — 72 часов. В этот период больные отмечают недомогание, общую слабость, повышенную утомляемость, снижение аппетита, головную боль, познабливание, урчание и неприятные ощущения в животе, умеренно выраженные катаральные явления: заложенность носа, першение в горле, легкий кашель.
В клинической картине ротавирусного гастроэнтерита в период развернутых клинических проявлений ведущими являются синдромы гастроэнтерита и интоксикации. Выраженность диареи и обусловленной ею той или иной степени дегидратации организма, а также токсикоза, продолжительность этих симптомов в значительной мере определяет тяжесть течения заболевания.
Синдром гастроэнтерита характеризуется развитием диареи, снижением аппетита, появлением урчания и болей в животе, тошноты и рвоты. Наиболее типичен для ротавирусного гастроэнтерита обильный водянистый пенистый стул желтого или желто-зеленого цвета. У больных с легким течением заболевания стул может быть кашицеобразным. Как правило, патологические примеси в стуле отсутствуют. Боль локализуется преимущественно в верхней половине живота или является диффузной, она может быть разной интенсивности. Почти всегда она сопровождается громким урчанием в животе.
Синдром интоксикации появляется в самом начале заболевания. Слабость, зачастую резкая, является наиболее частым проявлением этого синдрома; реже отмечается головная боль. При более тяжелом течении имеют место головокружение, обморочное состояние, коллапс. Обращает на себя внимание следующая особенность ротавирусного гастроэнтерита: два ведущих в клинической картине болезни синдрома развиваются в процессе заболевания не всегда однонаправленно; у некоторых больных на фоне сравнительно слабо выраженных диспепсических явлений могут наблюдаться резко выраженные симптомы общей интоксикации, особенно слабость.
Повышение температуры тела не всегда может отмечаться при ротавирусном гастроэнтерите, особенно у взрослых. У некоторых больных может быть озноб без повышения температуры. В то же время нередко в разгар заболевания выраженность лихорадочной реакции варьируется от субфебрильных цифр и выше и может достигать 38 — 39°С как у детей, так и у взрослых.
Важным в диагностическом плане для ротавирусного гастроэнтерита считается сочетание двух ведущих клинических синдромов с симптомами поражения верхних дыхательных путей. Катаральный синдром встречается приблизительно у 50% больных и проявляется в виде гиперемии и зернистости слизистых оболочек мягкого неба, небных дужек, язычка, задней стенки глотки, а также насморка, заложенности носа, кашля, болей в горле. В ряде случаев катаральные симптомы наблюдаются уже в продромальном периоде, до проявления симптомов гастроэнтерита.
В разгар болезни отмечается изменение функционального состояния сердечно-сосудистой системы, чаще у пациентов с более тяжелым течением и при наличии сопутствующих заболеваний органов кровообращения. У большинства пациентов отмечается тенденция к артериальной гипертензии, тахикардия, определяется глухость сердечных тонов при аускультации. У больных с тяжелым течением заболевания, как правило, возникают обмороки и коллапсы из-за выраженных расстройств гемоциркуляции, в генезе которых наряду с токсическими воздействиями существенное значение имеет гиповолемия. Потери жидкости и электролитов вследствие рвоты и диареи могут быть значительными и приводят к развитию дегидратации. Клинические проявления дегидратации зависят от ее степени. При легком и среднетяжелом течении ротавирусного гастроэнтерита отмечается жажда, сухость во рту, слабость, бледность (дегидратация I — II степени), при тяжелом течении наряду с этими симптомами наблюдаются также осиплость голоса, судороги мышц конечностей, акроцианоз, снижение тургора кожи, уменьшение диуреза (дегидратация III степени).
В связи с развитием при ротавирусном гастроэнтерите возможных осложнений, главным образом циркуляторных расстройств, острой сердечно-сосудистой недостаточности, нарушений гомеостаза, выделяют группы больных повышенного риска, в которые включают новорожденных, детей младшего возраста, лиц пожилого возраста, а также больных с тяжелыми сопутствующими заболеваниями. Описанные в литературе и наблюдавшиеся нами случаи ротавирусного заболевания с летальным исходом относятся именно к этим группам.
Выделяются две основные клинические формы ротавирусного заболевания — гастроэнтерическая и энтерическая. Симптомы только острого гастрита (гастритический вариант) встречаются в 3 — 10% случаев. Функциональные и морфологические нарушения со стороны желудочно-кишечного тракта, возникающие при ротавирусном гастроэнтерите в случае наличия у пациентов фоновой гастроэнтерологической патологии, нередко способствуют развитию таких осложнений основного заболевания, как обострение сопутствующих болезней: хронического гастрита, энтероколита, панкреатита, часто в сочетании с выраженными явлениями дисбактериоза кишечника, требующими коррекции при лечении.
Методы диагностики ротавирусной инфекции
При ротавирусном гастроэнтерите гемограмма изменяется следующим образом: в остром периоде заболевания с высокой частотой выявляются лейкоцитоз с нейтрофилезом и повышенная СОЭ. В периоде реконвалесценции картина крови обычно нормализуется полностью. Изменения урограммы у большинства больных имеют кратковременный характер и проявляются чаще всего небольшой протеин-, лейкоцит- и эритроцитурией; в редких случаях в моче появляются гиалиновые цилиндры в незначительном количестве. При тяжелом течении заболевания нарушения функции почек могут быть более выраженными, с повышением уровня мочевины крови, олигоурией или анурией, снижением клубочковой фильтрации. На фоне проводимой терапии указанные изменения быстро исчезают и при повторных обследованиях не отмечаются.
В качестве примера, иллюстрирующего особенности клинического течения ротавирусного гастроэнтерита, приводим выписку из истории болезни.
Лечение: обильное питье солевых растворов, парентеральная регидратационная и дезинтоксикационная терапия — трисоль 1000 мл внутривенное капельное введение, внутрь ферментные препараты: абомин, панкреатин, тансол, карболен. Течение заболевания без осложнений. На третий день болезни — субфебрильная температура, оставалась слабость; боли в животе прекратились. Стул кашицеобразный до пятого дня от начала заболевания. Полное выздоровление наступило на седьмой день болезни.
Дифференциальный диагноз у больных ротавирусным гастроэнтеритом проводят с другими острыми кишечными инфекциями как вирусной так и бактериальной этиологии, прежде всего в тех случаях, когда в клинической картине на первый план выступает синдром гастроэнтерита: с вирусными диареями различной этиологии (аденовирусы, коронавирусы, астровирусы, калицивирусы, вирус Норфолк, энтеровирусы Коксаки и ЕСНО); с гастроинтестинальной формой сальмонеллеза, с гастроэнтеритическим и гастроэнтероколитическим вариантами острой дизентерии, с пищевыми токсикоинфекциями, вызванными условно-патогенными бактериями; с холерой.
Обнаружение специфических антител и нарастание их титра в сыворотке крови больных и переболевших ротавирусным гастроэнтеритом при помощи серологических реакций с целью текущей диагностики на практике в настоящее время широкого распространения не получило и используется в основном для ретроспективного анализа различных эпидемиологических ситуаций.
Методы обнаружения вирусспецифической РНК, которые можно назвать высокочувствительными и специфичными, имеют, однако, ряд недостатков, ограничивающих их практическое применение (необходимость наличия специальной аппаратуры, реактивов, квалифицированного персонала и др.) Наиболее простой метод в этой группе — электрофорез ротавирусной РНК в полиакриламидном геле. Этот метод, позволяющий идентифицировать штаммы вирусов, вызвавшие заболевание, и дать характеристику штаммов, циркулирующих на данной территории, в основном применяется при эпидемиологических исследованиях.
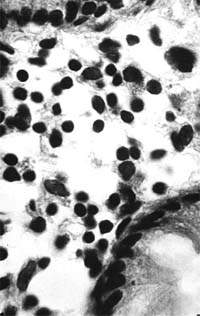 |
| Рисунок 2. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимальное содержание плазматических клеток в собственной пластинке, увеличение в ней числа макрофагов. х 400 |
В клинической практике врач нередко сталкивается с обстоятельствами (сомнительные результаты вирусологических и серологических исследований, случаи микст-инфекций), когда возникает необходимость в применении дополнительных методов для верификации диагноза. С этой целью может быть использован доступный для практического здравоохранения интрументальный метод исследования — ректороманоскопия с аспирационной биопсией слизистой оболочки толстой кишки. При гистологическом, морфометрическом и гистохимическом исследованиях биоптатов при ротавирусном гастроэнтерите выявляются характерные изменения в виде поверхностного минимально выраженного катарального колита с незначительной дистрофией эпителия (рис. 1), снижения числа серотонинсодержащих желудочно-кишечных эндокриноцитов (ЕС-клетки) в эпителиальном пласте кишечных желез, умеренной инфильтрацией собственной пластинки плазматическими клетками и увеличением в ней числа макрофагов (рис. 2). Эти особенности имеют дифференциально-диагностическое значение, поскольку отличаются указанным показателем от других острых кишечных инфекций, что может быть использовано в диагностически сложных случаях.
Здравоохранение в настоящее время не располагает препаратами, обладающими специфическим антиротавирусным действием, поэтому терапия ротавирусного гастроэнтерита является патогенетической. Основные ее цели — борьба с дегидратацией, токсикозом и связанными с ними наиболее часто встречающимися при ротавирусном гастроэнтерите нарушениями функции жизненно важных органов — сердечно-сосудистой системы и органов мочевыделения, степень выраженности которых во многом определяет тяжесть течения заболевания и его прогноз.
Для правильного выбора характера и объема проводимой регидратационной терапии в первую очередь необходимо установить степень дегидратации у того или иного пациента. При эксикозе I — II степени следует ограничиваться пероральной регидратационной терапией (препараты регидрон, глюксолан и др.). При дегидратации III степени целесообразно прибегать к комбинированной парентеральной и пероральной регидратации. Для парентеральной регидратации применяют растворы трисоль, квартасоль, ацесоль и др. С целью дезинтоксикации и улучшения гемодинамики при среднетяжелом и тяжелом течении заболевания показаны коллоидные растворы (гемодез, полиглюкин и др.).
| Для ротавирусной инфекции характерно сочетание гастроэнтерита, интоксикации и симптомов поражения верхних дыхательных путей |
Современными представлениями о патогенезе диарейного синдрома при ротавирусном гастроэнтерите обусловлено и назначение соответствующих средств, способствующих нормализации состояния пищеварительного тракта, а также диеты. Учитывая нарушения активности ряда пищеварительных ферментов, в частности лактазы, рекомендуется исключить в острый период заболевания из пищевого рациона больных молоко и молочные продукты. Кроме того, по этой же причине целесообразно ограничивать и пищу, богатую углеводами. В связи с вышеизложенным, в острый период необходимы энзимные препараты (панзинорм-форте, фестал и др). Кроме того, в остром периоде заболевания могут быть использованы адсорбирующие и вяжущие средства, способствующие ускоренному формированию стула (смекта, карболен и др.) также возможно применение хилака-форте. Высокой частотой дисбактериозов кишечника различной степени выраженности у больных ротавирусным гастроэнтеритом обусловлена необходимость применения в комплексной терапии бактерийных биологических препаратов. Лучшая терапевтическая эффективность при ротавирусном гастроэнтерите отмечена при применении лактосодержащих бактерийных биологических препаратов (ацилакт, лактобактерин и др.), что, по-видимому, связано с заместительным действием бактериальной лактазы, содержащейся в лактобактериях. В последние годы в комплексной терапии ротавирусного гастроэнтерита начал применяться комплексный иммуноглобулиновый препарат (КИП), который разработан и выпускается в МНИИЭМ им. Г. Н. Габричевского. Это первый отечественный иммуноглобулиновый препарат для энтерального применения. КИП характеризуется повышенной концентрацией антител к микроорганизмам, возбудителям острых кишечных инфекций, в том числе ротавирусам, сальмонеллам, шигеллам, эшерихиям и др. Применение КИП в комплексной терапии больных ротавирусным гастроэнтеритом оказывает отчетливый положительный терапевтический эффект, существенно сокращая продолжительность интоксикации и диареи, что открывает новые возможности в лечении этого заболевания.
Литература
1. Букринская А. Г., Грачева Н. М., Васильева В. И. Ротавирусная инфекция. М., 1989.
2. Дроздов С. Г., Покровский В. И., Шекоян Л. А., Машилов В. П. и др. Ротавирусный гастроэнтерит. М., 1982.
3. Новикова А. В. и др. Архив патологии, 1989, №6.
4. Щербаков И. Т. и др. Архив патологии, 2995, №3.
5. Юшук Н. Д., Царегородцев А. Д.. Лекции по инфекционным болезням. М., 1996.
Изучены частота, характер и продолжительность внекишечных проявлений в зависимости от проводимой терапии у детей с норовирусной инфекцией. Установлено, что при норовирусной инфекции у детей, помимо гастроинтестинальных симптомов, нередко отмечаются и друг
Features of the clinical course and approaches to the therapy of norovirus infection in children R. V. Popova, T. A. Ruzhentsova
The frequency, nature and duration of extra-intestinal manifestations depending on the therapy in children with norovirus infection were studied. It was found that in norovirus infection in children, in addition to gastrointestinal symptoms, there are often other symptoms that affect the upper respiratory tract, pancreas, hepatobiliary and urinary systems and heart. An effective drug that relieves the symptoms of norovirus infection, prevents the development of extra-intestinal manifestations and complications, is colloidal silicon dioxide.
Острые кишечные инфекции (ОКИ) продолжают занимать одно из ведущих мест по распространенности среди других заболеваний. В последние десятилетия анализ их этиологической структуры и характера свидетельствует о существенных изменениях, происходящих как за счет появления новых лабораторных методов диагностики, так и за счет модификации возбудителей. Важную роль играет и трансформация иммунного ответа организма человека под влиянием неблагоприятной экологической обстановки, резкого снижения количества натуральных продуктов питания с увеличением употребления консервантов и стабилизаторов.
По данным исследователей, в настоящее время во многих странах, несмотря на достижения здравоохранения, отмечается рост числа вирусных ОКИ [1–6].
Ведущими возбудителями по-прежнему остаются ротавирусы. Наряду с ними в последние годы отмечается значительный рост частоты регистрации норовирусной инфекции с 2–5% из всех случаев секреторных диарей до 10–26,5% от всех выявленных эпизодов ОКИ [1, 7–10]. Пик заболеваемости, по данным различных авторов, приходится на период с января по апрель [1, 2, 9]. Болеют преимущественно дети в возрасте от рождения до 3 лет, среди которых чаще регистрируются среднетяжелые формы заболевания [1].
Наиболее вероятно, что частота норовирусной инфекции существенно выше, поскольку многие взрослые и подростки к врачам не обращаются из-за нетяжелого течения с преобладанием легких форм. В то же время, по результатам исследований проб питьевой воды, норовирусы нередко опережают ротавирусы по частоте их выявления, выходя на второе место после аденовирусов [11].
Активизации эпидемического процесса норовирусной инфекции может способствовать и длительный период выделения вируса после купирования симптомов ОКИ, составляющий в среднем 28 суток и достигающий 182 дня у иммуноскомпрометированных пациентов [12]. В связи с этим, в соответствии с действующими на сегодняшний день рекомендациями, при отсутствии клинической симптоматики дети могут посещать организованные коллективы вне зависимости от результатов лабораторной диагностики, что сопровождается неуточненным в настоящее время риском распространения инфекции. В то же время норовирусная инфекция отличается высокой контагиозностью: всего 10 частиц вируса достаточно для передачи ее от больного к восприимчивому организму [13]. Возбудитель сохраняет свою жизнеспособность в окружающей среде, на различных поверхностях до 4 недель, устойчив к физическим и химическим воздействиям. Как показали исследования, среди пациентов с подтвержденной норовирусной этиологией ОКИ преобладают дети из организованных коллективов (61%) с моноинфекцией — 93% [1]. Помимо того, в ходе изучения особенностей возбудителя была доказана высокая скорость молекулярной эволюции норовирусов, приводящая к частому возникновению и быстрому глобальному распространению его новых эпидемических вариантов [14]. Все это диктует необходимость своевременного выявления и адекватного лечения больных.
При лабораторном исследовании в копрограмме может быть непереваренная клетчатка, нейтральный жир, зерна крахмала, лейкоциты [1]. В анализе крови у большинства пациентов отмечается лимфоцитоз при нормальном количестве лейкоцитов, при выраженной клинической симптоматике возможны нейтрофильный лейкоцитоз, увеличение скорости оседания эритроцитов и повышение концентрации мочевины. Проявления ОКИ нередко не ограничиваются желудочно-кишечным трактом. Помимо гастроэнтеритического синдрома, почти у всех пациентов отмечается интоксикация, проявляющаяся вялостью, слабостью, адинамией, снижением аппетита, бледностью кожных покровов [1].
Лечение норовирусной инфекции проводится по принятым в Российской Федерации стандартам терапии ОКИ, включающим регидратационные растворы, энтеросорбенты, пробиотики, при необходимости жаропонижающие [15, 17]. Отечественными авторами рекомендуется назначение противовирусной терапии, хотя этот вопрос по-прежнему, учитывая зарубежные данные, остается дискутабельным. В опубликованных ранее работах было показано возможное появление катаральных изменений верхних дыхательных путей: насморка, кашля, признаков ринофарингита при норовирусной инфекции [5, 15, 16].
В литературе есть единичные указания на возможность развития у пациентов, больных норовирусной инфекцией, пневмоний, отитов, цистита, кардиомиопатии, менингита [17–19]. Зарубежные авторы отмечают, что при норовирусной этиологии чаще, чем при ротавирусной, отмечается судорожный синдром [18]. Однако подробного анализа распространенности, факторов риска развития, особенностей течения, характера и длительности внекишечных проявлений и связанных с этим осложнений не проводилось. Не было оценено влияние различных подходов к терапии норовирусной инфекции на формирование той или иной симптоматики у пациентов.
Целью данного исследования было изучить частоту, характер и продолжительность внекишечных проявлений в зависимости от проводимой терапии у детей с норовирусной инфекцией.
Материалы и методы исследования
В исследование включили 80 детей в возрасте от 8 месяцев до 6 лет, госпитализированных в инфекционное отделение для детей ГБУЗ МО МГКБ г. Мытищи. У всех пациентов норовирусная этиология ОКИ была подтверждена лабораторно методом полимеразно-цепной реакции. Преобладали дети в возрасте от одного года до трех лет (42 ребенка — 52%), 27 пациентов (34%) относились к возрастной группе от трех до 6 лет и 11 (14%) — от 8 месяцев до одного года. Большинство пациентов (94%) имели среднетяжелую форму ОКИ. Продолжительность заболевания от момента начала до включения в исследование составила от 1 до 3 суток включительно. Выявление какой-либо другой этиологии относилось к критериям исключения.
При поступлении в стационар, помимо клинического осмотра, всем детям были проведены лабораторные и инструментальные обследования для уточнения состояния органов брюшной полости, сердечно-сосудистой и мочевыделительной систем. Оценивали выраженность гастроэнтерологических, респираторных и интоксикационных проявлений, результаты клинического анализа крови, общего анализа мочи, уровни МВ-креатинкиназы, лактатдегидрогеназы, аспарагиновой трансаминазы, аланиновой трансаминазы в сыворотке крови. Детям проводили электрокардиографию (ЭКГ), а также ультразвуковое исследование (УЗИ) органов брюшной полости и почек. Этиологию ОКИ определяли при помощи полимеразно-цепной реакции.
Пациентов с наличием в анамнезе заболеваний сердечно-сосудистой, мочевыделительной и панкреатогепатобилиарной систем в исследование не включали.
Повторные клинические осмотры до купирования симптомов осуществляли ежедневно и, при необходимости, чаще, оценивали длительность каждого из проявлений. При наличии отклонений по результатам лабораторного и/или инструментального обследования или выявлении показаний в последующие дни нахождения в стационаре через 3–5 дней оценивали показатели повторно, а при отсутствии нормализации — еще раз, на 18–25 день от начала заболевания.
Все пациенты получали стандартную, рекомендуемую при ОКИ, безлактозную диету. Детям первого года жизни, находящимся на грудном вскармливании, его рекомендовали продолжить. Базисная терапия состояла из регидратационных глюкозосолевых растворов, назначенных только перорально — в 39%, парентерально — в 25% и парентерально, а затем перорально — в 36%. Энтеросорбенты получали 81% детей, пробиотики — 89%, жаропонижающие (ибупрофен и/или парацетамол) при температуре более 38–39 °C — 64%.
В зависимости от особенностей стартовой терапии, которая в большинстве случаев начиналась на дому, пациенты были распределены на три группы. В 1?ю группу было отнесено 24 ребенка, получавших с первого дня проявлений заболевания энтеросорбенты и регидратационную терапию, во 2?ю группу вошел 41 больной, которым комплексная терапия была назначена позднее, на вторые или третьи сутки, в 3?ю было включено 15 пациентов, не принимавших энтеросорбенты. Эти препараты не были назначены врачами в большинстве случаев из-за отсутствия диареи, иногда — из-за отказа или негативной реакции у детей.
Статистическая обработка всех полученных данных осуществлялась на персональном компьютере с использованием программы Statistica, версия 6.1 (StatSoft Inc., США). Различия между рассчитанными показателями в группах оценивали по двустороннему Z-критерию, статистически значимыми считали при вероятности > 95% (p < 0,05).
Результаты и обсуждение
Среди основных клинических симптомов у всех пациентов были выделены: рвота от 1 до 25 раз в сутки, отсутствие аппетита, вялость, бледность и повышение температуры тела. Диарея наблюдалась у 81% детей, чаще с конца первых или на вторые сутки. На боли в животе жаловались 48% (13 детей) пациентов из возрастной группы от 3 до 6 лет. У детей более раннего возраста болевой синдром не оценивали из-за высокой вероятности неправильного определения.
У наблюдавшихся пациентов регистрировали разнообразные внекишечные проявления, представленные на рис. Из них лечащие врачи в первую очередь отмечали признаки ринита с заложенностью носа, умеренными водянистыми выделениями, гиперемией и отечностью носовых ходов в сочетании с незначительно или умеренно выраженным фарингитом (у 34% — 27 детей).
По данным дополнительных исследований, среди детей с норовирусной инфекцией в 71,25% (у 57 детей) были выявлены те или иные отклонения на ЭКГ: нарушения реполяризации (у 54% — 43 детей), снижение вольтажа (у 20% — 16 детей), суправентрикулярная или вентрикулярная экстрасистолия (у 7,5% — 6 детей). У 8 детей было отмечено сочетание изменений. Повышение уровней активности МВ?креатинкиназы изолированно или одновременно с увеличением значений лактатдегидрогеназы и/или соотношения аспарагиновой и аланиновой трансаминаз регистрировали у 36% детей.
По результатам УЗИ органов брюшной полости, изменения печени и/или поджелудочной железы были выявлены у 42 детей (53%). Нарушения структуры почек, чаще — уплотнения стенок чашечно-лоханочной системы, было выявлено у 30 детей (38%).
Основные симптомы ОКИ у всех пациентов были купированы в течение 2–4 суток от момента начала адекватной терапии.
Отклонения, выявленные по данным ЭКГ и лабораторного обследования, у 64% при повторной оценке показателей, через 3–5 дней, не выявлялись. Однако у 7,5% пациентов сохранялись нарушения реполяризации, снижение вольтажа и повышение МВ?креатинкиназы сохранялись, несмотря на отсутствие основных симптомов ОКИ, что позволило подозревать вероятный миокардит у этих детей. Через 18–25 дней отклонения сохранялись у 2 пациентов (3,5% из группы детей с выявленными нарушениями на ЭКГ).
По данным УЗИ, через 3 недели купировались изменения поджелудочной железы у 81% (34 детей), печени — у 74% (у 31 ребенка), почек — в 100%. Симптомы инфекции мочевыводящих путей также не отмечались ни в одном случае.
Анализ результатов лабораторного и инструментального обследования в группах, различавшихся по особенностям терапии энтеросорбентами, показал, что в 1?й группе, у детей, получавших с первых суток Полисорб МП, не было случаев сохранения симптоматики внекишечных проявлений более 3 недель. Нарушения на ЭКГ, полностью купировавшиеся к моменту повторного обследования через 3–5 суток, были выявлены у 2 детей (8%). У 3 пациентов (12,5%) были выявлены изменения поджелудочной железы и у 2 из них — печени. Инфекций мочевыводящих путей и уплотнений чашечно-лоханочной системы, по данным УЗИ, в этой группе пациентов не выявляли. У 2 детей (8%) была отмечена анемия легкой степени.
Как видно из табл., частота длительно сохраняющихся внекишечных изменений была выше в группе, не получавшей энтеросорбенты. Очевидно, что отсутствие диареи во многих случаях было связано как с преимущественным поражением верхних отделов желудочно-кишечного тракта, так и, возможно, с обезвоживанием, что также усугубляло внекишечную симптоматику и не могло служить поводом для отказа от энтеросорбирующей терапии. Назначение энтеросорбентов на 2–3 сутки от начала заболевания приводило к снижению частоты внекишечных проявлений по сравнению с группой, которым энтеросорбирующие препараты назначены не были.
Анализ терапии показал, что применение диоксида кремния коллоидного (Полисорб МП) с первых суток у 12 детей прерывало симптомы ОКИ. На фоне терапии диарея ограничивалась неоформленным стулом 2–5 раз в течение одного дня или не проявлялась вовсе, температура тела снижалась до нормальных значений. Изменения поджелудочной железы, выявленные у 1 ребенка, были незначительны и купировались вместе с основными проявлениями ОКИ. Случаев отказа от терапии диоксидом кремния коллоидным из-за органолептических свойств, индивидуальной непереносимости или нежелательных явлений не было.
Выбор данного препарата обусловлен его доказанной безопасностью, а также высокой эффективностью (с высокой удельной поверхностью сорбции частиц более 300 м 2 /г), а также отличными протеонектическими свойствами, всеми прочими свойствами современных энтеросорбентов и длительным постклиническим опытом применения (более 20 лет). Протеонектическими свойствами Полисорба МП объясняется его способность связывать значительные количества микроорганизмов — до 10 млрд микробных тел на 1 г препарата и более, независимо от видовой принадлежности, а также различные эндо и экзотоксины [20].
Таким образом, полученные результаты подчеркивают разнообразие проявлений ОКИ, не ограничивающихся только желудочно-кишечным трактом. Выявленные изменения печени, поджелудочной железы, мочевыделительной системы, сердца у некоторых пациентов сохраняются длительно, более 3 недель с момента появления первых симптомов норовирусной инфекции.
Выводы
- При норовирусной инфекции у детей помимо гастроинтестинальных симптомов нередко отмечаются и другие, затрагивающие верхние дыхательные пути, поджелудочную железу, гепатобилиарную и мочевыделительную систему, сердце.
- Комплексная терапия, соответствующая стандартам лечения ОКИ вирусной этиологии, должна проводиться с первого дня заболевания.
- Эффективным лекарственным препаратом, купирующим симптомы норовирусной инфекции, препятствующим развитию внекишечных проявлений и осложнений, является Полисорб МП.
Литература
Р. В. Попова
Т. А. Руженцова 1 , доктор медицинских наук
ФБУН ЦНИИЭ Роспотребнадзора, Москва
Особенности течения и подходы к терапии норовирусной инфекции у детей/ Р. В. Попова, Т. А. Руженцова
Для цитирования: Лечащий врач № 11/2018; Номера страниц в выпуске: 44-48
Теги: вирусная инфекция, дети, внекишечные проявления
Комплексное молекулярно-генетическое исследование для выявления и дифференциации наиболее распространенных возбудителей острых кишечных инфекций (ОКИ) – ротавирусы группы А (Rotavirus), норовирусы 2 генотипа (Norovirus 2 генонотип), астровирусы (Astrovirus). Исследование позволяет выявить генетический материал (РНК) возбудителей в кале и установить этиологию заболевания. Данные патогены являются основной причиной наиболее тяжелого гастроэнтерита у детей грудного и раннего возраста, а также у взрослых.
Анализ качественный - по каждому виду инфекции выдается результат "обнаружено/не обнаружено".
Синонимы русские
Скрининг на кишечные инфекции: ротавирус, норовирус, астровирус.
Какой биоматериал можно использовать для исследования?
Метод исследования
ПЦР в режиме реального времени.
Как правильно подготовиться к исследованию?
- Исследование рекомендуется проводить до начала приема антибиотиков и других антибактериальных химиотерапевтических препаратов.
- Исключить прием слабительных препаратов, введение ректальных свечей, масел, ограничить (по согласованию с врачом) прием медикаментов, влияющих на перистальтику кишечника (белладонна, пилокарпин и др.), и препаратов, влияющих на окраску кала (железо, висмут, сернокислый барий), в течение 72 часов до сбора кала.
Общая информация об исследовании
Острые кишечные инфекции (ОКИ) – группа заболеваний, обусловленных вирусами, бактериями или паразитами, для которых характерен фекально-оральный механизм передачи. Общими для данных инфекций являются факторы передачи: пищевые продукты, вода, инфицированные бытовые предметы и грязные руки. Первые симптомы возникают через несколько часов или дней после инфицирования, начало резкое, с появлением частого жидкого стула, рвоты, боли в животе, признаков интоксикации (лихорадки, озноба, тошноты). Заболевание может носить групповой характер и проявиться у нескольких человек, употреблявших инфицированную пищу или воду.
Согласно официальной статистике, в России до 65-67% заболеваний этой группы составляют ОКИ неуточненной этиологии. Если возбудитель инфекции неизвестен, эффективность противоэпидемических мероприятий ограничивается. Соотношение частоты выявления вирусных и бактериальных патогенов варьируется в разных возрастах: у детей до 3 лет на долю вирусных агентов приходится 80-90% заболеваний, на долю бактериальных – 10-20%; среди взрослых пациентов доля вирусных возбудителей снижается до 30%.
Ротавирусная инфекция – это острое вирусное заболевание, передающееся фекально-оральным путем. Его возбудителями являются РНКсодержащие ротавирусы (Rotavirus). Источник инфекции – больной человек.
Для ротавирусов характерна сезонность: чаще всего ими заражаются в холодное время года. Инкубационный период длится от 15 часов до нескольких суток, начало заболевания острое, с тошнотой, рвотой, диареей, иногда лихорадкой. Если болезнь не лечить, к ним могут добавиться обезвоживание и нарушение электролитного и кислотно-щелочного баланса. Хотя иногда ротавирусная инфекция протекает бессимптомно. После перенесенного заболевания иммунитет нестойкий, поэтому возможен рецидив.
В соответствии с данными зарубежной литературы, норовирус – наиболее частый возбудитель вспышек ОКИ небактериальной этиологии. Эта особенность связана с низкой инфицирующей дозой и высокой устойчивостью в окружающей среде. ПЦР является "золотым стандартом" в клинической диагностике норовирусных инфекций.
Норовирус (Norovirus) – это РНКсодержащий вирус, относящийся к семейству Caliciviridae и приводящий к возникновению желудочно-кишечной инфекции в форме острого гастроэнтерита. Норовирусы классифицируются на шесть геногрупп: GI – GVI. В соответствии со сложившейся номенклатурой, известно около 38 генотипов данных вирусов. Для человека наиболее патогенными являются норовирусы GI, GII, GIV. По современным литературным данным, самой распространенной геногруппой в инфицировании человека является геногруппа GII. Она содержит до 19 генотипов и генотипы GII.3, GII.6, GII.12 ассоциированы с передачей инфекции через продукты питания. Норовирусная инфекция является высококонтагиозным заболеванием и может протекать в виде единичных случаев, групповых случаев и вспышек. Данный возбудитель является причиной возникновения более 90% небактериальной природы и около 50 % всех случаев гастроэнтеритов. К инфекции восприимчивы люди всех возрастных групп, но чаще описываются случаи заболевания у детей школьного возраста и взрослых.
Несмотря на несколько меньшую в сравнении с рота- и норовирусами распространенность, астровирусы составляют значительный пласт кишечных инфекций, у трети пациентов протекающий с явлениями колита. Ротавирусы группы А являются наиболее частой причиной спорадических заболеваний ОКИ у детей, а ДНКсодержащий аденовирус F (серотипы 40 и 41) нередко вызывает вспышки гастроэнтеритов у детей младшего возраста.
Астровирусная инфекция – это острое вирусное заболевание с фекально-оральным путем передачи. Его возбудителями являются РНКсодержащие астровирусы (Astrovirus). Пик заболеваемости приходится на холодное время года. Инкубационный период составляет 3-4 дня. Инфекция проявляется в виде острого гастроэнтерита (общее недомогание, головная боль, тошнота, диарея, небольшое повышение температуры, иногда рвота) и чаще развивается у детей (особенно в возрасте до 2 лет), однако может встречаться и у взрослых. Она напоминает ротовирусную инфекцию, однако протекает легче. Заболевание длится, как правило, не более 5 дней, специфического лечения не требует и заканчивается выздоровлением.
Нередко астровирусная инфекция протекает бессимптомно. Выделение вируса с калом происходит в течение 3 недель с момента заражения, поэтому выявление возбудителя методом ПЦР рекомендуется проводить именно в это время.
Для выявления и дифференциальной диагностики кишечных инфекций используются культуральные и молекулярно-генетические методы исследования генетического материала возбудителя в кале и определение концентрации специфических иммуноглобулинов в крови. ПЦР обладает преимуществом перед культуральными методами благодаря высокой специфичности и чувствительности исследования. Данный анализ позволяет со 100-процентной точностью определить возбудителя кишечного заболевания, а быстрая диагностика острых кишечных инфекций помогает избежать лишних процедур и оперативных вмешательств, своевременно начать лечение и ограничить очаг распространения инфекции.
Для чего используется исследование?
- Для установления этиологического фактора острой кишечной инфекции;
- для дифференциальной диагностики причин острого гастроэнтероколита (воспаления ЖКТ).
Когда назначается исследование?
- Установление этиологического фактора острой кишечной инфекции;
- дифференциальная диагностика причин острого гастроэнтерита;
- дифференциальная диагностика причин острой диареи;
- при симптомах вирусного гастроэнтерита (боли в животе, диарея, рвота, метеоризм, лихорадка);
- одновременное или последовательное развитие ОКИ у нескольких членов семьи, у детей в детском учреждении или пациентов в стационаре;
- "обострение" симптоматики ОКИ у госпитализированного с этим диагнозом пациента (внутрибольничная инфекция);
- по эпидемиологическим показаниям.
Что означают результаты?
Референсные значения: не обнаружено.
Norovirus 2 генотип
Анализ результатов проводят с помощью программного обеспечения используемого прибора для проведения ПЦР c детекцией в режиме "реального времени".
- отсутствие РНК возбудителя в исследуемом материале;
- уровень РНК в исследуемом материале ниже пределов детекции метода.
Также рекомендуется
112 Острые кишечные инфекции, скрининг (Shigellaspp., E. coli (EIEC), Salmonella spp., Campylobacter spp., Adenovirus F, Rotavirus A, Norovirus 2 генотип, Astrovirus)
38 Yersinia pseudotuberculosis, ДНК [ПЦР]
13 Посев кала на условно-патогенную флору с определением чувствительности к антибиотикам
Читайте также:

