Атипичная хроническая инфекция что это
Обновлено: 23.04.2024
Татьяна Владимировна Спичак, профессор, доктор медицинских наук:
В сегодняшней лекции я хотела бы коснуться ряда вопросов, связанных с атипичными инфекциями. Они по-прежнему продолжают волновать многих практикующих врачей. Ни для кого из нас не секрет, что успех лечения инфекции дыхательных путей в значительной мере определяется достоверностью этиологической диагностики.
С этим вопросом у нас, к сожалению, особенно в амбулаторной практике дело обстоит не очень благополучно. Если говорить о распространенности атипичных инфекций у детей, то литературные источники приводят нам достаточно большой разброс данных.
Мы знаем, что острый бронхит, как правило, обусловлен вирусной этиологией болезни. Что касается атипичных возбудителей, то с. Pneumonia и m. Pnemoniae диагностируют в 4% и 17% случаев.
При внебольничной пневмонии микоплазменная инфекция встречается у детей от 7% до 27%. А инфекция с. Pneumonia в 6% или 32%.
В последнее время большое внимание уделяется ассоциациям пневмококковой и атипичной инфекции, которые по данным наших зарубежных коллег составляют от 8% до 23%. Мы неспроста затрагиваем этот вопрос, потому что (как мы убедились на собственном опыте) ассоциация пневмококковой и микоплазменной инфекции действительно приводит к более тяжелому течению пневмонии по сравнению с монобактериальной этиологией пневмонии.
Всем хорошо известно, что этиологическая структура пневмонии имеет определенную возрастную зависимость, которая распространяется и на атипичные возбудители. По крайней мере, микоплазменную инфекцию чаще диагностируюn у детей 2-4-х лет и подростков.
С. Trachomatis, как правило, диагностируют у детей первого полугодия жизни. С. Pneumonia инфицирует чаще всего детей старше пяти лет. Хламидийная инфекция может произойти в любой последующий период жизни.
Появилось много литературных данных о роли хламидийной инфекции при бронхиальной астме у детей, особенно при ее тяжелом течении. Но если обратить внимание на представленную таблицу, мы видим очень большой разброс данных по частоте встречаемости хламидийной инфекции при бронхиальной астме. Причем зачастую несопоставимых из-за того, что используются разные методы исследований.
Кроме того, я хотела бы обратить внимание не только тех, кто получает из этой лекции просто информацию, но и тех, кто проводит подобные исследования. Очень важно иметь контрольную группу. К сожалению, во многих исследованиях это отсутствует.
Диагностика атипичных инфекций остается достаточно сложной по сегодняшний день. Это связано с тем, что при данных инфекциях отсутствуют специфические клинические и рентгенологические признаки, которые помогли бы нам в этиологической диагностике.
Главным образом это касается респираторно-хламидийной инфекции. Микоплазменную инфекцию мы еще можем как-то заподозрить по клиническим признакам, основываясь на своеобразных крепитирующих мелкопузырчатых влажных хрипах, нередко ассиметричных. По маловыразительной рентгенологической картине, при которой, как правило, мы наблюдаем усиление мелких элементов легочного рисунка. В большинстве случаев отсутствуют типичные легочные инфильтрации.
Основными методами диагностики атипичных инфекций являются лабораторные методы диагностики. Несмотря на большое число существующих методов, которые, казалось бы, должны нам помогать в диагностике этих инфекций, здесь тоже есть определенные проблемы.
Наибольшее распространение получили иммунологические методы исследования. В последнее время все чаще и шире используется полимеразная цепная реакция. Культуральный и морфологический методы используются, главным образом, в научных целях.
Я хотела бы обратить ваше внимание на то, что, несмотря на многообразие методов исследования, чувствительность и специфичность таковы, что ни один из методов не позволяет нам выявлять возбудитель в 100% случаев. Нам приходится пользоваться, как минимум, двумя методами исследования по более достоверной диагностике.
Есть проблема. Все перечисленные методы исследования могут нам давать либо ложноположительные, либо ложноотрицательные результаты. Это вполне естественно чревато либо лечением псевдобольных, либо распространением инфекции у нераспознанных больных.
Иммунологические методы основаны на использовании диагностикумы на основе родо- и видоспецифических антигенов. На выявлении специфических антител в сыворотке крови и секретах инфицированного организма в процессе иммунного ответа не внедрение возбудителей.
Из этих методов рекомендуется в настоящее время пользоваться методом микроиммунофлюоресценции (МИФ) и иммуноферментным анализом (ИФА).
Методы имеют безусловные достоинства. Прежде всего, возможность избежать ложноотрицательных результатов. В ряде случаев определить стадию заболевания. Но серьезным недостатком метода серологической диагностики является ретроспективная диагностика. Антитела класса М появляются лишь на пятый день от начала болезни.
Мы не можем ставить диагноз на основании данных методов исследования в более ранние сроки. Антитела класса М могут самостоятельно исчезнуть через 2-3 месяца, даже не прибегая к лечению. Что касается антител класса А, то они появляются гораздо позже – на 5 – 14 день – и тоже, как правило, исчезают через 2-3 месяца, но уже при условии проведения специальной терапии.
Если этого не происходит, то обнаружение антител класса А в более поздние сроки указывает на хроническую или персистирующую инфекцию.
Самыми последними появляются антитела класса G. На 15 – 20 день. Особенностью этих антител является то, что они могут сохраняться в низких титрах на протяжении ряда лет, отражая так называемую следовую реакцию после перенесенной инфекции.
Что касается диагностики микоплазменной инфекции, то следует обратить внимание на то, что при данной инфекции наблюдается длительная циркуляция АТ класса М. Для данной инфекции характерно большее развитие острых процессов. А реинфицирование отмечается редко.
Для выявления антигена возбудителя используют метод иммунофлюоресцентной микроскопии. К сожалению, этот метод не лишен недостатков, поскольку его чувствительность невысока, специфичность зависит от навыков персонала.
Полимеразная цепная реакция. Как известно, метод относится к молекулярно-биологическим. Основан на выявлении в составе биологического материала фрагментов ДНК или РНК, специфических для вида возбудителя. Этот метод отличает высочайшая чувствительность и специфичность. С помощью данного метода мы можем диагностировать на ранних стадиях болезнь и выявлять минимальное количество возбудителей вне зависимости от его жизнеспособности.
К сожалению, и этот метод не лишен недостатков. Мы имеем возможность получить и ложноположительные результаты в силу такой высокой чувствительности метода. Любая загрязняющая ДНК может дать нам такой результат.
Реакция может быть подавлена биологическим материалом. Это может привести к ложноотрицательному результату.
Показания к назначению лечения при атипичных инфекциях достаточно традиционные. Принято лечить острую инфекцию, реинфекцию и обострение хронической инфекции. Казалось бы, все просто. Но, к сожалению, достаточно непросто в реальной жизни определить стадию болезни и правильно сориентироваться с лечением, руководствуясь не только теми результатами, которые мы получаем на листах бумаги.
При диагностике респираторной хламидийной инфекции многие клиницисты до сих пор используют критерии Грейстона (Grayston G. T.). Они основаны на результатах реакции по определению специфических антител класса М и G. При выявлении специфических антител класса М и высоких титров антител класса G или при четырехкратном увеличении титра антител класса G в парных сыворотках можно говорить об острой инфекции.
При реинфекции хламидийной инфекции антитела класса М отсутствуют. Но наблюдается быстрое, буквально в течение одной-двух недель, появление антител класса G. Или также как при острой инфекции четырехкратное увеличение в парных сыворотках.
Но поскольку речь идет о лечении детей, то мы предъявляем особые требования к антибактериальным препаратам. Они должны быть не только эффективными, но и максимально безопасными. Наш выбор сводится к макролидным препаратам.
Я не буду останавливаться на классификации макролидов. Она вам прекрасно известна. Хочу еще раз подчеркнуть их уникальные свойства как группы антибактериальных препаратов. Они относятся к числу наиболее безопасных антибиотиков и являются тканевыми антибиотиками, поскольку концентрация в инфицированных тканях во много раз превышает сывороточные.
Фармакодинамика современных макролидов позволяет их назначать 2-3 раза в сутки, что повышает комлпаентность.
Данная группа препаратов обладает уникальным постантибиотическим эффектом. Даже после прекращения введения антибактериального препарата, сохраняясь в инфицированных тканях, препарат продолжает еще обеспечивать терапевтические концентрации в течение еще 5-7 дней.
По сравнению с четырнадцатью членами макролидов его характеризует низкая частота лекарственных взаимодействий, хороший профиль безопасности и низкий уровень приобретенной резистентности.
В отношении длительности курсового лечения при атипичных инфекциях принято во многих руководствах пользоваться десятидневными курсами лечения макролидными препаратами. Но некоторые руководства предлагают более длительные курсы лечения в течение 2-3 недель. Полагают, что это позволит осуществить профилактику персистирующей или хронической инфекции.
Подобное лечение острых инфекций может вызвать вполне оправданные возражения.
Что касается хронической инфекции (а здесь речь идет о хронической хламидийной инфекции), то приняты более длительные трехнедельные курсы лечения.
Оценка эффективности терапии осуществляется по исчезновению антигенового возбудителя, по снижению или исчезновению титра специфических антител. Я неспроста обращала ваше внимание на особенности динамики антителообразования при атипичных инфекциях. Контрольное исследование следует проводить не ранее, чем через 2-3 месяца.
В заключение я хотела бы привести результаты недавно завершенного нами исследования по определению этиологической структуры внебольничных пневмоний у детей и оценке эффективности рациональной антибиотиковой терапии.
Для этих целей мы использовали ПЦР-диагностику. Определили специфические антитела указанных классов методом ИФА.
Из 63-х детей у 57-ми был определен инфекционный патоген, что обеспечило 90,5% выявления этиологически значимого агента.
По совокупности лабораторных методов исследования современная этиологическая структура внебольничной пневмонии у детей по нашим данным выглядит следующим образом. Мы видим, что пневмококк остается лидирующим или весьма значимым типичным бактериальным патогеном при внебольничных пневмониях.
В то же время мы видим, что высока частота и микоплазменных инфекций при пневмонии у детей. Этого нельзя сказать о хламидийных пневмониях, потому что их частота не превышала в наших данных 14%. В каждом седьмом случае мы имели дело со смешанной бактериальной инфекцией при внебольничной пневмонии, обусловленной, главным образом, сочетанием пневмококка и микоплазменной инфекции.
Течение пневмонии было более тяжелым, чем при монопневмококковой инфекции.
Наши наблюдения (несмотря на то, что когда мы уточнили этиологию, группы оказались не такими многочисленными) позволили отметить особенности внебольничных пневмоний, на которые обращают внимание в современных руководствах. По крайней мере, в зарубежных.
Действительно в первые дни маловыразительная клиническая картина. Достаточно редко определяются хрипы и типичная физикальная симптоматика. Но у большинства детей присутствует синдром дыхательных расстройств. Это, в первую очередь, касается пневмококковых пневмоний. В меньшей степени это касается микоплазменной и хламидийной пневмонии.
Синдром дыхательных расстройств, который ведет в число наиболее достоверных диагностических и клинических признаков, в большей степени работает у детей до пяти лет. Дети с микоплазменной и хламидийной пневмонией в нашем наблюдении были школьного возраста.
При лечении внебольничных пневмоний мы поступали также, как поступают все практикующие врачи. Мы назначали антибактериальную терапию эмпирически, в соответствии с принципами рациональной антибиотиковой терапии до получения результатов проведенных нами биологических и других исследований.
В заключение я хотела бы сказать о том, что атипичные инфекции остаются достаточно хорошо распространенными у детей и подростков при инфекциях дыхательных путей. Если мы хотим повысить эффективность и улучшить диагностику атипичных инфекций, то нам надо обращать внимание на микробиологические лаборатории, на то оборудование, на котором они работают, и на приобретение качественных тест-систем.
Мы можем сказать, что макролидные антибиотики являются препаратами выбора при инфекции дыхательных путей и внебольничной пневмонии. В первую очередь, в период сезонных вспышек микоплазменной или хламидийной инфекции. А также у детей, имеющих признаки аллергии на бета-лактамные антибиотики.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус Эпштейна–Барр: причины появления, симптомы, диагностика и способы лечения.
Вирус Эпштейна–Барр может инфицировать различные типы клеток, включая B-клетки иммунной системы (разновидность лейкоцитов – белых кровяных телец) и эпителиальные клетки слизистых оболочек.
ВЭБ является представителем ДНК-содержащих вирусов из семейства Herpesviridae (герпесвирусы), подсемейства гамма-герпесвирусов и рода лимфокриптовирусов. В процессе репликации (самокопирования) вируса экспрессируется свыше 70 различных вирусспецифических белков. В настоящее время выделены группы иммуногенных белков, определение антител к которым дает возможность дифференцировать стадию инфекции (ЕА – ранний антиген, ЕВNА-1 — ядерный антиген, VCA — капсидный антиген, LMP — латентный мембранный белок).
Другой способ заражения – контактно-бытовой (вирус передается через зубные щетки, столовые приборы, полотенца и т.д.). ВЭБ также может распространяться через кровь и сперму.
ВЭБ размножается в В-лимфоцитах и эпителиальных клетках, в связи с чем характерно многообразие клинических проявлений данной патологии. Важной отличительной чертой вируса является то, что он не тормозит и не нарушает размножение В-лимфоцитов, а, наоборот, стимулирует его. В этом заключается особенность возбудителя - он размножается в клетках иммунной системы, заставляя их клонировать свою, вирусную, ДНК.
Хронический воспалительный процесс, вызванный ВЭБ, приводит к структурным и метаболическим нарушениям пораженных тканей, что является причиной возникновения разнообразной соматической патологии.
Классификация вируса Эпштейна-Барр
Единой классификации вирусной инфекции Эпштейна-Барр (ВИЭБ) не существует, к использованию в практической медицине предлагается следующая:
- по времени инфицирования – врожденная и приобретенная;
- по форме заболевания – типичная (инфекционный мононуклеоз) и атипичная: стертая, асимптомная, с поражением внутренних органов;
- по тяжести течения – легкая, средней степени и тяжелая;
- по продолжительности течения – острая, затяжная, хроническая;
- по фазе активности – активная и неактивная;
- смешанная инфекция – чаще всего наблюдается в сочетании с цитомегаловирусом.
- Инфекционный мононуклеоз (железистая лихорадка, болезнь Филатова) – распространенное инфекционное заболевание, основными проявлениями которого является подъем температуры до высоких значений, увеличение лимфатических узлов, воспаление слизистой оболочки глотки, увеличение печени и селезенки. ВЭБ в данном случае проникает через эпителий слизистых оболочек верхних дыхательных путей.
- Лимфогранулематоз (болезнь Ходжкина) и некоторые виды неходжкинских лимфом – группа заболеваний, объединенных злокачественной моноклональной пролиферацией лимфоидных клеток в лимфоузлах, костном мозге, селезенке, печени и желудочно-кишечном тракте.
- Синдром хронической усталости – состояние, характеризующееся длительным чувством усталости, которое не проходит после продолжительного отдыха.
- Синдром Алисы в стране чудес – состояние, клиническим проявлением которого является нарушение ощущения своего тела и отдельных его частей. Человек ощущает себя или части своего тела очень большими или очень маленькими по сравнению с действительностью.
- Гепатит, спровоцированный ВЭБ, часто является осложнением инфекционного мононуклеоза. Появляется слабость, тошнота, желтушность кожи и слизистых, увеличивается печень.
- Герпетическая инфекция в виде генитального или лабиального (на губах) поражения. Также возможен стоматит, вызванный ВЭБ. При активации инфекции появляется чувство жжения и боль, а затем множество маленьких пузырьков.
- Посттрансплантационная лимфопролиферативная болезнь – вторичное злокачественное заболевание, развивающееся после трансплантации гемопоэтических стволовых клеток (метод лечения, применяемый при онкологии, заболеваниях крови и др.), ассоциированное с ВЭБ-инфекцией.
- Рассеянный склероз – хроническое аутоиммунное заболевание, при котором поражается миелиновая оболочка нервных волокон головного и спинного мозга. Характеризуется большим количеством симптомов и зависит от уровня поражения: часто снижается мышечная сила, угасают рефлексы, появляются параличи (обездвиженность) различных локализаций.
- Волосатая лейкоплакия – на слизистой оболочке языка по бокам, на спинке либо на его нижней части появляются белые участки с шероховатой поверхностью. Они безболезненны и не причиняют существенного дискомфорта. Основная опасность заключается в возможности озлокачествления измененных клеток слизистой.
- Назофарингеальная карцинома – злокачественное образование глотки. Среди его симптомов часто встречаются заложенность носа, потеря слуха, частые отиты, появление крови в слюне, кровянистые выделения из носа, увеличение лимфоузлов, головные боли.
- Аутоиммунный тиреоидит – хроническое заболевание щитовидной железы, при котором в организме образуются антитела к тканям щитовидной железы. При данном заболевании возможно появление зоба (увеличение щитовидной железы), развитие симптомов гипотиреоза: отеки, повышенная утомляемость, сонливость, запоры, сухость кожи, выпадение волос.
Лабораторное обследование включает:
-
вирус Эпштейна–Барр, определение ДНК в крови (Epstein Barr virus, DNA);
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Инфекционный мононуклеоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Инфекционный мононуклеоз – заболевание вирусной природы, при котором развивается лихорадка, увеличиваются печень и селезенка, лимфатические узлы, поражаются гортань, глотка. В крови регистрируются свойственные только этой патологии изменения (появление атипичных мононуклеаров, лимфоцитоз). В ряде случаев инфекционный мононуклеоз имеет хроническое течение, при некоторых состояниях клиническая картина стерта, что существенно затрудняет диагностику и постановку верного диагноза.
Причины появления инфекционного мононуклеоза
Заболевание вызывают вирусы семейства герпесвирусов, самым частым возбудителем считается вирус Эпштейна–Барр (ВЭБ, или вирус герпеса человека 4-го типа). Большинство людей переносят его в стертой клинической форме в детстве и юношестве, что подтверждается анализами крови на содержание иммуноглобулинов, которые вырабатываются в ответ на попадание вирусов в организм человека: по статистике у 9 из 10 взрослых положительные анализы крови на ДНК этого вируса.
Пути передачи вируса, вызывающего инфекционный мононуклеоз:
- Воздушно-капельный.
- Контактно-бытовой (в том числе половой).
- Парентеральный – во время переливания крови, пересадки органов и тканей в течение 6 предшествующих заболеванию месяцев.
К предрасполагающим факторам развития болезни относятся такие состояния, как снижение иммунитета, длительно текущие заболевания или обострение хронических патологий, неблагоприятная психоэмоциональная и экологическая обстановка.
Классификация заболевания
Единой общепринятой классификации инфекционного мононуклеоза нет. Для удобства формулировки диагноза используются следующие разделения патологии на группы:
По возбудителю:
- Вирус Эпштейна–Барр (ВЭБ).
- Цитомегаловирус.
- Вирус герпеса 6-го и 7-го типов (HV6, HV7).
- Аденовирус.
- Вирус иммунодефицита.
- Toxoplasma gondii (токсоплазма).
- Типичный – свойственная мононуклеозу клиническая картина и патогномоничные (характерные только для этого заболевания) изменения в анализах крови.
- Атипичный – стертая клиника, бессимптомное течение.
- Острый инфекционный мононуклеоз – проявления заболевания регистрируются в течение не более 3 месяцев.
- Затяжное течение (3–6 месяцев).
- Рецидивирующее течение – симптомы патологии возникают вновь через 1 месяц и менее после перенесенного заболевания.
- Хроническое – симптомы беспокоят более 6 месяцев.
Симптомы инфекционного мононуклеоза
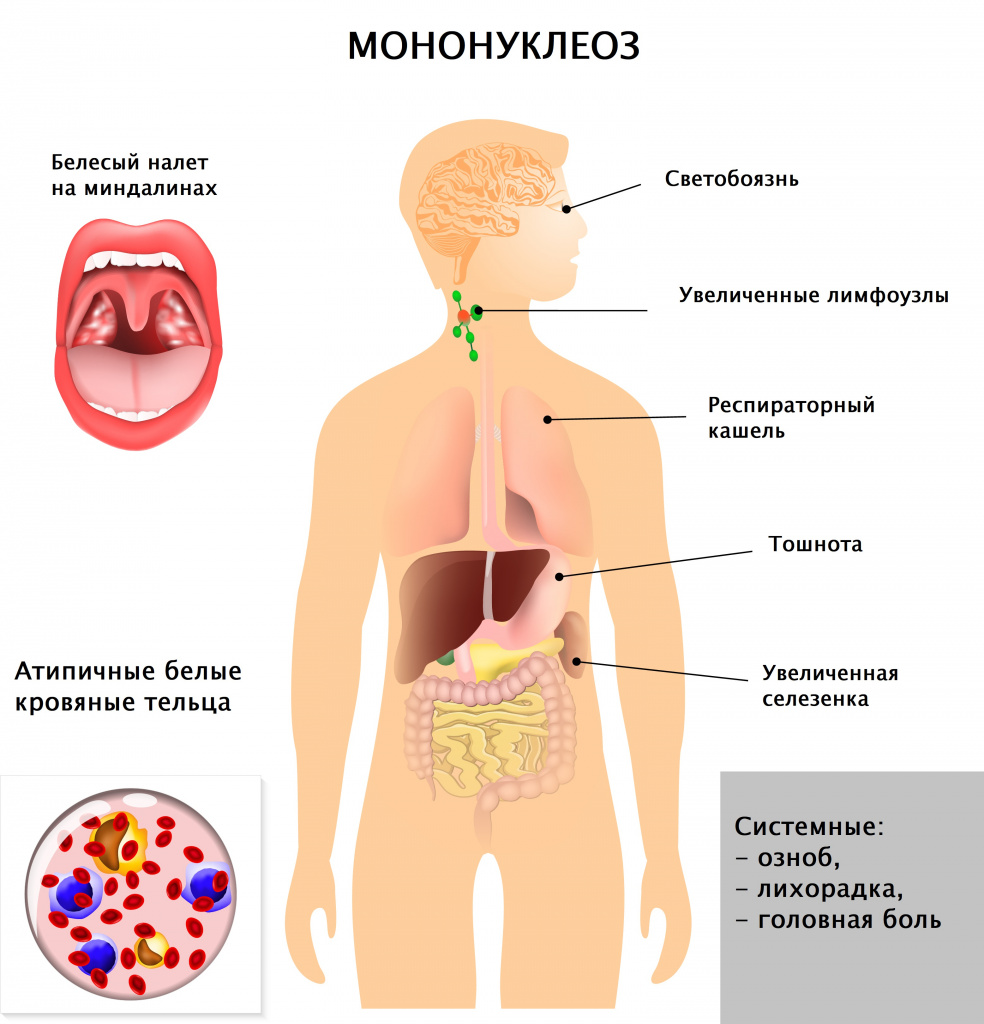
Диагностика инфекционного мононуклеоза
Врач в первую очередь собирает анамнез и проводит визуальный осмотр пациента. При осмотре обращают на себя внимание увеличенные группы лимфатических узлов (в тяжелых случаях не только шейной группы, но даже внутренние лимфатические узлы), гиперемия (краснота) зева, увеличение селезенки и печени, которое врач выявляет при пальпации и перкуссии живота.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Вирус Эпштейна-Барр относится к семейству герпесвирусов, подсемейство g-герпесвирусов - вирус герпеса человека IV типа. Вирусная частица состоит из нуклеоида, капсида и оболочки.
Нуклеоид содержит двухцепочечную ДНК, он окружен капсидом, состоящим из белковых субъединиц. Нуклеоид и капсид (нуклеокапсид) окружены липидсодержащей внешней оболочкой, образующейся из ядерной или наружной мембраны клетки-хозяина, в которую ещё до начала сборки вирусной частицы встраиваются некоторые вирусные белки.
При инфицировании вирус проникает в эпителий ротоглотки и слюнных желёз человека и вызывает активную инфекцию с лизисом клеток и высвобождением вирусных частиц, в результате чего вирус обнаруживается в слюне. Кроме того, он может проникать в В-лимфоциты и эпителий носоглотки и вызывать латентную инфекцию. Вирус Эпштейна-Барр можно обнаружить в оральных секретах здоровых, но латентно инфицированных людей. Вирус тропен к В-лимфоцитам, Т-лимфоциты он не поражает. Проникнув в лимфоциты, вирус Эпштейна-Барр может вызывать их трансформацию, в результате которой образуются способные к неограниченной пролиферации клоны атипичных лимфоцитов, содержащие кольцевую вирусную ДНК в виде плазмиды. Рецептором вируса на эпителиальных клетках и В-лимфоцитах служит молекула CD21, которая служит также рецептором фрагмента комплемента C3d. Вирус запускает как гуморальный, так и клеточный ответ. Среди образующихся антител есть специфические к антигенам вируса и неспецифические, гетерофильные. Последние появляются в результате поликлональной активации В-лимфоцитов (это может быть причиной интерференции при проведении ряда серологических исследований у людей с активной инфекцией вирусом Эпштейна-Барр). Главную роль в элиминации данной инфекции играет клеточный иммунитет. При острой инфекции первичная репродукция вируса в В-лимфоцитах сменяется выраженной пролиферацией Т-лимфоцитов с соотношением CD4/CD8 меньше 1.
Острая инфекция вирусом Эпштейна-Барр известна под названиями инфекционный мононуклеоз, болезнь Филатова, моноцитарная ангина, идиопатическая железистая лихорадка, болезнь Афейффера, острый доброкачественный лимфобластоз.
Вирус Эпштейна-Барр - главная причина мононуклеоподобного синдрома (хотя острая первичная инфекция, вызванная этим вирусом, и инфекционный мононуклеоз не являются синонимами). Для острой инфекции характерно повышение температуры, боли в горле и увеличение заднешейных лимфоузлов (реже – переднешейных и локтевых, встречается генерализованное увеличение лимфоузлов). В 50% случаев выявляется увеличение селезенки, в 10 - 30% случаев – увеличение печени. Другими проявлениями инфекции могут быть сыпь и периорбитальный отек. Изредка наблюдаются осложнения, в том числе, неврологические, изменения со стороны системы крови в виде гемолитической или апластической анемии, нейтропении, тромбоцитопении. После перенесённого заболевания иногда подолгу сохраняется фарингит, увеличение лимфоузлов, утомляемость и неспособность концентрации внимания.
Заболевание малоконтагиозно. Инкубационный период (период активного размножения и распространения вируса по всей лимфоидной ткани) может длиться от 30 до 50 суток. Инфицирование данным вирусом в любом возрасте, а у детей особенно, в большинстве случаев может протекать бессимптомно или как респираторная инфекция. Доля серопозитивных лиц (имеющих специфические антитела к антигенам вируса) уже среди подростков в разных странах составляет от 50 до 90%, среди взрослых людей серологические признаки инфекции обнаруживаются почти в 100% случаев. Вирус выделяется со слюной, передается через поцелуи и другие контакты слизистой со слюной или загрязнёнными ею предметами. Трансплацентарная передача вируса происходит редко. Иммунитет при инфекционном мононуклеозе стойкий.
Хотя канцерогенность вируса окончательно не доказана, есть основания полагать, что он может играть роль в развитии ряда злокачественных новообразований – лимфомы Беркитта, рака носоглотки, лимфогранулематоза и ряда посттрансплантационных лимфопролиферативных синдромов. На фоне нарушения клеточного иммунитета (СПИД, иммуносупрессия при трансплантации и пр.) вирус Эпштейна - Барр может вызывать инфекционный мононуклеоз с летальным исходом или лимфопролиферативные синдромы с развитием В-клеточных лимфом.
Диагностика инфекционного мононуклеоза основывается на клинической картине, характерных изменениях в клиническом анализе крови:
Синонимы: ОАК. CBC without differential. Краткая характеристика исследования Общий анализ крови Кровь состоит из жидкой части (плазмы) и клеточных, форменных элементов (эритроциты, лейкоциты, тромбоциты). Состав и концентрация клеточных элементов в крови меняются при различных физио.
Читайте также:

