Атипичные возбудители инфекций дыхательных путей
Обновлено: 15.04.2024
Владимир Трофимович Ивашкин, академик РАМН, доктор медицинских наук:
Владимир Кириллович Таточенко, доктор медицинских наук, профессор:
- Простой вопрос: что такое рациональное использование антибиотика (АБ). Это использование антибиотика только тогда, когда есть бактериальная инфекция. Выбор только такого АБ, к которому чувствителен предполагаемый возбудитель. Применение дозировок АБ, которые способны обеспечить концентрации, подавляющие возбудителя в очаге воспаления. Отказ от профилактического применения АБ, за очень небольшим исключением. Есть несколько позиций, при которых это рекомендуется.
АБ применяют чаще всего, когда у ребенка есть лихорадка. Надо всегда помнить, что лихорадка – защитная, мобилизующая иммунитет реакция. Особо переживать по поводу лихорадки не нужно. Это не гипертермия, не перегрев. Ничего плохого обычно не бывает.
Сейчас сложилась такая ситуация, что мы не имеем дифтерии, кори. Сейчас появилось десятка два случаев. Раньше миллион случаев было в год. Коклюш, туберкулез, паротит, полиомиелит – все это более-менее в прошлом, а лихорадящие дети остались.
У педиатра есть две сложные проблемы:
2. Обеспечить лихорадящих детей с вирусными инфекциями, для которых нет этиотропных средств, обоснованной патогенетической и симптоматической терапией, избегая полипрагмазии.
Несмотря на то, что есть приказ министра о том, что больше пяти средств одновременно нельзя применять, регулярно дети с насморком получают бесконечное количество снадобий. Большая часть из них, кроме рекламы, никаких серьезных поддерживающих материалов не имеет.
Выловить бактериальных и оставить в покое детей с насморком, с кашлем, с бронхитом, который сам проходит – очень сложная задача.
Создавшаяся ситуация очень неблагоприятная. Я сошлюсь на только опубликованные данные. Во Владивостоке 86% детей с ОРЗ и бронхитом получают макролиды. В нашей клинике вы увидите, что получают 1-3%.
Выбор АБ происходит эмпирическим путем с учетом вероятной этиологии, чувствительности предполагаемого возбудителя. Хотя хорошо известно, что если бронхит и вызывает бактерии, то крайне-крайне редко. Бронхит – вирусное заболевание.
В Америке оценка качества лечебной работы включает процент больных с бронхитом, леченных АБ. Чем выше этот процент, тем хуже качество.
Наши данные о том, как часто мы используем АБ. При ОРВИ, при крупе, при бронхитах используются очень редко. Неоправданно. Иногда бывает отит у ребенка (с крупом обычно). Обычно несколько процентов получают. Либо родители отказываются отменить АБ.
Это нам дает резкое сокращение длительности пребывания в стационаре. Красным показаны данные, которые мы взяли из городской больницы. Зеленым наши данные. Обычно это 2-3, максимум 4 дня у детей с бронхиолитом. Мы дожидаемся, когда они перестанут свистеть. АБ мы им не даем.
Это преамбула к моей лекции.
Если взять острые лихорадочные заболевания. Мы взяли 1800 детей, госпитализированных в последние годы. Их можно разделить на две неравные части. Это дети с лихорадкой и выраженными катаральными явлениями и дети с лихорадкой без катаральных явлений. Это хорошее деление, потому что катаральные явления видно издали.
Распределение с катаральными явлениями. 35% – поражения только верхних дыхательных путей. 30% – поражение нижних дыхательных путей. Желтым показаны формы, при которых не надо давать АБ.
Если взять без катаральных явлений, дети с поносом и рвотой…
У нас сейчас огромное количество ротавирусной и других вирусных диарей. Боковирус третьего типа тоже вызывает диареи, третьи после рота- и норовируса. Без видимого очага инфекций, относительно редкий контингент – здесь тоже есть вирусные инфекции, которые не дают в первые дни признаков катаральных явлений. Имеется бактериальная инфекция – бактериемия – инфекция мочевых путей, которая представляет большую сложность.
Если взять формы и посмотреть соотношение, то получается, что дети с лихорадкой и катаром – 67% случаев не нуждаются в АБ. Это по больнице. Если взять в поликлинике, которых не госпитализируют, соотношение будет еще более контрастное.
Если взять детей с лихорадкой и без катаральных явлений, то имеем обратное соотношение. 60% детей требуют антибактериальной терапии. Лихорадка без катара случается, но это только 40%.
Когда педиатр сталкивается с ребенком, он меньше всего интересуется уровнем. Меня интересуют другие признаки бактериального заболевания. Такие как нарушение общего состояния, токсичность ребенка, аппетит, пьет он или не пьет. Эти симптомы. Смотрит в глаза или не смотрит. Ребенок с тяжелым бактериальным заболеванием не смотрит в глаза врачу. Это хороший признак.
Да хоть 40,5. Ничего страшного. Дайте ему жаропонижающее. От этого большого вреда не будет. Только иммунитет укрепит.
Что у нас делается по бактериальным заболеваниям. На одной руке хватает пальцев, чтобы перечислить бактериальных возбудителей. Это пневмококки, H. influenza, стрептококк гемолитический (БГСА), Mycoplasma и Moraxella. Стафилококка золотистого больше при кожной инфекции. Chlamydophila бывает у пневмонии. Еще речь о E. сoli при почечных инфекциях.
Мы имеем дело с четырьмя основными возбудителями, которые вызывают практически весь спектр респираторных бактериальных заболеваний.
Если говорить об оральных антибиотиках первого выбора (у детей надо шире применять оральные препараты)…
Сегодня опубликована статья о том, что все почечные инфекции, включая пиелонефриты, прекрасно лечатся оральными препаратами и дают такой же процент рубцов на паренхиме, как и действие только внутривенных препаратов. Колоть лишний раз ребенка не нужно.
Маленьким детям (которым месяц, два, три) дать препарат внутрь бывает сложнее, чем ввести ему в вену. Сейчас ставим, он лежит спокойно.
При каких формах их применять. Отит, синусит, тонзиллит, типичная пневмония, инфекции мочевых путей.
Макролиды – незаменимые препараты при атипичных инфекциях (микоплазмозе и хламидиозе). Или как заменитель лактамов, если у ребенка имеется какая-то аллергия к ним.
Лечение острого отита или синусита. Здесь основная флора – это пневмококк или гемофильная палочка у леченных ранее детей, недавно получавших АБ. У них может быть моракселла. Гемолитический стрептококк.
Американцы, у которых чаще устойчивость к лактамам пневмококка, рекомендуют сейчас 100 мг и для лечения пневмонии. Хотя для пневмонии достаточно 50 мг, в легких он хорошо концентрируется, накапливается.
Лихорадка или боль в ухе. Привожу два примера. Ребенок первого года, болен два дня. Температура 38,5. Иногда вскрикивает. Мутная барабанная перепонка, виден экссудат, 15 тысяч лейкоцитов. Ясно, что здесь гнойный отит.
Повышение дозы до 100 мг. Парацентез пришлось сделать – привело к быстрому снижению температуры. Выбор, может быть, не столько выбор, сколько выбор дозировки препарата. Никакой сложности здесь нет.
85% детей после первой дозы поправляются. У них прекращается стеноз. Некоторые требуют две дозы. Очень редко три дозы.
С такой же клинической картиной, но без катаральных явлений, с ознобом, признаками токсичности, без изменения голоса (голос просто сдавленный, но не хриплый) – это эпиглоттит (воспаление надгортанника). У нас еще не проводится массовая вакцинация против гемофилиса В.
Здесь лечение должно быть обязательно внутривенным. Очень ранняя инкубация. Очень легко западает надгортанник. Инкубация на сутки, больше не нужно.
Пневмония. Иногда приходится слышать, что сейчас какие-то другие возбудители, и все они устойчивы. Ничего подобного. Пневмококк как был основным возбудителем, так и остался. Конечно, у детей первых месяцев жизни, чаще всего это аспирация пищи, муковисцидоз – такие причины пневмонии.
Примерно 10% заражаются от старших сипсов – это пневмококк или гемофилис. Иногда бывает хламидия трахоматис. От шести месяцев до пяти лет практически 85 – 90% – это пневмококк и гемофилис. Атипичная – микоплазма и хламидии – бывают в этом возрасте редко.
После пяти лет получается 50/50. Примерно половина – это типичная пневмококковая пневмония. Вторая половина – микоплазмы. Значительно реже хламидии.
Чем отличается атипичная пневмония от типичной. Симптомы. Микоплазменная пневмония протекает с обилием хрипов. При типичной пневмонии хрипов или нет или их очень мало. Это самая распространенная ошибка. Нет хрипов – нет пневмонии. Наоборот, когда я не слышу хрипы, мне кажется, что нужно посмотреть за этим ребенком.
Если я слышу много хрипов – это бронхит или атипичная пневмония. Микоплазменная пневмония протекает с красными коньюктивами.
Разница небольшая – 5%. Но если вы будете лечить 100 детей и в пяти случаях не попадете – это будет достаточно неприятно. В педиатрии допустимо одновременное назначение бета-лактама и макролида. Хотя у взрослых считается стандартной практикой начинать лечить (особенно пожилых) при не очень тяжелых пневмониях сразу давать оральный лактам и макролид. Мы рекомендуем, если доктор не уверен.
Разрешите проиллюстрировать примером то, что я сказал. Хламидийная пневмония. В чем ее отличие. При ней бывает очень высокий лейкоцитоз. У данного ребенка лейкоцитоз был 37 тысяч. Умеренная эозинофилия. Это очень необычная ситуация. Множественные мелкие очаги. Очень похоже на милиарный туберкулез. Милиарный туберкулез большинство терапевтов не видело. Сравнение некорректное.
Дозировка прописана, которая везде рекомендуется (45мг/кг). Какой-то иезуит сделал такую дозировку. Если ребенок весит 17 кг, перемножьте, сколько мы должны дать ему. Мне кажется, что здесь расщеплять волосы и быть точными не нужно. 50 мг.
Американцы честно помножили на два и дают 90 мг. 17 на 90 тоже не очень просто помножить. 50, 100 легко помножить. Конечно, доза привязывается к размеру таблетки, к размеру ложки. Но не нужна эта излишняя точность.
Та же история. Здесь нам удалось поймать иммуноглобулин М. Обычно иммуноглобулин М появляется к концу второй недели. Когда вы берете свежего ребенка и делаете ему иммуноглобулин М, он оказывается отрицательный. Вы считаете, что здесь нет микоплазмоза.
Еще один ребенок. На шестой день болезни IgM отрицательный. Хотя здесь не было совершенно никаких сомнений, что это пневмония микоплазма.
Теперь я хочу показать один случай. Если вы полезете в литературу, никто не описывает, как выглядит хламидийная пневмония. Мы тоже не очень верим в легковерность, что это хламидийная пневмония. Пришлось на компьютерной томограмме показывать. Очаги на рентгенограмме были не очень яркие, какие-то совершенно необычные и справа и слева.
Такое необычное начало с обструкцией описано как хламидийная пневмония. Нам удалось один раз такое поймать и доказать. Будем считать, что здесь ничего не напутали. Правда, у ребенка IgM 1133 ЕД/мл. Обструкция могла быть совершенно спокойно астматического порядка.
На томографии плеврит слева, не очень заметны изменения были на рентгенограмме. Несмотря на такое лечение, на 22-й день болезни были еще очень большие изменения. СОЭ очень высокое. С такими больными трудно.
Деструкция. Мы не боимся деструкции. При пневмококковой пневмонии это достаточно частое явления. Маленький ребенок с пневмонией верхушки нижней доли слева. Он поступил 29 сентября. 3 октября у него появились просветления.
Мы к этому тоже относимся очень спокойно. Недавно вышли американские рекомендации. Там немножко они все еще волнуются. На этом фоне развился участок буллезного деструктивного процесса. Все рассосалось без хирургии.
Маленький ребенок, казалось бы, с небольшой пневмонией. После начала лечения дает длительную лихорадку. Метапневмонический плеврит одновременно возникает на месте очага. Слева возникает полностью с уровнем жидкости. Но мы не рассматриваем как настоящие абсцессы. Продолжаем лечение.
На фоне температуры довольно быстро перешли на оральный препарат. АБ здесь для успокоения родителей. Скорее всего, для лечения.
Недавно у нас такой же случай. Пневмония с деструкцией. Падение температуры и образование метапневмонического, видимо, междолевого плеврита. Мы его не пунктировали. Мы знаем, что это все рассосется.
Очень характерно ускорение СОЭ на фоне метапневмонического плеврита. При поступлении СОЭ было 12, стало 61 при падении числа лейкоцитов. Опорожнилась полость, раздулась немножко. Ребенок выписался.
Атипичная пневмония – это инфекционно-воспалительные поражения легких, вызываемые нехарактерными (атипичными) возбудителями – хламидиями, микоплазмами, легионеллами, вирусами. Атипичные пневмонии протекают с явлениями общего недомогания, высокой лихорадкой, ознобами, потливостью, мышечной и головной болью, кашлем, одышкой. В тяжелых случаях может развиться легочно-сердечная недостаточность и наступить гибель пациента. Диагностика атипичной пневмонии требует учета данных эпиданамнеза, идентификации возбудителя (методами ИФА, РИФ, ПЦР, культурального посева и др.), проведения рентгенографии легких. С учетом этиологии лечение атипичной пневмонии проводится противомикробными (макролидами, фторхинолонами, тертрациклинами) и противовирусными химиопрепаратами. Основная трудность терапии заключается в том, что против некоторых вирусных возбудителей атипичной пневмонии до настоящего времени не найдено действенных препаратов.
МКБ-10
Общие сведения

Причины
На сегодняшний день к так называемым атипичным микроорганизмам - возбудителям атипичной пневмонии относится многочисленная группа инфекционных агентов. Атипичные пневмонии могут вызываться микоплазменной (Mycoplasma pneumoniae) и хламидийной (Chlamydophila pneumoniae) инфекцией, легионеллой (Legionella spp.), коксиеллой (Coxiella burnetti), вирусами (респираторными вирусами парагриппа 1, 2 и 3; гриппа А и В; вирусом EpsteinBarr, респираторным синцитиальным вирусом), возбудителями лептоспироза (Leptospira spp.), туляремии (Francisella tularensis), хантавирусами, коронавирусом ТОРС (SARS-CoV) и др. Несмотря на значительные различия эпидемиологической и микробиологической характеристики возбудителей, а также патоморфологической картины инфекционного процесса, данные микроорганизмы объединены устойчивостью к антибиотикам пенициллинового ряда и другим β-лактамам, а также общими подходами к лабораторной верификации.
Заражение атипичной пневмонией происходит обычно при тесном контакте в коллективах; путь передачи - воздушно-капельный. Восприимчивость к SARS высокая вне зависимости от возраста: среди болеющих атипичной пневмонией преобладают люди моложе 40 лет, обладающие крепким здоровьем. Инкубационный период при атипичной пневмонии длится от 3-х до 10 дней. В зависимости от возбудителя выделяют следующие основные формы атипичной пневмонии: микоплазменную пневмонию, лихорадку Q, легионеллезную пневмонию, хламидийную пневмонию, тяжелый острый респираторный синдром и др.
Атипичная микоплазменная пневмония
Симптомы
Атипичная микоплазменная пневмония составляет около 10-20% случаев от всех воспалений легких у детей и подростков и 2-3% случаев – у взрослых. В детских коллективах возможны очаговые эпидемические вспышки микоплазменной пневмонии. Клинически респираторный микоплазмоз может протекать в виде назофарингита, трахеита, бронхита, атипичной пневмонии.
Течение микоплазменной пневмонии, как правило, легкое или среднетяжелое. После инкубационного периода (3-11 дней) наступает непродолжительный продромальный период (1-2 суток), в течение которого беспокоит сухость слизистых верхних дыхательных путей, першение в горле, сухой кашель, головная боль и незначительное недомогание. Клиника собственно атипичной микоплазменной пневмонии характеризуется субфебрильной температурой, не поднимающейся выше 38°С; приступообразным непродуктивным кашлем, который беспокоит около 2-3 недель. В 20-30% случаев микоплазменное воспаление легких является двусторонним.
В тяжелых случаях атипичная микоплазменная пневмония протекает с высокой лихорадкой, выраженной интоксикацией, артралгией, миалгией, носовыми кровотечениями, полиморфной сыпью на коже, шейным лимфаденитом, альбуминурией и микрогематурией, гепатоспленомегалией, дистрофическими изменениями миокарда. Однако обычно, по сравнению с бактериальным воспалением, микоплазменная пневмония имеет более вялое и стертое течение. Осложнениями микоплазменной пневмонии могут являться деформирующий бронхит, бронхиолит, бронхоэктазы, пневмосклероз.
Диагностика
Лечение
Своевременная и адекватная этиотропная терапия способствует быстрому регрессу клинических проявлений атипичной микоплазменной пневмонии. Между тем, рентгенологические изменения могут сохраняться длительно, до 4-6 недель. В терапии атипичной пневмонии, вызываемой микоплазмой, используются макролиды (азитромицин, эритромицин), линкозамины (клиндамицин) основным курсом не менее 7 дней и дополнительным - 2 дня после стихания симптомов. Одновременно проводится симптоматическая (жаропонижающая, муколитическая, бронхолитическая) терапия, при бронхиолите назначаются глюкокортикостероиды.
Атипичная хламидийная пневмония
Симптомы
Микроорганизмы из рода Chlamydophila (С.trachomatis, С.pneumoniae) обладают тропностью к эпителиальным клеткам мочеполовой системы, конъюнктивы, бронхов, легких, вызывая у человека урогенитальный хламидиоз, хламидийный конъюнктивит, острый бронхит, пневмохламидиоз. На долю хламидийных пневмоний приходится не менее 10% случаев всех воспалений легких. Заболеваемости атипичной хламидийной пневмонией наиболее часто подвержены дети и подростки, а также люди пожилого и старческого возраста. Chlamydophila pneumoniae иногда длительно существует в организме, не вызывая инфекционных проявлений.
Диагностика
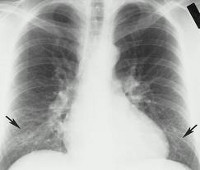
Физикальные изменения при атипичной хламидийной пневмонии сохраняются 7-10 дней, а рентгенологические – до 12-30 суток. Стетоакустическое обследование выявляет в легких сухие и влажные хрипы. Рентгенологические изменения характеризуются мелкоочаговой и/или интерстициальной инфильтрацией чаще с двух сторон. Присутствие в организме хламидии определяется с помощью культурального, микроскопического, ИФА, ПЦР исследования биологических сред. Наибольшее диагностическое значение при атипичной хламидийной пневмонии имеет определение IgA, IgG, IgM к антигенам белков внешней мембраны.
Лечение
Препаратами этиотропного действия при атипичной хламидийной пневмонии служат тетрациклины и макролиды. Курс терапии должен продолжаться не менее 10-14 дней, поскольку короткие циклы могут способствовать хронизации и рецидивированию пневмохламидиоза. В некоторых случаях прибегают к назначению фторхинолонов (спарфлоксацина, офлоксацина и др.), доксициклина.
Атипичная легионеллезная пневмония
Симптомы
Атипичная легионеллезная пневмония встречается преимущественно среди лиц среднего и пожилого возраста. К ее возникновению предрасполагает курение, иммуносупрессия, хроническая почечная недостаточность. Инфекция чаще развивается в летние месяцы и регистрируется в виде спорадических случаев или массовых вспышек. Данная форма атипичной пневмонии протекает по типу долевой пневмонии, с вовлечением в патологический процесс терминальных бронхиол и альвеол, массивной экссудацией и выраженным отеком интерстициальной ткани в зоне поражения.
Атипичная легионеллезная пневмония имеет тяжелое клиническое течение. Симптоматика характеризуется подъемом температуры в течение 24-48 ч до 40°С и выше, сильнейшими ознобами и головной болью. Одновременно присоединяется кашель: вначале сухой, затем – с отделением слизистой или слизисто-гнойной мокроты. В 20% случаев отмечается кровохарканье. Общая картина отягощается одышкой, мышечными и плевральными болями, тошнотой, рвотой, диареей, тахикардией, абдоминальными болями. Наиболее грозными осложнениями атипичной легионеллезной пневмонии служат дыхательная недостаточность и вторичная почечная недостаточность, приводящие к гибели больных.
Диагностика
При диагностике атипичной легионеллезной пневмонии учитываются эпидемиологические данные, тяжелое клиническое течение пневмонии, результаты инструментальных и лабораторных исследований. При аускультации в легких выслушиваются влажные хрипы. С помощью рентгенографии (КТ, МРТ легких) определяются округлые инфильтраты, занимающие не менее одной доли легкого и имеющие тенденцию к слиянию. У трети пациентов выявляется плеврит с небольшим количеством плеврального выпота.
Как правило, посев крови и мокроты на наличие легионелл дает отрицательный результат. Диагноз атипичной легионеллезной пневмонии удается подтвердить путем посева на специальные среды трахеального аспирата, лаважной жидкости, плеврального выпота. С целью получения необходимого биологического материала проводится трахеальная аспирация, бронхоскопия с забором мокроты, бронхоальвеолярный лаваж, плевральная пункция. Также используется РИФ, ИФА диагностика.
Лечение
Прогрессирующее ухудшение состояния при атипичной пневмонии, вызываемой легионеллой, часто диктует необходимость перевода пациента на ИВЛ. Клиническое улучшение, как правило, появляется на 4-5 сутки после начала интенсивного применения антибиотиков (эритромицина, рифампицина, доксициклина, ципрофлоксацина). Лихорадка при атипичной легионеллезной пневмонии в среднем продолжается около 2-х недель; разрешение инфильтратов в легочной ткани занимает до 1 мес. В некоторых случаях после атипичной пневмонии остаются участки ограниченного пневмосклероза в легких. Реконвалесценция протекает медленно, длительно сохраняется слабость и утомляемость.
Атипичная пневмония (тяжелый острый респираторный синдром)
Симптомы
Атипичная пневмония – малоизвестная форма острой респираторной инфекции, поражающей нижние дыхательные пути. Известно, что возбудителями атипичной пневмонии является ТОРС (SARS)-коронавирус, входящий в семейство Сoronaviridae. В настоящее время продолжается эпидемиологическое, лабораторное и клиническое изучение ТОРС-коронавируса. Большинство заболевших атипичной пневмонией в 2002-2003 г.г. составили лица 25-70 лет; отмечены единичные случаи заболеваемости детей до 15 лет. Основной механизм передачи коронавируса - воздушно-капельный, однако выявление возбудителя в моче и фекалиях не исключает возможности фекально-орального заражения.
Инкубационный период при атипичной пневмонии составляет 2-7, в отдельных случаях - 10 дней. Вначале симптомы атипичной пневмонии малоспецифичные: заболевание манифестирует с высокой лихорадки (выше 38°С), которая сопровождается ознобами, потливостью, головными болями, миалгией. В ряде случаев на высоте лихорадочного состояния отмечается рвота и диарея.
На 3-7 сутки атипичной пневмонии развивается сухой кашель, одышка, прогрессирующая гипоксемия. Нарастающая гипоксия сопровождается цианозом носогубного треугольника, тахикардией, глухостью сердечных тонов, гипотонией. В последующие 6-7 суток у части пациентов наблюдается улучшение самочувствие и стихание симптоматики; в других случаях - развивается респираторный дистресс-синдром, требующий перехода к ИВЛ. В последней группе пациентов отмечается высокая летальность от токсико-инфекционного шока, острой дыхательной и сердечной недостаточности, сопутствующих осложнений.
Диагностика
Отсутствие достоверных диагностических тест-систем тяжелого острого респираторного синдрома и сложность дифференциальной диагностики заболевания в начальном периоде, диктует необходимость предполагать атипичную пневмонию у пациентов, посещавших в течение 10 дней эпидемически неблагополучные районы, а также лиц, страдающих лихорадочным состоянием с симптомами респираторного поражения.
Аускультативно при атипичной пневмонии определяется ослабление дыхания, крепитация, влажные мелкопузырчатые хрипы. При перкуссии выявляется притупление легочного звука. Рентгенологически в разгар атипичной пневмонии обнаруживаются двусторонние внутритканевые инфильтраты на периферии легочных полей. В лабораторных тестах крови выявляется лимфопения, тромбоцитопения, повышение уровня печеночных ферментов, изменение газового состава крови (снижение насыщения крови О2). Для идентификации возбудителя атипичной пневмонии используются ИФА, РИФ, молекулярные тесты.
Лечение
Поскольку атипичная пневмония является новым и малоизученным заболеванием, эффективной этиологической терапии пока не разработано. Согласно рекомендациям ВОЗ, при атипичной пневмонии необходимо включение в схему лечения нескольких противомикробных препаратов (фторхинолонов, ß-лактамов, цефалоспоринов, тетрациклинов). Данные меры позволяют предупредить наслоение бактериальной инфекции.
Прогноз и профилактикаи
Прогноз атипичной пневмонии зависит от формы заболевания: при микоплазменной и хламидийной пневмонии он, как правило, благоприятный для жизни; при легионеллезной и особенно ТОРС-инфекции – очень серьезный. С целью профилактики заражения и распространения атипичной пневмонии ВОЗ рекомендует воздерживаться от посещения эпидемически неблагоприятных регионов; установить строгий эпидконтроль лиц, прибывающих из данных районов; проводить дезинфекцию транспортных средств; использовать индивидуальные маски однократного применения при необходимости контакта с пациентами, подозрительными в отношении инфекции. В настоящее время работа по созданию эффективной вакцины и специфических тестов ранней диагностики атипичных пневмоний продолжается.
2. Современные подходы к диагностике атипичных пневмоний/ Тартаковский И.С.// Клиническая микробиология и антимикробная химиотерапия – 2000 - Том 2, № 1.
3. Атипичная пневмония - значимая проблема детского возраста/ Горбич О. А.// Медицинский журнал. - 2016. - № 3.

- Streptococcus pneumoniae - грамположительные кокки, самые частые возбудители пневмонии во всех возрастных группах (30% и более всех случаев);
- Haemophilus influenzae - грамотрицательные палочки, ответственные за развитие пневмонии у 5-18% взрослых, чаще у курильщиков и больных хроническим обструктивным бронхитом;
- Moraxella (Branhamella) catarrhalis - грамотрицательные коккобациллы, неактуальный возбудитель пневмонии (у 1-2% больных), имеет этиологическое значение, как правило, у больных с сопутствующим хроническим обструктивным бронхитом.
Другие часто выявляемые этиологические агенты ВП отличаются от перечисленных выше микроорганизмов несколько иной патогенностью и биологическими свойствами. Бессимптомная колонизация верхних дыхательных путей этими микроорганизмами маловероятна.
Основными способами заражения микроорганизмами при ВП, вызванной атипичными возбудителями, являются аспирация содержимого ротоглотки и ингаляция микробного аэрозоля — в случае легионеллезной пневмонии. В нормальных условиях ряд микроорганизмов, например S. pneumoniae, могут колонизировать ротоглотку, но нижние дыхательные пути при этом остаются стерильными. Микроаспирация секрета ротоглотки — физиологический феномен, наблюдающийся у 70% здоровых лиц, преимущественно во время сна. Однако слаженная работа мукоцилиарного клиренса, наряду с бактерицидным действием находящихся в бронхиальном секрете лактоферрина, лизоцима, интерферона и секреторного иммуноглобулина класса А, препятствует адгезии и колонизации микроорганизмов и последующему развитию ВП.
Частота микоплазменных пневмоний возрастает во время эпидемических вспышек, повторяющихся каждые 4–5 лет, и может достигать в среднем 20% от общего числа ВП в осенне-зимний период. Этот возбудитель чаще вызывает заболевания у молодых людей, клиническая картина обычно включает лихорадку, фарингит, миалгии, астению и внелегочные осложнения. Заболевание может излечиваться спонтанно в течение 1–2 нед, но нередко продолжается на протяжении 4–6 нед и сопровождается всеми характерными для него проявлениями, включая кашель со слизистой мокротой. Культуральная диагностика микоплазменной инфекции затруднительна. Диагноз может быть подтвержден выявлением 4-кратной сероконверсии специфических антител класса IgM к микоплазме с помощью теста Elisa.
Пневмонии, вызванные хламидиями, стали известны сравнительно недавно. Cl. pneumoniae вызывает инфекцию по крайней мере у 10% больных молодого возраста. Клиническая картина этой инфекции, кроме проявлений собственно бронхита и пневмонии, включает фарингит и ларингит. Обычными признаками являются осиплость голоса, небольшая лихорадка и постоянный кашель, который часто остается сухим, а отделяемая мокрота обычно слизистая и не бывает гнойной. У больных бронхиальной астмой хламидийная инфекция нередко провоцирует учащение приступов удушья. Воспаление бронхов, вызванное хламидией, как правило, встречается у молодых больных и практически не наблюдается в старческом возрасте. Диагноз может быть подтвержден данными сероконверсии, наиболее современным считается тест Elisa. В настоящее время для диагностики микоплазменной и хламидийной инфекции стали использовать полимеразную цепную реакцию (ПЦР).
Пневмония, вызванная L. Pneumophila, не является частым возбудителем ВП, но обычно характеризуется тяжелым течением и развитием системной воспалительной реакции и экстрапульмональной симптоматикой. Наиболее высокой природной активностью против легионелл обладает рифампицин, который часто используют в комбинации с эритромицином. Также эффективны другие макролиды (особенно кларитромицин и азитромицин, создающие высокие концентрации в бронхиальном секрете), новые и ранние фторхинолоны.
Клинико-рентгенологические симптомы атипичных ВП
Крупные мультицентровые исследования, основанные на принципах доказательной медицины, убедительно показали, что в большинстве случаев, основываясь на анализе клинико-рентгенологической картины заболевания, не удается с достаточной степенью определенности высказаться о вероятной этиологии ВП.
В частности, разделение ВП на типичную (например, пневмококковую) и атипичную (микоплазменную или хламидийную) лишено особого клинического значения, так как не влияет на выбор стартового антибиотика для эмпирической терапии. Однако были отмечены некоторые особенности атипичной ВП: образование полостей деструкции в легких не характерно для пневмококковой, микоплазменной и хламидийной пневмоний, а скорее свидетельствует в пользу стафилококковой инфекции, аэробных грамотрицательных энтеробактерий и анаэробов; ретикулонодулярная инфильтрация в базальных отделах легких характерна для микоплазменной ВП (в 20% случаев микоплазменная пневмония может сопровождаться очагово-сливной инфильтрацией в проекции нескольких сегментов или даже доли).
Лабораторная диагностика атипичных ВП
Серологическая диагностика инфекций, вызванных M. pneumoniae, C. pneumoniae и Legionella spp., не рассматривается в ряду обязательных методов исследования, поскольку с учетом необходимости повторного забора сыворотки крови в острый период болезни и в период реконвалесценции (через несколько недель от начала заболевания) это не клинический, эпидемиологический уровень диагностики. В последнее время получил распространение иммуноферментный тест — с определением в моче специфичного растворимого антигена L. pneumophila (1-й серотип), однако в нашей стране использование этих методов экспресс-диагностики практикуется лишь в отдельных клинических центрах.
Лечение атипичных ВП
Распространенную в некоторых регионах Российской Федерации практику широкого использования аминогликозидов (гентамицин и др.) при лечении ВП следует признать ошибочной, так как они не активны в отношении пневмококка и атипичных возбудителей.
M. pneumoniae обладают природной устойчивостью к β-лактамным антибиотикам, так как лишены клеточной стенки и ее составной части — пептидогликана, который является мишенью действия β-лактамов. Наибольшей природной активностью характеризуются макролиды и тетрациклины, а новые фторхинолоны по активности превосходят ранние фторхинолоны.
Cl. pneumoniae тоже устойчивы к β-лактамам, аминогликозидам, а препаратами выбора для лечения хламидийных ВП являются макролидные антибиотики и тетрациклины. Эритромицин или доксициклин являются препаратами выбора при пневмониях, вызванных распространенными возбудителями. У больных с непереносимостью указанных препаратов, выражающейся в виде желудочно-кишечных нарушений, рекомендуется другой макролид, например азитромицин или кларитромицин.
Эритромицин или доксициклин должны обеспечивать адекватное лечение пневмоний, вызванных большинством штаммов S. pneumoniae, а также атипичными возбудителями: Mycoplasma, Chlamydia pneumoniae и Legionella. Эритромицин может оказаться неэффективным при постгриппозной пневмонии, которую чаще вызывают более резистентные возбудители, такие, как Staphylococcus aureus и Haemophilus influenzae. Необходимо принимать во внимание частоту побочных эффектов в отношении желудочно-кишечного тракта (ЖКТ) и вероятность лекарственного взаимодействия. Доксициклин противопоказан при беременности.
Среди макролидов особого внимания заслуживает азитромицин (азитрал и сумамед), который быстро абсорбируется из ЖКТ, что обусловлено его устойчивостью в кислой среде и липофильностью, а также хорошо проникает в дыхательные пути. Высокая концентрация в тканях (в 10–50 раз выше, чем в плазме крови) и длительный TЅ обусловлены низким связыванием азитромицина с белками плазмы крови. Способность азитромицина накапливаться преимущественно в лизосомах особенно важна для элиминации внутриклеточных возбудителей. Доказано, что фагоциты доставляют азитромицин в места локализации инфекции, где он высвобождается в процессе фагоцитоза. Концентрация азитромицина в очагах инфекции достоверно выше, чем в здоровых тканях (в среднем на 24–34%), и коррелирует со степенью воспалительного отека. Несмотря на высокую концентрацию в фагоцитах, азитромицин не оказывает существенного влияния на их функцию. Азитромицин сохраняется в бактерицидных концентрациях в очаге воспаления в течение 5–7 дней после приема последней дозы, что позволило разработать короткие (3-дневные и 5-дневные) курсы лечения и применять препарат 1 раз в сутки.
Высокой активностью характеризуются новые фторхинолоны, а из ранних фторхинолонов наиболее активным против хламидий признан офлоксацин. Левофлоксацин рекомендуется у больных, которые не переносят препаратов первой линии. Этот фторхинолон имеет расширенный спектр активности, позволяющий использовать его при инфекциях дыхательных путей. Он удобен тем, что вводится однократно в сутки.
Литература
Г. И. Сторожаков, доктор медицинских наук, профессор, академик РАМН
Д. Б. Утешев, доктор медицинских наук, профессор
РГМУ, Москва
Какие назначения необходимы при подозрении на инфекцию нижних дыхательных путей? Какие патогенные факторы играют существенную роль? Как вести больных? Респираторные заболевания являются частой причиной обращения к врачу в Великобритании,
Какие назначения необходимы при подозрении на инфекцию нижних дыхательных путей?
Какие патогенные факторы играют существенную роль?
Как вести больных?
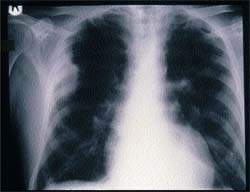 |
Респираторные заболевания являются частой причиной обращения к врачу в Великобритании, причем в большинстве случаев они относятся к инфекционным [1]. Трем четвертям пациентов, обращающихся с признаками острого заболевания нижних дыхательных путей, врач общей практики назначает антибиотики, хотя лишь в немногих случаях удается выделить возбудителя и антибиотики или вообще не влияют, или мало влияют на естественный ход заболевания [2,3].
Назначая антибиотики, врач руководствуется ожиданиями пациента и старается действовать согласно определенной терапевтической стратегии, хотя зачастую, выписывая рецепт, чувствует, что при этом состоянии антибиотики будут неэффективны [4,5].
Причины, по которым пациент первый раз приходит на прием к своему врачу и затем повторно обращается за консультацией, довольно сложны и часто никак не соотносятся с течением болезни. Как правило, они обусловлены обеспокоенностью своим здоровьем или давлением со стороны друзей, семьи и сотрудников.
При необходимости назначить антибиотик для лечения инфекции нижних дыхательных путей обычно выбирают амоксициллин. Пациенты, повторно обращающиеся к врачу, скорее всего, получат другой антибиотик, например эритромицин или новейшее средство из группы макролидов, хинолонов или пероральный цефалоспорин [3,6].
Проведенные нами недавно исследования показали, что повторное обращение пациентов с инфекциями нижних дыхательных путей, уже получивших назначения на первичном приеме, никак не связано с антибиотикотерапией. Только у 4% таких больных сохранялась бактериальная инфекция и ни у одного из них не было устойчивости к амоксициллину [7]. Повторно приходить на прием побуждают пациентов немедицинские факторы, такие как привычка обращаться к врачу.
Таблица 1. Почему пациенты повторно обращаются к врачу при острой инфекции нижних дыхательных путей
- Пациент неверно представляет себе естественное течение болезни
- Пациент продолжает беспокоиться по поводу симптомов болезни
- Пациенту нравится ходить на прием к врачу
- По настоянию членов семьи, друзей, сотрудников
- У пациента появились соображения, касающиеся важности симптомов
- Инфекция хронизируется или к ней присоединяется другая инфекция
- Проявляется серьезное основное заболевание
При повторном обращении по поводу респираторного заболевания врач общей практики прежде всего должен попытаться установить причину такого обращения (табл. 1). Вполне возможно, что оно вызвано необоснованными ожиданиями пациента, и наилучшим средством здесь было бы объяснение нормальных сроков выздоровления от простуды. Или же есть какое-то основное заболевание, не распознанное на первичной консультации, например астма, недолеченное хроническое обструктивное легочное заболевание, рак или бронхоэктазы.
В том случае если врач считает, что причина в продолжающейся инфекции, необходимо определить возможного возбудителя и выбрать соответствующий антибиотик (табл. 2). Ниже мы обсудим некоторые сложные случаи, которые необходимо иметь в виду [8,9]. Однако нужно помнить, что наиболее распространенными возбудителями остаются Streptоcoccus pneumoniae и респираторные вирусы, а сложные случаи составляют скорее исключение, чем правило в ежедневной общей практике.
Пенициллин-резистентный Streptococcus pneumoniae. Хотя число случаев развития лекарственной устойчивости неуклонно возрастает и представляет серьезную проблему для целого ряда европейских стран, в Англии антибиотикорезистентность пока не считается причиной неудачного лечения инфекций дыхательных путей. Нужно убеждать врачей общей практики проводить пневмококковую вакцинацию населения, входящего в группу риска, а антибиотики назначать строго по показаниям и в адекватной дозе.
Амоксициллин-резистентный Haemophilus influenzae. Haemophilus influenza (Hi) является частой бактериальной причиной обострения хронических обструктивых заболеваний легких (ХОЗЛ), а также вызывает персистирующий бронхит у здоровых взрослых людей. Некоторые антибиотики, такие как эритромицин и цефалоспорины первого поколения, недостаточно эффективны в отношении Hi. Наличие b-лактамазы объясняет отсутствие реакции на амоксициллин. Такие штаммы называются амоксициллин-резистентными Hi (АRHi).
Таблица 2. Возможная причина отсутствия цикла терапии острой инфекции нижних отделов дыхательных путей, назначенной на первом приеме*
Заболеваемость, обусловленная АRHi, растет и составляет сегодня в Великобритании 10-25% общего числа респираторных заболеваний в зависимости от региона. В других странах, таких как Испания, Португалия и некоторые районы Франции, уровень лекарственной устойчивости гораздо выше — это нужно иметь в виду в тех случаях, когда пациент мог заразиться зарубежом.
Об этом возбудителе следует помнить, если у пациента с ХОЗЛ после лечения часто повторяющимися курсами амоксициллина сохраняются симптомы заболевания и гнойная мокрота. В данном случае целесообразным будет недельный курс хинолона или коамоксиклава. От назначения ципрофлоксацина следует воздержаться, если пациент принимает теофиллин.
Moraxella catarrhalis. Некоторым название этого микроорганизма может показаться незнакомым, поскольку раньше его относили к роду Neisseria вида Branhamella.
Это грамотрицательный диплококк, входящий в нормальную микрофлору молодых и пожилых людей. Вслед за Haemophilus influenza и Streptococcus pneumoniae он является третьей по распространенности причиной обострения ХОЗЛ и часто поражает пациентов с тяжелыми хроническими легочными заболеваниями или раком легких.
Обнаружение этого микроорганизма служит показателем тяжести процесса. Сообщалось о недавнем наблюдении 42 случаев пневмонии, вызванной M. catarrhalis, когда около половины пациентов погибло от основного заболевания в течение трех месяцев после обнаружения инфекции.
Важно и то обстоятельство, что практически все штаммы сегодня являются b-лактамазопродуцирующими и соответственно амоксициллинорезистентными. Имеется предположение, что b-лактамаза, продуцируемая M. Catarrhalis, обеспечивает устойчивость к амоксициллину в норме чувствительных респираторных возбудителей, таких как S. pneumoniae и H. influenzae. Проводимая терапия не отличается от той, которая применяется в случаях АРHi (см. выше).
Pseudomonas aeruginosa. Об этом возбудителе нужно помнить в связи с возможностью развития бронхоэктазов и кистозной болезни. Стоит один раз заразиться Pseudomonas aeruginosa, и рецидивы могут следовать один за одним. В настоящее время единственным эффективным пероральным средством является ципрофлоксацин, но к нему быстро развивается устойчивость, и пациентов приходится госпитализировать для проведения внутривенной антибиотикотерапии и физиотерапии.
Другие бактериальные возбудители. Изредка выделяют грамотрицательную кишечную палочку, или Staphylococcus aureus. Эти возбудители чаще связаны с больничными пневмониями, но иногда обнаруживаются у пациентов, недавно выписавшихся из больницы.
Под атипичными обычно подразумеваются инфекции, вызываемые Mycoplasma pneumoniae, Chlamydia psittaci, Chlamydia pneumoniae, Coxiella burnetti и Legionella pneumophila. Лихорадка Q, возбудителем которой служит Coxiella burnetti, встречается редко (как правило, в сельской местности), поэтому не будет упоминаться в дальнейшем. Все атипичные инфекции трудно поддаются распознаванию на ранних стадиях; серологические исследования, проведенные как в острый период, так и в период реконвалесценции, редко дают положительный ответ и не представляют клинической ценности.
Ни один из возбудителей атипичных инфекций не поддается воздействию b-лактамных антибиотиков, что объясняет отсутствие эффекта от назначения амоксициллина.
Mycoplasma pneumoniae. Эпидемия, вызванная этим возбудителем, случается каждые три-четыре года, и в такой период может составлять значительную часть всех респираторных заболеваний.
Обычно она охватывает школьников, студентов и людей среднего возраста; маленькие дети и старики страдают редко.
В отличие от бактериальных инфекций, заболевание начинается постепенно, через 10-14 дней после заражения, проявляясь сухим кашлем или выделением скудной чистой мокроты. Общее недомогание и повышение температуры тела обычно умеренные, при исследовании грудной клетки обнаруживаются незначительные изменения. Иногда такие проявления, как сыпь, буллезный мирингит, а также выявление холодовых агглютининов помогают поставить диагноз.
Микоплазменную инфекцию следует заподозрить, если взрослый человек, до этого не жаловавшийся на здоровье, при отсутствии серьезных патологических симптомов и признаков интоксикации не поддается лечению амоксициллином. В этом случае имеет смысл попробовать назначить антибиотик из группы макролидов; альтернативный подход — тетрациклины. Кашель, как правило, медленно поддается лечению.
Хламидии. Большинствo врачей общей практики время от времени сталкиваются со случаями пситаккоза, вызванного длительным контактом с какой-нибудь любимой домашней птичкой. В последние годы установлено, что наиболее распространенным возбудителем инфекций дыхательных путей является Chlamydia pneumoniae, передающаяся от человека к человеку [10]. Эта инфекция проявляется такими же стертыми симптомами, как и микоплазменная, среди которых выделяются кашель и фарингит. Но, в противоположность микоплазменной инфекции, данное заболевание поражает и пожилых людей, часто вследствие реинфекции.
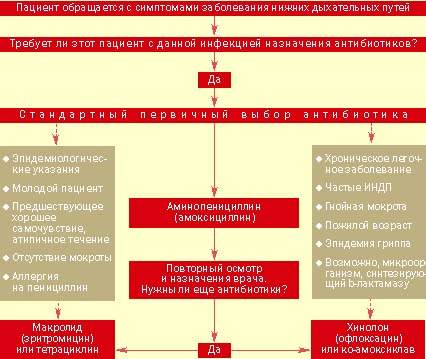 |
| Рисунок 2. Тактика ведения больного с выраженными клиническими показаниями для назначения антибиотиков при остром заболевании нижних дыхательных путей |
В некоторых исследованиях обнаружена связь между Chlamydia pneumoniaе и болезнями коронарных артерий и бронхиальной астмой, возможно обусловленная наличием хламидиального антигена, прикрепляющегося к эндотелию и эпителию. Рекомендуемое лечение — антибиотик из группы макролидов или тетрациклинов.
Legionella pneumophila. Болезнь легионеров все еще находится в центре внимания. Легионелла — редкий возбудитель пневмонии, развивающейся в местах большого скопления людей. Похоже, что легионелла не вызывает такие менее тяжелые заболевания дыхательной системы, как бронхит или инфекции верхних дыхательных путей. Состояние пациентов с болезнью легионеров достаточно тяжелое; обычно им требуется лечение в условиях стационара.
Известна связь этого заболевания с зараженными легионеллами источниками воды, поэтому упоминание пациента о заграничной поездке, пребывании в отеле или больнице, ванне джакузи помогает врачу общей практики правильно поставить диагноз. Нередко встречаются такие осложнения, как дыхательная недостаточность и энцефалит, поэтому все больные, даже в сомнительных случаях, должны быть направлены на госпитальное обследование.
- Практические советы по ведению больных с инфекциями дыхательных путей
Назначение антибиотиков. Подход к ведению больных с острыми инфекциями нижних дыхательных путей представлен на рис. 2. Ключевым моментом является принятие решения о назначении или неназначении антибиотиков. Большинство врачей общей практики считают необходимым применение антибиотиков при серьезных системных нарушениях, постоянном выделении гнойной мокроты, появлении местных признаков поражения легких и отягощенности предшествующими заболеваниями. Если уже решено использовать этот вид лечения, выбор нужного препарата не представляет особого труда.
 |
| Рисунок 3. Пациентам, входящим в группу риска, необходимо провести пневмококковую вакцинацию |
В большинстве случаев назначается амоксициллин. Согласно последним рекомендациям, доза амоксициллина принята равной 500 мг (а не 250 мг, как было раньше), чтобы снизить частоту развития резистентности пневмококков. Однако эта проблема лучше разрешается путем уменьшения общего количества назначений антибиотиков при инфекциях нижних дыхательных путей.
Врач общей практики не должен рекомендовать больному прием антибиотиков просто потому, что это самый легкий способ, или в случае, когда нет четких клинических показаний для их назначения. Проблемы резистентности возбудителей инфекций дыхательных путей решаются при назначении антибиотиков, обусловленном строгими показаниями. Снабжение пациентов простыми информационными листками значительно снижает необходимость повторных консультаций.
Литература
1. Office of Population Censuses and Surveys. Morbidity statistics from general practice: foutrh national study 1992. London: HMSO, 1995 (Series MB5;3).
2. Orr P. H., Scherer K., Macdonald A., Moffatt M. E. Randomosed placebo controlled trials of antibiotics for acute bronchitis: a critical review of the literature. J Fam Pract 1993; 36:507–512.
3. Macfarlane J. T., Holmes W. F., Macfarlane R. M., Lewis S. Contemporary use of antibiotics in 1089 adults presenting with acute lower respiratory tract illness in general practice in the UK: implications for developing managment guidelines. Respiratory Medicine, 1997; 91:427–434.
4. Holmes W. F., Macfarlane J. T., Macfarlane R. M., Lewis S. The influence of antibiotics and other factors on reconsultation for acute lower respiratory tract illness in primary care. Br J Gen Pract (in press).
5. Macfarlane J. T., Holmes W. F., Macfarlane R. M. Acutr lower respiratory tract illness in general practice; a study of the view on 787 patients and their influence on antibiotic prescribing. BMJ, 1997; 315:1211–1214.
6. Macfarlane J. T, Colville A., Guion A., Macfarlane R. M., Rose D. H. Prospective study of aetiology and outcome of adult lower respiratory tract infection in the community. Lancet, 1993; 341:511–514.
7. Macfarlane J., Prewett J., Rose D., Gard P., Guion A., Cunnigham R., Myint S. A prospective, case control study of the aetiology of community acquired lower respiratory tract infections in adult who felt to improve with initial antibiotics. BMJ, 1997; 315:1206–1210.
8. Venkatesan P., Innes J. A. Antibiotic resistance in common acute respiratory pathogenes. Thorax, 1995; 50:481–483.
9. Anon. Lower respiratory tract infections. MeReC Bulletin 1994; 5:5–8.
10. Torres A., ElEbiary M. Relevance of Chlamydia pneumoniae in community acquired respiratory infections. Eur Respir J, 1993; 6:7–8.
11. Macfarlane J. T., Holmes W. F., Macfarlane R. Reducing reconsultations for acute lower respiratory tract illness with an information leaflet. Br J Gen Pract, 1997; 47:710–722.
Читайте также:

