Атрофия мышц при интоксикациях
Обновлено: 25.04.2024
АМИОТРОФИЯ (amyotrophia; греческий отрицательная приставка a-, mys, myos — мышца и trophē — питание) — нарушение трофики мышц вследствие поражения периферического мотонейрона, сопровождающееся их дегенеративно-дистрофическими изменениями, истончением и нарушением сократительной функции. Различают группу наследственно обусловленных амиотрофией, среди которых выделяют спинальные амиотрофии и невральные. Амиотрофия может быть также результатом поражения мышц при коллагенозах, интоксикациях, инфекционно-паразитарных заболеваниях, эндокринных нарушениях, рефлекторных расстройствах и другое. (см. Атрофия мышечная).
Амиотрофии обусловлены вовлечением в патологический процесс клеток передних рогов спинного мозга,а также их отростков и спинномозговых нервов и характеризуются постепенным развитием параличей иннервируемых мышц, качественной реакцией перерождения мышц, снижением их электровозбудимости. Атрофии подвергаются как саркоплазма, так и миофибриллы. Атрофия мышечного волокна, возникающая в результате нарушения его иннервации, называется денервационной, вторичной амиотрофией, в отличие от первичного атрофического процесса в мышцах, при котором функция двигательного нейрона не страдает (см. Миопатия).
Гистологически при неврогенных повреждениях выявляется пучковый характер распределения атрофии мышечных волокон, сохранение наряду с атрофированными мышечными группами неатрофированных волокон. При электромиографии (см.) выявляется уменьшение амплитуды и длительности потенциала, изменение формы потенциала (полифазность типа группирования или типа потенциалов с короткими пиками).
При поражении передних рогов спинного мозга в атрофированных мышцах проксимальных отделов конечностей и туловища выявляются фибриллярные подергивания, асимметрия поражения; рано появляется атрофия и реакция перерождения мышц при исследовании электровозбудимости. При поражении двигательных корешков или волокон в составе периферического нерва возникают парезы или параличи преимущественно в дистальных отделах конечностей, расстройства чувствительности по полиневритическому типу, фибриллярные подергивания отсутствуют.
Среди наследственных амиотрофией, протекающих с преимущественным поражением клеток передних рогов спинного мозга, различают болезнь Верднига—Гоффманна, болезнь Кугельберга—Веландера, болезнь Арана—Дюшенна и заболевания с преимущественным поражением периферических нервов (невральная амиотрофия Шарко—Мари—Тута, гипертрофический неврит Дежерина—Сотта).
Спинальная амиотрофия Верднига—Гоффманна — заболевание, характеризующееся преимущественным перерождением клеток передних рогов спинного мозга. Впервые описано Верднигом (G. Werdnig, 1891) и Гоффманном (J. Hoffmann, 1893) у детей раннего возраста и рассматривалось как типичная форма амиотрофии. Современные представления о заболевании во многом отличаются от классического описания Верднига и Гоффманна. Это относится прежде всего к изменению представлений о времени развития клинических симптомов заболевания, о возможном доброкачественном течении, распространении морфологических изменений за пределы передних рогов спинного мозга. Болезнь нередко имеет семейный характер и передается по аутосомно-рецессивному типу.
При патологоанатомическом исследовании выявляются дегенеративные изменения и гибель клеток передних рогов, вторичное перерождение передних корешков и двигательных волокон периферических нервов. В некоторых случаях поражаются клетки задних и боковых рогов грудного отдела спинного мозга, задние и боковые столбы, ядра мозжечка.
Содержание
Клинические проявления
Клинические проявления весьма разнообразны по тяжести и течению. Наряду с тяжелыми формами болезни, протекающими с развитием мышечной слабости и расстройствами дыхания вскоре после рождения, с нарушениями, приводящими к смерти в первые годы жизни, имеются относительно доброкачественные формы, при которых больные доживают до юношеского или зрелого возраста.
Различают раннюю детскую (врожденную), а также детскую и поздние формы заболевания.
Ранняя детская форма амиотрофии клинически может проявляться во внутриутробном периоде или на первом году жизни. Отмечается позднее и вялое шевеление плода. Ребенок рождается с двигательными нарушениями, почти полным отсутствием движений в первые месяцы жизни. При обследовании обнаруживается отсутствие или снижение сухожильных рефлексов, атрофия мышц, разболтанность суставов. Врожденная миатония (см.) описана Оппенгеймом (Н. Oppenheim, 1900). По мнению автора, считавшего ее самостоятельной болезнью, в отличие от амиотрофии Верднига—Гоффманна, при этой форме не отмечается прогрессирования. Ведущим симптомом является атония мышц, мышечная слабость в проксимальных отделах конечностей и туловища, сухожильные рефлексы снижены. Однако многие современные авторы полагают, что врожденная миатония является доброкачественным вариантом ранней формы амиотрофии Верднига—Гоффманна. При ранней детской форме продолжительность жизни от 1 до 7 лет.
Детская форма амиотрофии начинается в возрасте до 4 лет, отличается от первой более медленным течением. Болезнь носит прогрессирующий характер. Длительность заболевания различна. Летальный исход наступает обычно до 14 лет.
Поздние формы спинальной амиотрофии: ювенильная форма амиотрофии и форма с более поздним началом — амиотрофия Кугельберга—Веландера. Описаны Кугельбергом и Веландером (Е. Kugelberg, L. Welander, 1954).
Заболевание характеризуется медленно прогрессирующей мышечной слабостью, атрофией мышц, наличием фасцикуляций, отсутствием пирамидных симптомов. Передается по аутосомно-рецессивному типу. Встречается у мужчин в 2 раза чаще, чем у женщин. У большинства больных наблюдается слабость проксимальных отделов верхних и нижних конечностей. Атрофия мышц, возникающая во всех случаях, может быть завуалирована наличием жировой клетчатки, часто обнаруживается гипертрофия ягодичных и икроножных мышц. Заболевание медленно прогрессирует, больные живут в среднем до 40 лет, иногда дольше. В более поздних стадиях в патологический процесс вовлекается мускулатура дистальных отделов конечностей, однако течение заболевания доброкачественное и в поздних его стадиях двигательные функции относительно сохранены, больные способны передвигаться, обслуживать себя.
Течение
Несмотря на различные варианты течения заболевания, развитие спинальной амиотрофии проходит определенные стадии.
Первая — препаралитическая — стадия характеризуется мышечной гипотонией, слабостью в проксимальных отделах конечностей, снижением рефлексов. Больные свободно передвигаются, мышечная слабость выявляется при физических нагрузках. Во второй стадии — паретической — развиваются глубокие парезы мышц конечностей, снижение рефлексов, слабость дыхательной мускулатуры. Заметно ограничена двигательная активность. На электромиограмме выявляется спонтанная активность, ритм частокола. Третья стадия — паралитическая. Больные обездвижены, у них отмечается излишнее отложение жира на конечностях и туловище, что часто маскирует атрофию мышц и фибриллярные подергивания. Параличи выражены в проксимальных и дистальных отделах конечностей. Четвертая стадия — кахектическая — характеризуется общим похуданием и диффузной атрофией мышц, спонтанными фасцикуляциями в мышцах. На электромиограмме — характерный ритм частокола. Пятая стадия — терминальная — характеризуется развитием контрактур с грубой деформацией скелета, при этом мелкие суставы кистей и пальцев стоп остаются менее пораженными.
При всех вариантах для спинальной амиотрофии характерно развитие парезов, параличей преимущественно проксимальных отделов конечностей. В большей степени поражаются сгибатели нижних конечностей. Характерно отсутствие глубоких рефлексов, фасцикулярные и фибриллярные подергивания скелетных мышц и мышц языка. Вследствие поражения дыхательных мышц возникает спинальный тип расстройства дыхания (ограничение подвижности грудной клетки, участие в акте дыхания вспомогательных мышц, снижение объема легочной вентиляции, артериальная гипоксемия и гиперкапния). Чувствительность и координационная сфера не нарушены, функция тазовых органов сохранена, интеллект не изменен.

Рис. 1. Электромиограмма больного спинальной амиотрофией Кугельберга—Веландера. Запись с четырехглавой мышцы. Максимальное мышечное напряжение: вверху — высокоамплитудные залповые потенциалы; внизу — потенциалы фасцикуляций с длительностью в 2—5 мсек
Электромиографическое исследование подтверждает неврогенный характер повреждения (ритм частокола, полифазия, фибрилляции и фасцикуляций (рис. 1).
Прогноз в тяжелых случаях неблагоприятный в связи с отсутствием специфической терапии. Непосредственной причиной смерти является пневмония или интеркуррентные инфекции.
Спинальная амиотрофия Арана—Дюшенна. Заболевание впервые было описано Дюшенном (G. В. A. Duchenne) в 1849 году и Араном (F.-A. Aran) в 1850 году. Нозологическая самостоятельность заболевания оспаривается многими авторами. Однако С. Н. Давиденков подчеркивает, что спинальная амиотрофия взрослых существует в качестве самостоятельной формы. В основе заболевания лежит хронический дегенеративный процесс в клетках передних рогов спинного мозга, передних корешках и периферических нервах. При гистологическом исследовании мышечных волокон выявляется пучковый характер атрофии, при электромиографическом — изменения, характерные для невральных атрофии.
Заболевание медленно, в течение ряда лет, прогрессирует. Летальный исход наступает обычно в результате интеркуррентных заболеваний.
Невральная амиотрофия Шарко—Мари—Тута — заболевание, относящееся к группе невральных амиотрофий. Описано Шарко и Мари (J. M. Charcot, P. Marie) в 1886 году во Франции и Тутом (Н. Н. Tooth) в 1886 году в Англии. Заболевание начинается в различном возрасте (преимущественно в возрасте 10—30 лет), чаще наблюдается у лиц женского пола. Передается по аутосомно-доминантному, реже — по аутосомно-рецессивному типу и рецессивному, сцепленному с полом.
Существует ряд атипичных, переходных форм заболевания, что затрудняет дифференциальную диагностику. В основе заболевания лежит так называемая хроническая периферическая невропатия (поражение нервов и изменение в интерстициальной соединительной ткани), изменения в двигательных клетках спинного мозга и в некоторых случаях в боковых и задних столбах спинного мозга. В мышцах в начальный период заболевания отмечается пучковый характер атрофии, в дальнейшем развивается гиперплазия соединительной ткани, выявляются дистрофические изменения мышечных волокон.
Электромиографическое исследование

Рис. 2. Электромиограмма больного невральной амиотрофией Шарко—Мари. Запись с передней болынеберцовой мышцы: вверху — максимальное мышечное напряжение; внизу — слабое мышечное напряжение. Сочетание потенциалов фибрилляций с однофазными денервационными потенциалами
Электромиографическое исследование позволяет обнаружить патологические изменения на ранних стадиях заболевания; при этом выявляются фибрилляции, длинные денервационные потенциалы, синхронизация потенциалов (рис. 2).
Гипертрофический неврит (семейная гипертрофическая невропатия) Дежерина—Сотта. Нозологическая самостоятельность этого заболевания не доказана. Одни авторы рассматривают гипертрофический неврит как один из вариантов невральной амиотрофии, другие — как самостоятельную форму болезни (см. Дежерина—Сотта гипертрофический неврит).
Диагноз ставят на основании клинической картины и данных лабораторных исследований.
Биохимические исследования
При амиотрофии установлено умеренное повышение активности ферментов: альдолазы, креатинфосфокиназы, трансаминаз в сыворотке крови. Однако по сравнению с первичными миопатиями (см.) это повышение выражено значительно слабее. Другим характерным биохимическим признаком амиотрофии является креатинурия, отражающая степень атрофии мышечной ткани; одновременно у больных снижается экскреция с мочой креатинина. Креатининовый показатель мочи, представляющий отношение креатинина к сумме креатина и креатинина и в норме равный единице, снижается до 0,8 (С. Н. Давиденков). Содержание в плазме крови и в моче у больных амиотрофией свободных аминокислот существенно не меняется. Наследственные амиотрофии следует дифференцировать с мышечными атрофиями (см. Атрофия мышечная). Прогноз неблагоприятный при ранних и быстротекущих формах амиотрофии — больные погибают в детском возрасте. При поздних и медленно текущих формах прогноз относительно благоприятный: больные благодаря сохранным мышечным группам могут компенсировать функцию пораженных мышц. Следует избегать переохлаждения и переутомления, ведущих к обострению заболевания.
Родителям, имеющим ребенка, больного спинальной или невральной амиотрофией, рекомендуется воздержание от дальнейшего деторождения.
Лечение
При всех формах амиотрофии рекомендуется АТФ, витаминотерапия (витамины группы В, витамин Е), аминокислоты (метионин, глутаминовая кислота и другие), анаболические гормоны (неробол, ретаболил), антихолинэстеразные препараты (прозерин, галантамин, нивалин). Лечение проводится курсами, длительность каждого курса составляет 1—11/2, месчцев. В год проводится несколько курсов лечения. Особое внимание должно быть направлено на предотвращение контрактур (массаж, гимнастика).
Библиография
Бадалян Л. О., Таболин В. А. и Вельтищев Ю. Е. Наследственные болезни у детей, с. 322, М., 1971; Бадалян Л. О. и др. Некоторые биохимические нарушения при прогрессирующих мышечных дистрофиях Вести. АМН СССР, № 8, с. 73, 1968, библиогр.; Давиденков С. Н. Наследственные болезни нервной системы, с. 154, М., 1932; он же, Клиника и терапия прогрессивных мышечных атрофии, Л., 1954; Иванов И. И. и Юрьев В. А. Биохимия и патобиохимия мышц, Л., 1961; Маньковский Б. Н. Прогрессирующие заболевания мышечного и нервно-мышечного аппарата, Многотомн. руководство по неврологии, под ред. С. Н. Давиденкова, т. 7, с. 13, Л., 1960; Наследственные болезни нервно-мышечной системы, под ред. Л. О. Бадаляна, М., 1974; Adams R. D., Denny-Brown D. а. Pearson С. М. Diseases of muscle, N. Y., 1954; Mc Kusick V. A. Mendelian inheritance in man, Baltimore, 1968, bibliogr.
Миозит — поражение мышечных тканей в результате воспаления или интоксикации. Характеризуется ослаблением мышц, возможна атрофия. Болезнь затрагивает мышечные ткани скелета. Миозит влияет на состояние кожных покровов и костные ткани. Требует консультации врача.
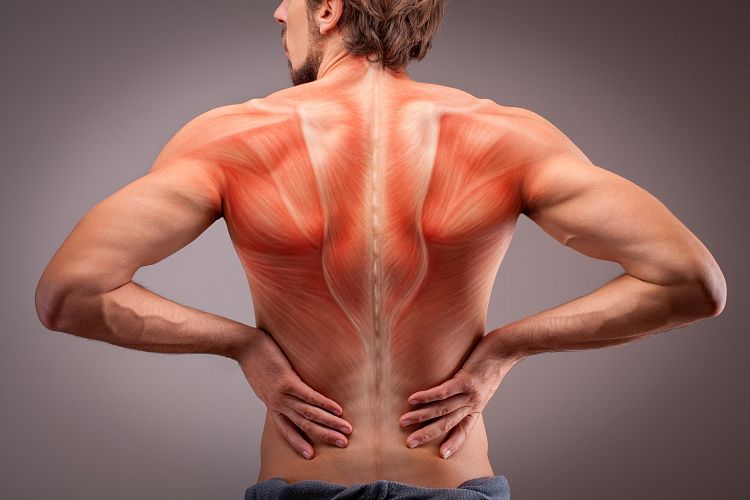
Симптомы миозита
Заболевание имеет следующую симптоматику:
- болезненные ощущения — основной признак миозита. Боль имеет острый или тупой характер, в зависимости от разновидности болезни. Дискомфорт усиливается при движениях и пальпации. Интенсивность болезненных ощущений увеличивается по мере прогрессирования недуга. На пораженной области возникает небольшая припухлость, мышечные ткани напрягаются, образуются уплотнения;
- увеличивается чувствительность кожных покровов пораженной области;
- слабость мышечных тканей характерная для хронической стадии заболевания. Объясняется дегенеративным процессом мышц, ограниченностью движений. Изначально симптом развивается при физической нагрузке, по мере прогрессирования болезни начинает беспокоить постоянно;
- повышенная температура тела, симптом развивается на острой стадии миозита, возможна лихорадка, увеличение местной температуры;
- невралгия.
Статью проверил
Дата публикации: 24 Марта 2021 года
Дата проверки: 24 Марта 2021 года
Дата обновления: 22 Апреля 2022 года
Содержание статьи
Причины
Существует несколько факторов, увеличивающих риск прогрессирования миозита:
- заболевание инфекционного характера, болезнь распространяется по кровеносной системе на ткани мышц;
- болезнь системного типа, организм воспринимает некоторые собственные клетки как раздражитель, начинает с ними борьбу;
- инвазия паразитарного характера, в случае проникновения паразита в мышечную ткань провоцирует воспалительный процесс;
- укусы насекомых;
- употребление алкогольных напитков, курение, прием наркотических препаратов, объясняется воздействием спиртов и ядов на мышечные ткани;
- перенесенные ранее физические повреждения, разрыв мышечных тканей провоцирует развитие недуга;
- вакцинации;
- неправильный прием лекарств;
- длительное пребывание на солнце;
- миозит — профессиональное заболевание для пианистов и водителей, объясняется длительной физической нагрузкой на группу мышечных тканей;
- длительное пребывание в неудобном положении;
- переохлаждения;
- вирусные заболевания;
- шейный остеохондроз.
Стадии развития миозита
Врачи выделяют несколько стадий:
- острая стадия, характеризуется ярко выраженной симптоматикой, болезненные ощущения усиливаются в зависимости от окружающей среды, например при похолодании;
- хроническая стадия развивается при отсутствии лечения острой, боли принимают постоянный характер.
Разновидности
Шейный миозит
Чаще развивается вследствие инфекционного заболевания, например после ОРВИ. Воспалительный процесс затрагивает длинные мышечные ткани головы и шеи. Болезненные ощущения имеют ноющий характер, постоянно сопровождают больного. При миозите мышц спины возможно сдавливание нервных отростков и сосудистых каналов.
Миозит мышц спины
Чаще развивается при невралгии межреберного характера или после физического повреждения. Характеризуется тупыми болезненными ощущениями, которые усиливаются при движении или вдохе. Объясняется изменением мышечных тканей грудной области. Чаще диагностируется миозит поясничных мышц, боли могут отдавать в нижние конечности.
Миозит плеча
Прогрессирует после интенсивной физической нагрузки или травмировании плечевой области. Характеризуется небольшой отёчностью, напряжением мышечных тканей, резкими болезненными ощущениями, которые усиливаются при движении верхними конечностями.
Миозит икроножных мышц
Развивается на фоне системных болезней, например красная волчанка. Основной симптом — слабость нижних конечностей. Возникает при физических нагрузках. По мере прогрессирования заболевания появляются болезненные ощущения. В тяжелых случаях возможно разрастание соединительной ткани и атрофия мышц.
Дерматомиозит
Заболевание затрагивает мышечные ткани кожи и внутренних органов. Патология отображается на работе всего организма. Характеризуется постепенным или резким ухудшением самочувствия больного. Врачи отмечают жалобы на дискомфорт во время движения. При отсутствии лечения развивается болезненность в состоянии покоя, атрофирование мышц.
Оссифицирующий миозит
Заболевание генетического характера, сопровождается окостенением мышечных тканей. Объясняется нарушением генов процесса формирования костей. Встречается редко.
Полимиозит
Подразумевает воспаление поперечно-полосатой мышечной ткани. Приводит к атрофированию мышц при отсутствии лечения.
Диагностика
Для постановки диагноза назначают общий анализ крови, биохимическое исследование кровеносных телец и урины. При необходимости используют инструментальные методы. Пациента направляют на рентгенографию, флюорографию, электромиографию. В сети клиник ЦМРТ для диагностики миозита используют следующие методы:
МРТ (магнитно-резонансная томография)
УЗИ (ультразвуковое исследование)
Дуплексное сканирование
Компьютерная топография позвоночника Diers

Чек-ап (комплексное обследование организма)

К какому врачу обратиться
Диагностикой и лечением миозита занимается терапевт. В зависимости от причины и тяжести заболевания может понадобиться консультация невролога, ревматолога или хирурга.
Мозжечковая дегенерация (атаксия мозжечка) — это расстройства работы мозжечка, расположенного в затылочной области головного мозга и отвечающего за координацию движений. Болезнь развивается в виде омертвения мозговых нейронов и провоцирует нарушение многих функций организма, от умственных и речевых до двигательных способностей человека. Возникает вследствие патологических отклонений в неврологии, а также при хронических заболеваниях нервной системы и головного мозга, образовании опухолей, интоксикации и алкоголизме. Чтобы вылечить патологию или облегчить состояние больного, следует обращаться к неврологу, наркологу, психиатру.

Клиники ЦМРТ более 10 лет специализируются на консервативном лечении мозжечковой дегенерации. Центры оснащены современным экспертным оборудованием для точной диагностики, эффективного лечения и реабилитации. Опытные специалисты применяют индивидуальный подход, составляя комплекс лечебных мероприятий, направленных на борьбу с патологией на всех стадиях.
Запишитесь на прием к неврологу
Поставить точный диагноз, определив причины и характер заболевания, назначить эффективное лечение может только квалифицированный врач на очном приеме.
Запишитесь к врачу через онлайн-форму на сайте или по телефону
Невролог
стаж 8 лет
Невролог • Остеопат • Мануальный терапевт
стаж 28 лет
Невролог
стаж 8 лет
Невролог • Остеопат • Реабилитолог • Вертебролог • Рефлексотерапевт
стаж 37 лет
Невролог • Мануальный терапевт
стаж 23 года
Адреса лечебных клиник в Москве
Симптомы мозжечковой дегенерации
Дегенерация мозжечка проявляется в виде различных симптомов:
- быстрые и резкие неконтролируемые вращательные движения глаз;
- разные формы нистагм (непроизвольных вращений глазных яблок) и саккад (вращений глаз в одном направлении);
- нарушения фокусировки взгляда на движущихся объектах;
- расстройства координации движений при ходьбе;
- атрофия мышц, тремор верхних и нижних конечностей;
- обострение нейродегенеративных болезней;
- нарушения речи, памяти, внимания и мышления;
- появление мозжечковой атаксии динамического или статико-локомоторного типа;
- нарушения мелкой моторики рук.
Статью проверил
Дата публикации: 24 Марта 2021 года
Дата проверки: 24 Марта 2021 года
Дата обновления: 22 Апреля 2022 года
Содержание статьи
Причины
Источники патологии бывают врождёнными (аутосомно-доминантного типа, или генетическими) и приобретёнными вследствие различных повреждений головы, нервов или хронических заболеваний. Основные причины мозжечковой атаксии:
- эмболия церебральных артерий;
- ишемический инсульт;
- атеросклеротические окклюзии;
- геморрагический инсульт;
- черепно-мозговые травмы;
- повреждения червя мозжечка (нервных волокон);
- повреждения коры головного мозга;
- внутримозговые опухоли и гематомы;
- нарушения кровоснабжения мозга;
- болезни эндокринной системы;
- рассеянный склероз;
- полирадикулоневропатия;
- раковые опухоли в теле;
- операции на голове и спинном мозге;
- родовые травмы;
- патологии левого или правого полушария;
- компрессия затылка;
- аномалии плода в утробе;
- острые и хронические инфекции;
- разные формы гидроцефалии;
- расстройства обменных процессов;
- внутримозговые кровоизлияния;
- острые интоксикации;
- дефицит витаминов;
- ишемическая атака;
- аллергические реакции на вакцинацию;
- энцефалит;
- менингиома;
- менингит;
- алкоголизм;
- наркомания.
Стадии развития мозжечковой дегенерации
Поражения полушарий и червя мозжечка могут иметь две формы течения болезни:
- Острую. Возникает резко с сильно выраженными признаками расстройства, чаще при сосудистых нарушениях (геморрагический или ишемический инсульт). Другие причины — травмы головы, рассеянный склероз, нагноение внутримозговой полости, отравление лекарствами или алкоголем. Сопровождается головокружением, головными болями, тошнотой, снижением умственных и двигательных функций. Грозит развитием гидроцефалии.
- Хроническую. Может возникнуть как вследствие наследственных факторов, так и перенесённых заболеваний. Появляется при наличии внутричерепных опухолей или системных раковых поражений. Выглядит как прогрессирующая стадия с периодическим ослаблением и обострением признаков. Основные причины — алкоголизм, наркомания, недостаток витамина B12, интоксикации, эндокринные болезни.
Разновидности
Атаксию классифицируют по различным признакам — происхождение и характер течения заболевания, выраженные симптомы, последствия и способы лечения.
Статическая мозжечковая дегенерация
- стоять прямо с вытянутыми вперёд руками;
- ровно пройти по условной линии;
- сделать равномерные приставные шаги;
- сделать несколько шагов сначала вперёд, потом назад;
- лечь и резко встать с ровной спиной.
Динамическая мозжечковая дегенерация
В отличие от статического типа, поражает сами полушария мозжечка. Болезнь такого вида выражается в отсутствии равномерности, плавности и точности движений. У пациента наблюдают дрожание конечностей, прерывистую речь, нистагмы и саккады, изменения почерка и походки.
Атрофия мозжечка Холмса
Сопровождается доброкачественным течением патологии. Развивается вследствие повреждений и нарушений функций нервных клеток и коры полушарий мозжечка. Выражается в снижении или отсутствии естественных двигательных рефлексов рук и ног.
Мозжечковая дегенерация Пьера-Мари
Обычно появляется в возрасте 25-45 лет из-за генетических факторов или возрастных изменений. Поражает обе стороны тела (двусторонний тип). Возникает при расстройствах пирамидной нервной системы спинного мозга и повреждениях ядер мозжечковой коры.
Диагностика
Чтобы правильно обследовать пациента, привлекают таких специалистов, как невролог, генетик, онколог, эндокринолог, нейрохирург. Невролог на визуальном осмотре выявляет локацию поражения. Если присутствуют расстройства речи, координации движений, зрения — повреждён червь, если снижен тонус мышц, деформированы походка и движения конечностей — поражены полушария. После осмотра врач направляет больного на диагностику:
Мышечная атрофия ведет к потере объема и числа волокон поперечно-полосатых мышц. Эта патология вызывается множеством разнообразных причин. Она развивается от длительного ограничения физической активности. Атрофия мышц обусловлена различными заболеваниями или травмами.
Некоторые разновидности атрофии вызваны генетическими проблемами. Если не обращаться к врачам и не лечить эти нарушения, пациент может потерять возможность передвигаться. Поэтому при ощущении слабости и болезненности в мышцах, надо как можно скорее посетить врача.
Описание
Мышечной атрофией называют расстройство трофики мышечной ткани. Его сопровождает постепенное истончение, а затем и перерождение волокон. С течением времени уменьшается их сократительная способность. Мышцы уменьшаются в объеме. Их волокна истончаются до полного исчезновения.
Мышечная ткань заменяется соединительно-тканными волокнами. Они неспособны сокращаться. У больного страдает двигательная функция. У него падает мышечная сила и тонус. Это приводит к потере двигательной активности или ее резкому снижению. Выделяют простую и дегенеративную разновидность расстройства.
Атрофия мышц дегенеративного характера – ведущий признак группы нервно-мышечных наследственных патологий. Простая атрофия мышц развивается из-за повышенной чувствительности мышечных волокон к повреждающим факторам различного характера.
Это расстройство может быть синдромом при различных болезнях, интоксикациях, травмах. Атрофия мышц наступает из-за истощения, гипоксии тканей, повреждения нервов, расстройства микроциркуляции, интоксикации, сдавливания опухолями, обменных нарушений.
Причины
Мышечная атрофия развивается по следующим причинам:
- наследственная предрасположенность;
- механические травмы;
- тяжелый физический труд;
- инфекции;
- миопатия;
- сахарный диабет;
- злокачественные новообразования;
- старение организма;
- паралич при поражении периферических нервов;
- голодание;
- интоксикация;
- расстройство процессов обмена;
- патологический процесс в верхне-теменной доле;
- длительная неподвижность;
- поражение спинного мозга;
- тромбоз крупных сосудов;
- родовая травма;
- неврологические расстройства;
- полиомиелит;
- миозиты;
- патологии поджелудочной железы.
При травме спины с поражением спинного мозга отмечается дистрофия мышц в зоне иннервации поврежденных сегментов.
Симптомы
При начальных проявлениях атрофии мышц больной быстро утомляется. Отмечают существенное снижение мышечного тонуса и заметны подергивания конечностей. При атрофии инфекционного или травматического генеза возникает повреждение двигательных нейронов.
Оно ведет к двигательным расстройствам, которые выражены в различной степени от небольшого ограничения движений в верхних и нижних конечностях до паралича. У пациента появляется слабость в ногах.
Ему трудно идти дальше, если вынужденно остановится. Пациент отмечает ощущение тяжести в ногах. У него затруднены движения, появляется онемение, нарушена походка. Затем возникает атрофия мышц ягодичной области.
У пациента формируется переваливающаяся походка. Выявляют онемение в зоне ягодиц. Характерно побледнение кожных покровов. Атрофия мышц в верхних конечностях выражается в ограничении возможности движений.
Больного беспокоит покалывание и онемение в кистях, снижение тактильной чувствительности. Механическое воздействие на ткани доставляет выраженный дискомфорт. У пациента нарушается трофика тканей, которая приводит к посинению кожных покровов.
Диагностика
При выявлении признаков мышечной атрофии необходимо обратиться к терапевту, травматологу, неврологу или ортопеду. Для уточнения диагноза производят следующие исследования:
- общеклинический анализ крови;
- электронейромиография
- электромиография;
- биопсия мышечной ткани;
- биохимия крови;
- генетическое обследование.
Для выявления причин развития атрофии мышц необходима диагностика состояния поджелудочной, щитовидной железы, печени.
Лечение
Терапия атрофии мышц определяется степенью потери этой ткани, а также характером основного заболевания. Это замедляет прогрессирование разрушения мышечных волокон. В качестве дополнительных мероприятий назначают ЛФК.
Комплекс состоит из растяжек, а также упражнений для предотвращения развития неподвижности конечностей. Они увеличивают мышечную силу, улучшают кровообращение, снижают спастичность.
Активно применяется при лечении метод функциональной электрической стимуляции. Здесь для стимуляции мышц применяют электрические импульсы. Электроды накладывают на пораженные зоны. Ток, проходя по тканям, взывает мышечное сокращение.
Специфическая лекарственная терапия будет зависеть от основного заболевания. Для этого как можно раньше выявить причину мышечной атрофии и приступить к лечению.
Читайте также:

