Бактериальная дизентерия окраска по граму
Обновлено: 19.04.2024
Нормальная микрофлора влагалища женщин репродуктивного возраста является одним из показателей здоровья, так как играет большую роль в поддержании микроэкологического статуса. Взаимодействие между представителями нормальной микрофлоры и клетками вагиналь
Нормальная микрофлора влагалища женщин репродуктивного возраста является одним из показателей здоровья, так как играет большую роль в поддержании микроэкологического статуса. Взаимодействие между представителями нормальной микрофлоры и клетками вагинального эпителия осуществляется на клеточном и молекулярном уровнях и постоянно контролируется со стороны ряда систем макроорганизма. Результатом этого взаимодействия являются создание и поддержание высокой колонизационной резистентности вагинального эпителия к внедрению патогенных и условно-патогенных микроорганизмов [1–6].
Бактериальный вагиноз выделен из категории неспецифических вагинитов в отдельную нозологическую форму. К нему относят патологические состояния во влагалище, сопровождающиеся нарушениями качественного и количественного состава нормальной микрофлоры и не связанные с бактериальными инфекциями, передаваемыми половым путем (ИППП), грибами или простейшими.
Согласно современным представлениям, бактериальный вагиноз — инфекционный невоспалительный синдром полимикробной этиологии, который связан с дисбиозом вагинального биотопа. Нарушение микроэкологии влагалища при бактериальном вагинозе характеризуется резким снижением количества или отсутствием лактобактерий, продуцирующих перекись водорода и увеличением количества Gardnerella vaginalis, грамотрицательных анаэробных бактерий (Bacteroides spp., Mobiluncus spp., Fusobacterium spp., Peptostreptoicoccus spp., M. hominis, U. urealyticum).
Гарднереллы, как и лактобациллы, обладают выраженной способностью к адгезии на поверхности вагинальных эпителиоцитов. Gardnerella vaginalis могут продуцировать токсические биопродукты, к которым относятся муколитические ферменты и гемолизин, являющийся лейкотоксическим фактором. Гемолизин, воздействуя на эритроциты, вызывает образование многочисленных пор в эритроцитарной мембране, а также оказывает влияние на лейкоциты, вызывая их структурные и функциональные нарушения. Этим и объясняется отсутствие существенной лейкоцитарной инфильтрации, т. е. активности лейкоцитов в присутствии Gardnerella vaginalis.
Определенную роль в патогенезе бактериального вагиноза играют представители семейства Mycoplasmataceae — Mycoplasma hominis и Ureaplasma urealyticum. 70% выделенных штаммов Ureaplasma urealyticum относятся к биовару Parvo, 23,3% — к биовару Т960. Большинство пациенток, у которых была выделена Ureaplasma urealyticum, относящаяся к биовару Parvo, имели в прошлом раннее начало половой жизни, частую смену половых партнеров, наличие одновременно нескольких половых партнеров, большое количество беременностей и абортов, а также сопутствующие гинекологические заболевания и ИППП.
При обследовании половых партнеров пациенток с бактериальным вагинозом морфотипы ассоциированных с бактериальным вагинозом микроорганизмов выявлялись у 25% мужчин, при этом клинические проявления (баланопостит) наблюдались только у 3,1% [2].
В результате субмикроскопического исследования вагинального экссудата пациенток с бактериальным вагинозом определены структурно-функциональные особенности микробных клеток, участвующих во взаимодействии друг с другом, при этом клетки организма-хозяина представлены преимущественно плоским эпителием. Установлена грамвариабельность Gardnerella vaginalis вне зависимости от характера микробных ассоциаций. Анализ электронограмм продемонстрировал, что структурная организация Gardnerella vaginalis, адгезированных на поверхности эпителиальных клеток, не зависела от сочетания бактериального вагиноза с другими инфекционными агентами.
При сочетании бактериального вагиноза с Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum наблюдали значительное количество микроорганизмов в межклеточном пространстве и бактерий, морфологически идентичных микоплазмам [2].
Пациентки предъявляют жалобы на обильные выделения из половых путей белого или серого цвета, часто с неприятным запахом, особенно после полового акта или во время менструации. При длительно текущем процессе выделения приобретают желтовато-зеленую окраску, становятся более густыми, нередко напоминают творожистую массу, обладают свойством пениться; слегка тягучие и липкие, они равномерно распределяются по стенкам влагалища. Количество белей варьирует от умеренных до весьма обильных, составляя в среднем 20 мл в сутки. Жалобы на зуд и дизурические расстройства встречаются редко: они могут совсем отсутствовать или появляться периодически. Эти симптомы обнаруживаются у 16–23% пациенток с нарушениями микрофлоры влагалища. Характерным признаком бактериального вагиноза является отсутствие воспалительного процесса стенок влагалища. Нередко женщины с бактериальным вагинозом жалуются на обильное менструальное кровотечение, боли в низу живота. В то же время у части пациенток какие-либо субъективные ощущения отсутствуют.
Диагностика бактериального вагиноза основана на данных анамнеза, оценке субъективных и объективных симптомов заболевания, результатах лабораторных тестов — микроскопического исследования материала, аминного теста и рН вагинального экссудата [3].
При сборе анамнеза выясняют:
- проведение в прошлом терапии антибиотиками, цитостатиками, кортикостероидами, противовирусными и противогрибковыми препаратами;
- наличие гинекологических, эндокринных заболеваний, заболеваний желудочно-кишечного тракта и др.;
- соблюдение правил личной и половой гигиены;
- данные о половых партнерах, практике сексуальных контактов и состоянии органов мочеполовой системы половых партнеров;
- применение и методы контрацепции.
Диагноз бактериального вагиноза устанавливается на основании наличия трех критериев из нижеперечисленных:
- гомогенные выделения беловато-серого цвета, равномерно адгезированные на слизистой оболочке вульвы и влагалища, имеющие неприятный запах;
- рН влагалищного экссудата > 4,5;
- положительный результат аминного теста (появление рыбного запаха при смешивании на предметном стекле влагалищного отделяемого с 10%-ным раствором КОН в равных пропорциях);
- изменения микроценоза влагалища, выявляемые при микроскопическом исследовании вагинального экссудата.
Обследование пациентки следует проводить не ранее, чем через 72 ч после последнего полового контакта (без использования презерватива); оно не проводится также во время менструации. В течение 3 нед до обследования женщина не должна получать терапию системными и местнодействующими антибактериальными препаратами [3].
При микроскопическом исследовании нативного и окрашенного по Граму вагинального мазка определяются следующие признаки:
Оценка общей микробной обсемененности вагинального отделяемого проводится по 4-балльной системе — по числу микробных клеток, обнаруживаемых в одном поле зрения при иммерсионной микроскопии:
1 балл (+) — до 10 микробных клеток в поле зрения, незначительное их количество (скудный рост);
2 балла (++) — от 11 до 100 микробных клеток в поле зрения, умеренное их количество;
3 балла (+++) — от 100 до 1000 микробных клеток в поле зрения, большое их количество;
4 балла (++++) — более 1000 микробных клеток в поле зрения, массивное их количество.
Так как Gardnerella vaginalis может быть обнаружена у здоровых женщин, культуральное исследование и ПЦР-диагностику для идентификации Gardnerella vaginalis не проводят. Культуральное исследование проводят при наличии показаний для определения видового и количественного состава вагинального микроценоза и исключения возбудителей ИППП.
При культуральном исследовании могут быть обнаружены изменения, характерные для бактериального вагиноза: общая микробная обсемененность превышает 10 9 КОЕ/мл; при использовании только аэробных условий культивирования рост микроорганизмов отсутствует или наблюдается рост сопутствующих условно-патогенных микроорганизмов (чаще в небольшом титре); полимикробный характер микрофлоры с абсолютным преобладанием облигатно-анаэробных видов и Gardnerella vaginalis; отсутствие роста лактобацилл или резкое снижение их титра (< 10 4 КОЕ/мл).
На основании проведенных исследований в настоящее время рекомендуется в план ведения пациенток включать:
- анализ субъективных и объективных проявлений заболевания, данных акушерско-гинекологического и полового анамнеза с акцентом на перенесенные или сопутствующие заболевания урогенитальной системы;
- комплексную оценку микробиоценоза влагалища, включающую идентификацию возбудителей ИППП;
- идентификацию Mycoplasma hominis, Ureaplasma urealyticum культуральным методом с количественной оценкой возбудителей;
- определение биопринадлежности Ureaplasma urealyticum для решения вопроса о выборе тактики дальнейшего ведения пациентки;
- целесообразно привлекать специалистов смежных дисциплин (гинекологов, урологов) при наличии сопутствующих заболеваний урогенитальной системы;
- клинико-микробиологическое обследование половых партнеров (профилактическое лечение половых партнеров пациенток с бактериальным вагинозом в настоящее время признано нецелесообразным).
Целью лечения является уменьшение выраженности клинических симптомов, нормализация лабораторных показателей, предотвращение развития возможных осложнений в период беременности, а также в послеродовом периоде и при выполнении инвазивных гинекологических процедур.
Результаты лабораторных исследований в норме следующие.
Лечение
Основное направление терапии — применение местных или системных антибактериальных препаратов с антианаэробным эффектом.
Показано применение клиндамицина. Препарат является 7-дезоксипроизводным линкомицина, ингибирует синтез белков в микроорганизмах, оказывает бактериостатическое или бактерицидное действие в зависимости от концентрации в макроорганизме и чувствительности микроорганизма. Препарат эффективен в отношении грамположительных микроорганизмов (стафилококков, стрептококков, пневмококков, палочки дифтерии), гарднерелл, микоплазм. Устойчивость микроорганизмов к клиндамицину вырабатывается медленно. При приеме внутрь клиндамицин всасывается лучше, чем линкомицин. После внутримышечного введения максимум его концентрации в крови отмечается через 2–2,5 ч. Препарат хорошо проникает в жидкости и ткани организма, выводится с мочой и желчью. При нарушении функции почек и печени выведение клиндамицина замедляется. При бактериальном вагинозе можно назначать одну из лекарственных форм клиндамицина: крем 2%-ный 5 г в аппликаторе (разовая доза) интравагинально 1 раз в день (на ночь) в течение 6 дней; овули 100 мг интравагинально на ночь в течение 3 дней; капсулы 300 мг внутрь 2 раза/сут в течение 7 дней.
Клиндамицин разрешенн к применению у беременных в виде 2%-го крема 5 г (разовая доза) интравагинально 2 раза/сут в течение 5 дней.
Также при бактериальном вагинозе можно назначать метронидазол. Он обладает широким спектром действия в отношении простейших, подавляет развитие Trichomonas vaginalis, Entamoeba histolytica и лямблий. В отношении анаэробных бактерий препарат высокоэффективен. Метронидазол хорошо всасывается при приеме внутрь, проникает в органы и ткани, проходит через плаценту и гематоэнцефалический барьер, накапливается в печени. Период полувыведения препарата составляет 8–10 ч, полностью выводится из организма через 1–2 сут после введения. Метронидазол в основном выводится с мочой в неизмененном виде и в виде метаболитов, частично — с калом. При применении метронидазола могут отмечаться потеря аппетита, сухость и неприятный вкус во рту, тошнота, рвота, диарея, головная боль, крапивница, зуд. Эти явления проходят после окончания лечения или отмены препарата. Возможна лейкопения. Препарат противопоказан при беременности и кормлении грудью, нарушениях кроветворения, остром течении заболеваний центральной нервной системы. Во избежание развития тяжелых побочных реакций следует предупреждать пациентов о недопустимости приема алкоголя и содержащих его продуктов как в ходе терапии метронидазолом, так и в течение 24 ч после ее окончания. При бактериальном вагинозе можно применять одну из следующих схем лечения с использованием метронидазола:
- гель 0,75% 5 г (разовая доза) интравагинально (на ночь) в течение 5 дней;
- таблетки 500 мг внутрь 2 раза/сут в течение 7 дней;
- таблетки 2 г внутрь однократно.
Также используют и другие производные метронидазола:
- тинидазол (Тинидазол-Акри, Веро-тинидазол), таблетки 2 г внутрь однократно;
- орнидазол (Орнидазол-Веро), таблетки 500 мг внутрь 2 раза/сут в течение 5 дней.
Ранее было проведено сравнительное изучение эффективности местнодействующих пробиотиков. Поскольку не было выявлено достоверных отличий в результатах лечения у пациенток, получавших и не получавших эти средства, в настоящее время их не рекомендуют при лечении бактериального вагиноза [3].
При сочетании бактериального вагиноза с ИППП, одновременно применяют антибактериальные препараты в соответствии с нозологической формой заболевания [2]. При неосложненной гонорейной инфекции назначают цефтриаксон однократно внутримышечно в дозе 250 мг (препарат является цефалоспориновым антибиотиком III поколения; после внутримышечного введения пик концентрации в крови отмечается через 1,5 ч; из организма выводится медленно). При обнаружении хламидий и/или микоплазм показано применение антибиотиков — макролидов, тетрациклинов.
Высокий терапевтический эффект, хорошая переносимость способствовали значительному распространению применения макролидов. Их антимикробный эффект обусловлен нарушением синтеза белка в рибосомах микробной клетки. Как правило, макролиды оказывают бактериостатическое действие, но в высоких концентрациях способны вызывать и бактерицидный эффект. Кроме антибактериального действия, макролиды обладают умеренной иммуномодулирующей и противовоспалительной активностью. Представителем III поколения макролидов является джозамицин (Вильпрафен). Этот антибиотик быстро абсорбируется из желудочно-кишечного тракта (ЖКТ), хорошо проникает через биологические мембраны и накапливается в тканях. Максимальная концентрация достигается через 1–2 ч после приема. Через 45 мин после приема дозы 1 г средняя концентрация джозамицина в плазме составляет 2,41 мг/л; связывание с белками плазмы не превышает 15%. Прием препарата с интервалом в 12 ч обеспечивает сохранение эффективной концентрации джозамицина в тканях в течение суток. Равновесное состояние достигается через 2–4 дня регулярного приема. Концентрация джозамицина в полиморфонуклеарных лейкоцитах человека, моноцитах и альвеолярных макрофагах примерно в 20 раз выше, чем в других клетках организма. Препарат биотрансформируется в печени до менее активных метаболитов. Джозамицин выводится главным образом с желчью, выведение же с мочой составляет менее 20%. Препарат назначается по 500 мг 2 раза в день в течение 10 дней.
Из группы тетрациклинов при ИППП наиболее эффективен доксициклин; в последние годы широко применяется Юнидокс Солютаб. Препарат отличается от Доксициклина гидрохлорида нейтральной реакцией, оказывает меньшее раздражающее действие на слизистую оболочку пищеварительного тракта и обладает улучшенными противомикробными и фармакокинетическими свойствами. Юнидокс Солютаб блокирует рибосомальную полимеразу и тормозит синтез белка в микроорганизмах.
Таблетки Юнидокс Солютаб обладают контролируемой растворимостью. Их можно не только принимать внутрь целиком или по частям, но и быстро приготовить из них сироп, суспензию (растворив таблетку в 20 мл воды) или раствор (растворив таблетку в 100 мл воды), которые обладают приятным вкусом. Таблетки растворяются в воде в течение 5–10 с, в биологических жидкостях — в течение 1 мин, превращаясь в равномерную суспензию.
Юнидокс Солютаб всасывается полностью. Биодоступность препарата составляет 95%. Через 2 ч после приема (200 мг в первый день и 100 мг в последующие дни) уровень в сыворотке составляет от 1,5 до 3 мг/мл. Препарат на 80–90% связывается с белками плазмы, хорошо проникает в ткани, накапливается в ретикулоэндотелиальной системе. Период полувыведения составляет 16–18 ч, после приема повторных доз — 22–23 ч.
Ранее были отмечены преимущества, заключающиеся в отсутствии побочных эффектов по типу эзофагитов, встречающихся при применении обычных форм Доксициклина гидрохлорида, способности накапливаться в высоких концентрациях в репродуктивных органах и активно воздействовать на инфекционный агент.
Юнидокс Солютаб назначают в дозе 200 мг в течение 10 дней.
Лабораторный контроль эффективности терапии следует проводить непосредственно по окончании этиотропного лечения: при микроскопии вагинальных мазков, окрашенных по Граму, необходимо констатировать степень эрадикации микроорганизмов, ассоциированных с бактериальным вагинозом; при посеве вагинального отделяемого — выявлять случаи колонизации факультативно анаэробными условно-патогенными микроорганизмами.
При сочетании бактериального вагиноза с урогенитальным хламидиозом и/или микоплазмозом лабораторный контроль необходимо повторить через 3 нед по окончании терапии.
По вопросам литературы обращайтесь в редакцию.
И. В. Хамаганова, доктор медицинских наук, профессор
РГМУ, Москва
Что такое дизентерия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Шигеллёзы, или дизентерия — это группа острых/хронических заболеваний, вызываемых бактериями рода Шигелла, которые поражают желудочно-кишечный тракт (преимущественно дистальный отдел толстой кишки). Манифестные формы (клиническая картина) дизентерии: синдром общей инфекционной интоксикации, синдром поражения желудочно-кишечного тракта (дистальный колит), синдром обезвоживания. При отсутствии адекватного лечения приводит к серьёзным осложнениям и хронизации.
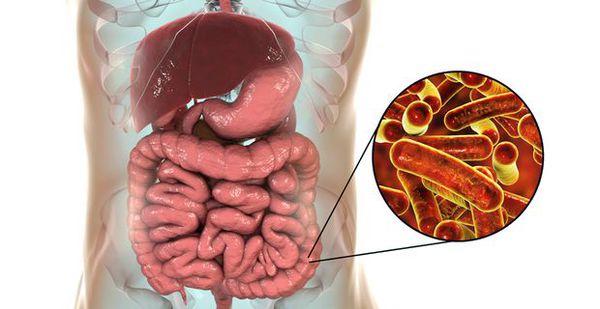
Возбудитель дизентерии
семейство — кишечные бактерии (Enterobacteriaceae)
род — Шигелла (Shigella)
виды — 4 основных:
- Dysenteriae (серовары — шигелла Григорьева-Шига, Штутцера-Шмитца, Ларджа-Сакса);
- Flexneri (Флекснера);
- Boydii (Боудии);
- Sonnei (Зонне).
Являются факультативно-анаэробными (способны существовать как при наличии, так и при отсутствии кислорода), граммотрицательными, неподвижными палочками. Хорошо растут на обычных питательных средах.
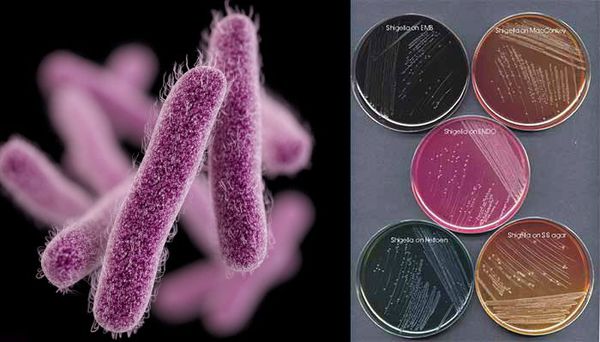
Имеют О-антиген (серологическая специфичность) и К-антиген (оболочечная структура). Клеточная стенка частично состоит из эндотоксина (липополисахарида), высвобождающегося при гибели микроорганизма. Бактерии вида Shigella Dysenteriae серовара Григорьева-Шига продуцируют высокоактивный цитотоксин, который нарушает синтез белка рибосомами клеток кишечного эпителия. Цитотоксин в совокупности с энтеротоксином (усиливающим секрецию жидкости и солей в просвет кишки) и нейротоксином (оказывающим нейротоксическое действие на сплетения Ауэрбаха) образует экзотоксином — токсин, выделяемый в процессе жизнедеятельности шигелл (Цитотоксин + энтеротоксин + нейротоксин = экзотоксин). Также у данной группы микроорганизмов происходит выделение гемолизинов — веществ, разрушающих эндотелий капилляров и вызывающий ишемию в тканях кишечника).
Факторы патогенности шигелл (механизм приспособления бактерий):
- адгезия (прикрепление к слизистой оболочке кишечника);
- инвазия (проникновение в эпителиальные клетки слизистой оболочки толстого кишечника);
- токсинообразование;
- внутриклеточное размножение.
Тинкториальные свойства (особенности микроорганизмов при окрашивании): быстро изменяют чувствительность к антибактериальным препаратам. Характерна высокая выживаемость во внешней среде (в воде, почве и пище при комнатной температуре сохраняются до 14 дней, в канализационных стоках — до 30 дней, при благоприятных условиях могут быть жизнеспособны до 4 месяцев). Способны к размножению в пищевых продуктах. При воздействии УФО (ультрафиолетового облучения) погибают за 10 минут, в 1% феноле — за 30 минут, при кипячении — мгновенно.
Интересная особенность: чем выше ферментативная активность возбудителя дизентерии, тем ниже вирулентность (минимальная доза возбудителя, способная заразить человека) и наоборот. [3] [6]
Эпидемиология
Антропоноз (повсеместное распространение).
Источник инфекции — человек (больной, носитель и лица с субклинической формой заболевания).
Минимальная инфицирующая доза для бактерии Григорьева-Шига — 10 микробных тел в 1 грамме вещества, для Флекснера — 10 2 бактерий, для Зонне — от 10 7 .
Длительное время в РФ превалировали случаи заражения, вызванные шигеллой Флекснера 2а, однако в настоящее время ввиду широкого развития туризма длительного преобладания какой-либо формы нет.
Механизм передачи — фекально-оральный (пищевой, водный, контактно-бытовой), из них преимущественно:
- Григорьева-Шига (контактно-бытовой путь);
- Зонне (с молоком и молочными продуктами);
- Флекснера (водный путь);
- Дизентериа (пищевой путь).
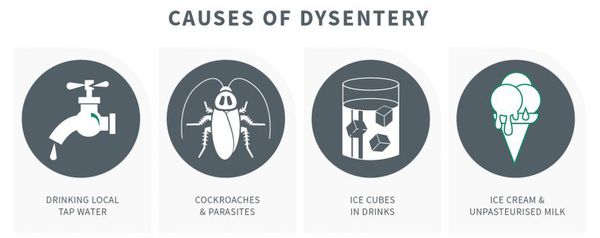
Наибольшую опасность представляют работники питания и водоснабжения. Больные заразны с начала болезни (конца инкубационного периода) и до трёх недель болезни.
Иммунитет непродолжителен и моноспецифичен (вырабатывается только к одному серотипу, который вызвал заболевание). [1] [4] [5]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы дизентерии
Инкубационный период — от 1 до 7 дней.
Начало заболевания острое (развитие основных синдромов наблюдается в первые сутки заболевания), характерна лихорадка постоянного типа.
Морфологические свойства дизентерии. Культуральные свойства дизентерии. Биохимические свойства дизентерии.
По морфологическим признакам шигеллы не отличимы от других представителей семейства Enterobacteriaceae. Бактерии дизентерии капсул не имеют, на твёрдых средах образуют гладкие (S-) и шероховатые (R-) колонии. S-колонии круглые, куполообразные, гладкие, полупрозрачные в проходящем свете.
R-колонии дизентерии неправильной формы, плоские, тусклые, с шероховатой поверхностью и неровными краями. Б жидких средах S-формы дизентерии дают равномерное помутнение, R-формы образуют придонный осадок, среда остаётся прозрачной.
Биохимические свойства дизентерии
• Наименьшей ферментативной активностью обладает S. dysenteriae (палочка Григорьева-Шига-Крузе). Бактерии ферментируют лишь глюкозу без газообразования. Поскольку они не разлагают маннит, а другие виды его ферментируют, они также известны как маннит-негативные шигеллы.
• S. flexneri (палочка Флекснера) не ферментирует лактозу, дульцит и ксилозу; почти все палочки образуют индол. Бактерии 6-й серологической группы (также известные как шигеллы Манчестер и Ньюкасл) образуют небольшое количество газа при ферментации глюкозы и других сбраживаемых углеводов.
• Весьма сходной биохимической активностью обладают и S. boydii, но они также ферментируют ксилозу, дульцит и арабинозу (обычно в первые 24 ч). Некоторые шигеллы Бонда также способны ферментировать мальтозу (на 6-20-е сутки), что имеет практическое значение при идентификации культур.
• S. sonnei не ферментируют сорбит и дульцит, не образуют индол, но расщепляют ксилозу и арабинозу, что сближает их с шигеллами Бонда. Отличительная особенность — способность расти при 45 С, ферментировать рамнозу, а также лактозу и сахарозу в более поздние сроки.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Шигеллёз — острая инфекционная болезнь, вызываемая бактериями рода Shigella с фекально-оральным механизмом передачи возбудителя и характеризующаяся картиной дистального колита и интоксикацией.
Классификация
Классификация шигеллёза, принятая в настоящее время, учитывает выраженность основных синдромов, характер течения болезни, вид возбудителя.
Классификация форм и клинических вариантов инфекционного процесса при шигеллёзе
| Форма | Клинический вариант | Тяжесть течения | Особенности течения | Этиология |
| Острый шигеллёз | Колитический Гастроэнтеро- колитический |
Этиология и патогенез
Шигеллёз вызывается рядом биологически близких между собой микроорганизмов, относящихся к семейству Enterobacteriacea и объединённых в род Shigella.
• группа A: Shigella Dysenteriae, 1 — Григорьева-Шиги, Shigella Dysenteriae, 2 — Штутцера-Шмитца и Shigella Dysenteriae 3-7 — Ларджа-Сакса;
• группа В: Shigella Flexneri с подвидом Shigella Flexneri 6 — Newcastle; серовары 1-6, каждый из которых подразделяют на подсеровары а и b, а также серовары 6, X и Y;
Шигеллы — грамотрицательные неподвижные палочки, факультативные аэробы. Палочка Григорьева-Шиги образует шигитоксин (экзотоксин), остальные виды содержат термолабильный эндотоксин — ЛПС. Наименьшая заражающая доза характерна для бактерий Григорьева-Шиги, большая — для бактерий Флекснера и наибольшая — для бактерий Зонне. Представители последних двух видов наиболее устойчивы в окружающей среде: на посуде и влажном белье они могут сохраняться в течение месяцев, в почве — до 3 мес, на продуктах питания — несколько суток, в воде — до 3 мес. При нагревании до 60 °С они гибнут через 10 мин, при кипячении — немедленно, в дезинфицирующих растворах — в течение нескольких минут. Из антибактериальных препаратов наибольшая чувствительность in vitro отмечена к фторхинолонам (100%).
В течение суток (иногда и дольше) шигеллы могут находиться в желудке. При этом некоторые из них здесь же распадаются, выделяя эндотоксин. Оставшиеся бактерии попадают в тонкую кишку, где могут задерживаться до нескольких суток и даже размножаться. Далее шигеллы продвигаются в нижележащие отделы кишечника, где также размножаются и распадаются в большем количестве, чем в тонкой кишке. Определяющий момент в развитии инфекционного процесса при шигеллёзе — способность шигелл к внутриклеточной инвазии. Первостепенное значение среди защитных механизмов имеет состояние естественных факторов резистентности, особенно местных (лизоцим и (β-лизины слизистой оболочки дистального отдела толстой кишки). Вместе с гуморальными факторами (бактерицидная активность, лизоцим, комплемент сыворотки крови) они реагируют на развитие инфекционного процесса на протяжении всего заболевания.
Степень неспецифической резистентности в известной мере определена генетически, но в то же время она зависит от ряда факторов: возраста больного, полноценности питания, сопутствующих заболеваний.
Эпидемиология
Единственный источник возбудителя шигеллёза — человек, больной манифестной или стёртой формой болезни, а также бактериовыделитель. Наибольшую опасность представляют больные, которые по роду своей работы связаны с приготовлением пищи, хранением, транспортировкой и продажей пищевых продуктов. Шигеллёз распространяется с помощью фекально-орального механизма передачи возбудителя. Этот механизм включает передачу возбудителя контактно-бытовым, водным, пищевым путём. Болезнь распространена повсеместно, но заболеваемость преобладает в развивающихся странах среди контингента населения с неудовлетворительным социально-экономическим и санитарно-гигиеническим статусом. Для стран с умеренным климатом характерна летне-осенняя сезонность.
Восприимчивость населения к шигеллёзу высока во всех возрастных группах, наиболее часто болеют дети. После перенесённого заболевания формируется непродолжительный типоспецифический иммунитет.
Специфическая профилактика не разработана. Меры неспецифической профилактики состоят в повышении санитарной культуры населения, обеззараживании питьевой воды (хлорирование, кипячение и др.), а также в соблюдении правил приготовления, хранения и реализации пищевых продуктов. Работники пищевых предприятий и лица, к ним приравненные, допускаются к работе только после отрицательного бактериологического анализа на шигеллёз, а после перенесённого заболевания шигеллёзом — после двух отрицательных результатов анализов, взятых не ранее чем на 3-й день после лечения, и отсутствии клинических проявлений. В случае пребывания больного в домашних условиях в квартире проводят текущую дезинфекцию. За лицами, находившимися в контакте с больными, устанавливают медицинское наблюдение в течение 7 дней.
Клиническая картина
Cимптомы, течение
Инкубационный период при остром шигеллёзе в большинстве случаев ограничивается 2 - 5 сут. Продолжительность заболевания составляет от нескольких дней до 3 мес, шигеллёз длительностью свыше 3 мес расценивают как хронический.
Этот вариант течения заболевания диагностируют чаще всего в клинической практике. При нём определяют характерные признаки шигеллёза, особенно при тяжёлом и среднетяжёлом течении. Заболевание, как правило, начинается остро, у некоторых больных удаётся установить кратковременный продромальный период, проявляющийся непродолжительным чувством дискомфорта в животе, лёгким ознобом, головной болью, слабостью. После продромального периода (а чаще на фоне полного здоровья) появляются характерные симптомы заболевания. Прежде всего возникают схваткообразные боли в нижней части живота, преимущественно в левой подвздошной области; иногда боль имеет разлитой характер, атипичную локализацию (эпигастральная, умбиликальная, правая подвздошная область). Особенность болевого синдрома — его уменьшение или кратковременное исчезновение после дефекации. Позывы к дефекации появляются одновременно с болью или несколько позже. Стул первоначально каловый, постепенно объём каловых масс уменьшается, появляется примесь слизи и крови, частота дефекаций нарастает. В разгаре болезни испражнения могут терять каловый характер и имеют вид так называемого ректального плевка, т.е. состоят лишь из скудного количества слизи и крови. Дефекация может сопровождаться тенезмами (тянущими судорожными болями в заднем проходе), часто возникают ложные позывы. Примесь крови чаще всего незначительна (в виде кровяных точек или прожилок). При пальпации живота отмечают спазм, реже — болезненность сигмовидной кишки, иногда — метеоризм. С первого дня заболевания появляются признаки интоксикации: лихорадка, недомогание, головная боль, головокружение. Возможны сердечно-сосудистые расстройства, тесно связанные с синдромом интоксикации (экстрасистолия, систолический шум на верхушке, приглушённость тонов сердца, колебания АД, наличие изменений на электрокардиограмме, свидетельствующие о диффузных изменениях миокарда левого желудочка, перегрузке правых отделов сердца).
Длительность клинической симптоматики при неосложнённом течении острого шигеллёза — 5-10 дней. У большинства больных сначала нормализуется температура и исчезают другие признаки интоксикации, а затем нормализуется стул. Более длительно сохраняются боли в животе. Критерий тяжести течения у больных шигеллёзом — выраженность интоксикации, поражения ЖКТ, а также состояние сердечнососудистой, ЦНС и характер поражения дистального отдела толстой кишки.
Клинические особенности этого варианта заключаются в том, что начало болезни напоминает ПТИ, а в разгар заболевания появляются и выходят на первый план симптомы колита. Гастроэнтеритический вариант острого шигеллёза по течению соответствует начальному периоду гастроэнтероколитического варианта. Отличие состоит в том, что в более поздние сроки симптомы энтероколита не доминируют и клинически этот вариант течения более сходен с ПТИ. При ректороманоскопии обычно наблюдают менее выраженные изменения.
Характеризуется кратковременными и невыраженнными клиническими симптомами (1-2-кратное расстройство стула, кратковременные боли в животе), отсутствием симптомов интоксикации. Подобные случаи заболевания диагностируют при определении ректороманоскопических изменений (как правило, катаральных) и выделении шигелл из испражнений. О затяжном течении острого шигеллёза говорят, когда основные клинические симптомы не исчезают или возобновляются после кратковременной ремиссии в течение 3 н е д - 3 мес.
К этой форме инфекционного процесса относят случаи, когда отсутствуют клинические симптомы на момент обследования и в предшествовавшие 3 мес, при ректороманоскопии и выделении шигелл из испражнений не выявляют изменений на слизистой оболочке толстой кишки. Бактерионосительство может быть реконвалесцентным (сразу после перенесённого острого шигеллёза) и субклиническим, если шигеллы выделяют у лиц, не имеющих клинических проявлений и изменений в слизистой оболочке дистального отдела толстой кишки.
Хроническое заболевание регистрируют в тех случаях, когда патологический процесс продолжается более 3 мес. Хронический шигеллёз по клиническому течению подразделяют на две формы — рецидивирующую и непрерывную. При рецидивирующей форме периоды обострений сменяются ремиссией. Обострения характеризуются клинической симптоматикой, характерной для колитического или гастроэнтероколитического варианта острого шигеллёза, но слабой выраженностью интоксикации. При непрерывном течении колитический синдром не стихает, отмечают гепатомегалию. При хроническом шигеллёзе на ректороманоскопии обнаруживают также умеренные воспалительные и атрофические изменения.
Протекает в основном тяжело, характеризуется острым началом, интенсивными схваткообразными болями в животе, ознобом, повышением температуры тела до 40 °С. Стул в первые сутки по внешнему виду напоминает мясные помои, затем объём испражнений уменьшается, появляется примесь крови и гноя. Отмечают тенезмы. В ряде случаев наблюдают инфекционно ИТШ, сепсис с высевом возбудителя из крови, может развиться гемолитико-уремический синдром. Гиповолемический шок встречается при обильном стуле и раннем присоединении рвоты.
Диагностика
Клинически диагноз шигеллёза можно установить только в случаях типичного колитического варианта течения болезни. Для уточнения диагноза в не подтверждённых лабораторно случаях проводят ректороманоскопию, которая во всех случаях шигеллёза выявляет картину колита (катарального, геморрагического или эрозивно-язвенного) с поражением слизистой оболочки дистального отдела толстой кишки, часто сфинктерит. Гастроэнтеритический и гастроэнтероколитический варианты диагностируют только в случае лабораторного подтверждения. Наиболее достоверный метод лабораторной диагностики шигеллёза — выделение копрокультуры шигелл. Для исследования проводят забор частиц испражнений, содержащих слизь и гной (но не кровь), возможен забор материала из прямой кишки ректальной трубкой. Для посева используют 20% жёлчный бульон, комбинированную среду Кауфмана, селенитовый бульон. Результаты бактериологического исследования можно получить не ранее чем через 3 - 4 дня от начала заболевания. Выделение гемокультуры имеет значение при шигеллёзе Григорьева-Шиги. В некоторых случаях гастроэнтеритов, предположительно шигеллёзной этиологии, проводят бактериологическое исследование промывных вод желудка. Диагноз может быть подтверждён также серологическими методами. Из них наиболее распространён метод со стандартными эритроцитарными диагностикумами. Диагностическим считают нарастание антител в парных сыворотках, взятых в конце первой недели болезни и через 7-10 сут, и увеличение титра в четыре раза. Также используют ИФА, РКА, возможно применение реакций агрегатгемагглютинации и РСК. Вспомогательный метод диагностики — копрологическое исследование, при котором обнаруживают повышенное содержание нейтрофилов, их скопления, наличие эритроцитов и слизи в мазке.
Из инструментальных методов основное значение имеют эндоскопические (ректороманоскопия и колонофиброскопия), которые подтверждают характерные изменения слизистой оболочки толстой кишки.
Дифференциальный диагноз
Чаще всего проводят с другими диарейными инфекциями, острой хирургической патологией органов живота, ЯК, опухолями дистального отдела толстой кишки. Наиболее актуальна дифференциальная диагностика с болезнями, представленными в таблице:
Сальмонеллёз представляет трудности для дифференциальной диагностики при наличии колитического синдрома, острый аппендицит — при атипичном течении (диарея, необычная локализация боли), мезентериальный тромбоз — при наличии крови в испражнениях, острый или подострый варианты ЯК — в случаях с лихорадкой, быстрым нарастанием диареи и появлением крови в испражнениях, раке дистального отдела толстой кишки — при малосимптомном течении болезни, если диарея и интоксикация развиваются в связи с инфицированием опухоли.
Осложнения
ИТШ, серозный (пропотевание кишечной стенки) или перфоративный (при циркулярных некрозах или глубоких язвенных дефектах) перитониты, острый панкреатит. Расстройства моторики могут привести к развитию инвагинации кишечника. Описаны кишечные и желудочные кровотечения, миокардит, полиартрит, нефрит, иридоциклит, полиневрит, токсический гепатит. У больных с неблагоприятным преморбидным фоном и тяжёлым течением шигеллёза развиваются пневмония и острая сердечно-сосудистая недостаточность, представляющие собой одну из основных причин летальных исходов.
Летальность в России в 7 0 - 8 0 - х гг. прошлого века не превышала 0,2%, в 90-е гг. за счёт преобладания высокопатогенного возбудителя шигеллы Флекснера 2А летальность возросла в пять раз, а во время отдельных вспышек (Санкт-Петербург, 1992-1994) достигала 6%. С конца 90-х гг. отмечают снижение летальности.
Лечение
При тяжёлом и среднетяжёлом течении показан постельный, при лёгком — палатный режим. В остром периоде при значительных кишечных расстройствах назначают стол № 4 по Певзнеру. При улучшении состояния, уменьшении дисфункции кишечника и появлении аппетита больных переводят на стол № 2 или № 13, а за 2 - 3 дня до выписки из стационара — на общий стол № 15.
• Назначать больному антибактериальный препарат необходимо с учётом сведений о территориальном пейзаже лекарственной устойчивости, т.е. о чувствительности к нему штаммов шигелл, выделяемых от больных в данной местности в последнее время.
• Продолжительность курса этиотропной терапии определяется улучшением состояния больного. При среднетяжёлой форме инфекции курс этиотропной терапии ограничен 3 - 4 днями, при тяжёлой — 5 - 6 днями.
• Комбинации из двух и более антибиотиков (химиопрепаратов) должны быть строго ограничены тяжёлыми случаями заболевания.
Больным с лёгкой формой шигеллёза в разгаре заболевания назначают фуразолидон в дозе 0,1 г четыре раза в сутки. При среднетяжёлом течении шигеллёза назначают препараты группы фторхинолонов: офлоксацин в дозе 0,2-0,4 г два раза в сутки или ципрофлоксацин в дозе по 0,25-0,5 г два раза в сутки; при тяжёлом течении — офлоксацин в дозе по 0,4 г два раза в сутки или ципрофлоксацин по 0,5 г два раза в сутки; фторхинолоны в комбинации с цефалоспоринами II поколения (цефуроксим в дозе 1 г три раза в сутки) или III поколения (цефтазидим или цефоперазон по 1 г т ри раза в сутки). В первые 2 - 3 дня лечения препараты вводят парентерально, затем переходят на приём внутрь.
Для лечения шигеллёза Григорьева-Шиги рекомендуют ампициллин и налидиксовую кислоту. Ампициллин вводят внутримышечно в суточной дозе 100-150 мг/кг каждые 4 - 6 ч в течение 5-7 дней. Налидиксовую кислоту назначают в дозе 1 г четыре раза в сутки в течение 5-7 дней.
При шигеллёзе Флекснера и Зонне эффективен поливалентный дизентерийный бактериофаг. Препарат выпускают в жидком виде и в таблетках с кислотоустойчивым покрытием. Принимают за 1 ч до еды внутрь в дозе 30-40 мл т ри раза в сутки или по 2 - 3 таблетки три раза в сутки. Возможно ректальное введение жидкого бактериофага. При тяжёлом течении препарат не показан из-за опасности массивного лизиса шигелл и утяжеления интоксикации.
• Проводят регидратационную терапию. При лёгкой форме — пероральное применение растворов оралит, регидрон, циклоглюкосолан. Скорость введения растворов 1-1,5 л / ч . При среднетяжёлом и тяжёлом течении применяют в /в введение кристаллоидных р-ров хлосоль, квартасоль, трисоль с учётом степени обезвоживания и массы тела больного со скоростью 60-100 м л / м и н и выше.
• При отсутствии выраженного обезвоживания и признаках интоксикации применяют 5% раствор глюкозы и плазмозаменители (гемодез, реополиглюкин). При гастроэнтеритическом варианте острого шигеллёза оказание медицинской помощи больному следует начинать с промывания желудка водой или 0,5% раствором натрия гидрокарбоната, применяя для этого желудочный зонд.
• Для связывания и выведения токсина из кишечника назначают один из энтеросорбентов: полифепан по одной столовой ложке три раза в сутки, активированный уголь в дозе 15-20 г т ри раза в сутки, энтеродез по 5 г т ри раза в сутки, полисорб МП по 3 г т ри раза в сутки, смекту по одному пакетику три раза в сутки.
• Кишечные антисептики: оксихинолин (по одной таблетке три раза в сутки), энтерол — противодиарейный препарат биологического происхождения (из дрожжей Saccharomyces boulardii) назначают по 1-2 капсулы два раза в сутки.
• Для коррекции и компенсации пищеварительной недостаточности применяют ферментные препараты: ацидин-пепсин, панкреатин, панзинорм в сочетании с препаратами кальция (в дозе 0,5 г два раза в сутки).
• В остром периоде для купирования спазма толстой кишки назначают дротаверина гидрохлорид (но-шпа) по 0,04 г т р и раза в сутки, препараты красавки (белластезин, бесалол).
• В течение всего периода лечения рекомендуют комплекс витаминов, состоящий из аскорбиновой (500-600 мг/сут), никотиновой кислоты (60 мг/сут), тиамина и рибофлавина (по 9 мг/сут).
• С целью коррекции биоценоза кишечника больным с выраженным колитическим синдромом при поступлении назначают препараты на основе микроорганизмов рода Bacillus: биоспорин, бактиспорин* по две дозы два раза в день в течение 5-7 дней. При выборе препарата предпочтение следует отдавать современным комплексным препаратам: пробифору, линексу, бифидумбактерину-форте, флорину форте и др.
При лёгкой форме — 7 - 1 0 дней, при среднетяжёлой — до 16-18 дней, при тяжёлой форме и осложнениях — до месяца и более. Пациентов из декретированной группы не допускают к работе, пока не получат двух отрицательных результатов бактериологического исследования испражнений.
Диспансерному наблюдению подлежат больные хронической дизентерией, работники пищевых предприятий и лица, к ним приравненные (в течение 3 мес, а при хронической дизентерии — в течение 6 мес).
Этиология. С 1930 г. бациллы, выделяемые от больных дизентерией, официально были объединены в род Shigella, семейство Enterobacteriaceae. Идентификация шигелл осуществляется по их биохимическим и антигенным свойствам (О — антигенам), в соответствии с чем выделяют четыре группы шигелл (см. таблицу 1).
По своим морфологическим свойствам шигеллы представляют собой неподвижные, грамотрицательные бактерии. Общим и важнейшим свойством всех представителей рода Shigella является инвазивность, т. е. способность бактерий к инвазии в эпителиальные клетки кишечника с последующим размножением и паразитированием в них. Различные виды шигелл сильно отличаются по своим исходным биологическим свойствам, что, собственно, и определяет степень их вирулентности и патогенности для человека. Наиболее высокой вирулентностью обладают Sh. dysenteriae 1, что обусловлено прежде всего их способностью продуцировать один из мощнейших природных токсинов — Шига-токсин. Некоторые другие виды шигелл также способны продуцировать шига-подобные токсины, но с существенно более низкой активностью. Исключительно высокие вирулентные свойства Sh. dysenteriae 1 определяют крайне низкую инфицирующую дозу, которая составляет всего десятки или сотни микробных клеток. Для других видов шигелл инфицирующая доза определяется на один-два порядка выше.
Шигеллы относительно устойчивы к факторам внешней среды и способны длительно сохраняться на предметах домашнего обихода, в воде они сохраняют свою жизнеспособность до двух-трех недель, а в высушенном и замороженном состоянии — до нескольких месяцев. Высокие же температуры, наоборот, способствуют быстрой их гибели: при температуре +60°С — в течение 10 мин, а при кипячении — мгновенно. Достаточно высокую чувствительность шигеллы проявляют к дезинфицирующим средствам, ультрафиолетовым и прямым солнечным лучам.
Несмотря на разнообразие возбудителей шигеллезов, наибольшее эпидемическое значение для большинства стран мира имеют Sh. flexneri и Sh. sonnei. Хотя шигеллы распространены повсеместно (антропонозная инфекция), наиболее высокие показатели заболеваемости регистрируются в странах и регионах с низкой санитарией и высокой плотностью населения, что существенно облегчает возможность передачи возбудителя от человека к человеку. По расчетным данным, ежегодно в мире регистрируется около 140 млн случаев заболеваний шигеллезами. Восприимчивость к шигеллезной инфекции у лиц разных возрастных групп неодинакова. Наиболее восприимчивы к ним дети до двух-трех лет.
Патогенез. Основу патогенеза инфекционных заболеваний составляют особенности и характер взаимодействия микробов не только с клетками макроорганизма, но и с неспецифическими и специфическими защитными системами организма.
Шигеллы обладают достаточно выраженными вирулентными свойствами, вследствие чего заболевание может развиваться и при невысокой инфицирующей дозе (в сравнении с такими энтеропатогенными бактериями, как сальмонеллы и кишечные палочки). Благодаря относительной резистентности к действию желудочного сока и желчных кислот, шигеллы, не теряя своей вирулентности, проходят через желудочный барьер и проксимальные отделы тонкой кишки. В патогенезе заболевания выделяют тонко- и толстокишечные фазы, степень выраженности которых в конечном итоге и определяет вариант течения заболевания. У больных с типичным, колитическим вариантом острой дизентерии, тонкокишечная фаза клинически вообще не манифестируется, и заболевание изначально проявляется поражением дистального отдела толстой кишки. Тонкокишечная фаза обычно бывает непродолжительной и ограничивается двумя-тремя днями. Первичная транслокация шигелл через эпителиальный барьер осуществляется специализированными М-клетками, способными транспортировать как сами бактерии, так и их антигены в лимфатические образования кишечника (фолликулы, Пейеровы бляшки) с последующим их проникновением в эпителиальные клетки и резидентные макрофаги. Высвобождаемые в процессе транслокации шигелл токсические субстанции (экзо- и эндотоксины, энтеротоксины и т. д.) инициируют развитие синдрома интоксикации [3], который при шигеллезах всегда предшествует развитию диарейного синдрома.
Ключевым фактором вирулентности шигелл является их инвазивность, т. е. способность к внутриклеточному проникновению, размножению и паразитированию в клетках слизистой оболочки толстой кишки (преимущественно в дистальном отделе) и резидентных макрофагах собственной пластинки (см. рисунок 1). Посредством макроцитопиноза шигеллы проникают в цитоплазму эпителиальных клеток, где очень быстро лизируют фагосомальную мембрану, что приводит к повреждению клеток и их гибели. Последующее распространение шигелл происходит через базолатеральные мембраны эпителиальных клеток. Повреждение и разрушение эпителиальных клеток сопровождаются развитием воспалительной инфильтрации полиморфно-ядерными лейкоцитами собственной пластинки, формированием язв и эрозий слизистой оболочки толстой кишки, что клинически проявляется развитием диареи экссудативного типа. Способность к инвазии и внутриклеточному размножению шигелл кодируется генетическими механизмами, экспрессия которых происходит только в условиях in vivo. Несмотря на инвазивность, шигеллы не способны к глубокому распространению, в силу чего системной диссеминации возбудителя при шигеллезах, как правило, не происходит (за исключением Sh. dysenteriae 1).
Моторика кишечника является важным защитным механизмом, ограничивающим и препятствующим прикреплению и инвазии шигелл к эпителиальным клеткам, что наглядно демонстрируют затягивание и утяжеление инфекционного процесса у лиц, получающих препараты, подавляющие моторику кишечника.
Наблюдаемые у больных с шигеллезами дисбиотические изменения в составе нормальной микрофлоры толстого кишечника оказывают существенное влияние на скорость репарации слизистой в стадии реконвалесценции и восстановление функциональной активности кишечника.
После перенесенного заболевания у больных формируется непродолжительный (до одного года) типо- и видоспецифический иммунитет, в силу чего возможно реинфицирование.
Клиника. Клиническая картина шигеллезов весьма вариабельна, что нашло свое отражение в применяемой клинической классификации заболевания (см. таблицу 2). Хотя считается, что Sh. sonnei, как менее вирулентные штаммы шигелл, чаще вызывают более легкие формы заболевания, следует помнить, что этиология шигеллеза лишь предопределяет, но не определяет особенностей течения заболевания у конкретных больных (по форме, варианту и тяжести течения).
Хроническая форма дизентерии в настоящее время встречается достаточно редко и, по данным литературы, не превышает в 1-2% случаев, хотя существует мнение, что столь низкий ее удельный вес может быть обусловлен недостаточно разработанными критериями диагностики. Значительно чаще врачи в своей практической деятельности встречаются с острыми формами шигеллезов, которые и представляют наибольший интерес в плане адекватной оценки выявляемой у больного клинической картины заболевания, полноты обследования, правильности и своевременности проводимой терапии.
Инкубационный период при шигеллезах может варьировать от 8—12 ч (при гастроэнтеритическом варианте) до пяти дней (при колитическом варианте заболевания), составляя, в среднем, два–три дня.
Если примесь слизи в стуле является типичным признаком острой дизентерии, то кровь может присутствовать в микроскопических количествах и обнаруживаться только при копроцитоскопическом исследовании. Визуализируемая примесь крови в стуле определяется в виде прожилок. При более тяжелом течении заболевания дефекация может заканчиваться выделением небольшого количества слизи с прожилками крови.
Критериями тяжести течения колитического варианта острой дизентерии являются выраженность интоксикационного синдрома и характер поражения дистального отдела слизистой толстого кишечника (см. таблицу 3). Выраженного обезвоживания у больных при колитическом варианте острой дизентерии не выявляется ввиду отсутствия рвоты и скудного характера стула.
Гастроэнтероколитический вариант дизентерии также характеризуется острым началом заболевания: с озноба, лихорадки, головной боли и одновременным появлением синдрома гастроэнтерита — спастических болей в эпигастральной области, тошноты, рвоты, жидкого водянистого стула. Клинические признаки колита в первые сутки заболевания, как правило, отсутствуют и появляются лишь спустя один—три дня, что соответствует патоморфологическим этапам поражения слизистой желудочно-кишечного тракта. В зависимости от кратности рвоты и интенсивности диарейного синдрома, у больных достаточно рано выявляются признаки обезвоживания организма (сухость слизистых ротоглотки, бледность кожных покровов и цианоз, заостренные черты лица, снижение артериального давления, олигоурия и др.). С момента распространения патологического процесса на слизистую толстого кишечника проявления гастроэнтерита постепенно купируются: рвота прекращается, уменьшается объем испражнений, в стуле появляются патологические примеси (слизь и кровь). В зависимости от характера поражения слизистой дистального отдела толстой кишки, больные могут отмечать появление тенезмов и ложных позывов. При пальпации живота в первые дни заболевания отмечается урчание по ходу толстого кишечника, а в последующие дни появляется и нарастает болезненность и спазм сигмовидной кишки.
Тяжесть течения гастроэнтероколитического варианта дизентерии определяется на основании выраженности интоксикации и обезвоживания организма. В большинстве случаев оно не превышает II-III степени.
Редким вариантом течения острой дизентерии является гастроэнтеритический, характеризующийся большим сходством с пищевыми токсикоинфекциями.
Осложнения. Хотя наиболее высок риск развития осложнений у больных дизентерией, вызванной Sh. dysenteriae 1, на современном этапе прослеживается отчетливая тенденция к увеличению тяжелых форм дизентерии, обусловленных другими видами шигелл (в частности, Sh. flexneri), что, соответственно, отражается и на возможности развития осложнений. К числу наиболее грозных осложнений относятся: инфекционно-токсический шок; перфорация кишечника с развитием перитонита; энцефалический синдром (синдром фатальной энцефалопатии или синдром Ekiri), который преимущественно развивается у детей и иммунокомпрометированных пациентов при дизентерии, обусловленной Sh. sonnei или Sh. flexneri; бактериемия, выявляющаяся при дизентерии Sh. dysenteriae 1 в 8% случаев и крайне редко — при инфицировании другими видами шигелл (у детей до года, ослабленных, истощенных и иммунокомпрометированных пациентов); гемолитико-уремический синдром, развивающийся через неделю от начала заболевания и характеризующийся микроангиопатической гемолитической анемией, тромбоцитопенией и острой почечной недостаточностью. Нередко у больных могут развиваться осложнения, связанные с активизацией вторичной микрофлоры: пневмонии, отиты, инфекции мочевыводящих путей и др. К числу редких, но вероятных осложнений относятся реактивный артрит и синдром Рейтера (около 2% заболевших, экспрессирующих HLA-B27). В последние годы обсуждается возможная роль шигеллезов в формировании синдрома раздраженного кишечника.
Диагностика и дифференциальная диагностика. Специфическая диагностика шигеллезов основана на выделении и идентификации шигелл из испражнений больного и проведения серологических и/или иммунологических исследований, направленных на обнаружение антигенов шигелл или антител к ним. Без лабораторного подтверждения диагноз дизентерии может быть установлен только при типичной клинической картине.
Хотя диагностическая ценность эндоскопического исследования толстой кишки (ректороманоскопия и фиброколоноскопия) у больных с подозрением на шигеллезы ограничена, полученная при ее проведении информация позволяет: а) объективно оценить характер поражения слизистой толстой кишки; б) проводить дифференциальную диагностику и в) контролировать эффективность проводимой терапии.
В зависимости от характера поражения выделяют следующие варианты проктосигмоидита: катаральный, катарально-геморрагический, эрозивный, эрозивно-язвенный и фибринозный, которые, как правило, соответствуют тяжести течения заболевания.
При проведении дифференциальной диагностики в первую очередь необходимо исключить другие острые кишечные инфекционные заболевания, для которых типично развитие экссудативной диареи, а именно энтероинвазивные эшерихиозы, сальмонеллез, иерсиниоз (Y. enterocolitica), кампилобактериоз (Campylobacter jejuni), инфекция Clostridium difficile и амебиаз (протозойное заболевание, обусловленные Entamoeba histolytica). Кроме этого, необходимо помнить, что под маской шигеллезов могут дебютировать такие заболевания, как неспецифический язвенный колит и болезнь Крона.
Лечение. Лечение больных дизентерией может осуществляться не только в условиях специализированного инфекционного отделения, но и амбулаторно, что определяется клиническими и эпидемиологическими показаниями. В первую очередь следует госпитализировать пациентов со среднетяжелыми и тяжелыми формами заболевания, при затяжном и хроническом течении — пациентов с тяжелыми сопутствующими заболеваниями, детей до одного года и пожилых, а также лиц, представляющих эпидемическую опасность (независимо от варианта и тяжести течения заболевания) — работников пищевых предприятий и лиц, к ним приравненных.
Учитывая характер поражения слизистой кишечника, пациенты с дизентерией, особенно в острый период болезни, нуждаются в строгом соблюдении лечебного питания. Из рациона следует исключить любые продукты, оказывающие раздражающее (механическое, химическое и др.) действие. Ввиду формирующейся у больных недостаточности лактозы, из диеты исключается цельное молоко. Расширение диеты осуществляют постепенно, только по мере выздоровления больного. И все же переход на обычное питание следует осуществлять не ранее полного выздоровления, характеризующееся репарацией слизистой (см. таблицу 3).
Поскольку антибактериальная терапия всегда рекомендовалась для лечения больных дизентерией, серьезную проблему на сегодняшний день представляет формирование у шигелл резистентности к антимикробным препаратам, особенно в тех странах, где осуществляется их безрецептурная продажа и самолечение [5]. Недавно проведенные в нашей стране исследования [6] подтвердили высокую частоту резистентности у Sh. flexneri и Sh. sonnei к цефотаксиму (96,6 и 94,2%, соответственно), тетрациклину (97,7 и 92,8%), левомицетину (93,2 и 50,7%), ампициллину (95,5 и 26,1) и ампициллину/сульбактаму (95,5 и 23,2%). Резистентность не была выявлена лишь к ципрофлоксацину, норфлоксацину и налидиксовой кислоте.
Выбор антимикробного препарата и схема его применения у больных дизентерией определяются вариантом и тяжестью течения заболевания. При гастроэнтеритическом варианте антимикробная терапия не показана и больным назначают лишь патогенетическую терапию. При легком течении колитического и гастроэнтероколитического вариантов дизентерии больным целесообразно назначать фуразолидон по 0,1 г четыре раза в день или налидиксовую кислоту (невиграмон) по 0,5-1,0 г четыре раза в день в течение трех—пяти дней. Наиболее эффективными средствами для лечения больных со среднетяжелым и тяжелым течением дизентерии являются препараты фторхинолонового ряда (ципрофлоксацин, норфлоксацин и др.), цефалоспорины III поколения (цефотаксим), которые назначают в общетерапевтических дозах в течение пяти—семи дней. При тяжелом течении может проводиться комбинированная антибактериальная терапия (фторхинолоны и аминогликозиды; цефалоспорины и аминогликозиды).
Кроме антибактериальной терапии важное место в лечении больных дизентерией занимает патогенетическое лечение, включающее проведение дезинтоксикации и регидратации. В острый период заболевания больным целесообразно назначать десмол и смекту, обладающие противовоспалительным и мембраностабилизирующим действием на слизистую кишечника. После купирования интоксикационного синдрома больным показаны препараты, нормализующие процессы пищеварения и всасывания (дигестал, мезим-форте, панзинорм, фестал, холензим, ораза и др.). Коррекцию микробиоценоза кишечника следует проводить только в периоде реконвалесценции, когда купирована островоспалительная реакция. В этот же период больным показаны физиотерапевтические процедуры, ускоряющие процесс репарации слизистой толстого кишечника.
Литература
В. А. Малов, доктор медицинских наук, профессор
А. Н. Горобченко, кандидат медицинских наук
ММА им. И.М. Сеченова
Читайте также:

