Бактериальный вагиноз и стафилококк
Обновлено: 17.04.2024
Бактериальный вагиноз (БВ) — общий инфекционный невоспалительный синдром, связанный с дисбиозом влагалищного биотопа и сопровождающийся чрезмерно высокой концентрацией облигатно- и факультативно-анаэробных условно-патогенных микроорганизмов (УПМ) и
Бактериальный вагиноз (БВ) — общий инфекционный невоспалительный синдром, связанный с дисбиозом влагалищного биотопа и сопровождающийся чрезмерно высокой концентрацией облигатно- и факультативно-анаэробных условно-патогенных микроорганизмов (УПМ) и резким снижением или отсутствием молочнокислых бактерий в отделяемом влагалища [1].
Кроме рассмотренных нами терминов, в современной литературе встречаются и другие: аминокольпит, гарднереллез, влагалищные выделения с ключевыми клетками и др. [10, 26, 27], подразумевая по сути одно и то же патологическое состояние. Совершенно очевидно, что подобное положение далеко не лучшим образом сказывается на практической деятельности врачей, а следовательно, и на качестве оказания медицинской помощи. И сегодня в зарубежной специальной литературе нет единства в терминологии. Наиболее распространенным является термин бактериальный вагиноз.
По данным различных авторов, на долю БВ приходится от 1/3 до 1/2 всех вульвовагинальных инфекций нижнего отдела половых путей [3, 6, 9].
БВ можно рассматривать как синдром с полимикробной этиологией [2]. Е. Ф. Кира в 1995 г. была предложена оригинальная классификация [4], сочетающая в себе микробиологическую интерпретацию вагинального мазка, клиническую картину и конкретную нозологическую форму (табл.).
Таким образом, при БВ нарушается микробиоценоз влагалища и возрастает роль УПМ. При этом происходит замещение нормальной микрофлоры влагалища (лактобактерий) другими микроорганизмами, в частности бактероидами, фузобактериями, пептококками, вайлонеллами, а также гарднереллами и микоплазмами [2].
С проблемой БВ сталкиваются врачи различных специальностей, но чаще акушеры-гинекологи и дерматовенерологи. Так, в странах Европы и США выявление бактериального вагиноза в клинике венерических болезней составляет 33–64%, в общей гинекологической клинике — 15–23%, по данным службы планирования семьи — 23–29%, в акушерской клинике — 10–26% [1].
Отмечено, что примерно 20% женщин репродуктивного возраста страдают БВ. В 35–50% наблюдений заболевание ассоциируется с другими урогенитальными инфекциями: гонореей, хламидиозом, уреаплазмозом, трихомониазом и др. [14].
Предложено несколько гипотез развития БВ. Несомненно влияние гормональных факторов [11]. Функция яичников определяет синтез гликогена эпителиальными клетками влагалища и, следовательно, активность репродукции лактофлоры. Гормональный компонент в этиологии БВ предполагает тот факт, что заболевание редко наблюдается в ювенильном возрасте и периоде менопаузы, что предполагает гормональный компонент в его этиологии [27]. Однако использование гормональных контрацептивов не влияет на частоту БВ, хотя теоретически пероральные контрацептивы также, как и стероидная терапия, могут влиять на состав влагалищной микрофлоры [20]. Возможно, изменения в составе лактофлоры (уменьшение видового разнообразия и общего количества, потеря способности продуцировать перекись водорода и др.) могут быть связаны с нарушением синтеза специфических рецепторов клетками-эукариотами, что меняет силу адгезии бактерий. Однако этот вопрос малоизучен [1].
Другая гипотеза придает первостепенное значение микробному антагонизму, когда лактобактерии начинают снижать продукцию кислых метаболитов [12, 20]. Саморегуляция количества лактофлоры происходит с помощью бактерицидоподобных веществ — лактоцинов, которые вырабатывают сами лактобактерии и которые ограничивают в определенной степени их размножение. Кроме того, продукция перекиси водорода лактобактериями подавляет рост УПМ, не имеющих фермента каталазы. При БВ исчезают продуцирующие перекись водорода лактобактерии (или их количество резко снижается) [17]. Нельзя также не учитывать роль таких антимикробных факторов влагалищного отделяемого, как гликопротеин, лактоферрин, ионы некоторых металлов (цинк, марганец, железо), а также лизоцим, фибропектин, которые играют заметную роль в персистенции таких УПМ, как стафилококки, стрептококки, энтеробактерии [1, 5, 15, 25]. Установлено, что внутриматочная спираль (ВМС) нарушает противобактериальную защиту цервикального канала, при этом значительно возрастает риск возникновения БВ и других инфекций. По мнению многих отечественных и зарубежных авторов, БВ встречается у 50% женщин, использующих ВМС [4, 20]. Применение антибиотиков системного или местного действия часто предшествует развитию БВ [4, 11].
К настоящему времени накоплен ряд убедительных доказательств отсутствия полового пути передачи БВ [21]. Скептическая точка зрения на трансмиссионный характер БВ опровергается результатами исследований, в которых достоверно доказано отсутствие половой передачи БВ: частота БВ не увеличивается при увеличении числа половых партнеров (только 6,1% женщин связывали начало заболевания с новым половым партнером); БВ обнаружен у 6–13% лесбиянок, тогда как классические венерические заболевания в этой группе очень редки; БВ выявлен у 15% подростков, ведущих активную половую жизнь, и у 12% девственниц; лечение половых партнеров пациенток с БВ не влияет на частоту рецидива заболевания [8].
БВ сопровождается выраженными нарушениями в системе местного иммунитета, которые проявляются уменьшением концентрации IgA, IgG и увеличением концентрации IgM. Нарушения в системе общего иммунитета выражаются в умеренном напряжении гуморальных факторов (увеличение содержания IgA, IgM, трансферрина и реакции торможения миграции лейкоцитов) в отсутствие реакции клеточных факторов [1].
Поскольку у 71% женщин, страдающих БВ, выявляется дисбиоз желудочно-кишечного тракта, то можно предполагать единый дисбиотический процесс в организме с доминирующим проявлением либо в репродуктивной, либо в пищеварительной системе, что подтверждают многие авторы [4, 22].
Известно, что БВ является фактором риска, а иногда и одной из причин возникновения тяжелой патологии женских половых органов и осложнений беременности и родов. Исследования ряда авторов показали, что БВ может привести к развитию хориоамнионита, послеродового эндометрита, преждевременных родов и рождению детей с низкой массой тела, возникновению воспалительных процессов половых органов, гнойно-септических осложнений у матери и ребенка в послеродовом периоде и т. д., влияя на частоту акушерской и неонатальной патологии [2].
Но в ряде работ, выполненных в последние годы, достоверно показано, что у больных с БВ плоскоклеточные интраэпителиальные поражения встречались не чаще, чем у пациенток с нормальной влагалищной микрофлорой. Значительная разница количества нитрозаминов также не была выявлена у женщин с БВ и нормальной влагалищной флорой. В этих работах корреляции между БВ и ПИП выявлено не было [18, 27, 28].
Однако ряд исследований показывают, что БВ может увеличивать риск заражения и активации ВПЧ, что связано с тем, что влагалищная среда играет определенную роль в восприимчивости к ВПЧ. Папилломавирусной инфекции отводится ведущая роль в развитии ПИП. Но БВ не влияет на персистенцию ВПЧ, и эффекта БВ недостаточно для развития цервикальной интраэпителиальной неоплазии [28].
Ю. К. Скрипкин выделяет 3 фазы течения БВ: свежий, торпидный и хронический БВ с инкубационным периодом от 5 дней до 3 недель. В остром периоде возможна гиперемия слизистой шейки матки и влагалища.
Первый тест имеет низкую чувствительность (56,3%) и специфичность (48,9%) [25].
рН-метрия вагинального отделяемого обладает высокой чувствительностью (80–98%), но, к сожалению, этот тест малоспецифичен (50–70%) [25].
Так называемые ключевые клетки (Glue cells) — эпителиальные клетки влагалища, плотно покрытые грамвариабельными палочками, обнаруживаются при бактериоскопии влагалищного содержимого у 70–90% женщин с БВ. Однако наибольшей чувствительности (76,7%) и специфичности (92,4–98%) этот метод достигает при окраске по Граму.
обнаружение при увеличении с иммерсией менее 5 лактобацилл в поле зрения. Культуральное исследование на G. vaginalis для диагностики БВ не рекомендуется, поскольку не является специфичным.
Существуют непрямые методы диагностики БВ, имеющие большое научное значение, такие как газожидкостная хроматография, которая позволяет сравнить содержание в вагинальном отделяемом основных продуктов метаболизма лактобацилл и облигатно-анаэробных микроорганизмов — гарднерелл: молочной (Lactic acid) и янтарной (Succinic acid) кислот. В норме соотношение янтарной и молочной кислот менее 0,4, а при БВ — более 0,4. Для диагностики БВ используют определение ферментов полиаминопептидазы и сиалидазы, а также классическое микробиологическое исследование с использованием аэробной и анаэробной техники культивирования микроорганизмов и количественной оценкой микроорганизмов-ассоциантов в составе микроценоза. Эти методы необходимы для изучения этиологической структуры и патогенетических механизмов развития дисбиотических процессов в вагинальном биотопе, а также служат критерием для оценки клинического значения ускоренных методов диагностики БВ и эффективности этиотропной терапии [1].
Успешное лечение БВ, как и любого заболевания, зависит от правильной и своевременной постановки диагноза и проведения патогенетически обоснованной терапии. Цель лечения бактериального вагиноза — восстановить нормальную микрофлору влагалища, задержать рост микроорганизмов, не свойственных этому микроценозу. Терапия бактериального вагиноза остается нелегкой задачей ввиду частого рецидивирования или низкой эффективности ряда предложенных препаратов.
Результаты лечения БВ значительно улучшаются при использовании двухэтапного метода комплексной этиотропной и патогенетической терапии, разработанного в 1995 г. Е. Ф. Кирой:
1) ликвидация возбудителей БВ (облигатно-анаэробный компонент микрофлоры влагалища);
2) восстановление биоценоза влагалища.
Препаратами первого этапа для этиотропной терапии БВ являются медикаментозные препараты против анаэробной микрофлоры. Наиболее эффективно лечение метронидазолом, клиндамицином, орнидазолом, поливидон-йодом, хлоргексидином [7]. Клиническая и бактериологическая эффективность указанных препаратов достигает 85–94%. Одновременно с применением антибактериальной терапии проводится системная профилактика вагинального кандидоза [19].
Многочисленные работы последних лет свидетельствуют о том, что препаратами выбора в настоящее время считаются метронидазол и клиндамицин, которые эффективны против анаэробной микрофлоры [1, 5, 8].
Эффективным препаратом для лечения БВ является метронидазол (Метрогил ® , Трихопол ® ), который относится к группе антибактериальных препаратов, содержащих имидазольное кольцо. Проникая внутрь микробной клетки, метронидазол превращается в активную форму, связывается с ДНК и блокирует синтез нуклеиновых кислот. Он широко применяется в различных схемах, причем описана эффективность препарата как при разовых схемах в дозе 2 г, так и при 7-дневных курсах лечения по 500 мг внутрь 2 раза в день. Однако пероральное применение препарата нередко вызывает побочные реакции, такие как металлический вкус во рту, диспепсические расстройства, аллергические реакции, тем самым ограничивая его использование. В результате многочисленных исследований установлено, что влагалищный путь лечения бактериального вагиноза не уступает по эффективности пероральной терапии. Кроме того, влагалищный путь лечения является более предпочтительным из-за меньшей вероятности развития побочных реакций.
Возможен комбинированный метод лечения: одновременное назначение в течение 7–10 дней пероральной формы метронидазола (Метрогил ® или Трихопол ® 250 мг 2 раза в день) и вагинальной формы метронидазола (Метрогил ® гель вагинальный по 1 аппликатору 2 раза в день в течение 5 дней или Трихопол® в виде вагинальных таблеток по 500 мг 1 раз в день в течение 7–10 дней). Таблетки метронидазола для перорального применения можно использовать независимо от приема пищи. Вагинальную таблетку Трихопола ® , смоченную в кипяченой воде, вводят во влагалище. Комбинированный вариант применения вагинальных форм метронидазола в комплексе с пероральным применением препарата увеличивает эффективность лечения бактериального вагиноза, а также снижает риск возникновения побочных реакций, наступающих при пероральной монотерапии метронидазолом. При необходимости в схему лечения можно добавить противогрибковый препарат.
Среди местных форм лечения применение нашел клиндамицин — антибиотик группы линкозамидов. Известно, что он обладает выраженной антибактериальной активностью, подавляя синтез белка в микробной клетке, взаимодействуя с 50S-субъединицами рибосом. Клиндамицин применяют как перорально, так и местно внутривлагалищно в виде кремов и овулей. Среди неблагоприятных эффектов описаны аллергические реакции, рост дрожжеподобных грибов и т. д.
В настоящее время при лечении БВ возможно использование и других препаратов группы нитроимидазола (тинидазол, орнидазол).
Особого внимания заслуживает применение для лечения БВ Метрогил ® Плюс. Это комбинированный препарат для интравагинального применения, эффективность которого обусловлена наличием в его составе двух компонентов: метронидазола и клотримазола. После интравагинального введения метронидазол подвергается системной абсорбции (около 56%). Относительная биодоступность вагинального геля в 2 раза выше биодоступности одноразовой дозы (500 мг) влагалищных таблеток метронидазола. При применении клотримазола интравагинально абсорбируется не более 3–10% от введенной дозы. Высокие концентрации в вагинальном секрете и низкие концентрации в крови сохраняются в течение 48–72 часов. Препарат вводится интравагинально. Разовая доза составляет 5 г (один полный аппликатор) 2 раза в день (утром и вечером). Курс лечения — 5 дней. При необходимости курс лечения можно повторить через 2 недели.
На втором этапе лечения применяются препараты, направленные на восстановление влагалищного микроценоза. Это осуществляется путем местного применения эубиотиков — Лактобактерина, Ацилакта, Бифидумбактерина, стимулирующих рост собственной лактофлоры влагалища и способствующих снижению числа рецидивов заболевания за счет повышения защитных свойств влагалища. Эубиотики назначают по 1 свече на ночь в течение 10 дней после обязательного контрольного микробиологического подтверждения отсутствия грибов. Эубиотики являются эффективным средством восстановления нормального биоценоза влагалища.
В Омской государственной медицинской академии проведено исследование влияния нормализации микробиоценоза влагалища на возможность элиминации ВПЧ. Нами обследовано 98 женщин с папилломовирусной инфекцией (ПВИ). Всем женщинам проведено микробиологическое исследование, полимеразная цепная реакция для выявления ВПЧ, цитологическое исследование по Папаниколау и по показаниям (наличие ПИП) — гистологическое исследование биоптатов, полученных прицельно после кольпоскопии. При этом только у 29,6% (29 человек) женщин с нормоценозом состояние микроэкологии полностью соответствовало критериям нормы репродуктивного возраста: у остальных имелись отклонения, связанные либо с лейкоцитарной реакцией, либо с недостаточным количеством лактобацилл, либо с нарастанием титра факультативных условно-патогенных микроорганизмов. Интерес представляла группа женщин в количестве 24 (24,5%) человек, у которых имелось сочетание ВПЧ с БВ. Наличие БВ было подтверждено микробиологически, наличие ПВИ — методом ПЦР, цито- и гистологически.
Для лечения БВ у 24 женщин с ПВИ и БВ применялся Метрогил ® Плюс по стандартной 5-дневной схеме. После указанной терапии для восстановления нормальной микрофлоры всем женщинам был назначен эубиотик Ацилакт внутривлагалищно по 1 свече в течение 10 дней. Было отмечено полное излечение БВ на основании указанных выше критериев у 19 (79,2%) из 24 женщин, только у 2 (8,3%) пациенток эффект отсутствовал, у остальных 3 женщин имелся частичный эффект. Генитальный кандидоз развился лишь в одном случае у женщины с часто рецидивирующим кандидозом, по поводу чего было назначено соответствующее лечение антимикотическим препаратом (Микосист по 150 мг per os в течение 2 дней).
После проведенного лечения БВ через 1 месяц проведено обследование на ПВИ. При этом у 7 (29,2%) женщин с положительным эффектом лечения БВ ВПЧ не выявлялся методом ПЦР. У этих же пациенток цитологически изначально выявлялся незначительный койлоцитоз, а после лечения — исчезновение койлоцитоза отмечено у 3 (21%) женщин из 7. Вероятно, полученный факт свидетельствует о том, что лечение БВ создает благоприятные условия для элиминации ВПЧ, находящегося в эписомной (свободной) форме.
Таким образом, БВ является достаточно распространенным заболеванием экосистемы влагалища женщин репродуктивного возраста, требующим своевременной диагностики, комплексной и адекватной терапии. БВ нередко сочетается с ПВИ гениталий у женщин и другими инфекциями, передаваемыми половым путем (ИППП). Полученные различными исследователями результаты свидетельствуют о целесообразности обследования пациенток с ПВИ влагалища и шейки матки с целью выявления нарушений микробиоценоза влагалища, предпочтительно с применением микробиологического обследования [2]. При обнаружении тех или иных нарушений следует проводить соответствующее лечение, направленное на восстановление микробиоценоза, и только после этого проводить терапию ПВИ гениталий, что не только повышает ее эффективность, но и позволяет избежать возможных осложнений. Адекватное лечение БВ может уменьшать риск инфицирования ВПЧ. Необходимость дальнейшего изучения проблемы БВ ввиду своей актуальности не вызывает сомнений. Последовательное ее решение будет способствовать улучшению репродуктивного здоровья и качества жизни женщин.
По вопросам литературы обращайтесь в редакцию.
Е. Б. Рудакова, доктор медицинских наук, профессор
С. И. Мозговой, кандидат медицинских наук, доцент
О. В. Лазарева
ОмГМА, Омск
В поликлинику г. Махачкалы 20 декабря 2019 года обратилась женщина 29 лет с жалобами на выделения из половых путей с неприятным запахом.
Жалобы
Симптомы появились 2 недели назад. Выделения обильные, приходится часто менять прокладки. Также пациентка отмечает дискомфорт в промежности, умеренную болезненность при половом контакте.
Анамнез
Впервые аналогичное состояние появилось 3-4 года назад во время студенчества, вне замужества и половой жизни. Женщина связывала его с переохлаждением. К врачу не обращалась, лечение не проводила. Выделения и запах прошли самостоятельно.
В этот раз симптомы появились после перенесённого фарингита (воспаления глотки и миндалин) и лечения антибиотиками цефалоспоринового ряда. Пациентка связывает данное состояние с развившимся дисбактериозом кишечника.
У пациентки в анамнезе аппендэктомия (удаление аппендицита), носительство ВПЧ 18 типа, 2 года назад эпизод кандидоза. Одна беременность (протекала гладко, роды естественные, вес ребёнка 3300 г), выкидышей и абортов не было. Контрацепция — внутриматочная спираль.
Обследование
- Наружные половые органы развиты правильно, оволосение по женскому типу.
- В зеркалах слизистые влагалища розовые.
- Выделения из половых путей — пенистые, обильные с выраженным рыбным запахом.
- Шейка матки цилиндрической формы, зев щелевидный.
- Шейка матки гипертрофирована (увеличена), эктопия цилиндрического эпителия.
- Влагалище рожавшей, шейка матки по центру отклонена кзади, плотная.
- Матка anteflexio (изгиб впереди).
- Придатки: слева без особенностей, безболезненны; справа без особенностей, безболезненны.
- В сводах: без особенностей.
- Лимфатические узлы: без особенностей.
- Осмотр заднепроходного отверстия: без особенностей.
Фемофлор 16 ( расширенное молекулярно-биологическое исследование качественного и количественного состава микрофлоры мочеполовых путей у женщин )
- Atopobium vaginae — 20-15 %.
- Gardnerella vaginalis, Prevotella bivia, Porphyromonas spp. — 80-70 %.
- Eubacterium spp. — 5-8 %.
- Lactobacillus spp. — 0-4 %.
- Mycoplasma hominis, Ureaplasma (urealyticum + parvum) — нет.
- Candida spp. — нет.
- Mycoplasma genitalium — нет.
- Chlamydia trachomatis — нет.
- Trichomonas vaginalis — нет.
- Neisseria gonorrhoeae — нет
Цитология в пределах нормы, атипических клеток нет (NILM — негативный в отношении дисплазии или рака результат).
Диагноз
Лечение
Внутриматочная спираль удалена. Пациентке назначен клиндамицин по одной свече один раз в день на ночь глубоко во влагалище в течение 6 дней.
- Полный отказ от использования ежедневных прокладок.
- Частая смена и использование только хлопкового нижнего белья.
- Отказ от средств интимной гигиены с отдушками.
- На время лечения строгая контрацепция барьерными методами либо половой покой.
- Контрольный осмотр через месяц, если симптомы не исчезнут, то после последней свечи.
Уже после второй свечи пациентка почувствовала улучшение состояния. После полного курса отмечает значительный положительный эффект:
- объём выделений намного уменьшился;
- нет необходимости в применении ежедневных прокладок;
- половой контакт стал безболезненным.
Учитывая достигнутый положительный эффект дальнейшее пероральное лечение назначено не было. Пациентка отметила полное прекращение выделений и отсутствие запаха, что намного улучшило её самочувствие и качество жизни.
Заключение
Данный клинический случай подтверждает высокую эффективность монотерапии клиндамицином при бактериальном вагинозе. Стоит отметить, что исследование Фемофлор 16 наиболее удобное и информативное для диагностики состояния урогенитального тракта.
Нормальная микрофлора влагалища женщин репродуктивного возраста является одним из показателей здоровья, так как играет большую роль в поддержании микроэкологического статуса. Взаимодействие между представителями нормальной микрофлоры и клетками вагиналь
Нормальная микрофлора влагалища женщин репродуктивного возраста является одним из показателей здоровья, так как играет большую роль в поддержании микроэкологического статуса. Взаимодействие между представителями нормальной микрофлоры и клетками вагинального эпителия осуществляется на клеточном и молекулярном уровнях и постоянно контролируется со стороны ряда систем макроорганизма. Результатом этого взаимодействия являются создание и поддержание высокой колонизационной резистентности вагинального эпителия к внедрению патогенных и условно-патогенных микроорганизмов [1–6].
Бактериальный вагиноз выделен из категории неспецифических вагинитов в отдельную нозологическую форму. К нему относят патологические состояния во влагалище, сопровождающиеся нарушениями качественного и количественного состава нормальной микрофлоры и не связанные с бактериальными инфекциями, передаваемыми половым путем (ИППП), грибами или простейшими.
Согласно современным представлениям, бактериальный вагиноз — инфекционный невоспалительный синдром полимикробной этиологии, который связан с дисбиозом вагинального биотопа. Нарушение микроэкологии влагалища при бактериальном вагинозе характеризуется резким снижением количества или отсутствием лактобактерий, продуцирующих перекись водорода и увеличением количества Gardnerella vaginalis, грамотрицательных анаэробных бактерий (Bacteroides spp., Mobiluncus spp., Fusobacterium spp., Peptostreptoicoccus spp., M. hominis, U. urealyticum).
Гарднереллы, как и лактобациллы, обладают выраженной способностью к адгезии на поверхности вагинальных эпителиоцитов. Gardnerella vaginalis могут продуцировать токсические биопродукты, к которым относятся муколитические ферменты и гемолизин, являющийся лейкотоксическим фактором. Гемолизин, воздействуя на эритроциты, вызывает образование многочисленных пор в эритроцитарной мембране, а также оказывает влияние на лейкоциты, вызывая их структурные и функциональные нарушения. Этим и объясняется отсутствие существенной лейкоцитарной инфильтрации, т. е. активности лейкоцитов в присутствии Gardnerella vaginalis.
Определенную роль в патогенезе бактериального вагиноза играют представители семейства Mycoplasmataceae — Mycoplasma hominis и Ureaplasma urealyticum. 70% выделенных штаммов Ureaplasma urealyticum относятся к биовару Parvo, 23,3% — к биовару Т960. Большинство пациенток, у которых была выделена Ureaplasma urealyticum, относящаяся к биовару Parvo, имели в прошлом раннее начало половой жизни, частую смену половых партнеров, наличие одновременно нескольких половых партнеров, большое количество беременностей и абортов, а также сопутствующие гинекологические заболевания и ИППП.
При обследовании половых партнеров пациенток с бактериальным вагинозом морфотипы ассоциированных с бактериальным вагинозом микроорганизмов выявлялись у 25% мужчин, при этом клинические проявления (баланопостит) наблюдались только у 3,1% [2].
В результате субмикроскопического исследования вагинального экссудата пациенток с бактериальным вагинозом определены структурно-функциональные особенности микробных клеток, участвующих во взаимодействии друг с другом, при этом клетки организма-хозяина представлены преимущественно плоским эпителием. Установлена грамвариабельность Gardnerella vaginalis вне зависимости от характера микробных ассоциаций. Анализ электронограмм продемонстрировал, что структурная организация Gardnerella vaginalis, адгезированных на поверхности эпителиальных клеток, не зависела от сочетания бактериального вагиноза с другими инфекционными агентами.
При сочетании бактериального вагиноза с Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum наблюдали значительное количество микроорганизмов в межклеточном пространстве и бактерий, морфологически идентичных микоплазмам [2].
Пациентки предъявляют жалобы на обильные выделения из половых путей белого или серого цвета, часто с неприятным запахом, особенно после полового акта или во время менструации. При длительно текущем процессе выделения приобретают желтовато-зеленую окраску, становятся более густыми, нередко напоминают творожистую массу, обладают свойством пениться; слегка тягучие и липкие, они равномерно распределяются по стенкам влагалища. Количество белей варьирует от умеренных до весьма обильных, составляя в среднем 20 мл в сутки. Жалобы на зуд и дизурические расстройства встречаются редко: они могут совсем отсутствовать или появляться периодически. Эти симптомы обнаруживаются у 16–23% пациенток с нарушениями микрофлоры влагалища. Характерным признаком бактериального вагиноза является отсутствие воспалительного процесса стенок влагалища. Нередко женщины с бактериальным вагинозом жалуются на обильное менструальное кровотечение, боли в низу живота. В то же время у части пациенток какие-либо субъективные ощущения отсутствуют.
Диагностика бактериального вагиноза основана на данных анамнеза, оценке субъективных и объективных симптомов заболевания, результатах лабораторных тестов — микроскопического исследования материала, аминного теста и рН вагинального экссудата [3].
При сборе анамнеза выясняют:
- проведение в прошлом терапии антибиотиками, цитостатиками, кортикостероидами, противовирусными и противогрибковыми препаратами;
- наличие гинекологических, эндокринных заболеваний, заболеваний желудочно-кишечного тракта и др.;
- соблюдение правил личной и половой гигиены;
- данные о половых партнерах, практике сексуальных контактов и состоянии органов мочеполовой системы половых партнеров;
- применение и методы контрацепции.
Диагноз бактериального вагиноза устанавливается на основании наличия трех критериев из нижеперечисленных:
- гомогенные выделения беловато-серого цвета, равномерно адгезированные на слизистой оболочке вульвы и влагалища, имеющие неприятный запах;
- рН влагалищного экссудата > 4,5;
- положительный результат аминного теста (появление рыбного запаха при смешивании на предметном стекле влагалищного отделяемого с 10%-ным раствором КОН в равных пропорциях);
- изменения микроценоза влагалища, выявляемые при микроскопическом исследовании вагинального экссудата.
Обследование пациентки следует проводить не ранее, чем через 72 ч после последнего полового контакта (без использования презерватива); оно не проводится также во время менструации. В течение 3 нед до обследования женщина не должна получать терапию системными и местнодействующими антибактериальными препаратами [3].
При микроскопическом исследовании нативного и окрашенного по Граму вагинального мазка определяются следующие признаки:
Оценка общей микробной обсемененности вагинального отделяемого проводится по 4-балльной системе — по числу микробных клеток, обнаруживаемых в одном поле зрения при иммерсионной микроскопии:
1 балл (+) — до 10 микробных клеток в поле зрения, незначительное их количество (скудный рост);
2 балла (++) — от 11 до 100 микробных клеток в поле зрения, умеренное их количество;
3 балла (+++) — от 100 до 1000 микробных клеток в поле зрения, большое их количество;
4 балла (++++) — более 1000 микробных клеток в поле зрения, массивное их количество.
Так как Gardnerella vaginalis может быть обнаружена у здоровых женщин, культуральное исследование и ПЦР-диагностику для идентификации Gardnerella vaginalis не проводят. Культуральное исследование проводят при наличии показаний для определения видового и количественного состава вагинального микроценоза и исключения возбудителей ИППП.
При культуральном исследовании могут быть обнаружены изменения, характерные для бактериального вагиноза: общая микробная обсемененность превышает 10 9 КОЕ/мл; при использовании только аэробных условий культивирования рост микроорганизмов отсутствует или наблюдается рост сопутствующих условно-патогенных микроорганизмов (чаще в небольшом титре); полимикробный характер микрофлоры с абсолютным преобладанием облигатно-анаэробных видов и Gardnerella vaginalis; отсутствие роста лактобацилл или резкое снижение их титра (< 10 4 КОЕ/мл).
На основании проведенных исследований в настоящее время рекомендуется в план ведения пациенток включать:
- анализ субъективных и объективных проявлений заболевания, данных акушерско-гинекологического и полового анамнеза с акцентом на перенесенные или сопутствующие заболевания урогенитальной системы;
- комплексную оценку микробиоценоза влагалища, включающую идентификацию возбудителей ИППП;
- идентификацию Mycoplasma hominis, Ureaplasma urealyticum культуральным методом с количественной оценкой возбудителей;
- определение биопринадлежности Ureaplasma urealyticum для решения вопроса о выборе тактики дальнейшего ведения пациентки;
- целесообразно привлекать специалистов смежных дисциплин (гинекологов, урологов) при наличии сопутствующих заболеваний урогенитальной системы;
- клинико-микробиологическое обследование половых партнеров (профилактическое лечение половых партнеров пациенток с бактериальным вагинозом в настоящее время признано нецелесообразным).
Целью лечения является уменьшение выраженности клинических симптомов, нормализация лабораторных показателей, предотвращение развития возможных осложнений в период беременности, а также в послеродовом периоде и при выполнении инвазивных гинекологических процедур.
Результаты лабораторных исследований в норме следующие.
Лечение
Основное направление терапии — применение местных или системных антибактериальных препаратов с антианаэробным эффектом.
Показано применение клиндамицина. Препарат является 7-дезоксипроизводным линкомицина, ингибирует синтез белков в микроорганизмах, оказывает бактериостатическое или бактерицидное действие в зависимости от концентрации в макроорганизме и чувствительности микроорганизма. Препарат эффективен в отношении грамположительных микроорганизмов (стафилококков, стрептококков, пневмококков, палочки дифтерии), гарднерелл, микоплазм. Устойчивость микроорганизмов к клиндамицину вырабатывается медленно. При приеме внутрь клиндамицин всасывается лучше, чем линкомицин. После внутримышечного введения максимум его концентрации в крови отмечается через 2–2,5 ч. Препарат хорошо проникает в жидкости и ткани организма, выводится с мочой и желчью. При нарушении функции почек и печени выведение клиндамицина замедляется. При бактериальном вагинозе можно назначать одну из лекарственных форм клиндамицина: крем 2%-ный 5 г в аппликаторе (разовая доза) интравагинально 1 раз в день (на ночь) в течение 6 дней; овули 100 мг интравагинально на ночь в течение 3 дней; капсулы 300 мг внутрь 2 раза/сут в течение 7 дней.
Клиндамицин разрешенн к применению у беременных в виде 2%-го крема 5 г (разовая доза) интравагинально 2 раза/сут в течение 5 дней.
Также при бактериальном вагинозе можно назначать метронидазол. Он обладает широким спектром действия в отношении простейших, подавляет развитие Trichomonas vaginalis, Entamoeba histolytica и лямблий. В отношении анаэробных бактерий препарат высокоэффективен. Метронидазол хорошо всасывается при приеме внутрь, проникает в органы и ткани, проходит через плаценту и гематоэнцефалический барьер, накапливается в печени. Период полувыведения препарата составляет 8–10 ч, полностью выводится из организма через 1–2 сут после введения. Метронидазол в основном выводится с мочой в неизмененном виде и в виде метаболитов, частично — с калом. При применении метронидазола могут отмечаться потеря аппетита, сухость и неприятный вкус во рту, тошнота, рвота, диарея, головная боль, крапивница, зуд. Эти явления проходят после окончания лечения или отмены препарата. Возможна лейкопения. Препарат противопоказан при беременности и кормлении грудью, нарушениях кроветворения, остром течении заболеваний центральной нервной системы. Во избежание развития тяжелых побочных реакций следует предупреждать пациентов о недопустимости приема алкоголя и содержащих его продуктов как в ходе терапии метронидазолом, так и в течение 24 ч после ее окончания. При бактериальном вагинозе можно применять одну из следующих схем лечения с использованием метронидазола:
- гель 0,75% 5 г (разовая доза) интравагинально (на ночь) в течение 5 дней;
- таблетки 500 мг внутрь 2 раза/сут в течение 7 дней;
- таблетки 2 г внутрь однократно.
Также используют и другие производные метронидазола:
- тинидазол (Тинидазол-Акри, Веро-тинидазол), таблетки 2 г внутрь однократно;
- орнидазол (Орнидазол-Веро), таблетки 500 мг внутрь 2 раза/сут в течение 5 дней.
Ранее было проведено сравнительное изучение эффективности местнодействующих пробиотиков. Поскольку не было выявлено достоверных отличий в результатах лечения у пациенток, получавших и не получавших эти средства, в настоящее время их не рекомендуют при лечении бактериального вагиноза [3].
При сочетании бактериального вагиноза с ИППП, одновременно применяют антибактериальные препараты в соответствии с нозологической формой заболевания [2]. При неосложненной гонорейной инфекции назначают цефтриаксон однократно внутримышечно в дозе 250 мг (препарат является цефалоспориновым антибиотиком III поколения; после внутримышечного введения пик концентрации в крови отмечается через 1,5 ч; из организма выводится медленно). При обнаружении хламидий и/или микоплазм показано применение антибиотиков — макролидов, тетрациклинов.
Высокий терапевтический эффект, хорошая переносимость способствовали значительному распространению применения макролидов. Их антимикробный эффект обусловлен нарушением синтеза белка в рибосомах микробной клетки. Как правило, макролиды оказывают бактериостатическое действие, но в высоких концентрациях способны вызывать и бактерицидный эффект. Кроме антибактериального действия, макролиды обладают умеренной иммуномодулирующей и противовоспалительной активностью. Представителем III поколения макролидов является джозамицин (Вильпрафен). Этот антибиотик быстро абсорбируется из желудочно-кишечного тракта (ЖКТ), хорошо проникает через биологические мембраны и накапливается в тканях. Максимальная концентрация достигается через 1–2 ч после приема. Через 45 мин после приема дозы 1 г средняя концентрация джозамицина в плазме составляет 2,41 мг/л; связывание с белками плазмы не превышает 15%. Прием препарата с интервалом в 12 ч обеспечивает сохранение эффективной концентрации джозамицина в тканях в течение суток. Равновесное состояние достигается через 2–4 дня регулярного приема. Концентрация джозамицина в полиморфонуклеарных лейкоцитах человека, моноцитах и альвеолярных макрофагах примерно в 20 раз выше, чем в других клетках организма. Препарат биотрансформируется в печени до менее активных метаболитов. Джозамицин выводится главным образом с желчью, выведение же с мочой составляет менее 20%. Препарат назначается по 500 мг 2 раза в день в течение 10 дней.
Из группы тетрациклинов при ИППП наиболее эффективен доксициклин; в последние годы широко применяется Юнидокс Солютаб. Препарат отличается от Доксициклина гидрохлорида нейтральной реакцией, оказывает меньшее раздражающее действие на слизистую оболочку пищеварительного тракта и обладает улучшенными противомикробными и фармакокинетическими свойствами. Юнидокс Солютаб блокирует рибосомальную полимеразу и тормозит синтез белка в микроорганизмах.
Таблетки Юнидокс Солютаб обладают контролируемой растворимостью. Их можно не только принимать внутрь целиком или по частям, но и быстро приготовить из них сироп, суспензию (растворив таблетку в 20 мл воды) или раствор (растворив таблетку в 100 мл воды), которые обладают приятным вкусом. Таблетки растворяются в воде в течение 5–10 с, в биологических жидкостях — в течение 1 мин, превращаясь в равномерную суспензию.
Юнидокс Солютаб всасывается полностью. Биодоступность препарата составляет 95%. Через 2 ч после приема (200 мг в первый день и 100 мг в последующие дни) уровень в сыворотке составляет от 1,5 до 3 мг/мл. Препарат на 80–90% связывается с белками плазмы, хорошо проникает в ткани, накапливается в ретикулоэндотелиальной системе. Период полувыведения составляет 16–18 ч, после приема повторных доз — 22–23 ч.
Ранее были отмечены преимущества, заключающиеся в отсутствии побочных эффектов по типу эзофагитов, встречающихся при применении обычных форм Доксициклина гидрохлорида, способности накапливаться в высоких концентрациях в репродуктивных органах и активно воздействовать на инфекционный агент.
Юнидокс Солютаб назначают в дозе 200 мг в течение 10 дней.
Лабораторный контроль эффективности терапии следует проводить непосредственно по окончании этиотропного лечения: при микроскопии вагинальных мазков, окрашенных по Граму, необходимо констатировать степень эрадикации микроорганизмов, ассоциированных с бактериальным вагинозом; при посеве вагинального отделяемого — выявлять случаи колонизации факультативно анаэробными условно-патогенными микроорганизмами.
При сочетании бактериального вагиноза с урогенитальным хламидиозом и/или микоплазмозом лабораторный контроль необходимо повторить через 3 нед по окончании терапии.
По вопросам литературы обращайтесь в редакцию.
И. В. Хамаганова, доктор медицинских наук, профессор
РГМУ, Москва
Монотерапия клиндамицином – оптимальное решение проблемы бактериального вагиноза, направленное на основную причину заболевания – специфические механизмы, приводящие к образованию биопленки и обеспечивающие резистентность к классическим антибиотикам.
Одной из самых частых жалоб в практике врача-гинеколога были и остаются патологические выделения из влагалища. Симптом, нередко кажущийся самим пациенткам незначительным, требует тщательной диагностики, так как обычно связан с инфекционной патологией половых путей и высоким риском грозных осложнений.
В 61-87% случаев выделения являются симптомом бактериального вагиноза – инфекционного невоспалительного синдрома, характеризующегося нарушением влагалищного микробиоценоза 1 . По разным данным среди всех вульвовагинальных инфекций доля бактериального вагиноза составляет от 12 до 80% 2 . Повышенный интерес к этому заболеванию объясняется не столько тяжестью клинических проявлений, сколько его неразрывной связью с воспалительными заболеваниями женской мочеполовой системы и осложнениями беременности и родов.
Несмотря на частоту заболевания, непрекращающиеся исследования и обилие фармпрепаратов, призванных бороться с патогенной микрофлорой, частота рецидивов бактериального вагиноза очень высока. Через 3 месяца после лечения она составляет 15-30%, а через 6–8 месяцев достигает 75–80% 3 . Тактика ведения рецидивирующего бактериального вагиноза остается во многом неопределенной и остается на личное усмотрение специалиста.
Среди причин высокой частоты рецидивов можно отметить, во-первых, специфические патогенетические механизмы развития заболевания, обеспечивающие устойчивость бактериальных агентов к таким классическим антибактериальными средствам, как метронидазол 4 , а во-вторых – низкую приверженность к лечению со стороны пациенток. Малозначительность симптоматики редко заставляет женщин завершать длительный курс терапии, особенно если он требует докупать новые упаковки препарата. Даже минимальное улучшение нередко расценивается ими как достаточный успех. В то же время незаконченная терапия повышает риск формирования резистентности к препаратам, вероятность скорого рецидива и развития осложнений 5 . Стоит также отметить, что применение комбинированных средств, также в изобилии присутствующих на рынке, приводит к суммированию вероятности побочных явлений, характерных для каждого из ее компонентов 6 , что не увеличивает комплаентность пациенток.
Таким образом, сегодня необычайно высока необходимость в препаратах, учитывающих патогенез бактериального вагиноза и направленных против бактерий, ответственных за формирование устойчивости и определяющих тенденцию к рецидивированию. Большим плюсом для лекарственного средства будет также его эффективность при кратком курсе применения, который повысит приверженность к терапии. На данный момент этим критериям соответствует только Далацин® — оригинальный клиндамицин – от компании Pfizer.
Влагалищный микробиоценоз в норме и в патологии
Микрофлора влагалища очень чувствительна к экзогенным и эндогенным факторам. Частые спринцевания, использование тампонов, смены половых партнеров, нейроэндокринные заболевания, сахарный диабет, гипотиреоз, нарушения менструального цикла, применение антибиотиков и гормональных средств, хирургические вмешательства, а также беременность и менопауза могут дисбалансировать хрупкую экосистему 8 .
Если доля лактобацилл снижается, их место в экосистеме занимают облигатно и факультативно анаэробные условно-патогенные микробы: Gardnerella vaginalis, Atopobium vaginae, Bacteroides spp., Peptostreptococcus spp., Mobiluncus spp., Mycoplasma hominis и многие другие.
Резкое снижение местной защиты при бактериальном вагинозе повышает риск заражения ВИЧ 9 , Neisseria gonorrhoeae, Clamydia trachomatis, Human herpes virus. Повышается восприимчивость и к вирусу папилломы человека, поэтому нарушения микрофлоры влагалища считаются кофактором развития неоплазии шейки матки 10 . Стоит отметить и тот факт, что в случае преждевременных родов, разрыве плодных оболочек 11 и инфекционных осложнений беременности 12 в амниотической жидкости чаще выявляются микробные агенты, связанные с бактериальным вагинозом.
Роль Atopobium vaginae и Gardnerella vaginalis в патогенезе рецидивирующего бактериального вагиноза
Появление методов амплификации нуклеиновых кислот в содержимом влагалища женщин с бактериальным вагинозом позволило выявить Atopobium vaginae, бактерию семейства Corinobacteriaceae spp., сегодня считающуюся высокоспецифичным маркером этого заболевания и имеющую ключевую роль в его патогенезе. Этот строго анаэробный микроорганизм часто существует в комбинации с Gardnerella vaginalis и существенно ослабляет иммунный ответ на локальном уровне.
Особенностью развития бактериального вагиноза и фактором, обеспечивающим его частое рецидивирование, является образование бактериальных ассоциаций, формирующих биопленки. Биопленки обнаруживаются у 90% женщин с бактериальным вагинозом 13 . В подавляющем большинстве случаев основную массу этих бактериальных ассоциаций составляют Gardnerella vaginalis и Atopobium vaginae 14 . Исследования показали, что Gardnerella vaginalis обладает наибольшей адгезивной способностью и цитотоксичностью по отношению к влагалищному эпителию, а формируемые ею биопленки отличаются наибольшей массивностью 15 . Именно этот факт может объяснять крайне низкую эффективность метронидазола для лечения бактериального вагиноза 16 .
- Повышает степень адгезии бактерий к поверхности эпителия и позволяет им наращивать ее массу
- Препятствует проникновению лекарственных препаратов
- Уменьшает скорость деления бактерий в своем составе, оставляя меньше мишеней для действия антибиотиков
- Способствует адаптивным реакциям и генетической изменчивости у персистирующих в ней бактерий. Кворумная сигнализация и обмен генетической информации позволяет быстро выработать резистентность к антибактериальному лечению 17 .
- Снижает воспалительную реакцию организма
- Помогает сохранить жизнеспособность микроорганизмов при некомфортных концентрациях перекиси водорода и молочной кислоты.
Таким образом, бактерии, образующие биопленку, являются основной мишенью патогенетически-обусловленной терапии. Препараты, высоко активные в отношении Atopobium vaginae и Gardnerella vaginalis, решают принципиально важную проблему элиминации патологических очагов на слизистой, которые становятся причиной возврата заболевания. И таким образом позволяют женщине, наконец, перестать обращаться к врачу с одними и теми же жалобами.
Фокусная терапия рецидивирующих форм бактериального вагиноза
Для пациенток с рецидивирующей формой бактериального вагиноза оптимальным решением является Далацин® (оригинальный клиндамицин), один из немногих препаратов, эффективных одновременно против Atopobium vaginae и Gardnerella vaginalis.
Клиндамицин, полусинтетический антибиотик группы линкозамидов, стал мировым стандартом лечения бактериального вагиноза и включен в отечественные и международные рекомендации 18, 19 . Далацин® для интравагинального введения (суппозитории или крем) предназначен для терапии только одного заболевания – бактериального вагиноза, и имеет уникальный по краткости курс применения – всего три дня. Клинически доказано, что трехдневный курс не уступает по эффективности 7-дневному применению метронидазола 20 или клиндамицина 21 . Это является существенным плюсом для пациенток, показывавших низкую приверженность к длительным курсам терапии, и снижает риск формирования резистентных форм и повторных случаев заболевания.
Эффективность фокусной терапии рецидивирующих форм бактериального вагиноза, ассоциированных с Atopobium vaginae, была не раз доказана в клинических исследованиях.
Многоцентровое исследование 2015 года 22 , в котором приняли участие 496 женщин с бактериальным вагинозом, показало, что эта бактерия действительно играет существенную роль в развитии повторных случаев заболевания. Если при первичном эпизоде колонизация влагалища Atopobium vaginae и Gardnerella Vaginalis составляла 12,3%, то при рецидивах – 70,3%. Сравнительный анализ эффективности лечения рецидивов бактериального вагиноза показал, что частота повторных эпизодов заболевания после применения метронидазола составила 98 (60,4%) случаев, что объясняется устойчивостью к нему А. vaginae, тогда как при использовании Далацин® – 51 (31,5%) 22 . Другая работа также свидетельствует о значительно большей эффективности клиндамицина (83,3%) по сравнению с метронидазолом (33,3%) в лечении бактериального вагиноза, ассоциированного с Atopobium vaginae 23 .
Симптомы бактериального вагиноза рецидивируют у каждой второй женщины в течение 12 месяцев после лечения 24 . В наибольшей степени возврату заболевания способствует ассоциация Atopobium vaginae с Gardnerella vaginalis, приводящая к образованию биопленки и формированию резистентности бактерий к различным антибактериальным препаратам. Далацин®, показывающий высокую активность против этих бактерий, показывает высокую терапевтическую эффективности и значимо снижает число рецидивов. Фокусная монотерапия препаратом Далацин® имеет более благоприятный профиль безопасности по сравнению с комбинированной терапией и имеет хороший потенциал в повышении приверженности к терапии, что также уменьшает количество повторных обращений к специалистам.
Инструкция по медицинскому применению лекарственного препарата Далацин®
Регистрационные удостоверения: крем – П N011553/01, суппозитории – П N011553/02.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Бактериальный вагиноз: причины появления, симптомы, диагностика и способы лечения.
Определение
Бактериальный вагиноз — это инфекционное полимикробное заболевание, связанное с изменением микрофлоры влагалища, при котором происходит значимое уменьшение количества или полное исчезновение палочек Додерлейна (лактобактерий) и их замещение факультативными анаэробными микроорганизмами и/или возбудителем гарднереллеза. Увеличение уровня лейкоцитов в вагинальном отделяемом и признаки воспаления стенок влагалища могут отсутствовать.
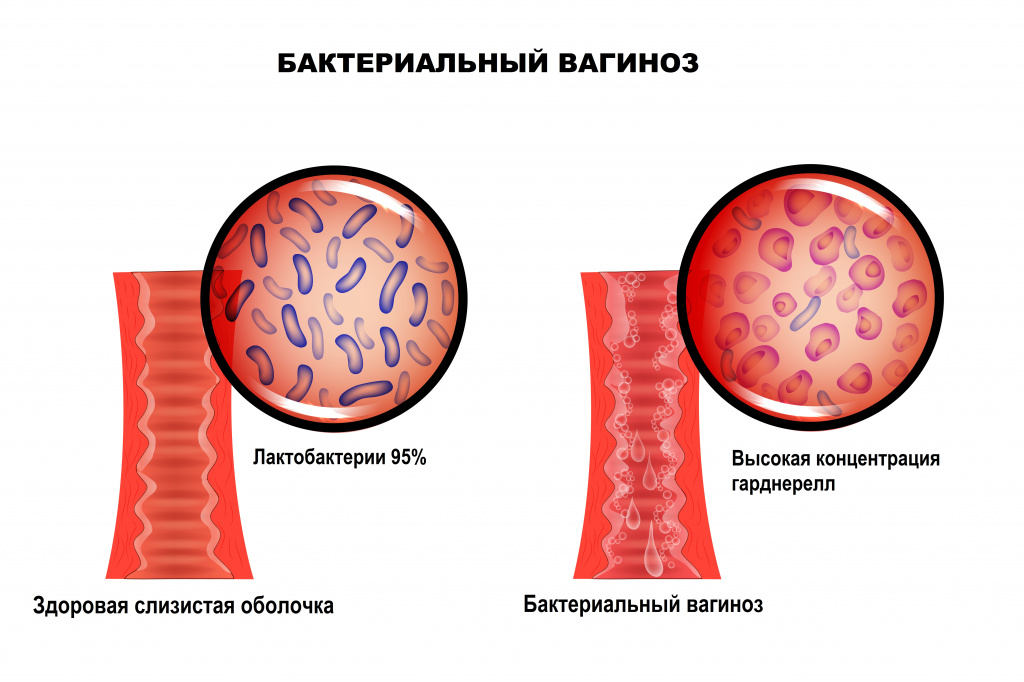
Отличительной особенностью заболевания является отсутствие какого-либо одного конкретного возбудителя. Микрофлора, приходящая на смену лактобактериям, может быть различной и чаще всего представлена условно-патогенными бактериями. Кислотность среды влагалища смещается в сторону ощелачивания. При нарушении экосистемы влагалища формируется хорошо структурированная полимикробная пленка (биопленка - форма микробных сообществ), покрывающая вагинальный эпителий и состоящая из анаэробных бактерий, что приводит к рецидивирующему течению бактериального вагиноза. В биопленках бактерии защищены от компонентов врожденного и приобретенного иммунитета.
В норме ведущее место (95%) в вагинальном микробиоценозе занимают палочки Додерлейна, продуцирующие перекись водорода и молочную кислоту.
Они поддерживают постоянство богатой кислородом кислой рН-среды и играют роль местных факторов защиты. В случае нарушения защитных механизмов патогенные или условно-патогенные микроорганизмы транзиторной или факультативной флоры прикрепляются к клеткам влагалищного эпителия с последующим размножением и повреждением тканей.
Бактериальный вагиноз является наиболее частой причиной патологических вагинальных выделений у женщин репродуктивного возраста, однако иногда он может наблюдаться и у девочек до менархе, и у женщин в период менопаузы.
Причины появления бактериального вагиноза
Предрасполагающие факторы, ведущие к развитию бактериального вагиноза:
- использование антибактериальных препаратов;
- длительное применение внутриматочных контрацептивов;
- ношение синтетического нижнего белья, злоупотребление прокладками на каждый день и тампонами, которые препятствуют проникновению кислорода;
- длительный прием антибиотиков;
- хронические заболевания кишечника и другие состояния, вызывающие дисбактериоз;
- использование пероральных контрацептивов;
- перенесенные ранее воспалительные заболевания урогенитального тракта;
- нарушение гормонального статуса, сопровождающееся нарушением менструального цикла, преимущественно по типу олигоменореи или аменореи;
- атрофия слизистой оболочки влагалища;
- снижение иммунитета;
- воздействие малых доз ионизирующего излучения;
- стрессовые воздействия на организм.
Классификация бактериального вагиноза на основании микроскопического исследования:
- Компенсированный бактериальный вагиноз — количество лактобактерий снижено, что является фактором риска заселения влагалища патогенными микроорганизмами.
- Субкомпенсированный — низкий уровень лактобактерий и растущее число условно-патогенных микроорганизмов.
- Декомпенсированный — в мазке выявляются условно-патогенные микроорганизмы, лактобактерии отсутствуют, выражены клинические симптомы бактериального вагиноза.
У большинства женщин бактериальный вагиноз протекает бессимптомно и может быть обнаружен случайно во время рутинного осмотра и взятия мазка.
Интенсивный рост факультативной флоры, образование патологических биопленок сопровождается появлением влагалищных выделений с характерным неприятным запахом.
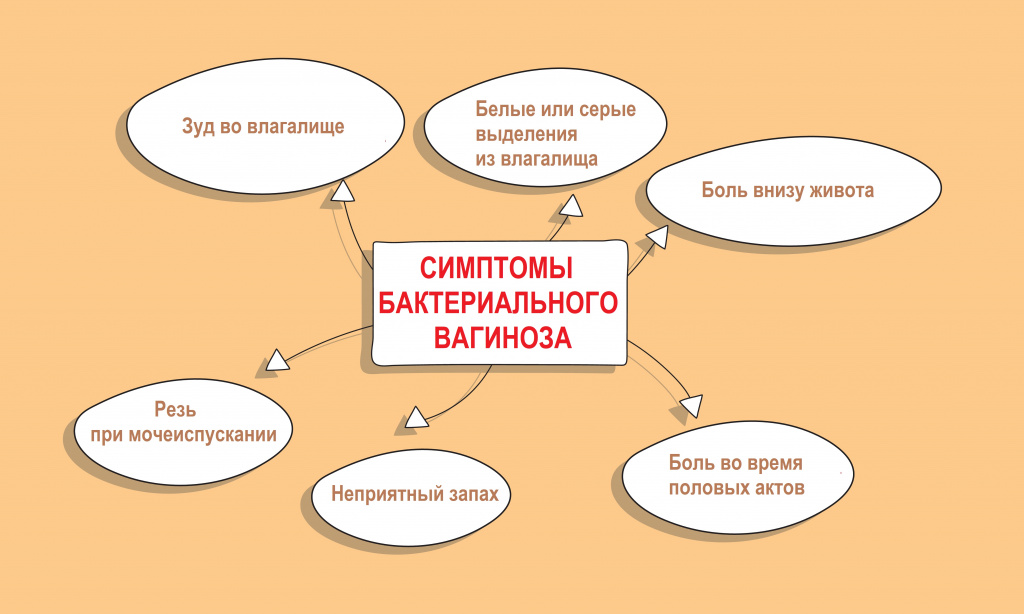
Хронический бактериальный вагиноз — это непрерывное течение заболевания более 2-х месяцев, несмотря на проводимое лечение. Как правило, он сочетается с нарушением гормонального фона и атрофией слизистой оболочки влагалища.
Диагностика бактериального вагиноза
При постановке диагноза у врача есть четыре критерия, которыми он пользуется. Наличие у пациентки трех из них говорит в пользу бактериального вагиноза.
Микроскопическое (бактериоскопическое) исследование мазка, окрашенного по Граму. Материалом для оценки состояния флоры влагалища служат гинекологические мазки (отделяемое наружных половых органов, уретры, влагалища, шейки матки, полости матки).
Читайте также:

