Белая клетка крови играющая важную роль в защите организма от инфекций
Обновлено: 23.04.2024
Фагоцитирующие клетки. Фагоциты. Полиморфно-ядерные лейкоциты ( гранулоциты ). Нейтрофилы. Феномен краевого стояния. Нейтрофилия. Эозинофилия.
Фагоциты выполняют не только защитные (поглощают и разрушают чужеродные агенты), но и дренажные функции (удаляют погибшие и деградировавшие структуры организма). Фагоциты представлены клетками миелопоэтического ряда (полиморфно-ядерные лейкоциты) и макрофагально-моноцитарной системы (моноциты, тканевые макрофаги). Основные свойства фагоцитирующих клеток представлены в табл. 10-5.
Полиморфно-ядерные лейкоциты имеют дольчатое ядро и множество мелких цитоплаз-матических гранул (поэтому их также называют гранулоциты). По окрашиванию гранул выделяют три типа клеток: нейтрофилы, эозинофилы и базофилы.
Таблица 10-5. Характеристики фагоцитирующих клеток
| Клетки | Источник | Формы участия в защитных реакциях |
| Нейтрофилы | Костный мозг; после дифференцировки выходят в кровоток | Адгезия к эндотелию и выход за пределы кровотока; хемотаксис; поглощение; дегрануляция; секреция О 2 -зависимых и О 2 -независимых микробицидных факторов |
| Эозинофилы | Тот же | Секреция О2-зависимых и 02-независимых микробицидных факторов, направленных против паразитов (простейшие и гельминты) |
| Моноциты | Костный мозг; после дифференцировки промоноциты выходят в кровоток | Адгезия к эндотелию и выход за пределы кровотока; хемотаксис; поглощение; дегрануляция; секреция О2-зависимых и О2-независимых микробицидных факторов (включая цитокины) |
| Макрофаги (клетки фон Купффера, альвеолярные макрофаги, гистиоциты, перитонеальные макрофаги, клетки мик-роглии, макрофаги селезёнки и др.) | Моноциты периферической крови | Адгезия к эндотелию и выход за пределы кровотока; хемотаксис; поглощение; дегрануля-ция; секреция О2-зависимых и О2-независимых микробицидных факторов; синтез компонентов комплемента, активатора ппазминогена и других протеаз; секреция медиаторов и компонентов клеточных мембран, включая продукты I и II классов МНС; участие в иммунных реакциях |
Нейтрофилы. Феномен краевого стояния. Нейтрофилия. Эозинофилия
Нейтрофилы — основные эффекторные клетки острого воспаления; у взрослых лиц они составляют самую многочисленную популяцию лейкоцитов. Основная часть нейтрофилов циркулирует в крови в течение 6-7 ч. Затем они скапливаются в капиллярах, где формируют краевой пул, прикрепляясь к эндотелию (по периметру кровотока); в таком состоянии нейтрофилы находятся в готовности немедленно покинуть кровеносное русло (феномен краевого стояния). Нейтрофилия (увеличение их количества в периферической крови) часто указывает на наличие воспалительной реакции.
Потенциал эозинофилов направлен не столько на фагоцитирование бактерий, сколько на нейтрализацию паразитов, особенно гельминтов (например, нематод). Поэтому, эозинофилия — признак, указывающий на возможную глистную инвазию. Кроме того, эозинофилы участвуют в разрушении гистамина, выделяя гистаминазу. Именно поэтому эозинофилию также наблюдают при аллергических заболеваниях. Определённая роль в подобной специализации эозинофилов принадлежит специфическим гранулам, содержащим пероксидазы и катионные белки (например, основный белок, катионные белки эозинофилов), активные именно в отношении паразитов. В активации эозинофилов важную роль играют IgE, образующиеся в ответ на сенсибилизацию организма аллергенами (в том числе микробными).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.

Примечание. На данной странице кратко рассмотрены функции и характеристики основных иммунокомпетентных клеток: Т- и В-лимфоцитов и дендритных клеток ( DCs ), а также понятия адаптивного иммунитета и врожденного иммунитета . Но в начале дана характеристика особому двойному функционалу иммунной системы, в которой основную роль играют лимфоциты. Поэтому стоит напомнить, что же из себя предсталяют эти клетки.
Лимфоциты - это клетки иммунной системы, представляющие собой разновидность лейкоцитов, которые обеспечивают гуморальный иммунитет ( выработка антител ), клеточный иммунитет (контактное взаимодействие с клетками-мишенями), а также регулируют деятельность клеток других типов. По морфологическим признакам выделяют два типа лимфоцитов: большие гранулярные лимфоциты (чаще всего ими являются NK-клетки и малые лимфоциты ( T-клетки и B-клетки ).

Те или иные механизмы иммунной защиты есть практически у всех животных. Эти механизмы сильно различаются по своей структуре, сложности, эффективности и, главное, по соотношению врожденных и приобретенных компонентов. У беспозвоночных преобладает врожденный иммунитет, хотя это далеко не абсолютное правило. У позвоночных вдобавок к врожденным защитным механизмам развилась необычайно сложная адаптивная иммунная система, способная приспосабливаться (адаптироваться) к всевозможным новым инфекциям, вырабатывать новые средства борьбы с ними и обладающая к тому же хорошей памятью (именно благодаря иммунной памяти мы получаем стойкий иммунитет ко многим болезням, однажды переболев ими).
T- и B-лимфоциты высших позвоночных обмениваются между собой разнообразными химическими сигналами (см. ниже интерлейкины). В соответствии с этим у разных типов лимфоцитов активны строго определенные гены, ответственные за прием и передачу этих сигналов.
Интерлейкины - группа цитокинов (белков), синтезируемая и секретируемая Т-лимфоцитами, В-лимфоцитами и NK-клетками, а также взаимодействующими с ними клетками. Цитокины - это небольшие пептидные информационные молекулы. Цитокины имеют молекулярную массу, не превышающую 30 кD. Цитокин выделяется на поверхность клетки А и взаимодействует с рецептором находящейся рядом клетки В. Таким образом, от клетки А к клетке В передается сигнал, который запускает в клетке В дальнейшие реакции. Их основными продуцентами являются лимфоциты (дополнительно о цитокинах см. здесь → ).

Более подробно о цитокинах см. в отдельном разделе:

Активация иммунитета и Дендритные клетки
В 2011 году Нобелевская премия по физиологии и медицине присуждена Брюсу Бойтлеру и Жюлю Хоффманну за открытие механизмов активации врождённого иммунитета, и Ральфу Штайнману за открытие дендритных клеток и их роли в активации адаптивного иммунитета. Эти исследования называют революционными, поскольку открытие врождённого иммунитета в корне изменило представление о функционировании иммунной системы.
В природе существуют две линии защиты, два вида иммунитета.
Адаптивный иммунитет
Процесс выработки антител запускается не сразу, у него есть определённый инкубационный период, зависящий от типа патогена. Зато, если уж процесс активации пошёл, как только та же самая инфекция попытается проникнуть в организм ещё раз, B-клетки моментально отреагируют выработкой антител, и инфекция будет уничтожена немедленно, не причинив никакого вреда. Именно поэтому на некоторые виды инфекций у человека вырабатывается иммунитет на всю оставшуюся жизнь.
Врожденный иммунитет
Каким образом система врождённого иммунитета подаёт знак системе приобретённого иммунитета на выработку специфических антител? Вот за решение этого ключевого вопроса иммунологии и присуждена Нобелевская премия 2011 года.
Таким образом, открытие врождённого иммунитета привело к появлению новых подходов в профилактике и лечении заболеваний, в разработке новых вакцин и противоопухолевых препаратов.
Активация адаптивной иммунной системы

Адаптивный иммунитет может дифференцировать между конкретными патогенами и нацелить ответ, который является специфическим для данного патогена. Он может быстро реагировать при повторном воздействии конкретного патогена, предотвращая развитие симптомов (иммунологическая память). Адаптивная иммунная система координируется лимфоцитами (класс лейкоцитов) и приводит к выработке антител. В-лимфоциты (В-клетки) являются антитело-продуцирующими клетками, которые распознают и нацеливают определенный фрагмент патогена (антиген). Хелперные Т-лимфоциты (Т-клетки) являются регуляторными клетками , которые высвобождают химические вещества ( цитокины ) для активации специфических В-лимфоцитов
- Когда фагоцитарные лейкоциты поглощают патоген, некоторые из них представляют переваренные фрагменты (антигены) на их поверхности
- Эти антигенпрезентирующие клетки ( дендритные клетки ) мигрируют в лимфатические узлы и активируют специфические хелперные Т-лимфоциты
- Затем хелперные Т-клетки высвобождают цитокины для активации конкретной В-клетки, способной продуцировать антитела, специфичные к антигену
- Активированная В-клетка будет делиться и дифференцироваться с образованием короткоживущих плазматических клеток, которые производят большое количество специфических антител
- Антитела будут нацелены на их специфический антиген, повышая способность иммунной системы распознавать и уничтожать патоген.
Небольшая доля активированной B-клетки (и активированной TH-клетки) будет развиваться в клетки памяти, чтобы обеспечить длительный иммунитет.
См. дополнительно:

B- и T-лимфоциты. Общая характеристика
1. Общая характеристика B-лимфоцитов

B-лимфоциты (B-клетки) - функциональный тип лимфоцитов, играющих важную роль в обеспечении гуморального иммунитета. При контакте с антигеном или стимуляции со стороны T-клеток некоторые B-лимфоциты трансформируются в плазматические клетки, способные к продукции антител . Другие активированные B-лимфоциты превращаются в B-клетки памяти. Помимо продукции антител, В-клетки выполняют множество других функций: выступают в качестве антигенпрезентирующих клеток, продуцируют цитокины и экзосомы.
B-лимфоциты продуцируют и секретируют в кровоток молекулы антител, являющиеся измененными формами антигенраспознающих рецепторов этих лимфоцитов. Возникновение антител в крови после появления любого чужеродного белка- антигена - независимо от того, вреден он или безвреден для организма, и представляет собой иммунный ответ. Появление антител не просто защитная реакция организма против инфекционных заболеваний, но явление, имеющее широкое биологическое значение: это общий механизм распознавания "чужого". Например, иммунная реакция распознает как чужой и постарается удалить из организма любой аномальный и, следовательно, потенциально опасный вариант клетки, в которой в результате мутации в хромосомной ДНК образуется мутантная белковая молекула.
B-лимфоциты млекопитающих дифференцируются сначала в печени плода, а после рождения - красном костном мозге. В цитоплазме покоящихся B-клеток отсутствуют гранулы, но имеются рассеянные рибосомы и канальцы шероховатого эндоплазматического ретикулума. Каждая B-клетка генетически запрограммирована на синтез молекул иммуноглобулина, встроенных в цитоплазматическую мембрану. Иммуноглобулины функционируют как антигенраспознающие рецепторы, специфичные к определенному антигену. На поверхности каждого лимфоцита экспрессируется около ста тысяч молекул рецепторов. Встретив и распознав антиген, соответствующий структуре антигенраспознающего рецептора B-клетки размножаются и дифференцируются в плазматические клетки, которые образуют и выделяют в растворимой форме большие количества таких рецепторных молекул - антител. Антитела представляют собой крупные гликопротеины и содержатся в крови и тканевой жидкости. Благодаря своей идентичности исходным рецепторным молекулам они взаимодействуют с тем антигеном, который первоначально активировал B-клетки, проявляя таким образом строгую специфичность.
После связывания антигена с рецепторами B-клетки клетка активируется. Активация B-клеток состоит из двух фаз: пролиферации и дифференцировки; все процессы индуцируются контактом с антигеном и T- хелперами.
В результате пролиферации увеличивается число клеток, способных реагировать с введенным в организм антигеном. Значение пролиферации велико, поскольку в неиммунизированном организме очень мало B-клеток, специфичных для определенных антигенов.
Часть клеток, пролиферирующих под действием антигена, созревает и дифференцируется последовательно в антителообразующие клетки нескольких морфологических типов, в том числе и плазматические клетки . Промежуточные стадии дифференцировки B-клеток отмечены меняющейся экспрессией разнообразных белков клеточной поверхности, необходимых для взаимодействия B-клеток с другими клетками.
Каждый лимфоцит, относящийся к B-лимфоцитам и дифференцирующийся в костном мозге, запрограмирован на образование антител только одной специфичности.
Молекулы антител не синтезируются никакими другими клетками организма, и все их многообразие обусловлено образованием нескольких миллионов клонов B-клеток. Они (молекулы антител) экспрессируются на поверхностной мембране лимфоцита и функционируют как рецепторы. При этом на поверхности каждого лимфоцита экспрессируется около ста тысяч молекул антител. Кроме того, B-лимфоциты секретируют в кровоток продуцированные ими молекулы антител, являющиеся измененными формами поверхностных рецепторов этих лимфоцитов.
Антитела формируются до появления антигена, и антиген сам отбирает для себя антитела. Как только антиген проникает в организм человека, он встречается буквально с войском лимфоцитов, несущих различные антитела, причем у каждого есть свой индивидуальный распознающий участок. Антиген соединяется только с теми рецепторами, которые в точности ему соответствуют. Лимфоциты, связавшие антиген, получают пусковой сигнал и дифференцируются в плазматические клетки, продуцирующие антитела. Поскольку лимфоцит запрограммирован на синтез антител только одной специфичности, антитела, секретируемые плазматической клеткой, будут идентичны своему оригиналу, т.е. поверхностному рецептору лимфоцита и, следовательно, будут хорошо связываться с антигеном. Так антиген сам отбирает антитела, распознающие его с высокой эффективностью.
2. Общая характеристика T-лимфоцитов

Дополнительно см.:
В образовании антител центральная роль принадлежит B-лимфоцитам. При этом B-лимфоциты обеспечивают специфический приобретенный иммунитет совместно с другими малыми лимфоцитами - T-лимфоцитами , используя разнообразные механизмы, направленные в большинстве случаев на расширение пределов эффективности врожденного иммунитета.
T-лимфоциты подразделяются на ряд подклассов. Главные из них это две различные, неперекрывающиеся субпопуляции: клетки одной из них несут маркер CD4 и в основном "помогают" в осуществлении иммунного ответа или индуцируют его ( T-хелперы ), клетки другой несут маркер CD8 и обладают преимущественно цитотоксической активностью (цитотоксические T-лимфоциты ( T-киллеры )). При этом, Т-хелперы стимулируют выработку антител, а Т-супрессоры тормозят её.
Одни CD4 + T-клетки участвуют в регуляции дифференцировки B-лимфоцитов и образования антител. Другие CD4 + T-клетки взаимодействуют с фагоцитами, помогая им в разрушении микробных клеток. Обе эти субпопуляции CD4 + T-клеток названы хелперными T-клетками. Получены очевидные функциональные доказательства существования отдельной субпопуляции антигенспецифичных T-супрессоров, способных подавить иммунный ответ либо путем прямого цитотоксического воздействия на антигенпрезентирующие клетки, либо путем выделения "супрессивных" растворимых белков - цитокинов, либо путем передачи сигнала отрицательной регуляции.
Третья группа T-лимфоцитов распознает и разрушает клетки, инфицированные вирусами или иными внутриклеточно размножающимися патогенами. Этот тип CD8 + T-лимфоцитов назван цитотоксическими T-лимфоцитами.
Как правило, распознавание антигена T-клетками происходит только при условии его презентации на поверхности других клеток в ассоциации с молекулами MHC . В распознавании участвует специфичный к антигену T-клеточный рецептор , функциональнои структурно сходный с тем поверхностным иммуноглобулином sIg, который у B-клеток служит антигенраспознающим рецептором.
Свои функции воздействия на другие клетки T-лимфоциты осуществляют путем выделения цитокинов , которые передают сигналы другим клеткам, или в результате прямых межклеточных контактов. Как и в случае B-лимфоцитов, отбор и активация T-лимфоцитов происходят после контакта с антигеном, затем они проходят стадию клональной экспансии и превращаются в зрелые T-хелперы и цитотоксические T-лимфоциты, а также формируют обширную популяцию клеток памяти.
Одна из важных регуляторных функций T-лимфоцитов - это их способность стимулировать B-клетки к пролиферации и дифференцировке. Другая важная регуляторная функция T-клеток состоит в их способности угнетать иммунный ответ. При этом T-хелперы и T-супрессоры обнаруживают комплексный тип антигенной специфичности.
Фундаментальным свойством T-клеток является их специфичность по отношению к продуктам главного комплекса гистосовместимости MHC . Специфическое иммунологическое распознавание патогенных организмов - это всецело прерогатива лимфоцитов, поэтому именно они инициируют реакции приобретенного (специфического) иммунитета.
Отдельно стоит отметить т.н. NK-клетки (естественные киллеры или натуральные киллеры)
В настоящее время NK-клетки рассматривают как отдельный класс лимфоцитов. NK являются одним из важнейших компонентов клеточного врождённого иммунитета. Естественные киллерные (NK) клетки - это лимфоциты, которые могут опосредовать лизис определенных опухолевых клеток и вирусно-инфицированных клеток без предварительной активации. Они также могут регулировать специфический гуморальный и клеточно-опосредованный иммунитет. Основная функция NK - уничтожение клеток организма, не несущих на своей поверхности MHC и таким образом недоступных для действия основного компонента противовирусного иммунитета - Т-киллеров.
Дополнительно о Т- и В-лимфоцитах см. здесь →
Дополнительно см.:
К разделам:
- Иммуноглобулин А, активный связующий элемент для гомеостаза микробиоты хозяина
- Вклад комменсальной микрофлоры в иммунологический гомеостаз
- Роль микробиоты в иммунитете и воспалении ( + видео )
- Микробиота кишечника и воспаление
- Микробиота кишечника и хроническое системное воспаление низкой степени
- Кишечный дисбиоз и иммунометаболические нарушения
- Микробиом, иммунитет и пробиотики
- Роль кишечной микробиоты и метаболитов в гомеостазе кишечника и заболеваниях человека
- Эпигенетика, короткоцепочечные жирные кислоты и врожденная иммунная память
Будьте здоровы!
ССЫЛКИ К РАЗДЕЛУ О ПРЕПАРАТАХ ПРОБИОТИКАХ
Типы белых клеток крови. Происхождение белых клеток крови
Лейкоциты, называемые также белыми клетками крови, являются подвижными единицами защитной системы организма. Они формируются в костном мозге (гранулоциты, моноциты и некоторые лимфоциты) и в лимфоидной ткани
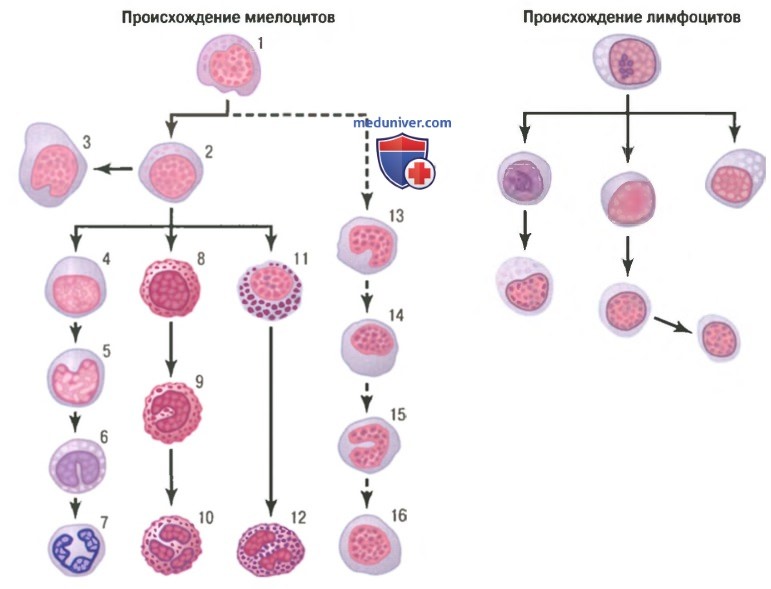
Происхождение белых клеток крови. Разные клетки миелоцитарного ряда:
1 - миелобласт; 2 -промиелоцит; 3 — мегакариоцит;
4 - нейтрофильный миелоцит; 5 — молодой нейтрофильный метамиелоцит; 6 - палочкоядерный нейтрофильный метамиелоцит;
7 - полиморфноядерный нейтрофил; 8 — эозинофильный миелоцит; 9 - эозинофильный метамиелоцит;
10 - полиморфноядерный эозинофил; 11 - базофильный миелоцит; 12 - полиморфноядерный базофил;
13-16 - стадии формирования моноцитов
Общая характеристика белых клеток крови
а) Типы белых клеток крови. В норме в крови присутствуют шесть типов белых клеток крови: полиморфноядерные нейтрофилы, полиморфноядерные эозинофилы, полиморфноядерные базофилы, моноциты, лимфоциты и иногда — плазматические клетки. Кроме того, существует большое количество тромбоцитов, представляющих фрагменты клеток другого типа — мегакариоцитов, которые, подобно лейкоцитам, обнаруживают в костном мозге. Первые три типа клеток имеют зернистость, как в клетках 7, 10 и 12 на рисунке выше, поэтому их называют гранулоцитами или, согласно клинической терминологии, полиморфноядерными клетками из-за многочисленных ядер.
Гранулоциты и моноциты защищают организм от внедряющихся агентов, главным образом путем их поглощения, т.е. фагоцитоза. Лимфоциты и плазматические клетки функционируют в основном в связи с иммунной системой. Наконец, специфической функцией тромбоцитов является активация механизма свертывания крови.
б) Концентрации разных типов лейкоцитов в крови. Взрослый человек имеет около 7000 белых клеток крови на микролитр крови (сравните с 5 млн красных клеток крови). По отношению к общему количеству лейкоцитов нормальное процентное содержание разных их типов приблизительно следующее.

Количество тромбоцитов, которые являются лишь фрагментами клеток, в каждом микролитре крови в норме — около 300000.
Происхождение белых клеток крови
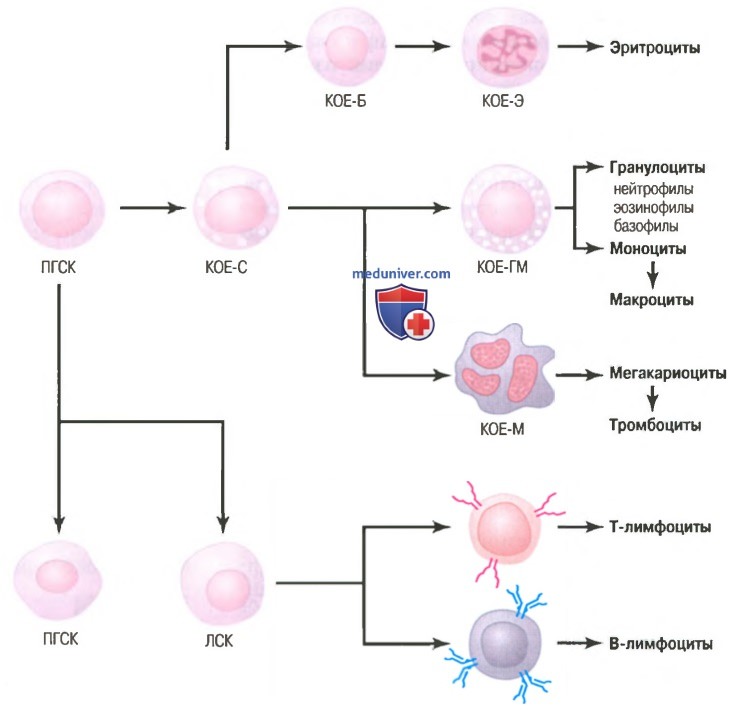
Образование множества различных клеток крови из исходной полипотентной гемопоэтической стволовой клетки в костном мозге.
КОЕ-Б - колониеобразующая единица бластная, КОЕ-ГМ - колониеобразующая единица гранулоцитарно моноцитарная,
КОЕ-М -колониеобразующая единица мегакариоцитарная, КОЕ-С - колонне образующая единица селезеночная,
ЛСК - лимфоидная стволовая клетка, ПГСК - полипотентная гемопоэтическая стволовая клетка
Ранняя дифференцировка полипотентной гемопоэтической стволовой клетки в разные типы коммитированных стволовых клеток показана на рисунке выше. Помимо клеток, предназначенных для образования эритроцитов, формируются два основных направления дифференцировки белых клеток крови: миелоцитарное и лимфоцитарное. Слева на самом верхнем рисунке в данной статье показано миелоцитарное направление дифференцировки, начинающееся с миелобласта; справа показано лимфоцитарное направление дифференцировки, начинающееся с лимфобласта.
Гранулоциты и моноциты формируются только в костном мозге. Лимфоциты и плазматические клетки образуются главным образом в разных лимфогенных тканях, особенно в лимфатических железах, селезенке, тимусе, миндалинах и в разнообразных очагах лимфоидной ткани повсюду в теле, например в костном мозге и так называемых пейеровых бляшках под эпителием кишечной стенки.
Лейкоциты, сформированные в костном мозге, хранятся там до тех пор, пока не возникнет необходимость их выхода в систему кровообращения. Выход осуществляется под действием различных факторов, которые обсуждаются далее. В норме в костном мозге хранятся примерно в 3 раза больше лейкоцитов по сравнению с количеством этих клеток, циркулирующих в крови. Это составляет примерно 6-суточный запас лейкоцитов.
Лимфоциты хранятся главным образом в различных лимфоидных тканях, за исключением небольшого их числа, временно транспортируемого в кровь.
Как показано на самом верхнем рисунке в данной статье, мегакариоциты (клетка 3) также формируются в костном мозге. Они фрагментируются, и небольшие фрагменты, известные как пластинки (или тромбоциты), затем выходят в кровь. Они очень важны для запуска процесса свертывания крови.
Видео физиология защитной функции крови (иммунитета) и группы крови - профессор, д.м.н. П.Е. Умрюхин
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Мононуклеары: моноциты и макрофаги
Мононуклеарным фагоцитам (моноцитам и макрофагам) принадлежит важнейшая роль в иммунных реакциях, защите организма от инфекций, а также восстановлении и перестройке тканей. Не бывает человека, у которого отсутствовала бы эта линия клеток, поскольку макрофаги, по-видимому, необходимы для удаления примитивных тканей по мере их замещения новыми в процессе эмбрионального развития.
Моноциты и различные формы тканевых макрофагов составляют систему мононуклеарных фагоцитов. Это именно система, так как все мононуклеары имеют общее происхождение, сходное строение и одинаковые функции (фагоцитоз).
Основная локализация макрофагов в тканях:
• Печень (купферовские клетки).
• Легкие (интерстициальные и альвеолярные макрофаги).
• Соединительная ткань.
• Серозные полости (плевральные и перитонеальные макрофаги).
• Кости (остеокласты).
• Головной мозг (реактивные клетки микроглии).
• Селезенка, лимфатические узлы, костный мозг.
• Стенка кишечника.
• Грудное молоко.
• Плацента.
• Гранулемы (многоядерные гигантские клетки).
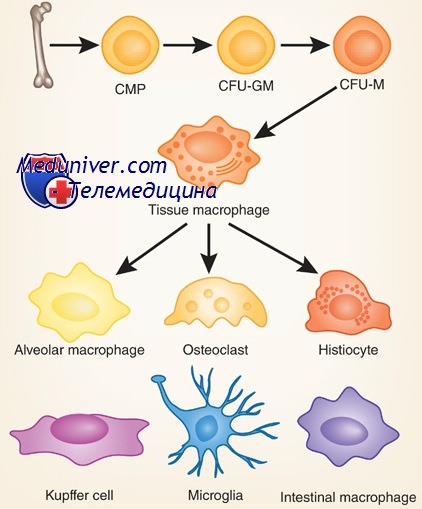
Моноциты — циркулирующие в крови предшественники тканевых макрофагов — развиваются в костном мозге быстрее и остаются в крови дольше нейтрофилов. Первый предшественник моноцита, монобласт, превращается в промоноцит, несколько более крупную клетку с цитоплазматическими гранулами и вдавленным ядром, состоящую из небольших глыбок хроматина, и, наконец, — в полностью развитый моноцит.
Зрелый моноцит по своим размерам больше нейтрофила, и его цитоплазма заполнена гранулами, содержащими гидролитические ферменты. Превращение монобласта в зрелый моноцит крови занимает около 6 сут. Моноциты сохраняют некоторую способность к делению и после попадания в ткани подвергаются дальнейшей дифференцировке; в тканях они могут оставаться в течение нескольких недель и месяцев.
В отсутствие воспаления моноциты, по-видимому, случайным образом попадают в ткани. Оказавшись там, они трансформируются в тканевые макрофаги, морфологические, а иногда и функциональные свойства которых зависят от конкретной ткани. Органоспецифические факторы влияют на дифференцировку моноцитов и определяют их метаболические и структурные особенности. В печени они превращаются в купферовские клетки, которые соединяют синусоиды, разделяющие соседние пластинки гепатоцитов.
В легких они представлены крупными эллипсоидными альвеолярными макрофагами, в костях — остеокластами. Все макрофаги обладают по крайней мере тремя основными функциями — антигенпредставляющей, фагоцитарной и иммуномодулирующей, связанной с секрецией многих цитокинов. В очагах воспаления моноциты и макрофаги могут сливаться друг с другом, образуя многоядерные гигантские клетки — последняя стадия развития мононуклеарных фагоцитов. Под действием некоторых цитокинов моноциты крови дифференцируются в дендритные клетки, которые особенно эффективно представляют антигены лимфоцитам.
Читайте также:

