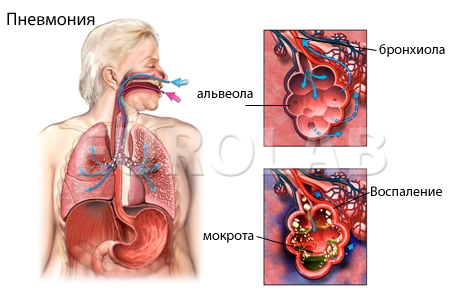
Болезнь филатова железистая лихорадка моноцитарная ангина болезнь пфейфера
Обновлено: 23.04.2024
Человек — существо называющее, особенно человек науки, которому необходимо давать названия новым изучаемым объектам. При этом одни явления до сих пор остаются неоткрытыми и неназванными, а другие, наоборот, получают даже избыточное количество различных наименований. В первую очередь это справедливо для медицины.
Например, болезнь Филатова, болезнь Филатова — Дьюка, болезнь Пфайффера, болезнь Тюрка, болезнь студентов, болезнь поцелуев, лихорадка железистая, острый доброкачественный лимфобластоз, мультинодулярный аденоз, моноцитарная ангина и пр., —
Время шло, росло число доступных методов исследования, и врачи выявляли все новые особенности болезни. Так, в первой половине XX в. исследователи отметили у пациентов с этим заболеванием характерную гематологическую картину: появление атипичных мононуклеаров, увеличение доли лимфоцитов и моноцитов в крови.
Одним из слушателей лекции был профессор Майкл Эпштейн (Michael Antony Epstein) — вирусолог, патолог и специалист в области электронной микроскопии. По всей видимости, новое заболевание так заинтересовало ученого, что в 1963 г. он начал культивировать и изучать клетки лимфомы. Из клеточной культуры Эпштейн выделил вирус, отнесенный к семейству герпесвирусов (лат. Herpesviridae).
Статья за авторством Майкла Эпштейна и его аспирантки Ивонны Барр была опубликована в 1964 г. в журнале Lancet, а открытый вирус назвали по имени ученых — вирус Эпштейна — Барр (ВЭБ).
Далее медицинская наука связала ВЭБ и болезнь Филатова. Британские исследователи отправили образцы клеточных линий в США Вернеру (Werner) и Гертруде Хенле (Gertrude Henle) из детского госпиталя в Филадельфии. Американцы нашли антитела к ВЭБ как у больных с лимфомой, так и у здоровых сотрудников лаборатории.
Вирус Эпштейна — Барр поражает в основном В-лимфоциты и эпителиоциты, в которых либо размножается, либо сохраняется в персистирующей форме. Размножение ВЭБ в клетках может активировать их пролиферацию, что в настоящее время связывают с развитием лимфомы Бёркитта и назофарингеальной карциномы. Также с наличием ВЭБ-инфекции ассоциируют и другие заболевания: волосатую лейкоплакию, общую вариабельную иммунную недостаточность, вирусный гепатит и прочие. Кроме того, активно обсуждается роль ВЭБ в развитии рассеянного склероза и синдрома Стивенса — Джонсона.
У девочек заболевание чаще всего диагностируется в возрасте 14–16 лет, у мальчиков — 16–18 лет. Согласно исследованиям, к 25–35 годам большая часть населения имеет пул циркулирующих антител к ВЭБ в крови, хотя далеко не у всех есть указания на клинические проявления в анамнезе. Часто ВЭБ-инфекция реактивируется у пациентов с иммунодефицитом, в том числе и у группы ВИЧ-инфицированных, возраст в данном случае не имеет значения.
Инкубационный период обычно составляет около 7–10 дней, но может достигать и трех недель. Период самого заболевания длится до двух месяцев.
Продром характеризуется постепенным нарастанием симптомов, субфебрильной температурой, усиливающейся вялостью. Симптомы при заражении вирусом Эпштейна-Барр:
- тонзиллита. Нередко развиваются аденоидит и воспаление слизистой оболочки нижней носовой раковины, в результате чего нарушается носовое дыхание.
- Увеличение лимфатических узлов (как правило, шейных), их болезненность. Без лечения могут расти не только размеры, но и количество вовлеченных узлов.
- Увеличение печени и/или селезенки. Описана также желтушная форма мононуклеоза, сопровождающаяся иктеричностью кожных покровов и склер. Биохимический анализ крови может выявлять повышение уровня печеночных трансаминаз, билирубина.
- Головные боли, головокружения. В редких случаях у пациентов описаны и более серьезные неврологические нарушения — невриты, менингиты, энцефалиты, мозжечковая атаксия, а также микропсия (синдром Алисы в Стране чудес, при котором объекты воспринимаются меньшими, чем они есть).
- Миалгии и артралгии.
- Катаральный трахеит, бронхит.
- Умеренный лейкоцитоз, нейтропения со сдвигом влево, лимфомоноцитоз (80–90 %), атипичные мононуклеары (10–60 %), по факту являющиеся В-лимфоцитами, несущими в себе вирусные частицы и претерпевшими в связи с этим функциональные и структурные изменения.
У пациентов с ИМ повышается частота других респираторных вирусных и бактериальных инфекций, а также поражения кожных покровов вирусом простого герпеса первого типа.
Клиническая картина для каждого пациента представляет собой сочетание указанных симптомов разной степени выраженности — от легких форм до форм с осложнениями, что обусловлено вторичной бактериальной инфекцией, острой печеночной недостаточностью, разрывами селезенки, гемолитической анемией, невритами.
Дифференциальную диагностику следует проводить с такими заболеваниями, как ангина, дифтерия, ОРЗ, псевдотуберкулез, туляремия, листериоз, вирусный гепатит, острый лейкоз, дебют лимфогранулематоза. Кроме того, нельзя забывать и о вероятном ВИЧ-позитивном статусе пациента.
46‑летний мужчина госпитализирован с лихорадкой, желтухой и общей слабостью, возникшими у него две недели назад. Семейный анамнез не отягощен, указаний на перенесенные заболевания печени нет. Пациент не употреблял алкоголь, не страдал наркотической зависимостью, был гетеросексуалом. Стаж курения— 10 лет. За последнее время не употреблял никаких лекарственных препаратов.
Температура тела — 37,8 °С. Выслушиваются сердечные шумы. Печень пальпируется на 2 см ниже края реберной дуги. Других отклонений не выявлено.
Результаты лабораторных исследований: повышение СОЭ (35 мм/ч), уровня гемоглобина (137 г/л), MCV (91,5 мкм); лейкоцитоз (11,6x1012/л), нейтрофилез до 78,3 %, 10 % атипичных лимфоцитов; тромбоцитоз до 196x109/л.
В биохимическом анализе крови: АСТ 121 Ед/л (норма 13–34 Ед/л), АЛТ 295 Ед/л (норма 8–44 Ед/л), щелочная фосфатаза 123 Ед/л (норма 37–114 Ед/л), общий билирубин 1,01 мг/дл (норма 0,5–1,3 мг/дл), сывороточный альбумин 28,8 г/л, нормальное протромбиновое время.
Выявлен высокий титр антител к ВЭБ класса IgM, без повышения титра антител к другим вирусам. Посевы крови, мочи — стерильны. В биоптате печени выявлены белки ВЭБ (LMP — latent membrane protein).
Однако через три недели возобновилась лихорадка (до 40 °С) с ознобом, пациент госпитализирован повторно. На рентгенограмме органов грудной клетки — небольшой двусторонний выпот в плевральной полости. По данным КТ — признаки кардиомегалии. Гемодинамическая декомпенсация потребовала срочного направления в отделение интенсивной терапии. Также назначены антибиотики широкого спектра действия.
Адаптировано из Mendez-Sanchez N., Uribe M.: Infectious mononucleosis hepatitis: a case-report. Annals of Hepatology, 2004. N 3 (2), P. 75–76
Ранее в лабораторной диагностике инфекционного мононуклеоза применялся метод изоляции вируса на лимфобластоидных клеточных линиях с последующим непрямым иммунофлюоресцентным анализом (ИФА), который сейчас имеет лишь историческое значение, поскольку неудобен, плохо стандартизуем и дорог. В настоящее время используются методы, связанные с детекцией ДНК вируса (полимеразная цепная реакция, ПЦР) либо определением антител к вирусным белкам (ИФА).
Определение титра специфических антител IgM и IgG и их авидности позволяет дифференцировать фазы ВЭБ-инфекции, в том числе отличать первичную инфекцию от паст-инфекции и реактивации инфекции, а также оценивать динамику иммунного ответа и эффект от проводимой терапии.
С помощью ПЦР-анализа определяют наличие ДНК вируса в различных биопробах, в частности в слюне. Исследователь может провести как качественное, так и количественное определение ДНК и оценить вирусную нагрузку. Отметим, что ПЦР- и ИФА-исследования следует использовать в комплексе для повышения эффективности диагностики.
Медицинская мысль, однако, не удовлетворилась этими рекомендациями и разработала еще ряд указаний: применение антипиретиков, десенсибилизирующей терапии, поливитаминов и гепатопротекторов (при наличии показаний). Обсуждается возможность назначения глюкокортикостероидов короткими курсами при осложненных формах ИМ.
Поскольку вирусная природа заболевания подтверждена, обоснованно применение противовирусных препаратов (аналогов нуклеозидов), а также иммуномодуляторов (в том числе интерферонов и индукторов синтеза интерферонов). Разрабатываются и методы клеточной иммунотерапии ВЭБ-инфекции, хотя это более оправданно при онкологической патологии, ассоциированной с вирусом.
Антибиотикотерапия при ИМ показана при вторичной бактериальной инфекции, однако популярных сегодня препаратов группы аминопенициллина следует избегать вследствие риска кожных высыпаний у пациентов с ИМ.
В целом заболевание протекает благоприятно. Человек, однажды перенесший ИМ, обычно не заболевает повторно, но остается вирусоносителем и потенциальным источником инфекции для окружающих. Кроме того, персистенция вируса в организме, видимо, может иметь в дальнейшем и иные проявления — от лимфопролиферативных заболеваний до такой распространенной патологии современности, как синдром хронической усталости.
Вирус Эпштейна — Барр характеризуется высокой изменчивостью, поэтому в настоящее время нет хороших вакцин, которые могли бы обнадежить медицинское сообщество.
Тем не менее, поскольку болезнь имеет множество аспектов, стоит ждать новых исследований и новых имен в истории ее изучения.
Причины и возбудитель
Возбудитель ИМ — вирус Эпштейн-Барра — ВЭБ (Epstein-Barr virus — EBV) — крупный оболочечный ДНК-содержащий вирус 4-типа из семейства Herpesviridae, подсемейства у Herpesviridae, рода Lymphocryptovirus.
На основании различий в строении генома и способности вызывать реакцию бласттрансформации В-лимфоцитов выделяют 2 штамма ВЭБ: наиболее активный в реакции тип 1(A) и менее активный — тип 2(B). Тип 1(A) имеет повсеместное распространение, тип 2(B) встречается преимущественно на Африканском континенте и ряде стран Северной Америки.
ВЭБ имеет овальную форму с диаметром 150-200 нм. Геном вируса представлен двумя молекулами ДНК, заключенными в икосаэдрический капсид, состоящий из 162 капсомеров. Комплекс капсидных белков вируса (р150, р18, р23) представляют его капсидный антиген — VCA (Viral capsid anti- gen). Иммунодоминантными белками в этом комплексе являются р 18 и р23.
На самых ранних этапах репликации EBV в организме инфицированного человека появляется высокоиммуногенный комплекс вирусных белков (р54 и р138), названный ранним антигеном ЕА (early antigen).
Мишенями для ВЭБ являются клетки, имеющие на своей поверхности рецептор CD21. Это эпителиоциты слизистых оболочек носо- и ротоглотки, выводных протоков слюнных желез; В-лимфоциты (прежде всего, находящиеся в фолликуллярных структурах лимфоидного кольца Пирогова- Ланганса и периферической лимфоидной ткани); дендритные клетки; эпителий шейки матки.
Узнать больше
Иммуносупрессивное действие ВЭБ с одной стороны обуславливает длительную (пожизненную) персистенцию вируса в организме с возможностью периодических обострений заболевания, с другой — объясняет возможную роль вируса в развитии иммуно- и онкопатологии. Вирус неустойчив к факторам внешней среды, быстро погибает под действием дезинфектантов, при высыхании в режиме комнатной температуры.
Эпидемиология
Источник инфекции — человек с острой и хронической манифестной или латентной формой ЭБВИ. Инфицированные лица активно выделяют вирус с последних дней инкубации и на протяжении 6-18 месяцев после первичной инфекции. Более чем у 90% бессимптомных серопозитивных индивидуумов вирус содержится в орофарингеальном секрете.
Основной механизм передачи — воздушно-капельный, путь передачи — аэрозольный. В основном ВЭБ передается при прямом близком контакте через слюну (при поцелуях, через игрушки, на которых есть зараженная слюна), содержащую клетки орофарингеального эпителия. Заражение возможно при несоблюдении санитарно-гигиенических правил обработки посуды в системе общественного питания, а также при использовании "общих” стаканов, бутылок и т.п. Также возможен парентеральный (при трансплантации органов и гемотрансфузиях) и половой пути передачи. Установлена возможность вертикальной передачи возбудителя с развитием врожденной ЭБВИ. ВЭБ передается при переливании препаратов крови, а также при трансплантации. Восприимчивым к заражению является все неиммунное население независимо от возраста.
Патогенез
Поступление ВЭБ в фолликулярные лимфатические структуры слизистой ротоглотки, в регионарные лимфоузлы, внедрение его в В-лимфоциты, их трансформация в лимфобластоидные клетки. Презентация антигенов вируса макрофагами и ДК иммунокомпетентным клеткам - начало формирования гуморального и клеточного иммунитета. Лимфогенная и гематогенная диссеминация ВЭБ.
Начальный период (от нескольких часов до 1 недели). Основные проявления: боли в горле, тонзиллит, фарингит, аденоидит, увеличение регионарных лимфоузлов. Интоксикационный синдром проявляется лихорадкой, ознобами, потливостью, слабостью в теле.
Период разгара (от 1 до 3-х и более недель). Происходит нарастание специфического иммунитета, некротические изменения на слизистых в месте входных ворот. Может присоединиться или активизироваться бактериальная флора (фолликулярная, лакунарная, некротическая ангины). Происходит продолжение выделения вируса со слюной и отделяемым носо- и ротоглотки.
Период реконвалесценции (от 1 до 3-4 месяцев). Пик формирования специфического иммунитета. Пораженные органы и ткани восстанавливаются. В большинстве случаев наступает клиническое выздоровление. В организме большинства переболевших вирус будет пребывать всю их жизнь.
Патоморфология
В связи с низкой летальностью патоморфология ИМ представлена в основном по результатам исследований биопсийного материала.
При патологоанатомическом исследовании макроскопически констатируется увеличение всех групп лимфатических узлов, миндалин и других лимфоидных образований глотки, селезенки, печени. При гистологическом исследовании выявляют пролиферацию лимфоидных и ретикулярных клеток, в печени перипортальную инфильтрацию лимфоидными элементами. В тяжелых случаях возможны очаговые некрозы в лимфоидных органах, появление лимфоидных инфильтратов в легких, почках, ЦНС и других органах. Редкие смертельные исходы чаще всего обусловлены разрывом селезенки, гематологическими осложнениями (гемолиз, тромбоцитопеническая пурпура) или поражением ЦНС.
Симптомы и классификация
По типу инфекционный мононуклеоз бывает таких форм:
- типичная,
- атипичные (стертая, бессимптомная)
По тяжести выделяют такие формы болезни:
- легкая,
- среднетяжелая,
- тяжелая.
По течению ИМ бывает не осложненным или осложненным.
В МКБ-10 (1995) обозначается так: В27.0 "Мононуклеоз, вызванный гамма-герпетическим вирусом".
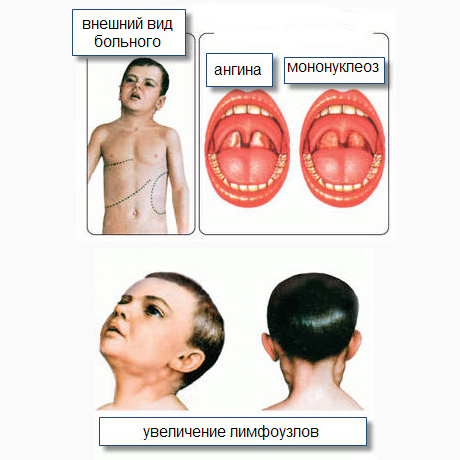
Ниже представлена наиболее типичная клиническая картина ИМ, наблюдаемая при среднетяжелом течении заболевания.
Инкубационный период — от 8 до 21 дней (максимально до 6-8 недель).
Начальный период (до 4-5 дней). Начало болезни может быть как острым, так и постепенным. Фебрильная лихорадка сопровождается прогрессирующей слабостью, головной болью, снижением аппетита и другими симптомами интоксикации. Гиперплазия третьей глоточной миндалины, расположенной на своде носоглотки, нарушение лимфооттока клинически реализуется появлением признаков аденоидита: заложенности носа, "гнусавости” голоса, ночного храпа (даже у маленьких детей), отека век, пастозности верхней половины лица.
Пациенты жалуются на умеренные боли в горле. Объективно — катаральные явления на миндалинах и слизистой ротоглотке. Обращает на себя внимание несоответствие умеренных катаральных явлений в ротоглотке с выраженностью интоксикационного синдрома. Уже сейчас могут изменяться контуры шеи за счет значительного увеличения шейных, затылочных, подчелюстных лимфоузлов. Лимфоузлы умеренно болезненны при пальпации, не спаяны между собой и с окружающими тканями, отчетливо контурированы, окружающая их подкожная клетчатка не отечна.
Период разгара (от 1 до 3-х и более недель) самочувствие больного ухудшается: лихорадка может достигать 40"С, сопровождается ознобом, усилением головной боли. Боли в горле при глотании усиливаются. Объективно выявляется симптоматика острого тонзиллофарингита, который может протекать в катаральной, фолликулярной, пленчатой или язвенно-некротической формах. Чаще всего наблюдается картина лакунарной ангины: гипертрофия миндалин до 2-3 степени, наличие на них рыхлых белесоватых налетов в виде островков, "столбов”. В некоторых случаях налеты могут напоминать дифтерийные - трудно снимаемые пленки, плотно связанные с подлежащей тканью.
На слизистой оболочке мягкого и твердого неба возможно появление множественных петехий, задняя стенка глотки резко гиперемированная, разрыхленная, зернистая, с множественными мелкими гиперплазированными фолликулами. Длительность ангины достигает 2-3 недель. Явления тонзиллита не имеют строгой корреляции с выраженностью интоксикационого синдрома.
Лимфоаденопатия приобретает генерализованный характер. Размеры лимфатических узлов варьируют от горошины до грецкого ореха (0,5-Зсм), пальпируются в виде единичных лимфоузлов или цепочки. Уже с 6-го дня болезни у большинства больных отмечается увеличение печени и селезенки. Стоит отметить, что селезенка увеличивается больше, чем печень.
Период реконвалесценции (от 1 до 3-4 месяцев).
Самочувствие больного постепенно улучшается, нормализуется температура тела, исчезают клинические симптомы острого тонзиллофарингита. Лимфоаденопатия регрессирует медленно — на протяжении 1,5 и более месяцев. Гепатолиенальный синдром может определяться в течение 3-6 месяцев. Длительность периода реконвалесценции индивидуальна, иногда субфебрильная температура тела сохраняются в течение нескольких недель. В периоде реконвалесценции выражен астенический синдром — слабость и недомогание могут сохраняться несколько месяцев. Если у больного нормальный иммунитет (защитные силы организма), он выздоравливает за 3-4 месяца.
Критериями тяжести течения ИМ служат:
- выраженность интоксикационного синдрома,
- выраженность изменений со стороны лимфоидной ткани,
- изменения гемограммы,
- наличие осложнений.
При легкой форме общее состояние пациента изменено незначительно, температура повышается до уровня 37-37,5˚ С, наблюдаются катаральные изменения носо- и ротоглотки воспалительного характера. Лимфатические узлы увеличены незначительно. Гепатоспленомегалия слабо выраженна. Обратное развитие симптомов происходит быстро (к концу 2-й нед).
При тяжелой форме фиксируется высокая лихорадка (температура тела свыше 39,5°С), выраженная интоксикация (вялость, адинамия, рвота, головная боль, анорексия) сохраняються свыше 3 недель. Гиперплазия лимфоидной ткани, расположенной на своде носоглотки проявляется в нарушении носового дыхания вплоть до его отсутствия, характерном внешнем виде больного (одутловатое "аденоидное лицо”). Поражение небных миндалин характеризуется тяжелым гнойно-некротическим, иногда фибринозным воспалением. Наблюдаются генерализованная лимфаденопатия, выраженная гепатоспленомегалия. Высокая вероятность осложнений. Обратное развитие симптомов происходит медленно, в течение 4-5 недель.
У больных инфекционным мононукпеозом отмечается параллелизм между тяжестью заболевания и количеством атипичных мононуклеаров в периферической крови.
Атипичные формы
Стертая — с неполным, со слабо выраженным, быстро проходящим симптомокомплексом.
Бессимптомная — клинические признаки болезни отсутствуют. Диагноз в этом случае возможен по лабораторным данным с учетом эпидемической ситуации.
Осложнения. Специфические:
-
(вследствие надгортанного стеноза, связанного со значительным увеличением лимфоидных образований глоточного кольца Пирогова-Вальдейера); , который может произойти спонтанно или от физических воздействий (например, при пальпации);
- поражения нервной системы (энцефалит, менингит, парезы черепных нервов, синдром Гийена-Барре); , тромбоцитопения, нейтропения.
- В редких случаях отмечают двустороннюю интерстициальную пневмонию с выраженной гипоксией.
Наиболее частое неспецифическое осложнение — присоединение бактериальных инфекций (отиты, синуситы, пневмонии и др.), вызванных золотистым стафилококком, стрептококками и др. Осложнения заболевания могут возникать в разные периоды, в том числе в периоде отдаленной реконвалесценции.
Исходы инфекционного мононуклеоза
1. Выздоровление. У большинства переболевших ИМ формируется стойкий противовирусный иммунитет, обеспечивающие полное клиническое выздоровление. Тем не менее, у них небольшое количество В-лимфоцитов (примерно от 1 до 50 на 1 млн. В-лимфоцитов), либо эпителиальных клеток содержат в ядре ДНК ЕВУ в виде циркулярной структуры (эписомы). При этом в непермиссивных (неразрешаюших) условиях репликация вируса столь низка, что не выявляется в ПЦР.
2. Переход в латентную инфекцию или бессимптомное вирусоносительство. При отсутствии у переболевшего клинических проявлений заболевания в 15-20% случаев методом ПЦР (при чувствительности метода 10 копий в пробе) в их эпителиоцитах (в слюне) или В-лимфоцитах выявляется репликация вируса. У таких пациентов спустя годы и даже десятилетия могут развиться ВЭБ-ассоциированные пролиферативные заболевания: развитие онкологического (лимфопролиферативного) процесса (множественные поликлональные лимфомы (лимфома Беркитта), назофарингеальная карцинома, лейкоплакии языка и слизистых ротовой полости, рак желудка и кишечника и др.).
3. Формирование хронической активной формы инфекции. У отдельных индивидуумов продолжающаяся активная репликация вируса сопровождается развитием клинической картины хронической формы ЭБВИ. У таких пациентов на протяжении от одного года до нескольких лет постоянно сохраняется или периодически возобновляется выраженная в различной степени мононуклеозоподобная симптоматика, нередко в сочетании с различными органными поражениями.
Поражение ЦНС, миокарда, почек, гемофагоцитрный синдром, длительный субфебрилитет неясного генеза, клинические признаки вторичного иммунодефицита (рецидивирующие бактериальные, грибковые и микст-инфекции респираторного, ЖКТ, кожи и слизистых) могут быть и единственными проявлениями хронической ЭБВИ. Критериями диагноза хронической EBV-инфекции у пациента являются: факт перенесения им не далее, чем за 6 месяцев до обращения ИМ и иммуно- гистологического подтверждения роли EBV в поражении органов по выявлению ядерного антигена вируса методом антикомплементарной иммунофлюоресценции.
4. Развитие аутоиммунных заболеваний — системной красной волчанки, ревматоидного артрита, синдрома Шегрена и др. Следует отметить, что две последние группы заболеваний могут развиваться через большой промежуток времени после инфицирования).
5. Развитие лимфопролиферативных процессов (лимфома, назофарингеальная карцинома, лейкоплакия языка и слизистых ротовой полости, рак желудка и кишечника и др.).
6. Обсуждается возможное участие ВЭБ в возникновении синдрома хронической усталости.
Внебольничная пневмония (один из видов пневмоний) развивается до госпитализации в лечебно-профилактическое учреждение, или в первые 48 часов с часа госпитализации. Уровень смертности у людей молодого возраста колеблется от 1 до 3%, при тяжелых внебольничных пневмониях он поднимается до 15-30% среди лиц пожилого и старческого возраста.
Симптомы внебольничной пневмонии
В типичных случаях пневмония начинается остро, у человека появляется сухой малопродуктивный кашель, температура тела повышается, больной замечает у себя одышку, боли при дыхании (плевральная боль), врачи отмечают крепитирующие, мелкопузырчатые хрипы.
Обследование
Проводятся такие мероприятия:
- Общий анализ крови;
- Рентгенография грудной клетки в двух проекциях;
- Биохимический анализ крови – креатинин, мочевина, электролиты, печеночные ферменты;
- Исследование газов артериальной крови (при тяжелом течении болезни): каждые сутки до нормализации показателей;
- Культуральное исследование мокроты для выделения возбудителя и оценки его чувствительности к антибиотикам;
- Микробиологическая диагностика: микроскопия мазка, окрашенного по Граму;
- ПЦР – для респираторных вирусов и атипичных возбудителей;
- При тяжелом течении внебольничной пневмонии у человека: исследование гемокультуры, предпочтительно до начала антибактериальной терапии;
- Диагностика туберкулеза.
Критерии тяжести и прогноз внебольничной пневмонии
Чтобы перевести больного в отделение реанимации и интенсивной терапии, или обоснованно отказать в переводе, медики применяют модифицированную шкалу Британского торакального общества CURB-65:
Азот мочевины крови > 7 ммоль на литр
Частота дыхания (ЧД) равно или более 30/мин
Диастолическое АД равно или менее 60 мм рт. ст. или систолическое артериальное давления
Возраст равен или больше 65 лет
Положительный ответ = 1 балл.
Интерпретация полученных результатов по шкале CURB-65 Количество баллов
Необходимо амбулаторное лечение
Показано стационарное лечение
Показано стационарное лечение. При 4-5 баллах – нужен перевод человека в ОРИТ
Лечение тяжелой внебольничной пневмонии
Крайне тяжелая пневмония
Начинать лечение нужно, как при септическом шоке. Приподнятое положение головного конца кровати на 35-45 градусов организуют после стабилизации гемодинамики. Если оксигенотерапия не приводит к приемлемым параметрам оксигенации (РаO2 больше 70 мм рт. ст., SрO2 > 92%), нужно применить какой-либо вариант респираторной поддержки. Назначается далее наиболее эффективная антибактериальная терапия.
В качестве стартовой терапии часто назначают больному внутривенно ванкомицин + меропенем + макролид. Другой вариант: в/в цефтаролин фосамил + макролид. Цефтаролин (Зинфоро) причисляют к предствителям 5-го поколения цефалоспоринов, он воздействует на метициллин-резистентный золотистоый стафилококк (MRSA).
Некоторые специалисты предлагают использовать последние две выше отмеченные комбинации по причине, что нет никакой удовлетворенности результатами лечения тяжелой пневмонии с использованием традиционных стартовых схем антибактериальной терапии – уровень смертности очень высокий. Медики предполагают, что предложенные комбинации должны обеспечить максимальную эффективность антибактериального лечения.
Стоит отметить, что в основном времени для смены антибиотика в случае неэффективности стартовой антибактериальной терапии при этой форме пневмонии все равно у врачей нет. В менее тяжелых случаях действуют согласно таким правилам:
- При тяжелой внебольничной пневмонии назначение антибиотиков нужно делать срочно; отсрочка в их назначении на 4 часа и более существенно уменьшает шансы человека на успешное выздоровление и ухудшает последствия;
- Для стартовой терапии в основном выбирают внутривенные цефалоспорины 3-го поколения (цефотаксим, цефтриаксон) или ингибиторозащищенные пенициллины (клавуланат /амоксициллин), комбинируя их с макролидами для внутривенного введения (спирамицин, кларитромицин, азитромицин). Эритромицин на сегодня специалистами не рекомендуется использовать в лечении ВП;
- Настоятельно не рекомендуется применять монотерапию (лечение одним лекарством) фторхинолонами, в том числе и респираторными, в лечении ВП независимо от тяжести.
Причину низкой эффективности левофлоксацина (Таваника) медики назвать на сегодня не могут. Не так давно это наблюдение подтвердилосьисследованием, где оценивалась эфективность респираторных фторхинолонов и комбинаци беталактамов и макролидов в лечении тяжелой ВП с септическим шоком. Комбинированная терапия дала в разы больший нужный эффект.
При начальном лечении фторхинолоны можно назначить как второй препарат, если имеется аллергия к бета-лактамам или макролидам. Стоит помнить, что изложенный подход противоречит рекомендациям по лечению ВП Российского респираторного общества, где респираторные фторхинолоны считаются оптимальным выбором в качестве препарата для стартовой терапии для многих категорий больных. Но очень близок к совместным рекомендациям Chest Societ и Department of Pulmonary Medicine, National College of Chest Physicians Indian.
Также медикам стоит учитывать плохое качество и фальсификацию антибактериальных средств. Так что и по этим причинам оптимально отдавать предпочтение комбинированному антибактериальному лечению.
Выбор антибиотика для стартовой терапии при внебольничных пневмониях
На сегодняшний день нет доказательств целесообразности назначения антигистаминных препаратов, биогенных стимуляторов, иммуномодуляторов (включая гранулоцитарный колониестимулирующий фактор), витаминов, а также длительного применения нестероидных противовоспалительных препаратов и ненаркотических анальгетиков при ВП.
Не рекомендуется назначать свежезамороженную плазму, если нет клинически значимой коагулопатии, а также кортикостероиды (если у человека нет септического шока). Нужно отдавать предпочтение макролидным антибиотикам с улучшенными фармакокинетическими свойствами – азитромицину, кларитромицину, спирамицину, моксифлоксацину.
Очень часто в России и Украине в состав стартовой антибактериальной терапии врачи включают метронидазол. На самом деле его назначение имеет какой-то смысл только при аспирационной пневмонии или абсцессе легкого. Не рекомендуется назначать для стартового антибактериального лечения цефазолин, лекарства из группы тетрациклина (в том числе тигециклин), клиндамицин, цефтазидим, линкомицин – эффективность этой группы препаратов при ВП слишком низкая.
Внутрибольничная (нозокомиальная) пневмония
Критерий диагностики внутрибольничной (нозокомиальной) пневмонии (НП): развивается после 48 часов (2 суток) с момента госпитализации в ЛПУ. Уровень смертей при этом состоянии составляет 20-50%.
Для успешного лечения врачу очень важно как можно быстрее установить этиологический диагноз. Многие из этих больных находятся на управляемом дыхании, что облегчает получение материала для микробиологических исследований путем эндотрахельной аспирации. Наиболее часто возбудителями НП являются аэробные грам (–) микроорганизмы – Escherichia coli, Pseudomonas . aeruginosa, Enterobacteriacae, Klebsiella pneumoniae, Acinetobacter spp. Достаточно часто выделяют грам (+) метициллинорезистентные штаммы Staphylococcus aureus (MRSA), относящийся к грам (+) бактериям.
В последнее время стали чаще встречаться полирезистентные микроорганизмы: Burkholderia cepacia и Stenotrophomonas maltophilia. В частых случаях заболевание вызывается сразу несколькими из перечисленных возбудителей. К микроорганизмам, которые не имеют этиологической значимости при НП у пациентов без иммунодефицитных состояний, относятся Enterococcus spp., Streptococcus viridans, Neisseria spp., коагулазанегативные стафилококки, грибы.
Лечение внутрибольничных (нозокомиальных) пневмоний
Выбор стартовой антибактериальной терапии специальная таблица, используемая врачами.
Базисные мероприятия
Они проводятся до выхода больного из тяжелого состояния. Лечение должно быть направлено на достижение следующих параметров гомеостаза:
- PetСO2 36-45 мм рт. ст;
- РаO2 > 70 мм рт. ст., а РаСO2 в границах 35-40 мм рт. ст;
- Уровень глюкозы в крови 3,4-10 ммоль/л;
- Насыщение гемоглобина смешанной венозной крови кислородом (ScvO2) > 70%;
- Осмолярность 285-295 мосм/л;
- Натрий крови 137-145 ммоль/л;
- Лактат менее 2 ммоль/л;
- Гематокрит > 30%, Нb > 80 г на литр;
- Диурез более 0,5 мл/кг/ч.
Непрерывная инфузия антибиотиков
Для экономии антибиотиков, при среднетяжелом или тяжелом течении внебольничной пневмонии, их можно вводить методом непрерывной инфузии. Также этот метод в ряде случаев уменьшает вероятность появления резистентных к антибактериальной терапии форм возбудителя (например, к меропенему).
При таком режиме введения расчетную суточную дозу антибиотика врачи уменьшают примерно на 30%. Этот режим введения антибиотиков не влияет на исходы (по сравнению с традиционным способом введения). Фторхинолоны, котримоксазол, аминогликозиды, метронидазол для непрерывного введения не рекомендуется использовать, потому что их эффективность напрямую зависит от концентрации препарата в крови, а она при непрерывном введении относительно невысока.
Если стартовая антибактериальная терапия неэффективна
При неэффективности стартовой антибактериальной терапии (по клиническим показателям и данным объективного контроля), производится ее коррекция. Как правило, назначаются антибиотики широкого спектра (или их комбинация), с бактерицидным типом действия.
При пневмонии легкой и средней тяжести, если препараты оказались неэффективны, их меняют через 2-3 суток; при тяжелой пневмонии – спустя 36-48 часов. Критериями прекращения антибактериального лечения служат: нормализация температуры на протяжении 3-х суток, исчезновение клинической и регрессия рентгенологической симптоматики.
Инфузионная терапия
Больные с пневмонией требуют дополнительного приема жидкости (температура тела выше нормальных значений, тахипноэ – потеря приблизительно 500-800 мл в сутки), в то же время избыточное введение жидкости приводит к тому, что больше жидкости накапливается в поврежденном легком, ухудшается оксигенация. Не рекомендуется всем больным с пневмонией назначать внутривенно инфузионную терапию, если у него сохраняется приемлемый уровень артериального давления, возможность самостоятельно принимать жидкости и пищу, нет олигурии. Стоит учесть: не нужно применять растворы глюкозы (если нет гипогликемии) и свежезамороженную плазму (если у человека нет клинически значимой коагулопатии).
У больных с тяжелой пневмонией нужно использовать 2-ступенчатый подход:
1. Сначала проводят энергичную инфузионную терапию, направленную на регидратацию и стабилизацию гемодинамических показателей, восстановление диуреза. Нужно вводить больному солевой раствор, и, при необходимости, раствор альбумина.
2. Если гемодинамика нормализовалась – проводится консервативное инфузионное лечение с ориентацией на поддержание нулевого суточного баланса.
Респираторная поддержка
Важно применять минимально инвазивный вид респираторной поддержки, который обеспечивает приемлемую степень оксигенации. Лучше, чтобы сохранялась дыхательная активность человека. Довольно успешно врачами применяются инвазивные или неинвазивные режимы с сохранением спонтанной вентиляции: Pressure support (PS) или Constant Positive Airway Pressure (CPAP).
В более тяжелых случаях рекомендуются режимы, при которых сохраняется спонтанная дыхательная активность, например, Biphasic Positive Airway Pressure (BIPAP) или Synchronized intermittent mandatory ventilation (SIMV). В крайне тяжелых случаях лучше проводить механическую вентиляцию легких.
Для седации используют: пропофол, наркотические анальгетики (фентанил, реже – морфин), кетамин, оксибутират натрия. Для поддержания ритма бодрствования пациента, близкого к естественному, нужно назначить пропофол в ночные часы – это позволяет снизить частоту возникновения делирия и экономить препарат. Бензодиазепины становятся причиной мышечной слабости и имеют длительный период полувыведения, поэтому их лучше не назначать в качестве седатиков.
Стоит помнить: при пневмонии, особенно внебольничного вида, чем длительней искусственная вентиляция легких – тем хуже исходы терапии. Врачам надо принимать все возможные меры, чтобы в наиболее ранние сроки перевести пациента на самостоятельное дыхание. Очень часто медики злоупотребляют ИВЛ. Например, после аспирации (отравления, анестезия и т.д) назначают длительную ИВЛ якобы для профилактики, хотя приемлемую оксигенацию больной может обеспечить, дыша самостоятельно, без поддержки аппарата. В данном случае ИВЛ в разы увеличивает риск неблагоприятного исхода болезни.
Другие рекомендации
У пациентов с тяжелой дыхательной недостаточностью есть большая вероятность возникновения стрессовых язв. Этим людям показано назначение ингибиторов протонной помпы (омепразол) или блокаторов Н2-гистаминовых ре-цепторов (ранитидин).
Для профилактики тромбозов и ТЭЛА у людей с тяжелой пневмонией рекомендуется назначать низкомолекулярный гепарин в профилактической дозировке. Большинству больных с пневмониями ингаляции не нужно приписывать. Но у больных с вязкой, труднооткашливаемой мокротой, можно применять ингаляции ацетилцистеина по 2-5 мл 20% раствора 3-4 раза в сутки или 40-60 мг фуросемида два-три раза в сутки.
В редких случаях, в основном у пациентов с хронически сниженным уровнем (например, при энцефалопатии) сознания (ШГ– 9-12 баллов) и ослабленным кашлевым рефлексом, можно наложить микротрахеостому. Каждые 2 часа медики должны вводить в нее 5,0 –0,9 % раствора натрия хлорида. При наличии гнойной мокроты – раствор натрия хлорида заменяют, как правило, 0,25% раствором диоксидина.
Медикам нужно учитывать, что пневмония – инфекционное заболевание, потому к вопросам собственной безопасности нужно подходить с повышенным вниманием.
Инфекционный мононуклеоз и листериоз. Ротоглотка при туляремии и менингококкемии
Инфекционный мононуклеоз нередко характеризуется поражением лимфоидной ткани носоглотки и миндалин. При генерализации инфекции наблюдается увеличение не только подчелюстных, но и других групп ЛУ (подмышечных, локтевых, паховых), особенно заднешейных, иногда трахеобронхиальных. Помимо преимущественного поражения лимфоидной ткани, вовлекается ретикулоэндотелий легких, сердца, печени, почек, нервной системы в виде интерстициального воспаления в них. Пролиферация лимфоидной ткани сопровождается появлением в периферической крови большого количества широкоплазменных мононуклеаров, гетерофильных антител, гипергамма-глобулинемией.
При мононуклеозе преобладает чаще триада симптомов лихорадка, лимфаденопатия и тонзиллит. Больные жалуются на боль в горле, дисфагию. Дыхание через нос затруднено. Речь с носовым оттенком. Миндалины увеличены, воспалены по типу катаральной, фолликулярной, лакунарной, а через несколько дней от начала болезни и пленчатой, язвенно-некротической ангины, иногда с паратонзиллитом. Изо рта своеобразный сладковато-приторный запах. Возможны также афтозный, везикулезный, язвенный стоматит, гингивит, катаральный или гранулезный конъюнктивит Лихорадка длится 1-3 недели, иногда дольше.
Она может быть постоянной, ремиттирующей, интермиттирующей, гектической, волнообразной, субфебрильной. Встречаются формы мононуклеоза без лихорадки. ЛУ при мононуклеозе не спаяны между собой и без явлений периаденита; они уменьшаются медленно и достигают нормальных размеров по сравнению с их состоянием при ангине только через несколько недель, реже через несколько месяцев и очень редко даже через год и позднее. В отличие от ангины и дифтерии при мононуклеозе возможны полиморфная кожная сыпь и желтуха. Обычно увеличены печень и селезенка.
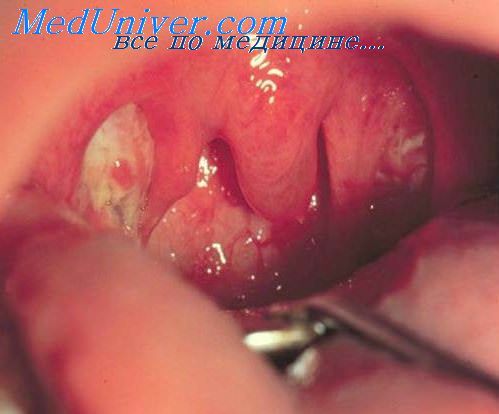
При листериозе изменения в ротоглотке в виде ангины - от катаральной до фибринозной и язвенной Заболевание протекает с высокой, нередко септической лихорадкой, ознобами, потливостью, с увеличением печени, селезенки и ЛУ. Выделяют ангинозно-железистую и ангинозно-септическую формы листериоза. В крови на фоне лейкопении отмечается моноцитарная и мононуклеарная реакция, на поздних стадиях сменяющаяся лейкоцитозом. Продолжительность лихорадки до 3 недель и более.
В отличие от ранее рассмотренных болезней с коротким инкубационным периодом при листериозе он достигает 2—4 недели, что может оказать большую диагностическую помощь. Заболевание носит характер локальных эпидемических вспышек, связанных с общим источником заражения. Источниками инфекции при листериозе являются больные сельскохозяйственные животные и птицы.
Близко к листериозу по эпидемиологическим особенностям стоит туляремия, при которой поражение ротоглотки может быть очень ярким В этих случаях выделяют ангинозно-железистую форму туляремии, характеризующуюся болью в горле, затруднением при глотании, высокой лихорадкой. Миндалины, задняя стенка глотки, мягкое небо гиперемированы, язычок и дужки отечны Налеты на миндалинах грязно-серого цвета, очень напоминают налеты при локализованной дифтерии. Наряду с некротической ангиной увеличены и болезненны шейные, околоушные, поднижнечелюстные лимфоузлы, приобретающие характер бубона, который подвергается гноевидному размягчению. Ангина при туляремии носит затяжной характер до 2-3 недель, сопровождается повышенной температурой.
Часты изменения в ротоглотке при инфекциях, вызванных менингококком и стрептококком. Менингококковый назофарингит отличается наибольшими изменениями слизистой оболочки в носовой части глотки. Задняя стенка глотки резко гиперемирована, отечна, видны множественные лимфоидные фолликулы. Дыхание через нос затруднено. При тенденции к генерализации инфекции (развитие менингококкцемии) нарастает токсикоз, возможно появление розеолезно-папулезных и типичных геморрагических элементов сыпи.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Лечение и профилактика ветряной оспы. Инфекционный мононуклеоз (болезнь Филатова)
Основана на характерных клинических проявлениях и данных эпидемиологического анамнеза (общение с больным ветряной оспой). К специфическим лабораторным методам подтверждения диагноза прибегать обычно нет необходимости. Возможно выделение вируса и постановка серореакций. Проводят дифференциальный диагноз с ИБ, протекающими с экзантемами.
Сыпь тушируется 5% раствором калия перманганата или 1% раствором бриллиантового зеленого. Проводят дезинтоксикационную терапию. При гнойных осложнениях назначают антибиотики. Лечение энцефалита проводят кортикостероидами и другими противовоспалительными препаратами, назначают дегидратационные средства. В I триместре беременности у женщин, больных ветряной оспой, возможны висцеральные поражения плода. Инфицирование в поздние сроки беременности (незадолго до родов) может привести к врожденной ветряной оспе.
Источник инфекции - только больной человек, заразный за сутки до появления сыпи и в течение всего периода подсыпания свежих элементов сыпи. Через 3 дня после прекращения подсыпаний больной человек перестает быть опасным для окружающих. В некоторых случаях контакт с больным ветряной оспой приводит к развитию опоясывающего лишая, поскольку возбудители их являются мутантами одного вируса, относящегося к группе герпес-вирусов. С профилактической целью больного изолируют на период до дня подсыхания везикул. Дети, не болевшие ветряной оспой, не допускаются в детские учреждения с 11 по 21-й день после последнего контакта с больным ветряной оспой. Детям, ослабленным тяжелыми болезнями, бывшим в контакте с больным ветряной оспой, вводят иммуноглобулин (по 3 мл внутримышечно).
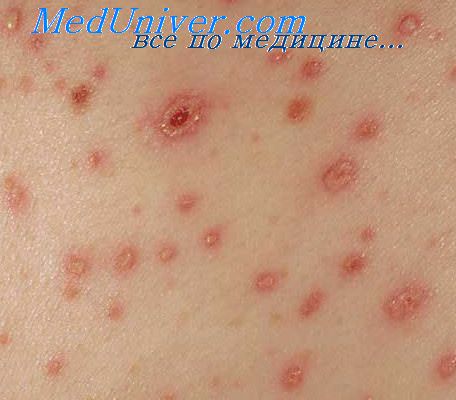
Инфекционный мононуклеоз (болезнь Филатова)
Болезнь Филатова, железистая лихорадка, моноцитарная ангина, болезнь Пфейфера, болезнь новобранцев, поцелуйная болезнь, Mononucleosis infectiosa-лат, Infectious mononucleosis-англ., Infectiosa mononucleos - исп., и др.
Инфекционный мононуклеоз - острое вирусное заболевание, проявляющееся лихорадкой, генерализованной лимфаденопатией, тонзиллитом, увеличением печени и селезенки, иногда только сыпью или только лихорадкой, и характерными изменениями гемограммы в виде мононуклеарной реакции.
Упоминание о болезни, похожей на мононуклеоз, имеются у Гиппократа, проследившего инфекционную заболеваемость в одном регионе в течение полного календарного года. Клинические проявления заболевания впервые описаны Н.Ф. Филатовым в 1885 г., что позволило выделить его в самостоятельную болезнь из группы железистых лихорадок. В 1889 г. это же сделал Е. Пфейфер и в 1915 г. Иреланд. Название болезни - инфекционный мононуклеоз дали Т. Спрэнт и Ф. Эванс, после чего оно получило официальное признание. Вирус - возбудитель болезни выделили английский патолог М.А. Эпстайн и канадская исследовательницавирусолог И. Барр (1964 г.) из клеток лимфомы Беркитта, распространенной в ряде стран Африки. Возбудитель получил название вируса Эпштейна-Барр, с ним стали связывать этиологию ИнМон, как самостоятельного заболевания.
Возбудитель - В-лимфотропный ДНК-содержащий вирус человека относится к вирусам герпеса /V типа (семейство Gerpes Viride, подсемейство Gamma herpes viridae). В эту же группу входят вирус простого герпеса (тип I и II), вирус ветряной оспы - опоясывающего герпеса (лишая) и цитомегаловирус. Вирус в диаметре 120-150 нм, окружен оболочкой, содержащей липиды; обладает тропизмом к В-лимфоцитам, имеющим рецепторы к этому вирусу. Кроме того, с ним связывают этиологию лимфомы Беркитта, назофарингеальной карциномы и некоторых лимфом, развивающихся у лиц с иммунодефицитом.
Вирус со слюной больного или серопозитивных здоровых лиц (встречаемость вируса у 15-25% здоровых - норма) попадает в дыхательные пути и поражает лимфоидную ткань носовой части глотки, проникает в кровь, вызывая генерализованную лимфаденопатию, сплено- и гепатомегалию. Избирательное поражение лимфоидной и ретикулярной ткани ведет к генерализованной выраженной пролиферации В-лимфоидных клеток.
Генерализованный характер поражений лежит в основе полиморфизма клинических проявлений мононуклеоза. В их развитии придают патогенетическое значение сенсибилизации к различным видам эндогенной микрофлоры, что является причиной суперинфекции. В частности, роль аутофлоры зримо проявляется при некротических поражениях ротоглотки, особенно миндалин. Длительное персистирование вируса Эпштейна-Барр обуславливает формирование хронических рецидивирующих форм мононуклеоза и реактивацию инфекции в любом возрасте при ВИЧ-инфекции и у ослабленных больных, способствуя развитию бактериальных осложнений (отит, холангит и др.), а также аутоиммунных - гемолитической анемии, тромбоцитопении и гранулоцитопении.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также: