Ботулизм это газовая анаэробная инфекция
Обновлено: 22.04.2024
Столбняк, хотя и ограниченный иммунизацией, распространен по всему миру. В США наиболее часто встречается среди неиммунизированных или не полностью иммунизированных пожилых лиц, а также после таких травм, как колотые раны, аборты или повреждения при контакте с землей.
Патогенез
При низком окислительновосстановительном потенциале в ране, загрязненной спорами Clostridium tetani, происходит прорастание спор, сопровождающееся образованием токсина. Токсин проникает в тело нервной клетки, мигрирует через синапс к пресинаптическому окончанию, блокируя высвобождение ингибирующих нейромедиаторов. Генерализованная мышечная ригидность возникает в результате повышения активности покоя амотонейронов при снижении действия ингибиторов.
Клинические проявления
Диагностика
Диагностика столбняка проводится клинически. Микробы часто не высеваются из ран больных столбняком и обнаруживаются в ранах больных, у которых столбняка нет.
Лечение
Цель лечения — устранение источника образования токсина, нейтрализация несвязанного токсина, предупреждение мышечных спазмов и обеспечение поддерживающей терапии (особенно в отношении дыхательной системы) до и после выздоровления. Больного помещают в тихую изолированную палату для проведения интенсивной терапии. Бензилпенициллин (10–12 млн. ЕД/сут внутривенно в течение 10 дней) вводят для устранения вегетативных форм. Вводят противостолбнячный иммуноглобулин G (TIG) в дозе 3000–6000 ЕД внутримышечно быстро для нейтрализации циркулирующего и несвязанного токсина. Лошадиный столбнячный антитоксин можно ввести в дозе 10 000 ЕД внутримышечно, но к нему часто отмечается гиперчувствительность, и период его полужизни короче, чем у TIG. Для лечения мышечного спазма применяют диазепам, при выраженном спазме показана нейромышечная блокада. При ларингоспазме может понадобиться ИВЛ для устранения гиперактивности симпатической НС. Оптимальная терапия при избыточной симпатической активности не разработана, применяют лабетолол, эсмолол, клонидин и морфина сульфат. Больным проводят активную иммунизацию против столбняка, поскольку естественное течение болезни не стимулирует иммунитет.
Профилактическая схема для взрослых — 3 дозы столбнячного анатоксина, первую и вторую вводят внутримышечно с промежутком в 48 нед, а третью через 6–12 мес после второй. Вспомогательная доза вводится каждые 10 лет. Профилактика при наличии ран: столбнячный анатоксин вводят при любой ране, если:
- иммунный статус больного неизвестен,
- в прошлом введено менее 3 доз или
- прошло более 10 лет после введения 3 доз.
При тяжелых и сильно загрязненных ранах иммунизацию проводят, если прошло более 5 лет после последнего эпизода вакцинации. При всех ранах необходимо вводить столбнячный иммуноглобулин 250 мг внутримышечно, если иммунный статус больного неясен или неполноценен; исключения составляют малые, чистые раны.
Ботулизм
Эпидемиология
Ботулизм как заболевание человека распространен повсеместно. Пищевой ботулизм возникает при употреблении пищевых продуктов, зараженных образовавшимся в них токсином (чаще эти пищевые продукты имеют домашнее происхождение). Раны, служащие источником болезни, должны быть заражены С1. Botulinum: к ним относятся раны, загрязненные почвой, раны у людей, злоупотребляющих медикаментами, и раны после кесарева сечения. Ботулизм может возникнуть, если ребенок поглощает споры и токсин высвобождается у него в кишечнике. Заражение детей ботулизмом по взрослому типу отмечается в старшем возрасте.
Клинические проявления
Пищевой ботулизм. Инкубационный период составляет 18–36 ч после употребления зараженной токсином пищи. Начало болезни связано с появлением черепномозговой симптоматики, обычно это диплопия, дизартрия и (или) дисфагия. Паралич развивается симметрично, опускается вниз и ведет к дыхательной недостаточности и смерти. До паралича или после его начала могут возникать тошнота, рвота и боли в животе. Характерны головокружение, нарушения зрения, сухость слизистой оболочки полости рта, а также сухость и боли в горле. Лихорадка нетипична.
Часто имеется птоз; фиксированные и расширенные зрачки отмечены у 50% больных. Рвотный рефлекс может быть подавлен, глубокие сухожильные рефлексы нормальны или снижены. Паралитическая непроходимость кишечника, выраженный запор, задержка мочеиспускания — все это характерно.
Раневой ботулизм. Картина этого варианта болезни сходна с наблюдаемой при пищевом ботулизме, но инкубационный период длиннее (10 дней) и не характерны нарушения ЖКТ.
Диагноз
Диагноз ставят по выявлению токсина в сыворотке крови; в то же время в присутствии явной инфекции тест может быть отрицателен, а его выполнение требует особого лабораторного оборудования. Другие биологические среды, в которых может быть обнаружен токсин, — это рвотные массы, желудочный сок и кал. Попытка выделить возбудитель из пищи диагностически несостоятельна.
Лечение
Необходимо мониторирование функций больного, особенно дыхания. При пищевой форме после получения лабораторных проб необходимо сразу же ввести трехвалентный лошадиный антитоксин (тип А, В и Е). Дозировка: два флакона (оба внутривенно или один внутривенно, другой внутримышечно). Повторная доза может потребоваться спустя 24 ч. Могут быть эффективны слабительные. Ценность антибиотиков сомнительна. При раневом ботулизме: обработка раны, бензилпенициллин (для устранения инфекции) и лошадиный антитоксин. Поддерживающая терапия применяется при ботулизме у детей.
Другие клостридиальные инфекции
Патогенез
Несмотря на частый высев клостридий из ран при серьезных травмах, частота тяжелых инфекций, обусловленных ими, невелика. В развитии тяжелой болезни определяющими являются два фактора: некроз тканей и низкий окислительновосстановительный потенциал. Клостридиальные инфекции опосредуются токсинами.
Клинические проявления
Пищевые отравления. Cl perfringens — одна из наиболее частых причин пищевых отравлений в США. Источником служат мясо при повторном его приготовлении, мясо и птицепродукты. Симптомы появляются через 8–24 ч после употребления пищи и включают боль в эпигастрии, тошноту и водную диарею длительностью 12–24 ч. Лихорадка и рвота нехарактерны.
Колит, связанный с применением антибиотиков. Продуцирующие токсины штаммы Cl. difficile, обнаруживаемые в кале, — главная причина колита у больных диареей, обусловленной применением антибиотиков. Различные противомикробные средства (включая метронидазол и ванкомицин, используемые для лечения этой инфекции) могут вызвать этот синдром, определяемый как диарея, у которой нет иных причин и возникающей в процессе антибактериального лечения или в течение 4 нед после его прекращения. Стул обычно водянистый, значителен по объему, без больших примесей крови или слизи. У многих больных отмечаются спастические боли в животе, болезненность при пальпации, лихорадка и лейкоцитоз.
Гнойная инфекция глубоких тканей. Клостридий часто обнаруживают в сочетании с другими микробами или изолированно, но обычно без общих признаков заболевания, вызываемого их токсинами. Сюда относятся: внутрибрюшной сепсис, эмпиема, абсцессы в полости малого таза, подкожные абсцессы, отморожения с газовой гангреной, инфекция культи после ампутации, абсцесс головного мозга, абсцесс предстательной железы, конъюнктивит, инфекция аортальных шунтов. Холецистит вызывается клостридиальной инфекцией, по крайней мере, в 50% случаев.
Инфекция кожи и мягких тканей. Локализованная. Проявления безболезненны, без признаков общей интоксикации и отека. Типичные поражения: целлюлит, периректальный абсцесс, диабетические язвы стоп. Газ может находиться в ране и в соседних тканях, но не в мышцах. Гнойный миозит встречается у наркоманов, применяющих героин.
Распространяющийся целлюлит. Синдром имеет острое начало с быстрым распространением гнойного процесса и газа по фасциям. Некроз мышечной ткани отсутствует, но весьма выражена токсемия, которая может быть фатальной. При осмотре находят выраженную крепитацию, местная боль выражена незначительно. Этот синдром чаще всего встречается среди больных карциномой, особенно при локализации в ситовидной или толстой кишке.
Клостридиальный мионекроз (газовая гангрена). Встречается при глубоких ранах с некрозом тканей, часто после травмы или операции. Инкубационный период всегда менее 3 сут, часто менее 24 ч. В отличие от распространяющегося целлюлита газовая гангрена начинается с внезапной боли в ране. Имеется локальный отек с незначительным геморрагическим экссудатом. Обязательны токсемия, снижение АД, почечная недостаточность и крепитация.
Клостридиалъная септицемия. Клостридиальная септицемия встречается нечасто, но она почти всегда фатальна и развивается вслед за клостридиальным инфиЦированием матки (особенно после септического аборта), толстой кишки или желчевыводящих путей. У больных развивается картина сепсиса спустя 13 дня после аборта, с лихорадкой, ознобом, слабостью, головной болью, тяжелой миалгиеи, болями в животе, тошнотой, рвотой и (иногда) диареей. Быстро, вслед за гемолизом, развиваются олигурия, снижение АД, желтуха, гемоглобинурия. Как и при газовой гангрене, больные с клостридиальной септицемией проявляют повышенную настороженность к происходящему. У больных с локализацией инфекции в кишечнике или в желчных путях заболевание часто приобретает системный характер. СреДи проявлений болезни следует назвать лихорадку, озноб, у половины больных внутрисосудистый гемолиз. У онкологических больных Cl. septicum вызывает быструю фатальную септицемию с лихорадкой, тахикардией, снижением АД, болью в животе, тошнотой, рвотой. Только у 20–30% этих больных развивается гемолиз; смерть наступает в течение 12ч.
Диагностика
Диагностика клостридиальной инфекции должна основываться прежде всего на клинической картине. Наличие газа на рентгенограмме дает врачу ключ к диагнозу, но это же встречается и при смешанной аэробноанаэробной инфекции. Диагноз клостридиального мионекроза можно поставить при исследовании препарата замороженного фрагмента мышцы. Колит, обусловленный Cl. difficile, может быть установлен при уточнении вида токсина в кале путем культуральных исследований на фоне адекватной нейтрализации антитоксином.
Лечение
Бензилпенициллин (20 млн. ЕД/сут) — антибиотик выбора при клостридиальной инфекции тканей. При аллергии к пенициллину могут быть назначены и другие антибиотики, но должна быть оценена чувствительность возбудителя к препаратам. При клостридиальном мионекрозе главным в лечении является дренирование и оперативное вмешательство на инфицированном участке. При быстром распространении инфекции по конечности молсет потребоваться ее ампутация; при мионекрозе мышц передней брюшной стенки иногда необходима повторная хирургическая обработка, а при мионекрозе матки выполняют гистерэктомию. При энтероколите, связанном с Cl. difficile, в качестве лечебной меры отменяют антибиотик, спровоцировавший осложнение. Назначают метронидазол (250 мг 4 раза или 500 мг 3 раза в сутки внутрь) или ванкомицин (125 мг 4 раза в день внутрь) на протяжении 7–10 дней, что смягчает и укорачивает проявление симптомов заболевания. Доза ванкомицина может быть увеличена до 500 мг 4 раза в сутки внутрь при тяжелом течении. В рефракторных случаях или при рецидиве в лечение вносят стратегические изменения: добавляют рифампицин к ванкомицину, уменьшают дозу ванкомицина, переходят от метронидазола или ванкомицина к альтернативным лекарственным средствам.
Смешанные анаэробные инфекции
Клинические проявления
Голова и шея. Инфекции головы и шеи, вызываемые анаэробами, включают гингивит, воспаление в глотке (включая ангину Людвига), инфекции фасциальных пространств, когда ротоглоточная микрофлора со слизистых оболочек или области стоматологического вмешательства распространяется в область головы и шеи, вызывая, в частности, отит и синусит. Осложнения этих инфекций: остеомиелит костей черепа или челюсти, внутричерепные инфекции (абсцесс головного мозга), медиастинит или плевропульмональная инфекция.
Центральная нервная система. При применении оптимальных бактериологических методов анаэробы обнаруживают в 85% случаев абсцессов головного мозга. Доминируют грамположительные анаэробные кокки; фузобактерии и Bacteroides встречаются реже.
Легкие и плевральная полость. Четыре клинических синдрома связаны с анаэробной плевролегочной инфекцией, возникающей при аспирации: аспирационная пневмония, некротизирующая пневмония, абсцесс легкого и эмпиема. Аспирационная пневмония развивается довольно медленно, с невысокой лихорадкой, слабостью, продуктивным кашлем у больных с предрасположенностью к аспирации. У больных с абсцессом легкого отмечается типичная картина лихорадки, озноб, слабость, похудание, выделение зловонной мокроты, что происходит на протяжении недель. Эмпиема плевры — проявление длительно существующей анаэробной легочной инфекции, клинически напоминает картину абсцесса легкого. Может отмечаться плевритная боль в груди и боль при пальпации участка грудной клетки. Поддиафрагмальный процесс может осложниться эмпиемой плевры.
Внутрибрюшные процессы
Малый таз. Часто анаэробная инфекция может вызвать тубоовариальный абсцесс, септический аборт, абсцессы в малом тазу, эндометрит, инфекцию послеоперационной раны, особенно после гистерэктомии.
Кожа и мягкие ткани. Иногда удается выделить анаэробы при крепитирующем целлюлите, синергическом целлюлите, гангрене, некротизирующем фасциите, кожных абсцессах, прямокишечном абсцессе, инфекции подмышечных потовых желез. Синергическая гангрена Мелени (Meleney) — прогрессирующее, очень болезненное заболевание с эритемой, отеком, индурацией, некрозом в центральной зоне. Обычно его вызывают анаэробные кокки и Staph. aureus. Хотя некротизирующий фасциит обычно вызывается стрептококками группы А, он может быть вызван и анаэробами, включая Peptostreptococcus и Bacteroides.
Кости и суставы. Анаэробный остеомиелит обычно развивается как продолжение инфекции мягких тканей; септический артрит часто имеет гематогенное происхождение.
Бактериемия. B.fragilis — единственный анаэроб, часто высеваемый из крови. В то время, как клинические проявления анаэробной бактериемии сходны с сепсисом, вызванным грамотрицательными аэробными бактериями, для первой не характерны септический тромбофлебит и септический шок.
Диагностика
Когда инфекция развивается вблизи поверхности слизистых оболочек, обычно заселенных анаэробами, их и следует рассматривать в качестве этиологических факторов. Культуры необходимо специально исследовать на наличие анаэробов, шскольку их лабораторное выделение требует времени, диагностика в ряде случаев может быть предположительной.
Лечение
Успешная терапия анаэробной инфекции требует назначения соответствующих антибиотиков, хирургической обработки очага поражения и его дренирования. При подозрении на анаэробную инфекцию почти всегда следует провести эмпирическую терапию, поскольку чувствительность возбудителя предсказуема. Бензилпенициллин целесообразен в лечении большинства оральных анаэробных инфекций и при анаэробной пневмонии. В лечении абсцесса легкого клиндамицин, повидимому, наиболее эффективен. При инфекции, связанной с B.fragilis, назначают метронидазол, но могут быть также применены клиндамицин, цефокситин, имипенем, ампициллинсульбактам, тикарциллинклавуланат. Если при анаэробной инфекции не удалось подобрать адекватную терапию, следует проанализировать клиническую ситуацию, в том числе устойчивость к антибиотикам, необходимость дополнительного дренирования очага, возможность суперинфекции аэробами.
Газовая гангрена – это чрезвычайно тяжелое инфекционное осложнение раневого процесса, которое вызывается анаэробными (размножающимися без доступа воздуха) микроорганизмами из рода клостридий. Как правило, развивается при обширных ранах с размозжением тканей. Сопровождается отечностью тканей, зловонным отделяемым, отхождением пузырьков газа и выраженной интоксикацией организма продуктами тканевого распада. Диагностируется на основании клинической картины, данных инструментальных и лабораторных исследований. Показано срочное оперативное лечение - вскрытие раны лампасными разрезами, при быстром прогрессировании процесса производят ампутацию.
МКБ-10
Общие сведения
Газовая гангрена – это очень тяжелый инфекционный процесс, который развивается в результате инфицирования ран анаэробными бактериями, обитающими в земле и уличной пыли. Особенно предрасположены к возникновению газовой гангрены пациенты с обширными ранами, сопровождающимися массивным размозжением мышечной ткани, возникновением карманов и участков с плохим кровоснабжением. Лечение патологии в зависимости от причин ее возникновения осуществляют специалисты в сфере гнойной хирургии, травматологии и ортопедии и других областях медицины.
Причины
Газовая гангрена вызывается бактериями из рода клостридий, которые в норме обитают в кишечнике травоядных домашних животных, откуда попадают в землю, уличную пыль, на одежду и т. д. В отдельных случаях обнаруживаются в фекалиях и на коже здоровых людей. Размножаются только в безкислородной среде, но в присутствии кислорода могут длительное время сохраняться в виде спор.
В 90% случаев возбудителем газовой гангрены является Clostridium perfringens, остальные приходятся на долю Cl. histolitycum, Cl. oedematiens, Cl. septicum, Cl. novii, Cl. fallax и т.д. Обычно газовая гангрена развивается в результате обширных размозженных ран и травматических отрывов конечностей, реже – в результате ранений толстого кишечника и попадания инородных тел. В отдельных случаях причиной возникновения могут стать даже небольшие раны (особенно – загрязненные обрывками одежды или частицами почвы).
Классификация
С учетом местных проявлений гнойные хирурги выделяют четыре формы газовой гангрены.
- Классическая или эмфизематозная форма. Наблюдается умеренный отек, постепенно сменяющийся омертвением тканей с выделением большого количества газа. Гной отсутствует. Раневая поверхность сухая, выявляются обширные очаги некроза. Грануляций нет, на дне виднеется омертвевшая серо-зеленая, не кровоточащая мышечная ткань с трупным запахом. При надавливании из раны выделяется газ и сукровичная жидкость. Кожа в зоне поражения холодная, бледная, покрытая буроватыми пятнами. По мере прогрессирования инфекции боли в ране сначала резко усиливаются, затем чувствительность теряется. Пульс на периферических артериях исчезает, конечность приобретает бурую окраску и омертвевает.
- Отечно-токсическая форма. Сопровождается обширным, быстро распространяющимся отеком, нарастающим буквально в течение каждой минуты. Рана без гнойного отделяемого, газ выделяется в малых количествах или отсутствует. Из-за быстро нарастающего отека мышцы сдавливаются и выбухают из раны. Подкожная клетчатка зеленоватая, желеобразная, мышечная ткань бледная, кожные покровы вокруг раны холодные, блестящие, резко напряженные. По мере развития воспаления периферический пульс исчезает, конечность становится бурой, развивается омертвение.
- Флегмонозная форма. Протекает более благоприятно, может быть развиваться на ограниченном участке. Отек окружающих тканей умеренный или незначительный, на дне раны – розовые мышцы с участками некроза. Из раны выделяется гной и пузырьки газа. Кожа вокруг раны теплая, без пятен. Пульс на периферических артериях сохранен.
- Гнилостная или путридная. Развивается в результате симбиоза анаэробных и гнилостных микроорганизмов. В отличие от других форм чаще возникает не на конечностях, а на туловище. Характеризуется молниеносным течением с бурным распадом тканей. Инфекция быстро распространяется по клетчаточным пространствам, вызывая омертвение клетчатки, мышц и фасций. Из раны выделяется газ и зловонное гнилостное отделяемое с кусочками разрушенных тканей. Присоединение гнилостной инфекции обуславливает разрушение стенок сосудов, поэтому при этой форме газовой гангрены часто наблюдаются вторичные кровотечения.
Симптомы газовой гангрены
Для патологии характерно раннее бурное начало. Симптомы обычно появляются на 1-3 день после травмы. Ткани вокруг раны отекают, появляется зловонное отделяемое с пузырьками газа. Отек стремительно распространяется на соседние участки, состояние больного быстро ухудшается, отмечаются признаки отравления организма продуктами распада тканей. Без специализированной медицинской помощи смерть наступает в течение 2-3 суток с момента начала болезни.
Особенности местных и общих проявлений зависят от вида возбудителя. Для Clostridium perfringens характерно фибринолитическое, токсико-гемолитическое и некротическое течение, для Clostridium septicum – серозно-кровянистый отек тканей, малое количество выделяемого газа и интенсивное разрушение эритроцитов. Clostridium oedematiens, напротив, образует большое количество газа и при этом также оказывает гемолитическое воздействие на организм. Clostridium histolitycum отличается особой агрессивностью по отношению к живым тканям. Всего в течение 10-12 часов она способна разрушить соединительную и мышечную ткань настолько, что будут видны кости.
Разрушение эритроцитов становится причиной быстро развивающейся анемии и гемолитической желтухи. В анализах крови выявляется снижение количества эритроцитов, снижение уровня гемоглобина, лейкоцитоз со сдвигом формулы влево и преобладанием юных форм нейтрофилов. К числу наиболее постоянных местных симптомов относится отек окружающих тканей, образование газа, разрушение мышечной ткани и отсутствие классических признаков воспаления.
Диагностика
Диагноз газовая гангрена выставляется на основании клинической картины и подтверждается дополнительными исследованиями. При изучении раневого отделяемого под микроскопом обнаруживаются клостридии. Рентгенологическое обследование подтверждает наличие газа в тканях. В процессе дифференциальной диагностики исключают фасциальную газообразующую флегмону, при которой не наблюдается разрушения мышц.
Лечение газовой гангрены
Лечение включает в себя неотложное оперативное лечение в сочетании с активной общей терапией. Рану широко вскрывают лампасными разрезами (широкими продольными разрезами на протяжении всего сегмента, включающими в себя разрез кожи, подкожной клетчатки и собственной фасции). Все нежизнеспособные ткани иссекают, рану промывают раствором перекиси водорода. При наличии подозрительных участков на соседних сегментах там также производят лампасные разрезы.
Раны обязательно оставляют открытыми и рыхло дренируют марлей, пропитанной раствором марганцовки или перекиси водорода. В течение первых 2-3 суток перевязки производятся 2-3 раза в день, в дальнейшем – ежедневно. При быстром прогрессировании, вовлечении в процесс всех мягких тканей и омертвении конечности выполняется ампутация или экзартикуляция. Ампутация проводится гильотинным способом, с отсечением всех слоев на одном уровне. Рану оставляют открытой, на культе выполняют лампасные разрезы, раны дренируют, используя марлю, смоченную в растворе перманганата калия или перекиси водорода.
Сразу после постановки диагноза начинают массивную инфузионную терапию с использованием плазмы, альбумина, растворов белков и электролитов. При анемии проводят переливание крови. Антибиотики вводят в высоких дозах внутриартериально или внутривенно. В послеоперационном периоде пациентам назначают гипербарическую оксигенацию. Выполняют внутривенное введение противогангренозной сыворотки. При установленном возбудителе используют моновалентную сыворотку, при неустановленном – поливалентную.
Прогноз и профилактика
Основным средством профилактики газовой гангрены является адекватная своевременная первичная обработка раневой поверхности и назначение антибиотиков широкого спектра действия. В процессе обработки должны быть иссечены все нежизнеспособные ткани, а также дно и края раны. Следует помнить, что антибиотикотерапия обязательна при любых обширных ранах, особенно – обильно загрязненных и сопровождающихся размозжением тканей. Профилактическое использование противогангренозных сывороток недостаточно эффективно и может стать причиной развития анафилактического шока.
Пациентов с газовой гангреной изолируют, выделяют им отдельный сестринский пост, перевязочный материал немедленно сжигают, инструменты и белье подвергают специальной обработке. Споры клостридий обладают высокой устойчивостью к кипячению, поэтому инструмент следует обрабатывать в условиях повышенного давления в паровом стерилизаторе либо в сухожаровом шкафу. Любые медицинские мероприятия необходимо проводить в резиновых перчатках, которые по окончании процедуры сжигают или погружают в дезинфицирующий состав (лизол, карболовую кислоту, хлорамин).
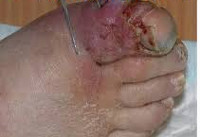
Анаэробная инфекция – это инфекционный процесс, вызываемый спорообразующими или неспорообразующими микроорганизмами в условиях, благоприятных для их жизнедеятельности. Характерными клиническими признаками анаэробной инфекции служат преобладание симптомов эндогенной интоксикации над местными проявлениями, гнилостный характер экссудата, газообразующие процессы в ране, быстро прогрессирующий некроз тканей. Анаэробная инфекция распознается на основании клинической картины, подтвержденной результатами микробиологической диагностики, газожидкостной хроматографии, масс-спектрометрии, иммуноэлектрофореза, ПЦР, ИФА и др. Лечение анаэробной инфекции предполагает радикальную хирургическую обработку гнойного очага, интенсивную дезинтоксикационную и антибактериальную терапию.
МКБ-10
Общие сведения
Анаэробная инфекция – патологический процесс, возбудителями которого выступают анаэробные бактерии, развивающиеся в условиях аноксии (отсутствия кислорода) или гипоксии (низкого напряжения кислорода). Анаэробная инфекция представляет собой тяжелую форму инфекционного процесса, сопровождающуюся поражением жизненно важных органов и высоким процентом летальности. В клинической практике с анаэробной инфекцией приходится сталкиваться специалистам в области хирургии, травматологии, педиатрии, нейрохиругии, отоларингологии, стоматологии, пульмонологии, гинекологии и других медицинских направлений. Анаэробная инфекция может возникнуть у пациентов любого возраста. Доля заболеваний, вызываемых анаэробной инфекцией, точно не известна; из гнойных очагов в мягких тканях, костях или суставах анаэробы высеваются примерно в 30% случаев; анаэробная бактериемия подтверждается в 2-5% случаев.

Причины
Анаэробы входят в состав нормальной микрофлоры кожи, слизистых оболочек, желудочно-кишечного тракта, органов мочеполовой системы и по своим вирулентным свойствам являются условно-патогенными. При определенных условиях они становятся возбудителями эндогенной анаэробной инфекции. Экзогенные анаэробы присутствуют в почве и разлагающихся органических массах и вызывают патологический процесс при попадании в рану извне. Анаэробные микроорганизмы делятся на:
- Факультативные. Способны выживать как в отсутствии, так и в присутствии кислорода. К ним принадлежат кишечная палочка, шигеллы, иерсинии, стрептококки, стафилококки и др.
- Облигатные. Их развитие и размножение осуществляется в бескислородной среде. Облигатные возбудители делятся на две группы:
- спорообразующие (клостридии) - являются возбудителями клостридиозов экзогенного происхождения (столбняка, газовой гангрены, ботулизма, пищевых токсикоинфекций и др.);
- неспорообразующие (неклостридиальные) анаэробы (фузобактерии, бактероиды, вейллонеллы, пропионибактерии, пептострептококки и др.). В большинстве случаев вызывают гнойно-воспалительные процессы эндогенной природы (абсцессы внутренних органов, перитонит, пневмонию, флегмоны челюстно-лицевой области, отит, сепсис и др.).
Факторы риска
Условиями, благоприятствующими развитию анаэробной инфекции, являются повреждение анатомических барьеров с проникновением анаэробов в ткани и кровеносное русло, а также снижение окислительно-восстановительного потенциала тканей (ишемия, кровотечение, некроз). Попадание анаэробов в ткани может происходить при оперативных вмешательствах, инвазивных манипуляциях (пункциях, биопсии, экстракции зуба и др.), перфорации внутренних органов, открытых травмах, ранениях, ожогах, укусах животных, синдроме длительного сдавления, криминальных абортах и т. д. Факторами, способствующими возникновению анаэробной инфекции, выступают:
- массивное загрязнение ран землей;
- наличие инородных тел в ране;
- гиповолемический и травматический шок;
- сопутствующие заболевания (коллагенозы, сахарный диабет, опухоли);
- иммунодефицит.
Кроме этого, большое значение имеет нерациональная антибиотикотерапия, направленная на подавление сопутствующей аэробной микрофлоры.
Патогенез
Основными факторами патогенности анаэробных микроорганизмов служат их количество в патологическом очаге, биологические свойства возбудителей, наличие бактерий-ассоциантов. В патогенезе анаэробной инфекции ведущая роль принадлежит продуцируемым микроорганизмами ферментам, эндо- и экзотоксинам, неспецифическим факторам метаболизма. Так, ферменты (гепариназа, гиалуронидаза, коллагеназа, дезоксирибонуклеаза) способны усиливать вирулентность анаэробов, деструкцию мышечной и соединительной тканей.
Эндо- и экзотоксины вызывают повреждение эндотелия сосудов, внутрисосудистый гемолиз и тромбоз. Кроме этого, некоторые клостридиальные токисины обладают нефротропным, нейротропным, кардиотропным действием. Также токсическое влияние на организм оказывают и неспецифические факторы метаболизма анаэробов - индол, жирные кислоты, сероводород, аммиак.
Классификация
В зависимости от локализации различают анаэробную инфекцию:
- центральной нервной системы (абсцесс мозга, менингит, субдуральная эмпиема и др.)
- головы и шеи (пародонтальный абсцесс, ангина Людвига, средний отит, синусит, флегмона шеи и т. д.)
- дыхательных путей и плевры (аспирационная пневмония, абсцесс легкого, эмпиема плевры и пр.)
- женской половой системы (сальпингит, аднексит, эндометрит, пельвиоперитонит)
- брюшной полости (абсцесс брюшной полости, перитонит)
- кожи и мягких тканей (клостридиальный целлюлит, газовая гангрена, некротизирующий фасциит, абсцессы и др.)
- костей и суставов (остеомиелит, гнойный артрит)
- бактериемию.
Течение анаэробной инфекции может быть молниеносным (в течение 1 суток с момента операции или травмы), острым (в течение 3-4 суток), подострым (более 4 суток).
Симптомы анаэробной инфекции
Независимо от вида возбудителя и локализации инфекционного очага, различным клиническим формам свойственны некоторые общие черты. В большинстве случаев анаэробная инфекция имеет острое начало и характеризуется сочетанием местных и общих симптомов. Инкубационный период может составлять от нескольких часов до нескольких суток (в среднем около 3-х дней).
Типичным признаком анаэробной инфекции служит преобладание симптомов общей интоксикации над местными воспалительными явлениями. Резкое ухудшение общего состояния больного обычно наступает еще до возникновения локальных симптомов. Проявлением тяжелого эндотоксикоза служит высокая лихорадка с ознобами, выраженная слабость, тошнота, головная боль, заторможенность. Характерны артериальная гипотония, тахипноэ, тахикардия, гемолитическая анемия, иктеричность кожи и склер, акроцианоз.
При раневой анаэробной инфекции ранним местным симптомом выступает сильная, нарастающая боль распирающего характера, эмфизема и крепитация мягких тканей, обусловленные газообразующими процессами в ране. К числу постоянных признаков относится зловонный ихорозный запах экссудата, связанный с выделением азота, водорода и метана при анаэробном окислении белкового субстрата. Экссудат имеет жидкую консистенцию, серозно-геморрагический, гнойно-геморрагический или гнойный характер, неоднородную окраску с вкраплениями жира и наличием пузырьков газа. На гнилостный характер воспаления также указывает внешний вид раны, содержащей ткани серо-зеленого или серо-коричневого цвета, иногда струпы черного цвета.
Осложнения
Анаэробная инфекция часто сопровождается развитием полиорганной недостаточности (почечной, печеночной, сердечно-легочной), инфекционно-токсического шока, тяжелого сепсиса, являющихся причиной летального исхода.
Диагностика
Для своевременной диагностики анаэробной инфекции большое значение имеет правильная оценка клинических симптомов, позволяющая своевременно оказать необходимую медицинскую помощь. В зависимости от локализации инфекционного очага диагностикой и лечением анаэробной инфекции могут заниматься клиницисты различных специальностей – общие хирурги, травматологи, нейрохирурги, гинекологи, отоларингологи, челюстно-лицевые и торакальные хирурги. С целью определения патогенного агента и тяжести инфекционного процесса используют:
- Методы детекции возбудителя. Методы экспресс-диагностики анаэробной инфекции включают бактериоскопию раневого отделяемого с окраской мазка по Грамму и газожидкостную хроматографию. В верификации возбудителя ведущая роль принадлежит бактериологическому посеву отделяемого раны или содержимого абсцесса, анализу плевральной жидкости, посеву крови на аэробные и анаэробные бактерии, иммуноферментному анализу, ПЦР.
- Другие анализы. В биохимических показателях крови при анаэробной инфекции обнаруживается снижение концентрации белков, увеличение уровня креатинина, мочевины, билирубина, активности трансаминаз и щелочной фосфатазы.
- Инструментальную диагностику. Наряду с клиническими и лабораторными исследования, выполняется рентгенография, при которой обнаруживается скопление газа в пораженных тканях или полостях.
Анаэробную инфекцию необходимо дифференцировать от рожистого воспаления мягких тканей, полиморфной экссудативной эритемы, тромбоза глубоких вен, пневмоторакса, пневмоперитонеума, перфорации полых органов брюшной полости.
Лечение анаэробной инфекции
Комплексный подход к лечению анаэробной инфекции предполагает проведение радикальной хирургической обработки гнойного очага, интенсивной дезинтоксикационной и антибактериальной терапии. Хирургический этап должен быть выполнен как можно раньше – от этого зависит жизнь больного. Как правило, он заключается в широком рассечении очага поражения с удалением некротизированных тканей, декомпрессии окружающих тканей, открытом дренировании с промыванием полостей и ран растворами антисептиков. Особенности течения анаэробной инфекции нередко требуют проведения повторных некрэктомий, раскрытия гнойных карманов, обработки ран ультразвуком и лазером, озонотерапии и т. д. При обширной деструкции тканей может быть показана ампутация или экзартикуляция конечности.
Важнейшими составляющими лечения анаэробной инфекции являются интенсивная инфузионная терапия и антибиотикотерапия препаратами широкого спектра действия, высокотропными к анаэробам. В рамках комплексного лечения анаэробной инфекции находят свое применение гипербарическая оксигенация, УФОК, экстракорпоральная гемокоррекция (гемосорбция, плазмаферез и др.). При необходимости пациенту вводится антитоксическая противогангренозная сыворотка.
Прогноз и профилактика
Исход анаэробной инфекции во многом зависит от клинической формы патологического процесса, преморбидного фона, своевременности установления диагноза и начала лечения. Уровень летальности при некоторых формах анаэробной инфекции превышает 20%. Профилактика анаэробной инфекции заключается в своевременной и адекватной ПХО ран, удалении инородных тел мягких тканей, соблюдении требований асептики и антисептики при проведении операций. При обширных раневых повреждениях и высоком риске развития анаэробной инфекции необходимо проведение специфической иммунизации и противомикробной профилактики.

Обзор
Бактерии, продуцирующие один из самых опасных ядов, могут жить прямо на вашей кухонной полке — в консервах и солениях — и приводить к серьезному заболеванию — ботулизму
Авторы
Редакторы

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.









Постер также доступен в формате pdf.
Ботулизм
Смертность
Несмотря на то, что BoNT — это мощный яд, предубеждение о том, что каждый или почти каждый случай возникновения ботулизма окажется смертельным, неверно. Статистически смертность от ботулизма очень низкая — так же, как и случаи заражения в целом. Около пятидесяти лет назад на каждые 100 человек с ботулизмом приходилось около 50 смертей. Однако, благодаря появлению анатоксина и надлежащему уходу за пациентами, сегодня смертность от ботулизма сократилась до 5 (и меньше) случаев на 100 заболевших [1].
История
Возбудители ботулизма
Ботулизм наиболее часто бывает вызван бактериями Clostridium botulinum. Вызывают его и другие клостридии: Clostridium butyricum и Clostridium baratii.
Clostridium botulinum — грамположительная бактерия в форме палочки (бацилла). Бациллы по своей природе способны к спорообразованию, что позволяет таким бактериям долгое время оставаться живыми даже в очень неблагоприятных условиях. В виде спор Clostridium botulinum не производят токсинов и абсолютно безопасны для взрослого человека. Когда же спора прорастает, бактерия начинает активно размножаться и выделять токсин.
- анаэробные (без O2);
- низкая кислотность среды: pH 7,3-7,6 для роста и 6,0-7,2 для прорастания спор;
- низкий уровень углеводов;
- низкая соленость среды;
- определенная температура — около 4–45°C.
Из-за необходимости бескислородной среды для жизнедеятельности Clostridium botulinum BoNT чаще всего можно найти в консервах.
Где прячется ботулизм, типы ботулизма
Существует несколько типов ботулизма:
BoNT — белок (150 кДа), имеет легкую и тяжелую цепи. Каждая цепь выполняет свою функцию при интоксикации организма [1].
Существует семь различных нейротоксинов BoNT: от А до H. Каждый из них связан с возникновением той или иной формы ботулизма. Ботулотоксины А, В, Е и иногда F опасны для человека [2].
Воздействие токсина, синаптическая передача, молекулярные механизмы
Тяжелая цепь BoNT’а ищет специфические рецепторы на поверхности нейронов-мишеней и способствует проникновению токсина внутрь клеток. Легкая цепь, попав внутрь, нарушает действие комплекса белков SNARE, участвующих в высвобождении медиаторов из окончаний двигательных нейронов. Чаще всего в качестве медиатора выступает ацетилхолин , [4]. При нарушении его высвобождения происходит блокирование передачи нервно-мышечного импульса. Когда нерв не может передать сигнал, чтобы заставить мышцу двигаться, мышца парализуется [5–7]. Вместе с кровью токсин распространяется по всему организму, парализуя многие мышцы одновременно.
Ацетилхолин — важный медиатор, который выделяется в синаптическую щель между нейронами и осуществляет дальнейшую передачу импульса.
Симптомы заболевания
Ботулизм начинает проявляться после инкубационного периода, который может длиться от 12 часов до 10–15 дней. Приводит к мышечному параличу. В первичной стадии интоксикации задействованы черепные нервы и мышцы лица, именно поэтому паралич начинается с верхней части туловища человека и распространяется вниз, поражая мышцы шеи, груди, рук и ног.
У отравленного человека:
- расширяются зрачки;
- туманится зрение;
- возникают мушки перед глазами;
- нарушается речь;
- становится трудно глотать;
- мышцы лица теряют подвижность, поэтому лицо начинает напоминать застывшую маску.
В конце концов, если паралич добирается до дыхательных мышц и мышц сердца — человек умирает.
Диагностика
В поисках ботулотоксина, антител к возбудителю или ДНК возбудителя у пациента собирают материал (мочу, кал, рвотные массы или кровь) и проводят клинические и лабораторные исследования. Важным методом подтверждения ботулизма является демонстрация действия токсина на мышах. Для этого из материала пациента выделяют бактерии и вводят их мышам. При наличии ботулотоксинов у мышей через 48 часов развивается паралич, который может быть подавлен введением анатоксина [12].
Лечение
Лечение ботулизма включает:
- обеззараживание желудочно-кишечного тракта (если это необходимо);
- введение антидота (анатоксина);
- при легочной недостаточности применяют респираторную поддержку (ИВЛ).
Анатоксин нейтрализует только еще не связанные с нервными окончаниями, свободно циркулирующие в крови токсины. Как только BoNT связывается с нервными окончаниями, анатоксин становится бесполезен [2], [5].
Даже после длительного лечения большинство пациентов имеют остаточные симптомы, а процесс восстановления может занять месяцы. Скорость восстановления зависит от скорости прорастания новых веточек моторных аксонов [1].
В качестве профилактики можно проводить вакцинацию против ботулизма. Вакцинацию применяют редко, потому что эффект вакцины непродолжителен. Она обеспечивает лишь временный иммунитет и требует повторного введения [13].
Терапевтическое использование BoNT
Несмотря на все опасные воздействия на организм человека, BoNT широко применяется в медицине и косметологии. Врачи используют способность BoNT’а вызывать вялый паралич.
В медицине BoNT помогает устранять неврологические расстройства — дистонию, спастичность, косоглазие и другие, а также лечить мигрень и гиперактивный мочевой пузырь [8].
Кристина В. и Тома П. работали над написанием текста. Екатерина Б. создала эти замечательные иллюстрации, за что ей отдельное спасибо! Тема статьи была задумана Кристиной В. Редактированием текста, рисунков и созданием постеров также занимались Кристина В. и Тома П.
Читайте также:

