Чем лечатся гнойные инфекции
Обновлено: 25.04.2024
Инфекции верхних дыхательных путей (ИВДП) включают поражение слизистой оболочки респираторного тракта от полости носа до трахеобронхиального дерева, за исключением терминальных бронхиол и альвеол. В связи с тем, что большинство
Инфекции верхних дыхательных путей (ИВДП) включают поражение слизистой оболочки респираторного тракта от полости носа до трахеобронхиального дерева, за исключением терминальных бронхиол и альвеол. В связи с тем, что большинство ИВДП изначально имеют вирусную природу, потенциал применения антибактериальных препаратов (АП) ограничен. Каждый случай назначения АП должен рассматриваться индивидуально. Подобный подход предполагает выделение случаев заболевания, при которых эффект антибактериальной терапии (АТ) преобладает над еe неблагоприятными последствиями.
Диагностика
Диагностическая значимость признаков риносинусита изучена в исследовании J. Williams и M. Lindbaek таблица. Последний выделил четыре симптома, с высокой степенью достоверности прогнозирующие заболевание. К ним относились: двухфазное течение заболевания, гнойная ринорея, гнойное содержимое в полости носа и скорость оседания эритроцитов (СОЭ) > 10 мм/ч. При наличии трех из четырех симптомов специфичность теста составила 81% при чувствительности 66%. В то же время для такого признака, как перимаксиллярный отeк, характерна специфичность 99%. Большинство же других симптомов, выявляемых при осмотре, характеризуются низкой прогностической ценностью.
Диагностика риносинусита строится преимущественно на клинических, анамнестических и лабораторных данных. В то же время частое выявление рентгенологических признаков риносинусита при ОРВИ ограничивает возможности лучевых методов исследования. Именно поэтому рентгенография исключена из перечня рутинных методов диагностики неосложнeнных форм риносинусита. Применение лучевых методов исследования в подавляющем большинстве нецелесообразно и по причине необоснованного повышения стоимости лечения.
Классификация
Согласно методическим рекомендациям, утверждeнным комиссией по антибиотической политике при Министерстве здравоохранения РФ и Российской академией медицинских наук, Межрегиональной ассоциацией по клинической микробиологии и антимикробной химиотерапии, принята классификация, выделяющая:
- Острый синусит ( < 3 мес).
- Рецидивирующий острый синусит (2–4 случая острого синусита за год).
- Хронический синусит (> 3 мес).
- Обострение хронического синусита (усиление имеющихся и/или появление новых симптомов).
В целях оптимизации лечебной тактики можно также предложить выделение следующих форм риносинуситов:
- По месту развития:
A.1. Внебольничный.
A.2. Нозокомиальный. - По длительности сохранения симптомов:
B.1. Острый (длительность < 4 нед).
B.2. Подострый (4–12 нед).
B.3. Хронический (> 12 нед, или ≥ 4 случаев острого рецидивирующего риносинусита длительностью > 7–10 сут при условии сохранения остаточных явлений в синусе через 4 нед после окончания терапии). - По преморбидному фону:
C.1. Риносинусит у лиц с нормальным иммунным статусом.
C.2. Риносинусит у лиц с иммуносупрессией.
C.2.1. Гуморальный иммунодефицит.
C.2.2. Клеточный иммунодефицит.
Вышеприведенные замечания к классификации были представлены в согласительных рекомендациях Американской академии оториноларингологии, Фонда хирургии головы и шеи, а также некоторых других обществ. Синусит подразделяется на четыре категории: острый (бактериальный) риносинусит, хронический риносинусит без полипов, хронический риносинусит с полипами и аллергический грибковый синусит. По мнению зарубежных специалистов, обновлeнная классификация позволяет более прицельно осуществлять лечение заболевания, однако обсуждение еe преимуществ выходит за рамки настоящей статьи.
Тактика АТ риносинусита, как и других инфекций респираторного тракта, зависит от тяжести течения заболевания и осложнений. Степень тяжести оценивается по совокупности симптомов. Например, при подозрении на орбитальные или внутричерепные осложнения течение всегда расценивается как тяжeлое, независимо от выраженности других симптомов.
По тяжести течения выделяют:
- лeгкое течение — заложенность носа, слизистые или слизисто-гнойные выделения из носа и/или в ротоглотку, повышение температуры тела до 37,5 °С, головная боль, слабость, гипосмия; на рентгенограмме околоносовых синусов — толщина слизистой оболочки менее 6 мм;
- среднетяжелое — заложенность носа, гнойные выделения из носа и/или в ротоглотку, температура тела выше 37,5 °С, боль и болезненность при пальпации в проекции синуса, головная боль, гипосмия, недомогание, могут быть иррадиирующие боли в зубы, уши; на рентгенограмме околоносовых синусов — утолщение слизистой оболочки более 6 мм, полное затемнение или уровень жидкости в одном или двух синусах;
- тяжeлое — заложенность, часто обильные гнойные выделения из носа и/или в ротоглотку (но может быть их полное отсутствие), температура тела выше 38 °С, сильная болезненность при пальпации в проекции синуса, головная боль, аносмия, выраженная слабость; на рентгенограмме околоносовых синусов — полное затемнение или уровень жидкости более чем в двух синусах; анализ крови: лейкоцитоз, сдвиг лейкоцитарной формулы влево, увеличение СОЭ; орбитальные, внутричерепные осложнения или подозрение на них. Крайне серьeзным осложнением является тромбоз кавернозного синуса, летальность при котором достигает 30% и не зависит от адекватности антибактериальной терапии.
Стандартом этиологической диагностики риносинусита является бактериологическое исследование аспирата, полученного при пункции синуса. Диагностически значимый титр составляет 10 5 КОЕ/мл. Возбудителя удаeтся выделить в 60% случаев; по некоторым данным, в 20–30% случаев определяется полимикробная этиология. Последняя более свойственна подострому и хроническому течению заболевания.
Имеется тесная зависимость роли возбудителей от варианта течения заболевания: при остром риносинусите и обострении хронического риносинусита основное значение имеют Streptococcus (Str.) pneumoniae (20–35%) и aemophilus (H.) influenzae (нетипируемые штаммы, 6–26%). Более тяжeлые случаи заболевания чаще связаны со Str. pneumoniae. Гораздо реже причиной риносинусита являются Moraxella (M.) catarrhalis (и другие грамотрицательные бациллы, 0–24%), Str. pyogenes (1–3%; до 20% у детей), Staphylococcus (S.) аureus (0–8%), анаэробы (0–10%). Роль грамотрицательных бактерий (Pseudomonas aeruginosa, Klebsiella pneumoniae, Escherichia coli, Proteus spp., Enterobacter spp., Citrobacter) при остром синусите минимальна, но возрастает при нозокомиальном инфицировании, а также у лиц с иммуносупрессией (нейтропения, СПИД) и лиц, получавших повторные курсы антибактериальной терапии. Возбудителями одонтогенного (5–10% от всех случаев гайморита) верхнечелюстного синусита являются: H. influenzae, реже Str. pneumoniae, энтеробактерии и неспорообразующие анаэробы.
Терапия
АП в сочетании с назальными и/или системными противоотeчными средствами, в том числе и интраназальными стероидами и орошением слизистой носа физиологическим раствором, занимают основное место в терапии острого, а также при обострении хронического, риносинусита. Применяются антихолинергические препараты: ипратропия бромид; местные деконгестанты: оксиметазолина гидрохлорид; системные деконгестанты: фенилпропаноламина гидрохлорид; комбинация псевдоэфедрина гидрохлорид + ацетаминофен. По показаниям (например, в целях этиологической диагностики, особенно при неэффективности терапии на 3-и сутки, подозрении на микоз; при выраженном болевом синдроме, требующем декомпрессии синуса и т. д.) применяются пункция синусов и другие методы лечения.
Заблуждением является назначение (при отсутствии явных признаков аллергического риносинусита) антигистаминных препаратов, способствующих увеличению вязкости секрета и затруднению дренажа пазух. Ещe одна ошибка заключается в профилактическом назначении АП пациентам с ОРВИ в первые сутки манифестации риносинусита. Попытка предотвращения бактериальных осложнений, в том числе и со стороны синусов, лишена смысла.
Антибактериальная терапия. Главная цель АТ состоит:
- в эрадикации возбудителя и восстановлении стерильности синуса;
- сокращении риска хронизации (на настоящий момент недостаточно данных, доказывающих способность АТ предотвращать переход процесса в хроническую форму или предупреждать развитие серьeзных осложнений);
- предотвращении осложнений;
- облегчении клинической симптоматики.
В первые дни болезни, когда наиболее вероятной причиной заболевания являются вирусы, в частности респираторно-синцитиальный вирус, назначения АП не требуется. При сохранении симптомов риносинусита > 7–10 сут, у 60% пациентов можно предполагать наличие бактериальной инфекции. Именно в пределах данной группы целесообразно проведение АТ. Последняя может начинаться и раньше. Основанием для этого служит лихорадка и цефалгия, плохо поддающиеся действию анальгетиков.
При лeгком и среднетяжeлом течении острого риносинусита терапия одинаковая. Препаратом выбора является амоксициллин. Учитывая вариабельность всасывания препарата, для обеспечения качественного лечения представляется целесообразным применение микроионизированной формы, обеспечивающей постоянство абсорбции на уровне 93% (солютаб). Длительность терапии — 7–14 сут. В случае эпидемиологической значимости (предлагается > 5% от выделяемых штаммов) пенициллиноустойчивых Str. pneumoniae минимальная подавляющая концентрация (МПК) пенициллина — 0,12–2,0 мг/л, доза амоксициллина составляет 3 г/сут. В этом случае преимущество высокоадсорбируемой растворимой формы очевидно.
Если в большинстве случаев амоксициллин является адекватным средством терапии острого риносинусита, то в случае подострого течения, как и при наличии нижеперечисленных признаков, требуется применение ингибиторозащищeнных аминопенициллинов (амоксициллин/клавуланат).
К факторам, требующим применения ингибиторозащищeнных аминопенициллинов, относятся:
- применение АП в предшествующий месяц;
- неблагоприятная эпидемиологическая ситуация (резистентность);
- курение;
- данные анамнеза о неэффективности предыдущего (если было) лечения;
- посещение детских дошкольных учреждений;
- возраст менее 2 лет;
- аллергия к амоксициллину;
- поражение лобных или сфеноидальных синусов;
- осложнeнный этмоидальный синусит;
- длительность симптомов > 30 сут.
К альтернативным, не менее эффективным препаратам, применяемым при непереносимости аминопенициллинов, относят:
- макролиды (азитромицин, кларитромицин);
- цефуроксим аксетил, цефпрозил, цефподоксим проксетил;
- доксициклин (применение ограничено в связи с ростом устойчивости пневмококка в России).
Относительно роли цефалоспоринов необходимо отметить следующее. Накапливается всe больше данных о взаимосвязи между уровнем потребления АП и уровнем резистентности микроорганизмов. В аналитическом обзоре J. Granizo продемонстрировано неблагоприятное влияние оральных цефалоспоринов на распространение резистентных к пенициллину штаммов Str. pneumoniae. Поэтому их применение, при наличии амоксициллина (амоксициллина/клавуланата) и современных макролидов, следует ограничивать случаями неэффективности АТ макролидами и непереносимости амоксициллина.
Препараты, применяемые при тяжелом течении риносинусита, вводятся внутривенно. При появлении признаков улучшения, наблюдаемого на 3–5-е сутки, практикуется переход на пероральную форму того же препарата (или амоксициллина/клавуланата при применении цефалоспоринов III поколения). Ступенчатая терапия эффективна, безопасна и позволяет сократить стоимость лечения.
Основными препаратами для лечения тяжeлых форм риносинусита являются:
- ингибиторозащищенные пенициллины (амоксициллин/клавуланат, предпочтительна микроионизированная растворимая форма солютаб);
- цефалоспорины III поколения (цефтриаксон, цефотаксим);
- при аллергии к β-лактамам — левофлоксацин, моксифлоксацин или хлорамфеникол парентерально.
При развитии осложнений со стороны центральной нервной системы (ЦНС) следует отдавать предпочтение цефтриаксону (2–4 г/сут в 2 приема) или цефотаксиму (12 г/сут в 4 приема). При развитии менингита, вызванного резистентными Str. pneumoniae (МПК ≥ 0,12 мкг/мл), дополнительно вводится ванкомицин (2 г/сут в 4 приема). Не исключено применение моксифлоксацина, однако данных, подтверждающих безопасность его применения, недостаточно.
Препараты, применяемые при неэффективности АТ
- При неэффективности амоксициллина или макролидов — амоксициллин/клавуланат или цефалоспорины III поколения;
- при неэффективности ингибиторозащищeнных аминопенициллинов и цефалоспоринов — респираторные фторхинолоны (левофлоксацин, моксифлоксацин) + компьютерная томография/эндоскопия/пункция придаточных пазух для исключения микоза.
В последнее время большие надежды в лечении синуситов, вызванных пенициллиноустойчивыми (МПК > 4 мг/л) пневмококками, возлагаются на респираторные фторхинолоны (гемифлоксацин, моксифлоксацин). Активность препаратов распространяется на пенициллиноустойчивые штаммы Str. pneumoniae, β-лактамазопродуцирующие штаммы H. influenzae, M. catarrhalis, а также на атипичные и анаэробные микроорганизмы.
Как видно, спектр применяемых в лечении синуситов АП представлен весьма широко, и достаточно сложно найти ту грань, когда оправдано применение аминопенициллинов, а когда следует выбрать их ингибиторозащищeнные формы, цефалоспорины или фторхинолоны. Существенную помощь в разрешении этой проблемы могут оказать выводы контролируемых исследований и метаанализов.
Согласно их данным, при нетяжeлых формах заболевания новые АП демонстрируют незначительное преимущество при сравнении с амоксициллином, тем более с его микроионизированной формой, а также с бензилпенициллином при лечении острых неосложнeнных синуситов. Такой вывод соответствует и результатам ретроспективного фармакоэпидемиологического исследования, выполненного в США. Общая эффективность терапии препаратами первой линии у 17329 пациентов оказалась несколько меньшей и составила 90,1%. В то же время у 11773 пациентов, получавших альтернативную терапию, эффект получен в 90,8% случаев. Разница составила 0,7% (95% доверительный интервал, 0,01%–1,40%; p < 0,05). Причиной такого положения дел является присутствие в исследуемых группах лиц, инфекционный процесс у которых мог бы разрешиться и без АТ, так как в 2/3 случаев острого заболевания наблюдается тенденция к спонтанному разрешению.
Оценка качества проводимой терапии. В период первичного осмотра и назначения терапии пациент должен быть проинформирован о возможных вариантах течения заболевания. В большинстве случаев процесс своевременно разрешается и дополнительных врачебных осмотров не требуется.
В случае отсутствия улучшения в первые 3 сут применения АТ осуществляется переход на ингибиторозащищeнный аминопенициллин (предпочтительнее форма солютаб) или макролид.
В этом же случае, как и при ухудшении состояния в любой момент терапии, ведeтся поиск причин ее неэффективности. Чаще всего к ним относятся: некомплаентность пациента, развитие внутричерепных осложнений, ошибочный диагноз, резистентность возбудителя к применяемому препарату (грибы, продукция β-лактамаз).
Причины неэффективности. При вирусной инфекции основными причинами неэффективности АТ неосложнeнного риносинусита является раннее начало терапии, до момента присоединения бактериальной инфекции (как правило, в первую неделю после появления симптомов ОРВИ).
Неэффективность терапии острых бактериальных риносинуситов при назначении незащищeнных пенициллинов может объясняться продукцией β-лактамаз H. influenzae и M. catarrhalis. Характерной причиной неудач при назначении доксициклина и макролидов является распространение устойчивых штаммов Str. pneumoniae и H. influenzae.
Особого внимания требует неэффективность терапии, связанная с нечeтким следованием пациента предписанному режиму терапии (некомплаентность). Чаще всего это отказ от продолжения терапии при первых признаках улучшения, наблюдаемых к 3-м суткам терапии, а также пропуск очередной дозы и/или сокращение частоты приeма препарата. В результате недооценки этих причин нередко назначается терапия ингибиторозащищeнными аминопенициллинами, цефалоспоринами и фторхинолонами.
Известно, что лучшая комплаентность наблюдается при применении препаратов, принимаемых 1 раз в сутки. Это подтверждено результатом недавно выполненного систематического анализа, показавшего комплаентность при применении препарата 1 раз в сутки в пределах 79 ± 14%, 2 раза в сутки — 69 ± 15%, 3 раза в сутки — 65 ± 16% и 4 раза в сутки — 51 ± 20%. В данном случае различие между первыми двумя режимами было статистически недостоверно. Характерно, что комплаентность при лечении инфекций респираторного тракта гораздо выше и достигает 97% (например, при использовании азитромицина). Применение макролидов, по данным сравнительных исследований, вообще характеризуется наилучшей комплаентностью.
Очень часто АП назначаются без явных показаний. Объяснением в большинстве случаев служит личный опыт, подтверждающий увеличение частоты повторных визитов в случае неприменения АТ. Ряд исследований отрицает подобную точку зрения. Оказалось, что пациенты, имеющие хороший контакт с врачом, уяснившие возможные варианты течения заболевания и не получающие АТ, без необходимости не приходят на прием повторно. Более того, не отмечено и увеличения случаев неудовлетворeнности лечением.
Длительность терапии зависит от формы и степени тяжести течения болезни. При остром синусите лечение продолжается от 1 сут (азитромицин 2 г — микросферическая форма) до 3–10 дней.
Выводы
- Симптомы риносинусита чаще всего обусловлены вирусной инфекцией.
- Основные возбудители бактериального риносинусита — Str. pneumoniae, H. influenzae и M. catarrhalis (чаще у детей).
- Диагностика бактериального риносинусита необходима для ограничения применения АП.
- Диагностика базируется на клинических и лабораторных критериях.
- Вероятность бактериального риносинусита возрастает при длительности симптомов > 10 сут.
- Ошибочно рутинное применение при неосложнeнных формах заболевания лучевых методов исследования.
- Культуральное исследование, цель: получение локальных данных по резистентности возбудителей и оценка возможной причины неэффективности терапии.
- АТ показана при бактериальном риносинусите.
- Амоксициллин — препарат выбора, альтернативное средство — амоксициллин/клавуланат (сульбактам), азитромицин, кларитромицин.
- Применение коротких курсов терапии, препаратов с однократным суточным приeмом и максимальной степенью всасывания активных ингредиентов предпочтительно, так как повышает комплаентность пациента, снижая риск нежелательных реакций.
По вопросам литературы обращайтесь в редакцию.
И. А. Гучев, кандидат медицинских наук
А. А. Колосов
421-й военный госпиталь МВО МО РФ, Смоленск
Лечение при гнойной инфекции. Консервативное лечение гнойной инфекции
Лечение при гнойной инфекции должно быть комплексным и соответствовать стадии развития гнойного воспаления с учетом нормергического, гиперергического или гипоергического его проявления, а также биологических особенностей возбудителя. Независимо от стадии развития гнойно-инфекционного процесса комплекс лечебных мер должен включать:
- местные и общие антипатогенетические воздействия на больного животного, основанные на принципе охранительной терапии;
- противомикробные и антитоксические воздействия, направленные на подавление микробного фактора и удаление токсических продуктов из патологического очага и из организма;
- оперативное или консервативное удаление мертвых тканей, которое, так же как и дезинтоксикация организма, влияет на течение инфекционного процесса;
- меры симптоматического воздействия, направленные на улучшение функционального состояния того или иного жизненно важного органа;
- витаминотерапию и полноценное кормление при сбалансированном ощелачивающем рационе;
- дозированный моцион и более широкое применение физиотерапевтических процедур на стадии выздоровления.
В начальных стадиях развития гнойной инфекции (стадии воспалительного отека и клеточковой инфильтрации) целесообразна короткая блокада 0,25%-ным раствором новокаина в сочетании с гидрокортизоном и одним или двумя антибиотиками, например, с натриевой (калиевой) солью бензилпенициллина и стрептомицинсульфатом либо с мономицином или с канамицином, но эффективнее с гентамицином. Раствор вводят вокруг развивающегося инфекционного очага и по возможности под него. На инфицированный очаг накладывают спиртовысыхающие повязки или спиртовые согревающие компрессы, используя 70%-ный этиловый, ихтиоловый, камфорный спирт, и организуют другие тепловые процедуры.
На стадии воспалительного отека такое лечение предупреждает перераздражение нервных центров, нормализует воспалительную реакцию, трофику, повышает активность физиологической системы соединительной ткани, способствует фиксации, локализации и подавлению возбудителей. В результате этого начавшийся инфекционный процесс нередко обрывается и наступает выздоровление.
На стадии клеточной инфильтрации, как и на стадии абсцеди-рования, целесообразно дополнительно внутримышечно применять антибиотики широкого спектра действия. Особого внимания заслуживают внутривенные введения 0,25%-ного новокаина с соответствующим'антибиотиком или сульфаниламидом. Более эффективны внутриартериальные введения их в магистральную артерию, доставляющую с кровью введенный раствор непосредственно в инфекционный очаг (глубокая антисептика).
Некоторые авторы рекомендуют применять при этих стадиях и даже на стадии абсцедирования местную гипотермию. Но это допустимо лишь на стадии воспалительного отека и притом кратковременно в виде наложения резинового пузыря со снегом или толченым льдом на 10—15 мин, 2—3раза; с такими же перерывами либо на такой же срок накладывают охлаждающие повязки. Допустимо орошать зону инфицированного очага хлорэтилом через легкую бинтовую повязку или марлевую салфетку в течение 20—30 с при передвижении струи со скоростью 1—2 см в 1 с. Процедуру повторяют 2—3 раза с интервалом 1—1,5 ч. Местная гипотермия уменьшает боль, предупреждает чрезмерную проницаемость сосудов, снижает отек и внутритканевое давление. Однако при длительном применении она понижает фагоцитарную реакцию, способствует некротизации и активизации возбудителя. Поэтому мы рекомендуем применять ее осторожно и только на стадии отека при фурункулезе и быстропрогрессирующих воспалительных отеках (гиперергическое развитие острогнойного воспаления).
Описанный комплекс лечения на стадии клеточной инфильтрации нормализует в инфекционном очаге трофику, активирует физиологическую систему соединительной ткани, фагоцитоз и ферментолиз, обеспечивает формирование клеточного барьера, предупреждает генерализацию, снижает и даже подавляет активность возбудителя. Инфекционный процесс купируется и приобретает благоприятное течение.
На стадии абсцедирования целесообразны также короткая новокаиновая блокада, спиртовысыхающие повязки, внутривенные и внутриартериальные введения антибиотиков и сульфаниламидов на 0,25%-ном растворе новокаина, облучение лампами соллюкс, Минина, но недопустимо применять согревающие компрессы, особенно припарки, горячие ванны, парафиновые и озокеритовые аппликации. Использование их допустимо лишь на стадии клеточковой инфильтрации преимущественно при анергической воспалительной реакции. Такие тепловые процедуры, особенно при гиперергическом воспалении, усиливают отек и внутритканевое давление, в результате чего ухудшается кровообращение и лимфоотток, расширяется зона некроза, создаются условия для проникновения гноя и возбудителя в здоровые ткани или анатомические полости.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Инфекционные заболевания костей и суставов - остеомиелиты и артриты: причины, диагностика, лечение
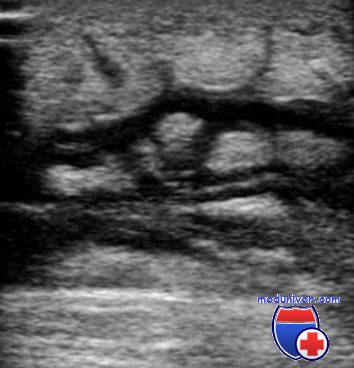
Остеомиелит (инфекция костной ткани) возникает в результате гематогенного распространения инфекции или поражения кости вследствие заболеваний суставов, а также после травмы и хирургического вмешательства. Образование гноя способствует развитию ишемии и некроза тканей. Омертвевшую часть кости называют секвестром. Вокруг очага инфекции происходит формирование новой костной ткани (оболочки).
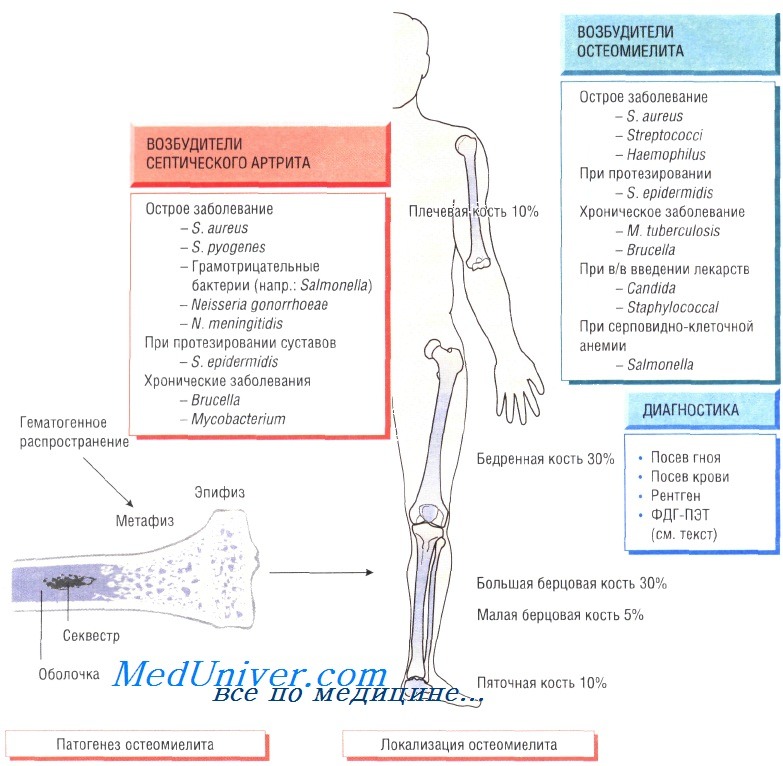
У детей чаще всего отмечают поражение метафизов трубчатых костей (бедренной, большеберцовой и плечевой). У взрослых также может развиться остеомиелит позвоночника.
В 90% случаев в роли возбудителя остеомиелита выступает Staphylococcus aureus, реже — Streptococcus pyogenes (4%), Haemophilus influenzae (4%), Escherichia coli, Mycobacterium tuberculosis и микроорганизмы родов Salmonella и Brucella. У пациентов с серповидно-клеточной анемией чаще всего диагностируют сальмонеллёзную этиологию заболевания.
Клинические признаки остеомиелита. У пациентов отмечают гипертермию и болевой синдром, причём у некоторых из них (особенно в молодом возрасте) боль чётко не локализована. Дети часто перестают двигать поражённой конечностью (псевдопаралич). При прогрессировании заболевания наблюдают отёчность мягких тканей, сопровождающуюся образованием полостей.
При отсутствии необходимого лечения и поздней диагностики возникают патологические переломы. Кроме того, повышается риск развития хронической формы остеомиелита. Очень часто очаги острой или хронической инфекции возникают вокруг инородных тел (хирургические нитки, осколки при травме).
Диагностика остеомиелита. Изменения, определяемые при радиологических исследованиях, возникают только на поздних стадиях болезни, когда происходит деминерализация костей. Сцинтиграфия позволяет обнаружить инфекцию, но не дифференцировать инфекционный и воспалительный процессы. Наиболее чувствительный метод — позитронно-эмиссионная томография с использованием фтордеоксиглюкозы (ФДГ-ПЭТ). Большое значение имеет посев образцов крови пациента, хотя на ранних стадиях инфекции результат может быть отрицательным. Для идентификации возбудителя и определения его чувствительности к антибиотикам осуществляют посев гноя, отобранного при помощи иглы или прямой биопсии.
Лечение остеомиелита. Основной метод лечения — дренирование и иссечение секвестра. Эмпирическую антибиотикотерапию (флуклоксациллин и фузидовая кислота) необходимо начинать как можно быстрее, не дожидаясь результатов посева, так как в большинстве случаев заболевание вызывают стафилококки и стрептококки. Другие препараты (ципрофлоксацин) назначают при выделении чистой культуры сальмонелл или подозрении на сальмонеллёзную инфекцию у пациентов с серповидно-клеточной анемией. Лечение продолжают до очевидного выздоровления и исчезновения признаков воспаления (около 6 нед).
Хронический остеомиелит
При неправильном лечении, а также после хирургической операции или травмы болезнь переходит в хроническую форму. С внедрением в клиническую практику протезирования у пожилых людей всё чаще обнаруживают хронический остеомиелит, связанный с контаминацией протезов слабовирулентными микроорганизмами (коагулаза-отрицательными стафилококками).
У 50% больных возбудителем становятся Staphylococcus aureus, в остальных случаях чаще — грамотрицательные бактерии (рода Pseudomonas, Proteus и Е. coli). Основные симптомы — постоянный болевой синдром, отёк, деформация тканей и хронические выделения из свищей. Для диагностики необходимо выполнить посев гноя, отобранного в асептических условиях. Залогом эффективного лечения считают правильно подобранную антибактериальную терапию и успешное выполнение хирургического вмешательства. При возникновении инфекции в месте установки протеза его необходимо удалить (для эффективности лечения).
Гнойный артрит
Гнойный артрит обычно возникает на фоне бактериемии, при этом в 95% случаев возбудителем являются S. aureus и S. pyogenes. Кроме того, в этиологии заболевания участвуют кишечные бактерии, сальмонеллы, бруцеллы, Neisseria gonorrhoeae, Н. influenzae, Borrelia burgdorferi, Pasteurella и M. tuberculosis. Чаще происходит поражение крупных суставов (например, коленного), но нередко отмечают инфекции плечевого, тазобедренного, голеностопного, локтевого и запястного суставов.
Очень часто заболевание возникает при протезировании суставов, когда во время операции или в результате гематогенного распространения на протезе развиваются микроорганизмы, входящие в состав микрофлоры кожи (обычно S. aureus или Staphylococcus epidermidis). Источник инфекции может быть на удалённом расстоянии от места развития артрита.
Клинические признаки гнойного артрита. У детей болезнь начинается с внезапного повышения температуры, возникновения боли и отёчности, затрудняющих движения в поражённом суставе. У взрослых артрит может развиваться постепенно. В ряде случаев в анамнезе есть указания на заболевания мочевыводящих путей или сальмонеллёз. Другие характерные симптомы — развитие целлюлита или появление сыпи (например, сыпь при гонококковой инфекции).
Перед установлением диагноза необходимо исключить такие заболевания, как ревматоидный артрит, остеоартрит, подагра, псевдоподагра и реактивный артрит. Для диагностики выполняют пункцию сустава. Проводят бактериологическое исследование суставной жидкости (окраска по Граму), возможно повышение количества лейкоцитов. Результаты посева оценивают через 48 ч. При подозрении на бруцеллёз для посева отбирают образцы костного мозга пациента.
Лечение следует начинать с внутривенного введения антибиотиков, эффективных в отношении определённого или предполагаемого возбудителя. Затем продолжают курс антибактериальной терапии (приём препаратов внутрь) до 6 нед. Иногда необходима пункция и промывание сустава.
Вирусный артрит
Некоторые вирусы (например, вирус краснухи, паротита и гепатита В) могут стать причиной артрита. Артрит, вызванный вирусом краснухи (чаще наблюдается у женщин), развивается через несколько дней после возникновения сыпи. Некоторые альфавирусы способны вызывать тяжёлые заболевания костей и суставов. Иногда артрит возникает вследствие иммунной реакции на возбудителя в периоде реконвалесценции некоторых инфекционных заболеваний (например, после менингококковой инфекции, шигеллёза или хламидиоза). При хламидиозе возможно развитие синдрома Рейтера — сочетание увеита и артрита.
Инфекции суставов после протезирования
Суставные протезы могут подвергнуться микробной контаминации во время операции и при гематогенном распространении инфекции. Возбудителями обычно становятся низковирулентные микроорганизмы (например, S. epidermidis). Тяжёлые последствия наблюдают в результате инфекции, вызванной S. aureus (особенно его метициллинрезистентны-ми штаммами). Для лечения назначают внутривенное введение антибактериальных препаратов (по результатам исследования чувствительности микроорганизмов к антибиотикам).
В связи с развитием инфекции суставной протез необходимо удалить, при этом следует соблюдать меры предосторожности для недопущения распространения инфекции. Пациентам, которым предстоит протезирование суставов, назначают курс профилактической антибиотикотерапии препаратами, эффективными в отношении S. aureus.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
- Вернуться в раздел "Микробиология"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Лечение гнойных и септических осложнений ранений: устранение очага инфекции, антибиотикотерапия
Лечение любого гнойно-септического осложнения является комплексным и включает в себя следующие мероприятия:
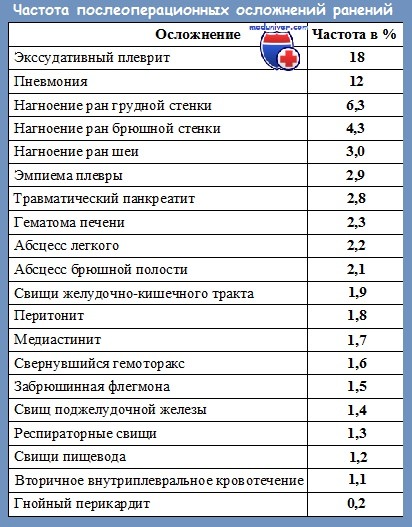
1) Устранение первичного очага инфекции хирургическим путем. Хирургическое вмешательство прекращает дальнейшее поступление микроорганизмов. Это может быть ушивание дефекта стенки полого органа, его резекция или удаление. После этого следует санация очага гнойной инфекции, которая заключается в механическом удалении гнойного экссудата, пропитанных гноем некротических тканей из серозных полостей, средостения и забрюшинного пространства. Заключительным этапом хирургического метода лечения является полноценное дренирование гнойного очага.
Наиболее эффективным мы считаем метод активного дренирования с аспирацией и промыванием, принципы и детали которого изложены ниже, в разделах, посвященных специфическим осложнениям ранений.
2) Устранение расстройств внешнего дыхания достигается:
— обогащением кислородом вдыхаемой смеси;
— ИВЛ с положительным давлением в конце выдоха;
— постоянной санацией трахеобронхиального дерева.
Для предупреждения пневмонии применяют аэрозольные ингаляции с антибиотиками, парокислородные ингаляции, муколитики, вибромассаж груди (при отсутствии противопоказаний).
3) Коррекция расстройств системного кровообращения достигается:
— устранением дефицита объема внеклеточной жидкости (кристаллоиды, коллоиды, альбумин, кровь, по показаниям — вазопрессоры);
— снижением вязкости циркулирующей крови.
При проведении инфузионно-трансфузиониой терапии нельзя допускать возникновения легочной артериальной гипертензии.
4) Антибактериальная терапия. На протяжении нескольких десятилетий при лечении гнойных осложнений применялась эскалационная (восходящая) методика антибактериальной терапии, когда при неэффективности препаратов первого ряда назначались более мощные антибиотики.
Так, в прошлом достаточно эффективным было применение амоксициллина или ампициллина с сульбактамом, цефалоспоринов второго поколения (цефуроксима, цефокситина), третьего (цефтриаксона, цефоперазона) или четвертого (цефенима) поколений, фторхинолонов (ципрофлоксацина, левофлоксацина).
Эти препараты обычно применяли в комбинации с аминогликозидами, ванкомицином и антиаэробными средствами (метронидазол, линкомицин, клиндамицин).
Такой подход был клинически и экономически оправдан в условиях низкого уровня резистентности микроорганизмов. Однако во второй половине 80-х и в 90-х годах XX в. отмечен повсеместный рост резистентности, обусловленный как неблагоприятными изменениями внешней среды обитания (экология, социальные условия, алкоголизм, наркомания), так и бесконтрольным употреблением антибиотиков.
В настоящее время устойчивость микроорганизмов объявлена угрозой для человечества в целом. В таких условиях для лечения гнойно-септических осложнений приходится применять деэскалационную методику, которая заключается в максимально раннем назначении массивных доз антибиотика, спектр действия которого максимально охватывает всех возможных возбудителей с последующим (при получении результатов микробиологического исследования) переходом па препараты более узкого спектра.
В этом плане наиболее эффективными в настоящее время являются антибиотики из группы карбоненемов. Несмотря на более чем 20-летнее использование, уровень устойчивости к ним клинически значимых возбудителей остается низким, возможно из-за их устойчивости к бета-лактамазам, выделяемым микроорганизмами для разрушения антибиотиков.
5) Интенсивное парентеральное и энтералъное питание. В первую очередь необходимо обеспечить введение аминокислот, вследствие их усиленного потребления для сохранения барьерной функции кишечника и клеток иммунной системы. Наиболее эффективными в этом смысле являются смеси для энтерального введения, содержащие омега-3 жирные кислоты, глютамин, аргинин, а также пектин.
6) Активные методы детоксикации. Среди методов экстракорпоральной детоксикации у пострадавших с множественными и сочетанными ранениями шеи, груди и живота, осложненными сепсисом, самым распространеным и хорошо изученным является плаз-маферез.
Положительный эффект плазмафереза основан на удалении высокомолекулярных белков острой фазы воспаления, а также нормализации реологических свойств крови. Метод позволяет быстро удалять из циркулирующей крови токсины (как водорастворимые, так и связанные с белками), свободный миоглобин, активированные компоненты свертывающей системы крови, С-реактивный белок, цитокины, комплемент, лизосомальные ферменты, аутоантитела, иммунные комплексы и просто обломки разрушенных клеток и клеток в состоянии апоптоза.
Метод существует в двух модификациях: прерывистый и непрерывный. Не останавливаясь на деталях этих модификаций, необходимо подчеркнуть, что у пострадавших в критическом состоянии используют непрерывную технологию, которая меньше оказывает отрицательное влияние на гемодинамику.
7) Торможение образования медиаторов воспалительной реакции. В настоящее время большие надежды возлагаются на восполнение дефицита селена — микроэлемента, входящего в состав фермента (глютатионпероксидазы), отвечающего за антиоксидантную систему защиты клеток. В частности, достаточное количество этого фермента обеспечивает преобразование свободных радикалов в спирты и таким образом сохраняет целость клеточной мембраны.
Препараты селена при лечении гнойно-септических осложнений применяются в виде пентагидрата селенита натрия. К сожалению, в настоящее время пока нет возможности четко определить закономерности в реакциях и взаимодействиях сотен различных медиаторов, а следовательно, и избирательную нейтрализацию активности циркулирующих в крови медиаторов, как воспалительных, так и противовоспалительных.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Гнойные заболевания являются достаточно широко распространенными.
Такие заболевания опасны тем, что при несвоевременно начатом лечении очень велика вероятность возникновения осложнений, среди которых может быть даже частичное, а в редких тяжелых случаях – и полная потеря трудоспособности.
СИМПТОМЫ РАЗВИТИЯ ГНОЙНЫХ ЗАБОЛЕВАНИЙ
При данной патологии возникает воспалительная реакция с развитием общих и местных изменений.
Степень выраженности болезни зависит от обширности воспалительного процесса и общей реактивности организма.
При этом существует универсальное правило, согласно которому показанием к проведению хирургического лечения заболевания является любой гнойный процесс.
Повышение температуры тела (иногда до фебрильных значений),
Симптомы гнойной интоксикации – головная боль, слабость, ухудшение работоспособности, апатия, адинамия, снижение аппетита, сонливость или, напротив, нарушение сна.
Боль в месте воспаления.
Гиперемия кожного покрова в зоне воспаления
Местное повышение температуры над очагом воспаления, сглаженность контуров борозд и линий
Кроме того, отмечаются специфические признаки для каждого в отдельности заболевания.
В зависимости от расположения можно определить вовлечение в патологический процесс определенных областей и вероятность развития осложнений.
Фурункул - это острое гнойно-некротическое воспаление волосяного фолликула, сальной железы и окружающей подкожной клетчатки.
Панариций - скопление отделяемого преимущественно гнойного характера под кожей в области фаланги. При этом могут отмечаться общие симптомы заболевания, однако чаще всего они выражены незначительно. При осмотре на одной из фаланг пальцев, преимущественно проксимальной, определяется зона припухлости, гиперемии.
Фурункулез – это наличие нескольких фурункулов в различных областях, имеющих рецидивирующее течение. При фурункулезе больных необходимо обследовать для выявления нарушений обмена веществ (сахарный диабет, авитаминоз). Лечение проводится комплексное, включая и иммунотерапию.
Карбункул – это острое разлитое гнойно-некротическое воспаление нескольких близлежащих волосяных фолликулов и сальных желез с образованием некроза кожи и подкожной клетчатки, сопровождающееся признаками гнойной интоксикации. Локализация карбункулов чаще всего наблюдается на задней поверхности шеи, межлопаточной области. Обычно карбункул сопровождается лимфаденитом, а при локализации на конечностях – лимфангитом.
Флегмона – это острое гнойное разлитое воспаление клеточных пространств, не имеющие тенденцию к отграничению. Вызывается это заболевание чаще всего стафилококком, а также любой другой гноеродной микрофлорой. Инфекция может проникать в ткани через повреждения кожи и слизистых, после различных инъекций (так называемые постинъекционные флегмоны), лимфогенным и гематогенным путем, при переходе воспаления с лимфатических узлов, карбункула, фурункула и т.д. на окружающую их клетчатку.
Абсцесс – это ограниченное скопление гноя в различных тканях или органах, окруженное пиогенной капсулой. Возбудители и пути проникновения инфекции в ткани такие же как при флегмонах, хотя процент анаэробных возбудителей значительно выше.
Гидраденит- это гнойное воспаление потовых желез. Инфекция попадает при несоблюдении правил гигиены и повышенной потливости.
Мастит - это острое воспаление молочной железы. Мастит в основном развивается в послеродовом периоде во время лактации (лактационный мастит). Инфекция проникает в ткань железы через микротрещины в соске, а также и через молочные ходы при лактостазе.
Рожа. Рожей называют острое серозно-эксудативное воспаление кожи или слизистой. Инфекция попадает через микротрещины, ранки на кожном покрове.
ОСОБЕННОСТИ ЛЕЧЕНИЯ ГНОЙНЫХ ЗАБОЛЕВАНИЙ.
Местная терапия болезни включает в себя консервативные и оперативные методы.
Консервативные методы лечения применяются на ранних стадиях заболевания до образования гнойника, а также в сочетании с оперативным лечением с целью более быстрого и эффективного лечения.
Местное лечение в стадии инфильтрата включает в себя воздействие на него с помощью физиотерапевтических методик.
Обязательно необходимо применение мазей, в состав которых входят антибиотик и противомикробные вещества.
В зависимости от размера гнойного очага при лечении возможно использование обезболивания.
После вскрытия гнойника в ходе хирургического лечения заболевания производят его очищение от гнойного экссудата.
Затем его промывают антисептическим веществом, растворами антибиотиков.
После окончания операции рану никогда не зашивают наглухо, для наилучшего дренирования.
Перевязки заключаются в удалении дренажей и замене их новыми, промывании раны раствором антисептика, заполнении раны мазью, содержащей антибиотик, наложении повязки для предотвращения инфицирования раны.
Профилактика гнойных заболеваний:
В профилактике многих гнойных заболеваний большое значение имеет оздоровление внешней среды, в которой живет и работает человек, т. е. улучшение условий труда и быта.
Так, например, в профилактике целого ряда гнойных заболеваний (фурункулез, пиодермиты и т. п.) большую роль играют мероприятия общегигиенического характера и уход за кожей (особенно рук) и др.
Читайте также:

