Чем отличается токсоплазмоз от токсокароза
Обновлено: 19.04.2024
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
- Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
- Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).

Основными хозяевами токсоплазмы являются кошачьи, они заражаются при поедании мяса птиц и грызунов. После попадания в организм кошек паразит запускает цикл размножения. Кошка выделяет инфекционные ооцисты с фекалиями в окружающую среду в течение 1-2 недель. Большинство кошек выделяют ооцисты лишь раз в жизни. При этом ооцисты устойчивы к воздействию неблагоприятных факторов окружающей среды и могут сохранять жизнеспособность до нескольких месяцев. При случайном проглатывании ооцист человеком паразиты проникают в эпителий кишечника и распространяются по всему телу, проникают в нервную и мышечную ткань, где могут оставаться в спящей форме в виде цист на протяжении всей жизни хозяина - это называется латентная инфекция. При снижении иммунитета организма оболочки цист могут разрушиться и паразиты будут размножаться, вызывая обострение инфекции.
Существует четыре основных способа заражения человека токсоплазмозом:
Попадание в организм инфекционных ооцист из окружающей среды (при смене кошачьего лотка, при работе с землей, песком - садоводство)
Проглатывание тканевых кист в мясе инфицированного животного (употребление в пищу плохо термически обработанного мяса)
Вертикальная передача от инфицированной матери ее плоду
Передача при трансплантации органа от инфицированного донора
У иммунокомпетентных пациентов в большинстве случаев не бывает клинических проявлений инфекции, тогда как у пациентов с ослабленным иммунитетом риск развития тяжелой инфекции с осложнениями гораздо выше. К тяжелым формам токсоплазмоза относятся энцефалит, пневмонит, миокардит, хориоретинит.
Опасен токсоплазмоз и для беременных, которые при первичном инфицировании могут инфицировать плод, тем самым подвергая новорожденного ребенка опасности развития тяжелого токсоплазмоза.
Токсоплазмоз у иммунокомпетентных людей.
В редких случаях у некоторых людей инфицирование токсоплазмой может проявляться как острая системная инфекция, которая обычно развивается через 5–23 дня после инфицирования. Симптомы неспецифичны - лихорадка, озноб и пот; головные боли, миалгии, фарингит, гепатоспленомегалия и / или диффузная не зудящая макулопапулезная сыпь, данные симптомы могут сохраняться в течение 2-3 дней.
Наиболее распространенным проявлением является двусторонняя, симметричная, безболезненная шейная лимфаденопатией. Приблизительно у 20-30 процентов развивается генерализованная лимфаденопатия. Лимфатические узлы обычно меньше 3 сантиметров в размере и неподвижны. В отличие от лихорадки, которая длится недолго, лимфаденопатия может сохраняться неделями.
Лабораторные данные неспецифичны - небольшой лимфоцитоз с атипичными клетками (менее 10%) или без них, в биохимическом анализе крови иногда повышение печеночных трансаминаз, С-реактивного белка.
Как правило, первичное инфицирование токсоплазмой такой категории пациентов не требует специфической терапии, симптомы проходят самостоятельно.
Токсоплазмоз при ВИЧ-инфекции.
Токсоплазмоз любой локализации является оппортунистическим заболеванием для пациентов с ВИЧ и указывает на прогрессирование основного заболевания.
К другим опасным формам реактивации токсоплазмоза относятся пневмонит, миокардит, хориоретинит в зависимости от того, где осели и сформировали цисты токсоплазмы во время первичного инфицирования.
Диагностика основана на интерпретации клинической картины: часто при выявлении неврологической симптоматики у пациента с продвинутой стадией ВИЧ-инфекции, врач может заподозрить токсоплазменный энцефалит. В таком случае назначается терапия Бисептолом в лечебных дозах, а подтверждение диагноза проводится уже на фоне терапии, так как очень важно не потерять время. Для подтверждения диагноза могут понадобиться МРТ головного мозга (с контрастом или без), люмбальная пункция с исследованием ликвора - общий анализ и биохимический, а также ПЦР ликвора, позволяющая выделить ДНК токсоплазмы. Иногда на помощь приходят серологические методы обследования - антитела к токсоплазме классов IgG, IgM.
Лечение при реактивации токсоплазмоза проводят также Бисептолом. На фоне терапии улучшение состояния пациента наступает обычно в течение 1-2 недель. Но стоит помнить, что при отрицательном обследовании на токсоплазмоз, отсутствии специфического очага поражения с перифокальным отеком в головном мозге, при отсутствии клинической динамики на фоне проводимого лечения - необходимо исключать другую причину поражения головного мозга. Чаще всего - это лимфома ЦНС.
При подозрении на хориоретинит, пневмонит, миокардит требуются дообследования у профильных специалистов (офтальмолог, кардиолог, пульмонолог), даже может потребоваться проведение биопсии тканей органов.
Токсоплазмоз у беременных.
Своевременное серологическое обследование до наступления беременности, а также установление диагноза токсоплазмоза у беременных женщин определяет тактику ведения беременности.
Для самой беременной первичная инфекция токсоплазмой не так опасна, как для плода. Плод инфицируется от матери, и инфекция может быть как бессимптомной, так и с умеренными/тяжелыми клиническими проявлениями. Три наиболее распространенных вида поражения - ретинохориоидит (15-26%), внутричерепные кальцификации (9-13%) и гидроцефалия (1-2,4%).
Частота инфицирования плода резко возрастает с увеличением гестационного возраста на момент инфицирования матери. Оценочная вероятность передачи в зависимости от срока беременности при документально подтвержденной сероконверсии составляет:
В 13 недель - 15%
На 26 неделе - 44%
На 36 неделе - 71%
Наиболее часто инфицирование плода происходит при первичной инфекции токсоплазмой. Согласно приказу МЗ РФ №572 обследование на антитела класса IgM, IgG к вирусу краснуху и к токсоплазме являются обязательными для всех беременных. При отсутствии антител класса G к токсоплазме беременная должна быть проинформирована о том, как предотвратить первичное инфицирование токсоплазмозом.
При выявлении антител к токсоплазме используют дополнительные методы диагностики для определения давности инфицирования - исследования в парных сыворотках и анализ крови на авидность (или сродство) антител класса IgG к антигену токсоплазмы. Обнаружение низкоавидных антител свидетельствует о недавнем инфицировании.
Не беременные женщины, у которых диагностирован острый токсоплазмоз, должны отложить планирование беременности на 6 месяцев.
Каждая беременная, у которой при скрининге выявлено отсутствие антител IgG к токсоплазме, должна очень тщательно профилактировать заражение во время беременности. Основные меры профилактики токсоплазмоза:
Употреблять в пищу хорошо термически обработанное мясо (при Т более 67С) либо предварительно замораживать его до Т -20С.
Мыть разделочные доски и другую кухонную утварь горячей водой с мылом после контакта с сырым мясом, тщательно мыть руки.
Не есть сырые яйца и не пить сырое молоко, мыть фрукты и овощи, не пить необработанную воду.
Надевать перчатки и мыть руки водой с мылом при контакте с почвой или песком, которые могут быть загрязнены кошачьими фекалиями.
Надевать перчатки и мыть руки водой с мылом при работе с кошачьим лотком, кормить питомцев сухим или консервированным мясом. Домашние кошки, которых кормят сухим или консервированным кормом для кошек, не представляют опасности.
Таким образом, тактика обследования и лечения пациента в любой ситуации (и для пациента с иммунодефицитом, и для беременной или планирующей беременность женщины) достаточно индивидуальная и определяется только лечащим врачом-инфекционистом, либо консилиумом врачей.
Стоит упомянуть, что некоторые пациенты, иммунокомпетентные и не беременные, в процессе обследования могут получить положительный результат анализа на антитела к токсоплазме, но в большинстве случаев это не требует никаких вмешательств - ни специфической терапии, ни тем более ликвидации домашней кошки :)
да, это действительно так - наибольшую опасность представляют уличные кошки и те, которых подкармливают необработанным мясом, тем более выделение ооцист в окружающую среду происходит как правило только один раз.
По любым результатам анализов Вас всегда могут проконсультировать и помочь определиться с тактикой дальнейших действий врачи Университетсткой клиники H-clinic.
Услуги, упомянутые в статье*:
041601 - Возбудитель токсоплазмоза (Тoxoplasma gondii), количественное определение антител класса IgG
041602 - Возбудитель токсоплазмоза (Тoxoplasma gondii), качественное определение антител класса IgМ
041603 - Определение индекса авидности IgG к токсоплазме (Toxoplasma gondii), полуколичественное определение
*Назначение и интерпретация результатов анализов должны проводиться только лечащим врачом
Автор: врач-инфекционист Университетской клиники H-Clinic Коновалова Анастасия Александровна.
Медицинский редактор: руководитель Университетской клиники, к.м.н., врач-инфекционист Коннов Данила Сергеевич.
Что такое токсоплазмоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Токсоплазмоз — это острое и хроническое паразитарное заболевание человека в виде манифестных форм или носительства, вызываемое простейшими внутриклеточными паразитами — токсоплазмами, которые попадая в организм человека могут при условиях иммунодефицита поражать нервную ткань, среды глаза, сердечно-сосудистую и ретикулоэндотелиальную системы, вызывая поражение организма той или иной степени тяжести. Болезнь относится к группе TORCH-комплекса, т. е. вызывает врождённую патологию.
Этиология
Таксономия:
Вид — Toxoplasma gondii
Токсоплазмы обитают в мире в трёх формах:
- трофозоиты (тахизоиты);
- цисты (брадизоиты);
- ооцисты.
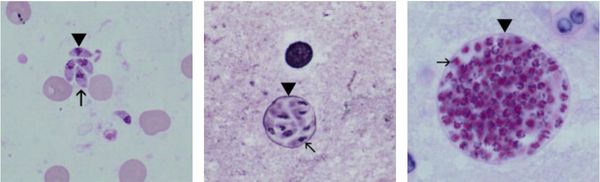
Трофозоиты достигают 4-7 мкм в длину и 2-4 мкм в ширину. Их тело по форме напоминает полумесяц с заострённым передним и закруглённым задним концами, состоит из пелликулы (покровной ткани) и различных органелл. Такие паразиты обитают во всех клетках млекопитающих кроме эритроцитов, размножаются путём деления. Могут создавать движение, активно проникая в клетки хозяина через клеточную мембрану или посредством фагоцитоза (захвата и переваривания клетки). Обнаруживаются в тканях в острой стадии инфекции. Их скопление внутри одной клетки называют псевдоцистой. Трофозоиты неустойчивы вне клетки и во внешней среде, быстро погибают при высушивании, прогревании и применении дезинфицирующих средств. Хорошо окрашиваются по Романовскому. Чувствительны к различным химиопрепаратам (сульфаниламидам, некоторым макролидам и другим).
Цисты размерами до 100 мкм отличаются плотной оболочкой, через которую не могут проникнуть антитела или лекарственные препараты. Внутри оболочки сосредоточено 3000-5000 паразитов, со временем они увеличиваются. Цисты формируются в организме хозяина (в основном в скелетных мышцах, миокарде и ЦНС) и живут там десятки лет. Чрезвычайно устойчивы к воздействиям внешних факторов. При адекватной иммунной системе могут пожизненно находиться в состоянии функционального покоя и не приносить никакого вреда организму человека.
Ооцисты играют основную роль в передаче инфекции. Они представляют собой овальные образования 10-12 мкм в диаметре. Их развитие и формирование длится 3-24 дня и проходит в слизистой оболочке тонкой кишки кошек. Затем в течение 7-20 дней паразиты выделяются с испражнениями, после этого срока новые фекалии кошки уже не заразны. За сутки с испражнениях животного выделяется до 10 миллионов ооцист. Спустя 2-3 дня при температуре 24 °C происходит споруляция ооцист — образование спор. При благоприятных условиях микроорганизмы сохраняются во внешней среде до года и дольше.
Существует множество штаммов токсоплазм, одни из которых отличаются высокой вирулентностью, а другие относительно маловирулентны. [1] [2] [7] [9]
Эпидемиология
Учитывая большое количество латентных форм, заболевание не поддаётся общему исчислению — им может быть заражено не менее 1,5 миллиардов человек. Только ежегодно регистрируется около 200 тысяч случаев внутриутробного инфицирования.
Распространение возбудителя повсеместное — токсоплазма обнаружена на всех материках. После заражения паразиты способны пожизненно сохранятся в организме большинства животных и птиц. Количество случаев приобретённого токсоплазмоза в разных странах колеблется: от 85 % во Франции и Мадагаскаре до 15 % в США и Англии.
- Фекально-оральный:
- водный и пищевой путь — при недостаточной термической обработке, чаще при употреблении сырого мяса и фарша;
- контактно-бытовой путь — при несоблюдении санитарных норм в повседневной жизни, например, при общении с кошками.
- Вертикальный путь (от матери к плоду) — преимущественно при первичном заражении матери во время беременности, часто у ВИЧ-инфицированных в стадии СПИДа.
- Артифициальный путь — при пересадке органов, в которых расположены цисты, пациенту с плохим иммунитету.
- Аэрогенный путь — при попадании инфицированной ооцистами пыли в рот человека.
- Контактный путь — при повреждении целостности кожных покровов. Встречается крайне редко, в основном у работников лабораторий и скотобоен, отмечен лишь в некоторых источниках, явного практического значения не имеет.
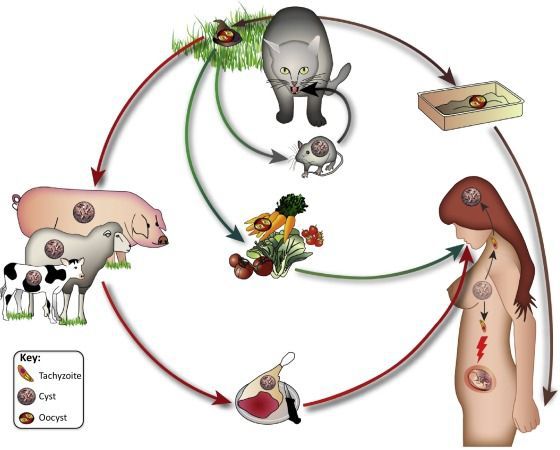
От человека к человеку заболевание не предаётся (кроме случаев каннибализма). Нельзя заразиться посредством укуса насекомых и при половом контакте.
Инфицирование токсоплазмой вызывает устойчивый пожизненный иммунитет к повторному заражению, однако известны случаи рецидива первичной инфекции при заражении другим высоковирулентным штаммом (у беременных, заразившихся при употреблении сырого мяса с другого континента). [1] [3] [5] [8] [9]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы токсоплазмоза
Инкубационный период при манифестных формах (явных проявлениях болезни) длится от двух недель до двух месяцев.
Специфичных симптомов, характерных именно для токсоплазмоза, не существует.
В большинстве случаев приобретённого токсоплазмоза заболевание протекает бессимптомно или со стёртой клиникой, напоминающей нетяжёлое ОРЗ: кратковременная лихорадка, слабость, недомогание, повышение температуры до 38,0 °C, увеличение периферических лимфоузлов, небольшое увеличение печени и селезёнки.
Доказано, что токсоплазма может оказывать влияние на психику человека. Это выражается в учащении рискованных действий, снижении концентрации внимания, повышенной нервозности, у лиц с тяжёлым острым или длительным хроническим активным течением повышен риск развития шизофрении.
Иногда заболевание проявляется изолированной глазной формой — длительно текущие увеиты, иридоциклиты и хориоретиниты. Как правило, эти нарушения являются поздними проявлениями нераспознанного ранее врождённого процесса.
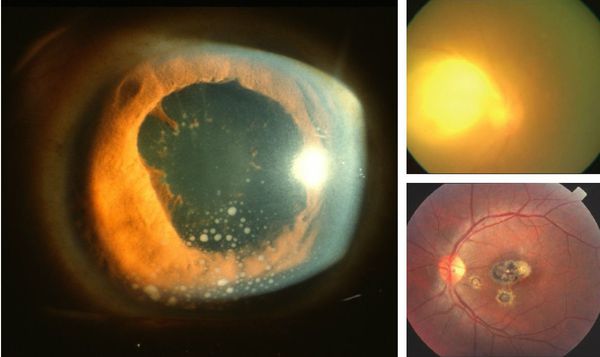
У людей с выраженным иммунодефицитом (ВИЧ, пересадка органов с последующей цитостатической терапией) возможно развитие генерализованного процесса с поражением нескольких органов (головного мозга, сердца, печени, почек, лёгких), нередко очень тяжёлого течения, проявляющегося в виде синдрома полиорганной недостаточности.
Токсоплазмоз у беременных может протекать в различных клинических вариантах и представляет опасность не столько для самой беременной (исключая тяжело протекающие патологии у беременных со СПИДом), сколько для плода.
При первичном заражении беременной токсоплазмозом имеет значение срок гестации:
- При инфицировании в первом триместре передача возбудителя плоду происходит лишь в 4 % случаев (к 13 неделе — в 6 %), но заканчивается, как правило, гибелью плода и выкидышем на ранних сроках. Если первичная инфекция у матери в первом триместре доказано, но выкидыш до 13 недели беременности не произошёл, то крайне высока вероятность, что внутриутробной передачи не было и ребёнок будет здоров.
- При инфицировании во втором триместре (особенно на 24-26 неделях) риск внутриутробной передачи резко возрастает и достигает 30-40 %, причём сопровождается развитием тяжёлых проявлений заболевания — одновременное увеличение селезёнки и печени, воспаление сосудистой оболочки и сетчатки глаза, поражения ЦНС в виде гидроцефалии, кальцификация, сыпь, миокардит, пневмония и другие.
- При заражении матери в третьем триместре передача инфекции ребёнку происходит с частотой до 90 %, однако проявления заболевания являются латентными или субклиническими и могут появиться спустя годы после рождения (отставание в развитии, нарушения зрения). [1][2][4][9]
Патогенез токсоплазмоза
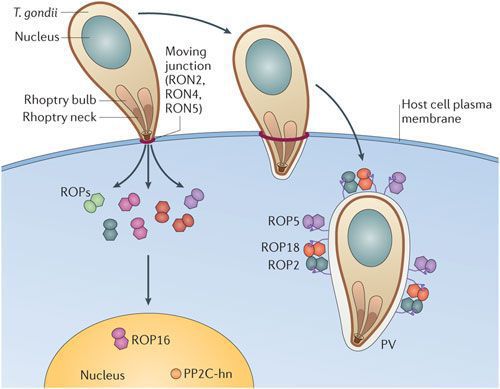
По мере развития и размножения токсоплазм поражённые клетки разрушаются, происходит заражение новых здоровых клеток, и при попадании возбудителя в кровоток паразиты разносятся по всему организму. Образуются некрозы с формированием фиброзной ткани и кальцификацией (отложение солей кальция в организме).
Под воздействием иммунитета безоболочечные трофозоиты превращаются в брадизоиты (оболочечные скопления токсоплазм), т.е. в тканевые цисты, которые сохраняются десятками лет в неактивном состоянии и при значительном снижении иммунитета способны к обратной трансформации с развитием обострения.
При первичной инфекции у беременных возбудитель проникает в ткани плода и вызывает воспалительный процесс, причём в разные периоды развития наблюдается различный характер воспаления: у эмбриона происходит лишь альтерация (дистрофия и некроз ткани без фиброза), в раннем фетальном периоде дополняется повышенным образованием соединительной ткани (фиброзом), а в позднем фетальном периоде присоединяется сосудистый компонент. Отсюда вытекают различные по характеру и тяжести поражения плода, которые зависят от сроков инфицирования матери. [1] [2]
Классификация и стадии развития токсоплазмоза
По течению процесса токсоплазмоз бывает:
- острым — до одного месяца;
- подострым - 1-3 месяц;
- хроническим — более трёх месяцев.
По клиническим признакам выделяют пять форм заболевания:
- Врождённый острый токсоплазмоз:
- манифестная форма (с указанием ведущих проявлений);
- субклиническая форма (с указанием способа верификации диагноза).
- Врождённый хронический токсоплазмоз:
- обострение / ремиссия;
- с резидуальными (остаточными) явлениями / без резидуальных явлений.
- Врождённый латентный токсоплазмоз.
- Приобретённый острый токсоплазмоз.
- Приобретённый хронический токсоплазмоз.
По степени тяжести заболевание бывает:
- лёгким;
- среднетяжёлым;
- тяжёлым (врождённая инфекция, токсоплазмоз при СПИДе).
По наличию осложнений выделяют:
- осложнённый токсоплазмоз;
- неосложнённый токсоплазмоз.
В Международной классификации болезней 10 пересмотра выделены шесть типов заболевания:
- B58.0 Токсоплазмозная окулопатия;
- B58.1 Токсоплазмозный гепатит (K77.0*);
- B58.2 Токсоплазмозный менингоэнцефалит (G05.2*);
- B58.3 Легочный токсоплазмоз (J17.3*);
- B58.8 Токсоплазмоз с поражением других органов;
- B58.9 Токсоплазмоз неуточнённый. [1][2][3]
Осложнения токсоплазмоза
При врождённой форме может возникнуть гидроцефалия, микроцефалия, задержка психомоторного развития и слепота. Эти осложнения сопровождаются увеличением или уменьшением размеров черепа, различными неврологическими расстройствами — косоглазием, судорогами, трудностью с сидением и держанием головы, рвотой и другими.
При глазной форме заболевания развивается слепота, снижение остроты зрения и воспалительные явления всех сред глаза. Причём возможно как рождение с грубыми дефектами зрения, так и появление воспалительных явлений и нарушения зрения спустя много лет после рождения.
Токсоплазмоз у иммунокомпрометированных людей осложняется шизофренией, токсоплазменный энцефалитом и полиорганной недостаточностью — тяжёлой патологией различных органов при выраженном иммунодефиците. При этом свойственна картина тяжёлого энцефалита. Прогноз, как правило, неблагоприятный. [1] [5] [8] [9]
Диагностика токсоплазмоза
Лабораторная диагностика:
- Клинический анализ крови: снижение уровня тромбоцитов, увеличение количества лимфоцитов и эозинофилов.
- Биохимический анализ крови: возможно повышение уровня трансаминаз и билирубина.
- Иммуноферментный анализ (ИФА):
- Выявление специфических антител класса M — острая инфекция или её реактивация. Имеет ряд недостатков — низкая специфичность, длительная циркуляция в организме, иногда до года после острого процесса. В сложных случаях уточнение следует производить при помощи метода "двойной сэндвич" или "иммунозахват" IgM ELISA.
- Выявление специфических антител класса G (клеток памяти) — носительство, инфицированность — появляются в среднем со второй недели заболевания и достигают пика на 1-2 месяце, сохраняются пожизненно, за исключением СПИД-ассоциированных заболеваний.
- Авидность IgG — уточнение давности заболевания. Недостатком является отсутствие стандартизации результатов, что зачастую приводит к различным ошибкам интерпретации. Наибольшее значение имеет высокая авидность, остальные результаты низкой и слабой авидности могут быть ошибочными и не должны трактоваться как недавно перенесённое заболевание при отсутствии других подтверждающих этот факт тестов.
- ПЦР-диагностика: выявление ДНК токсоплазмы в крови, других жидкостях и тканях человеческого организма. Особенно информативна в диагностике генерализованного, глазного и врождённого токсоплазмоза, в т. ч. в антенатальном периоде путём проведения амнио (не ранее 16 недель) и кордоцентеза (с 18 недели беременности).
- УЗИ-диагностика: внутриутробное выявление гидро- и микроцефалии, кальцификатов, гепатоспленомегалии и выраженной задержки развития. [1][2][4][5][6]
Дифференциальная диагностика
Токсоплазмоз — это инфекция с необычайно разнообразными проявлениями, поэтому ввиду неспецифичности проявлений основное место в дифференциальной диагностике отводиться лабораторному обследованию, а именно специфическим серологическим тестам.
Необходимо исключить следующие заболевания:
-
(ВЭБ-инфекцию) — боли в горле, преимущественное увеличение затылочных и заднешейных лимфоузлов, характерные изменения гемограммы (появление большого количества атипичных мононуклеаров и отсутствие столь выраженных изменений при врождённом течении), положительные IgM и ПЦР крови; — лимфоцитарный характер гемограммы, частое поражение слюнных желёз, положительные IgM, ПЦР крови;
- туберкулёз — длительное постепенное начало, лёгкий субфебрилитет (до 38,0 °C), ночная потливость, нездоровый румянец на щеках, кашель, специфические изменения в лёгких, положительные пробы на туберкулёз, выявление бациллы Коха в мокроте;
- лимфопролиферативные заболевания (лимфома Ходжкина, неходжкинские лимфомы) — специфические изменения при биопсии поражённой ткани (лимфоузлов);
- ВИЧ-инфекция — наличие факта возможного заражения, увеличение всех групп лимфоузлов, положительная серология;
- саркоидоз — специфические изменения в лёгких, положительные результаты гистологического исследования. [1][2][5]
Лечение токсоплазмоза
Большинство случаев приобретённого токсоплазмоза протекают в лёгкой или бессимптомной форме, они не регистрируются и, по-видимому, не нуждаются в каком-либо лечении.
Необходимость проведения специфической этиотропной терапии возникает лишь у некоторых групп пациентов:
- беременные с доказанным первичным инфицированием (в ряде случаев при реактивации хронической инфекции);
- дети с врождённой формой токсоплазмоза (при наличии явных клинических и лабораторных проявлений заболевания, субклинических и инаппарантных формах) — сроки и объём терапии зависят от конкретных данных;
- иммунокомпрометированные люди, у которых токсоплазмоз (острый или в фазе реактивации хронического процесса) протекает с выраженными клинико-лабораторными проявлениями. Основное направление воздействия в этом случае должно быть на устранение причины иммунодефицита, повышение уровня СД4 клеток.
Проведение лечения может осуществляться как в стационаре, так и амбулаторно в зависимости от выраженности процесса, реакции пациента на вводимые препараты, необходимости тех или иных вариантов патогенетического и симптоматического обеспечения. [1] [4] [7]
Прогноз. Профилактика
При приобретённом токсоплазмозе у иммунокомпетентных лиц прогноз благоприятный, у иммунокомпрометированных лиц (СПИД) прогноз серьёзен, нередки летальные исходы.
При врождённом токсоплазмозе исход заболевания зависит от сроков инфицирования плода:
- при инфицировании в первом триместре, как правило, происходит выкидыш;
- в более поздние сроки последствия варьируются от тяжёлых до резидуальных форм.
Основным методом профилактики приобретённого и врождённого токсоплазмоза является соблюдение санитарно-гигиенических правил, особенно беременными, не имеющими антител класса G к токсоплазмам:
- ограничение контакта с кошками;
- запрет на употребление сырого мяса, фарша и морепродуктов;
- тщательная промывка зелени, фруктов и овощей;
- мытьё рук перед едой;
- работа на приусадебном участке только в перчатках.
Для беременных особенно важен скрининг антител к токсоплазме, позволяющий выявить активно протекающее заболевание или риск его возникновения, а также вовремя провести медикаментозную профилактику острого токсоплазмоза беременной и снизить риск врождённой инфекции на 60 %. При отсутствии антител класса G в первом триместре необходимо отслеживать антитела IgM и IgG не только в тертьем, но и во втором триместре беременности.
В очаге токсоплазмоза противоэпидемические мероприятия не проводятся, вакцина на разработана. [2] [3]

Желудочно-кишечный тракт
Токсоплазмоз, токсокароз – одни из самых распространенных заболеваний. Хотя они и разные, но у них очень схожие причины, симптомы, диагностика, лечение и профилактика. Что это за заболевания?
Определения
Токсоплазмоз – заболевание, вызванное паразитарной деятельностью простейших микроорганизмов, называемых токсоплазмами. При токсокарозе в организм попадают токсокары, круглые черви, именуемые глистами. И те и другие ведут паразитирующую жизнь в своем носителе.

Каковы их симптомы? Как проводить лечение токсокароза у детей? Как лечить токсоплазмоз у детей?
Причины возникновения
Оба заболевания передаются, обычно, от животных, их шерсти, слюны, или через экскременты. Сами животные являются носителями, во внешнюю среду токсоплазмы попадают с их испражнениями. А испражняются коты/кошки в песок. На детских площадках есть песочницы, в которые не запретить бродячему животному испражнится. Случайно проконтактировав с ними и, не помыв руки, коснутся рта или какой-то слизистой, глаз, токсоплазма может, таким образом, легко попасть в организм ребенка. Именно поэтому среди детей это заболевание очень распространено. Помимо песочницы, вот еще потенциальные источники заражения:
- немытые фрукты, соприкасавшиеся с инфицированной средой;
- продукты из мяса, молока, которые термически не были обработаны либо обработаны плохо;
- грязная вода;
- заражение плода в утробе матери;
- пересадка органов или переливание крови.
Что происходит после заражения?
Токсоплазмоз. Токсоплазмы могут поражать центральную нервную систему, мышцы, глаза, миокарду (мышца сердца), селезенку, костный мозг, лимфатические узлы. Они даже могут влиять на личность, поведение человека.
Токсокароз. Токсокары (глисты) тоже стремятся попасть, размножится во внутренних органах и их системах. В отдельных случаях могут быть летальные исходы, если поражен жизненно важный орган, сердце или центральная нервная система. Особенно подвержены этим заболеваниям дети.
Особенно опасно внутриутробное заражение младенца любым из упомянутых заболеваний. Если женщина заболела до беременности, ничего страшного малышу не грозит, а если во время беременности, тогда это грозит патологиями развития ребенка, которые могут быть несовместимыми с жизнью, чревато гибелью плода, выкидышем, мертворождением. В лучшем случае, если заражение произошло на последних сроках беременности, у младенца будут врожденные хронические болезни.
При заражении токсокарозом, токсокары начинают через кровоток и другие пути проникать в любой уголок организма. Без надлежащего лечения заболевание протекает медленно и тяжело. Токсокары вызывают кожный зуд, аллергические реакции, экземы и тому подобное. Эти паразиты поражают дыхательные пути. Когда они добираются до головного мозга, они нарушают полноценную жизнедеятельность. Такому ребенку тяжело сосредоточится, читать, воспринимать поступающую информацию.

Симптомы
Если токсоплазмоз у ребенка врожденный или приобретенный, симптомы такие:
- лихорадка;
- повышение температуры;
- увеличение внутренних органов (печень, селезенка) ;
- желтушность;
- слабость;
- происходит помутнение хрусталика глаза;
- развивается косоглазие;
- исчезновение слуха и зрения;
- изменяется форма и состояние внутренних органов;
- появление сыпи на теле розового или красного цвета.
В первые 14 дней жизни ребенка болезнь будет прогрессировать, потому есть риск летального исхода.
- длительная, повторяющаяся лихорадка;
- приступ сухого кашля;
- увеличенная печень или селезенка;
- заболевания бронх и легких;
- трудности с желудочно-кишечным трактом;
- сыпь на теле;
- зуд;
- тошнота, рвота;
- расстройство кишечника;
- болезнь глаз, приводящая к слепоте или косоглазию.
Обычно, когда личинка токсокара попала в глаза, заболевают не оба, а какой-то один глаз. Если эти симптомы наблюдаются, велика вероятность наличия заражения.
Диагностика
Если у ребенка были замечены вышеупомянутые симптомы заболеваний токсоплазмоза и токсокароза, первым делом нужно обратиться к специалисту-врачу. Диагностика очень важна для установления правильного диагноза, ведь только так можно назначить правильное лечение.
При обоих заболеваниях, врачи проверят больного, есть ли другие признаки, свидетельствующие о наличии активных паразитов в организме. Обширная диагностика токсоплазмоза проводится при помощи:
- иммунофлуоресценция;
- пробы Сэбина-Фельдмана;
- кожной пробы;
- МРТ мозга;
- биопсия мозга;
- проверяется анализ крови;
- анализ спинномозговой жидкости.
Диагностика же при токсокарозе несколько проще. Врач проверит глаза на поражение токсокарами, проверит анализ крови. Узнает у больного, имеют ли место другие проявления болезни.
Лечение
Лечение токсоплазмоза у детей должно быть комплексным. Если проходит лечение беременная – лечится и малыш, до и после рождения последнего.
Если анализ показал у матери наличие токсоплазмы, но отсутствовали явные симптомы самого заболевания, беременной не назначают лечение. Опасно заболеть в начале беременности. Некоторые прописывают химиотерапию. Но только не в первые три месяца. Химиотерапия навредит младенцу, даст врожденный порок.
Из антибиотиков при лечении назначают сульфазин, хлоридин. Клиндамицин применяют для внутривенных инъекций. Если токсоплазма достигла центральной нервной системы, то следующие препараты рекомендуют такие: азитромицин, кларитромицин.
Лечение токсокароза проводится такими препаратами: мебендазол, медамин, тиабендазол. Они убивают микроорганизмы, даже если недуг врожденный. Не убивают только личинки, альбедазол уничтожит и личинки. Но его нужно принимать лишь после рекомендации врача.

При глазном поражении токсокарами лечат только инъекциями. В составе этих инъекций есть депо-медрол. Бывают же случаи (это покажет диагностика) когда без оперативного вмешательства проблему не решить.
Профилактика
Профилактическая работа для детей – это самое дешевое средство от токсоплазмоза, токсокароза. Всякий раз, когда приходится посещать уборную, нужно мыть руки. Этому следует научить своих детей. Нужно меньше контактировать с животными, особенно, бездомными. Если дома есть кот/кошка или собака, нельзя целовать ее. Каждый раз, после контакта с домашним животным, мыть руки обязательно.
Все это также хорошо применимо к замене туалета у домашних питомцев. Это действо должно происходить в перчатках.Регулярно своих питомцев нужно водить к ветеринару, который мог бы следит за здоровьем животного, чтобы вовремя предупредить болезнь.
Читайте также:

