Чем питается дизентерийная амеба в кишечнике
Обновлено: 18.04.2024
Суммируя сказанное, еще раз вкратце проследим, какое место в биосфере Земли занимает тот микроорганизм, речь о котором пойдет ниже.
Амебиаз
Источниками, которые ориентируются на данные ВОЗ, доля носителей гистолитической амебы оценивается на уровне 10% населения Земли. Независимые авторы публикуют более сдержанные оценки: примерно 6%, что, впрочем, тоже составляет огромное число людей – около полумиллиарда человек. Активная клиническая форма заболевания развивается у каждого десятого, при этом у каждого десятого из заболевших – по фульминантному (молниеносному) типу. Прогноз считается благоприятным, однако в статистике смертности от паразитарных заболеваний амебная дизентерия занимает второе место, уступая лишь малярии. Летальность составляет один-два случая на тысячу заболевших.
Жизненный цикл
Просветная форма получила свое название в силу того, что обитает она в межстеночном пространстве толстой кишки, обычно в проксимальных (центральных, средних) отделах, питаясь перевариваемым детритом и представителями симбиотического кишечного микробиома. Для организма-хозяина это означает бессимптомное носительство. Большая вегетативная форма, или forma magna, является эритрофагом: она кормится захватом и поглощением красных кровяных телец – эритроцитов. Forma magna способна выделять ферменты, поражать поверхностную слизистую оболочку и, кроме того, внедряться более глубоко, в незащищенные подслизистые уровни кишечной стенки, где метаморфирует в сугубо патогенную тканевую форму. Если это произошло, то по мере дальнейшего размножения амебы (уже как внутритканного паразита) развивается специфическая клиника. Тканевая форма амебы остается эритрофагом, однако также продуцирует ферменты-цитолизины, которые растворяют и разлагают клетки кишечной стенки, вследствие чего образуются абсцессы, а после их вскрытия в просвет кишки – глубокие язвы, заполненные творожистым гнойно-некротическим содержимым; таким образом, амебиаз фактически приобретает характер язвенного колита. Утяжеляющим фактором является инокуляция: в образовавшиеся язвенные дефекты может дополнительно проникнуть иная патогенная микрофлора, попавшая в кишечник. При длительном или хроническом течении формируются гранулемы (амебиомы) – плотные опухолевидные образования из клеток соединительной ткани.
Заражение
Таким образом, основные пути заражения – алиментарный (с зараженными продуктами питания или водой) и контактно-бытовой. Инфицирование гистолитической и другими патогенными амебами может также произойти при купании в загрязненных стоячих водоемах. Прослеживается определенная сезонность (весна-лето) и эндемичность: амебиаз особенно распространен в теплых и жарких странах третьего мира, которые характеризуются низким уровнем социально-экономического развития, санитарно-гигиенической культуры и системы здравоохранения. В более развитых северных государствах вспышки заболеваемости ранее отмечались спорадически; как правило, очагом становились учреждения закрытого типа, где большие группы людей находятся в постоянном тесном контакте, а основной причиной оказывалась зараженная цистами вода. Однако в последнее время, – с интенсификацией трудовых и вынужденных миграционных процессов, делового и культурного туризма, – во многих регионах, ранее амебиазу практически не подверженных, отмечается достоверная тенденция к учащению отдельных клинических случаев и эпидемических вспышек.
Главными факторами риска выступает несоблюдение элементарной гигиены, потребление необработанной пищи и ослабленный иммунитет.
Симптоматика
В отсутствие лечения амебиаз из острой фазы за 1-1,5 мес приобретает хроническое (иногда непрерывное) течение, которое характеризуется чередованием ремиссий и рецидивов; в такой форме амебная дизентерия может протекать до десяти и более лет, если раньше не разовьется одно из присущих этому заболеванию тяжелых осложнений, – например, язвенное прободение кишечной стенки с последующим перитонитом, кишечное кровотечение, нагноение гранулематозных инфильтратов, фиброзная облитерация просвета (вплоть до непроходимости кишечника), гангрена толстой кишки и т.д.
Внекишечные формы проявляются симптоматикой, специфической для поражаемых органов, т.е. клиникой гепатита, плевропневмонии, абсцесса легкого и т.д. Кожная форма обычно присоединяется к кишечной (у длительно болеющих и потому тотально астенизированных пациентов), локализуется, в основном, в перианальной области и характеризуется глубокими зловонными язвами, кишащими вегетативной формой возбудителя. В редких случаях гистолитическая амеба попадает в головной мозг или околосердечную сумку, и практически всегда такая экспансия стремительно приводит к летальному исходу.
Диагностика
При остром начале или обострении заболевания убедительным свидетельством его амебной этиологии является обнаружение тканевой формы возбудителя в каловых массах (присутствие только цист и/или просветных форм не может считаться достаточным для постановки диагноза, поскольку доказывает лишь носительство). Однако микроскопия, учитывая нестойкость тканевой и большой вегетативной форм гистолитической энтамебы, должна производиться непосредственно после дефекации (в первые 10-15 минут). Кроме того, диагностику может усложнить присутствие в толстом кишечнике других, морфологически близких, но условно-патогенных или непатогенных амебных популяций.
В ходе ректороманоскопии или колоноскопии (сигмоидоскопии) на слизистой кишечника с 4-5 дня от манифестации обнаруживаются первые небольшие, до 0,5 см, гнойные изъязвления, которые к концу второй недели увеличиваются в количестве и размерах, достигая 2 см в диаметре и образуя, таким образом, характерную для заболевания картину. Однако очаг поражения может находиться выше предела досягаемости эндоскопических зондов, т.е. отсутствие наблюдаемых язв не исключает присутствия гистолитической амебы выше по кишечнику. Кроме того, даже при обнаружении изъязвленных участков необходима дифференциальная диагностика с другими видами язвенных колитов. Поэтому микроскопическое исследование препаратов кала, мокроты, гнойного отделяемого и т.д. повторяют многократно, пока возбудитель не будет установлен однозначно. По показаниям, – например, для выявления абсцессов в других зонах, – применяют ультразвуковое исследование, томографические методы, биопсию с последующим гистологическим анализом. Большое диагностическое значение имеют серологические методы, в основе которых лежит поиск специфических по отношению к гистолитической амебе антител (анализы РНИФ, ИФА и т.п.), однако эффективность этих методов существенно выше при внекишечной форме амебиаза (вероятность обнаружения патогена составляет 95% против 75% при кишечном амебиазе). Иногда для генетической идентификации возбудителя применяют полимеразную цепную реакцию (ПЦР).
Однако первоочередным шагом при подозрении на паразитарный характер состояния становится сбор и изучение подробных анамнестических сведений: где и как долго пребывал пациент в последнее время, купался ли в водоемах, употреблял ли во время зарубежных поездок местную экзотическую пищу и т.д.
Лечение
С 1960 года стандартом в лечении амебиазов, а также многих других протозойных и некоторых бактериальных инвазий, становится специально разработанная группа 5‑нитроимидазолов: метронидазол, более поздний тинидазол и другие производные (сегодня выпускается множество дженериков с теми же действующими веществами, но под собственными названиями, приводить которые здесь нет смысла). Кроме того, позже были созданы антипротозойные препараты прицельного действия, особо эффективные в отношении тканевых либо просветных форм (соответственно, тканевые и просветные амебоциды). После успешной эрадикации тканевой формы системным амебоцидом рекомендуется во избежание рецидивов применить просветный амебоцид. В некоторых случаях как основной или дополнительный препарат применяют антибиотики тетрациклинового ряда.
Больной госпитализируется; лечение в изолированном инфекционном боксе продолжается до тех пор, пока вероятность присутствия возбудителя в кишечнике не достигнет приемлемого минимума.
В запущенных и/или осложненных случаях зачастую не обойтись без жизнесохраняющего хирургического вмешательства.
Следует заметить, что собственная иммунная система пациента оказывает активное сопротивление гистолитической амебе, вырабатывая антитела и пытаясь ее уничтожить. Однако даже после успешного и полного излечения стойкий иммунитет не формируется, т.е. повторное инфицирование с развитием той же (или более тяжелой) клинической картины является вполне возможным.
Острые кишечные инфекции (ОКИ) — это большая группа инфекционных заболеваний человека с энтеральным механизмом заражения, вызываемых патогенными и условно-патогенными бактериями, вирусами или простейшими
Острые кишечные инфекции (ОКИ) — это большая группа инфекционных заболеваний человека с энтеральным (фекально-оральным) механизмом заражения, вызываемых патогенными (шигеллы, сальмонеллы и др.) и условно-патогенными бактериями (протеи, клебсиеллы, клостридии и др.), вирусами (рота-, астро-, адено-, калицивирусы) или простейшими (амеба дизентерийная, криптоспоридии, балантидия коли и др.).
Ведущим компонентом терапии ОКИ является рациональное лечебное питание, адаптированное к возрасту ребенка, характеру предшествующего заболевания и вскармливания.
Цель диетотерапии — уменьшение воспалительных изменений в желудочно-кишечном тракте, нормализация функциональной активности и процессов пищеварения, максимальное щажение слизистой оболочки кишечника.
Основные требования к диете при ОКИ:
включение в диеты низко- и безлактозных продуктов и кисломолочных продуктов, обогащенных бифидо- и лактобактериями;
снижение объема пищи в первые дни болезни на 15–20% (при тяжелых формах до 50%) от физиологической потребности;
Из диеты исключаются стимуляторы перистальтики кишечника, продукты и блюда, усиливающие процессы брожения и гниения в кишечнике: сырые, кислые ягоды и фрукты, соки, сырые овощи, сливочное и растительные масла (в чистом виде), сладости, свежая выпечка. Не следует давать бобовые, свеклу, огурцы, квашеную капусту, редис, апельсины, груши, мандарины, сливы, виноград. Не рекомендуется овсяная крупа, так как она усиливает бродильные процессы. Должны быть исключены из питания жирные сорта мясных и рыбных продуктов (свинина, баранина, гусь, утка, лосось и др.).
Цельное молоко в остром периоде кишечных инфекций назначать не следует, так как оно усиливает перистальтику кишечника и бродильные процессы в результате нарушения расщепления молочного сахара (лактозы), что сопровождается усилением водянистой диареи и вздутием живота.
В первые дни заболевания исключается также черный хлеб, способствующий усилению перистальтики кишечника и учащению стула.
При уменьшении проявлений интоксикации, прекращении рвоты и улучшении аппетита вводится творог, мясо (говядина, телятина, индейка, кролик в виде котлет, фрикаделек, кнелей), рыба нежирных сортов, яичный желток и паровой омлет. Разрешаются тонко нарезанные сухари из белого хлеба, каши на воде (кроме пшенной и перловой), супы слизистые, крупяные с разваренной вермишелью на слабом мясном бульоне.
В остром периоде заболевания рекомендуется использовать молочнокислые продукты (кефир, ацидофильные смеси и др.). Молочнокислые продукты за счет активного действия содержащихся в них лактобактерий, бифидобактерий, конечных продуктов протеолиза казеина (аминокислот и пептидов, глутаминовой кислоты, треонина и др.), увеличенного количества витаминов В, С и др. способствуют улучшению процессов пищеварения и усвоению пищи, оказывают стимулирующее влияние на секреторную и моторную функции кишечника, улучшают усвоение азота, солей кальция и жира. Кроме того, кефир обладает антитоксическим и бактерицидным действием на патогенную и условно-патогенную флору за счет наличия молочной кислоты и лактобактерий. Однако длительное применение только кефира или других молочнокислых смесей нецелесообразно, поскольку эти продукты бедны белками и жирами. Лечебным кисломолочным продуктом является Лактофидус — низколактозный продукт, обогащенный бифидобактериями.
При лечении детей с ОКИ в периоде выздоровления необходимо широко использовать плодово-овощные продукты (яблоки, морковь, картофель и др.), так как они содержат большое количество пектина. Пектин — коллоид, обладающий способностью связывать воду и набухать, образуя пенистую массу, которая, проходя по кишечному тракту, адсорбирует остатки пищевых веществ, бактерий, токсических продуктов. В кислой среде от пектина легко отщепляется кальций, оказывая противовоспалительное действие на слизистую оболочку кишечника. Фрукты и овощи содержат органические кислоты, обладающие бактерицидным действием, а также большое количество витаминов, глюкозу, фруктозу, каротин и др. Применение вареных овощей и печеных фруктов уже в остром периоде кишечных инфекций способствует более быстрому исчезновению интоксикации, нормализации стула и выздоровлению.
Питание детей грудного возраста
В последнее время в клинике кишечных инфекций предпочтение отдается назначению детям, находящимся на искусственном вскармливании, низко- и безлактозных смесей (Низколактозный Нутрилон, Фрисопеп, Хумана ЛП+СЦТ, соевые смеси). При тяжелых формах ОКИ и развитии гипотрофии широко используются гидролизованные смеси (Нутрилон Пепти ТСЦ, Нутримиген, Алфаре, Прегестимил и др.), способствующие быстрому восстановлению процессов секреции и всасывания в кишечнике и усвоению белков, жиров и углеводов, что предупреждает развитие ферментопатии в исходе кишечной инфекции (табл).
По нашим данным, в результате клинико-лабораторной оценки влияния низколактозных смесей на клиническую картину и состояние микробиоценоза кишечника при вирусных диареях у детей раннего возраста был получен положительный эффект стимуляции функциональной активности нормальной и, в первую очередь, сахаролитической микрофлоры (по стабилизации показателей уксусной, масляной и пропионовой кислот), а также регулирующее влияние на процессы метаболизма углеводов и жиров в острый период заболевания. Клинический эффект заключался в быстром и стойком купировании основных проявлений болезни: рвоты, диареи, абдоминального синдрома и эксикоза, что наряду с хорошей переносимостью позволило рекомендовать низколактозные смеси для использования в качестве лечебного питания у детей раннего возраста в острый период кишечных инфекций вирусной этиологии.
При разгрузке в питании ежедневно объем пищи увеличивается на 20–30 мл на одно кормление и соответственно изменяется кратность кормлений, то есть увеличивается интервал между кормлениями. При положительной динамике заболеваний и улучшении аппетита необходимо довести суточный объем пищи до физиологической потребности не позднее 3–5 дня от начала лечения.
Детям 5–6 месяцев при улучшении состояния и положительной динамике со стороны желудочно-кишечного тракта назначается прикорм кашей, приготовленной из рисовой, манной, гречневой круп на половинном молоке (или воде при ротавирусной инфекции). Кашу назначают в количестве 50–100–150 г в зависимости от возраста ребенка и способа вскармливания до заболевания. Через несколько дней добавляют к этому прикорму 10–20 г творога, приготовленного из кипяченого молока, а затем — овощные пюре, ягодный или фруктовый кисель в количестве 50–100–150 мл, соки.
Питание детей 7–8 месяцев должно быть более разнообразным. При улучшении состояния им назначают не только каши, творог и кисели, но и овощные пюре, желток куриного яйца на 1/2 или 1/4 части, затем бульоны, овощной суп и мясной фарш. В каши и овощное пюре разрешается добавлять сливочное масло. Желток (яйцо должно быть сварено вкрутую) можно давать отдельно или добавлять его в кашу, овощное пюре, суп.
Питание детей старше года строится по такому же принципу, как и у детей грудного возраста. Увеличивается лишь разовый объем пищи и быстрее включаются в рацион продукты, рекомендуемые для питания здоровых детей этого возраста. В остром периоде болезни, особенно при наличии частой рвоты, следует провести разгрузку в питании. В первый день ребенку назначают кефир по 100–150–200 мл (в зависимости от возраста) через 3–3,5 часа. Затем переходят на питание, соответствующее возрасту, но с исключением запрещенных продуктов. В остром периоде заболевания всю пищу дают в протертом виде, применяется паровое приготовление вторых блюд. Крупу для приготовления каши и гарнира, овощи разваривают до мягкости. Набор продуктов должен быть разнообразным и содержать кисломолочные смеси, кефир, творог, сливки, сливочное масло, супы, мясо, рыбу, яйца, картофель, свежие овощи и фрукты. Можно пользоваться овощными и фруктовыми консервами для детского питания. Из рациона исключают продукты, богатые клетчаткой и вызывающие метеоризм (бобовые, свекла, репа, ржаной хлеб, огурцы и др.). Рекомендуются арбузы, черника, лимоны, кисели из различных ягод, желе, компоты, муссы, в которые желательно добавлять свежевыделенный сок из клюквы, лимона.
Правильно организованное питание ребенка с кишечной инфекцией с первых дней заболевания является одним из основных условий гладкого течения заболевания и быстрого выздоровления. Неадекватное питание и погрешности в диете могут ухудшить состояние ребенка, равно как и длительные ограничения в питании. Важно помнить, что на всех этапах лечения ОКИ необходимо стремиться к полноценному физиологическому питанию с учетом возраста и функционального состояния желудочно-кишечного тракта ребенка.
Значительные трудности в диетотерапии возникают у детей с развитием постинфекционной ферментопатии, которая развивается в разные сроки заболевания и характеризуется нарушением переваривания и всасывания пищи вследствие недостатка ферментов.
При ОКИ, особенно при сальмонеллезе, кампилобактериозе, протекающих с реактивным панкреатитом, наблюдается нарушение всасывания жира и появление стеатореи — стул обильный с блеском, светло-серый с неприятным запахом. Диетотерапия при стеаторее проводится с ограничением жира в рационе, но не более 3–4 мг/кг массы тела в сутки для детей первого года жизни. Это достигается путем замены части молочных продуктов специализированными низкожировыми продуктами (Ацидолакт) и смесями зарубежного производства, в состав которых в качестве жирового компонента входят среднецепочечные триглицериды, практически не нуждающиеся в панкреатической липазе для усвоения (Нутрилон Пепти ТСЦ, Хумана ЛП+СЦТ, Алфаре, Прегестимил, Фрисопеп и др.). При появлении признаков острого панкреатита из рациона исключают свежие фрукты, ягоды, овощи, концентрированные фруктовые соки на срок до 1 мес.
При лактазной недостаточности рекомендуется использование адаптированных низколактозных смесей (Низколактозный Нутрилон, Фрисопеп, Хумана ЛП+СЦТ и др.) или соевых смесей (Нутрилон Соя, Фрисосой, Хумана СЛ, Симилак Изомил, Энфамил Соя и др.). При их отсутствии — 3-суточный кефир; детям первых трех месяцев жизни можно давать смесь типа В-кефир, состоящую из 1/3 рисового отвара и 2/3 3-суточного кефира с добавлением 5% сахара (глюкозы, фруктозы), 10% каши на воде, овощных отварах.
В качестве прикорма этим больным дают безмолочные каши и овощные пюре на воде с растительным или сливочным маслом, отмытый от сыворотки творог, мясное пюре, печеное яблоко. Схемы введения прикормов могут быть индивидуализированы, следует обратить внимание на раннее назначение мясного (суточная доза в 3–4 приема). Избегают применения сладких фруктовых соков, продуктов, повышающих газообразование в кишечнике и усиливающих перистальтику (ржаной хлеб, белокочанная капуста, свекла и другие овощи с грубой клетчаткой, кожура фруктов, чернослив, сухофрукты). Длительность соблюдения низколактозной диеты индивидуальна — от 1,5–2 до 6 месяцев.
После тяжелых кишечных инфекций может возникнуть непереносимость не только лактозы, но и других дисахаридов, реже — полная углеводная интолерантность (глюкозо-галактозная мальабсорбция), при которой у больных отмечается выраженная диарея, усиливающаяся при применении смесей и продуктов, содержащих дисахариды, моносахариды и крахмал (молочные и соевые смеси, крупы и практически все фрукты и овощи). Это чрезвычайно тяжелое состояние, приводящее к обезвоживанию и прогрессирующей дистрофии, требует строгого безуглеводного питания и парентерального введения глюкозы или полного парентерального питания. В отдельных случаях возможно пероральное введение фруктозы. При индивидуальной переносимости в диете сохраняются белок и жиросодержащие продукты: нежирное мясо — индейка, конина, говядина, кролик, растительное масло, ограниченный ассортимент овощей с низким содержанием сахарозы и глюкозы — цветная и брюссельская капуста, шпинат, стручковая фасоль, салат.
Дефицит белка возникает за счет нарушения утилизации, всасывания либо за счет потери эндогенного белка, особенно у детей с исходной гипотрофией. Коррекция потерь белка проводится путем назначения гидролизованных смесей (Нутрилон Пепти ТСЦ, Нутримиген, Алфаре, Прегестимил, Фрисопеп и др.).
При длительных постинфекционных диареях, особенно у детей, получавших повторные курсы антибактериальных препаратов, возможно развитие вторичной пищевой аллергии, сопровождающейся сенсибилизацией к белкам коровьего молока, реже — к яичному протеину, белкам злаковых культур. Такие нарушения могут возникать не только у детей с аллергическим диатезом, но и у больных без отягощенного преморбидного фона. Клинически постинфекционная пищевая аллергия проявляется гиперчувствительностью к ранее хорошо переносимым продуктам — молочным смесям, молочным кашам, творогу и др. У детей отмечаются боли в животе, вздутие после кормления, срыгивания, жидкий стул с мутной стекловидной слизью, иногда с прожилками крови, при копрологическом исследовании в кале обнаруживаются эозинофилы. Характерна остановка прибавки массы тела, вплоть до развития гипотрофии.
При выявлении аллергии к белкам коровьего молока в питании детей первого года жизни используются смеси на соевой основе (Нутрилак Соя, Нутрилон Соя, Фрисосой, Хумана СЛ, Энфамил Соя и др.) и на основе гидролизатов белка (Нутрилон Пепти ТСЦ, Нутримиген, Прегестимил, Фрисопеп и др.).
Отсутствие специализированных продуктов не является непреодолимым препятствием в организации безмолочного рациона. Элиминационная диета в этом случае составляется на основе безмолочных протертых каш (рисовой, гречневой, кукурузной), фруктовых и овощных пюре, картофеля, кабачков, цветной капусты, тыквы, из печеного яблока, банана, растительного и сливочного масла, мясного пюре. При этом необходимо учитывать физиологические потребности ребенка в основных пищевых веществах и энергии. Мясное пюре, как основной источник белка, при отсутствии специализированных смесей можно назначать с 2–3-месячного возраста. Предпочтительно использовать конину, мясо кролика, птицы, постную свинину, а также диетические мясные консервы — Конек-Горбунок, Чебурашка, Петушок, Пюре из свинины и др.
У детей старше года принцип составления рациона тот же. При назначении безмолочной диеты необходимо полностью компенсировать недостающее количество животного белка протеинами мяса, соевых смесей, а также исключить из диеты продукты, обладающие повышенной сенсибилизирующей активностью (шоколад, рыба, цитрусовые, морковь, свекла, красные яблоки, абрикосы и другие плоды оранжевой или красной окраски, орехи, мед). При постинфекционной пищевой аллергии срок соблюдения указанной диеты составляет не менее 3 месяцев, а чаще — от 6 до 12 месяцев. Эффект от элиминационной диеты оценивается по исчезновению симптомов заболевания, прибавке массы тела, нормализации стула.
Л. Н. Мазанкова, доктор медицинских наук, профессор Н. О. Ильина, кандидат медицинских наук Л. В. Бегиашвили РМАПО, Москва

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.

Кишечная амёба – неболезнетворный микроорганизм, который обитает в просвете нижнего отдела тонкого и верхнем толстого кишечника. Она является постоянным паразитирующем организмом, но может существовать и вне его.
Во внешней среде кишечная амёба хорошо сохраняется, в отдельных случаях может размножаться, но всё же благоприятным местом для неё является кишечник человека или другого живого организма. В качестве питания используются неживые органические субстраты (бактерии, остатки различной пищи), при этом амёба не выделяет фермент, расщепляющий белки на аминокислоты. Благодаря этому в большинстве случаев не происходит проникновения в стенку кишечника, а значит не наносится вред хозяину. Такое явление называется носительством. При ослаблении иммунитета и стечении других обстоятельств амёба проникает под слизистую кишечника и усиленно начинает размножаться.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Структура кишечной амёбы
Кишечная амёба относится к типу простейших. Структура кишечной амёбы состоит из тела и ядра. В теле находится протоплазма (жидкая субстанция со специализированными живыми структурами) и одним, двумя, редко несколькими ядрами. Протоплазма имеет два слоя: внутренний (эндоплазма) и наружный (эктоплазма). Ядро напоминает пузырёк.
Есть две фазы существования кишечной амёбы: вегетативной особи (трофозоитов) и цисты. У трофозоитов есть хорошо различимое ядро диаметром 20-40мкм. Амёба постоянно меняет свою форму из-за появления ложноножек, с помощью которых происходит передвижение и захват пищи. Благодаря форме псевдоподий, ядер, их количеству, идентифицируется тот или другой вид амёб. Движения её медленные, напоминают топтание на месте. Размножение происходит путём деления вначале ядер, потом протоплазмы.

[11], [12], [13], [14], [15], [16], [17], [18]
Жизненный цикл кишечной амёбы
Жизненный цикл кишечная амёба проходит, начиная с заражения организма-хозяина фекально-оральным путём. С немытыми руками, овощами, фруктами, благодаря различным переносчикам (мухам, тараканам) цисты амёбы попадают во внутрь человека. Благодаря своей оболочке, они неповреждёнными проходят агрессивную для них среду желудка, двенадцатиперстной кишки, попадая в кишечник. Его ферменты растворяют оболочку, давая выход кишечной амёбе.
Вегетативная стадия развития имеет следующие формы: тканевую, просветную и предцистную. Из них тканевая фаза самая подвижная, именно в это время амёба наиболее инвазивна. Две другие – малоподвижны. Из просветной формы часть амёб переходит в предцистную, другая внедряется под слизистую кишки, образуя патогенную тканевую форму. В результате своей жизнедеятельности последняя выделяет цитолизины, расплавляющие ткани и создающие условия для размножения. Циста же неподвижна, во время дефекации она покидает кишечник. При сильном заражении до 300млн особей в день покидает организм.

[19], [20], [21]
Цисты кишечной амёбы
После нескольких циклов размножений, при наступлении неблагоприятных условий для вегетативной особи она покрывается оболочкой, образуя цисту. Цисты кишечной амёбы имеют круглую или овальную форму, размером 10-30мкм. Иногда в них содержится запас питательных веществ. На разной стадии развития цисты имеют разное количество ядер: от двух до восьми. Выходят наружу с калом, при сильном заражении в больших количествах и имеют способность долго сохраняться. Попадая опять внутрь живого организма они лопаются, превращаясь в амёбу.

[22], [23], [24], [25], [26], [27], [28], [29]
Симптомы
Большое скопление кишечной амёбы, что бывает в случае снижения иммунитета человека после перенесенных стрессов, вирусных инфекций, респираторных заболеваний, вызывает болезнь, которая носит название амебиаз. Чаще она бывает кишечной и внекишечной. Кишечная приводит к язвенным поражениям толстого кишечника и, как следствие, затяжному протеканию. В этом случае амёба вместе с кровью проникает в другие внутренние органы, чаще в печень, и повреждает их, вызывая внекишечные абсцессы.
Симптомами амёбиаза, в первую очередь, является жидкий стул, который может быть малинового цвета. Болевые ощущения возникают в правой верхней части живота, т.к. локализация этих организмов происходит в верхнем отделе толстого кишечника. Может подняться температура, бить озноб, появиться желтуха.
Кишечная амёба у детей
Механизм заражения кишечной амёбы у детей такой же, как и у взрослых, а источник - немытые руки, мухи, грязные игрушки и бытовые предметы. Амебиаз может протекать бессимптомно, манифестно, в острой или хронической форме. Бессимптомная незаметна для ребёнка. О манифестной форме свидетельствует ухудшение самочувствия, слабость, снижение аппетита. Температура может быть нормальной или немного повышаться. Появляется понос, дефекация происходит несколько раз в день, учащаясь до 10-20 раз. В зловонном жидком кале появляется слизь с кровью. Малиновым цвет кала бывает не всегда. Отмечаются приступообразные боли в правой стороне живота, усиливающиеся перед опорожнением. Без лечения острая стадия длится месяц-полтора, постепенно затихая. После стадии ремиссии вспыхивает с новой силой.

[30], [31], [32], [33], [34], [35], [36], [37]
Диагностика
Диагностика кишечной амёбы происходит, начиная с выяснения анамнеза заболевшего: какие симптомы, как давно появились, пребывал ли пациент в странах с жарким влажным климатом и низкой санитарной культурой. Именно там амёба широко распространёна и именно оттуда может быть завезена.
Проводится анализ крови, кала и мочи. Возбудители обнаруживаются в кале, при этом важно выявить вегетативную форму амёбы. Анализ необходимо сделать не позже 15 минут после испражнения. Также амёбы могут выявляться в тканях при ректороманоскопии – визуальном осмотре слизистой прямой кишки с помощью специального прибора. Ректороманоскоп даёт возможность увидеть язвы или свежие рубцы на её внутренней поверхности. Не выявление следов поражений слизистой ещё не говорит об отсутствии амебиаза, т.к. они могут находиться в более высоких отделах кишечника. Существует анализ крови на выявление антител к амёбам, он подтвердит или опровергнет диагноз.
С помощью УЗИ, рентгеноскопии, томографии определяют локализацию абсцессов при внекишечном амебиазе. Кишечный амебиаз дифференцируют с язвенным колитом, а амёбные абсцессы - с абсцессами другой природы.
Отличие кишечной амёбы от дизентерийной
Отличие кишечной амёбы от дизентерийной в её структуре: оболочка дизентерийной двуконтурная, преломляющая свет, у неё 4 ядра (у кишечной – 8), расположенные эксцентрично, в неё включены кровяные тельца, чего нет в кишечной. Дизентерийная амёба более энергична в передвижениях.

[38], [39], [40], [41], [42], [43], [44], [45], [46], [47]
Лечение
Лечение кишечной амёбы проводится в зависимости от тяжести и формы болезни. Применяемые препараты для устранения недуга делятся на амебоциды универсального действия (метронидазол, тинидазол) и прямого, направленного на конкретную локализацию возбудителя: в просвете кишечника (хиниофон (ятрен), мексаформ и др.); в стенке кишечника, печени и других органах (эметина гидрохлорид, дегидроэметин и др.). Антибиотики тетрациклинового ряда – это косвенные амебоциды, поражающие амёб в просвете кишечника и в его стенках.
Бессимптомный кишечный амебиаз лечат ятреном. Во время острой вспышки назначается метронидазол или тинидазол. При тяжёлой форме совмещают метронидазол с ятреном или антибиотиками тетрациклинового ряда, возможно добавление дегидроэметина. В случае внекишечных абсцессов лечат метронидазолом с ятреном или хингамином с дегидроэметина. Диспансерное наблюдение проводится в течение года.
Профилактика кишечной амёбы
Лучшей профилактикой кишечной амёбы является соблюдение личной гигиены – частое мытьё рук, сырых овощей и фруктов под проточной водой, не употребление воды из-под крана или открытых источников. Особенно строго этих правил следует придерживаться во время поездок в страны с жарким и влажным климатом.
Изоляция заболевших до полного выздоровления – ещё одна необходимая мера профилактики. Если возбудитель выявлен у работника общепита, дезинфицируется всё помещение.

[48], [49], [50]
Прогноз
Своевременное выявление кишечной амёбы даёт благоприятный прогноз лечения. Длительное заражение без применения лечения осложняется образованием спаек в кишечнике, прободением амёбных язв, перитонитом, что очень опасно.
После излечения недуга повторного заражения может не быть или болезнь проходит легко, т.к. вырабатывается иммунитет. В случае возникновения внекишечных абсцессов и поздней их диагностики возможен летальный исход.

[51], [52], [53], [54], [55], [56], [57], [58]

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.

Дизентерийная амеба представляет собой простейший паразит, который, попадая во внутрь человека, вызывают тяжёлые патологии: амебную дизентерию и амебный колит. Как и другие амебы, они приспособились к паразитирующему существованию внутри человека в толстой кишке, но при определённых условиях могут вызвать тяжёлое заболевание — амебиазу. Описаны впервые в 1875 году учёным Лёшем, широко распространены по всему земному шару, но больше всего подвержены заболеванию обитатели тропических и субтропических стран. В других климатических поясах люди чаще являются носителями дизентерийной амебы, а вспышки амебиазы встречаются довольно редко.

[1], [2], [3], [4]
Структура дизентерийной амебы
Структура дизентерийной амебы следующая: это особь, постоянно меняющая свои контуры, величиной 20-30мкм, имеет сферическое ядро внутри эндоплазмы — внутреннего содержимого, обтянута эктоплазмой — внешним слоем клеточной цитоплазмы, нет скелета, очень подвижная, передвигается при помощи своеобразных отростков, носящих название псевдоподии или ложноножки. Движение её напоминает перетекание из одного очертания в другое. Существуют просветная, тканевая, большая вегетативная форма амебы и в виде цист. Размер просветной около 20мкм, находится она в просвете верхнего отдела толстого кишечника, питается его бактериями и не приносит никакого вреда носителю.

[5], [6], [7], [8], [9]
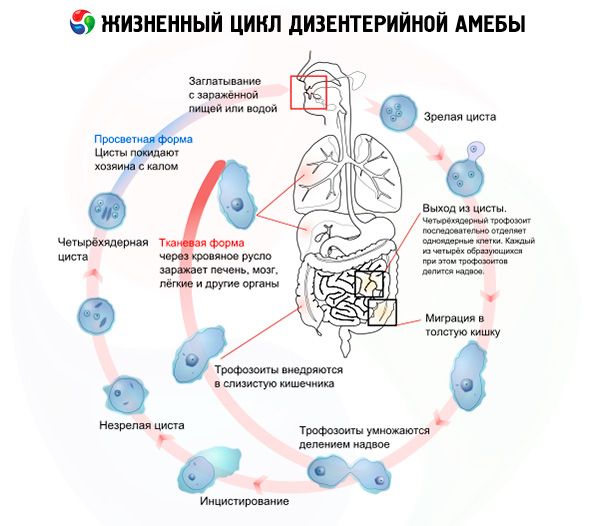
Жизненный цикл дизентерийной амебы
Жизненный цикл дизентерийной амебы начинается при попадании в желудочно-кишечный тракт. Пути заражения дизентерийной амебой фекально-оральные, бытовые. Вместе с фекалиями цисты попадают в окружающую среду, за сутки их выделяется более 300млн. Они проявляют большую устойчивость к температурным перепадам и другим неблагоприятным воздействиям. Так, цисты способны в течение месяца сохраняться при температуре 20ºС, неделю во влажной и затемнённой среде, до недели в охлаждённой пище, несколько месяцев при минусовых показателях. Попадают внутрь человека с грязными руками, немытыми продуктами, заражённой водой, путём тактильного контакта с руками больного человека. Их переносчиками бывают мухи и тараканы. Факторами, сопутствующими развитию патологии, являются беременность, дефицит белка, дисбактериоз, глисты — всё то, что снижает иммунитет.

[10], [11], [12], [13]
Циста дизентерийной амебы
Цисты дизентерийной амебы появляются из вегетативной после затихания острой фазы болезни. Часть их превращается в просветную, другие, оказываясь в среде сгущённых фекалий, становятся меньше, покрываются оболочкой и инцистируются. Они имеет 4 ядра и устроены так же, как и ядра вегетативной формы. Незрелые цисты могут иметь от одного до трёх ядер. Это самая жизнестойкая форма дизентерийной амебы, способная выжить в неблагоприятной внешней среде и, попав внутрь человека, возобновить жизненный цикл.

[14], [15], [16]
Инвазионная стадия дизентерийной амебы
Инвазионная стадия дизентерийной амебы характеризуется инкубационным периодом, который длится до двух недель. В это время происходит движение цист по отделам кишечника. По пути своего продвижения они внедряются в его слизистую. При этом более всего подвержены поражению поперечно-ободочный и нисходящий отделы толстого кишечника. На этом этапе двигаясь, цисты превращаются в вегетативную форму, содержащую в себе разрушительные для стенок кишечника ферменты - пепсин и трипсин. Это помогает паразиту внедряться в его слои, вплоть до мышечных, что становится ощутимым для человека.
Тканевая форма дизентерийных амеб
Тканевая форма дизентерийной амебы образуется при внедрении просветной в стенки кишечника. До сих пор учёные не выяснили причину, почему это происходит. Но на этой стадии амеба наносит повреждения слизистой оболочке толстой кишки. Именно эту форму её существования обнаруживают у больных на амебиаз. Размножаясь, она провоцирует образование язв на стенках кишечника, которые приводят к скоплению гноя, крови, слизи. Создаются условия для превращения просветных и тканевых форм в большую вегетативную. Они увеличиваются до 30мкм и способны поглощать эритроциты. Выходя наружу, вегетативная форма погибает.
Симптомы
С момента повреждения стенок проявляются клинические симптомы дизентерийной амебы. Признаки острого амебиаза нарастают постепенно с очевидной динамикой. Вначале учащается стул до 4-6 раз в сутки, каловые массы жидкой консистенции со слизью, имеющие резкий и неприятный запах. Постепенно походы в туалет всё увеличиваются и могут достичь 20 раз, появляются ложные позывы на дефекацию, в стекловидной слизи обнаруживаются кровяные сгустки. Повышается температура тела до 38ºС, которая держится несколько дней, живот вздут и болезненный. Лечение заболевания может длиться до полутора месяца, если же его не проводить, то наступает ремиссия и патология переходит в хроническую форму. Её симптомы выражаются в белом налёте на языке, неприятном запахе изо рта, плохом аппетите, похудении, признаках витаминодефицита (выпадении волос, ломкости ногтей, бледности кожи), болезненности живота. Со временем могут проявляться нарушения со стороны сердца и печени.

[17], [18], [19], [20], [21]
Диагностика
Диагностика проводится по методу от простого к более сложному и первоначально основывается на рассказе пациента о симптоматике: частоте и характере стула, болевых ощущениях, динамике развития болезни, а также измеряется температура. Далее берётся материал для лабораторных исследований. Если для этого нет возможности получить испражнения, с помощью эндоскопии берут биоптаты, а также исследуют стенки кишечника на предмет их повреждения, наличия язв. В качестве дополнительных методов прибегают к УЗИ почек, органов брюшной полости для оценки их состояния.
Лабораторная диагностика
Лабораторная диагностика заключается в исследовании под микроскопом кала, биоптатов, взятых из повреждённых очагов. В случае осложнений берут соскобы из носоглотки. Наличие в исследуемом материале цист и вегетативной формы амебы (трофозоитов) подтверждает диагноз. Для их лучшего их выявления мазки окрашиваются. В биоптатах при амебиазе обнаруживают трофозоиты с эритроцитами внутри. Используют также экспресс-диагностику с помощью метода Кунса для определения антител. Заключается он в том, что мазок окрашивают люминесцирующей сывороткой, бактерии на этом фоне имеют по периметру зелёный ободок. Другой подобный метод - иммуноферментный, основывающийся на реакции антиген-антитело, также используется в лабораторной диагностике.
При выявлении случая заболевания дизентерией необходимо определить источник-носитель, чтобы воспрепятствовать распространению массового заражения. Для этого про дизентерийную амебу сообщают в санитарную службу, которая проводит дезинфекцию точек общественного питания, если заражение произошло там, или других мест. Также исследуют лица, пребывающие в контакте с больным или работающих в общепите на носительство цист.

[22], [23], [24], [25], [26]
Дифференциальная диагностика
Задача дифференциальной диагностики состоит в том, чтобы отличить дизентерийную амебу от кишечной. Их отличие в структуре: оболочка дизентерийной двуконтурная, преломляющая свет, у неё 4 ядра (у кишечной — 8), расположенные эксцентрично, в неё включены кровяные тельца, чего нет в кишечной. Дизентерийная амеба более энергична в передвижениях.
Во многом симптомы схожи с малярией. Её возбудитель - малярийный плазмодий. Переносчиками плазмодия являются комары, а человек — промежуточный хозяин. С укусом насекомого, в отличие от дизентерийной амебы, плазмодий попадает в кровь, а потом в печень, где и происходит бесполое размножение, так называемая тканевая шизогония. В результате многократного деления, которое происходит в инкубационный период, появляется множество дочерних особей, поглощающих гемоглобин и разрушающих клетки печени. Малярия сопровождается тяжёлыми приступами лихорадки, озноба и признаками интоксикации организма.

[27], [28], [29], [30], [31]
Лечение
Профилактика дизентерийной амебы
Специальных профилактических мероприятий не существует. Лучшей профилактикой является соблюдение санитарно-гигиенических правил: частое мытьё рук, овощей и фруктов, кипячение питьевой воды, предотвращение попадания на грядки фекалий из туалетов, борьба с тараканами. При выявлении вспышек заболеваний важно выявить носителей дизентерийной амебы.

[32], [33]
Прогноз
Прогноз амебиаза при своевременно начатом лечении благоприятный. В случае, если состояние пациента осложнено прорывом абсцессов, кишечным кровотечением, сужением участков кишечника или же проникновением дизентерийных амеб в другие органы: печень, мозг, лёгкие, то возможен летальный исход.

[34], [35], [36], [37]
Интересные факты
Известно, что 50млн. людей на Земле заражены дизентерийной амебой. И если учесть, что во многих странах Африки не ведётся никакой учёт заболеваемости, а среда для распространения амебиаза самая подходящая, то не трудно представить масштабы распространения. Статистика утверждает, что ежегодно от этого заболевания умирает около 100тыс. человек. Интересен тот факт, что учёные до сих пор не могут понять, почему в одних организмах особи мирно уживаются с хозяином, в других — агрессивно внедряются в ткани его внутренностей, поедая живые клетки и принося существенный вред организму.
Читайте также:

