Что будет если не долечить кишечную инфекцию
Обновлено: 18.04.2024
Что понимают под дисбактериозом? Какие методы диагностики являются современными и достоверными? Какие лекарственные препараты применяются при дисбактериозе? Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых
Что понимают под дисбактериозом?
Какие методы диагностики являются современными и достоверными?
Какие лекарственные препараты применяются при дисбактериозе?
Вкишечнике человека находится свыше 500 различных видов микробов, общее количество которых достигает 10 14 , что на порядок выше общей численности клеточного состава человеческого организма. Количество микроорганизмов увеличивается в дистальном направлении, и в толстой кишке в 1 г кала содержится 10 11 бактерий, что составляет 30% сухого остатка кишечного содержимого.
Нормальная микробная флора кишечника
В тощей кишке здоровых людей находится до 10 5 бактерий в 1 мл кишечного содержимого. Основную массу этих бактерий составляют стрептококки, стафилококки, молочнокислые палочки, другие грамположительные аэробные бактерии и грибы. В дистальном отделе подвздошной кишки количество микробов увеличивается до 10 7 –10 8 , в первую очередь за счет энтерококков, кишечной палочки, бактероидов и анаэробных бактерий. Недавно нами было установлено, что концентрация пристеночной микрофлоры тощей кишки на 6 порядков выше, чем в ее полости, и составляет 10 11 кл/мл. Около 50% биомассы пристеночной микрофлоры составляют актиномицеты, примерно 25% — аэробные кокки (стафилококки, стрептококки, энтерококки и коринеформные бактерии), от 20 до 30% приходится на бифидобактерии и лактобациллы.
Количество анаэробов (пептострептококки, бактероиды, клостридии, пропионобактерии) составляет около 10% в тонкой и до 20% в толстой кишке. На долю энтеробактерий приходится 1% от суммарной микрофлоры слизистой оболочки.
До 90-95% микробов в толстой кишке составляют анаэробы (бифидобактерии и бактероиды), и только 5-10% всех бактерий приходится на строгую аэробную и факультативную флору (молочнокислые и кишечные палочки, энтерококки, стафилококки, грибы, протей).
Кишечные палочки, энтерококки, бифидобактерии и ацидофильные палочки обладают выраженными антагонистическими свойствами. В условиях нормально функционирующего кишечника они способны подавлять рост несвойственных нормальной микрофлоре микроорганизмов.
Площадь внутренней поверхности кишечника составляет около 200 м 2 . Она надежно защищена от проникновения пищевых антигенов, микробов и вирусов. Важную роль в организации этой защиты играет иммунная система организма. Около 85% лимфатической ткани человека сосредоточено в стенке кишечника, где продуцируется секреторный IgA. Кишечная микрофлора стимулирует иммунную защиту. Кишечные антигены и токсины кишечных микробов значительно увеличивают секрецию IgA в просвет кишки.
Расщепление непереваренных пищевых веществ в толстой кишке осуществляется ферментами бактерий, при этом образуются разнообразные амины, фенолы, органические кислоты и другие соединения. Токсические продукты микробного метаболизма (кадаверин, гистамин и другие амины) выводятся с мочой и в норме не оказывают влияния на организм. При утилизации микробами неперевариваемых углеводов (клетчатки) образуются короткоцепочечные жирные кислоты. Они обеспечивают клетки кишки энергоносителями и, следовательно, улучшают трофику слизистой оболочки. При дефиците клетчатки может нарушаться проницаемость кишечного барьера вследствие дефицита короткоцепочечных жирных кислот. В результате кишечные микробы могут проникать в кровь.
Под влиянием микробных ферментов в дистальных отделах подвздошной кишки происходит деконъюгация желчных кислот и преобразование первичных желчных кислот во вторичные. В физиологических условиях от 80 до 95% желчных кислот реабсорбируется, остальные выделяются с фекалиями в виде бактериальных метаболитов. Последние способствуют нормальному формированию каловых масс: тормозят всасывание воды и тем самым препятствуют излишней дегидратации кала.
Дисбактериоз
В понятие дисбактериоза кишечника входит избыточное микробное обсеменение тонкой кишки и изменение микробного состава толстой кишки. Нарушение микробиоценоза происходит в той или иной степени у большинства больных с патологией кишечника и других органов пищеварения. Следовательно, дисбактериоз является бактериологическим понятием. Он может рассматриваться как одно из проявлений или осложнение заболевания, но не самостоятельная нозологическая форма.
Крайней степенью дисбактериоза кишечника является появление бактерий желудочно-кишечного тракта в крови (бактериемия) или даже развитие сепсиса.
Состав микрофлоры кишечника нарушается при болезнях кишечника и других органов пищеварения, лечении антибиотиками и иммунодепрессантами, воздействиях вредных факторов внешней среды.
Клинические проявления дисбактериоза зависят от локализации дисбиотических изменений.
Дисбактериоз тонкой кишки
При дисбактериозе тонкой кишки численность одних микробов в слизистой оболочке тонкой кишки увеличена, а других уменьшена. Отмечается увеличение Eubacterium (в 30 раз), α-стрептококков (в 25 раз), энтерококков (в 10 раз), кандид (в 15 раз), появление бактерий рода Acinetobacter и вирусов герпеса. Уменьшается от 2 до 30 раз количество большинства анаэробов, актиномицетов, клебсиелл и других микроорганизмов, являющихся естественными обитателями кишечника.
Причиной дисбактериоза могут быть: а) избыточное поступление микроорганизмов в тонкую кишку при ахилии и нарушении функции илеоцекального клапана; б) благоприятные условия для развития патологических микроорганизмов в случаях нарушения кишечного пищеварения и всасывания, развития иммунодефицита и нарушений проходимости кишечника.
Повышенная пролиферация микробов в тонкой кишке приводит к преждевременной деконъюгации желчных кислот и потере их с калом. Избыток желчных кислот усиливает моторику толстой кишки и вызывает диарею и стеаторею, а дефицит желчных кислот приводит к нарушению всасывания жирорастворимых витаминов и развитию желчнокаменной болезни.
Бактериальные токсины и метаболиты, например фенолы и биогенные амины, могут связывать витамин В12.
Некоторые микроорганизмы обладают цитотоксическим действием и повреждают эпителий тонкой кишки. Это ведет к уменьшению высоты ворсинок и углублению крипт. При электронной микроскопии выявляется дегенерация микроворсинок, митохондрий и эндоплазматической сети.
Дисбактериоз толстой кишки
Состав микрофлоры толстой кишки может меняться под влиянием различных факторов и неблагоприятных воздействий, ослабляющих защитные механизмы организма (экстремальные климатогеографические условия, загрязнение биосферы промышленными отходами и различными химическими веществами, инфекционные заболевания, болезни органов пищеварения, неполноценное питание, ионизирующая радиация).
В развитии дисбактериоза толстой кишки большую роль играют ятрогенные факторы: применение антибиотиков и сульфаниламидов, иммунодепрессантов, стероидных гормонов, рентгенотерапия, хирургические вмешательства. Антибактериальные препараты значительно подавляют не только патогенную микробную флору, но и рост нормальной микрофлоры в толстой кишке. В результате размножаются микробы, попавшие извне, или эндогенные виды, устойчивые к лекарственным препаратам (стафилококки, протей, дрожжевые грибы, энтерококки, синегнойная палочка).
Клинические особенности дисбактериоза
Клинические проявления чрезмерного роста микроорганизмов в тонкой кишке могут полностью отсутствовать, выступать в качестве одного из патогенетических факторов хронической рецидивирующей диареи, а при некоторых болезнях, например, дивертикулезе тонкой кишки, частичной кишечной непроходимости или после хирургических операций на желудке и кишечнике, приводить к тяжелой диарее, стеаторее и В 12 -дефицитной анемии.
Особенностей клинического течения заболевания у больных с различными вариантами дисбактериоза толстой кишки, по данным бактериологических анализов кала, в большинстве случаев установить не удается. Можно отметить, что больные хроническими заболеваниями кишечника чаще инфицируются острыми кишечными инфекциями по сравнению со здоровыми. Вероятно, это связано со снижением у них антагонистических свойств нормальной микрофлоры кишечника и, прежде всего, частым отсутствием бифидобактерий.
Особенно большую опасность представляет псевдомембранозный колит, развивающийся у некоторых больных, длительно лечившихся антибиотиками широкого спектра действия. Этот тяжелый вариант дисбактериоза вызывается токсинами, выделяемыми синегнойной палочкой Clostridium difficile, которая размножается в кишечнике при угнетении нормальной микробной флоры.
Очень редко наблюдается молниеносное течение псевдомембранозного колита, напоминающее холеру. Обезвоживание развивается в течение нескольких часов и заканчивается летальным исходом.
Таким образом, оценка клинической значимости дисбиотических изменений должна основываться прежде всего на клинических проявлениях, а не только на результатах исследования микрофлоры кала.
Методы диагностики
Диагностика дисбактериоза представляет собой сложную и трудоемкую задачу. Для диагностики дисбактериоза тонкой кишки применяют посев сока тонкой кишки, полученного с помощью стерильного зонда. Дисбактериоз толстой кишки выявляют с помощью бактериологических исследований кала.
Микробная флора образует большое количество газов, в том числе водорода. Это явление используют для диагностики дисбактериоза. Концентрация водорода в выдыхаемом воздухе натощак находится в прямой зависимости от выраженности бактериального обсеменения тонкой кишки. У больных с заболеваниями кишечника, протекающими с хронической рецидивирующей диареей и бактериальным обсеменением тонкой кишки, концентрация водорода в выдыхаемом воздухе значительно превышает 15 ppm.
Для диагностики дисбактериоза применяют также нагрузку лактулозой. В норме лактулоза не расщепляется в тонкой кишке и метаболизируется микробной флорой толстой кишки. В результате количество водорода в выдыхаемом воздухе повышается (рис. 1).
Наиболее частыми бактериологическими признаками дисбактериоза толстой кишки являются отсутствие основных бактериальных симбионтов — бифидобактерий и уменьшение количества молочнокислых палочек. Увеличивается количество кишечных палочек, энтерококков, клостридий, стафилококков, дрожжеподобных грибов и протея. У отдельных бактериальных симбионтов появляются патологические формы. К ним относятся гемолизирующая флора, кишечные палочки со слабо выраженными ферментативными свойствами, энтеропатогенные кишечные палочки и т. д.
Углубленное изучение микробиоценоза показало, что традиционные методы не позволяют получить истинную информацию о состоянии микрофлоры кишечника. Из 500 известных видов микробов в целях диагностики обычно изучаются лишь 10-20 микроорганизмов. Важно, в каком отделе — в тощей, подвздошной или толстой кишках — исследуется микробный состав. Поэтому перспективы разработки клинических проблем дисбактериоза в настоящее время связывают с применением химических методов дифференциации микроорганизмов, позволяющих получить универсальную информацию о состоянии микробиоценоза. Наиболее широко для этих целей используются газовая хроматография (ГХ) и газовая хроматография в сочетании с масс-спектрометрией (ГХ-МС). Этот метод позволяет получить уникальную информацию о составе мономерных химических компонентов микробной клетки и метаболитов. Маркеры такого рода могут быть определены и использованы для детектирования микроорганизмов. Главным преимуществом и принципиальным отличием этого метода от бактериологических является возможность количественного определения более 170 таксонов клинически значимых микроорганизмов в различных средах организма. При этом результаты исследования могут быть получены в течение нескольких часов.
Проведенные нами исследования микробиоценоза в крови и биоптатов слизистой оболочки тонкой и толстой кишок у больных с синдромом раздраженного кишечника позволили обнаружить отклонения от нормы до 30-кратного увеличения или уменьшения многих компонентов. Существует возможность оценки изменений микрофлоры кишечника на основании данных анализа крови методом ГХ-МС-микробных маркеров.
Лечение
Лечение дисбактериоза должно быть комплексным (схема) и включать в себя следующие мероприятия:
- устранение избыточного бактериального обсеменения тонкой кишки;
- восстановление нормальной микробной флоры толстой кишки;
- улучшение кишечного пищеварения и всасывания;
- восстановление нарушенной моторики кишечника;
- стимулирование реактивности организма.
Антибактериальные препараты
Антибактериальные препараты необходимы в первую очередь для подавления избыточного роста микробной флоры в тонкой кишке. Наиболее широко применяются антибиотики из группы тетрациклинов, пенициллинов, цефалоспорины, хинолоны (таривид, нитроксолин) и метронидазол.
Однако антибиотики широкого спектра действия в значительной степени нарушают эубиоз в толстой кишке. Поэтому они должны применяться только при заболеваниях, сопровождающихся нарушениями всасывания и моторики кишечника, при которых, как правило, отмечается выраженный рост микробной флоры в просвете тонкой кишки.
Антибиотики назначают внутрь в обычных дозах в течение 7–10 дней.
При заболеваниях, сопровождающихся дисбактериозом толстой кишки, лечение лучше проводить препаратами, которые оказывают минимальное влияние на симбионтную микробную флору и подавляют рост протея, стафилококков, дрожжевых грибов и других агрессивных штаммов микробов. К ним относятся антисептики: интетрикс, эрсефурил, нитроксолин, фуразолидон и др.
При тяжелых формах стафилококкового дисбактериоза применяют антибиотики: таривид, палин, метронидазол (трихопол), а также бисептол-480, невиграмон.
Антибактериальные препараты назначают в течение 10–14 дней. В случае появления в кале или кишечном соке грибов показано применение нистатина или леворина.
У всех больных с диареей, ассоциированной с антибиотиками, протекающей с интоксикацией и лейкоцитозом, возникновение острой диареи следует связывать с Cl. difficile.
В этом случае срочно делают посев кала на Cl. difficile и назначают ванкомицин по 125 мг внутрь 4 раза в сутки; при необходимости доза может быть увеличена до 500 мг 4 раза в день. Лечение продолжают в течение 7-10 суток. Эффективен также метронидазол в дозе 500 мг внутрь 2 раза в сутки, бацитрацин по 25 000 МЕ внутрь 4 раза в сутки. Бацитрацин почти не всасывается, в связи с чем в толстой кишке можно создать более высокую концентрацию препарата. При обезвоживании применяют адекватную инфузионную терапию для коррекции водно-электролитного баланса. Для связывания токсина Cl. difficile используют холестирамин (квестран).
Бактериальные препараты
Живые культуры нормальной микробной флоры выживают в кишечнике человека от 1 до 10% от общей дозы и способны в какой-то мере выполнять физиологическую функцию нормальной микробной флоры. Бактериальные препараты можно назначать без предварительной антибактериальной терапии или после нее. Применяют бифидумбактерин, бификол, лактобактерин, бактисубтил, линекс, энтерол и др. Курс лечения длится 1-2 месяца.
Возможен еще один способ устранения дисбактериоза — воздействие на патогенную микробную флору продуктами метаболизма нормальных микроорганизмов. К таким препаратам относится хилак форте. Он создан 50 лет назад и до настоящего времени применяется для лечения больных с патологией кишечника. Хилак форте представляет собой стерильный концентрат продуктов обмена веществ нормальной микрофлоры кишечника: молочной кислоты, лактозы, аминокислот и жирных кислот. Эти вещества способствуют восстановлению в кишечнике биологической среды, необходимой для существования нормальной микрофлоры, и подавляют рост патогенных бактерий. Возможно, продукты метаболизма улучшают трофику и функцию эпителиоцитов и колоноцитов. 1 мл препарата соответствует биосинтетическим активным веществам 100 млрд. нормальных микроорганизмов. Хилак форте назначают по 40–60 капель 3 раза в день на срок до 4 недель в сочетании с препаратами антибактериального действия или после их применения.
Регуляторы пищеварения и моторики кишечника
У больных с нарушением полостного пищеварения применяют креон, панцитрат и другие панкреатические ферменты. С целью улучшения функции всасывания назначают эссенциале, легалон или карсил, т. к. они стабилизируют мембраны кишечного эпителия. Пропульсивную функцию кишечника улучшают имодиум (лоперамид) и тримебутин (дебридат).
Стимуляторы реактивности организма
Для повышения реактивности организма ослабленным больным целесообразно применять тактивин, тималин, тимоген, иммунал, иммунофан и другие иммуностимулирующие средства. Курс лечения должен составлять в среднем 4 недели. Одновременно назначаются витамины.
Профилактика дисбактериоза
Первичная профилактика дисбактериоза представляет очень сложную задачу. Ее решение связано с общими профилактическими проблемами: улучшением экологии, рациональным питанием, улучшением благосостояния и прочими многочисленными факторами внешней и внутренней среды.
Вторичная профилактика предполагает рациональное применение антибиотиков и других медикаментов, нарушающих эубиоз, своевременное и оптимальное лечение болезней органов пищеварения, сопровождающихся нарушением микробиоценоза.
Тем не менее человека, ни разу не болевшего кишечной инфекцией, просто не существует. Не существует хотя бы потому, что имеется множество способов нейтрализации всех многочисленных защитных сил — глотать, не пережевывая, чтобы слюна не успела до микробов добраться, переедать, нейтрализовать щелочными напитками кислый желудочный сок, убивать собственных микробов антибиотиками и т. д.
Но наиглавнейшей причиной кишечных инфекций было, есть и будет несоблюдение элементарных гигиенических норм — неправильное хранение пищевых продуктов, немытые руки, снующие между обеденным столом и туалетом мухи. В конце концов, какими бы замечательными защитными силами человеческий организм ни обладал, всегда найдется такое количество микробов, нейтрализовать которое просто невозможно.
Возбудителями кишечных инфекций могут быть бактерии (дизентерийная палочка, сальмонелла, стафилококк, палочка брюшного тифа, вибрион холеры) и некоторые вирусы.
Конкретное имя конкретного возбудителя конкретной кишечной инфекции интересует, прежде всего, медицинских работников. Объем, направленность и интенсивность противоэпидемических мероприятий во многом определяется именно видом возбудителя.
Одни бактерии распространяются через воду, другие — через продукты питания, причем продукты эти не какие угодно, а совершенно определенные. В одном случае — овощи, в другом — яйца, в третьем — молочные продукты и т. д.
Одни бактерии очень(!) заразны (например возбудитель холеры), другие — поменьше.
В одном случае заболевание развивается стремительно и представляет собой реальную угрозу человеческой жизни, в другом — симптомы развиваются медленно, а сама болезнь не особенно опасна.
Микробы, возбудители кишечных инфекций, могут (как правило, так оно и происходит) поражать не весь желудочно-кишечный тракт, а определенные его отделы. Воспалительный процесс в каждом таком отделе имеет свое медицинское название: воспаление желудка — ГАСТРИТ, двенадцатиперстной кишки — ДУОДЕНИТ, тонкого кишечника — ЭНТЕРИТ, толстого кишечника — КОЛИТ.
После проникновения в человеческий организм возбудители кишечных инфекций начинают активно размножаться, что приводит, во-первых, к нарушениям процесса пищеварения и, во-вторых, к воспалению клеток слизистой оболочки кишечника. Типичным и наиболее характерным следствием двух указанных процессов является основной симптом любой кишечной инфекции — понос[1]. Другие признаки болезни — тошнота, рвота, боли в животе, повышение температуры тела, отсутствие аппетита, общая слабость — встречаются часто, но обязательными спутниками кишечной инфекции не являются.
Кстати, следует отметить, что на бытовом и на медицинском уровне понятия кишечной инфекции весьма разнятся. Для обычного человека ясно: раз есть понос, значит, и кишечная инфекция есть, а для врача главное не симптомы, а путь заражения. С медицинских позиций, любая болезнь, передающаяся через рот (с пищей, водой, немытыми руками — так называемый фекально-оральный путь инфицирования), является типичной кишечной инфекцией. Наиболее показательный пример — вирусный гепатит А (болезнь Боткина). Заражение вирусом всегда происходит при его попадании в желудочно-кишечный тракт, но поражается печень, а никакого поноса в большинстве случаев нет.
Пути профилактики кишечных инфекций достаточно очевидны и сводятся к соблюдению элементарных гигиенических норм: мытью рук, особенно тщательно после посещения туалета, термической обработке пищи и воды, выполнению правил хранения пищевых продуктов, изоляции больных и, как минимум, обязательному выделению им отдельной посуды.
Всегда следует помнить, что наиболее страшным и опасным последствием любого поноса является потеря организмом жидкости и солей. Без пищи человеческий организм более или менее благополучно может просуществовать пару недель, но без адекватного обеспечения водой и солями калия, натрия, кальция человек жить не может: в этом случае счет идет на часы.
Запасы воды и солей особенно невелики в организме ребенка, и именно для детей кишечные инфекции представляют собой реальную угрозу здоровью и жизни.
Таким образом, истинная тяжесть кишечной инфекции зачастую определяется не частотой стула, не запахом и цветом испражнений, а именно степенью обезвоживания. Определить тяжесть кишечной инфекции может только врач, но вероятность того, что по поводу каждого поноса люди будут обращаться за медицинской помощью, очень невелика. Поэтому подчеркнем, что вне зависимости от того, как называется конкретная кишечная инфекция, существуют совершенно определенные правила поведения больного и его родственников.
- Всегда следует задуматься над тем, что это вы такое съели или чем накормили ребенка. Полбеды, если это ваш личный кулинарный шедевр, но если это пирожное из близлежащего магазина, то следует проявить сознательность и подумать о тех, кто может пойти по вашим следам. Узнать телефон районной санитарной станции совсем не трудно.
- Кишечная инфекция у любого члена семьи — сигнал тревоги для всех остальных. Больному — отдельная посуда, всем остальным — организовать идеальную чистоту, тщательно мыть руки, убрать от греха подальше подозрительные продукты, всю посуду перекипятить, не жалеть дезинфицирующих средств.
- И понос, и рвота являются способами защиты организма. В упрощенном варианте это выглядит так: в желудочно-кишечный тракт попало что-то не то, и организм всеми возможными способами пытается эту гадость удалить. Поэтому в первые часы кишечной инфекции мы вовсе не заинтересованы в том, чтобы понос и рвота прекратились. Наоборот, в обоих направлениях организму следует помогать — пить и рвать (а если не хочется — сознательно вызывать рвоту, промывая тем самым желудок), очистить толстый кишечник с помощью клизмы. Для клизмы используется обычная кипяченая вода, ни в коем случае не теплая (оптимальная температура около 20 °С), обязательно следить за тем, чтобы вышла вся введенная жидкость.
- Главный принцип помощи — восполнение потерь жидкости и солей. Для этой цели идеально подходят лекарственные средства, имеющиеся в любой аптеке и представляющие собой заранее приготовленную смесь различных солей, которую перед употреблением разводят кипяченой водой. Если же аптека далеко, вполне подойдут минеральные воды, отвары изюма, трав, шиповника, компот из сухофруктов, можно чай, лучше зеленый, чем черный. В конце концов, лучше пить то, что есть под рукой, чем не пить ничего.
- Температура напитков ориентировочно должна быть равна температуре тела — при этом всасывание жидкости из желудка в кровь будет максимально быстрым.
- При упорно повторяющейся рвоте помните, чтонадо пить чаще, но малыми порциями, чтобы не растягивался желудок, а использование любых противорвотных препаратов всегда согласовывать с врачом.
- По большому счету, существует лишь два абсолютно безопасных способа самостоятельного лечения кишечных инфекций — голод и обильное питье. Любые лекарственные препараты могут привести к самым неожиданным последствиям, ну разве что кишечные сорбенты[2] целесообразны и показаны практически всегда.
- Интенсивность ваших волнений должна быть теснейшим образом связана с общим состоянием ребенка, а не с тем, сколько раз он запачкал пеленки (попросился на горшок, сбегал в туалет). Следите за цветом мочи: если она светлая — дефицита жидкости нет.
- Обращение к врачу обязательно при поносе у детей первого года жизни и, вне зависимости от возраста, при отсутствии тенденции к улучшению в течение суток.
10. Немедленно обращайтесь за медицинской помощью, если:
- наиболее волнующим симптомом кишечной инфекции является боль в животе;
- из-за упорной рвоты вы не можете ребенка напоить;
- более 6 часов нет мочи;
- сухой язык,запавшие глаза, кожа приобрела сероватый оттенок;
- в кале имеется примесь крови;
- понос прекратился, но при этом усилилась рвота, и (или) резко поднялась температура тела, и (или) появились боли в животе.
11. При улучшении состояния не торопитесь скармливать детенышу все подряд. Чай с нежирным творожком, рисовая и овсяная кашки — пусть потерпит-поголодает сутки-двое, здоровее будет.
Следует отметить: современная терапия кишечных инфекций вовсе не предусматривает глотание всеми любимых фталазола и левомицетина хотя бы потому, что причиной каждого второго поноса являются вирусы[3], на которых упомянутые антибактериальные препараты не действуют вообще. Но даже если это бактерия, отношение к использованию антибактериальных препаратов неоднозначно. Так, при дизентерии антибиотики используются практически всегда, а при сальмонеллезе — значительно реже.
Парадоксальность лечения кишечных инфекций состоит прежде всего в том, что строгая диета, восполнение потерь жидкости и солей да плюс время и терпение — это почти всегда достаточные условия для выздоровления (соблюдение при этом правил гигиены подразумевается).
Тем не менее с грустью приходится признавать, что, несмотря на теоретическую логичность и привлекательность, практическое применение и эубиотиков, и бактериофагов вовсе не приводит к выздоровлению быстрее, нежели все те же диета да питье.
Неудивительно, что в подавляющем большинстве стран мира эти лекарственные средства не применяются (и не выпускаются, и не регистрируются), поскольку доказать их эффективность медицинская наука пока еще не в состоянии[4].
В стационаре основным способом оказания неотложной помощи при кишечных инфекциях является инфузионная терапия, т. е. внутривенное введение жидкости и солей для быстрого возмещения потерь.
При самой опасной кишечной инфекции — холере — инфузионная терапия вообще является наиглавнейшей. Возбудитель холеры вырабатывает экзотоксин (он называется холероген), который находится в просвете кишечника, и его в этой связи не удается нейтрализовать сывороткой. Под действием холерогена клетки слизистой оболочки кишечника как бы сморщиваются и теряют жидкость литрами! Вот и приходится в огромных количествах вводить препараты внутривенно и проводить очень активное лечение до тех пор, пока в организме не появятся антитела к токсину.
[2] Кишечные сорбенты — многочисленная группа лекарственных препаратов, способных связывать (сорбировать) и обезвреживать яды (токсины), находящиеся в просвете кишечника. Самым известным кишечным сорбентом является знаменитый активированный уголь, хотя есть и другие препараты, в десятки и сотни раз более активные.
[3] Самым известным вирусом, вызывающим у детей тяжелейшие кишечные инфекции, является так называемый ротавирус, чаще всего поражающий малышей первых двух лет жизни. Неудивительно в этой связи, что вакцинация от ротавирусной инфекции присутствует в календаре прививок многих стран мира.
Острая кишечная инфекция (ОКИ) — это инфекционное воспаление желудка и кишечника, которое проявляется диареей (жидкий стул более 3 раз в сутки), иногда тошнотой, рвотой и повышением температуры тела. Примерно в 80% случаев кишечная инфекция вызывается вирусами (очень часто это ротавирус), то есть применение антибиотиков не будет иметь никакого эффекта.
Чего нужно бояться при кишечной инфекции и как не попасть в больницу
Самое опасное для ребенка с поносом и рвотой — обезвоживание. Именно из-за него приходится госпитализировать ребенка, если родители не смогли его отпоить. Как этого не допустить, мы с вами очень подробно разберем ниже.
Что мне делать, если мой ребенок заболел ОКИ?
Чаще всего нетяжелые кишечные инфекции можно лечить в домашних условиях. При появлении симптомов заболевания желательно связаться со своим врачом и предупредить его, что ваш ребенок заболел, и подробно описать всю ситуацию. Диарея и рвота (плюс еще и повышение температуры) — это потеря воды и солей, а значит, первое и основное, что должны сделать родители — восполнить уже имеющиеся потери и постоянно компенсировать то, что будет теряться дальше.
Сколько давать жидкости?
В среднем для отпаивания ребенка при острой кишечной инфекции нужно примерно 100 мл на каждый килограмм массы тела (1000 мл для малыша весом 10 кг), но может понадобиться и больше. Чтобы было более удобно, вам нужно следить за тем, чтобы у ребенка была влажная кожа и писал он примерно раз в три часа. Если писаете реже – значит, недоработали, давайте больше пить, пока мочеиспускания не участятся.
Чем отпаивать?
Чем кормить?
Пока у ребенка рвота, ему вообще нет смысла давать еду — только жидкость. Когда рвота прекратится, то параллельно с отпаиванием вы можете предлагать уже и еду, но строго по аппетиту! Не нужно кормить насильно — это только вызовет рвоту и усилит понос. Дети на грудном вскармливании прекрасно обходятся грудным молоком + солевые растворы или компот при необходимости. Более старшие дети могут начинать с легко усваиваемых продуктов: фруктовые кисели, сухари с чаем, галетное печенье, рисовая каша (с компотом, например), супы не на бульоне.
Основное правило — давайте часто, но понемногу. Через день-два уже можно возвращаться к прежним продуктам (тому, что ел до болезни), исключив на некоторое время жареное, жирное и острое.
Какое еще лечение эффективно при кишечной инфекции?
Всемирная организация здравоохранения и другие крупные медицинские организации рекомендуют помимо восполнения жидкости и продолжения кормления принимать препараты цинка. Многочисленные исследования показали, что прием препаратов цинка (10–20 мг в сутки вплоть до прекращения диареи) существенно снижает тяжесть и продолжительность диареи у детей младше 5 лет. В настоящее время на основании проведенных исследований рекомендуется вводить цинк (10–20 мг/день) в рацион всех детей с диареей в течение 10–14 дней.
Также вы много слышали о пробиотиках. Доказано, что пробиотики снижают длительность диареи у детей на фоне кишечной инфекции в среднем на 24 часа. Это все, на что вы можете рассчитывать.
Можно ли детям назначать противодиарейный препарат лоперамид?
Нет. Это лекарство запрещено для применения детям в связи с риском развития угрожающих жизни побочных эффектов.
Если почти 80 % всех кишечных инфекций вызываются вирусами, значит, будут очень полезны противовирусные препараты?
А когда нужно давать антибиотики?
Антибиотики при острых кишечных инфекциях показаны довольно редко, в основном это так называемые инвазивные диареи, когда в кале появляется кровь. Еще их применяют в случае заболевания холерой, а также внекишечными бактериальными инфекциями, которые приводят к развитию диареи (пневмония, средний отит и т. д.). Как вы уже поняли, примерно в 80 % всех случаев кишечных инфекций антибиотики назначаются зря. И это как минимум.
Я не хочу, чтобы мой ребенок заболел. Как предотвратить это?
Как все запутано! А можно на примере объяснить, как же все-таки правильно лечить острую кишечную инфекцию?
А если у ребенка поднимается температура?
Вы можете дать жаропонижающий препарат для облегчения состояния — ибупрофен или парацетамол в обычной дозировке. Подробнее о лихорадке и методах борьбы с ней можете почитать Правда и мифы о лихорадке.
Малыш отказывается пить. Как поступить?
Сколько будет длиться этот понос?
В большинстве случаев самая острая фаза диареи прекращается за 5–7, реже — 9 дней. После этого у ребенка может оставаться на некоторое время жидковатый неоформленный стул, пока не восстановится кишечник, но это уже не профузный понос 10–20 раз за сутки.
Когда нужно немедленно обращаться к врачу?
По большому счету, в двух ситуациях:
1) если у ребенка в кале появилась кровь. Появление крови в кале говорит о поражении толстого кишечника, что чаще всего бывает при бактериальных кишечных инфекциях, — в таком случае может понадобиться антибиотик;
2) если вы не справились с отпаиванием, то есть, вопреки всем вашим стараниям, у ребенка кожа стала сухой и он не писал в течение 6 часов (у грудных детей памперс сухой на протяжении 6 часов), вам нужно обратиться за медицинской помощью, поскольку, скорее всего, понадобится внутривенное восполнение жидкости.
опубликовано 02/05/2016 16:26
обновлено 03/03/2019
— Инфекционные болезни
Кишечные инфекции появляются в результате распространения вредных бактерий. Чаще всего они развиваются у детей, но нередко могут стать и причиной недомогания любого члена семьи. В этой статье мы поговорим о том, какие есть виды кишечных инфекций, как они появляются в организме человека и как их правильно и эффективно лечить.
Кишечные инфекции появляются в результате распространения вредных бактерий. Чаще всего они развиваются у детей, но нередко могут стать и причиной недомогания любого члена семьи. В этой статье мы поговорим о том, какие есть виды кишечных инфекций, как они появляются в организме человека и как их правильно и эффективно лечить.
Несмотря на схожие симптомы и способ заражения, каждый вид имеет свои отличительные черты и представляют различную опасность для человека.
Виды кишечных инфекций
Возбудитель появляется и паразитирует в желудочно-кишечном тракте. Может воспаляться слизистая оболочка желудка, нарушаться процессы пищеварения, ухудшаться общее самочувствие человека.
Вирусные инфекции
При вирусном заражении поражаются стенки желудка, кишечника, дыхательных органов, в редких случаях могут затрагиваться другие органы. Инфекция может передаться несколькими способами: фекально-оральным, воздушно-капельным, контактно-бытовым.
Вылечить инфекцию можно всего за одну неделю, но человек может продолжать быть переносчиком еще на протяжении 3-4 недель. Важно на время лечения придерживаться строгой диеты, пить много чистой воды и применять противовирусные препараты, выписанные врачом после диагностики организма.
Бактериальные инфекции
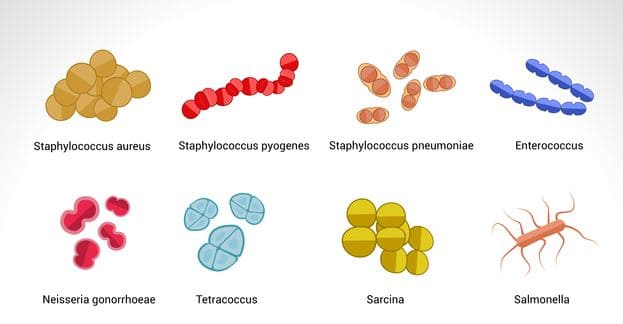
Такое заболевание считается более опасным, так как существует большая вероятность осложнений. Заразиться можно фекально-оральным и контактно-бытовым путем. Инфекция затрагивает желудочно-кишечный тракт, мочевыводящие каналы.
Бактерии, распространяясь в желудочно-кишечном тракте, выделяют токсичные вещества. При большом количестве таких веществ, поступающих в организм, может настать токсический шок.
Больному понадобится комплексное лечение. Нужно не только избавиться от вредоносных микроорганизмов, но и очистить организм от токсичных веществ, а также устранить симптоматику. В таких случаях прописывают антибиотики.
Протозойные инфекции
Считаются менее распространенными, но при этом очень опасными. Они передаются не только фекально-оральным и контактно-бытовым путем, но и во время полового акта. Несмотря на активное распространение в желудке и кишечнике, болезнь может продолжительное время не давать о себе знать, что в дальнейшем затруднит процесс лечения.
Симптомы кишечной инфекции у взрослых
Первые симптомы дают о себе знать достаточно быстро – проходит от 6 до 48 часов после того, как возбудитель инфекции попадает в организм. Кишечная инфекция также может начинаться как простуда: с першения в горле, невысокой температуры, до 37,5.

Появляются характерные признаки:
- лихорадка
- рвота, диарея
- боль внизу живота
- дискомфорт, иногда резкое повышение температуры тела (до 38–39 °С)
- слабость, бледность, одышка, может быть нарушение сердечной деятельности
- самое опасное в данном случае – потеря жидкости от рвоты и диареи
Если заболевание проходит в легкой форме, то эти симптомы могут не наблюдаться, а при острой кишечной инфекции симптоматика может принять ярко-выраженный характер.
Стафилококк
Заболевание вызывают условно-патогенные микробы, которые опасны для здоровья человека. Обитая в организме постоянно, они находятся под контролем иммунитета. Но при ослаблении защиты могут спровоцировать воспалительный процесс.
Стафилококк – это неподвижный грамположительный микроорганизм шаровидной формы, образующий многочисленные колонии. Может развиваться и паразитировать в организме без участия кислорода в закрытой среде. Штаммов бактерий насчитывается более двадцати. Некоторые из них довольно безобидны, а другие вызывают мощные патологические реакции в человеческом организме.
Патология чаще всего появляется на коже, слизистых оболочках, соединительной ткани, подкожной клетчатке, сердечной мышце. Поражая их, микробы вырабатывают токсичные вещества, провоцируют воспаления, в тяжелых случаях приводящие к сепсису, необратимым изменениям структур.
Наиболее распространенной разновидностью является золотистый стафилококк. Название получил из-за характерного желтого пигмента на поверхности. Проникая в организм, синтезирует фермент коагулазу, может вызывать гнойные воспаления почти любых внутренних органов.
Симптомы стафилококковой инфекции
Два основных признака, которые можно наблюдать в теле у зараженного человека, это интоксикация и воспалительный процесс. Могут появляться болезненные выпуклые узелки, наполненные гноем. Поражение пазух носа стафилококком проявляется банальным насморком с вязкими желтоватыми или зелеными выделениями. Также могут появиться следующие признаки:
- заложенность в области переносицы
- ощущение тяжести, распирания с пораженной стороны
- затрудненное дыхание
- густые гнойные выделения из носа
- повышение температуры тела выше +37°С
Нередко инфекция распространяется на среднее ухо, вызывая отит: резкие стреляющие боли, снижение слуха. При поражении слизистых глаз развивается нагноение конъюнктивы, склеры краснеют и отекают. Стафилококк часто встречается у детей до 12 лет и проявляет себя точно также, как у взрослых.
Для быстрого подавления активности патогенов применяют комбинации различных групп препаратов. Относительно новые и эффективные: макролиды и фторхинолоны. Лекарства этих категорий разрушают и уничтожают белковые оболочки бактерий, не давая им времени для развития резистентности. Курс лечения стафилококка должен проводиться по четким указаниям врача и не должен прерываться.
Сальмонеллез
Еще одна разновидность бактериальной инфекции, которая поражает человека и животных, передается фекально-оральным путем, обычно поражает желудок и тонкий кишечник. Характер течения заболевания отличается в каждом конкретном случае, от бессимптомного поражения до тяжелых форм с токсическим и дегидратационным шоком.
Причиной возникновения заболевания являются бактерии сальмонеллы. Они хорошо сохраняются и долго живут в окружающей среде. Им не страшен холод, поэтому заморозка продуктов не предотвращает заражение. Зато при кипячении эти бактерии погибают мгновенно.
Сальмонеллы проникают в желудочно-кишечный тракт с пищей, водой или через загрязненные руки, беспрепятственно проходят кислотный барьер желудка и заселяются в тонком кишечнике. В борьбе с иммунными клетками они вырабатывают опасный для жизнедеятельности человека токсин. С током крови они попадают в другие внутренник органы: печень, селезенку, легкие, кости.
Симптомы сальмонеллеза:
Инкубационный период продолжается от нескольких часов до 2 суток. Резко поднимается температура тела, появляется выраженный болевой синдром, тяжесть в голове, слабость. Расстройство стула при сальмонеллезе – один из основных симптомов. Каловые массы становятся водянистыми, пенистыми и чрезвычайно зловонными. Дефекация сопровождается позывами к рвоте. Слизистая оболочка рта и язык покрываются белым налетом, становятся излишне сухими.
Пациенты, страдающие от тяжелой формы сальмонеллеза или осложнений, подлежат госпитализации. Взрослые и дети, переживающие течение инфекции в легкой форме, проходят лечение на дому. Лечение сальмонеллеза начинается с базовой процедуры промывания желудка и кишечника.
Затем восстановление баланса электролитов в организме пациента и коррекция водно-солевого баланса. Это делается с помощью потребления солевого раствора внутрь. При тяжелом обезвоживании проводится внутривенная инфузионная терапия, в состав которой входят полиионные растворы.
Лечение кишечных инфекций

При появлении признаков инфекции необходимо обратиться на прием к врачу. Многие заболевания имеют схожие симптомы. Поэтому чтобы провести грамотную терапию, необходимо пройти полную диагностику. Только лабораторные методы диагностики покажут правильный результат.
Что делать, если в семье больной?
- Заболевшему придерживаться постельного режима. Желательно лечь в отдельную комнату, куда не стоит пускать детей. Если тошнит, принести тазик.
- Если зараженного тошнит, накройте его пледом. Желательно таким, который легко потом отстирать.
- Для питья выделите заболевшему отдельную посуду.
Для лечения назначают медицинские средства. Активированный уголь (1 таблетка на 10 кг веса) и другие сорбенты, регидрон (назначается при большой потере жидкости, особенно для людей с недостатком веса, при обезвоживании), жаропонижающие. Также обязательно надо пить побольше воды, можно минеральной без газов.
Из рациона питания следует убрать все молочные продукты и несколько дней соблюдать диету. Каша на воде (лучше рисовая), сухарики из белого или серого хлеба, исключить овощи и фрукты, которые вызывают брожение – виноград, капуста, черный хлеб, бобовые.
При кишечной инфекции больному назначают теплое питье. Это могут быть:
- морсы (из свежих или замороженных ягод)
- несладкий чай, можно травяной
- сок (лучше разбавленный)
- особенно хорош кисель – из-за своих вяжущих свойств
Профилактика кишечной инфекции у взрослых и детей
- Для сырых мяса и рыбы на кухне должны быть отдельные ножи и отдельные разделочные доски. Нельзя одними приборами резать сырое мясо (рыбу) и овощи.
- Горячие блюда должны готовиться при температуре выше 70 градусов. Такая температура смертельна для микробов.
- Не оставляйте приготовленную пищу при комнатной температуре дольше чем на два часа.
- Не размораживайте пищу при комнатной температуре. Лучше в холодильнике.
Где лечить кишечные инфекции в Красноярске?
- заболевания, вызываемые неустановленным возбудителем (около 70% случаев);
- острые кишечные инфекции, вызываемые установленным возбудителем (около 20%);
- бактериальная дизентерия (около 10%).
Важно, что в наиболее обширную группу ОКИ неустановленной этиологии входят и большинство так называемых пищевых токсикоинфекций (ПТИ) — эту группу составляют приблизительно 20 этиологически разных, но патогенетически и клинически сходных заболеваний, не представляющих эпидемической опасности.
Более чем в половине случаев этиологию ОКИ не удается установить ни клинически, ни лабораторно. Эта задача, равно как и выбор патогенетического лечения, тем более не может быть решена (да и не ставится) на этапе догоспитальной помощи. Усилия врача скорой медицинской помощи (СМП) должны быть направлены на:
- коррекцию тяжелых нарушений жизненно важных функций организма больного;
- дифференцирование инфекционного, терапевтического или хирургического генеза заболевания;
- решение вопроса о необходимости госпитализации больного для специализированного лечения или проведения противоэпидемических мероприятий.
Клиническая картина ОКИ
ОКИ — заболевания различной этиологии и семиотики — объединяют общий для всех этих состояний, преимущественно фекально-оральный, способ передачи возбудителя и развитие вследствие этого характерного симптомокомплекса острой диареи (табл. 1).
ПТИ также относятся к БД, так как вызываются условно-патогенными бактериями и в ряде случаев имеют групповой, эксплозивный характер. Однако в подавляющем большинстве случаев ПТИ протекают спорадически с развитием острого гастрита, гастроэнтерита или гастроэнтероколита, с той или иной степенью обезвоживания и интоксикации и имеют благоприятный прогноз.
При диарее вирусной этиологии (ВД) целостность слизистой оболочки желудочно-кишечного тракта в большинстве случаев не нарушается и в процесс редко вовлекается толстая кишка. Инкубационный период, как правило, более короткий, чем при эпидемической БД. Острый вирусный гастроэнтерит, хотя и сопровождается лихорадкой и нарушением общего состояния больного, редко приводит к тяжелой интоксикации, развитию выраженной воспалительной реакции и дегидратации организма больного. К числу значимых дифференциальных критериев ВД можно отнести отсутствие при этих заболеваниях выраженной боли в животе, водянистый, а не слизисто-гнойный и кровавый характер испражнений. ВД нередко сопровождается острым респираторным заболеванием, особенно у детей. Продолжительность ВД редко превышает 3 дня, и в целом заболевание имеет благоприятный прогноз. Пациенты с относительно легким течением ВД в госпитализации не нуждаются.
Из ОКИ паразитарного происхождения (ПД) наибольшее клиническое значение имеют амебиаз и лямблиоз. Известно, что клиническая картина амебной дизентерии развивается приблизительно у 10% инфицированных амебой больных. Амебный колит характеризуется сильнейшей болью в животе, лихорадкой и кровавой диареей, которая чревата перфорацией толстой кишки. Генерализация амебиаза сопровождается септикопиемией с образованием абсцессов печени, легких или головного мозга и крайне неблагоприятным прогнозом для жизни больного. Заболевание носит эндемичный характер. Лямблиоз на территории России распространен очень широко и в 25-50% случаев приводит к развитию острого или хронического энтерита, сопровождающегося диареей. Наибольшую помощь в постановке доклинического диагноза при ПД может оказать тщательный сбор анамнеза настоящего заболевания и анамнеза жизни пациента, поскольку особую группу риска образуют лица, практикующие анальные сексуальные контакты.
В современной классификации ОКИ выделяют так называемые особые формы заболевания:
- диарея путешественников;
- диарея у мужчин-гомосексуалов;
- диарея у ВИЧ-инфицированных;
- антибиотико-ассоциированная диарея;
- синдром избыточного роста бактерий в желудочно-кишечном тракте.
Из особых форм ОКИ для практики врача СМП имеет значение лишь один из вариантов антибиотико-ассоциированной диареи — псевдомембранозный колит. Это заболевание развивается во время или значительно после приема антибактериальных препаратов и связано с колонизацией кишечника условно-патогенным микроорганизмом сlostridium difficile. Протекает псевдомембранозный колит с высокой лихорадкой, кровавой диареей, болью в животе и сопровождается существенной интоксикацией со всеми возможными осложнениями острой профузной диареи. При подозрении на псевдомембранозный колит больной должен быть госпитализирован в инфекционный стационар.
Доклиническая и дифференциальная диагностика ОД
Всестороннее изучение анамнеза настоящего заболевания является первым шагом в обследовании пациентов, имеющих характерные признаки ОКИ (табл. 1).
У больных необходимо выяснить:
- когда и как началось заболевание (например, внезапное или постепенное развитие заболевания, наличие инкубационного или продромального периода);
- характер испражнений (водянистые, кровянистые, с примесью слизи или гноя, жирные и т. д.);
- частоту стула, количество и болезненность испражнений;
- наличие симптомов дизентерии (лихорадка, тенезмы, примесь крови и/или гноя в испражнениях).
В беседе с больным очень важно установить наличие и, что особенно существенно, развитие субъективных и объективных проявлений обезвоживания (жажды, тахикардии, ортостатических реакций, уменьшения диуреза, вялости и нарушений сознания, судорог, снижения тургора кожи) и интоксикации (головной боли, тошноты, рвоты, мышечных болей).
На догоспитальном этапе ОКИ необходимо дифференцировать с рядом острых неинфекционных заболеваний хирургического, терапевтического, гинекологического и иного профиля. Единственной целью дифференциального диагноза в данном случае является выбор направления госпитализации больного. Основные критерии для проведения дифференциального диагноза отражены в предлагаемом нами алгоритме догоспитальной медицинской помощи (рис. 2).
Распространенность ошибочной диагностики ОКИ иллюстрируют данные DuPont H. L. (1997). Предоставленные автором данные анализа более 50 тысяч случаев госпитализации больных с ОКИ констатируют, что в 7,4% случаев этот диагноз был установлен при таких заболеваниях, как острый аппендицит, острый холецистопанкреатит, странгуляционная кишечная непроходимость, тромбоз мезентериальных сосудов, инфаркт миокарда, крупозная пневмония, декомпенсация сахарного диабета, гипертонический криз. Напротив, указанные выше заболевания были ошибочно диагностированы у больных с ОКИ в 11,1% случаев.
Догоспитальная терапия ОД
Наибольшую угрозу для пациентов с ОКИ представляет развитие дегидратации и ассоциированной с ней артериальной гипотензии на фоне интоксикации, провоцирующей падение артериального давления и нарушение функции центральной нервной системы. Объем догоспитальной терапии при ОКИ базируется на мониторинге жизненно важных функций организма больного: состоянии сознания и функции внешнего дыхания, уровне АД и гидратации пациента. При наличии соответствующего оснащения бригады СМП терапия клинически значимой гиповолемической и инфекционно-токсической артериальной гипотензии должна осуществляться под контролем центрального венозного давления. В соответствии со стандартными рекомендациями терапия на этом этапе направлена:
- на восстановление сердечного ритма;
- на оптимизацию объема циркулирующей крови;
- на устранение гипоксии и нормализацию кислотно-щелочного равновесия;
- на проведение инотропной/вазопрессорной терапии.
Для устранения гипоксии больному назначают оксигенотерапию газовой смесью с 35%-ным содержанием кислорода.
Регидратацию больного начинают с диагностики обезвоживания, тяжесть которой может варьировать от I до IV степени (табл. 2).
При дегидратации I и II степеней (85-95% больных ОКИ) восполнение потери жидкости может и должно осуществляться оральным путем. ВОЗ рекомендует применять для оральной регидратации растворы следующей прописи: 3,5 г NaCl, 2,5 г NaHCO3 (или 2,9 г цитрата натрия), 1,5 г KCl и 20 г глюкозы или ее полимеров (например, 40 г сахарозы, или 4 столовые ложки сахара, или 50-60 г вареного риса, кукурузы, сорго, проса, пшеницы или картофеля) на 1 л воды. Это позволяет получить раствор, содержащий приблизительно 90 ммоль Na, 20 ммоль K, 80 ммоль Cl, 30 ммоль HCO3 и 111 ммоль глюкозы. Можно с успехом использовать любой из готовых растворов для оральной регидратации (цитроглюкосалан, регидрон, гастролит). Количество выпитой жидкости должно в 1,5 раза превышать ее потери с испражнениями и мочой. Компенсация обезвоживания сопровождается очевидным уменьшением жажды, нормализацией диуреза и улучшением общего состояния больного.
Дегидратация III и IV степеней, выраженная тошнота или рвота, а также бессознательное состояние больного требуют неотложной инфузионной терапии. Для внутривенной регидратации используют полиионные кристаллоидные растворы: трисоль, квартасоль, хлосоль, ацесоль. Менее эффективно введение моноионных растворов (физиологического раствора хлорида натрия, 5%-ного раствора глюкозы), а также несбалансированных полиионных растворов (раствора Рингера, мафусола, лактасола). Коллоидные растворы (гемодез, реополиглюкин, рефортан) вводят только в случаях упорной гипотонии, после восстановления объема циркулирующей крови в целом. В тяжелых случаях инфузия водно-электролитных смесей начинается с объемной скоростью 70-90 мл/мин, при средней тяжести состояния больного — с объемной скоростью 60-80 мл/мин. В ряде случаев необходимая скорость инфузии обеспечивается путем одновременного вливания в 2-3 вены. После стабилизации артериального давления скорость инфузии снижается до 10-20 мл/мин. Для предотвращения прогрессирования обезвоживания, развития гемодинамической недостаточности, отека легких, пневмонии, ДВС-синдрома и острой почечной недостаточности объем жидкости, вводимой после стабилизации состояния больного, может составлять 50-120 мл на 1 кг веса.
Назначение антибактериальной терапии среднетяжелых и тяжелых ОКИ на доклиническом этапе не только не входит в задачи врача СМП, но и категорически противопоказано, поскольку может существенно ухудшить состояние больного и затруднить лабораторную верификацию возбудителя заболевания. Возрастающая угроза инфекций, вызванных антибиотико-резистентными штаммами микроорганизмов, наличие нежелательных реакций при применении антимикробных препаратов, суперинфекция, связанная с эрадикацией нормальной микрофлоры антибактериальными средствами, и возможность индукции антибиотиками некоторых факторов вирулентности у энтеропатогенов (например, индукция фторхинолонами фага, ответственного за продукцию шигеллезного токсина), заставляют тщательно взвешивать все за и против при решении вопроса об антимикробной терапии и назначать ее только после точной диагностики возбудителя ОКИ. В связи с вышеизложенным антибактериальные препараты особенно не рекомендуются при гастроэнтеритическом варианте ОД любой степени тяжести, при легком, стертом течении колитического варианта и в период реконвалесценции при любой форме кишечного заболевания.
Эмпирическое назначение антибиотиков возможно в случае легкопротекающей и среднетяжелой ОКИ любой этиологии, а также при диарее путешественников, наиболее вероятным возбудителем которой являются энтеротоксигенные штаммы E.coli или другие бактериальные патогены. В этом случае взрослым назначают фторхинолоны, а детям — ко-тримоксазол, применение которых позволяет сократить длительность заболевания с 3-5 до 1-2 дней. Этой категории больных, как правило, не нуждающихся в госпитализации, можно рекомендовать амбулаторный прием антисептиков кишечного действия: эрцефурила, интетрикса или энтероседива в стандартных дозах в течение 5-7 дней, а также препаратов неантимикробного действия, облегчающих течение диареи (табл. 3).
Столь же опасным, как антибиотики, в отношении усугубления интоксикации является применение при ОКИ любого клинического течения сильных противодиарейных препаратов (имодиума) и противотошнотных средств (церукала, торекана).
Особое значение при ОКИ имеет коррекция микробиоценоза кишечника пробиотиками, проводимая на различных этапах лечения: в остром периоде — в целях конкурентного вытеснения патогенной микрофлоры, у реконвалесцентов — для обеспечения реабилитационных процессов. Весьма эффективно раннее, не позже второго дня болезни, назначение бифидумбактерина форте в ударных дозах (по 50 доз 3 раза каждые 2 часа в первый день лечения) с последующим приемом поддерживающих доз (30 доз в день, по показаниям — до 6 дней).
Пробиотик IV поколения бифидумбактерин форте обеспечивает высокую локальную колонизацию слизистой оболочки кишечника, элиминацию патогенной и условно-патогенной микрофлоры. Положительный клинический эффект при сальмонеллезе средней тяжести отмечен через 1-2 дня, при тяжелом течении сальмонеллеза и дизентерии — к окончанию курса. Из пробиотиков, приготовленных на основе микроорганизмов рода Bacillus, препаратом выбора является биоспорин, назначаемый по 2 дозы 2-3 раза в день в течение 5-7 дней. Препарат обладает выраженным антибактериальным, антитоксическим и иммуномодуляторным действием, индуцирует синтез эндогенного интерферона, стимулирует активность лейкоцитов крови, синтез иммуноглобулинов. При преобладании энтеритического синдрома рекомендуется энтерол, получаемый из сахаромицетов Буларди. Он назначается по 250 мг 2 раза в день в течение 5 дней. В периоде реконвалесценции наряду с традиционными патогенетическими средствами (стимуляторами репарации, общего и местного иммунного ответа) целесообразно применение препаратов облигатной флоры, оптимально — бифидумбактерина форте, оказывающего стабилизирующее влияние на микробиоценоз кишечника и гомеостатические процессы.
Несмотря на расширение возможностей по верификации возбудителя и большой выбор методов этиопатогенетической терапии, появившихся в арсенале врача за последние 20 лет, ОКИ и сегодня по-прежнему сопряжены с высокой летальностью. Так, по данным Н. Д. Ющука, при ПТИ и сальмонеллезе летальность составляет около 0,1%, а при дизентерии — 1,4%, при этом причиной 20% летальных исходов при бактериальной дизентерии и 44,4% летальных исходов при всех остальных ОКИ является инфекционно-токсический шок. Причины столь высокой летальности, вероятно, кроются в неадекватной оценке прогноза и тяжести состояния больного ОКИ и неоказании ему, в том числе по причинам недостаточного инструментального, медикаментозного и информационного обеспечения, неотложной помощи именно на догоспитальном этапе. Хочется надеяться, что предложенный нами простой алгоритм догоспитальной медицинской помощи при ОД (рис. 2) окажется небесполезным для практикующих врачей и их пациентов.
Читайте также:

