Что это полиомиелит и гемофильная инфекция типа b
Обновлено: 24.04.2024
Принципы и цели вакцинации
Гемофильная инфекция типа b является предотвращаемой путем вакцинации причиной возникновения серьезных заболеваний (менингита и пневмонии) и смерти среди младенцев и детей раннего возраста.
Вакцинация остается единственным эффективным методом профилактики - ХИБ-инфекции, который становится все более важным в свете возрастающей резистентности возбудителя к антибиотикам. В отличие от детей старшего возраста и взрослых дети в возрасте до 5 лет, в силу недостаточного развития иммунной системы, не могут самостоятельно, без прививки формировать адекватный иммунитет к ХИБ.
К концу 2013 года вакцина против ХИБ была введена в 189 странах. Глобальный охват тремя дозами этой вакцины оценивается на уровне 52%. Уровни охвата в регионах варьируются в больших пределах. В Америке охват оценивается на уровне 90%, в то время как в регионах для стран западной части Тихого океана и Юго-Восточной Азии он составляет лишь 18% и 27% соответственно.
Хорошая переносимость позволяет сочетать и комбинировать ХИБ-вакцины с другими вакцинами календаря прививок и ,в частности, с АКДС-вакцинами.
Конъюгирование основного антигена ХИБ с молекулой белка позволило задействовать так называемый бустер-эффект. Другими словами, ХИБ-вакцины обладают эффектом ревакцинации, когда повторное введение вакцины вызывает не просто линейное повышение концентрации антител, а увеличение их концентрации в геометрической прогрессии. Особенность бустер-эффекта заключается в том, что до определенной стадии с каждым повторным введением растет и кратность увеличения количества антител. Это объясняет то, почему курс первичной вакцинации состоит из нескольких прививок, а последующие ревакцинации всегда проводятся всего одной дозой вакцины. На этом основана базовая схема применения ХИБ-вакцин, когда в рамках первичного курса делаются 3 прививки с однократной ревакцинацией.
Эффективность вакцин
Современные ХИБ-вакцины очень эффективны. Заболеваемость всеми формами инфекции в развитых странах, где проводится плановая иммунизация, снизилась на 85-98%. Этого удается достичь как за счет индивидуальной защиты привитых, так и за счет эффекта коллективной защиты, который объясняется прерыванием цепочки передачи бактерии иммунитетом привитых. В одном из российских исследований, проведенных в закрытых детских коллективах Московской области, вакцинация за год позволила снизить уровень носительства гемофильной палочки с 41% до 3%, сократив заболеваемость всеми пневмотропными заболеваниями (ОРИ, бронхит, пневмония и др.) в несколько раз.
Эффективность вакцинации сегодня оценивается как 95 – 100%. Проводились многочисленные испытания полисахаридных вакцин в Европе и Северной Америке. В частности, клиническое испытание в Великобритании (1991—1993) показало снижение на 87 % заболеваемости менингитом гемофильной этиологии. В Голландии, при проведении аналогичного исследования, было зафиксировано полное отсутствие случаев менингита гемофильной этиологии в течение 2-х лет после начала иммунизации.
Поcтвакцинальные реакции
У большинства детей никаких побочных явлений после вакцинации нет. Могут быть небольшое повышение температуры тела, покраснение и болезненность в месте введения. Реакции в месте введения препарата (покраснение, уплотнение) отмечаются не более, чем у 5-7% привитых. Температурные реакции редки и встречаются у 1% привитых. Эти реакции не влияют на привычный образ жизни, не требуют лечения и самопроизвольно проходят в течение 1-2 дней.
Риск поствакцинальных осложнений
Специфических осложнений нет, однако таковые возможны у лиц с аллергией на столбнячный анатоксин.
Противопоказания
Обострение хронических заболеваний, аллергия к ингредиентам вакцины (особенно к столбнячному анатоксину), аллергическая реакция на предшествующее введение вакцины для профилактики инфекции, вызываемой Haemophilus influenzae тип b (ХИБ-инфекции). Прививки проводят через 2-4 недели после выздоровления (ремиссии). При нетяжелых формах респираторной и кишечной инфекции вакцинацию можно проводить сразу же после нормализации температуры.
Когда прививать?
Вакцинация согласно календарю прививок России должна проводиться в возрасте 3; 4,5 и 6 месяцев с ревакцинацией в 18 месяцев.
Примечание. В данной подрубрике кодируются только острые бронхиты, вызванные Haemophilus influenzae (палочка инфлюэнцы, палочка Пфейффера-Афанасьева), которая может выступать возбудителем острого воспаления верхних дыхательных путей, отита, менингита у человека.
Этиология и патогенез
Источник и резервуар инфекции - только человек. Заболевание распространяется воздушно-капельным путем, но у маленьких детей может передаваться и контактным путем. Возбудитель локализуется на слизистой оболочке верхних дыхательных путей.
Эпидемиология
H.influenzae можно выделить из носоглотки 90% здоровых людей, при этом на более вирулентный тип b приходится около 5% всех выделенных штаммов. Здоровое (бессимптомное) носительство может продолжаться от нескольких дней до нескольких месяцев. Оно сохраняется даже при высоком титре специфических антител или при назначении высоких доз антибиотиков.
У детей авирулентные штаммы H.influenzae могут выделяться из носоглотки в 30-50% случаев. При этом носителями вирулентных штаммов являются от 1 до 33% детей. Наиболее часто заболевают дети в возрасте от 6 месяцев до 4 лет; реже болеют новорожденные, дети более старшего возраста и взрослые.
У взрослых гемофильная палочка вызывает острый гнойный трахеобронхит в 50% случаев (Лукьянов С.В., 2005).
Факторы и группы риска
1. Дети до 2-х лет.
2. Пожилые люди.
3. Дети, посещающие дошкольные учреждения (по данным одного из исследований, до 50% инвазивных форм можно отнести на счет посещения детских учреждений).
4. Лица с низким социально-экономическим статусом, при скученном проживании риск заболевания возрастает.
5. Лица с различными видами иммунодефицита.
6. Ослабленные, страдающие алкоголизмом.
7. Курящие.
8. Дети на грудном вскармливании. Данный фактор отчасти является гипотетическим, поскольку механизм воздействия на защиту от гемофильной инфекции до конце не выяснен. Здесь могут играть роль как питательные, так и иммунные факторы, находящиеся в грудном молоке. После иммунизации женщин полисахаридной вакциной на 36-39 неделях беременности было отмечено 20-кратное возрастание выделения специфических антител с грудным молоком в послеродовом периоде.
9. Представители неевропейских рас - достаточно спорный фактор риска, но, по данным исследований, отмечается более высокая заболеваемость среди детей неевропейских рас.
10. Лимфогранулематоз (болезнь Ходжкина), серповидно-клеточная анемия.
11. Лица, подвергшиеся спленэктомии Спленэктомия - хирургическая операция: удаление селезенки
.
Клиническая картина
Cимптомы, течение
Инкубационный период достоверно не выяснен, так как инфекция может манифестировать после бессимптомного носительства неопределенной длительности (вторичная гемофильная инфекция).
Клиника практически неотличима от клиники других острых бронхитов за исключением постепенного начала и развития гнойного острого бронхита. Возможны ассоциированные гемофильные поражения - отит, менингит, пневмония, артрит, целлюлит (при инфицировании штаммом Hib).
Диагностика
Анамнез. Учитываются эпидемиологическая обстановка, возрастная группа, курение, факты рецидивов бронхита, наличие или отсутствие вакцинации и сопутствующих поражений вероятной гемофильной этиологии у контактных лиц (конъюктивит, отит, синусит - для штаммов NTHi и менингита, артрита, пневмонии, эпиглоттита Эпиглоттит - воспаление слизистой оболочки надгортанника (подвижный хрящ в виде лепестка; играет роль клапана между трахеей и глоткой), которое может привести к резкому нарушению проходимости дыхательных путей
Подробно - для Hib).
Клиника. Как правило, катарально-гнойный рецидивирующий острый или хронический бронхит.
Рентгенологическое исследование может выявить склонность процесса к распространению (пневмония) или показать только признаки бронхита.
Лабораторная диагностика
Общий анализ крови демонстрирует неспецифические признаки общевоспалительной реакции. В тяжелых случаях могут отмечаться как тромбоцитоз, так и тромбоцитопения. Выраженные признаки воспаления, включая значительное при выделенном возбудителе, свидетельствуют о распространении инфекции. Значительное повышение СОЭ может быть признаком развития артрита.
Бактериоскопическое исследование мокроты, мазков из зева и носоглотки показывает небольшие, грамотрицательные, плеоморфные коккобациллы с большим количеством полиморфноядерных клеток. Это считается надежным диагностическим признаком факта носительства гемофильной палочки.
Исследование культуры является более надежным способом диагностики возбудителя. Реакция агглютинации культуры с определенным типом сыворотки позволяет провести серотипирование.
Б актериологические методы остаются важными и для обнаружения инфекции с целью установления биотипа бактерии (различают биотипы I - VIII, наиболее распространены биотипы I, II, III) и определения чувствительности к антибиотикам. Необходимость данных исследований обусловлена тем, что палочка приобретает устойчивость к антибиотикам (например, к ампициллину, эритромицину). При выделении Haemophilus influenzae типа B у детей, данный штамм в 44 % случаев оказывался устойчивым к ампициллину.
Серологические тесты выбора - латекс-агглютинация и реакция преципитации. Особенно важны они для диагностики в тех случаях, когда антимикробная терапия была начата до посева культуры.
Широкое носительство в верхних дыхательных путях данной палочки среди населения (может достигать 90% среди здоровых лиц) обуславливает тот факт, что ее выделение из носоглотки и проведение бактериологического посева не всегда имеет важное диагностическое значение. В связи с этим для диагностики (и дифференциальной диагностики) заболеваний, ассоциированных с гемофильной палочкой, ее выявление целесообразно проводить в крови, мокроте, плевральной и суставной жидкости, моче при помощи бактериологических методов и ПЦР -диагностики.
Дифференциальный диагноз
Осложнения
Лечение
Лечение представляет существенные сложности в связи с формированием устойчивости возбудителя к большинству антибиотиков.
Этиотропная терапия
В идеале должна осуществляться с учетом чувствительности выделенной культуры к антибиотикам. В силу очевидных причин это условие невозможно выполнить сразу же.
Для клинически предполагаемых NTHi (поражение только слизистых) и в случае нетяжелого течения:
1. Устойчивость к ампициллину и амоксициллину достигает 50%. Однако с учетом институциональных особенностей эти препараты могут быть использованы в качестве "стартовой" терапии вследствие относительной безопасности и низкой стоимости. Ампициллин вводят парентерально в суточной дозе 200-400 мг/кг/сутки - детям и 6 г/сутки - взрослым. Амоксициллин возможно назначать перорально в дозе 80-90 мг/кг/сутки. При неэффективности возможно использовать амоксициллин-клавуланат или цефалоспорины устойчивые к бета-лактамазам, продуцируемым бактерией.
2. При аллергии на пенициллин рекомендуются макролиды (кларитромицин, азитромицин), левомицетин, фторхинолы, бисептол.
Для клинически предполагаемого штамма Hib или тяжелого течения:
1. Парентеральное введение антибиотиков.
2. Комбинация двух антибитиков различных групп. Например, цефалоспорины+левомицетин.
Длительность курса составляет 10-14 дней.
Существуют отдельные работы, показывающие эффективность терапии нетяжелых форм короткими курсами (7 дней) макролидов или амоксиклава. Смена антибиотика в отсутствие клинического эффекта при эмпирической антибактериальной терапии не должна производиться ранее чем через 5 дней после ее начала. Рекомендуется проведение полного минимального курса в 10 дней с последующей клинической и лабораторной оценкой эффективности. Однако признаки распространения инфекции, утяжеление состояния пациента или появление лабораторных данных о резистентности штамма диктуют немедленную смену антибиотика и/или применение комбинации антибиотиков.
Патогенетическая терапия:
- бронхолитики;
- муколитики;
- оксигенация;
- респираторная поддержка при необходимости;
- ингаляции солевых растворов.
Симптоматическая терапия: противокашлевые.
Прогноз
При остром бронхите, вызванном гемофильной палочкой, имеется риск формирования хронического бронхита.
Гемофильная палочка или палочка Афанасьева-Пфейффера (лат. Haemophilus influenzae) - грамотрицательная неподвижная палочковидная бактерия семейства Pasteurellaceae. Является возбудителем гемофильной инфекции у человека, одно из проявлений которой - пневмония.
Данное заболевание выделено в отдельную подрубрику вследствие:
- модифицируемости этиологического фактора (важность вакцинации);
- большой вероятности развития фатальных проявлений инвазивной гемофильной инфекции у детей (менингит, сепсис);
- трудностями лечения (большая резистентность возбудителя к антибактериальной терапии) .
Этиология и патогенез
Возбудитель заболевания - гемофильная палочка - является составляющей нормальной микрофлоры верхних дыхательных путей.
Следует различать инкапсулированные штаммы Hia, Hib и неинкапсулированные штаммы NTHi. По разным данным, носительство гемофильной палочки встречается у 25-70% людей. Наиболее опасный тип b (Hib) встречается в 5-20% случаев среди всех выявленных носителей гемофильной палочки. Наименее опасный тип NHTi регистрируется у 80% выявленных носителей.
Патогенез существенно не отличается от общего патогенеза бронхопневмоний.
Эпидемиология
Инфекция циркулирует только среди людей и ее источником выступает больной человек или носитель (в закрытых коллективах число носителей может достигать 70%). Пути распространения - воздушно-капельный и контактный.
Факторы и группы риска
Клиническая картина
Клинические критерии диагностики
- одышка - тахипноэ - лихорадка более 4 дней - физикальные признаки пневмониии - дошкольный возраст - сопутствующие поражения слизистых оболочек
Cимптомы, течение
Диагностика
Компьютерная томография выполняется при отсутствии достоверных рентгенологических признаков пневмонии и для проведении дифференциальной диагностики.
Лабораторная диагностика
Общий анализ крови демонстрирует неспецифические признаки общевоспалительной реакции. В тяжелых случаях могут отмечаться как тромбоцитоз, так и тромбоцитопения. Выраженные признаки воспаления, включая значительное при выделенном возбудителе, свидетельствуют о распространении инфекции. Значительное повышение СОЭ может быть признаком развития артрита.
Бактериоскопическое исследование мокроты показывает небольшие, грамотрицательные, плеоморфные коккобациллы с большим количеством полиморфноядерных клеток. Это считается надежным диагностическим признаком факта носительства гемофильной палочки.
Наличие в материале более 25 эпителиальных клеток свидетельствует о контаминации его отделяемым ротоглотки и делает непригодным для диагностики пневмонии (диагностируется только носительство).
При пневмониях, вызванных гемофильной палочкой, высокую диагностическую ценность имеет исследование транстрахеального аспирата и бронхоальвеолярного смыва. Присутствие в образцах большого числа плеоморфных тонких коккобацилл, часто внутри полиморфноядерных лейкоцитов, достоверно свидетельствует в пользу пневмонии, обусловленной гемофильной палочкой. При колонизации нижних дыхательных путей штаммами NTHi в мазке ничего не обнаруживают.
Исследование культуры является более надежным способом диагностики возбудителя. Реакция агглютинации культуры с определенным типом сыворотки позволяет провести серотипирование.
Бактериологические методы остаются важными и для обнаружения инфекции с целью установления биотипа бактерии (различают биотипы I - VIII, наиболее распространены биотипы I, II, III) и определения чувствительности к антибиотикам. Необходимость данных исследований обусловлена тем, что палочка приобретает устойчивость к антибиотикам (например, к ампициллину, эритромицину). При выделении Haemophilus influenzae типа B у детей, данный штамм в 44 % случаев оказывался устойчивым к ампициллину.
Серологические тесты выбора - латекс-агглютинация и реакция преципитации. Особенно важны они для диагностики в тех случаях, когда антимикробная терапия была начата до посева культуры.
Широкое носительство в верхних дыхательных путях данной палочки среди населения (может достигать 90% среди здоровых лиц) обуславливает тот факт, что ее выделение из носоглотки и проведение бактериологического посева не всегда имеет важное диагностическое значение. В связи с этим для диагностики (и дифференциальной диагностики) заболеваний, ассоциированных с гемофильной палочкой, ее выявление целесообразно проводить в крови, мокроте, плевральной и суставной жидкости, моче при помощи бактериологических методов и ПЦР ПЦР - полимеразная цепная реакция
-диагностики.
Дифференциальный диагноз
Дифференциальная диагностика проводится с другими бактериальными пневмониями, гриппом, острым бронхитом, вызванным H.influenzae.
Что такое ХИБ инфекция?
Бактерия Haemophilus influenzae является причиной бактериальных инфекций, которые часто могут быть тяжелыми, особенно у детей.
Бактерия была впервые описана в 1892 году бактериологом Рихардом Пфейфером. Во время вспышки гриппа он обнаружил в мокроте больных бактерии и предположил наличие причинной связи между этой бактерией и заболеванием, называемым тогда инфлюэнца.
В 1920 микроорганизм получил название Haemophilus. В 1933 году установлено, что грипп вызывается вирусом, а бактерия H. influenzaeбыла причиной развития вторичной инфекции.
В 1930 году бактериолог Маргарет Питтман показала, что бактерия H. influenzae может быть выделена в капсульных и некапсульных формах. Она идентифицировала шесть капсульных типов (a, b, c, d, e, f), и отметила, что практически все штаммы, выделенные из спинномозговой жидкости (ликвора) и крови относились к капсульному типу b.
Гемофильная палочка типа b называется Haemophilus influenzae типb или сокращенно ХИБ (Hib). Инфекция, вызываемая этой бактерией, называется ХИБ-инфекция.
Как написано выше, гемофильные палочки подразделяются на нетипируемые и типируемые. Типируемые разделяются на типы a, b, c, d, e, f. Из них гемофильная палочка типа b является самой патогенной, часто вызывающей тяжелейшие инфекции у маленьких детей.
Некапсульные и другие (не b) штаммы могут вызывать инвазивные заболевания, но, гораздо менее опасны, чем штамм b. Некапсульные штаммы редко становятся причинами серьезных инфекций у детей, но являются частой причиной отитов у детей и бронхита у взрослых.
Неизвестно. Скорее всего нет. ХИБ – это гемофильная палочка тип b, для её выявления надо не просто выделить гемофильные палочки, но и типировать их, чтобы понять – это тип b или какие то другие типы (капсулитрованные или некапсулированные).
Развитие ХИБ-инфекции
Бактерии ХИБ попадают в организм через носоглотку, колонизируют её и могут оставаться там кратковременно или в течение нескольких месяцев при отсутствии клинических симптомов (бессимптомное носительство). Если в стране не проводится массовая вакцинация детей против ХИБ, то бактерия может быть выделена из носоглотки у 0,5-3% здоровых младенцев и детей, но редко встречается у взрослых.
У некоторых лиц ХИБ может вызывать инвазивные инфекции (пневмонию, менингит, сепсис). Фактором риска может быть предшествующая вирусная инфекции верхних дыхательных путей. Бактерии распространяются по крови в другие участки тела. Наиболее часто затрагиваются мозговые оболочки и развивается ХИБ-менингит.
Особенностью ХИБ-инфекции является восприимчивость, зависящая от возраста – частота заболеваемости не одинакова на протяжении первых 5 лет жизни, наиболее высока она у младенцев. Пик заболеваемости регистрируется в возрасте 6-7 мес, затем постепенно снижается к 5 годам. Поэтому, чтобы обеспечить детей иммунной защитой к этому возрасту, их начинают прививать против ХИБ-инфекции с возраста 2-3 мес, в некоторых странах – с возраста 6 недель.
Если в стране не проводится массовая вакцинация детей против ХИБ, большинство детей приобретают иммунитет к возрасту 5-6 лет за счет бессимптомной или клинически выраженной ХИБ-инфекции.
Клинические проявления ХИБ-инфекции
Инвазивные заболевания, вызванные ХИБ, могут затрагивать многие органы и системы. Наиболее распространенные типы инвазивных ХИБ-инфекций – гнойных ХИБ-менингит, эпиглоттит, пневмония, артрит, целлюлит (воспалительное поражение кожи).
Менингит является инфекцией оболочек мозга и является наиболее распространенным клиническим проявлением инвазивной ХИБ-инфекции, составляет по данным научных публикаций 50-65% от всех случаев инвазивных ХИБ-инфекций.
Признаками ХИБ-менингита являются высокая температура, заторможенность, ригидность затылочных мышц (эти симптомы также возникают при менингитах, вызванных другими бактериями). Нарушение слуха или другие неврологические осложнения встречаются у 15-30% выживших после ХИБ-менингита пациентов. Летальность составляет 2-5%, несмотря на соответствующее антибактериальное лечение.
Эпиглоттит это инфекция и отек надгортанника. Эпиглоттит может привести к опасной для жизни обструкции дыхательных путей.
Септический артрит (инфекция сустава), целлюлит (быстро прогрессирующая инфекция кожи, которая обычно вовлекает лицо, голову или шею) и пневмония (которая может быть как легкой, так и очень тяжелой) являются частыми проявлениями инвазивной ХИБ-инфекции.
Остеомиелит (инфекция кости) и перикардит (воспаление оболочки сердца) – менее распространенные формы инвазивной ХИБ-инфекции.
Средний отит и острый бронхит, как правило, вызваны нетипируемыми штаммами гемофильной палочки, а не ХИБ. На ХИБ приходится около 5 -10% от гемофильных отитов среднего уха.
История применения вакцин против ХИБ-инфекции
ХИБ-вакцины первого поколения применялась в 1985-88 годах у детей с возраста 18 мес. Второе поколение – конъюгированные ХИБ-вакцины, лицензированы с 1987 года и широко применяются в календарях вакцинации в мире. Эти вакцины могут вводиться, начиная с возраста 6 недель.
ХИБ-вакцины являются высоко иммуногенными у младенцев. Более 95% детей вырабатывают защитный уровень антител после серии первичной вакцинации из трех или двух прививок (зависит от возраста начала вакцинации). Клиническая эффективность была оценена на уровне 95-100%. Инвазивные ХИБ-инфекции у полностью вакцинированных детей являются редкостью.
ХИБ-вакцины иммуногены также у пациентов с повышенным риском развития инвазивной инфекции, например, при серповидно-клеточной анемии, лейкозе, ВИЧ-инфекции, отсутствии селезенки.
График вакцинации
Всем детям, в том числе недоношенным, показана вакцинация против ХИБ-инфекции. Серия первичной вакцинации состоит из трех прививок, при начале вакцинации в первом полугодии жизни. Ревакцинация проводится на втором году жизни.
В различных странах начало плановой вакцинации младенцев против ХИБ-инфекции осуществляется по различным графикам. В некоторых странах она начинается с возраста 6 недель, в других – с возраста 2 или 3 мес.
Ранее невакцинированные дети в возрасте до 6 мес должны получить три дозы вакцины, введенные с интервалом не менее 1 мес друг от друга, затем проводится ревакцинация на втором году жизни, обычно одновременно с ревакцинацией против дифтерии-столбняка-коклюша-полиомиелита.
Непривитые ранее дети в возрасте от 7 до 11 мес должны получить две дозы вакцины, введенные с интервалом не менее 1 мес друг от друга, затем проводится ревакцинация на втором году жизни, обычно одновременно с ревакцинацией против дифтерии-столбняка-коклюша-полиомиелита.
Непривитые дети в возрасте с 12 месяц, должны получить одну дозу вакцины.
Да. ХИБ-вакцины являются взаимозаменяемыми. Вакцинация, проведенная вакцинами разных производителей, вызывает выработку защитного уровня антител.
Какими документами регламентируется вакцинация против ХИБ-инфекции в мире (развивающихся и развитых странах)?
- Федеральный закон от 17 сентября 1998 г. N 157-ФЗ "Об иммунопрофилактике инфекционных болезней"(с изменениями от 7 авг 2000 г., 10 янв 2003 г., 22 авг, 29 дек 2004 г., 30 июня 2006 г., 18 окт, 1 дек 2007 г., 23 июля, 25, 30 дек 2008 г., 24 ноя 2010 г).
Статья 9. Национальный календарь профилактических прививок - Национальный календарь профилактических прививок включает в себя профилактические прививки против гепатита В, дифтерии, коклюша, кори, краснухи, полиомиелита, столбняка, туберкулеза, эпидемического паротита, гемофильной инфекции и гриппа.
- Приказ Министерства здравоохранения РФ от 21.03.2014 г. N 125н "Об утверждении национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям"
Курс плановой вакцинации против ХИБ инфекции начинается в возрасте 3 мес.
Дети, не привитые на первом году жизни против гемофильной инфекции могут прививаться и в более старшем возрасте
Изложены современные представления об инфекции, вызываемой бактерией вида Haemophilus influenzae типа b (Hib), и также называемой Hib-инфекцией. Рассмотрены эпидемиологические особенности Hib-инфекции, представлены данные о заболеваемости Hib-инфекцией в Российской Федерации и странах мира.
Особое внимание уделено проблеме вакцинопрофилактики Hib-инфекции. Дана характеристика конъюгированных Hib-вакцин, рассмотрены медицинские показания и противопоказания к их применению, возможные побочные реакции, а также порядок проведения вакцинации этими препаратами.
Приказ Министерства здравоохранения РФ от 21.03.2014 г. №125н "Об утверждении национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям"
Вакцинация проводится детям, относящимся к группам риска:
- с иммунодефицитными состояниями или анатомическими дефектами, приводящими к резко повышенной опасности заболевания гемофильной инфекцией;
- с онкогематологическими заболеваниями и/или длительно получающим иммуносупрессивную терапию;
- детям, рожденным от матерей с ВИЧ-инфекцией;
- детям с ВИЧ-инфекцией;
- детям, находящимся в домах ребенка.
Курс вакцинации против гемофильной инфекции для детей в возрасте от 3 до 6 мес состоит из 3 инъекций по 0,5 мл с интервалом 1-1,5 мес.
Для детей, не получивших первую вакцинацию в 3 мес иммунизация проводится по следующей схеме:
- для детей в возрасте от 6 до 12 мес из 2 инъекций по 0,5 мл с интервалом в 1-1,5 мес;
- для детей от 1 года до 5 лет однократная инъекция 0,5 мл.
Почему в календаре РФ вакцинация против ХИБ-инфекции регламентирована только для детей из групп риска? Значит ли это, что остальным детям эта вакцинация не нужна?
Национальный календарь РФ является не только графиком прививок, но и финансовой гарантией государства – те прививки, которые входят в него всегда обеспечиваются для граждан бесплатно за государственный счет.
Пока, видимо, у государства не выделено средств на вакцинацию всех детей первых лет жизни в РФ против ХИБ-инфекции, как это рекомендуется и проводится в мире.
Пока указаны только некоторые контингенты детей:
- с иммунодефицитными состояниями или анатомическими дефектами, приводящими к резко повышенной опасности заболевания гемофильной инфекцией;
- с онкогематологическими заболеваниями и/или длительно получающим иммуносупрессивную терапию;
- детям, рожденным от матерей с ВИЧ-инфекцией;
- детям с ВИЧ-инфекцией;
- детям, находящимся в домах ребенка.
В настоящее время Федеральной службой Роспотребнадзора готовится обоснование для изменения Национального календаря прививок о целесообразности плановой ХИБ-вакцинации всех детей первых лет жизни.
Вакцинация детей старшего возраста и взрослых
В целом, ХИБ-вакцинация детей старше 59-месячного возраста не рекомендуется. Большинство детей к этому возрасту уже имеют иммунитет к ХИБ-инфекции, поэтому тяжелые формы ХИБ-инфекции у детей старшего возраста уже неактуальны.
Однако, некоторые дети старшего возраста и взрослые имеют повышенный риск инвазивных ХИБ-инфекций и могут быть вакцинированы, если они не были привиты в детстве.
К ним относятся:
- люди с функциональной или анатомической аспленией (например, серповидно-клеточная анемия, люди с удаленной селезенкой)
- иммуноглобулиновым иммунодефицитом
- иммуносупрессией при химиотерапии онкологических заболеваний
- ВИЧ-инфекции
- с пересадкой гемопоэтических стволовых клеток.
Ранее невакцинированных лиц старше 59 мес с одним из таких состояний рекомендуется прививать, по крайней мере, одной дозой любой вакцины против ХИБ.
В настоящий момент медицинское назначение Hib-вакцин взрослым не предусмотрено в российских инструкциях по применению данных вакцин.
Однако в "Политическом заявлении ВОЗ по конъюгированной вакцине против Hib-инфекции" указано: «…дети и взрослые должны быть вакцинированы в случае повышенного риска заболевания инвазивной формой инфекции при наличии соответствующих ресурсов.
В группу повышенного риска входят:
- лица с ВИЧ-инфекцией и иммуноглобулиновым дефицитом
- лица с имплантированными стволовыми клетками
- пациенты, получающие химиотерапию по поводу злокачественных новообразований
- лица с аспленией (например, в результате серповидно-клеточной анемии или спленэктомии)
Одна вакцина российского и 2 вакцины зарубежного производства
- Пятикомпонентная вакцина против дифтерии-столбняка-коклюша-полиомиелита-ХИБ (производство Санофи Пастер)
- Шестикомпонентная вакцина против дифтерии-столбняка-коклюша-полиомиелита-гепатита В-ХИБ (производство ГлаксоСмитКляйн)
Можно ли применять ХИБ-компонент комбинированной вакцины (флакончик с ХИБ-компонентом) как отдельную вакцину?
В соответствии с законодательством, подготовка вакцины к введению осуществляется в строгом соответствии с инструкцией по применению препарата.
Перед использованием любой вакцины или растворителя к вакцине следует проверить в том числе соответствует ли выбранный растворитель данной вакцине. Для растворения ХИБ-компонента во флаконе используется компонент комбинированной вакцины в шприце.
Неправда, это какое-то заблуждение. Если ребенок на первом году жизни по каким-то причинам не привит против ХИБ, то с возраста 1 года ему рекомендуется сделать одну прививку против ХИБ-инфекции, которая обеспечит его защитой на дошкольный период. Ревакцинацию в таком случае проводить не нужно.
Вакцинация против ХИБ-инфекции рекомендуется всем детям до 5 лет.
Ребенку уже 4 года, третью прививку против ХИБ он получил в возрасте 6 мес, ревакцинация на втором году жизни не проводилась. Нужно ли провести ревакцинацию сейчас?
Детям в возрасте до 5 лет рекомендуется введение, по крайней мере, одной прививки против ХИБ-инфекции после их первого дня рождения для формирования длительной защиты.
Ребенок возрастом 7 лет не прививался против ХИБ-инфекции. Показана ли ему ХИБ-вакцинация в этом возрасте?
Нет рекомендаций прививать против ХИБ-инфекции обычных детей в возрасте старше 59 мес, даже если они ранее не были привиты.
Случаи, когда по состоянию здоровья старшие дети и взрослые могут быть привиты против ХИБ-инфекции, указаны выше.
Официальных рекомендаций в РФ по этому поводу нет. Международные научные публикации говорят, что у детей, перенесших ХИБ-менингит, защитные антитела против ХИБ находят, в лучшем случае, у половины переболевших.
В некоторых исследованиях вообще ни один переболевший не имел защитного иммунитета после ХИБ менингита. Введение ХИБ-вакцины таким детям, как описано в тех же исследованиях, позволяло получить иммунитет на защитном уровне.
". дети, перенесшие инвазивную ХИБ-инфекцию в возрасте младше 24 мес. могут иметь риск развития повторного эпизода заболевания. Эти дети должны быть привиты по соответствующему возрасту графику как невакцинированные и не получавшие ранее ХИБ-вакцину. Вакцинация должна быть начата через 1 месяц после начала заболевания или в наиболее возможно ближайший после выздоровления период.."
Ни в отечественных, ни в зарубежных документах нигде не написано, что ХИБ-вакцинация в соответствии с возрастом таким детям противопоказана.
Противопоказания к ХИБ-вакцинации. Временный отвод.
ХИБ-вакцины не вводятся детям младше 6 недель в связи с возможностью развития иммунологической толерантности к ним в дальнейшем — утратой или ослаблением способности организма к иммунному ответу на данный антиген в результате предшествующего контакта с тем же антигеном.
Вакцинация должна быть отложена у детей при наличии острого заболевания.
Побочные реакции после проведения вакцинации.
Побочные реакции на введение ХИБ-вакцин случаются нечасто, описаны в инструкции по применению вакцин.
Общие реакции, такие как повышение температуры тела выше 38ºС и раздражительность регистрируются редко. Серьезные побочные реакции встречаются редко.
Имеющаяся информация о частоте побочных реакций показывает, что риск развития местных и общих реакций после введения комбинированных вакцин, содержащих ХИБ-компонент, аналогичен одновременному введению отдельных компонентов вакцины, и чаще всего связан с компонентом против дифтерии-столбняка-коклюша.
С подробной информацией можно ознакомиться в инструкции по применению конкретных вакцин.
Что такое коклюш? Причины возникновения, диагностику и методы лечения разберем в статье доктора Каминской Ольги Николаевны, инфекциониста со стажем в 21 год.
Над статьей доктора Каминской Ольги Николаевны работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Коклюш (от франц. coqueluche) — острое инфекционное заболевание, вызываемое бактерией Bordetella pertussis. Клинически характеризуется респираторным синдромом (поражением верхних дыхательных путей) с приступообразным кашлем. Имеет характерное название "стодневный кашель", так как симптомы держатся длительно — 3-4 месяца [1] [2] [3] [4] [5] .

Этиология
Вид — Bordetella pertussis
Бактерия представляет собой мелкую палочку с закруглёнными концами. Она неподвижная, хорошо окрашивается анилиновыми красителями (при микроскопии данные красители окрашивают коклюшный микроб в красный цвет ) [6] [7] .
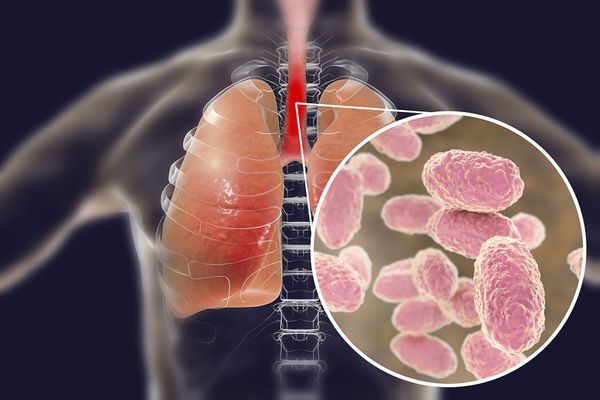
Строение Bordetella pertussis
Возбудитель коклюша (Bordetella pertussis) содержит чужеродные вещества (антигены), которые стимулируют образование в организме антител. Антигены, участвующие в реакции агглютинации (склеивания бактерий антителами) называются агглютиногенами , а антитела вызывающие этот процесс — агглютининами . А гглютиноген иначе называют фактором и обозначают цифрами от 1 до 14. Коклюшная палочка в своём строении имеет несколько таких факторов.
Именно по наличию в организме определённых факторов-агглютиногенов с помощью специальных лабораторных исследований возможно определить принадлежность микроба к данному виду. Схожее строение имеет Bordetella parapertussis, которая вызывает похожее заболевание. Отличие возможно только по лабораторным тестам.
Возбудитель неустойчив во внешней среде, поэтому посев нужно делать сразу после взятия материала. При высушивании, облучении ультрафиолетом, под действием дезинфицирующих веществ бактерия быстро погибает [4] [5] .
Эпидемиология
Заболевание коклюш является антропонозом, т. е. им болеют только люди. Источник инфекции — больные коклюшем, носители. В эпидемиологическом плане наиболее опасны бактериовыделители, которые не имеют жалоб и клинических симптомов, ведут активный образ жизни, но выделяют микроб во внешнюю среду, заражая окружающих.
Для коклюша характерен аэрозольный механизм передачи, т. е. заболевание передается воздушно-капельным путём, особенно часто заражение происходит при близком, семейном контакте. Чаще болеют дети дошкольного возраста.
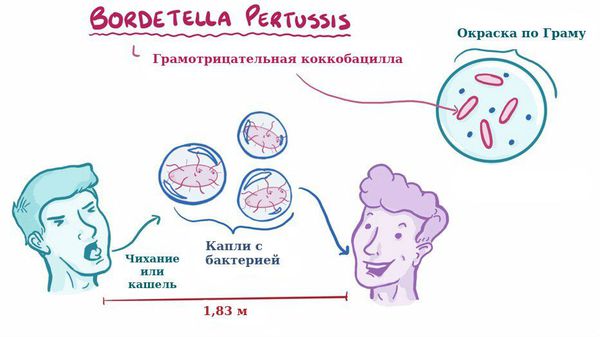
Отмечается высокая восприимчивость к инфекции, индекс контагиозности до 90 %, т. е из 100 человек, которые не болели коклюшем и не прививались, после контакта заболевает до 90 человек. В зимне-весенний период отмечается подъём заболеваемости.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы коклюша
Инкубационный период продолжается до 14 суток. В этот период пациент не предъявляет жалоб, но уже с конца данного периода становится опасен для окружающих, так как начинает выделять коклюшный микроб во внешнюю среду при кашле и чихании. Начало болезни постепенное без лихорадки с умеренно выраженной интоксикацией.
По мере развития заболевания появляются следующие синдромы:
- респираторный (кашель, скудный насморк без гнойного отделяемого);
- интоксикации — выражен умеренно, характеризуется кратковременной невысокой температурой. Высокая температура возможна при развитии осложнений (пневмонии).
Болезнь начинается с появления кашля на фоне слабой интоксикации и насморка. Интенсивность кашля постепенно нарастает, с 10-14 дня кашель становится мучительным, приступообразным с формированием характерных реприз с остановкой дыхания и затруднённым вздохом. Реприза представляет собой кашлевые толчки, сменяющиеся глубоким вдохом по типу "петушиного крика". В приступе кашля у больного синеет лицо, кончик языка при кашле направлен вверх, возможны кровоизлияния в кожу лица и склеры. В одном приступе может быть от 2 до 15 реприз. У детей приступы часто заканчиваются рвотой.
При тяжёлом течении с частотой реприз более 15 в сутки, большой частотой рвоты, связанной с кашлем, отмечается ухудшение физического состояния. Дети до года теряют в весе, начинают отставать в физическом и нервно-психическом развитии, теряют приобретённые навыки: перестают держать головку, переворачиваться, не сидят, хотя до развития заболевания данные навыки присутствовали.

При аускультации (выслушивании дыхания через фонендоскоп) выслушивается жёсткое дыхание, хрипов нет [4] [5] [6] .
Патогенез коклюша
Ворота инфекции — верхние дыхательные пути. Коклюшные палочки прикрепляются к слизистой дыхательных путей, вызывают воспаление без проникновения в кровоток. Коклюшная палочка не имеет факторов агрессии (ферментов), способных растворять клеточные мембраны, сосудистую стенку, поэтому её размножение происходит на поверхности бронха. На месте внедрения увеличивается секреция слизи, реснитчатый эпителий угнетается, формируются очаги некрозов (омертвения). Больше всего процесс затрагивает бронхи и бронхиолы.
В патогенезе судорожных приступов играет роль действие токсина коклюшной палочки. Токсин, попадая в кровоток, вызывает постоянное раздражение рецепторов бронхов, что приводит к перевозбуждению дыхательного центра. Также приступ может быть спровоцирован неинфекционными факторами, например холодным воздухом.
После перенесённого коклюша и вакцинации пожизненного иммунитета не формируется, он сохраняется до 5-6 лет, в дальнейшем возможны повторные заболевания.
Около 5 % случаев коклюша приходится на взрослых. Последние исследования показывают увеличение доли школьников среди заболевших коклюшем, что подтверждается результатами обследования длительно-кашляющих подростков на коклюш [4] [5] [6] [9] .
Классификация и стадии развития коклюша
Критерии тяжести протекания коклюша :
- лёгкая форма (до 15 реприз в сутки);
- средне-тяжёлая (15-25 реприз в сутки);
- тяжёлая (более 25 реприз в сутки) [7] .
По форме:
- Типичная форма коклюша — характерно наличие приступообразного кашля, этапность появления симптомов.
- Атипичная форма коклюша — характеризуется нетипичным покашливанием, отсутствием последовательной смены периодов болезни. Длительность кашля составляет до 50 дней, в среднем около 30 дней. Кашель носит сухой, навязчивый характер, наблюдается напряжение лица, чаще ночью с усилением на второй неделе от начала болезни. Иногда удаётся наблюдать появление единичных типичных приступов кашля при волнении ребёнка, во время еды или в связи с наслоением респираторной вирусной инфекции. Для этой формы характерно редкое повышение температуры и слабая выраженность катарального синдрома (воспаления) слизистых носа и зева [1][2][5][7] .
Клинические периоды (стадии) коклюша:
- Инкубационный период (3-14 дней) — симптомы не проявляются, пациент не предъявляет жалоб .
- Катаральный период (10-13 дней) — наблюдается клиническая картина, характерная для множества простудных заболеваний .
- Пароксизмальный, или спазматический период (1-6 недель) — проявления становятся более выраженными, пациента беспокоит мучительный приступообразный кашель.
- Период обратного развития, или реконвалесценции — приступы кашля становятся редкими , улучшается общее состояние. Этот период, в свою очередь, делят на ранний (развивается через 2-8 недель от начала клинических проявлений) и поздний (спустя 2-6 месяцев) [12] .
Осложнения коклюша
Наиболее частым осложнением является пневмония, которая может быть вызвана самой коклюшной палочкой или быть вторичной из-за активизации микрофлоры бронха.
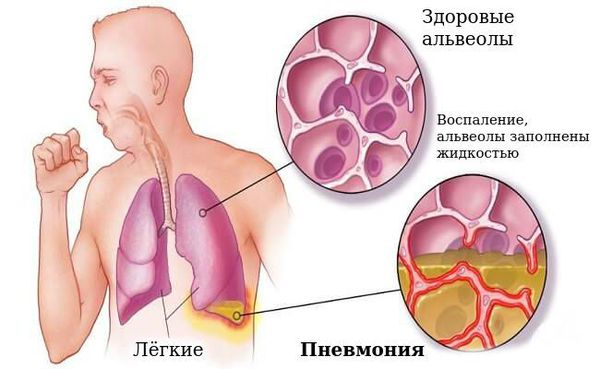
В период спазматического кашля возможны: остановка дыхания, ателектазы (спадение доли лёгкого), пупочная и паховая грыжи, энцефалопатия (нарушение поведения, расстройство внимания, у детей до года отставание в психомоторном развитии, беспокойный сон, раздражительность).
Данные осложнения чаще развиваются у грудных детей. У взрослых осложнения встречаются редко [5] [7] [9] .
Диагностика коклюша
К какому врачу обратиться при коклюше
При подозрении на коклюш следует обратиться к врачу-инфекционисту.
Лабораторная диагностика коклюша
К методам лабораторной диагностики относятся:
- Клинический анализ крови: при коклюше наблюдается лимфоцитарный лейкоцитоз, СОЭ (скорость оседания эритроцитов) повышена или в норме.
- Бактериальный посев с носоглотки (мазок) на коклюш.
- ПЦР диагностика (мазок с носоглотки).
- ИФА (иммуноферментный анализ) крови с определением маркеров проникновения инфекции — антител IgG и IgM, IgА к Bordetella pertussis. Исследование проводится двукратно с интервалом 10-14 дней, оценивается нарастание антител IgG (отвечают за устойчивый иммунитет к инфекции) в четыре раза в динамике. Наличие в крови IgM (первый ответ на инфекцию), IgА (обеспечивают местную защиту на уровне слизистых оболочек) к Bordetella pertussis является подтверждением диагноза [5][7][8][10] .
Дифференциальная диагностика
Длительный кашель может указывать не только на инфекционные заболевания, но и на патологии ЖКТ и других систем.
Инфекционный мононуклеоз может характеризоваться длительным кашлем из-за увеличения всех групп лимфоузлов, в том числе расположенных около бронха. Возникает синдром сдавления бронха, что вызывает длительный сухой кашель. Отличительная особенность — высокая и длительная лихорадка, кашель протекает без реприз. Диагноз подтверждается результатами обследования крови: в клиническом анализе крови на фоне повышения общего числа лейкоцитов с преобладанием лимфоцитов определяются специфичные клетки — мононуклеары, при серологическом исследовании крови определяются антитела класса IgM к вирусу Эбштейна — Барр.
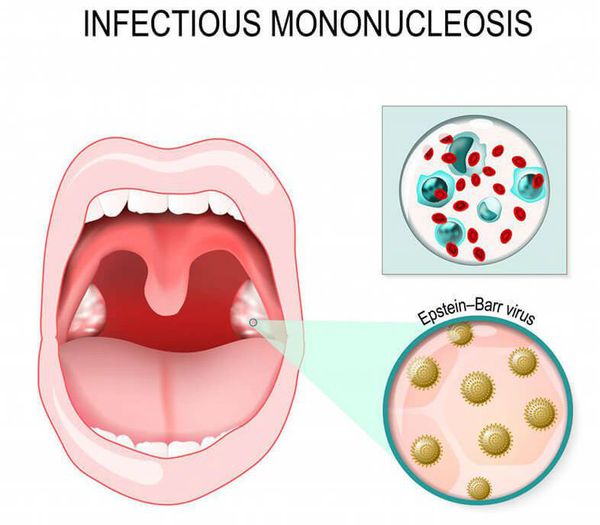
Паракоклюш — заболевание, клинически не отличимое от коклюша. Вызывается схожей бактерией Bordetella parapertussis. Диагностика совпадает с таковой при коклюше. Возможно только лабораторное подтверждение: выделение Bordetella parapertussis при бактериологическом посеве со слизистой носоглотки, при ПЦР-исследовании, нарастание титров антител к Bordetella parapertussis при обследовании крови метом ИФА.
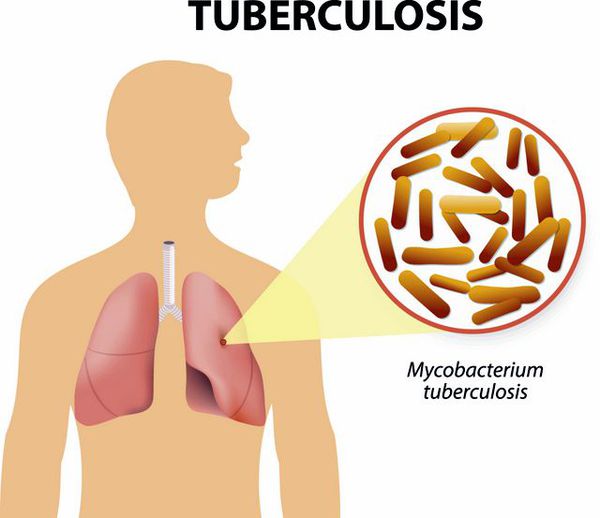
Туберкулёз — заражение туберкулёзной палочкой приводит к состоянию, для которого характерно поражение внутригрудных лимфоузлов (чаще у детей), лёгких (чаще у взрослых). В клинике преобладает длительный, навязчивый кашель, интоксикация, снижение массы тела. Репризы не характерны, необходимо дообследование у фтизиатра для исключения туберкулёза. Для уточнения диагноза применяют рентгенологические методы исследования лёгких, мультиспиральную компьютерную томографию (МСКТ) грудной клетки, учёт реакций туберкулиновых проб (реакция Манту, Диаскинтест), бактериологические методы исследования (посев мокроты на туберкулёзную палочку).
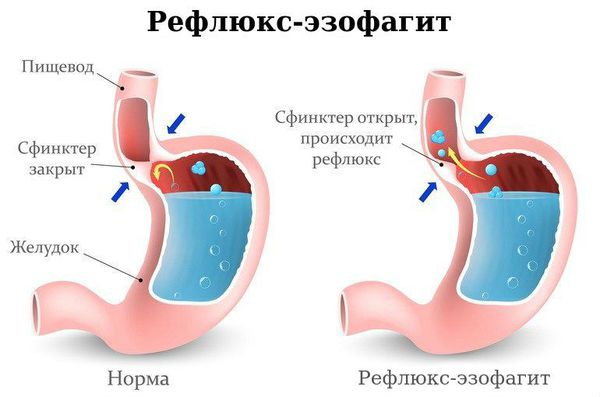
Рефлюкс-эзофагит — при данном состоянии возникает заброс кислого содержимого желудка в пищевод. Из-за близкого расположения пищевода и бронхов происходит раздражение последних и в клинике появляется кашель. Характерно появление кашля в положении лёжа, ночной кашель преобладает над дневным. Диагноз подтверждается проведением ультразвукового исследования желудка. Лечение рефлюкс-эзофагита проводит врач-гастроэнтеролог [5] [7] .
Дополнительные методы обследования: на рентгенограмме органов грудной клетки при неосложнённом коклюше отмечаются признаки усиления лёгочного рисунка: из-за отёка и воспаления на рентгеновском снимке тень лёгкого более выражена.
Лечение коклюша
В домашних условиях осуществляется лечение лёгких форм при условии отсутствия в семье непривитых детей.
Нужен ли постельный режим пациенту с коклюшем
Режим — домашний, постельный режим по самочувствию.
Когда необходимо лечение в стационаре
Тяжёлые формы подлежат госпитализации в инфекционный стационар. Показания для госпитализации: остановка дыхания, более 10 реприз в день, возраст до двух лет.
Диета при коклюше и общие рекомендации
Диета при коклюше — общий стол. Общие рекомендации: увлажнение воздуха (снижает раздражение рецепторов бронхов, уменьшает частоту реприз), витаминотерапия, исключение пассивного курения, проветривание и влажная уборка помещения.
Какие медикаменты и физиотерапевтические процедуры помогут при коклюше
В катаральный период показано применение антибактериальной терапии. Коклюшный микроб чувствителен к макропенам (азитромицин) и защищённым аминопенициллинам (амоксициллина клавуанат). В период спазматического кашля антибиотики малоэффективны, так как в этот период микроба уже нет в организме человека, клиника развивается на основании уже выделенного токсина.
Показаны ингаляции через небулайзер с гормонами (будесонид) [5] [6] [7] .

Как облегчить кашель при коклюше. Симптоматическая терапия
Облегчить кашель помогут препараты на основе кодеина или либексина, насморк — сосудосуживающие препараты в каплях или спрее.
Народные методы лечения коклюша
Народные методы не имеют доказанной эффективности, поэтому применение их может нанести вред здоровью. Отсутствие своевременного адекватного лечения коклюша, особенно у маленьких детей, опасно осложнениями — пневмонией и остановкой дыхания.
Прогноз. Профилактика
Прогноз обычно благоприятный. Симптомы коклюша нарастают в течение месяца, стихают за 2-4 месяца. Рецидивы связаны с наслоением ОРЗ, так как снова возникает раздражение слизистой бронха, усиливается кашель, учащаются репризы. На фоне лечения ОРЗ симптомы коклюша угасают.
Вакцинация против коклюша
Основным профилактическим мероприятием является вакцинация. Вакцинация позволяет сформировать иммунитет к коклюшу после введения в организм специальных иммунобиологических препаратов. Современные вакцины против коклюша входят в состав комплексных вакцин отечественного и зарубежного производства. В состав комплексных вакцин кроме коклюшного компонента может входить дифтерийный и столбнячный анатоксин, вакцина против гепатита В, гемофильной инфекции и полиомиелита (таблица 1).
В соответствии с Национальным календарём профилактических прививок вакцинация показана детям с трёх месяцев жизни. Курс прививок в первый год состоит из трёх вакцинаций с интервалом 45 дней. Дальнейшие прививки проводят на втором году жизни (через год от последней вакцинации). Вакцинацию против коклюша можно сочетать с другими прививками Национального календаря прививок: грипп, пневмококковая инфекция. Все вакцины, содержащие коклюшный компонент, взаимозаменяемы.
Таблица 1. Компоненты комплексных вакцин для профилактики коклюша
Комплексные вакцины имеют ограничение применения по возрасту пациента (таблица 2). У детей вакцинация от коклюша возможна до 4-6 лет. Длительность иммунного ответа после вакцинации составляет до 5-6 лет.
Читайте также:

