Что колоть для профилактики инфекций
Обновлено: 19.04.2024
В этой статье мы затронем одну из самых интересных тем антимикробной терапии, а именно периоперационную антибиотикопрофилактику. О нее за крайние годы сломано огромное количество копий и они, как ни странно, до сих пор продолжают ломаться.
Материалы предназначены исключительно для врачей и специалистов с высшим медицинским образованием. Статьи носят информационно-образовательный характер. Самолечение и самодиагностика крайне опасны для здоровья. Автор статей не дает медицинских консультаций: клинический фармаколог — это врач только и исключительно для врачей.
В этой статье мы затронем одну из самых интересных тем антимикробной терапии, а именно периоперационную антибиотикопрофилактику. О нее за крайние годы сломано огромное количество копий и они, как ни странно, до сих пор продолжают ломаться.
- особенностями преподавания принципов антибактериальной терапии в ВУЗах
- и достаточно легкого отношения к самим антимикробным препаратам бесконечно меняющиеся концепции антибактериальной терапии так же накладывают свой серьезный отпечаток.
Вы, наверное, помните, не так уж давно это было, как нас учили, что за неделю до операции пациент должен получить курс антибиотиков в качестве «подготовки к оперативном вмешательству. Потом передумали и стали проводить подобный курс уже после операции, причем абсолютно всем пациентам и вне зависимости от того, есть там инфекция или ее нет. Для профилактики. Чтобы было и не думалось. И этот подход так укоренился в сознании, что за 10 лет его никак не удается переломить.
Итак, чего бояться хирурги и почему они назначают антибактериальные препараты? А бояться они нагноения раны или говоря академическим языком – инфекции в области хирургического вмешательства (ИОХВ)
ИОХВ – это инфекция разреза, органа или полости, возникающая в течение 30 дней (без имплантата) или 1 года (с имплантатом) послеоперационного периода.
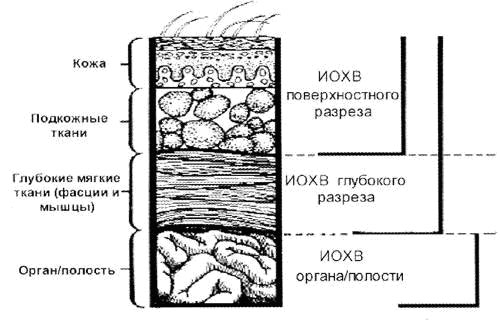
- Поверхностную ИОХВ разреза (кожа, подкожная клетчатка)
- Глубокую – ИОХВ разреза (фасция, мышцы)
- ИОХВ органа или полости
- Симптомов воспаления
- Гнойного отделяемого и лабораторное подтверждение наличия воспаления
- Достоверное микробиологическое подтверждение (окраска мазока по Граму, посев)
- необходимости вмешательство хирурга.
- Гнойное отделяемое из глубины разреза
- УЗИ и RG признаки поражения в сочетании с визуальной симптоматикой
- Спонтанное расхождение краев раны
- Присоединение глубокого поражения к поверхностному
- Необходимость хирургического вмешательства.
- Гнойного отделяемого по дренажам
- Достоверное микробиологическое подтверждение (окраска мазка по Граму, посев)
- Наличие абсцесса
Группу риска по развитию ИОХВ составляют:
- пациенты с пожилого возраста и новорожденные
- пациенты с недостатком массы тела
- больные СД
- ожирение
- сопутствующая инфекция другой локализации
- колонизация носоглотки S.aureus
- снижение местного и общего иммунитета, в т.ч. и в результате лечения.
- Особенности предоперационной подготовки – не надо брить операционное поле, это приводит к микротравматизации и увеличению риска ИОХВ
- Техника выполнения операции – при выполнении операции интернами, ординаторами и молодыми врачами, а так же в ситуациях, когда техника оперативного вмешательства еще не отточена, риски инфекции возрастают очень значительным образом.
- Несоблюдение правил асептики и антисептики
- Большая длительность операции.
- Большая кровопотеря в следствие оперативного вмешательства
- Отсутствие периоперационной антибиотикопрофилактики
- Дренирование раны
- Инфекции хирургического персонала (в том числе колонизация S.aureus)
- Степень микробной обсемененности раны
- Резистентность бактерий к антимикробной терапии.
- чистые,
- условно-чистые,
- контаминированные,
- грязные.
Чистая рана – характеризуется отсутствием признаков воспаления и вовлечения ЖКТ, МВП, дыхательных путей, а так же отсутствием технических нарушений при выполнении оперативного вмешательства.
Условно-чистая рана характеризуется вовлечением ЖКТ, мочеполовых и дыхательных путей; низкой вероятностью контаминации или незначительными техническими нарушениями при выполнении оперативного вмешательства
Контаминированная рана – имеет признаки острого негнойного воспаления; кроме того могут иметь место серьезные технические нарушения в ходе вмешательства (раны пациентов, оперированных начинающими врачами изначально должны считаться контаминированными из-за того, что техникой они еще не владеют в должном объеме)
Сюда же относится большой выброс содержимого полых органов, а также проникающие ранения со сроком менее 4 часов.
Грязные раны – характеризуются наличием гноя, предоперационной перфорацией органов и проникающими ранениями старше 4-х часов.
Итак, мы подошли к главному вопросу – когда же мы должны применить периоперационную антибиотикопрофилактику.
Периоперационную антибиотикопрофилактику мы применяем в первых трех видах ран, а в случае грязной мы с самого начала идем на антибиотикотерапию.
Почему именно тогда? В случае грязной раны возбудители могут быть какие угодно, а вот в случае первых трех, что доказано результатами многочисленных крупномасштабных исследований, ИОХВ вызовут в основном:
- Стафилококки
- Энтеробактер
- Коагулазонегативные стафилококки
- Энтерококки
- Стрептококки
- Кишечная палочка
А что же такое периоперационная антибиотикопрофилактика (ПАП) и какие цели мы перед ней ставим? Это предоперационное в/в введение антибиотика для уменьшения риска развития раневой инфекции, благодаря созданию в ране концентрации, достаточной для снижения уровня микробной контаминации тканей по ходу операционного разреза.
Давайте обратимся к очень известной картинке, которую всегда демонстрируют, когда речь идет о профилактике инфекций в хирургии:
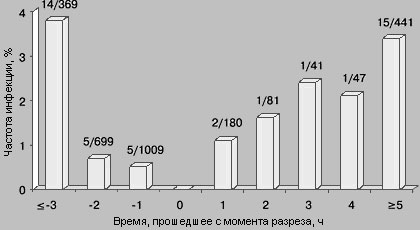
Обратите внимание, что с момента разреза контаминация тканей начинает расти в геометрической прогрессии. И введение антибиотика после операции выглядит как пальба из пушки по воробьям. При этом введение антибиотика не должно быть заблаговременным, ибо через 2-3 часа он уже будет выведен из организма, а значит и не подавит размножение микробов в ране. Таким образом, оптимальным интервалом введения, является введение антимикробного препарата за 30-40 минут до операционного разреза.
- В каких случаях следует проводить антибиотикопрофилактику?
- Какие препараты следует использовать?
- Когда необходимо начинать введение антибиотиков?
- Сколько препаратов необходимо назначить?
- Какова должна быть продолжительность антибиотикопрофилактики?
По первому пункту и третьему пунктам мы уже разобрались – профилактируем мы чистые, условно-чистые и контаминированные раны. Грязные мы начинаем сразу же лечить. А препарат вводим за 30-40 минут до разреза.
- Избирательность применения антимикробных препаратов. Т.е. препараты, применяющиеся с целью ПАП не должны больше использоваться ни в одной схеме антимикробной терапии в стационаре. Это делается для того, чтобы на максимально долгое время отсрочить развитие антибиотикорезистентности у микроорганизмов, вызывающих ИОХВ.
- Препарат должен вводится непосредственно перед операцией, за 30-40 минут до первого разреза.
- Пациентам с высокой массой тела необходимо пересчитывать дозу в сторону ее увеличения
- При длительных операциях препарат должен вводиться дважды, исходя из наиболее часто использующихся препаратов, повторная доза должна быть введена через 3-4 часа от начала оперативного вмешательства, так как это напрямую связано с фармакокинетикой антибиотика, конкретно с его периодом полувыведения (Т1/2)
- Применение ПАП более чем через 24 ч не приводит к увеличению ее эффективности. Исключением в данной ситуации являются оперативные вмешательства, проводимые молодыми врачами, осваивающими технику оперативных вмешательств. В этой ситуации антибиотикопрофилактика продляется до 72 часов.
- пациентов с трахеостомой или интубированных (для профилактики инфекций дыхательных путей);
- пациентов с постоянным мочевым катетером;
- пациентов с центральными венозными катетерами или дренажами плевральной полости;
- большинства пациентов с открытыми ранами, в том числе и ожоговыми.
Связано это с тем, что раны подвергаются постоянной контаминации и добиться там эрадикации не представляется возможным. За такими за пациентами необходим тщательный уход и контроль состояния, для того чтобы немедленно начать антибактериальную при первых же признаках инфекции
- По спектру активности – он должен включать всех наиболее часто встречающихся возбудителей
- Доза препарата должна быть обычной терапевтической (исключение – лица с ожирением)
- Время введения препарата 30-40 мин до разреза, строго!
- Кратность введения определяется Т1/2 и длительностью операции. Для основных препаратов для ПАП справедливо правило о повторном введении антибиотика через 3-4 часа от начала операции.
- легко доступен,
- дешев,
- не использоваться в схемах антибиотикотерапии в стационаре.
Почему только там? Цефазолин относится к препаратам с грам(+) активностью, он отлично воюет с грамположительными кокками, но совершенно непригоден в случае грамминус возбудителей.
Кроме того, применяя этот препарат следует помнить об общем класс-эффекте всех цефалоспоринов – лекарственные гипертермии. Примерно каждый сотый пациент выдает на цефазолин гипертермию, которая от истинной отличается тем, что проходит на фоне относительной брадикардии. Таким образом, если после АБП цефазолином у вашего пациента поднялась температура тела, а операция была чистой и в своей технике вы уверены, прежде чем паниковать и бросаться лечить его мощными антибиотиками – осмотрите рану, возьмите клинические анализы и посчитайте пульс!
Прекраснейший антибактериальный препарат, перекрывающий всех возбудителей ИОХВ и как следствие могущий использоваться при всех 3-х видах оперативных вмешательств в дозе 1,2 г в/в за 30-40 мин до разреза…
Во-вторых, его крайне сложно вывести из оборота в стационаре, так как он входит в схемы лечения многих инфекций, а что актуально конкретно для вас, так то, что он является препаратом первой линии в лечении сепсиса, тяжелых пневмоний и нейтропенических лихорадок, так же он является препаратом выбора в практике оториноларингологов. И если пациенты с подобными состояниями проходят лечение в ваших стационарах, использование амкоксициллин/клавуланата с целью ПАП принесет больше проблем, чем пользы, так как вызовет селекцию резистентных к нему штаммов. Если же подобные состояния у вас не встречаются – смело можете выводить данный препарат из общебольничной практики и использовать его в качестве периоперационной профилактики ИОХВ.
3) Ампициллин/сульбактам – перекрывает все тех же возбудителей, что и амоксициллин/клавуланат, но более дешев, легче выводится из общего оборота стационара.
Вводится по 3 г в/в за 30-40 мин до разреза. Повторная доза, если она потребуется, вводится через 3-4 часа от начала оперативного вмешательства
Отдельно следует упомянуть, что если пациент имеет в анамнезе данные об аллергических реакциях на препараты пенициллинового ряда, препаратом выбора в данной ситуации становится Клиндамицин в дозе 0,6 г.
Более подробно о методах и схемах периоперационной антибиотикопрофилактики вы можете познакомиться в следующих руководствах:
5) Антибактериальная профилактика инфекций в области хирургического вмешательства в колоректальной хирургии.
Лучшая защита от ИППП – тщательный подбор половых партнеров. Если с этим есть проблемы, презерватив обязателен. Хотя и он не дает 100% гарантии, потому что может порваться. Также риск ЗППП останется при очагах инфекции на открытых участках тела.
Своевременная профилактика после такого контакта предупредит заражение. В тяжелых случаях потребуется прием сильных антибиотиков, которые остановят размножение бактерий. Их тип и продолжительность приема подбирает врач по результатам анализов.
Стоимость консультации по предупреждению ЗППП
Расчет стоимости лечения Все цены
Экстренная профилактика ЗППП
После незащищенного акта у вас есть не больше 5 часов, чтобы позаботиться о своем здоровье. Лучше всего антисептики действуют против ЗППП в первые 2 часа, потом эффективность будет снижаться. После 5 часов профилактика заболеваний, передающихся половым путем, бесполезна. За это время нужно успеть:
- обильно помочиться, чтобы возбудители ЗППП не прошли по уретре дальше;
- сменить нижнее белье;
- обработать наружные половые органы и внутреннюю сторону бедер антисептиком;
- ввести антисептический раствор во влагалище и уретру;
- выполнить обработку других частей тела, соприкасавшихся с очагами ИППП.
Специалисты

Средства для дезинфекции
- Хлоргексидин или Мирамистин. Предназначены для профилактики поражения слизистых оболочек ЗППП. Для мужчин в комплекте есть специальная насадка. Женщинам рекомендуется использовать спринцевание.
- Гексикон. Свечи для женщин, действующее вещество – хлоргексидин. Средство обеспечит защиту от гонококков, вируса герпеса, хламидии, стрептококков, кишечной палочки и стафилококков. Не подходит для профилактики при высокой чувствительности к хлоргексидину.
- Бетадин. Это вагинальные свечи с повидон-йодом. Нужны для предохранения от грибков, вирусов и бактериальных заболеваний, передающихся половым путем. Средство не вызывает привыкания, плохо всасывается в кровь, противопоказаний мало. Профилактика не рекомендована при чувствительности к йоду и дисфункции щитовидной железы.
Перечисленные меры профилактики различных ИППП только снижают вероятность заражения в 2-3 раза, но не дают гарантии. Поэтому экстренная обработка должна проводиться в редких случаях, а не становиться частью регулярного ритуала. Обнаружить заражение можно уже на 3 день, поэтому не стоит затягивать поход к врачу.
Антисептические препараты нельзя применять слишком часто, такая профилактика только навредит. Обеззараживающие составы уничтожают и возбудителей ЗППП, и полезные бактерии, приводя к нарушению баланса. Для его восстановления потребуется дополнительное лечение, без этого риск ЗППП вырастет в несколько раз.
Медикаменты против ЗППП
Не существует универсальных таблеток, которые спасут от любого типа инфекций, передающихся половым путем. Поэтому выбором профилактических мероприятий должен заниматься врач. Против вирусов, которые вызывают ВПЧ, гепатит В или генитальный герпес, применяется вакцинация. Возможна личная непереносимость компонентов прививки.
Вариант подходит для страховки от ИППП, но не для экстренных случаев. После случайной связи может потребоваться медикаментозная помощь. Профилактику или лечение должны проходить оба партнера, чтобы предотвратить повторное заражение и распространение заболеваний, передающихся половым путем.
Антибиотики
- Тикарциллин, Оксациллин и Ампиокс. Это препараты пенициллиновой группы, которые применяют для лечения сифилиса. Лекарства быстро растворяются в желудке, из-за этого чаще назначаются в виде инъекций в вену или мышцу.
- Сумамед, Азитромицин, Эритромицин. Используются, если ИППП не удалось уничтожить при помощи пенициллина. Макролиды эффективны против сифилиса, хламидиоза и гонореи, имеют мало противопоказаний и побочных действий. Для борьбы с инфекциями, передающимися половым путем, выписываются в виде таблеток или инъекций.
- Цефтриаксон, Цефтаролин, Цефиксим и Цефпиром. Антибиотики работают против ряда ЗППП: гонореи, патогенных микроорганизмов и сифилиса. Цефалоспорины оказывают сильное воздействие, профилактика с их помощью проводится под строгим контролем. Для лечения ИППП назначаются уколы.
- Офлоксацин и Норфлоксацин. Используются для профилактики и лечения хламидиоза, гонококков. Препараты подходят для длительного приема, имеют несколько форм выпуска. Их включают в схему лечения при различной тяжести ЗППП.
- Окситетрациклин, Тетрациклин и Доксициклин. Мощные антибиотики, которые оказывают токсичное воздействие на организм. Редко назначаются для профилактики. Применяются только в случае тяжелых ЗППП, когда не помогли препараты других групп. Борются с осложненной гонореей, сифилисом и хламидиозом. Терапия ИППП этими средствами может вызвать повышение внутричерепного давления, сильную аллергию, проблемы пищеварения. По этой причине вводятся только внутривенно.
- Оринидазол, Метронидазол. Применяются для профилактики и терапии трихомониаза. Их токсичность оценивается, как умеренная. Подходят для комплексной борьбы с ЗППП, выпускаются в виде свечей и таблеток.
- Гентамицин, Немицин, Спектомицин и Амикацин. Вводятся внутримышечно. Нужны для профилактики гонореи и лечения ЗППП со скрытым течением. Также применяются для устранения тяжелых форм венерических болезней.
Профилактика после незащищенного акта не превышает 7 дней. При Продолжительность подбирает врач в зависимости от типа ИППП и тяжести поражения. Все антибиотики оказывают негативное влияние на организм. Поэтому их прием сочетают с приемом противогрибковых препаратов. При наличии проблем с пищеварением дополнительно назначаются пробиотики.
Противовирусные средства
Используются для профилактики или лечения генитального герпеса и ВПЧ. Необходимы, если от этих вирусов ранее не были сделаны прививки. Лекарства работают против внешних проявлений, вирус навсегда остается в организме. Предупредить появление этих ЗППП может только вакцина, но ее рекомендуется вводить в подростковом возрасте.
- Ацикловир. Выпускается в виде мази, из противопоказаний только личная непереносимость. Применяется для профилактики генитального герпеса и его рецидивов. Предотвращает появление новой сыпи, ускоряет заживление. Наносится с первого дня появления ИППП 4-6 раз в сутки. Курс составляет 5-10 дней. В сложных случаях рекомендуется дополнительно принимать таблетки. Для беременных и кормящих женщин обязателен контроль врача.
- Олететрин и Сафоцид. Препараты комбинированного действия, работают против ЗППП, вызванных вирусами, грибками и бактериями. Справляются с предупреждением гонореи, герпеса, хламидиоза и трихомониаза. Имеют множество побочных действий, применяются для лечения ЗППП с осторожностью. Не выписываются лекарства пациентам до 18 лет, при беременности, заболеваниях сосудов, печени и почек.
Противогрибковые средства
При незащищенном сексе нужно позаботиться и о предупреждении кандидоза. Заболевание может на первых этапах не вызывать сильного дискомфорта. Но игнорировать его нельзя, запущенные формы молочницы приводят к тяжелым последствиям. Для предотвращения ЗППП применяются следующие лекарства:
- Флуконазол. За один прием уничтожает всех возбудителей ИППП. Применяется для лечения разных степеней заболевания, в этом случае дозы и длительность терапии подбирается индивидуально. Имеет побочные действия, может стать причиной галлюцинаций при длительном приеме.
- Пимафуцин. Имеет разные формы выпуска, подходит для обоих партнеров. Имеет мало негативных эффектов, назначается беременным и кормящим мамам для лечения ИППП. Возможна личная непереносимость компонентов препарата.
- Нистатин. Выпускается в виде таблеток, мази и свечей. В малых дозах применяется для предотвращения ЗППП. При терапии назначается обеим партнерам, даже если возбудитель обнаружен у одного.
- Дифлюкан. Обладает сильным действием, работает даже против хронического течения. Убивает грибки разного происхождения, назначается с осторожностью. Нельзя принимать с некоторыми лекарствами. Запрещено применение при болезнях почек и сердца, не выписывается беременным и кормящим женщинам. Побочные действия встречаются редко.
- Тержинан. Производит комбинированный эффект: убивает грибки и патогенные микробы. Выпускается в виде вагинальных таблеток. Подходит для профилактики, имеет мало негативных последствий. Под наблюдением врача возможен прием при беременности и лактации.
Будьте внимательны: вся информация представлена только для ознакомления! Таблетки от венерических заболеваний назначает врач после обследования, бесконтрольный прием приведет к негативным последствиям. Не занимайтесь самолечением ИППП, обратитесь к специалисту МЖЦ за точным диагнозом.
Перед назначением препарата врач порекомендует сделать анализы, чтобы выявить возбудителя. Без этого не получится правильно подобрать лекарства, и предотвратить развитие болезни. ИППП опасны, легко передаются половым партнерам. Поэтому не забывайте о мерах защиты, а при небезопасном контакте не медлите с проведением профилактики.
Почему антибиотики эффективны в отношении ЗППП, вызванных бактериями, однако бессильны против вирусов, грибков или паразитов, и какая группа препаратов считается универсальной – узнаете из нашей статьи.
Замещающих препаратов для лечения ЗППП не существует. Условно-патогенные и патогенные бактерии – бледная трепонема, гонококки, гарднерелла, хламидии, уреаплазма и другие – проявляют чувствительность только к антибиотикам.
При каких ЗППП принимают антибиотики
Антибиотики эффективны только в отношении заболеваний, вызванных бактериями – гонореи, сифилиса, хламидиоза, трихомониаза, венерического лимфогранулематоза, СПИДа. Однако против вирусов, грибков или паразитов они бессильны.
Сложность подбора терапии заключается в трудности определения возбудителя. Возникновение некоторых венерических заболеваний, например, болезни Рейтера, связывают с перенесёнными инфекциями – гонореей и хламидиозом, но однозначно определить принадлежность к определённому типу учёным пока не удалось.
Группы антибиотиков от половых инфекций
При составлении схемы лечения венерологических заболеваний принято ориентироваться на фармакологические свойства антибиотиков. Только несколько препаратов можно назвать универсальными – это макролиды Эритромицин и Азитромицин. Остальные поражают только конкретного возбудителя либо принимаются в сочетании с другими лекарствами.
1. Пенициллины
Основа противосифилисной терапии. Пенициллин G короткого действия используется во всём мире как максимально эффективное средство на любой стадии заболевания.
Природные пенициллины, такие как Бензилпенициллин, оказывают непродолжительное действие, разрушаются в кислой среде желудка, поэтому выпускаются только в виде инъекций. Чтобы уменьшить кратность введения, используют синтетические антибиотики Тикарциллин, Карфециллин, которые отличаются более высокой биологической активностью.
2. Макролиды
Практически не имеют побочных эффектов, поэтому при невозможности применения пенициллинов и других антибиотиков легко замещают их. Подходят для лечения гонореи, сифилиса, в том числе сочетанных с хламидиозом.
Эритромицин и Азитромицин назначают, если антибиотиковая терапия после нескольких курсов не дала результата.
3. Тетрациклины
Тетрациклин, Доксициклин – высокотоксичные средства, но в отдельных случаях включаются в лечебный курс по уничтожению бактерий бледной трепонемы и хламидий. Переносятся тяжело – вызывают аллергию, провоцируют повышение внутричерепного давления, нарушение работы ЖКТ, поэтому желательно вводить их внутривенно.
4. Фторхинолоны
Препараты Норфлоксацин, Офлоксацин переносятся лучше, чем тетрациклины, поэтому их включают в схему при длительном лечении. Эффективны в отношении гонококковой инфекции (гонореи), урогенитального хламидиоза. Выпускаются в виде таблеток и инъекций.
5. Аминогликозиды
Спектиномицин, Неомицин оказывают бактерицидное действие независимо от фазы размножения бактерий, поэтому их целесообразно применять как при отсутствии симптомов заболевания, так и при тяжёлых формах, при угнетённом иммунитете. Принимаются при гонорее: мужчины – 1 раз, женщины – 2 раза (доза равна 2 г).
6. Цефалоспорины
Обладают мощным бактерицидным действием, аналогичным тому, какой дают пенициллины. Несмотря на схожесть механизма воздействия на клетки бактерий лекарства нового поколения Цефпиром, Цефтаролин значительно более активны, поэтому в венерологии используются для лечения любых форм гонореи и сифилиса.
7. Производные нитроимидазола
Метронидазол, Орнидазол назначаются при трихомониазе. Умеренно токсичны, выпускаются в форме вагинальных свечей и таблеток для приёма внутрь. Во время лечебного курса запрещено употреблять алкогольные напитки.
Правила подбора и приема антибиотиков от ЗППП
Самолечение при венерических заболеваниях категорически запрещено, поскольку универсальных схем приема антибиотиков в медицинской практике не существует.
Состав и периодичность курса рассчитывает врач, ориентируясь не только на данные лабораторных исследований, но даже на пол пациентов. Бессистемный приём препаратов приводит к развитию резистентности (устойчивости) бактерий, переходу заболевания в скрытые формы, провоцирует сопутствующие осложнения – распространение инфекции на другие органы (с поражением кожных покровов, слизистых), нарушению работы мочеполовой системы.
Какие таблетки пить для профилактики половых заболеваний
Не имея на руках данных лабораторных исследований, точного диагноза, принимать антибиотики с целью профилактики не рекомендуется. Меры предупреждения должны соблюдать люди, контактирующие с больными, но подбор средства нужно проводить вместе с доктором.
Профилактика нецелесообразна, если с момента контакта прошло более 3-х месяцев. Для подавления инфекции обычно назначается недельный курс инъекций бензатинбензилпенициллина.
Венерические заболевания без адекватной терапии не излечиваются. При подозрении на ЗППП мы рекомендуем проконсультироваться с профильным специалистом – гинекологом, андрологом, венерологом и пройти комплексное обследование.
Все диагностические процедуры – осмотр, анализы, УЗИ – вы можете пройти в МЖЦ.
врач акушер-гинеколог высшей категории, кандидат медицинских наук
При возникновении дополнительных вопросов, неясностей и сложностей, а также для записи на консультацию обращайтесь к специалисту Медицинского женского центра – Петрейкову Евгению Рафаиловичу – по номеру телефона
М.Н. ЗУБКОВ, доктор медицинских наук, профессор, вице-президент Межрегиональной ассоциации клинической микробиологии и антимикробной химиотерапии (МАКМАХ). ПРОФИЛАКТИКА И ТЕРАПИЯ ХИРУРГИЧЕСКОЙ ИНФЕКЦИИ
Основная роль антибиотикопрофилактики в хирургии заключается в предупреждении инфекций, возникающих вследствие операции или других инвазивных вмешательств либо имеющих прямую связь с ними, а побочная цель - в уменьшении продолжительности и стоимости пребывания больного в стационаре.
Ее суть состоит в достижении эффективных концентраций антибиотика в операционной зоне во время ее микробного загрязнения и поддержании бактерицидного уровня препарата в течение всей операции и первых 3-4 часов после оперативного вмешательства, поскольку этот отрезок времени является решающим для размножения и адгезии на клетках хозяина попавших в рану микробов, что служит пусковым механизмом для начала инфекционно-воспалительного процесса в ране. Антибиотикопрофилактика, начатая по истечении этого периода, является запоздалой, а ее продолжение после окончания операции в большинстве случаев излишним, поскольку профилактическая роль антибиотика в основном заключается в уменьшении пороговой концентрации бактерий в ране и препятствии адгезии возбудителя.
Антибиотикопрофилактика показана там, где особенно высок риск развития послеоперационной инфекции (например, при "условно чистых" операциях на органах брюшной, грудной полости и малого таза, затрагивающих слизистые оболочки, населенные микрофлорой) или если ее последствия могут представлять угрозу здоровью и жизни больного (при некоторых "чистых" операциях, связанных с имплантацией сосудистых шунтов или искусственных протезов, когда немногочисленные и малопатогенные микроорганизмы с поверхности кожи могут проникнуть глубоко в рану и вызвать ее нагноение). Если хирург заранее уверен, что встретится с инфекцией в процессе операции (например, при "условно чистых" или "загрязненных" вмешательствах), в качестве антибактериальной защиты проводят превентивную антибиотикотерапию, которая должна быть ограничена самыми жесткими показаниями: патофизиологическими предпосылками (например, перфорация органов желудочно-кишечного тракта в результате проникающего ранения или имеющая эндогенное происхождение, сопровождающаяся загрязнением кишечной микрофлорой брюшной полости и прилегающих к ней структур); наличием входных ворот инфекции (например, открытые переломы); биологией потенциального возбудителя. Раннее назначение антибиотиков, обычно в течение 12 часов с момента перфорации или травмы, расценивается как профилактика, более позднее, когда развились признаки серьезной инфекции, - как лечение.
В большинстве случаев для профилактики послеоперационной инфекции достаточно одной дозы антибиотика (во время премедикации; вторая доза вводится при 3-часовых и более длительных операциях) либо проводят сверхкраткий курс антибиотикопрофилактики, ограниченный двумя-тремя дозами препарата. Такая тактика, основанная на многочисленных клинических и экспериментальных наблюдениях, вполне эффективна, снижает вероятность побочных действий антибиотика, ограничивает возможность развития устойчивости бактерий к химиопрепаратам, обеспечивает меньшую стоимость лечения. Профилактическое применение антибиотиков задолго до операции или более 48 часов в послеоперационном периоде ведет к нарушению биоценоза желудочно-кишечного тракта и колонизации верхних его отделов микрофлорой толстой кишки с возможным развитием эндогенной инфекции путем бактериальной транслокации условных патогенов через лимфатическую систему тонкого кишечника. Кроме того, возрастает опасность суперинфекции у оперированных больных за счет селекции антибиотикорезистентных штаммов. Поэтому антибиотик следует вводить больному в соответствующей дозе непосредственно перед операцией (за 10-15 мин. внутривенно во время наркоза либо за 40-60 мин. до операции внутримышечно) с последующими повторными инъекциями по показаниям, но не более 24-48 часов.
Для профилактики раневой инфекции чаще всего назначают цефалоспорины 1-го и 2-го поколения (препараты 3-го поколения существенно дороже и используются в основном для лечения), так как они имеют достаточный спектр бактерицидной активности против наиболее распространенных возбудителей послеоперационных осложнений, и прежде всего стафилококков; при парентеральном введении создают высокие концентрации в операционной зоне; отличаются малой токсичностью и частотой побочных действий. К числу недостатков всех цефалоспоринов следует отнести неэффективность при энтерококковой инфекции; плохое проникновение через гематоэнцефалический барьер (кроме цефтазидима и некоторых других препаратов 3-го поколения); возможное увеличение нефротоксичности в комбинации с аминогликозидами.
Помимо цефалоспоринов при высоком риске стафилококковой хирургической инфекции у ортопедических и некоторых других категорий больных применяют ванкомицин. При колоректальных операциях наряду с пероральным промыванием кишечника изотоническим раствором за сутки до операции больному назначают внутрь неомицин, 1 г + эритромицин, 1 г в 13, 14 и 22 ч., а в день операции - цефалоспорины 1-2-го поколения в/в дважды с интервалом 8 ч. При катаральном и флегмонозном аппендиците достаточно однократного применения в/в цефазолина (1 г) или цефуроксима (1,5 г) либо проведения короткого курса (2-3 дозы). При гангренозном аппендиците дополнительно вводят метронидазол, 0,5 г в/в. Если в послеоперационном периоде возникает подозрение на перитонит и/или абсцедирование, продолжают применение антибиотиков в течение 3-5 суток. Схемы профилактики при других видах операций приведены в таблице 1.
Таблица 1
ВАРИАНТЫ АНТИБИОТИКОПРОФИЛАКТИКИ (АП) РАНЕВОЙ ИНФЕКЦИИ ПРИ НЕКОТОРЫХ ВИДАХ ХИРУРГИЧЕСКИХ ВМЕШАТЕЛЬСТВ*
1 Первую дозу цефалоспорина вводят в/в во время вводного наркоза (за 10-15 мин. до разреза); при операциях > 3 ч антибиотик вводят повторно; при реконструктивных операциях на сосудах и нервных окончаниях АП продлевают до 2-3 сут.
2 До 3 дней, по показаниям.
3 В/в капельно в течение 1 часа.
4 Профилактика газовой гангрены.
5 АП не показана при катетеризации сердца.
6 О преимуществах нетилмицино см. в тексте.
7 Цефалоспорины 2-го поколения, активные против анаэробов.
8 При брюшном доступе повторяют по 1 г в/в через 8 ч и 16 ч.
Антибиотикопрофилактику считают неэффективной, если в области первичного операционного разреза возникла послеоперационная инфекция; если появилась необходимость дренирования операционной зоны; если в течение 4-недельного периода после первичной операции понадобилось не находящее объяснений применение антимикробных препаратов.
При уже развившейся хирургической инфекции на начальном этапе лечения назначение антибиотиков носит эмпирический характер до получения результатов бактериологического исследования материалов из раны. При этом выбор тактики химиотерапии зависит от характера хирургической патологии и локализации гнойно-воспалительного процесса, определяющих специфику раневой инфекции. Вполне естественно, что при перитонитах, где превалирует анаэробная флора в ассоциации с энтеробактериями, и при инфекциях костей и мягких тканей, где ведущую роль играют стафилококки, алгоритмы эмпирической антибиотикотерапии будут различными.
При травматических ранах с признаками нагноения назначают комбинированную терапию, учитывая лидирующее положение стафилококков и высокий удельный вес микробных ассоциаций (до 70%) при посттравматических инфекциях. Обычно используют гентамицин (4,5 мг/кг/сут) в сочетании с оксациллином (4-6 г/сут), цефазолином (3 г/сут) или линкомицином (1200-1800 мг/сут) при высоком риске развития анаэробной инфекции.
Состав микрофлоры при перитонитах
Стрептококки - 11%
Энтеробактерии - 24%
Стафилококки - 5%
Псевдомонады - 12%
Анаэробы - 48%
Состав микрофлоры при инфекциях костей и мягких тканей
Стрептококки - 7%
Энтеробактерии - 15%
Стафилококки - 60%
Псевдомонады - 8%
Анаэробы - 10%
Но особенно следует выделить антисинегнойную активность пиперациллина и тазоцина, что позволяет использовать их для лечения внутрибольничных инфекций в виде монотерапии (4 г/0,5 г тазоцина) или в комбинации с нетилмицином (4,5 г/кг/сут).
При острых интраабдоминальных инфекциях (80% из них возникает вне стационара), когда точная локализация неизвестна, лечение направляют против смешанной флоры кишечника, включающей факультативные грамотрицательные бактерии и часто встречающиеся анаэробы (Clostridium spp. и Bacteroides spp.). Одна из применяемых в настоящее время схем противоинфекционной терапии предусматривает комбинацию аминогликозида с антианаэробным препаратом (метронидазол или клиндамицин). Многие хирурги предпочитают добавлять ампициллин для воздействия на энтерококки. Назначение тазоцина по эффективности не уступает комбинированному препарату имипенем-циластатин. Широко используются также комбинации цефалоспоринов 3-го поколения с клиндамицином или метронидазолом. Парентеральную терапию продолжают до исчезновения лихорадки, снижения числа лейкоцитов крови (< 1200 в 1 мкл), восстановления функции кишечника (обычно примерно после недельного курса лечения).
Инфицирование послеоперационных ран относится к разряду внутрибольничных инфекций, где возможны разные варианты эмпирической антибиотикотерапии в зависимости от тяжести течения раневой инфекции и особенностей формирования резистентности бактерий к антибиотикам. При неосложненных инфекциях мягких тканей, как правило, обходятся монотерапией, в то время как осложненные инфекции, требующие повторных оперативных вмешательств и нередко приобретающие системный характер, чаще нуждаются в назначении антибиотиков более широкого спектра действия или проведении комбинированной антибиотикотерапии.
При лечении тяжелых и жизнеугрожающих инфекций препаратами выбора становятся аминогликозиды, спектр действия которых охватывает подавляющее большинство аэробных грам(-) и грам(+) бактерий (за исключением стрептококков и пневмококков), а в комбинации с пенициллином они оказывают синергическое бактерицидное действие на энтерококки. Однако, несмотря на их активность против Staphylococcus spp., аминогликозиды не следует применять в качестве стартовой монотерапии при стафилококковой инфекции. Гентамицин наиболее широко применяется в практике, однако имеется много свидетельств о высоком удельном весе резистентных к нему микробных изолятов от стационарных больных, что снижает эффективность лечения хирургической инфекции. Наиболее активным среди аминогликозидов является нетилмицин (нетромицин), который, по нашим данным, превосходит другие антибиотики этой группы и некоторые цефалоспорины 3-го поколения и сопоставим по антимикробной эффективности лишь с фторхинолонами (см. табл. 2). У него наименее выражен ото- и нефротоксический эффект, что позволяет вводить суточную дозу препарата однократно без увеличения частоты побочных осложнений. Такой режим введения существенно увеличивает ударное антимикробное действие нетилмицина и имеет экономические преимущества. По стоимости он гораздо доступнее амикацина и, по нашему опыту, должен занять первостепенное положение среди аминогликозидов в лечении оппортунистических инфекций.
Таблица 2
АНТИБИОТИКОЧУВСТВИТЕЛЬНОСТЬ ГРАМ(-) БАКТЕРИЙ ПРИ ИНФЕКЦИЯХ КОСТЕЙ И МЯГКИХ ТКАНЕЙ (%)
| Антибиотики | E.col (n=28) | KES* (n=48) | Proteus spp. (n=22) | P.aeruginoza (n=37) | Acinetobacter (n=19) |
| Нетромицин | 100 | 90 | 73 | 74 | 88 |
| Амикацин | 75 | 40 | 57 | 67 | 75 |
| Тобрамицин | 58 | 34 | 22 | 63 | 43 |
| Гентамицин | 50 | 36 | 30 | 58 | 27 |
| Цефтазидим | 83 | 40 | 70 | 57 | 40 |
| Ципрофлоксацин | 100 | 88 | 79 | 83 | 80 |
Нельзя обойти вниманием и фторхинолоны, которые все чаще становятся препаратами выбора при системных инфекциях. Среди них ципрофлоксацин (ципробай, ципринол) занял прочное место в хирургической практике, в то время как другие препараты этой группы чаще используются для лечения больных терапевтического профиля. Наличие инфузионной формы препарата существенно повышает его конкурентоспособность при лечении больных в реанимационных отделениях, а возможность проведения так называемой ступенчатой терапии с переходом на пероральный прием антибиотика (без существенного снижения его концентрации в крови из-за высокой биоусвояемости при всасывании) значительно снижает стоимость курса лечения. Область применения ципрофлоксацина в хирургии с одинаковым успехом распространяется на инфекции костей и мягких тканей, интраабдоминальные инфекции, инфекции органов грудной полости и малого таза и, конечно, при лечении сепсиса.
Таким образом, применение антибиотиков в хирургии с профилактической и лечебной целью имеет свои особенности, а знание спектра возбудителей хирургических инфекций и антимикробного действия химиопрепаратов является основой правильного их применения в клинике.
Анаферон — противовирусное средство с иммуномодулирующей активностью, 9-ти летний опыт применения которого доказал эффективность и безопасность препарата в лечении и профилактики широкого спектра вирусных и бактериальных инфекционных заболеваний. Ключевыми механизмами действия анаферона является индукция эндогенных интерферонов I и II типов, а также аллостерическая модуляция рецептора интерферона гамма. Высокая безопасность препарата, возможность совместного приема с другими лекарственными средствами, отсутствие привыкания делают анаферон препаратом выбора для лечения и профилактики инфекционных заболеваний различной этиологии.
Anaferon — Effective Medicine for Treatment and Prophylaxis a Wide Spectrum of Infections
Anaferon — antiviral drug with immunomodulating activity. Nine-year-experience proved its efficacy and safety in the treatment and prophylaxis of a wide spectrum of viral and bacterial infections. The key mechanisms of anaferon action are induction of interferons I and II types production and allosteric modulation of interferon gamma receptor. Excellent safety profile, possibility of its combination with other medicines, absence of withdrawal have made it a drug of choice for the treatment and prophylaxis of various infections.
Арсенал существующих противовирусных препаратов довольно большой. Терапия вирусных инфекций является комплексной и включает не только этиотропные средства, действующие непосредственно на вирусы, но и иммуномодуляторы, корригирующие нарушения иммунитета, возникающие вследствие вирусных инфекций, симптоматические средства, оказывающие воздействие на общие симптомы вирусных заболеваний (повышенная температура, болевой синдром, кашель и др.), патогенетические средства, используемые при интоксикации, обезвоживании, аллергических реакциях.
Однако, несмотря на все это проблема эффективной профилактики и лечения вирусных инфекций далека от окончательного решения, что связано с высокой контагиозностью и скоростью распространения возбудителей, многочисленностью антигенно-самостоятельных вирусов, изменчивостью антигенных свойств вирусов, часто смешанным характером инфекции, быстро развивающейся резистентностью к препаратам, развитием вторичного иммунодефицита, специфичностью большинства средств лечения [2, 3].
В связи с высокой актуальностью лечения вирусных инфекций на современном этапе наряду с вакцинацией важной является задача по поиску новых противовирусных препаратов с принципиально новым механизмом действия, обладающих высоким профилем безопасности, эффективных в лечении и профилактике широкого спектра вирусных инфекций, микст-инфекций, предупреждающих угнетение иммунной системы. К противовирусным препаратам нового поколения относится отечественный препарат из класса лекарственных средств на основе сверхмалых доз антител к эндогенным регуляторам функций — анаферон (анаферон детский — лекарственная форма для детей).
В настоящей статье представлен обзор результатов клинических исследований эффективности и безопасности анаферона в лечении и профилактике вирусных инфекций, а также рассмотрены возможные механизмы действия препарата.
Рецептор интерферона гамма и каскад внутриклеточных реакций, инициируемых интерфероном гамма [4].
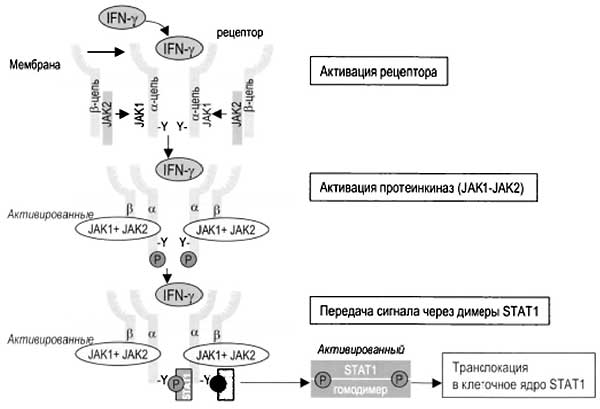
Основные биологические свойства интерферона гамма [4].
В результате проведенного группой европейских ученых из Франции и Бельгии скрининга рецепторов, вовлеченных в реализацию фармакологической активности анаферона было показано, что анаферон является положительным аллостерическим модулятором рецептора интерферона гамма: в модельной системе данный препарат более чем на 50% увеличивал количество интерферона гамма, связавшегося с рецептором, за счет восстановления эффективности лиганд-рецепторного взаимодействия и увеличения экспрессии рецепторов интерферона гамма на поверхности клеток мишеней.
Таким образом, анаферон потенцирует основные биологические эффекты интерферона гамма.
Профилактическая и/или лечебная эффективность и безопасность анаферона изучена в отношении широкого спектра инфекций (более 20 нозологий) в ходе контролируемых рандомизированных клинических исследований, проведенных в ряде ведущих медицинских учреждений России и Украины.
В проведенных рандомизированных двойных слепых плацебоконтролируемых и сравнительных клинических исследованиях приняли участие более 5500 пациентов, большинство из которых, в связи с высокой актуальностью вирусных инфекций именно в детской популяции, составляли дети в возрасте от 1 месяца до 17 лет (в том числе часто и длительно болеющие, дети с бронхиальной астмой, сердечно-сосудистой патологией, ВИЧ-инфицированные и с перинатальным контактом с ВИЧ-инфекцией).
При исследовании лечебной эффективности ана- ферона пациенты включались в исследование в острый период заболевания, при наличии яркой клинической симптоматики. Препарат назначали по лечебной схеме (первые 2 часа по 1 таблетке каждые 30 мин, затем по 1 таблетке 3 раза в день, начиная с этого же дня) в сочетании с традиционной терапией. Длительность лечебной терапии составляла минимум 5 дней и варьировалась в зависимости от типа вирусной инфекции и тяжести заболевания. Эффективность лечения оценивалась по длительности основных клинических проявлений заболевания; у части пациентов исследовали показатели иммунного и интерферонового статуса.
При исследовании профилактической эффективности препарат назначали по 1 таблетке 1 раз в сутки в течение всего эпидемического сезона. Профилактическую эффективность оценивали по влиянию препарата на частоту заболеваемости.
Клиническая эффективность и безопасность анаферона в лечении и профилактике самых массовых инфекций — острые респираторные вирусные инфекции (ОРВИ) и грипп, оценивалась в рамках мультицентрового и 5 рандомизированных исследований, проведенных в ряде ведущих медицинских учреждений России.
Проведенные исследования показали, что анаферон обладает выраженной лечебной и профилактической эффективностью при гриппе и других ОРВИ у детей, в том числе первого года жизни [5—8]. Профилактический прием анаферона в пре- и поствакциональном периоде увеличивает иммунологическую эффективность вакцинации, обеспечивает неспецифическую профилактику ОРВИ и гриппа в момент становления поствакционального иммунитета и предупреждает развитие интеркуррентных заболеваний в поствакцинальном периоде [9].
Следует отметить, что анаферон также эффективен и в отношении инфекций, вызванных респираторно-синцитиальным вирусом, которые чаще других ОР- ВИ сопровождаются осложнениями со стороны нижних дыхательных путей, а также для лечения которых в настоящее время не существует средств специфической терапии [10].
Высокая безопасность, практически полное отсутствие противопоказаний и способность препарата сокращать количество бактериальных осложнений, позволяет эффективно применять анаферон в лечении вирусных инфекций у детей со вторичными иммунодефицитными состояниями, а так же у детей с сопутствующей патологией. Так, уже имеется положительный опыт применения анаферона в профилактике ОРВИ у детей с ВИЧ-инфекцией — отмечено как снижение заболеваемости, так и уменьшение количества повторных ОРВИ по сравнению с контрольной группой [11].
Доказана эффективность анаферона в профилактике и реабилитации часто болеющих детей, относящихся к группе риска в связи со сниженным иммунитетом, применение препарата у которых позволяет существенно снизить респираторную заболеваемость и облегчить течение клинических симптомов ОРВИ [12].
Имеются достоверные доказательства эффективности анаферона в комплексе профилактики и лечения ОРВИ у детей с бронхиальной астмой. Включение анаферона в комплекс медикаментозной коррекции способствует уменьшению частоты приступов бронхиальной астмы и повышению качества ведения больных с атопией в эпидемиологически неблагоприятный период [13].
Клиническая эффективность анаферона в отношении герпесвирусных инфекций, относящихся к числу плохо контролируемых инфекций, была продемонстрирована в нескольких рандомизированных исследованиях. Доказана эффективность препарата в отношении 4 из 8 герпесвирусов патогенных для человека. Применение анаферона способствует элиминации вируса простого герпеса при бессимптомном носительстве. Анаферон существенно сокращает длительность симптомов ветряной оспы (длительность лихорадки, появления новых высыпаний, зуда) [14] и инфекционного мононуклеоза (длительность ангины, лимфоаденопатии и гепатолиенального синдрома) [15], а также частоту бактериальных осложнений.
Анаферон хорошо сочетается со средствами специфической терапии герпесвирусных инфекций (ацикловир, валцикловир) — комбинация с которыми эффективна в купировании общих и местных симптомов рецидивирующего генитального герпеса [16], терапии рецидивов офтальмогерпеса [17] и терапии инфекционного мононуклеоза [18].
Эффективность анаферона в комплексной терапии острых кишечных вирусных инфекций (ОКВИ), вызванных калицивирусами, ротавирусами и коронавирусами, оценивали в рамках 3 рандомизированных контролируемых клинических исследований. Включение анаферона в стандартную терапию ОКВИ статистически значимо сократило длительность основных симптомов заболевания: лихорадки, диареи и рвоты. ОКВИ относятся к числу наиболее распространенных вирусных инфекций (после ОРВИ), в настоящее время, в связи с отсутствием средств специфической терапии, в основе лечения лежит только патогенетическая терапия, поэтому доказанная эффективность анаферона в отношении данных инфекций играет большое значение для практической медицины.
Эффективность анаферона в профилактике инфекционных заболеваний нервной системы была показана на примере экстренной профилактики клещевого энцефалита, актуальность которого связана высокой летальностью (около 20%). На фоне 21-дневного применения анаферона из детей основной группы, в отличие от группы сравнения (дети, получавшие противоклещевой иммуноглобулин с профилактической целью), не заболел ни один пациент, кроме того более чем на три порядка сократилось количество пациентов у которых через месяц после укуса клеща выделялся антиген клещевого энцефалита. Таким образом, профилактическая эффективность анаферона в отношении клещевого энцефалита превосходит традиционную серопрофилактику [19].
В ходе клинических исследований также показано положительное действие анаферона в условиях вирусной инфекции на интерфероновый статус, на содержание в периферической крови лимфоцитов различных субпопуляций, на выработку секреторного IgA слизистыми и на содержание IgE в сыворотке.
В результате 9-летнего опыта применения анаферона доказана его эффективность в лечении и/или профилактике широкого спектра инфекционных заболеваний различной этиологии, а так же микст инфекций:
- острые респираторные вирусные инфекции, вызванные вирусом гриппа А (включая птичий грипп А/Н5Ш и свиной грипп А/НЖ1) и В, аденовирусом, респираторно синцитиальным вирусом, коронавирусом, вирусом парагриппа, и др;
- герпесвирусные инфекции, вызванные вирусом ветряной оспы, вирусом Эпшейн-Барр, вирусом простого герпеса (I и II типы);
- острые кишечные вирусные инфекции, вызванные калицивирусом, коронавирусом, ротавирусом;
- показана эффективность в лечении клещевого энцефалита, псевдотуберкулеза, иерсиниоза, коклюша, геморрагической лихорадки с почечным синдромом, тубулоинтерстициального нефрита, энтеровирусного и менингококкового менингита, хламидийной инфекции, эпидемического паротита, энтеровирусных инфекций (коксакивирусы А и В, ЕСНО).
Наличие у анаферона не только выраженного противовирусного действия, но и иммуномодулирую- щей активности позволяет эффективно его использовать на фоне вторичных иммунодефецитных состояний, а также в лечении хронических инфекций, которые наиболее трудно поддаются лечению в связи с высокой изменчивостью вирусов-возбудителей и их способностью подавлять иммунный ответ [20].
Таким образом, в экспериментально-клинических исследованиях, проведенных в соответствии с требованиями GLP и GCP доказан широкий спектр противовирусной и антибактериальной активности анаферона, сочетание которой с практически полным отсутствием нежелательных явлений, связанных с его приемом, делает анаферон препаратом выбора для лечения инфекционных заболеваний различной этиологии (в том числе у детей младше 1 года), а так же инфекций на фоне сопутствующей патологии.
Читайте также:

