Что относится к гнойно септическим заболеваниям
Обновлено: 25.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Абсцесс: причины появления, симптомы, диагностика и способы лечения.
Определение
Абсцесс - это ограниченное скопление гноя, окруженное оболочкой (пиогенной капсулой).
Причины появления абсцессов
Абсцессы могут быть асептическими и септическими. Асептические абсцессы развиваются после подкожного введения некоторых раздражающих химических веществ (скипидара, керосина, хлоралгидрата, хлористого кальция), которые вызывают некроз тканей. При этом некротизированные ткани растворяются лейкоцитами с образованием гноя, не содержащего микробов. Септические абсцессы чаще всего формируются в результате внедрения в ткани микроорганизмов (стафилококков, стрептококков, кишечной палочки, синегнойной палочки и т.д.), вызывающих гнойное воспаление.
Инфекционные агенты (бактерии, грибы) могут проникать в организм экзогенно через поврежденный эпителий кожи или слизистые оболочки (входные ворота) или эндогенно (из очага инфекции в самом организме).
Открытые повреждения кожи, инородные тела, медицинские манипуляции (инъекции, блокады, пункции), гематомы, серомы, а также гнойно-воспалительные процессы в организме (сепсис, гнойный лимфаденит, гнойный лимфангит, гнойный тромбофлебит, фурункул, карбункул и др.) могут приводить к развитию абсцесса.
На месте внедрения инфекции и воспаления ткани отмирают, и формируется гнойная полость, вокруг которой на границе со здоровой тканью начинает образовываться пиогенная капсула. Эта капсула служит своеобразным биологическим барьером, препятствующим распространению инфекции по организму. Чем дольше существует абсцесс, тем толще становится пиогенная капсула.
По распространенности самым частым считается абсцесс кожи, подкожной жировой клетчатки и мышечной ткани, хотя возникнуть он может в любом органе и ткани.
При прогрессировании гнойного процесса повышается риск разрыва пиогенной капсулы, в результате чего инфекционный процесс распространяется за ее пределы.
Классификация абсцессов
По причине возникновения:
а) стафилококковые;
б) стрептококковые;
в) пневмококковые;
г) колибациллярные;
д) гонококковые;
е) анаэробные неспорообразующие;
ж) клостридиальные анаэробные;
з) смешанные;
и) грибковые и др.
По происхождению и путям проникновения инфекции:
- метастатические (гематогенные) абсцессы, возникающие из отдаленных гнойных очагов;
- контактные абсцессы, происходящие из близлежащих очагов воспаления;
- травматические абсцессы, являющиеся следствием открытых и проникающих повреждений;
- криптогенные абсцессы, происхождение которых и пути проникновения инфекции установить не представляется возможным.
- поверхностные (поражение кожи и подкожной клетчатки);
- глубокие (в органах и тканях):
- острые абсцессы;
- хронические абсцессы.
Симптомы абсцессов
В начальной стадии формирования поверхностного абсцесса определяется отграниченная болезненная припухлость, горячая на ощупь. Через 3-4 дня в центре появляется размягчение, кожа в центре инфильтрата становится более тонкой и темной, а границы абсцесса - более четкими. На 4-7 сутки абсцесс вскрывается и из него выходит гнойное содержимое. При этом болезненность воспаленного участка уменьшается.
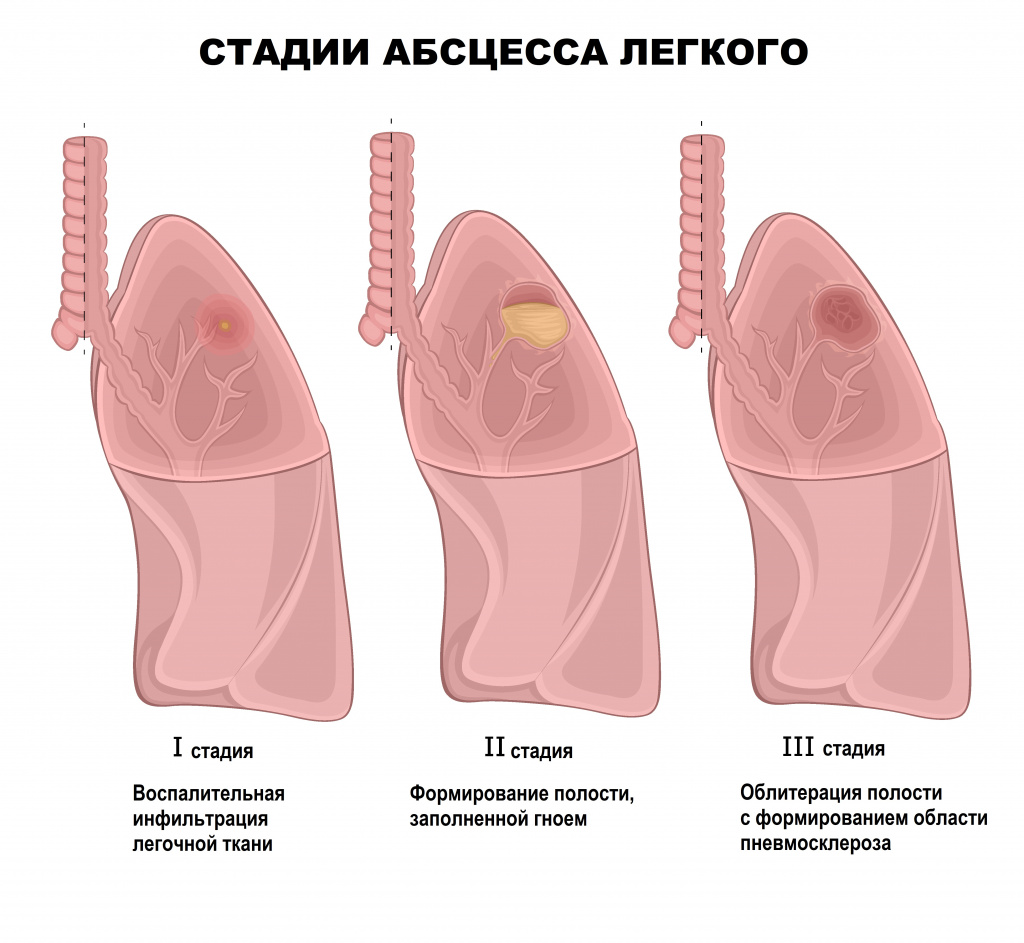
Абсцесс печени чаще всего возникает в результате распространения инфекции по сосудистому руслу из воспалительных очагов других органов или тканей брюшной полости (аппендицит, холангит, язвенный колит). Абсцессы могут быть одиночными или множественными. Для заболевания характерна высокая температура, озноб, боль и тяжесть в области печени, увеличение ее размеров.
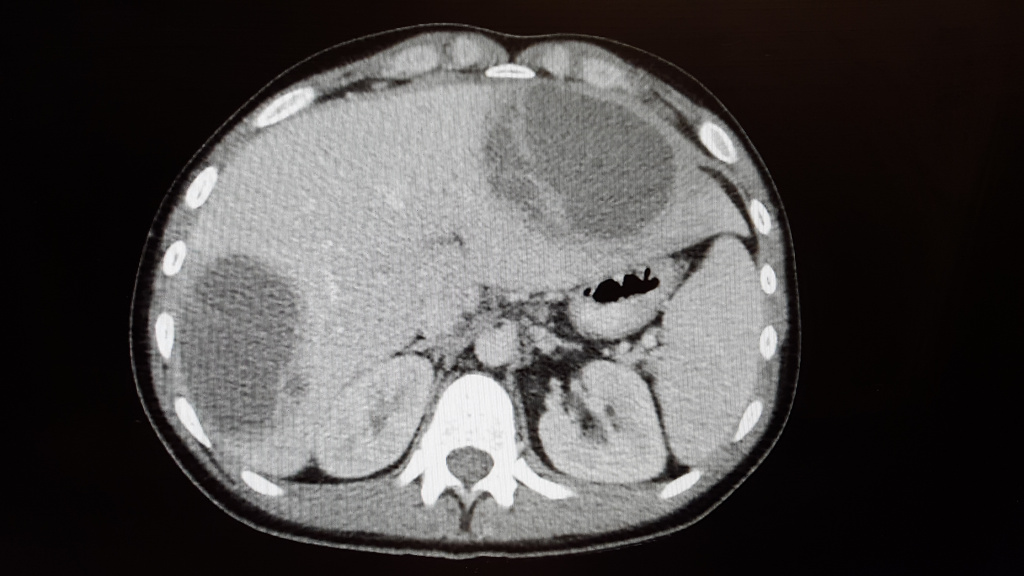
Абсцесс в печени
Абсцесс головного мозга может сформироваться в результате проникновения инфекции из среднего или внутреннего уха, придаточных пазух носа, из гнойных очагов мягких тканей головы. Абсцессы могут быть одиночными или множественными. Заболевание начинается с интоксикации, симптомов повышения внутричерепного давления (головной боли, тошноты и рвоты, сонливости, недомогания, нарушения памяти, расстройства внимания, нарушения зрения). Затем присоединяются общемозговые (головокружение, психомоторное возбуждение, галлюцинации) и очаговые симптомы (неврологические симптомы, свойственные местному поражению определенных структур центральной или периферической нервной системы).
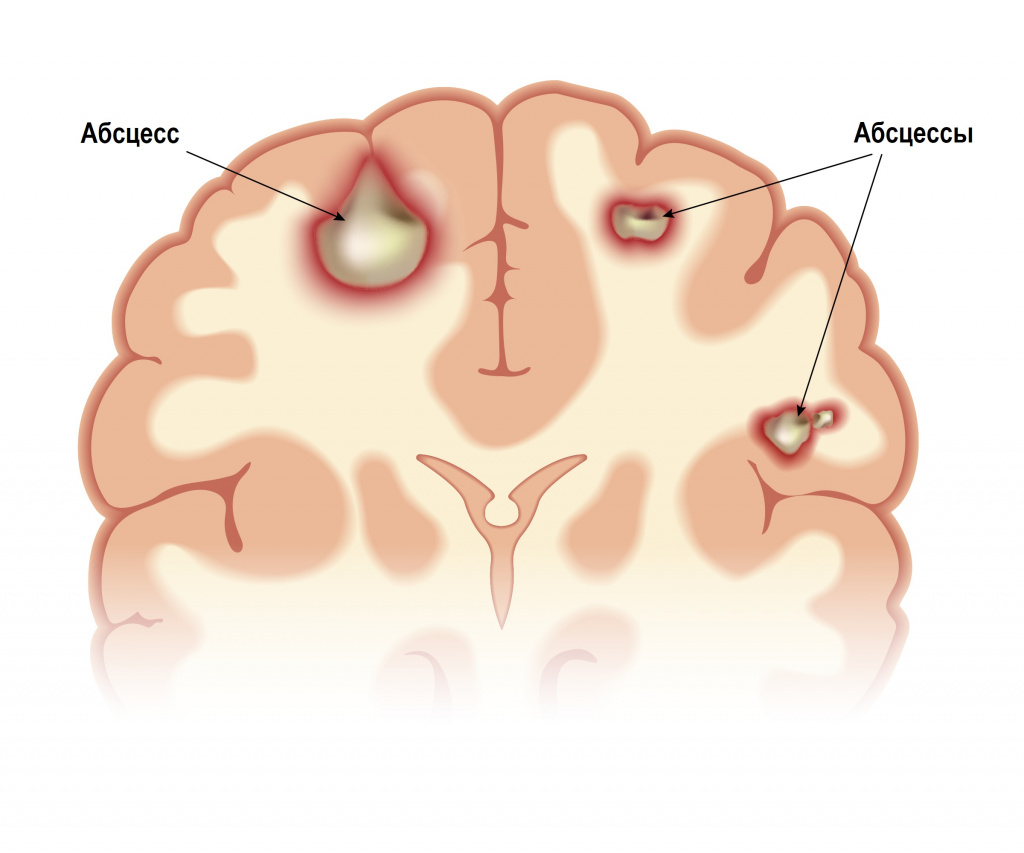
Внутримозговой абсцесс
Абсцессы брюшной полости встречаются в 30-35% у больных гнойным перитонитом. Обычно они располагаются в отлогих областях живота: подпеченочном, поддиафрагмальном пространстве, в подвздошных ямках и т.п. Клинике формирования абсцесса соответствует ухудшение состояния после небольшого светлого промежутка на фоне воспалительного заболевания брюшной полости (аппендицита, холецистита), наблюдается усиление интоксикации и боль в животе.
Внутрикостный абсцесс Броди – это отграниченный некроз губчатого вещества кости с преследующим расплавлением и образованием полости. Локализуется обычно в проксимальном отделе большеберцовой кости. Заболевание начинается с чувствительности к надавливанию. Нередко очаги ничем не проявляются, и боль носит эпизодический характер. Повышение температуры, озноб и другие симптомы интоксикации, как правило, отсутствуют, процесс может длиться годами.
Диагностика абсцессов
Диагностика поверхностного абсцесса не представляет трудностей. Диагноз устанавливается по совокупности жалоб и осмотра. Диагностика глубоких абсцессов может быть основана на результатах дополнительных лабораторных и инструментальных методов исследования.
-
Клинический анализ крови: общий анализ, лейкоформула, СОЭ (с микроскопией мазка крови при наличии патологических сдвигов) покажет присутствие в организме воспалительного процесса.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Внутрибольничные инфекции – различные инфекционные заболевания, заражение которыми произошло в условиях лечебного учреждения. В зависимости от степени распространения различают генерализованные (бактериемию, септицемию, септикопиемию, бактериальный шок) и локализованные формы внутрибольничных инфекций (с поражением кожи и подкожной клетчатки, дыхательной, сердечно-сосудистой, урогенитальной системы, костей и суставов, ЦНС и т. д.). Выявление возбудителей внутрибольничных инфекций проводится с помощью методов лабораторной диагностики (микроскопических, микробиологических, серологических, молекулярно-биологических). При лечении внутрибольничных инфекций используются антибиотики, антисептики, иммуностимуляторы, физиотерапия, экстракорпоральная гемокоррекция и т. д.

Общие сведения
Внутрибольничные (госпитальные, нозокомиальные) инфекции - инфекционные заболевания различной этиологии, возникшие у пациента или медицинского сотрудника в связи с пребыванием в лечебно-профилактическом учреждении. Инфекция считается внутрибольничной, если она развилась не ранее 48 часов после поступления больного в стационар. Распространенность внутрибольничных инфекций (ВБИ) в медицинских учреждениях различного профиля составляет 5-12%. Наибольший удельный вес внутрибольничных инфекций приходится на акушерские и хирургические стационары (отделения реанимации, абдоминальной хирургии, травматологии, ожоговой травмы, урологии, гинекологии, отоларингологии, стоматологии, онкологии и др.). Внутрибольничные инфекции представляют собой большую медико-социальную проблему, поскольку утяжеляют течение основного заболевания, увеличивают длительность лечения в 1,5 раза, а количество летальных исходов - в 5 раз.

Этиология и эпидемиология внутрибольничных инфекций
Основными возбудителями внутрибольничных инфекций (85% от общего числа) выступают условно-патогенные микроорганизмы: грамположительные кокки (эпидермальный и золотистый стафилококк, бета-гемолитический стрептококк, пневмококк, энтерококк) и грамотрицательные палочковидные бактерии (клебсиеллы, эшерихии, энтеробактер, протей, псевдомонады и др.). Кроме этого, в этиологии внутрибольничных инфекций велика удельная роль вирусных возбудителей простого герпеса, аденовирусной инфекции, гриппа, парагриппа, цитомегалии, вирусных гепатитов, респираторно-синцитиальной инфекции, а также риновирусов, ротавирусов, энтеровирусов и пр. Также внутрибольничные инфекции могут быть вызваны условно-патогенными и патогенными грибами (дрожжеподобными, плесневыми, лучистыми). Особенностью внутригоспитальных штаммов условно-патогенных микроорганизмов служит их высокая изменчивость, лекарственная резистентность и устойчивость к воздействию факторов среды (ультрафиолета, дезинфектантов и пр.).
Источниками внутрибольничных инфекций в большинстве случаев выступают пациенты или медицинский персонал, являющиеся бактерионосителями или больными стертыми и манифестными формами патологии. Как показывают исследования, роль третьих лиц (в частности, посетителей стационаров) в распространении ВБИ невелика. Передача различных форм госпитальной инфекции реализуется с помощью воздушно-капельного, фекально-орального, контактного, трансмиссивного механизма. Кроме этого, возможен парентеральный путь передачи внутрибольничной инфекции при проведении различных инвазивных медицинских манипуляций: забора крови, инъекций, вакцинации, инструментальных манипуляций, операций, ИВЛ, гемодиализа и пр. Таким образом в медучреждении возможно заразиться гепатитами В, С и D, гнойно-воспалительными заболеваниями, сифилисом, ВИЧ-инфекцией. Известны случаи внутрибольничных вспышек легионеллеза при приеме больными лечебного душа и вихревых ванн.
Факторами, участвующими в распространении внутрибольничной инфекции, могут выступать контаминированные предметы ухода и обстановки, медицинский инструментарий и аппаратура, растворы для инфузионной терапии, спецодежда и руки медперсонала, изделия медицинского назначения многоразового использования (зонды, катетеры, эндоскопы), питьевая вода, постельные принадлежности, шовный и перевязочный материал и мн. др.
Значимость тех или иных видов внутрибольничной инфекции во многом зависит от профиля лечебного учреждения. Так, в ожоговых отделениях преобладает синегнойная инфекция, которая в основном передается через предметы ухода и руки персонала, а главным источником внутрибольничной инфекции являются сами пациенты. В учреждениях родовспоможения основную проблему представляет стафилококковая инфекция, распространяемая медицинским персоналом-носителем золотистого стафилококка. В урологических отделениях доминирует инфекция, вызываемая грамотрицательной флорой: кишечной, синегнойной палочкой и др. В педиатрических стационарах особую значимость имеет проблема распространения детских инфекций – ветряной оспы, эпидемического паротита, краснухи, кори. Возникновению и распространению внутрибольничной инфекции способствуют нарушение санитарно-эпидемиологического режима ЛПУ (несоблюдение личной гигиены, асептики и антисептики, режима дезинфекции и стерилизации, несвоевременное выявление и изоляция лиц-источников инфекции и т. д.).
К группе риска, в наибольшей степени подверженной развитию внутрибольничной инфекции, относятся новорожденные (особенно недоношенные) и дети раннего возраста; пожилые и ослабленные пациенты; лица, страдающие хроническими заболеваниями (сахарным диабетом, болезнями крови, почечной недостаточностью), иммунодефицитом, онкопатологией. Восприимчивость человека к внутрибольничным инфекциям увеличивается при наличии у него открытых ран, полостных дренажей, внутрисосудистых и мочевых катетеров, трахеостомы и других инвазивных устройств. На частоту возникновения и тяжесть течения внутрибольничной инфекции влияет долгое нахождение пациента в стационаре, длительная антибиотикотерапия, иммуносупрессивная терапия.
Классификация внутрибольничных инфекций
По длительности течения внутрибольничные инфекции делятся на острые, подострые и хронические; по тяжести клинических проявлений – на легкие, среднетяжелые и тяжелые формы. В зависимости от степени распространенности инфекционного процесса различают генерализованные и локализованные формы внутрибольничной инфекции. Генерализованные инфекции представлены бактериемией, септицемией, бактериальным шоком. В свою очередь, среди локализованных форм выделяют:
- инфекции кожи, слизистых и подкожной клетчатки, в т. ч. послеоперационных, ожоговых, травматических ран. В частности, к их числу относятся омфалит, абсцессы и флегмоны, пиодермия, рожа, мастит, парапроктит, грибковые инфекции кожи и др.
- инфекции полости рта (стоматит) и ЛОР-органов (ангина, фарингит, ларингит, эпиглоттит, ринит, синусит, отит, мастоидит)
- инфекции бронхолегочной системы (бронхит, пневмония, плеврит, абсцесс легкого, гангрена легкого, эмпиема плевры, медиастинит)
- инфекции пищеварительной системы (гастрит, энтерит, колит, вирусные гепатиты)
- глазные инфекции (блефарит, конъюнктивит, кератит)
- инфекции урогенитального тракта (бактериурия, уретрит, цистит, пиелонефрит, эндометрит, аднексит)
- инфекции костно-суставной системы (бурсит, артрит, остеомиелит)
- инфекции сердца и сосудов (перикардит, миокардит, эндокардит, тромбофлебиты).
- инфекции ЦНС (абсцесс мозга, менингит, миелит и др.).
Диагностика внутрибольничных инфекций
Критериями, позволяющими думать о развитии внутрибольничной инфекции, служат: возникновение клинических признаков заболевания не ранее чем через 48 часов после поступления в стационар; связь с проведением инвазивного вмешательства; установление источника инфекции и фактора передачи. Окончательное суждение о характере инфекционного процесса получают после идентификации штамма возбудителя с помощью лабораторных методов диагностики.
Для исключения или подтверждения бактериемии проводится бактериологический посев крови на стерильность, желательно не менее 2-3-х раз. При локализованных формах внутрибольничной инфекции микробиологическое выделение возбудителя может быть произведено из других биологических сред, в связи с чем выполняется посев мочи, кала, мокроты, отделяемого ран, материала из зева, мазка с конъюнктивы, из половых путей на микрофлору. Дополнительно к культуральному методу выявления возбудителей внутрибольничных инфекций используются микроскопия, серологические реакции (РСК, РА, ИФА, РИА), вирусологический, молекулярно-биологический (ПЦР) методы.
Лечение внутрибольничных инфекций
Сложности лечения внутрибольничной инфекции обусловлены ее развитием в ослабленном организме, на фоне основной патологии, а также резистентностью госпитальных штаммов к традиционной фармакотерапии. Больные с диагностированными инфекционными процессами подлежат изоляции; в отделении проводится тщательная текущая и заключительная дезинфекция. Выбор противомикробного препарата основывается на особенностях антибиотикограммы: при внутрибольничной инфекции, вызванной грамположительной флорой наиболее эффективен ванкомицин; грамотрицательными микроорганизмами – карбапенемы, цефалоспорины IV поколения, аминогликозиды. Возможно дополнительное применение специфических бактериофагов, иммуностимуляторов, интерферона, лейкоцитарной массы, витаминотерапии.
При необходимости проводится чрескожное облучение крови (ВЛОК, УФОК), экстракорпоральная гемокоррекция (гемосорбция, лимфосорбция). Симптоматическая терапия осуществляется с учетом клинической формы внутрибольничной инфекции с участием специалистов соответствующего профиля: хирургов, травматологов, пульмонологов, урологов, гинекологов и др.
Профилактика внутрибольничных инфекций
Основные меры профилактики внутрибольничных инфекций сводятся к соблюдению санитарно-гигиенических и противоэпидемических требований. В первую очередь, это касается режима дезинфекции помещений и предметов ухода, применения современных высокоэффективных антисептиков, проведения качественной предстерилизационной обработки и стерилизации инструментария, безукоснительного следования правилам асептики и антисептики.
Медицинский персонал должен соблюдать меры индивидуальной защиты при проведении инвазивных процедур: работать в резиновых перчатках, защитных очках и маске; осторожно обращаться с медицинским инструментарием. Большое значение в профилактике внутрибольничных инфекций имеет вакцинация медработников от гепатита В, краснухи, гриппа, дифтерии, столбняка и других инфекций. Все сотрудники ЛПУ подлежат регулярному плановому диспансерному обследованию, направленному на выявление носительства патогенов. Предупредить возникновение и распространение внутрибольничных инфекций позволит сокращение сроков госпитализации пациентов, рациональная антибиотикотерапия, обоснованность проведения инвазивных диагностических и лечебных процедур, эпидемиологический контроль в ЛПУ.
Послеродовые инфекции – группа заболеваний инфекционной этиологии, развивающихся в течение 6-ти недель после родов и непосредственно связанных с ними. Включают в себя локальные раневые инфекции, инфекции органов малого таза, генерализованные септические инфекции. В диагностике послеродовых инфекций первостепенное значение имеет время их развития и связь с родами, картина периферической крови, данные гинекологического осмотра, УЗИ, бактериологического исследования. Лечение послеродовых инфекций включает антибиотикотерапию, иммуностимулирующую и инфузионную терапию, экстракорпоральную детоксикацию, санацию первичного очага и др.
Общие сведения
Послеродовые (пуэрперальные) инфекции - гнойно-воспалительные заболевания, патогенетически обусловленные беременностью и родами. Включают в себя раневые инфекции (послеродовые язвы, эндометрит), инфекции, ограниченные полостью малого таза (метрит, параметрит, сальпингоофорит, пельвиоперитонит, метротромбофлебит и др.), разлитые инфекции (перитонит, прогрессирующий тромбофлебит) и генерализованные инфекции (септический шок, сепсис). Временные рамки, в течение которых могут развиваться данные осложнения - от момента выделения последа до окончания шестой недели послеродового периода. Пуэрперальные заболевания инфекционной этиологии встречаются у 2-10% родильниц. Септические осложнения играют ведущую роль в структуре материнской смертности, что ставит их в ряд приоритетных проблем акушерства и гинекологии.

Причины послеродовых инфекций
Этиологическая структура послеродовых инфекций весьма динамична и вариабельна. Из условно-патогенных микроорганизмов преобладают аэробные бактерии (энтерококки, кишечная палочка, стафилококки, стрептококки группы В, клебсиелла, протей), однако довольно часто встречаются и анаэробы (фузобактерии, бактероиды, пептострептококки, пептококки). Велика значимость специфических возбудителей - хламидий, микоплазм, грибов, гонококков, трихомонад. Особенностью послеродовых инфекций является их полиэтиологичность: более чем в 80% наблюдений высеваются микробные ассоциации, которые обладают большей патогенностью и устойчивостью к антибиотикотерапии.
Риск развития послеродовых инфекций существенно повышен у женщин с патологией беременности (анемия, токсикоз) и родов (раннее отхождение вод, слабая родовая деятельность, пролонгированные роды, кровотечение, задержка частей плаценты, лохиометра и др.), экстрагенитальной патологией (туберкулез, ожирение, сахарный диабет). Эндогенными факторами, предрасполагающими к микробному обсеменению родовых путей, могут служить вульвовагиниты, кольпиты, цервициты, пиелонефрит, тонзиллит, синуситы у родильницы. При инфицировании высоковирулентной флорой либо значительном снижении иммунных механизмов у родильницы инфекция может распространяться за пределы первичного очага гематогенным, лимфогенным, интраканаликулярным, периневральным путем.
Классификация послеродовых инфекций
На основании анатомо-топографического и клинического подхода выделяют 4 этапа прогрессирования послеродовой инфекции (авторы - С. В. Сазонова, А. В. Бартельс).
- 1-й этап – местная инфекция, не распространяющаяся за область раневой поверхности (послеродовая язва промежности, влагалища и стенки матки, нагноение швов, нагноение гематом, послеродовой эндометрит)
- 2-й этап – послеродовая инфекция, выходящая за границы раневой поверхности, но ограниченная полостью малого таза (метроэндометрит, аднексит, параметрит, метротромбофлебит, ограниченный тазовый тромбофлебит, пельвиоперитонит)
- 3-й этап – разлитая послеродовая инфекция (перитонит, прогрессирующий тромбофлебит)
- 4-й этап – генерализованная септическая инфекция (сепсис, инфекционно-токсический шок).
В качестве отдельной формы послеродовой инфекции выделяют лактационный мастит. Тяжесть инфекционных осложнений после родов зависит от вирулентности микрофлоры и реактивности макроорганизма, поэтому течение заболеваний варьирует от легких и стертых форм до тяжелых и летальных случаев.
Симптомы послеродовых инфекций
Послеродовая язва образуется в результате инфицирования ссадин, трещин и разрывов кожи промежности, слизистой влагалища и шейки матки. В клинической картине данного послеродового осложнения преобладают местные симптомы, общее состояние обычно не нарушается, температура не превышает субфебрильных цифр. Родильница жалуется на боли в области швов, иногда зуд и дизурические явления. При осмотре родовых путей обнаруживается язва с четкими границами, локальный отек и воспалительная гиперемия. На дне язвы определяется серовато-желтый налет, участки некроза, слизисто-гнойное отделяемое. Язвенный дефект легко кровоточит при контакте.
Послеродовой параметрит развивается на 10–12 день при переходе инфекции на параметрий - околоматочную клетчатку. Типичная клиника включает озноб, фебрильную лихорадку, которая длится 7-10 дней, интоксикацию. Родильницу беспокоят боли в подвздошной области на стороне воспаления, которые постепенно нарастают, иррадиируют в поясницу и крестец. Через несколько дней от начала послеродовой инфекции в области боковой поверхности матки пальпируется болезненный инфильтрат сначала мягковатой, а затем плотной консистенции, спаянный с маткой. Исходами послеродового параметрита может быть рассасывание инфильтрата или его нагноение с формированием абсцесса. Самопроизвольное вскрытие гнойника может произойти во влагалище, мочевой пузырь, матку, прямую кишку, брюшную полость.
Послеродовые тромбофлебиты могут затрагивать поверхностные и глубокие вены. В последнем случае возможно развитие метротромбофлебита, тромбофлебита вен нижних конечностей и вен таза. Обычно проявляются в течение 2-3 недель после родов. Клиническими предвестниками послеродовых осложнений данного типа служат длительная лихорадка; стойкое ступенеобразное учащение пульса; боли в ногах при движении и надавливании на мягкие ткани; отеки в области лодыжек, голени или бедра; цианоз нижних конечностей. На развитие метротромбофлебита указывает тахикардия до 100 уд./мин., субинволюция матки, длительные кровяные выделения, пальпация болезненных тяжей по боковым поверхностям матки. Тромбофлебит вен таза опасен развитием илеофеморального венозного тромбоза и тромбоэмболии легочной артерии.
Послеродовой пельвиоперитонит, или воспаление брюшины малого таза, развивается на 3-4 день после родов. Манифестация острая: температура тела быстро нарастает до 39-40°С, появляются резкие боли внизу живота. Может возникать рвота, метеоризм, болезненная дефекация. Передняя брюшная стенка напряжена, матка увеличена. Послеродовая инфекция разрешается рассасыванием инфильтрата в малом тазу или образованием абсцесса дугласова пространства.
Диагностика послеродовых инфекций
Факторами, указывающими на развитие послеродовых инфекций, служат признаки инфекционно-гнойного воспаления в области родовой раны или органов малого таза, а также общие септические реакции, возникшие в ранний период после родов (до 6-8 недель). Такие осложнения, как послеродовая язва, нагноение швов или гематомы диагностируются на основании визуального осмотра родовых путей. Заподозрить послеродовые инфекции органов малого таза гинекологу позволяет влагалищное исследование. В этих случаях обычно обнаруживается замедленное сокращение матки, ее болезненность, пастозность околоматочного пространства, инфильтраты в малом тазу, мутные зловонные выделения из половых путей.
Дополнительные данные получают при проведении гинекологического УЗИ. В случае подозрения на тромбофлебит показана допплерография органов малого таза, УЗДГ вен нижних конечностей. При послеродовом эндометрите информативна гистероскопия; при гнойном параметрите - пункция заднего свода влагалища. По показаниям применяют лучевые способы диагностики: флебографию, гистерографию, радиоизотопное исследование.
Для всех клинических форм послеродовой инфекции характерно изменение картины периферической крови: значительный лейкоцитоз с нейтрофильным сдвигом влево, резкое увеличение СОЭ. С целью идентификации инфекционных агентов производится бакпосев отделяемого половых путей и содержимого матки. Гистологическое исследование последа может указывать на признаки воспаления и, следовательно, высокую вероятность развития послеродовых инфекций. Важную роль в планировании терапии и оценке тяжести течения осложнений имеет исследование биохимии крови, КЩС, электролитов крови, коагулограммы.
Лечение послеродовых инфекций
Весь комплекс лечебных мероприятий при послеродовых инфекциях делится на местные и общие. Постельный режим и прикладывание льда к животу помогает остановить дальнейшее распространение инфекции из полости таза.
Локальные процедуры включают обработку ран антисептиками, перевязки, мазевые аппликации, снятие швов и раскрытие раны при ее нагноении, удаление некротизированных тканей, местное применение протеолитических ферментов. При послеродовом эндометрите может потребоваться проведение кюретажа или вакуум-аспирации полости матки (при задержке в ней плацентарной ткани и других патологических включений), расширение цервикального канала, аспирационно-промывное дренирование. При формировании абсцесса параметрия производится его вскрытие через влагалище или путем лапаротомии и дренирование околоматочной клетчатки.
Местные мероприятия при послеродовых инфекциях проводятся на фоне интенсивной общей терапии. В первую очередь, подбираются антибактериальные средства, активные в отношении всех выделенных возбудителей (пенициллины широкого спектра действия, цефалоспорины, аминогликозиды и другие), которые вводятся внутримышечно или внутривенно в сочетании в метронидазолом. На время лечения целесообразно прервать грудное вскармливание. С целью дезинтоксикации и устранения водно-солевого дисбаланса используются инфузии коллоидных, белковых, солевых растворов. Возможно проведение экстракорпоральной детоксикации: гемосорбции, лимфосорбции, плазмафереза.
При послеродовых инфекциях стафилококковой этиологии с целью повышения специфической иммунологической реактивности применяется антистафилококковый гамма-глобулин, стафилококковый анатоксин, антистафилококковая плазма. С целью профилактики тромбозов назначают антикоагулянты, тромболитики, антиагреганты под контролем коагулограммы. В комплексе медикаментозной терапии широко используются антигистаминные препараты, витамины, глюкокортикоиды. На этапе реабилитации назначают лазеротерапию, местное УФО, УВЧ-терапию, ультразвук, электростимуляцию матки, бальнеотерапию и другие методы физиотерапевтического воздействия.
В отдельных случаях может потребоваться хирургическая помощь – удаление матки (гистерэктомия) при ее гнойном расплавлении; тромбэктомия, эмболэктомия или флебэктомия - при тромбофлебитах.
Прогноз и профилактика
При раневых инфекциях и инфекциях, ограниченных областью малого таза, прогноз удовлетворительный. Своевременная и адекватная терапия позволяет остановить дальнейшее прогрессирование послеродовых инфекций. Однако в отдаленном периоде прогноз в отношении репродуктивной функции может быть вариабельным. Наиболее тяжелые последствия для здоровья и жизни родильницы влекут за собой разлитой перитонит, сепсис и септический шок.
Профилактика послеродовых инфекций обеспечивается строгим и неукоснительным соблюдением санитарно-гигиенического режима в родовспомогательных учреждениях, правил асептики и антисептики, личной гигиены персонала. Важное значение имеет санация эндогенной инфекции на этапе планирования беременности.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
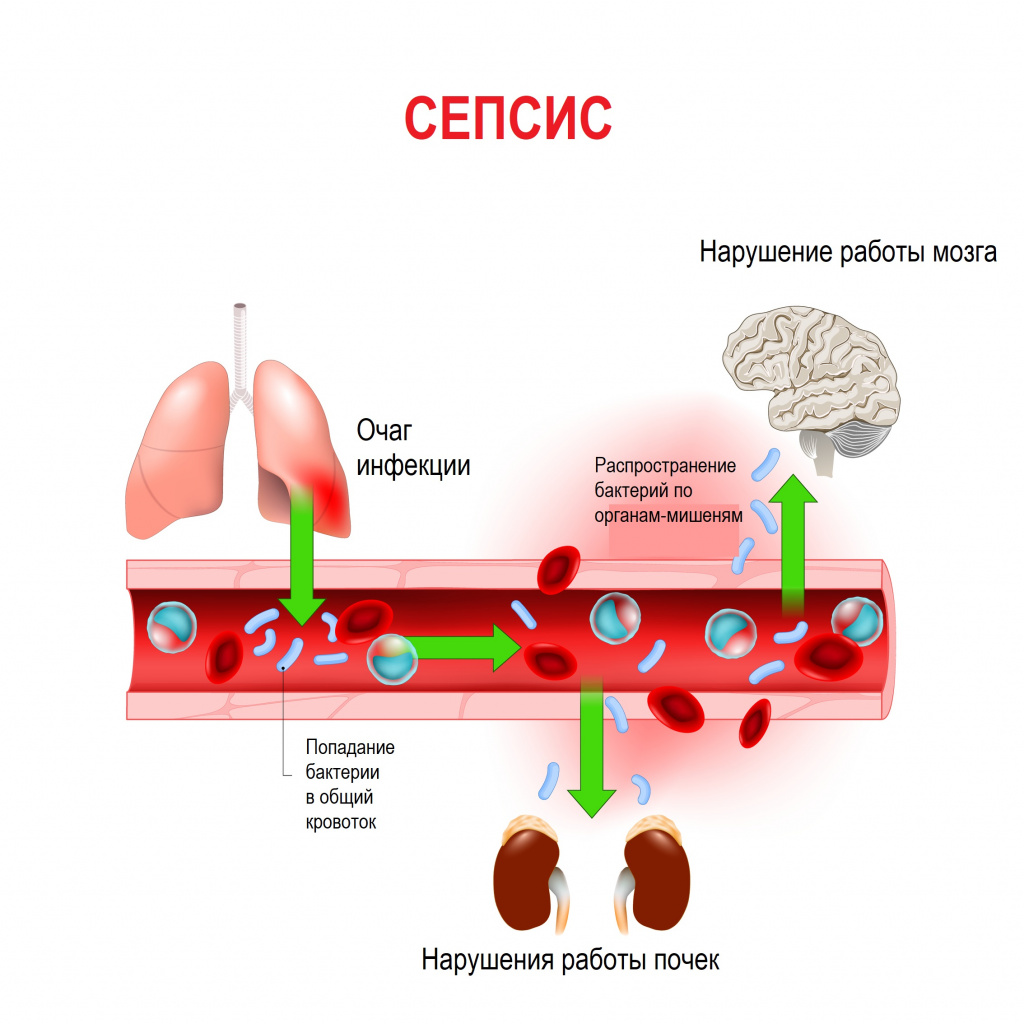
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
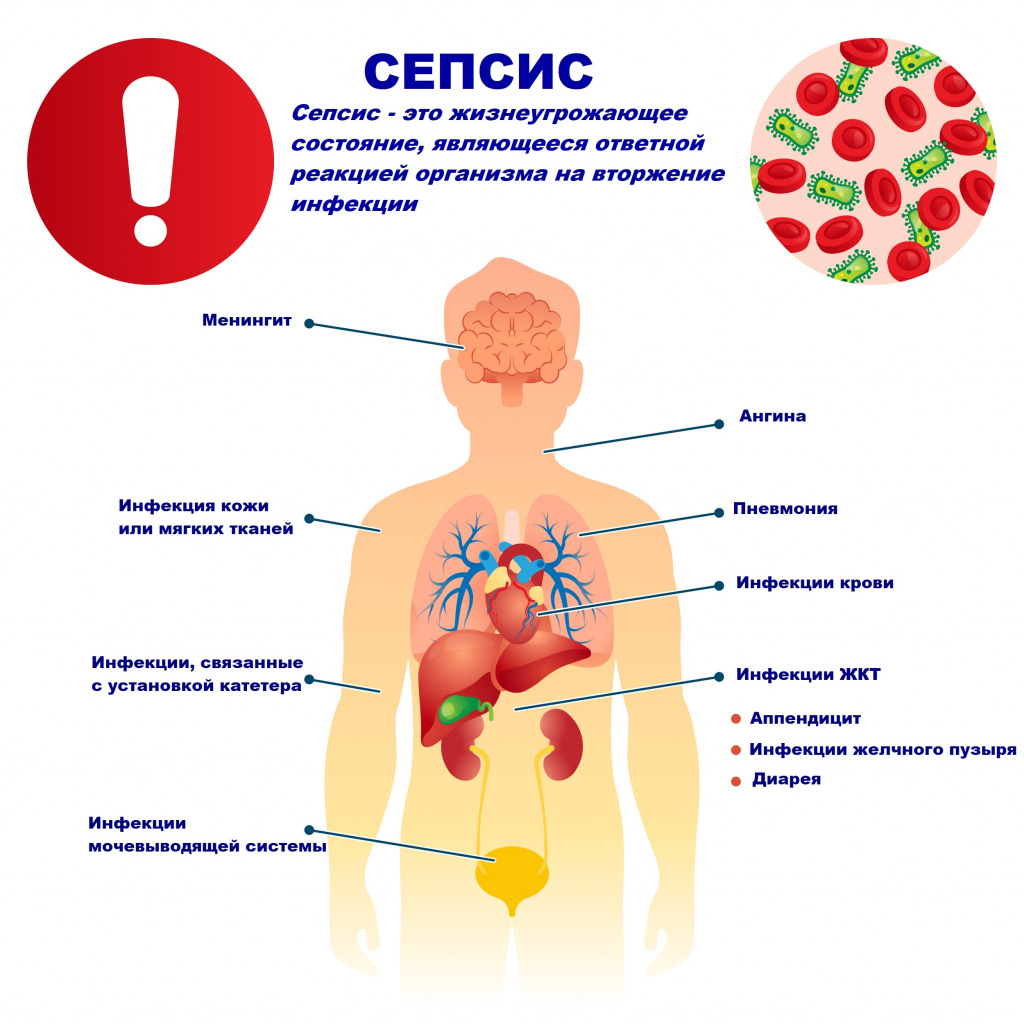
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Гнойные заболевания являются достаточно широко распространенными.
Такие заболевания опасны тем, что при несвоевременно начатом лечении очень велика вероятность возникновения осложнений, среди которых может быть даже частичное, а в редких тяжелых случаях – и полная потеря трудоспособности.
СИМПТОМЫ РАЗВИТИЯ ГНОЙНЫХ ЗАБОЛЕВАНИЙ
При данной патологии возникает воспалительная реакция с развитием общих и местных изменений.
Степень выраженности болезни зависит от обширности воспалительного процесса и общей реактивности организма.
При этом существует универсальное правило, согласно которому показанием к проведению хирургического лечения заболевания является любой гнойный процесс.
Повышение температуры тела (иногда до фебрильных значений),
Симптомы гнойной интоксикации – головная боль, слабость, ухудшение работоспособности, апатия, адинамия, снижение аппетита, сонливость или, напротив, нарушение сна.
Боль в месте воспаления.
Гиперемия кожного покрова в зоне воспаления
Местное повышение температуры над очагом воспаления, сглаженность контуров борозд и линий
Кроме того, отмечаются специфические признаки для каждого в отдельности заболевания.
В зависимости от расположения можно определить вовлечение в патологический процесс определенных областей и вероятность развития осложнений.
Фурункул - это острое гнойно-некротическое воспаление волосяного фолликула, сальной железы и окружающей подкожной клетчатки.
Панариций - скопление отделяемого преимущественно гнойного характера под кожей в области фаланги. При этом могут отмечаться общие симптомы заболевания, однако чаще всего они выражены незначительно. При осмотре на одной из фаланг пальцев, преимущественно проксимальной, определяется зона припухлости, гиперемии.
Фурункулез – это наличие нескольких фурункулов в различных областях, имеющих рецидивирующее течение. При фурункулезе больных необходимо обследовать для выявления нарушений обмена веществ (сахарный диабет, авитаминоз). Лечение проводится комплексное, включая и иммунотерапию.
Карбункул – это острое разлитое гнойно-некротическое воспаление нескольких близлежащих волосяных фолликулов и сальных желез с образованием некроза кожи и подкожной клетчатки, сопровождающееся признаками гнойной интоксикации. Локализация карбункулов чаще всего наблюдается на задней поверхности шеи, межлопаточной области. Обычно карбункул сопровождается лимфаденитом, а при локализации на конечностях – лимфангитом.
Флегмона – это острое гнойное разлитое воспаление клеточных пространств, не имеющие тенденцию к отграничению. Вызывается это заболевание чаще всего стафилококком, а также любой другой гноеродной микрофлорой. Инфекция может проникать в ткани через повреждения кожи и слизистых, после различных инъекций (так называемые постинъекционные флегмоны), лимфогенным и гематогенным путем, при переходе воспаления с лимфатических узлов, карбункула, фурункула и т.д. на окружающую их клетчатку.
Абсцесс – это ограниченное скопление гноя в различных тканях или органах, окруженное пиогенной капсулой. Возбудители и пути проникновения инфекции в ткани такие же как при флегмонах, хотя процент анаэробных возбудителей значительно выше.
Гидраденит- это гнойное воспаление потовых желез. Инфекция попадает при несоблюдении правил гигиены и повышенной потливости.
Мастит - это острое воспаление молочной железы. Мастит в основном развивается в послеродовом периоде во время лактации (лактационный мастит). Инфекция проникает в ткань железы через микротрещины в соске, а также и через молочные ходы при лактостазе.
Рожа. Рожей называют острое серозно-эксудативное воспаление кожи или слизистой. Инфекция попадает через микротрещины, ранки на кожном покрове.
ОСОБЕННОСТИ ЛЕЧЕНИЯ ГНОЙНЫХ ЗАБОЛЕВАНИЙ.
Местная терапия болезни включает в себя консервативные и оперативные методы.
Консервативные методы лечения применяются на ранних стадиях заболевания до образования гнойника, а также в сочетании с оперативным лечением с целью более быстрого и эффективного лечения.
Местное лечение в стадии инфильтрата включает в себя воздействие на него с помощью физиотерапевтических методик.
Обязательно необходимо применение мазей, в состав которых входят антибиотик и противомикробные вещества.
В зависимости от размера гнойного очага при лечении возможно использование обезболивания.
После вскрытия гнойника в ходе хирургического лечения заболевания производят его очищение от гнойного экссудата.
Затем его промывают антисептическим веществом, растворами антибиотиков.
После окончания операции рану никогда не зашивают наглухо, для наилучшего дренирования.
Перевязки заключаются в удалении дренажей и замене их новыми, промывании раны раствором антисептика, заполнении раны мазью, содержащей антибиотик, наложении повязки для предотвращения инфицирования раны.
Профилактика гнойных заболеваний:
В профилактике многих гнойных заболеваний большое значение имеет оздоровление внешней среды, в которой живет и работает человек, т. е. улучшение условий труда и быта.
Так, например, в профилактике целого ряда гнойных заболеваний (фурункулез, пиодермиты и т. п.) большую роль играют мероприятия общегигиенического характера и уход за кожей (особенно рук) и др.
Читайте также:

