Что такое амастиготные трихомонады
Обновлено: 19.04.2024
Известно более 50 разновидностей трихомонад, они обнаруживаются у различных животных в ротовой полости, кишечнике и мочеполовых органах, обитают в водоемах. У человека выделено 3 вида трихомонад: урогенитальная, ротовая и кишечная. В России впервые выявил урогенитальных трихомонад И.П.Лазаревич в 1870г. у беременных женщин и гинекологических больных.
Возбудитель инфекции — Trichomonas vaginalis, относится к царству Protozoa, подцарству Animalia, типу Sarcomastigophora, подтипу Mastigophora, классу Zoomastigophora, отряду Trichomonadidac. Т. vaginalis имеет грушевидное тело длиной 10-36 мкм, удлиненное ядро, смещенное в передний конец, и вакуолизированную цитоплазму. На переднем конце расположены жгутики. Имеется ундулирую-щая мембрана, доходящая до середины тела. Сквозь все тело проходит осевая нить — аксостиль. Эти патогены способны образовывать цис-топодобную форму, хотя они очень чувствительны к условиям среды обитания. Кроме того, паразитируя на клетках эпителия, Т. vaginalis способна повторять рельеф клетки-хозяина. Атипичные формы маскируют возбудителя, осложняя его выявление при микроскопии. Перевести возбудителя в типичную форму и сделать его легко узнаваемым можно только с помощью культивирования. Т. vaginalis хорошо растет на искусственных средах с рН 5,5-6,0 в анаэробных условиях в присутствии бактерий, которыми питаются. Т. vaginalis инфицирует исключительно сквамозный эпителий урогенитального тракта (УГТ), размножаются простейшие за счет деления, являются факультативными анаэробами. Инкубационный период от 4 до 28 дней у половины больных или 1-3 дня.
Урогенитальные трихомонады встречаются в трех формах: грушевидной (основная форма), амебоидной и округлой. Под влиянием специфической терапии изменяется форма и структура возбудителя, паразиты утрачивают способность к фагоцитозу и высвобождают ранее фагоцитированные микроорганизмы (бактерии, вирусы и пр.). Живые трихомонады видны как целые клетки, а погибшие превратились в облаковидные образования, выявляемые как слизь.
Урогенитальный трихомониаз (УТ) — широко распространенное инфекционное заболевание мочеполовой сферы. По данным ВОЗ, трихомониазом поражено около 10% населения. В отдельных социальных группах заболеваемость достигает 40%. ВОЗ ежегодно в мире регистрирует более 333 млн новых случаев инфекций, передающихся половым путем (ИППП), из них на мочеполовой трихомониаз приходится 170 млн случаев (Захаркив Ю. Ф., 2005; КираЕ. Ф. и др., 1996; Тихомиров А. Л. и др., 2003; Cates W., 1999).
В России на долю больных трихомонадными кольпитами приходится от 20 до 40% всех обращений в гинекологическую клинику и до 60% обращений в КВД. Лица, страдающие скрытыми и латентными формами инфекций, играют главную роль в ее распространении. В связи с этим лечению мочеполового трихомониаза подлежат партнеры выявленного больного даже в том случае, когда клинические проявления заболевания отсутствуют. В Российской Федерации ежегодно регистрируется более 2 млн больных ИППП, причем ведущее место в структуре воспалительных заболеваний урогенитального тракта (УГТ) занимает мочеполовой трихомониаз, в частности до 34,8% среди так называемых негонококковых уретритов (Захаркив Ю. Ф. и др., 2005).
Заболеваемость мочеполовым трихомониазом в различных регионах России существенно различается и составляет от 261 до 343 (и выше) на 100 000 населения (Адаскевич В. П., 1998; Скрипкин Ю. К. и др., 2001; Тихомиров А. Л. и др., 2003). Так, в Великом Новгороде заболеваемость УТ в 2000 г. составила 579,6 на 100 000 населения, в Иркутской области — 473,3, в Санкт-Петербурге — 263,6 на 100 000 населения. Причем заболеваемость УТ в Санкт-Петербурге снижается в последние годы (табл. 1).
Таблица 1. Заболеваемость некоторыми ИППП в Санкт-Петербурге за 1994-2004 гг. (Смирнова Т. С. и др., 2005)*
| Годы | Хламидиоз | Трихомониаз | Урогенитальный герпес | Уреаплазмоз | ||||
| Число больных | Показатель (на 100 000) | Число больных | Показатель (на 100 000) | Число больных | Показатель (на 100 000) | Число больных | Показатель (на 100 000) | |
| 1994 | 7807 | 158,8 | 24111 | 490,3 | 1251 | 25,4 | 7947 | 161,6 |
| 1995 | 13435 | 277,7 | 24050 | 497,0 | 998 | 20,6 | 12108 | 250,2 |
| 1996 | 13375 | 278,4 | 21081 | 438,9 | 1054 | 21,9 | 12066 | 251,2 |
| 1997 | 11702 | 244,9 | 18263 | 382,2 | 1408 | 29,5 | 11967 | 250,4 |
| 1998 | 11738 | 247,2 | 15414 | 324,6 | 1907 | 40,2 | 15290 | 322,0 |
| 1999 | 12242 | 258,9 | 14520 | 307,1 | 2490 | 52,7 | 18485 | 390,9 |
| 2000 | 11736 | 250,0 | 12375 | 263,6 | 3071 | 65,4 | 21842 | 465,3 |
| 2001 | 9903 | 212,5 | 10226 | 219,4 | 3606 | 77,4 | 21773 | 467,1 |
| 2002 | 8958 | 193,6 | 8856 | 191,4 | 3305 | 71,4 | 22188 | 479,5 |
| 2003 | 8399 | 184,0 | 7681 | 168,3 | 2825 | 61,9 | 24068 | 527,3 |
| 2004 | 8695 | 188,0 | 6943 | 128,5 | 2851 | 61,7 | 24424 | 528,2 |
*— СПб ГорКВД. Следует отметить, что низкие показатели заболеваемости гени-тальным герпесом (ГГ) обусловлены, очевидно, необязательностью регистрации ГГ и недостаточной лабораторной диагностикой.
Мочеполовой трихомониаз имеет большое медицинское и социально-экономическое значение в связи с высокой инфицированностью людей, клиническим полиморфизмом, нередко хроническим течением с рецидивами, поражением различных органов и систем. Трихомониазом страдают люди активного в половом отношении возраста — от 20 до 59 лет, редко дети. У женщин наиболее часто встречаются трихомонадные эндоцервициты (81%), вульвовагиниты (62%), реже — уретриты (18%), воспаления ампулы прямой кишки (Межевитинова Е. А. с соавт., 1999; Тихомиров А. Л. с соавт., 2003). Изолированное поражение того или иного участка мочеполовой системы наблюдается крайне редко. Мочеполовой трихомониаз у женщин часто проявляется в форме паразитоносительства или протекает в хронической форме (Thomason J. L., Gelbert S. M., 1989; При ленская В. Н., 2000; Тихомиров А. Л., Олейник Ч. Г., 2003, и др.).
При инфицированнии трихомонадами беременных наблюдается предрасположенность к повреждениям плаценты (Minkoff H. и др., 1984; Wilson Т. Е. и др., 1996), преждевременным родам и невынашиванию плода (CotchM. E, 1990). Трихомонадная инвазия может служить причиной развития опухолей шейки матки (Kharsany А. В. et al., 1993; Zhang Z. E et al., 1994), различных воспалительных заболеваний органов малого таза (ВЗОМТ) и бесплодия. Наряду с другими ИППП мочеполовой трихомониаз увеличивает риск инфицирования ВИЧ (Laga М. et al., 1993, 1994), так как в очаге воспаления наблюдается скопление ВИЧ-чувствительных Т-лимфоцитов (Laga M. et al., 1993; Swygard H. et al., 2004).
Среди девочек и подростков, страдающих неспецифическими вульвовагинитами, у 55,8% обнаружена хламидийная УГИ, у 10,2% — уреаплазменная, у 7,3% — гонококковая, у 5,8% — гарднереллезная и у 20,6% — трихомонадная инфекция. В 54,4% среди них обнаружена смешанная инфекция, а у 53,5% диагностированы ВЗОМТ (Chaika V. К. at al., 1995). В. В. Дубенский, В. П. Кузнецов (1996) выявляли урогенитальный хламидиоз у 62,1%, гонококковую инфекцию — у 24,3%, уреаплазменную — у 16,2%, герпетическую — у 16%, трихомонадную — у 14,8% обследованных больных.
Заболевание передается половым путем, при внебрачных половых связях инфицируется 67-71% выявленных больных трихомониазом (Клименко Б. В. и др., 2001). Очень редко регистрируются случаи заражения при бытовых контактах: через перчатки, подкладные клеенки и судна, ночные горшки, сиденья унитаза и пр.
В эпидемическом процессе имеют значение малосимптомные, вялые формы болезни, а также трихомонадоносительство. При этом признаки воспаления отсутствуют, а возбудитель выявляется при рецидивах воспалительных заболеваний у одного из половых партнеров. Трихомонадоносительство — это не простое транзиторное носительство простейших, а активный системный инфекционный процесс с реакцией микроорганизма на патогенный фактор. Частота носительства Т. vaginalis среди обследованных женщин составляет 10-35%, а среди мужчин 2-41% (Клименко Б. В. и др., 2001; Рыбников В. И., 1964). Иммунный ответ на инфицирование Т. vaginalis у трихомонадоносителей развивается недостаточно вследствие антигенного родства трихомонад с некоторыми тканями человека, отмечено повышение концентрации секреторного IgA в слизи влагалища и канала шейки матки. Трихомонадоносительство способствует эпидемиологическому распространению возбудителя среди половых партнеров.
Большое значение в клинике и эпидемиологии урогенитальных заболеваний, и особенно мочеполового трихомониаза, придается формированию микробиоценозов половых путей (Клименко Б. В., 2000; Копылов В. М. и др., 2001). Вместе с тем, вопросы о частоте выявления различных микроорганизмов в ассоциации с Т. vaginalis и механизмах их патогенного влияния в литературе освещены недостаточно. Считают, что сочетание возбудителей урогенитальных инфекций (УГИ) имеет неслучайный характер и определяется комплексом причин экзогенной и эндогенной природы, имеет значение среда организма хозяина (Дерябин Д. Г., Борисов С. Д., 1998). Основными патогенами, вызывающими УГИ, являются Т. vaginalis и С. trachomatis (Машкилейсон А. Д., ГомбергМ. А., 1994). При обследовании в 1991 г. 2519 мужчин различные УГИ были выявлены у 79% больных, из них в 48% случаев — УТ, в 42% — урогенитальный хламидиоз, в 22% — смешанная трихомонадно-хламидийная инфекция. Диагностированные УГИ у 38,6% больных характеризовались торпидным хроническим течением и устойчивостью к используемым химиопрепаратам (Чуприн А. Е., Якубович А. И., 2003). Рецидивирующее течение УГИ у мужчин способствует вовлечению в патологический процесс предстательной железы, семенных пузырьков, придатков яичек и пр.
На развитие хронических воспалительных процессов УГТ существенно влияет качественный и количественный состав микрофлоры. Показано, что отсутствие нормальной микрофлоры и высокие концентрации условно-патогенных микроорганизмов, превышающие в уретре значения 104 КОЕ/мл, способствуют более частому развитию воспаления УГТ (Сагалов А. В., 1999). Так, при изучении состава микрофлоры уретры 71 пациента с УТ у 35% больных простатитом трихомонады сочетались с хламидиями, у 17% — выявлены только трихомонады. В 16% случаев уретритов выявлена смешанная трихомонадно-хламидийная инфекция, в 35% — трихомонадная моноинфекция (Чуприн А. Е., Якубович А. И., 2003). Исследование сопутствующей микрофлоры выявило наличие условно-патогенных микроорганизмов: у 66% — Staph, epidermidis, у 40% — Е. faecalis, a E. coli и Staph, aureus — у 8% больных, причем концентрация выделенных микроорганизмов превышала 104 КОЕ/мл, что указывает на возможное участие микрофлоры в поддержании воспаления в уретре (Чуприн А. Е., Якубович А. И., 2003).
Бактериальный вагиноз встречается у 20% женщин детородного возраста. Бактериальный вагиноз — это заболевание, которое возникает в результате резкого дисбаланса вагинальной микрофлоры и вызванное замещением нормальной микрофлоры влагалища, в которой преобладают лактобактерии, анаэробными микроорганизмами, Gardnerella vaqinalis и Mycoplasma hominis. Помимо гарднерелл в вагинальном секрете женщин с бактериальным вагинозом обнаружены в большом количестве анаэробные бактерии: бактероиды, пептококки, пептострептококки.
Особую остроту приобретает также проблема лекарственно-устойчивых штаммов Т. vaginalis, их клиническое и эпидемиологическое значение (Таги Meri et al, 2000; Swygard H. et al, 2004). Однако исследования по этой проблеме пока еще немногочисленны, а полученные результаты противоречивы. Прогресс в ее изучении сдерживается также отсутствием доступных для широкой практики методов определения чувствительности Т. vaginalis к антипротозойным препаратам.
Что такое трихомониаз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Агапова Сергея Анатольевича, венеролога со стажем в 39 лет.
Над статьей доктора Агапова Сергея Анатольевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Урогенитальный трихомониаз — это передающаяся половым путём инфекция мочеполовой системы, вызванная влагалищной трихомонадой (Trichomonas vaginalis).
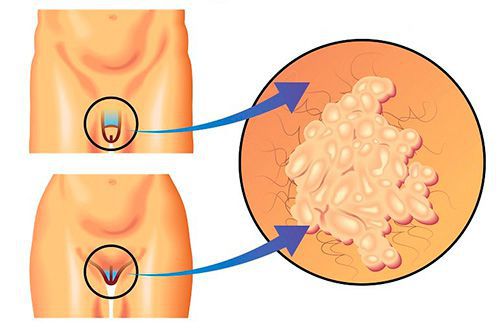
Насколько распространён трихомониаз
Что такое трихомониаз, трихомонады и их виды
Причиной заболевания является инфицирование мочеполовых органов влагалищной трихомонадой — одноклеточным жгутиковым простейшим организмом изменчивой формы, который в естественных условиях может существовать и размножаться только в организме человека. Помимо вагинальной трихомонады у человека могут паразитировать ещё два вида — кишечная трихомонада (Pentatrichomonas hominis) и ротовая (Trichomonas tenax), однако их роль в возникновении заболеваний мочеполовой системы не установлена.
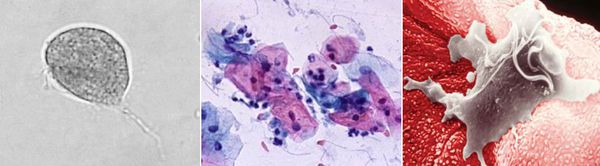
Трихомонада, так как не образует цист и других устойчивых форм, быстро погибает во внешней среде вследствие высыхания, легко разрушается при кипячении, воздействии антисептиков и этилового спирта. Однако может сохранять некоторое время жизнеспособность во влажной среде. Исследованиями установлено, что трихомонады могут выживать до 45 минут на сидениях унитазов, нижнем белье и в воде ванны. [3]
Как можно заразиться трихомониазом
Пути передачи инфекции:
Факторами риска являются:
- случайные половые связи;
- половой контакт, незащищённый барьерной контрацепцией (презервативом);
- злоупотребление алкоголем и наркомания; [7]
- атрофия шейки матки — вследствие снижения защитных свойств из-за уменьшения эстрогенов в тканях; [8]
- наличие других половых инфекций, таких как ВИЧ-инфекция, бактериальный вагиноз, вульвовагинальный кандидоз, генитальный герпес, хламидиоз. [9]
Защищает ли презерватив от трихомониаза
Использование презервативов снижает вероятность заражения. Однако микроорганизмы могут попасть на области, не закрытые ими, поэтому презервативы не могут полностью защитить от трихомониаза [52] .
Передаётся ли трихомониаз во время орального секса
Микроорганизмы способны поражать различные части тела, например, руки или рот. Оральный секс с инфицированным партнёром может привести к заражению трихомониазом ротовой полости [52] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы трихомониаза
Чаще трихомониаз диагностируется у женщин, чем у мужчин. У 10-30 % женщин и у 45-50 % мужчин отмечается асимптомное течение заболевания . [10]
Симптомы трихомониаза у женщин
У женщин трихомонады преимущественно поражают влагалище, откуда они могут проникать в уретру, бартолиновы железы, мочевой пузырь и канал шейки матки. В редких случаях трихомонады паразитируют в полости матки, маточных трубах, почечных лоханках и прямой кишке. [11]
Основными симптомами трихомониаза у женщин являются:
Редкими проявлениями трихомониаза у женщин являются:
- макулярный кольпит (клубничный цервикс) — кровоизлияния в слизистую влагалища и шейку матки, напоминающее ягоду клубники; [12]
- эрозивно-язвенные поражения вульвы и преддверия влагалища. [13]
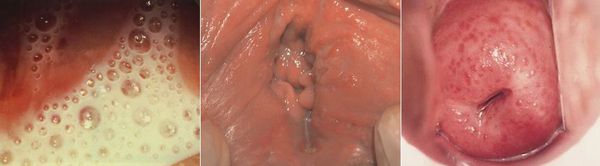
Симптомы трихомониаза у мужчин
У мужчин трихомонады поражают слизистую оболочку мочеиспускательного канала, нередко проникая в уретральные железы и лакуны. Ввиду неблагоприятных условий для существования в мужской уретре трихомонад, заболевание часто носит транзиторный (временный) характер. Этим же объясняется и большой процент асимптомных форм трихомониаза у мужчин. [14]
Основными симптомами трихомониаза у мужчин являются:
Редким проявлением трихомониаза у мужчин является баланопостит (воспаление головки и крайней плоти полового члена). Описаны его эрозивно-язвенные формы. [15]
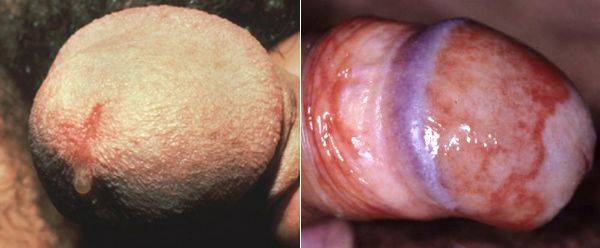
Патогенез трихомониаза
Проникая в урогенитальный тракт человека, трихомонады прикрепляются к эпителиальным клеткам, что приводит к повреждению и воспалительной реакции клеток эпителия. В этой реакции важное значение имеет адгезин — белок, продуцируемый паразитом. [16]
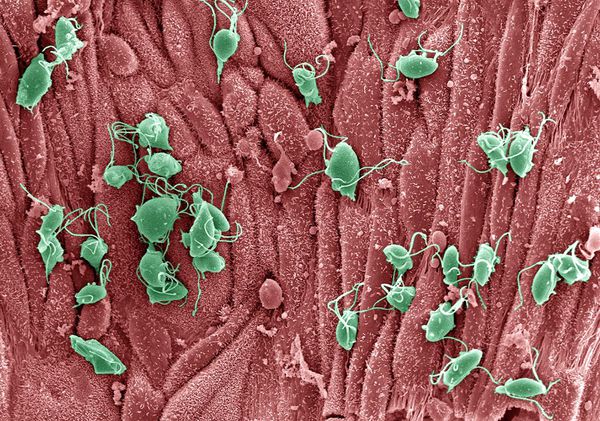
Трихомонады выделяют многочисленные протеолитические ферменты, которые участвуют в цитотоксичности, гемолизе (разрушении эритроцитов и выделении гемоглобина) и уклонении от иммунных реакций. Ферменты находятся во влагалищных выделениях инфицированных женщин вместе с антителами, которые их распознают. Важную роль играет фермент муциназа, который значительно облегчает проникновение трихомонад в слизистые оболочки. [17]
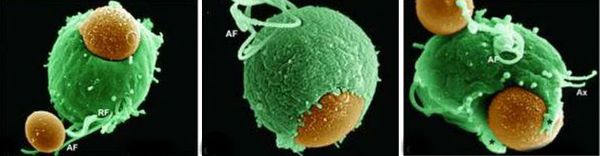
Трихомонадная инфекция вызывает клеточный, гуморальный и секреторный иммунные ответы. Однако эти реакции не способны защитить пациентов от реинфекции, поэтому повторное инфицирование встречается часто. Антитела и компоненты комплемента, присутствующие в сыворотке крови и секрете половых желез у некоторых больных, могут воздействовать на паразита путём стимуляции нейтрофилов, которые способствуют уничтожению трихомонад через классическую систему комплемента. Также антитела могут блокировать адгезию (прилипание) паразита к поверхности слизистой оболочки. [21]
Классификация и стадии развития трихомониаза
По Международной классификации болезней 10-го пересмотра трихомониаз разделяют на:
A59.0 Урогенитальный трихомониаз;
- Бели (вагинальные выделения), вызванные Trichomonas vaginalis; (N51.0), вызванный Trichomonas vaginalis;
A59.8 Трихомониаз других локализаций;
A59.9 Трихомониаз неуточнённый.
Стадии заболевания
После скрытого (инкубационного) периода, продолжающегося от 4 до 28 дней с момента заражения, приблизительно у 40-50% мужчин появляются признаки уретрита в виде слизистых выделений из уретры, а у 70-90% женщин — признаки вульвовагинита, характеризующегося зудом, жжением и наличием обильных мутных выделений из влагалища. [10] В остальных случаях болезнь протекает первоначально бессимптомно. В дальнейшем, если вовремя не получено лечение, развитие заболевания происходит по следующим сценариям:
- Длительное бессимптомное носительство, при котором нет никаких субъективных и объективных симптомов.
- Длительное рецидивирующее течение, при котором симптомы заболевания могут временно возобновляться и самопроизвольно исчезать.
- Ранее развитие осложнений может возникать как при течении заболевания с клиническими симптомами, так и при бессимптомном течении.
- Позднее развитие осложнений возникает при длительно текущем бессимптомном или хроническом рецидивирующем процессе.
Осложнения трихомониаза
В отличии от других половых инфекций – хламидийной и гонококковой — осложнения при трихомониазе встречаются гораздо реже.
Осложнения у мужчин
Эпидидимит — воспаление придатка яичка, очень редкое осложнение трихомонадной инфекции. Чаще всего это хронический процесс, хотя встречаются описания острых форм. [22]
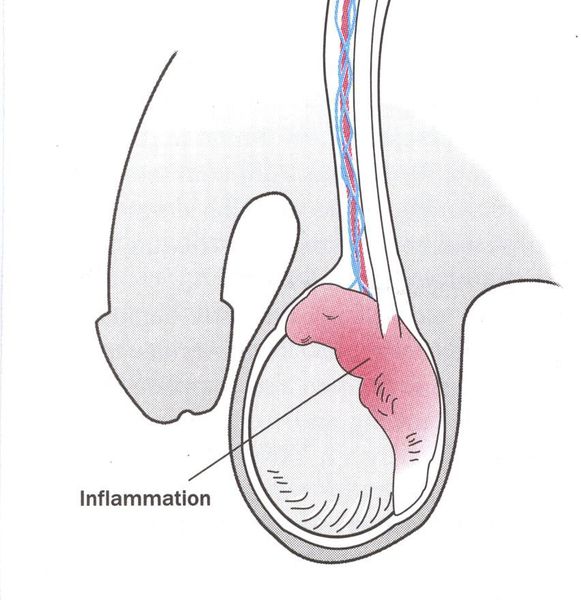
Редким осложнением трихомониаза является простатит. Сообщается о нескольких случаях хронического простатита, вызванного трихомонадной инфекцией. [23]
Нарушение фертильности. Проведенные исследования показывают негативное воздействие трихомонад на сперматозоиды мужчин в виде снижения их подвижности. [24]
Сообщается также о случае трихомонадного двухстороннего конъюнктивита. [31]
Осложнения у женщин
Воспалительные заболевания малого таза, вызванные вагинальной трихомонадной инфекцией, являющиеся причиной трубного бесплодия и синдрома хронической абдоминальной боли, описаны, в основном, у ВИЧ-позитивных женщин. [25]
Проведённые исследования указывают на повышенный риск преждевременных родов, рождения ребёнка с низким весом у инфицированных влагалищной трихомонадой женщин. [26]
Также трихомонадная инфекция в 2-3 раза увеличивает риск заражения ВИЧ. [32]
Очень редким осложнением трихомониаза является цистит. В медицинской литературе описано всего несколько случаев. [33]
Прочие осложнения
Сообщалось о паранефральном абсцессе [27] , абсцессе головного мозга [28] у новорождённого, абсцессе срединного шва полового члена [29] у мужчины, вызванных вагинальной трихомонадой.
Описаны случаи неонатальной трихомонадной пневмонии у новорождённых, успешно вылеченных метронидазолом. [30]
Диагностика трихомониаза
Для диагностики трихомониаза применяются микроскопические, цитологические, бактериологические, молекулярные лабораторные тесты и инструментальные методы обследования.
Показаниями для диагностики трихомониаза являются [2] :
- наличие признаков воспалительного процесса мочеполовых органов;
- беременность (при постановке на учёт по поводу беременности, при сроке беременности 27-30 недель и 36-40 недель, при поступлении на роды без документов о результатах обследования на половые инфекции);
- предстоящие оперативные вмешательства на половых органах и органах малого таза;
- бесплодие и выкидыши в анамнезе;
- половые контакты с больными половыми инфекциями;
- сексуальное насилие.
Микроскопическое исследование
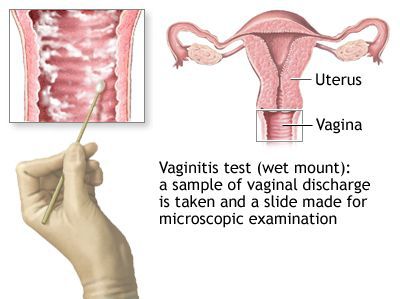
Микроскопия окрашенного препарата (окраска по Романовскому, Папаниколау) не рекомендуется из-за субъективизма при интерпретации результатов исследования. [2]
Культуральное исследование
Молекулярно-биологические методы
Материалом для исследования методом ПЦР при диагностике трихомониаза являются:
- у женщин: выделения из уретры, канала шейки матки, влагалища, первая порция мочи);
- у мужчин: выделения или соскоб из уретры, первая порция мочи, секрет предстательной железы, в редких случаях — сперма. [2]
Требования для получения достоверных результатов исследования:
- Забор материала должен осуществляться не ранее чем через месяц после полученного лечения.
- При отсутствии или скудных выделениях из уретры забор материала должен проводиться через 2-3 часа после последнего мочеиспускания, а при наличии обильных выделений — через 10-15 минут после мочеиспускания.
- Во время менструации забор материала для исследования проводить запрещается.
- Должны быть соблюдены сроки и условия доставки образцов в лабораторию.
Серологическое исследование
Метод иммуноферментного анализа (ИФА) для обнаружения антител классов IgA, IgM и IgG к антигенам T. vaginalis применять не допустимо. [2]
Применение биологических (парентеральное введение пирогенала, гоновакцины), химических (внутриуретральное введение растворов серебра) и алиментарных провокаций (приём алкоголя и острой пищи) с целью повышения выявляемости трихомонад при проведении лабораторных тестов нецелесообразно, так как эффективность этого метода не доказана. [2]
Лечение трихомониаза
Многочисленными исследованиями и клиническими испытаниями было установлено, что наиболее эффективными препаратами для лечения трихомониаза являются препараты группы 5-нитроимидазолов, а среди них — метронидазол, тинидазол и орнидазол.
Современными отечественными и зарубежными руководствами предложены следующие схемы лечения этими препаратами.
Метронидазол (Трихопол, Метрогил, Флагил) — эффективность его применения составляет 90-95%.
Для неосложнённых форм заболевания: 500 мг перорально 2 раза в сутки в течение 7 дней [36] или 2,0 г перорально однократно. [37]
Для осложнённых форм: 500 мг перорально 3 раза в сутки в течение 7 дней или 2,0 г внутрь 1 раз в сутки в течение 5 дней. [38]
Для беременных: 2,0 г однократно (лечение проводится не ранее II триместра беременности). [39]
Для детей: 10 мг на кг массы тела перорально 3 раза в сутки в течение 5 дней. [40]
Тинидазол (Фазижин, Тиниба) — эффективность применения составляет 86-100%.
Для неосложнённых форм заболевания: 500 мг перорально 2 раза в сутки в течение 5 дней или 2,0 г перорально однократно. [35]
Для осложнённых форм: 2,0 г перорально 1 раз в сутки в течение 3 дней. [37]
Орнидазол (Тиберал, Гайро, Дазолик) — эффективность применения составляет 90-100%.
Для неосложнённых форм заболевания: 500 мг перорально 2 раза в сутки в течение 5 дней [41] или 1,5 г перорально однократно. [42]
Для осложнённых форм: 500 мг перорально 2 раза в сутки в течение 10 дней. [38]
Для детей: 25 мг на кг массы тела перорально 1 раз в сутки в течение 5 дней. [39]
Другие препараты из группы 5-нитроимидазолов — менее распространены и изучены, чем вышеизложенные препараты, однако применяются в клинической практике:
- Тенонитрозол (Атрикан) — 250 мг перорально 2 раза в день в течение 4 дней; [43]
- Ниморазол (Наксоджин) — схемы применения при неосложнённом трихомониазе: 2,0 г перорально однократно или 1,0 г перорально через каждые 12 часов – три приёма, или 250 мг перорально 2 раза в день в течение 6 дней. [44]
- Секнидазол (Тагера) — 2,0 г перорально однократно (эффективность 97%). [45]
Причины неудач в лечении
В 5 % случаев трихомонады устойчивы (резистентны) к перечисленным препаратам [46] . Центры по контролю за заболеваемостью (США) в таких случаях рекомендуют увеличить дозировку и длительность применения медикаментов [47] : Метронидазол — 2,0 г перорально однократно в сутки в течении 7 дней или Тинидазол 2,0 г перорально однократно в сутки в течении 7 дней.
Дисульфирам-подобная реакция на препараты
Нитроимидазолы блокируют и снижают выработку фермента алкоголь-дегидрогеназы, что приводит к повышению уровня и накапливанию токсического ацетальдегида в крови. При приёме алкоголя в любых концентрациях во время лечения препаратами, входящими в группу нитроимидазолов, через 10-20 минут возникает реакция в виде тошноты, рвоты, головной боли, затруднения дыхания, судорог. Длительность её составляет несколько часов. Реакция наблюдается при приёме метронидазола, тинидазола [48] и орнидазола [49] .
Помимо исключения алкоголя, рекомендаций по изменению привычек или особенностям питания при лечении трихомониаза нет.
Установление излеченности трихомонадной инфекции
Проводится через две недели после окончания лечения микроскопией и культуральным посевом и через 4 недели методом ПЦР. При отрицательных результатах лабораторных тестов пациенты дальнейшему наблюдению не подлежат. [2]
Можно ли заниматься сексом при трихомониазе
Заниматься сексом можно через 7-10 дней после завершения лечения трихомониаза. Примерно каждый пятый выздоровевший заражается вновь в течение трёх месяцев после окончания лечения. Чтобы избежать повторного заражения, лечение должны пройти все сексуальные партнеры. Если симптомы возникли снова, нужно пройти повторное обследование [52] .
Прогноз. Профилактика
Прогноз при раннем выявлении и вовремя начатом лечении благоприятный. При неосложнённых формах трихомонадной инфекции после однократного курса выздоровление составляет 95-100%. Лица с осложнёнными формами и метронидазол-устойчивыми формами заболевания после проведённого лечения должны находиться под динамическим наблюдением.
Половые партнёры больных трихомониазом должны быть пролечены независимо от результатов их обследования на наличие трихомонад.
Самой эффективной мерой профилактики является использование презервативов при случайных половых контактах.
Ввиду бессимптомного течения инфекции лицам, имеющим несколько половых партнёров в год или случайные половые связи, рекомендовано ежегодное обследование на наличие трихомонад.
В настоящее время вакцины, предотвращающей заражение трихомониазом, не создано. В 80-е годы прошлого века была создана коммерческая вакцина Солкотриховак, состоящая из лиофилизата Lactobacillus acidophilus, которая по утверждению фирмы-производителя оказывает положительный эффект при рецидивирующем трихомониазе и бактериальном вагинозе. [50] Однако последующими исследованиями предположение о том, что защитный механизм действия вакцины связан на антигенном сходстве применяемых штаммов лактобацилл и вагинальной трихомонады, было отвергнуто. [51]
Для цитирования: Баткаев Э.А., Рюмин Д.В. Эффективность использования вакцины "СолкоТриховак" в лечении урогенитального трихомониаза у женщин и мужчин (клинико-лабораторное исследование). РМЖ. 2002;2:68.
У рогенитальный трихомониаз (УГТ) – заболевание урогенитального тракта человека, вызванное простейшим одноклеточным паразитом Trichomonas vaginalis. УГТ лидирует по частоте выявления среди инфекций, передаваемых половым путем (ИППП) у лиц, обратившихся за специализированной дерматовенерологической, акушерско–гинекологической и урологической помощью по поводу инфекционно–воспалительных заболеваний урогенитального тракта, представляя собой серьезную угрозу репродуктивному здоровью человека. Необходимо указать на возрастание частоты регистрации случаев торпидного течения заболевания и минимальных клинических проявлений у пациентов с УГТ, что особенно характерно для мужчин и способствует неуклонному росту инфекции в человеческой популяции.
Сложность и неоднозначность патогенеза трихомонадной инфекции обусловлены, наряду с состоянием клеточного и гуморального иммунитета, интеграционными и конкурентными взаимоотношениями патогенных микроорганизмов и симбионтов, формирующих индивидуальный микробиоценоз мочеполовых путей у больных с УГТ. Необходимо подчеркнуть, что способность влагалищных трихомонад осуществлять незавершенный фагоцитоз различных инфекционных агентов и служить резервуаром для многих патогенных бактерий и вирусов [3,13,15,19] объясняет как многоочаговость поражения при данном заболевании, так и проблемы, связанные с его лечением.
Необходимо подчеркнуть, что состояние эйфории по поводу ошеломляющей вначале эффективности метронидазола, синтезированного в 1959 г., а также его структурных аналогов при лечении УГТ у клиницистов длилось достаточно долго. Многими специалистами были незаслуженно забыты лучшие и приоритетные традиции Российской школы малой урологии, врачи практического звена здравоохранения все реже стали использовать в своей повседневной работе местные санирующие процедуры (инстилляции, бужирование, массажи уретры на буже и др.), крайне редко при контроле за излеченностью больных с урогенитальными инфекциями в последние годы используется уретроскопия.
По мнению большинства исследователей [3,4,11,12,20] применяемые сегодня методы этиотропной терапии УГТ недостаточно эффективны. Отчасти, данный факт объясняется увеличением в человеческой популяции штаммов влагалищных трихомонад, резистентных к действию метронидазола и его производных [1,4–6,18]. Интересно, что в течение последних 10–15 лет среди пациентов с УГТ увеличилась и частота выявления амастиготных форм влагалищных трихомонад – метаболически малоактивных особей паразита, лишенных органоидов движения (блефаропласта, жгутиков и ундулирующей мембраны), что значительно затрудняет диагностику инфекции и при отсутствии соответствующей терапии способствует формированию трихомонадоносительства у таких больных.
Следует также отметить наличие у влагалищных трихомонад хорошо выстроенной системы защиты против организма хозяина. Например, жгутики препятствуют контакту простейшего с клеткой–фагоцитом, а комплекс ферментов, выделяемых трихомонадами в окружающую среду (гиалуронидаза, нейраминидаза, клеточный разъединяющий фактор и др.) в зависимости от обстоятельств может использоваться паразитами как средства агрессии по отношению к клеткам и тканям человеческого организма, так и служить целям собственной защиты. Устойчивость Trichomonas vaginalis к комплементу зависит от высокой концентрации железа, в избытке присутствующего в менструальной крови. Вероятно, ионы железа регулирует экспрессию у трихомонад протеазных белков, которые могут разрушать С3–компонент комплемента на поверхности микроорганизма, что позволяет простейшим избегать комплемент–зависимого лизиса.
Кроме того, нужно добавить, что в течение последних 10–15 лет существенно изменилась и иммунореактивность самого организма человека. В экспериментальных исследованиях по проблемам общей патологии человеческого организма на рубеже II и III тысячелетий показано снижение частоты выявления в различных органах и тканях воспалительных, пролиферативно–клеточных и увеличение дегенеративно–клеточных (дистрофически–атрофических) процессов [10]. Поражение клеток имеет фенотип дистрофии, основа которой не альтерация цитопламатических органелл, а их недопроизводство; в финале возникает не некроз (парциальный или тотальный), а наблюдается атрофия клеток и их безнекротическая элиминация либо десквамация. При этом воспалительно–клеточная инфильтрация отсутствует или неадекватна имеющимся структурным изменениям, вследствие чего происходит развитие диффузного склероза стромы, обусловливающее неэффективность традиционной терапии [14].
Непосредственные сочлены – ассоцианты единого с Trichomonas vaginalis микробиоценоза тоже способны оказывать сопротивление факторам защиты хозяина, а весь комплекс межмикробных взаимоотношений, сформировавшихся в биотопе мочеполовых путей у больных УГТ следует рассматривать с точки зрения смешанной урогенитальной инфекции, что, в свою очередь, требует изменения тактики лечения таких больных.
Таким образом, проблемы терапии УГТ требуют, с одной стороны, модернизации уже существующих схем и методов лечения заболевания, а с другой – диктуют необходимость поиска альтернатив существующим способам санации инфекции.
Одним из принципиально отличных от традиционно применяемых в терапии УГТ способов его лечения является иммунотерапия, которая, как правило, проводится параллельно основному курсу приема протистоцидных препаратов и служит своего рода позитивным фоном, увеличивающим эффективность санирующих средств. В течение длительного периода времени наряду с применением различных иммуномодуляторов (метилурацил, ликопид, миелопид, циклоферон и др.) и неспецифической вакцинации (пирогенал, продигиозан) предпринимались неоднократные попытки создания вакцины, специфического антитрихомонадного действия, которые, однако, не увенчались успехом.
Лечение УГТ путем иммунизации имеет явные преимущества перед системным применением антимикробных препаратов в силу индукции прежде всего факторов местного иммунитета и опосредованного воздействия на возбудителя заболевания, так как позволяет исключить, либо в значительной степени снизить их дозу, а также уменьшить вероятность возникновения побочных эффектов, что касается, в первую очередь, дисбиоза влагалища [12].
Течение заболевания у 59% пациенток было осложнено различными воспалительными (цистит, кольпит, эндоцервицит, метроэндометрит, сальпингоофорит, эрозия шейки матки) и/или пролиферативными (эндометриоз, аденомиоз, кистома яичников) заболеваниями урогенитального тракта, что свидетельствовало о многоочаговости поражения у таких больных. В разработку не включались женщины с УГТ моложе 19 и старше 45 лет, пациентки с тяжелой соматической патологией.
Учитывая особенности патогенеза, течения и лечения смешанной урогенитальной инфекции, в выборку также не включались женщины и мужчины, при обследовании которых одновременно с влагалищными трихомонадами определялись миксты из нескольких патогенных микроорганизмов (Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum, Herpes sympl. virus, Cytomegalovirus, Neisseria gonorrhoeae, Mycoplasma genitalium).
При диагностике УГТ, скрининге ИППП, определении воспалительных заболеваний органов малого таза и последующих контролях за излеченностью инфекции использовались следующие методы:
- гинекологическое исследование;
- бактериоскопия: нативный мазок; соскобы из мочеполовых путей (уретра, вагина, цервикс) с окраской по Граму, Романовскому–Гимзе, Лейшману;
- полимеразная цепная реакция (ПЦР);
- бактериологическое исследование;
- рН–метрия отделяемого из вагины;
- аминотест;
- УЗИ органов малого таза.
- бактериоскопия: нативный мазок; исследование соскобов из уретры и секрета предстательной железы с окраской по Граму, Романовскому – Гимзе, Лейшману;
- ПЦР;
- бактериологическое исследование;
- УЗИ предстательной железы;
- трансректальное (пальпаторное) исследование простаты.
4–я группа (контроль – 50 чел.): лечились только метронидазолом (внутрь и интравагинально).
В зависимости от схемы лечения УГТ все мужчины (46 человек) были разделены на 3 группы:
3–я группа (контроль – 20 чел.): лечились только метронидазолом внутрь по вышеуказанной схеме.
Излеченность всех больных от УГТ устанавливали через 2 недели от момента окончания лечения.
Результаты изучения эффективности лечения УГТ у женщин и мужчин по вышеуказанным схемам отражены в таблицах 1 и 2 и представлены на рисунках 1 и 2 (соответственно).
Рис. 1. Эффективность терапии мочеполового трихомониаза
Рис. 2. Сравнительная эффективность лечения вакциной "СолкоТриховак" урогенитального трихомониаза у мужчин
Литература:
1. Амозов М.Л., Коссобудская Д.С. Тиберал в терапии свежего (острого) урогенитального трихомониаза // Заболевания, передаваемые половым путем. – 1996. – №4. – с. 79–80.
2. Анчупане И.С. Урогенитальный трихомониаз и смешанные трихомонадно–гонококко–хламидийные инфекции: Автореф. дис. канд. мед. наук., М.,1992. – 17 С.
3. Васильев М.М. Особенности клиники мочеполового трихомониаза, совершенствование диагностики и лечения (клинико–экспериментальное исследование): Автореф. дис. докт. мед. наук., М., 1990. – 28 С.
4. Васильев М.М., Рассейкина Е.Ю. Лечение больных урогенитальным трихомониазом // Проблемы репродукции. – 1996. – № 4. – с. 42–43.
5. Гултон Дж., Сквирз А. Trichomonas vaginalis, резистентный к метронидазолу // Lancet i.: 42 (1982).
6. Дмитриев Г.А., Брагина Е.Е., Кисина В.И. и соавт. Морфофункциональные особенности устойчивого к метронидазолу штамма Trichomonas vaginalis // Вестн. дерматол. – 1994. – № 4. – с. 12–15.
7. Земцов М.А. Современный метод лечения мочеполового трихомониаза и трихомонадно–хламидийной инфекции у женщин: Автореф. дис. канд. мед. наук., М., 1995. – 15 С.
8. Земцов М.А., Чеботарев В.В. Вакцина СолкоТриховак в комплексном лечении больных трихомониазом женщин // Вестн. дерматол. – 1996. – № 6. – с. 11–13.
9. Ильин И.И. / Негонококковые уретриты у мужчин. – М., 1991. – 228 С.
10. Казначеев В.П., Непомнящих Г.И. Мысли о проблемах общей патологии на рубеже ХХI века. – Новосибирск: НИИ общей патологии и экологии человека НЦ КЭМ СО РАМН; НИИ региональной патологии и патоморфологии НЦ КЭМ СО РАМН, 2000. – 47 с.
11. Кира Е.Ф. Применение орнидазола (тиберала) для лечения бактериального вагиноза и трихомониаза // Проблемы репродукции. – 1997. – № 3. – с. 26–28.
12. Кира Е.Ф. Иммунотерапия бактериального вагиноза и трихомониаза // Журнал акушерства и женских болезней. – 1997. – № 1. – с. 38–43.
13. Копылов В.М., Бокарев Е.Г., Говорун В.М. и соавт. Урогенитальный трихомониаз: актуальные вопросы диагностики и лечения (пособие для врачей). – М., 2001. – 40 с.
14. Непомнящих Г.И. Пограничные ткани (слизистые оболочки и кожа) в морфогенезе общепатологических процессов. – Актовая речь. – Новосибирск: Научно–исследовательский институт региональной патологии и патоморфологии СО РАМН, 1996. – 39 с.
16. Рюттгерс Х., Лоренц У. Клинический опыт использования СолкоТриховака в лечении инфекций, вызванных трихомонадами у женщин // Акушерство и гинекология. – 42 (1982) 736–738.
17. Суворов А.П., Оркин В.Ф., Капланов В.Д. Способ лечения трихомониаза // Вестн. дерматол. – 1991. – № 5. – с. 13–16.
18. Тейлор–Робинсон Д., Стрит Т. Trichomonas vaginalis, резистентный к метронидазолу // Lancet 11.: 1107 (1981).
20. Яговдик Н.З., Хилькеви Н.Д. Ассоциированные уреаплазменная и трихомонадная инфекция у мужчин, больных гонореей // Вестн. Дерматол. – 1992. – № 11–12. – с. 47–51.
Для цитирования: Фадеев А.А., Ломоносов К.М. Выбор оптимального препарата для терапии трихомониаза. РМЖ. 2004;4:176.
ММА имени И.М. Сеченова
Попадая в мочеполовой тракт, в среднем через 3–7 дней, трихомонады вызывают развитие воспаления в виде острого, подострого или торпидного уретрита (уретропростатита) у мужчин и вульвовагинита и уретрита у женщин. Как правило, процесс изначально протекает в виде острой или подострой формы, затем через 2 месяца воспалительная реакция стихает и трихомониаз переходит в хроническую форму или трихомонадоносительство.
Клиническая картина мочеполового трихомониаза неспецифичная. Трихомонада способна поражать любые органы урогенитального тракта, процесс может также локализоваться на слизистой миндалин, конъюнктивы, прямой кишки. Следует отметить, что в виде моноинфекции трихомониаз встречается лишь у 10–30% пациентов [1], в 70–80% случаев урогенитальный трихомониаз ассоциируется с другими микроорганизмами, в том числе и инфекциями, передаваемыми половым путем [5]. Чаще всего регистрируются трихомонадно–гонорейная, трихомонадно–бактериальная (в ассоциации с энтерококками, гемолитическими стрептококками, эпидермальным стафиллококком), а также трихомонадно–микотическая инфекции. Важен тот факт, что при микст–инфекции трихомонада является резервуаром сопутствующей инфекции, поэтому вследствие внутритрихомонадной персистенции гонококки, хламидии и др. неуязвимы для антибиотиков, что приводит к рецидиву заболевания.
Клиническая картина урогенитального трихомониаза не отличается от любой другой инфекции, передаваемой половым путем.
Терапия урогенитальных инфекций всегда остается актуальной и обсуждаемой проблемой дерматовенерологии, акушерства и гинекологии, урологии. В отношении трихомониаза основным предметом для дискуссий является терапия микст–инфекций, а так же выбор оптимального противопротозойного препарата. Поскольку за счет незавершенного фагоцитоза трихомонада зачастую является основной причиной неудач в терапии ИППП, при ассоциированных инфекциях необходимо в первую очередь проводить пульс–терапию трихомониаза. Для этого существует большой арсенал быстродействующих и эффективных антипротозойных средств. Все рекомендуемые препараты относятся к группе нитроимидазола. Родоначальником (впрочем, не потерявшим свою значимость и по сей день) является метронидазол. По данным Всемирной Организации Здравоохранения (2001 г.), однократный прием 2,0 г этого препарата приводит к излечению у 88% женщин, а при совместном лечении половых партнеров положительный эффект достигается в 95% случаев. Такая же высокая эффективность и у тинидазола. Как правило, для излечения достаточно однократного применения 2,0 г внутрь. Наиболее современными и эффективными антипротозойными препаратами являются орнидазол и секнидазол: однократный прием 1,5 г или 2,0 г соответственно гарантирует элиминацию возбудителя практически у всех больных с неосложненным трихомониазом. Однократные пульс–курсы терапии также удобны для лечения половых партнеров. Однако частое отсутствие клиники или ее минимальные проявления, невысокий лейкоцитоз не позволяют достоверно определить сроки инфицирования, довольно проблемно исключить и поражение трихомонадами парауретральных желез, простаты и т.д. В связи с этим мы рекомендуем использовать вышеназванные препараты пролонгированными курсами по 5–10 дней. Для курсового системного лечения могут быть использованы и другие препараты группы нитроимидазола: ниморазол и нифурател.
В последние годы в России появляется все большее количество методически рекомендаций, указаний, стандартов по терапии ИППП. Все они основаны на большом клиническом материале, а выпускают их ведущие дерматовенерологические учреждения, Ассоциация акушеров–гинекологов. Существуют так же международные европейские рекомендации, рекомендации ВОЗ. Все они построены по единому принципу и предлагают как рекомендуемые схемы терапии, так и альтернативные.
По данным ВОЗ, рекомендуемыми являются схемы терапии трихомониаза метронидазолом или тинидазолом в однократной дозировке 2,0 г. Альтернативным является применение тех же препаратов по 500 мг 2 раза в сутки в течение 5–7 дней. Сходные данные представляют специалисты США, выводя метронидазол на первое место – 2,0 г однократно.
Согласно данным европейских рекомендаций оптимальным способом лечения трихомониаза является прием метронидазола в течение 7 дней по 500 мг каждые 8 часов.
Итак, как же выбрать оптимальный антипротозойный препарат? По международному опыту, а также данным части отечественных исследователей – это метронидазол.
Однако не все так однозначно. Что касается эффективности при соблюдении рекомендаций врача и одновременном лечении половых партнеров, то она примерно одинакова у всех препаратов (все производные нитроимидазола). В удобстве применения так же все препараты схожи, но что касается побочных эффектов, то, по собственным данным и данным литературы, все–таки переносимость орнидазола и секнидазола несколько лучше, чем у метронидазола.
При приеме последнего чаще отмечаются диспептические растройства, головные боли, бессонница, аллергические реакции, чем у других препаратов данной группы.
Читайте также:

