Что такое атипичная форма инфекции
Обновлено: 17.04.2024
Заболевания, вызываемые вирусами семейства Adenoviridae, характеризуются высокой температурой тела, воспалением слизистых оболочек дыхательных путей и глаз, а также гиперплазией подслизистой оболочки и регионарных лимфатических узлов. Аденовирусная инфекция высоко контагиозна. Наиболее часто наблюдаемые разновидности • ОРВИ с выраженной лихорадкой (преимущественно страдают дети) • ОРВИ взрослых • Вирусные пневмонии • Острые аденовирусные ангины (развиваются у детей, особенно летом после купания) • Острые фолликулярные конъюнктивиты • Эпидемические кератоконъюнктивиты (преимущественно у взрослых) • Кишечные инфекции (энтериты), нередко осложняемые мезентериальными аденитами и инвагинациями. Частота. Очень часто регистрируемая инфекция, составляет 2–5% всех инфекций дыхательных путей. Чаще наблюдают у новорождённых и детей.
Этиология • Возбудители — ДНК-содержащие вирусы рода Mastadenovirus размером 60–90 нм; известно около 80 серотипов (сероваров) • Основные возбудители поражений человека •• Инфекции нижних отделов дыхательных путей (бронхиолиты, пневмонии) — серотипы 1, 2, 3, 5, 6, 7, 21 •• Фарингоконъюнктивиты — серотипы 1, 2, 3, 4, 6, 7, 14 •• ОРВИ — серотипы 3, 4, 7 •• Гастроэнтериты — серотипы 2, 3, 5, 40, 41 •• Конъюнктивиты — серотипы 2, 3, 5, 7, 8, 19, 21 •• Эпидемические кератоконъюнктивиты — серотипы 8, 19, 37 •• Геморрагические циститы — серотипы 11, 21 •• Менингоэнцефалиты — серотипы 2, 6, 7, 12, 32 •• Диссеминированные поражения — серотипы 5, 34, 35, 39 •• Цервициты и уретриты — серотип 37 •• Поражения, ассоциированные с целиакией, — серотип 12.
Эпидемиология. Аденовирусные инфекции человека широко распространены и составляют 5–10% всех вирусных заболеваний; большая часть поражений приходится на детский возраст (около 75%); при этом 35–40% регистрируют у детей до 5 лет, остальные — в возрасте до 14 лет. Основные пути передачи — воздушно-капельный и контактный.
Патоморфология • Варьирует для различных серотипов, при тяжёлой пневмонии можно выявить большое число внутриядерных включений • Возможен облитерирующий бронхиолит.
Клинические формы • Катар дыхательных путей • Фарингоконъюнктивальная лихорадка • Пленчатый конъюнктивит • Тонзиллофарингит (аденовирусная ангина) • Кишечная форма (вирусная диарея, гастроэнтерит) • Мезаденит • Вирусная пневмония.
Клиническая картина
• Катар дыхательных путей — самая распространённая форма, характеризующаяся выраженными катаральными изменениями со стороны дыхательных путей (ринофарингит, ларингит, трахеит, бронхит) при умеренных проявлениях общей интоксикации.
• Плёнчатый конъюнктивит. Обычно наблюдают у взрослых и детей старшего возраста. Односторонний (реже двусторонний) конъюнктивит с фибринозной плёнкой на поверхности слизистой оболочки (чаще нижнего века), сопровождающийся выраженным отёком окружающих тканей, болями, гиперемией и инъекцией сосудов конъюнктивы глаза, лихорадкой. Дыхательные пути в процесс не вовлекаются. Данная клиническая форма характерна только для аденовирусной инфекции (этиологически развёрнутый диагноз можно выставить без лабораторного подтверждения).
• Тонзиллофарингит. Типичен для детей дошкольного возраста. Характеризуется развитием воспалительных изменений тканей зева и нёбных миндалин с формированием ангины (катаральной, фибринозной, реже [при присоединении бактериальной инфекции] гнойной).
• Кишечная форма (гастроэнтерит, вирусная диарея). Характеризуется развитием умеренно выраженного гастроэнтерита, проявляющегося тошнотой, рвотой, жидким стулом без патологических примесей. Температурная тела субфебрильная. Возможно одновременное вовлечение в процесс органов дыхания (катаральный ринофарингит или ларинготрахеит).
• Вирусная пневмония. Самостоятельная клиническая форма с типичной симптоматикой острой пневмонии (интоксикация, признаки лёгочно-сердечной недостаточности). Выражен экссудативный компонент (множественные разнокалиберные хрипы по всем лёгочным полям, кашель с обильной мокротой и т.п.). При рентгенографии выявляют распространённые воспалительные изменения со стороны лёгких. Данная клиническая форма не исключает возможного бактериального суперинфицирования, потому необходима противомикробная терапия.
Методы исследования • Выделение возбудителя инокуляцией в культуры эпителиальных клеток человека; исследуемый материал — отделяемое носа, зева, конъюнктивы, фекалии и др. • Выявление Аг вирусов в клетках иммунофлюоресцентной микроскопией, а также постановка РСК, реакции торможения гемагглютинации (РТГА) и реакции нейтрализации цитопатического эффекта в культуре клеток • Рентгенодиагностика: бронхопневмония при тяжёлой респираторной инфекции • В тяжёлых или атипичных случаях — биопсия (лёгкого либо другой ткани).
ЛЕЧЕНИЕ
Режим • Амбулаторный, за исключением тяжело болеющих детей младшего возраста, больных с эпидемическим кератоконъюнктивитом и детей младшего возраста с тяжёлой пневмонией • Постельный режим на период повышенной температуры тела.
Лекарственная терапия — лечение симптоматическое • При необходимости — парацетамол по 0,2–0,4 г на приём 2–3 р/сут (10–15 мг/кг/сут). Не рекомендован приём ацетилсалициловой кислоты • Противокашлевые и отхаркивающие средства • ГК (местно) — при конъюнктивите (после консультации офтальмолога).
Течение и прогноз • Заболевание проходит самостоятельно практически без осложнений • Тяжёлое течение и летальный исход возможны среди детей и больных с нарушениями иммунитета.
Профилактика • Живые пероральные вакцины против аденовирусов типов 4 и 7, покрытые защищающей от переваривания в кишечнике капсулой, снижают частоту развития ОРВИ • Для персонала различных учреждений и членов семьи больного обязательно частое мытьё рук.
МКБ-10 • A08.2 Аденовирусный энтерит • A85.1+ Аденовирусный энцефалит (G05.1*) • A87.1+ Аденовирусный менингит (G02.0*) • B30.0+ Кератоконъюнктивит, вызванный аденовирусом (H19.2*) • B30.1+ Конъюнктивит, вызванный аденовирусом (H13.1*) • B34.0 Аденовирусная инфекция неуточнённая • J12.0 Аденовирусная пневмония • J02.8 Острый фарингит, вызванный другими уточнёнными возбудителями • J02.9 Острый фарингит неуточнённый • J03.9 Острый тонзиллит неуточнённый.
Приложение. Мезаденит (острый мезентериальный лимфаденит) — воспаление лимфатических узлов, расположенных в брыжейке тонкой кишки; наблюдают преимущественно у детей и подростков; симптоматика напоминает острый аппендицит. Этиология: вирусная инфекция, а также бактерии рода Yersinia. Клиническая картина — боль в животе (может быть сильной), тошнота, рвота и лихорадка; у некоторых больных отмечают дополнительные признаки вирусной инфекции (например, фарингит и миалгию). Диагноз обычно устанавливают при лапаротомии по поводу предполагаемого аппендицита. Лечение: при выделении Yersinia назначают антибиотики. МКБ-10. I88.0 Неспецифический брыжеечный мезаденит.
Татьяна Владимировна Спичак, профессор, доктор медицинских наук:
В сегодняшней лекции я хотела бы коснуться ряда вопросов, связанных с атипичными инфекциями. Они по-прежнему продолжают волновать многих практикующих врачей. Ни для кого из нас не секрет, что успех лечения инфекции дыхательных путей в значительной мере определяется достоверностью этиологической диагностики.
С этим вопросом у нас, к сожалению, особенно в амбулаторной практике дело обстоит не очень благополучно. Если говорить о распространенности атипичных инфекций у детей, то литературные источники приводят нам достаточно большой разброс данных.
Мы знаем, что острый бронхит, как правило, обусловлен вирусной этиологией болезни. Что касается атипичных возбудителей, то с. Pneumonia и m. Pnemoniae диагностируют в 4% и 17% случаев.
При внебольничной пневмонии микоплазменная инфекция встречается у детей от 7% до 27%. А инфекция с. Pneumonia в 6% или 32%.
В последнее время большое внимание уделяется ассоциациям пневмококковой и атипичной инфекции, которые по данным наших зарубежных коллег составляют от 8% до 23%. Мы неспроста затрагиваем этот вопрос, потому что (как мы убедились на собственном опыте) ассоциация пневмококковой и микоплазменной инфекции действительно приводит к более тяжелому течению пневмонии по сравнению с монобактериальной этиологией пневмонии.
Всем хорошо известно, что этиологическая структура пневмонии имеет определенную возрастную зависимость, которая распространяется и на атипичные возбудители. По крайней мере, микоплазменную инфекцию чаще диагностируюn у детей 2-4-х лет и подростков.
С. Trachomatis, как правило, диагностируют у детей первого полугодия жизни. С. Pneumonia инфицирует чаще всего детей старше пяти лет. Хламидийная инфекция может произойти в любой последующий период жизни.
Появилось много литературных данных о роли хламидийной инфекции при бронхиальной астме у детей, особенно при ее тяжелом течении. Но если обратить внимание на представленную таблицу, мы видим очень большой разброс данных по частоте встречаемости хламидийной инфекции при бронхиальной астме. Причем зачастую несопоставимых из-за того, что используются разные методы исследований.
Кроме того, я хотела бы обратить внимание не только тех, кто получает из этой лекции просто информацию, но и тех, кто проводит подобные исследования. Очень важно иметь контрольную группу. К сожалению, во многих исследованиях это отсутствует.
Диагностика атипичных инфекций остается достаточно сложной по сегодняшний день. Это связано с тем, что при данных инфекциях отсутствуют специфические клинические и рентгенологические признаки, которые помогли бы нам в этиологической диагностике.
Главным образом это касается респираторно-хламидийной инфекции. Микоплазменную инфекцию мы еще можем как-то заподозрить по клиническим признакам, основываясь на своеобразных крепитирующих мелкопузырчатых влажных хрипах, нередко ассиметричных. По маловыразительной рентгенологической картине, при которой, как правило, мы наблюдаем усиление мелких элементов легочного рисунка. В большинстве случаев отсутствуют типичные легочные инфильтрации.
Основными методами диагностики атипичных инфекций являются лабораторные методы диагностики. Несмотря на большое число существующих методов, которые, казалось бы, должны нам помогать в диагностике этих инфекций, здесь тоже есть определенные проблемы.
Наибольшее распространение получили иммунологические методы исследования. В последнее время все чаще и шире используется полимеразная цепная реакция. Культуральный и морфологический методы используются, главным образом, в научных целях.
Я хотела бы обратить ваше внимание на то, что, несмотря на многообразие методов исследования, чувствительность и специфичность таковы, что ни один из методов не позволяет нам выявлять возбудитель в 100% случаев. Нам приходится пользоваться, как минимум, двумя методами исследования по более достоверной диагностике.
Есть проблема. Все перечисленные методы исследования могут нам давать либо ложноположительные, либо ложноотрицательные результаты. Это вполне естественно чревато либо лечением псевдобольных, либо распространением инфекции у нераспознанных больных.
Иммунологические методы основаны на использовании диагностикумы на основе родо- и видоспецифических антигенов. На выявлении специфических антител в сыворотке крови и секретах инфицированного организма в процессе иммунного ответа не внедрение возбудителей.
Из этих методов рекомендуется в настоящее время пользоваться методом микроиммунофлюоресценции (МИФ) и иммуноферментным анализом (ИФА).
Методы имеют безусловные достоинства. Прежде всего, возможность избежать ложноотрицательных результатов. В ряде случаев определить стадию заболевания. Но серьезным недостатком метода серологической диагностики является ретроспективная диагностика. Антитела класса М появляются лишь на пятый день от начала болезни.
Мы не можем ставить диагноз на основании данных методов исследования в более ранние сроки. Антитела класса М могут самостоятельно исчезнуть через 2-3 месяца, даже не прибегая к лечению. Что касается антител класса А, то они появляются гораздо позже – на 5 – 14 день – и тоже, как правило, исчезают через 2-3 месяца, но уже при условии проведения специальной терапии.
Если этого не происходит, то обнаружение антител класса А в более поздние сроки указывает на хроническую или персистирующую инфекцию.
Самыми последними появляются антитела класса G. На 15 – 20 день. Особенностью этих антител является то, что они могут сохраняться в низких титрах на протяжении ряда лет, отражая так называемую следовую реакцию после перенесенной инфекции.
Что касается диагностики микоплазменной инфекции, то следует обратить внимание на то, что при данной инфекции наблюдается длительная циркуляция АТ класса М. Для данной инфекции характерно большее развитие острых процессов. А реинфицирование отмечается редко.
Для выявления антигена возбудителя используют метод иммунофлюоресцентной микроскопии. К сожалению, этот метод не лишен недостатков, поскольку его чувствительность невысока, специфичность зависит от навыков персонала.
Полимеразная цепная реакция. Как известно, метод относится к молекулярно-биологическим. Основан на выявлении в составе биологического материала фрагментов ДНК или РНК, специфических для вида возбудителя. Этот метод отличает высочайшая чувствительность и специфичность. С помощью данного метода мы можем диагностировать на ранних стадиях болезнь и выявлять минимальное количество возбудителей вне зависимости от его жизнеспособности.
К сожалению, и этот метод не лишен недостатков. Мы имеем возможность получить и ложноположительные результаты в силу такой высокой чувствительности метода. Любая загрязняющая ДНК может дать нам такой результат.
Реакция может быть подавлена биологическим материалом. Это может привести к ложноотрицательному результату.
Показания к назначению лечения при атипичных инфекциях достаточно традиционные. Принято лечить острую инфекцию, реинфекцию и обострение хронической инфекции. Казалось бы, все просто. Но, к сожалению, достаточно непросто в реальной жизни определить стадию болезни и правильно сориентироваться с лечением, руководствуясь не только теми результатами, которые мы получаем на листах бумаги.
При диагностике респираторной хламидийной инфекции многие клиницисты до сих пор используют критерии Грейстона (Grayston G. T.). Они основаны на результатах реакции по определению специфических антител класса М и G. При выявлении специфических антител класса М и высоких титров антител класса G или при четырехкратном увеличении титра антител класса G в парных сыворотках можно говорить об острой инфекции.
При реинфекции хламидийной инфекции антитела класса М отсутствуют. Но наблюдается быстрое, буквально в течение одной-двух недель, появление антител класса G. Или также как при острой инфекции четырехкратное увеличение в парных сыворотках.
Но поскольку речь идет о лечении детей, то мы предъявляем особые требования к антибактериальным препаратам. Они должны быть не только эффективными, но и максимально безопасными. Наш выбор сводится к макролидным препаратам.
Я не буду останавливаться на классификации макролидов. Она вам прекрасно известна. Хочу еще раз подчеркнуть их уникальные свойства как группы антибактериальных препаратов. Они относятся к числу наиболее безопасных антибиотиков и являются тканевыми антибиотиками, поскольку концентрация в инфицированных тканях во много раз превышает сывороточные.
Фармакодинамика современных макролидов позволяет их назначать 2-3 раза в сутки, что повышает комлпаентность.
Данная группа препаратов обладает уникальным постантибиотическим эффектом. Даже после прекращения введения антибактериального препарата, сохраняясь в инфицированных тканях, препарат продолжает еще обеспечивать терапевтические концентрации в течение еще 5-7 дней.
По сравнению с четырнадцатью членами макролидов его характеризует низкая частота лекарственных взаимодействий, хороший профиль безопасности и низкий уровень приобретенной резистентности.
В отношении длительности курсового лечения при атипичных инфекциях принято во многих руководствах пользоваться десятидневными курсами лечения макролидными препаратами. Но некоторые руководства предлагают более длительные курсы лечения в течение 2-3 недель. Полагают, что это позволит осуществить профилактику персистирующей или хронической инфекции.
Подобное лечение острых инфекций может вызвать вполне оправданные возражения.
Что касается хронической инфекции (а здесь речь идет о хронической хламидийной инфекции), то приняты более длительные трехнедельные курсы лечения.
Оценка эффективности терапии осуществляется по исчезновению антигенового возбудителя, по снижению или исчезновению титра специфических антител. Я неспроста обращала ваше внимание на особенности динамики антителообразования при атипичных инфекциях. Контрольное исследование следует проводить не ранее, чем через 2-3 месяца.
В заключение я хотела бы привести результаты недавно завершенного нами исследования по определению этиологической структуры внебольничных пневмоний у детей и оценке эффективности рациональной антибиотиковой терапии.
Для этих целей мы использовали ПЦР-диагностику. Определили специфические антитела указанных классов методом ИФА.
Из 63-х детей у 57-ми был определен инфекционный патоген, что обеспечило 90,5% выявления этиологически значимого агента.
По совокупности лабораторных методов исследования современная этиологическая структура внебольничной пневмонии у детей по нашим данным выглядит следующим образом. Мы видим, что пневмококк остается лидирующим или весьма значимым типичным бактериальным патогеном при внебольничных пневмониях.
В то же время мы видим, что высока частота и микоплазменных инфекций при пневмонии у детей. Этого нельзя сказать о хламидийных пневмониях, потому что их частота не превышала в наших данных 14%. В каждом седьмом случае мы имели дело со смешанной бактериальной инфекцией при внебольничной пневмонии, обусловленной, главным образом, сочетанием пневмококка и микоплазменной инфекции.
Течение пневмонии было более тяжелым, чем при монопневмококковой инфекции.
Наши наблюдения (несмотря на то, что когда мы уточнили этиологию, группы оказались не такими многочисленными) позволили отметить особенности внебольничных пневмоний, на которые обращают внимание в современных руководствах. По крайней мере, в зарубежных.
Действительно в первые дни маловыразительная клиническая картина. Достаточно редко определяются хрипы и типичная физикальная симптоматика. Но у большинства детей присутствует синдром дыхательных расстройств. Это, в первую очередь, касается пневмококковых пневмоний. В меньшей степени это касается микоплазменной и хламидийной пневмонии.
Синдром дыхательных расстройств, который ведет в число наиболее достоверных диагностических и клинических признаков, в большей степени работает у детей до пяти лет. Дети с микоплазменной и хламидийной пневмонией в нашем наблюдении были школьного возраста.
При лечении внебольничных пневмоний мы поступали также, как поступают все практикующие врачи. Мы назначали антибактериальную терапию эмпирически, в соответствии с принципами рациональной антибиотиковой терапии до получения результатов проведенных нами биологических и других исследований.
В заключение я хотела бы сказать о том, что атипичные инфекции остаются достаточно хорошо распространенными у детей и подростков при инфекциях дыхательных путей. Если мы хотим повысить эффективность и улучшить диагностику атипичных инфекций, то нам надо обращать внимание на микробиологические лаборатории, на то оборудование, на котором они работают, и на приобретение качественных тест-систем.
Мы можем сказать, что макролидные антибиотики являются препаратами выбора при инфекции дыхательных путей и внебольничной пневмонии. В первую очередь, в период сезонных вспышек микоплазменной или хламидийной инфекции. А также у детей, имеющих признаки аллергии на бета-лактамные антибиотики.
Инфицирование атипичными микобактериаями. Инфекции атипичных микобактерий.
По данным исследований, проведенных в Москве, Киеве, Ленинграде, Львове, Фрунзе и других городах, атипичные микобактерий составляют в среднем 1,67% среди 17 495 выделенных культур. Неодинакова и частота различных видов атипичных микобактерий. По данным Н. М. Макаревич (1973), среди общего числа ското-хромогенные штаммы высеваются в 55,8% случаев, нефотохромогенные— в 25%, быстро растущие — в 10,8%, фотохромогенные — в 8,3%.
Сравнительно чаще выделяют атипичные микобактерий из пораженных периферических лимфатических узлов у детей. По данным Schroder (1969), они составили 12% среди всех видов микобактерий туберкулеза, обнаруженных при этой форме процесса в 1958—1966 гг. в ФРГ.
Следует, однако, подчеркнуть, что патогенными считаются лишь те атипичные кислотоустойчивые микобактерий, которые повторно высеиваются из мокроты одного и того же больного или из резецированного легкого и другого органа, образуют многочисленные колонии в культурах и вызывают патологические изменения в организме у некоторых лабораторных животных, например у белых мышей.
Уверенность в заражении такими микобактериями возрастает, если больные реагируют на гомологичные сенситины, полученные из того или иного вида типичных микобактерий, более интенсивными внутрикожными реакциями, чем на стандартный туберкулин. Известным подтверждением этиологической роли атипичных микобактерий в генезе болезни служит также обнаружение методом двойной диффузии в агаре специфических антител в сыворотке крови больных (Jenkins, 1959).
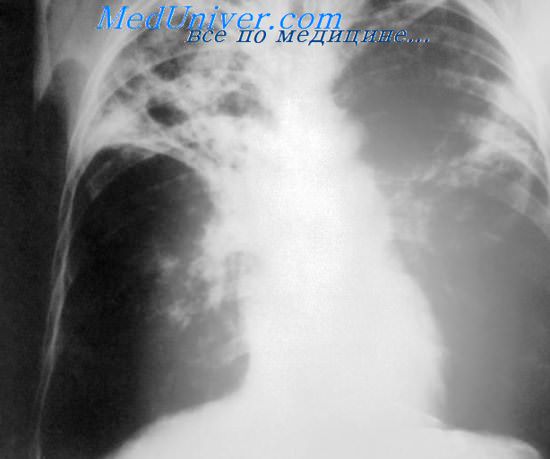
Атипичные микобактерии могут проникнуть в организм различными путями: с воздухом, пылью, водой, с плохо обработанными продуктами от животных, при контакте с зараженными домашними животными и птицами. Возможность передачи инфекции от человека человеку не установлена.
Н. М. Макаревич (1973) выделила атипичные микобактерий из мокроты 102 больных, 84 из которых поступили в клинику с диагнозом: туберкулез легких. Однако этиологическая роль этих видов микробов в развитии болезни была подтверждена лишь в 25 случаях; в остальных — они были сопутствующими микобактериями и не влияли на клинику и течение специфического легочного процесса.
Обращает на себя внимание, что большинство больных микобактериозами — мужчины преимущественно среднего и пожилого возраста. Часть из них заняты в профессиях, связанных с уходом за животными и с вдыханием угольной или металлической пыли. У них не отмечается контакта с бацилловыделителями. Заболевание протекает хронически на протяжении многих лет с выраженной наклонностью к фиброзу, развитию эмфиземы и возникновению кровохарканья. Образующиеся каверны в легких часто тонкостенные и не сопровождаются бронхогенпым обсеменением. При всех указанных формах болезни туберкулостатические препараты I ряда оказываются неэффективными из-за устойчивости к ним атипичных штаммов микобактерий. В последнее время установлено известное терапевтическое действие в этих случаях циклосерина, канамицина, этамбутола и рифампицина, к которым атипичные микобактерий оказываются чувствительными.
Совместно с Н. М. Макаревич и Б. Я. Бакаповой мы имели возможность наблюдать больного М., 65 лет, страдавшего микобактериозом, вызванным М. fortuitum.
Микобактериоз — болезнь будущего, утверждают некоторые авторы. Трудно сказать, оправдается ли это предположение. Тем не менее повсеместно накапливающиеся клинико-лабораторные наблюдения побуждают к дальнейшим углубленным исследованиям в этой области и уточнению взаимосвязи туберкулеза и микобактериоза.
Обобщая приведенные данные, следует, таким образом, прийти к выводу, что форма и характер течения туберкулеза в какой-то степени определяются теми или иными биологическими свойствами микобактерий.
Известную роль в клинических проявлениях болезни играют пути заражения. При крайне редко встречающемся внутриутробном инфицировании поражаются главным образом печень, селезенка, брюшина, мезен-териальные лимфатические узлы и в меньшей степени — легкие. Подобное явление отмечается и при заражении большой дозой микобактерий алиментарным путем. На это указывают, например, результаты клинического и секционного исследования детей в Любеке, которым при вакцинации ошибочно была введена культура вирулентных микобактерий человеческого типа. Первичный комплекс среди умерших у 85% находился в брюшной полости и у 15% — в легких. У 104 человек из 174 оставшихся в живых и длительно наблюдавшихся крупные обызвествленные очаги обнаруживались в забрюшинных лимфатических узлах, у 59 — в шейных и лишь у 11 — в легких и во внутригрудных лимфатических узлах.
В Баварии, где еще в 1952 г. был широко распространен туберкулез среди рогатого скота, а население часто пользовалось сырым молоком и непастеризованными молочными продуктами, при обследовании большой группы клинически здоровых школьников у 43% из них были обнаружены обызвествленные забрюшинные и брыжеечные лимфатические узлы. В этих случаях, очевидно, имело место энтеральное заражение микобактериями бычьего типа.
- Вернуться в оглавление раздела "Пульмонология."
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Атипичная микобактериальная инфекция — комплекс гранулематозных поражений, вызываемых микобактериями, отличающимися от классических патогенов — возбудителей туберкулёза и лепры.
Этиология. Возбудители — кислотоустойчивые бактерии Mycobacterium ulcerans, M. marinum (M. balnei), M. kansasii, M. avium-intracellulare, M. xenopi, M. scrofulaceum.
Эпидемиология. Большинство возбудителей широко распространено в окружающей среде; некоторые обитают в воде и прибрежной зоне, вызывая заболевания у рыб, другие (например, Mycobacterium avium-intracellulare) — у птиц. Наиболее часто заражение происходит при вдыхании микобактерий, употреблении заражённых продуктов и проникновении возбудителя через микротравмы кожи и слизистых оболочек.
Патогенез. Проникшие микобактерии фагоцитируются макрофагами и транспортируются в регионарные лимфатические узлы; фагоцитарные реакции незавершённые, и возбудитель персистирует в цитоплазме макрофагов. Воспалительная реакция незначительная, но в месте проникновения развивается первичный аффект. В динамике по ходу регионарных лимфатических путей и узлов формируется первичный комплекс, характеризующийся развитием гранулём. Микроскопия биоптатов выявляет в последних очаги неказеозного некроза, содержащие кислотоустойчивые бактерии.
Клиническая картина
• Туберкулёзоподобные поражения. В патологический процесс вовлекаются лёгкие, почки, кожные покровы и костно-суставная система. Часто осложняют течение эмфизематозных процессов. У 40–50% больных с иммунодефицитными состояниями вызывают генерализованные поражения.
• Лимфадениты. Клинически чаще проявляются поражениями шейных лимфатических узлов (так называемые скрофулы); последние безболезненны, могут изъязвляться либо дренироваться наружу; системные проявления слабые или чаще отсутствуют.
• Кожные поражения. Типичным считают инфицирование ран конечностей, полученных при ударе о стенку бассейна или любой объект на дне и берегах водоёма. Чаще наблюдают образование изъязвляющейся гранулёмы, спонтанно ограничивающейся в течение нескольких недель, в более редких случаях формируется хроническая инфекция.
Методы исследования • Выделение и идентификация возбудителя по скорости роста, образованию пигментов (на свету или в темноте) и патогенности для лабораторных животных • АТ к Mycobacterium kansasii перекрёстно реагируют с Аг Mycobacterium tuberculosis и у инфицированных лиц отмечают положительную реакцию Манту.
Дифференциальная диагностика • Лепра • Туберкулёз • Боррелиоз • Чума.
Лечение • При лёгочных поражениях •• Рекомендовано сочетание изониазида 600 мг, рифампицина 300 мг, стрептомицина 1 г и этамбутола 15–25 мг/кг 1 р/сут •• При поражении M. marinum — миноциклин по 100 мг каждые 12 ч в течение 6–8 нед •• При поражении M. kansasii и M. xenopi эффективна стандартная противотуберкулёзная терапия с обязательным назначением рифампицина •• Оперативное вмешательство рекомендовано при локализованных поражениях у пациентов молодого возраста без патологии других органов и систем • При лимфадените — у детей от 1 до 5 лет показано хирургическое лечение • При кожных поражениях, вызванных M. marinum, — тетрациклин (1–2 г/сут) и сочетание рифампицина и этамбутола в течение 3–6 мес • При инфекциях, вызванных ранами или инородными телами •• Хирургическая обработка раны и удаление инородного тела •• Лекарственная терапия: доксициклин (200–400 мг/сут), цефокситин (200 мг/кг/сут), амикацин (10–15 мг/сут) в течение 3–6 мес • При диссеминированных поражениях — сочетание противотуберкулёзных средств (как при лёгочных поражениях) лишь уменьшает бактериемию и временно ослабляет симптомы.
Течение и прогноз. Течение — прогрессирующее. Более чем у 20% пациентов отмечают рецидивы заболевания в течение 5 лет.
МКБ-10. A31 Инфекции, вызванные другими микобактериями
Код вставки на сайт
Атипичная микобактериальная инфекция — комплекс гранулематозных поражений, вызываемых микобактериями, отличающимися от классических патогенов — возбудителей туберкулёза и лепры.
Этиология. Возбудители — кислотоустойчивые бактерии Mycobacterium ulcerans, M. marinum (M. balnei), M. kansasii, M. avium-intracellulare, M. xenopi, M. scrofulaceum.
Эпидемиология. Большинство возбудителей широко распространено в окружающей среде; некоторые обитают в воде и прибрежной зоне, вызывая заболевания у рыб, другие (например, Mycobacterium avium-intracellulare) — у птиц. Наиболее часто заражение происходит при вдыхании микобактерий, употреблении заражённых продуктов и проникновении возбудителя через микротравмы кожи и слизистых оболочек.
Патогенез. Проникшие микобактерии фагоцитируются макрофагами и транспортируются в регионарные лимфатические узлы; фагоцитарные реакции незавершённые, и возбудитель персистирует в цитоплазме макрофагов. Воспалительная реакция незначительная, но в месте проникновения развивается первичный аффект. В динамике по ходу регионарных лимфатических путей и узлов формируется первичный комплекс, характеризующийся развитием гранулём. Микроскопия биоптатов выявляет в последних очаги неказеозного некроза, содержащие кислотоустойчивые бактерии.
Клиническая картина
• Туберкулёзоподобные поражения. В патологический процесс вовлекаются лёгкие, почки, кожные покровы и костно-суставная система. Часто осложняют течение эмфизематозных процессов. У 40–50% больных с иммунодефицитными состояниями вызывают генерализованные поражения.
• Лимфадениты. Клинически чаще проявляются поражениями шейных лимфатических узлов (так называемые скрофулы); последние безболезненны, могут изъязвляться либо дренироваться наружу; системные проявления слабые или чаще отсутствуют.
• Кожные поражения. Типичным считают инфицирование ран конечностей, полученных при ударе о стенку бассейна или любой объект на дне и берегах водоёма. Чаще наблюдают образование изъязвляющейся гранулёмы, спонтанно ограничивающейся в течение нескольких недель, в более редких случаях формируется хроническая инфекция.
Методы исследования • Выделение и идентификация возбудителя по скорости роста, образованию пигментов (на свету или в темноте) и патогенности для лабораторных животных • АТ к Mycobacterium kansasii перекрёстно реагируют с Аг Mycobacterium tuberculosis и у инфицированных лиц отмечают положительную реакцию Манту.
Дифференциальная диагностика • Лепра • Туберкулёз • Боррелиоз • Чума.
Лечение • При лёгочных поражениях •• Рекомендовано сочетание изониазида 600 мг, рифампицина 300 мг, стрептомицина 1 г и этамбутола 15–25 мг/кг 1 р/сут •• При поражении M. marinum — миноциклин по 100 мг каждые 12 ч в течение 6–8 нед •• При поражении M. kansasii и M. xenopi эффективна стандартная противотуберкулёзная терапия с обязательным назначением рифампицина •• Оперативное вмешательство рекомендовано при локализованных поражениях у пациентов молодого возраста без патологии других органов и систем • При лимфадените — у детей от 1 до 5 лет показано хирургическое лечение • При кожных поражениях, вызванных M. marinum, — тетрациклин (1–2 г/сут) и сочетание рифампицина и этамбутола в течение 3–6 мес • При инфекциях, вызванных ранами или инородными телами •• Хирургическая обработка раны и удаление инородного тела •• Лекарственная терапия: доксициклин (200–400 мг/сут), цефокситин (200 мг/кг/сут), амикацин (10–15 мг/сут) в течение 3–6 мес • При диссеминированных поражениях — сочетание противотуберкулёзных средств (как при лёгочных поражениях) лишь уменьшает бактериемию и временно ослабляет симптомы.
Течение и прогноз. Течение — прогрессирующее. Более чем у 20% пациентов отмечают рецидивы заболевания в течение 5 лет.
Читайте также:

