Что такое цитомегаловирусный энцефалит
Обновлено: 19.04.2024
Цитомегаловирусный энцефалит является редким проявлением цигомегалии и характеризуется тяжелым поражением мозга с высокой летальностью и инвалидизацией.
Что провоцирует / Причины Цитомегаловирусного энцефалита:
Возбудитель (Cytomegalovirus hominis) относится к вирусам герпеса (семейство Herpesviridae). Диаметр вириона около 180 нм, вирус содержит ДНК, при развитии вируса в ядрах инфицированных клеток образуются включения. Может развиваться на культурах фибробластов человека. Под воздействием вируса нормальные клетки превращаются в цитомегалические, диаметр которых достигает 25-40 мкм. В культуре тканей не выявлено существенных нарушений хромосомного аппарата. Возможность онкогенного действия вируса окончательно не изучена. Имеются антигенные различия между отдельными штаммами вируса. Обладает свойствами, общими для всех вирусов группы герпеса.
Частота цитомегаловирусного энцефалита у детей составляет 2-3% среди других форм острых энцефалитов.
Патогенез (что происходит?) во время Цитомегаловирусного энцефалита:
В зависимости от путей передачи воротами инфекции могут служить слизистые оболочки верхних отделов респираторного тракта, органов пищеварения и половых органов. Каких-либо изменений на месте ворот инфекции не отмечается. Не сказывается характер инфицирования и на клинических проявлениях болезни. Вирус имеет тропизм к ткани слюнных желез и при локализованных формах обнаруживается только в этих железах.
Вирус персистирует в организме пожизненно. В ответ на первичное внедрение развивается иммунная перестройка организма. Переход латентной цитомегаловирусной инфекции в клинически выраженные формы обычно провоцируется какими-либо ослабляющими факторами, например, интеркуррентными заболеваниями, назначением цитостатиков и других иммунодепрессантов. В последние годы особенно актуальной стала проблема обострения цитомегаловирусной инфекции у ВИЧ-инфицированных лиц.
У беременных с латентной цитомегаловирусной инфекцией плод поражается далеко не всегда. Необходимым условием для этого является обострение у матери латентной инфекции с развитием вирусемии с последующим заражением плода. Вероятность заражения плода будет значительно выше при инфицировании матери во время беременности. Во время фазы вирусемии при отсутствии антител у матери (а, следовательно, у плода) передача инфекции плоду осуществляется значительно легче, чем в иммунном организме ранее инфицированной матери.
Симптомы Цитомегаловирусного энцефалита:
Цитомегаловирусный энцефалит зачастую не имеет четкого начала. Дети становятся беспокойными, плохо спят, отказываются от еды, часто срыгивают, теряют массу тела. Типичны гипертензионно-гидроцефальный синдром или гидроцефалия с выбуханием и напряжением родничка, расхождением черепных швов, увеличением окружности головы. Повышается мышечный тонус, отмечаются тремор конечностей, сухожильная гиперрефлексия, клонусы стоп. Возможно развитие центральных парезов и параличей, чаще по гемитипу. Периодически могут наблюдаться генерализованные клонико-тонические судороги. Ребенок значительно отстает в психическом развитии или теряет уже приобретенные умственные и двигательные навыки. Изменения цереброспинальной жидкости (увеличение содержания белка, умеренный лимфоцитарный или смешанный плеоцитоз) бывают лишь в начальном периоде болезни. Характерна генерализация процесса с гепатолиенальным синдромом, почечной недостаточностью. На этом фоне присоединяется бактериальная инфекция. Больные умирают в течение 1-2 лет.
Диагностика Цитомегаловирусного энцефалита:
Клиническая диагностика генерализованных форм ЦМВ-инфекции представляет значительные трудности, т.к. клиническая картина ее полиморфна, часто не имеет специфических проявлений и протекает под маской других заболеваний
Лабораторная диагностика ЦМВ-инфекции:
– определение методом ИФА специфических антител класса IgG
– определение методом ИФА специфических антител класса IgM
– цитологические исследования (анализ на клетки –цитомегалы)
– определение методом ПЦР ДНК ЦМВ в разных биосубстратах (плазма крови, моча, ликвор, слеза, слюна, амниотическая жидкость и др.)
– МРТ выявляет перивентрикулярные сливные очаги с усилением контраста.
– ПЦР на цитомегаловирус в СМЖ обладает чувствительностью >80% и специфичностью 90%.
– Выделить культуру ЦМВ из СМЖ обычно не удается.
Лечение Цитомегаловирусного энцефалита:
Этиотропного лечения нет. Противогерпетические препараты (ацикловир, видарабин), успешно применяемые при других болезнях, при цитомегалии оказались неэффективными. Имеются данные, что препарат Cymeven (ganciclovir sodium) оказывает некоторый эффект при цитомегаловирусной инфекции, однако требуется дальнейшее его изучение, тем более, что он вызывает побочные реакции (гранулоцитопению и др.). При приобретенной цитомегаловирусной инфекции беременных основной задачей является предупреждение генерализации инфекции и внутриутробного заражения плода. С этой целью проводят десенсибилизацию и общеукрепляющую терапию. Рекомендуется также введение нормального человеческого иммуноглобулина, содержащего специфические антитела, вводят его внутримышечно по 6-12 мл с интервалами 2-3 нед в течение первых 3 мес беременности. При трансплантации почки профилактический эффект оказывало введение альфа-интерферона.
Профилактика Цитомегаловирусного энцефалита:
Специфическая профилактика не разработана. При переливании крови новорожденным, а также лицам с ослабленным иммунитетом следует использовать кровь от доноров, у которых отсутствуют антитела против цитомегаловирусов. Мероприятия в очаге не проводятся.
К каким докторам следует обращаться если у Вас Цитомегаловирусный энцефалит:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Цитомегаловирусного энцефалита, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Цитомегаловирусная инфекция у детей (ЦМВИ) – типичный представитель оппортунистических инфекционных заболеваний, клинически проявляющихся только на фоне иммунодефицитных состояний.
Цитомегалия — это вирусное заболевание, которое проявляется множеством симптомов, которые возникаюь из-за образования гигантских клеток с типичными внутриядерными и цитоплазматическими включениями в слюнных железах, висцеральных органах и центральной нервной системе.
Цитомегаловирусная инфекция, согласно международной классификации, бывает таких видов:
- цитомегаловирусный панкреатит
- цитомегаловирусный гепатит
- цитомегаловирусная пневмония
- другие цитомегаловирусньте болезни
- неуточненная цитомегаловирусная болезнь.
Также существует врожденная цитомегаловирусная инфекция и цитомегаловирусный мононуклеоз.
Цитомегалия бывает врожденной или приобретенной. При врожденной могут быть поражены многие органы и системы ребенка, такую форму болезни называют генерализированной.
Приобретенная цитомегалия у детей раннего возраст протекает по типу мононуклеозоподобного синдрома. В некоторых случаях вирус преимущественно поражает желудочно-кишечный тракт, легкие, печень. Или же болезнь может принять генерализированную форму. Обе формы (врожденная и приобретенная) могут проходить бессимптомно. Согласно классификации по признаку течения, цитомегалия бывает острой и хронической.
Что провоцирует / Причины Цитомегаловирусной инфекции у детей:
Возбудитель – ДНК-содержащий вирус семейства Herpes-viriae – Cytomegalovirus hominis. Источником цитомегаловирусной инфекции у детей является мать. Механизмы передачи: вертикальный и интранатальный.
Пути передачи – гематогенный (трансплацентарный), восходящий, контактный, аспирационный (при заглатывании инфицированных околоплодных вод). У детей первого года жизни возможно инфицирование через грудное молоко. Дети раннего возраста могут инфицироваться контактно-бытовым, воздушно-капельным, трансфузионным путем.
Эпидемиологические особенности ЦМВИ (широкое распространение цитомегаловируса в человеческой популяции, различные механизмы и пути передачи, преобладание субклинических форм инфекции), а также особенности иммунитета у беременных и плода способствуют повышенному риску внутриутробного инфицирования вирусом цитомегалии.

У больных цитомегаловирусной инфекцией клетки, зараженные вирусом, обнаруживают в осадке мочи, слюне, спинномозговой жидкости и пораженных органах. Вирус сохраняет жизнедеятельность в среде, имеющей комнатную температуру. Он имеет чувствительность к дезинфицирующим средствам и эфиру. Вирус устойчив к антибиотикам.
Патогенез (что происходит?) во время Цитомегаловирусной инфекции у детей:
У новорожденных детей встречается в 0,2-2,5% случаев. Клинические формы врожденной цитомегаловирусной инфекции у детей: бессимптомная, генерализованная. У 80% детей, перенесших генерализованную ЦМВИ, в дальнейшем отмечается неврологическая симптоматика, у 17% детей при бессимптомном течении заболевания отмечается минимальная мозговая дисфункция, задержка развития, неврозоподобные расстройства.
Скорость репликации и инфицирования дочерними вирусами незараженных клеток зависит от функционального состояния иммунной системы. Неспецифические факторы иммунитета – система интерферона, комплемента, естественные киллеры – на первых этапах инфекционного процесса замедляют скорость распространения возбудителя, а в дальнейшем потенцируют активность специфического иммунитета и препятствуют инфицированию непораженных клеток. Однако наиболее действенной защитой от ЦМВИ является создание специфического иммунитета (образование специфических антител и специфических Т-лимфоцитов). Специфическая иммунная защита может формироваться только в том случае, если вирусы расположены и неклеточно. Внутриклеточное расположение вируса защищает его от иммунного воздействия.
Клинические проявления: риск инфицирования плода, тяжесть заболевания новорожденного ребенка и дальнейший прогноз при внутриутробной ЦМВИ зависят от характера течения инфекционного процесса у матери в период беременности. Если женщина, не имеющая иммунитета к вирусу цитомегалии, впервые инфицируется им в период беременности, то это приводит к развитию у нее первичной ЦМВИ. Частота передачи цитомегаловируса при первичной инфекции от серонегативной беременной плоду составляет от 30 до 50%. Следует отметить, что в большинстве случаев отмечается бессимптомное течение инфекции у женщин. При вторичной цитомегаловирусной инфекции риск внутриутробного инфицирования плода значительно ниже (2%).
Симптомы Цитомегаловирусной инфекции у детей:
Клинические проявления внутриутробной ЦМВИ:
- петехиальная сыпь (мелкие кожные кровоизлияния) – 60-80%
- тромбоцитопеническая пурпура – 76%;
- желтуха – 67%;
- гепатоспленомегалия – 60%;
- микроцефалия – 53%;
- гипотрофия – 50%;
- недоношенность – 34%;
- гепатит – 20%;
- энцефалит –15%;
- хориоретинит – 12%.
Клиническая картина приобретенной цитомегалии. Инкубационный период может длиться минимум 15 дней, максимум 3 месяца. Всё это время ребенок является носителем инфекции.
При приобретенной цитомегалии ребенок заражается от матери или медперсоналав роддоме в том случае, если данные взрослые – носители вируса. Если малышу делают переливание плазмы/крови от доноров, и кровь недостаточно проверена, возможно заражение.
Болезнь может проявиться в изолированном поражении слюнных желез, либо инфекция поражает, помимо слюнных желез, еще и висцеральные органы. Приобретенная цитомегалия редко бывает генерализированной. У ребенка постепенно повышается температура. Среди симптомов отмечают такие: боли в горле, увеличение шейных лимфатических узлов, печени и селезенки. Могут быть головные боли, боли в животе, анорексия, ощущение слабости в теле.
Слизиста оболочка ротоглотки чуть красновата, можно наблюдать увеличение небных миндалин.
В других случаях могут проявляться симптомы интерстициальной пневмонии, такие как цианоз, одышка и пр. Не исключены желудочно-кишечные расстройства, проявляющиеся в учащении стула и рвоте. Может наблюдаться также нарушение печеночных функций, например, потемнение мочи, желтуха и т. д., а также изменения в мочи.
Болезнь длится долго. Температура может ежедневно повышаться до уровня 39—40 ˚ С. Ребенок во время подъемов температуры ощущает озноб, что может длиться от 2 до 4 недель, редко – более длительный срок.
Если заражение возникло вследствие переливания крови, через 5-6 недель после процедуры возникает цитомегаловирусный мононуклеозоподобный синдром.
Генерализированная форма приобретенной цитомегаловирусной инфекции отличается тем, что вирус постепенно поражает многие органы и системы в организме ребенка. Лихорадка длительная, проявляется общеинфекционный токсикоз. Вирус поражает легкие, что приводит к интерстициальной пневмонии. Поражение желудочно-кишечного тракта проявляется в повторяющихся приступах рвоты и жидком многократном стуле. Вирус при генерализированной форме поражает сердечно-сосудистую систему. Фиксируются явления паренхиматозного гепатита, энцефалита. Течение генерализированной формы длительное.
Диагностика Цитомегаловирусной инфекции у детей:
Чтобы диагностировать наличие цитомегаловирусной инфекции у детей проводиться лабороторное исследование крови на специфические антитела к цитомегаловирусу – иммуноглобулинов М и G.
Обнаружение иммуноглобулинов М может указывать на первичное заражение цитомегаловирусами либо на реактивацию хронической цитомегаловирусной инфекции. Высокие титры IgМ у беременных могут способствовать инфицированию плода. Повышение IgМ определяется в крови через 4-7 недель после заражения вирусом и наблюдается в течение16-20 недель.
Повышенные иммуноглобулины G развиваются в период снижения активности цитомегаловирусной инфекции. Их наличие в крови указывает на цитомегаловирус в организме, но не показывает активности инфекционного процесса.
С помощью ПЦР-диагностики определяется ДНК цитомегаловируса в клетках крови и слизистых – соскобы из уретры и цервикального канала, мокроты, слюна и т.д. Эффективным способом диагностики является проведение количественной ПЦР, которая показывает активность цитомегаловируса и вызываемого им инфекционного процесса. Диагноз ставится, когда выделение цитомегаловируса в забранном материале пошается.
Зависимо от того, какой орган пострадал от инфекции, пациент проходит осмотр гинеколога, гастроэнтеролога, андролога или других докторов. Дополнительно может назначаться проведение УЗИ органов брюшной полости, гастроскопия, кольпоскопия, МРТ головного мозга и другое.
Лечение Цитомегаловирусной инфекции у детей:
В настоящее время существует два основных направления терапии и профилактики вирусных инфекций. Это виростатические препараты и специфические иммуноглобулины. Эти два вида терапии имеют принципиальные отличия в механизме противовирусного действия.
Ганцикловир назначают внутрь во время еды, а также вводят внутривенно. Биоусвоение из желудочно-кишечного тракта равно 15-20%, тем не менее этого достаточно для оказания эффекта. У препарата высокая активность и он обладает способностью избирательно накапливаться в клетках, инфицированных вирусом, но не в интактных клетках. Его концентрация в инфицированных клетках может в 30-120 раз быть больше, чем в плазме крови. Это важное обстоятельство объясняет большую широту терапевтического действия данного препарата по сравнению с другими и меньшую опасность осложнений. Связывание с белками плазмы крови всего 9-30%, поэтому препарат хорошо проникает в различные ткани и жидкости (включая ликвор). Большая часть препарата (80-90%) в неизмененном виде и в виде метаболита 9-карбоксиметоксиметилгуанина выводится почками. Период полувыведения примерно 3,3 ч, однако при почечной недостаточности он может увеличиваться до 20 ч, поэтому необходимо корректировать дозирование. Так, при скорости клубочковой фильтрации (СКФ) менее 70 мл/мин — дозу препарата снижают в 2 раза; при СКФ менее 50 мл/мин – дозу уменьшают еще на треть; при СКФ менее 25 мл/мин еще на '/2 и при СКФ менее 10 мл/мин – в 3 раза.
Нежелательные эффекты ганцикловира: гематотоксичность (нейтро-, лейко-, тромбоцитопения); энцефалопатические реакции; иммунодепрессия; повреждение репродуктивной функции у мужчин и женщин; мутагенное, тератогенное и канцерогенное действие.
Фоскарнет (фосфоноформат) вводят внутривенно. Период его полувыведения от 2 до 4 ч. Экскретируется в неизмененном виде почками. Фоскарнет может вызывать костномозговую депрессию, иммунодепрессию, нарушения функции печени и почек; он обладает тератогенным, мутагенным и канцерогенным свойством.
При использовании ганцикловира и фоскарнета необходимо каждые 2 дня анализ крови. При выраженной нейтропении (меньше 500/мкл) и тромбоцитопении (менее 25 000/мкл) препараты срочно отменяют.
Ганцикловир и фоскарнет являются цитостатиками, поэтому при лечении ЦМВИ их иногда комбинируют с иммуностимуляторами или с интерфероногенами (например, с циклофероном и др.), а также со стимуляторами кроветворения (например, с филграстимом и др.) и с иммуноглобулинами (цитотект).
Цитотект – иммуноглобулин с повышенным содержанием специфических антител к цитомегаловирусу. Его применяют как средство заместительной терапии.
Индивидуальная непереносимость препарата проявляется головной болью, тошнотой, головокружением, рвотой, диареей, тахикардией, цианозом, одышкой, гипертермией, ознобом, повышенным потоотделением, болью в спине, миалгией. Перечисленные симптомы могут появиться уже через 30 мин после начала инфузии и наблюдаться в течение первых суток. Тяжелая анафилактическая реакция может наблюдаться у больных с отсутствием или выраженным дефицитом IgA, что примерно в 30% случаев связано с наличием у них антител против названного иммуноглобулина. Когда такие больные получают иммуноглобулиновый препарат, у них образуются макромолекулярный комплекс IgA – анти-IgA, приводящий к анафилаксии. Целесообразно у всех больных определять IgA в сыворотке крови перед введением цитотекта.
Профилактика Цитомегаловирусной инфекции у детей:
К методам профилактики принадлежат неспецифические: соблюдение личной гигиены, к специфическим относятся медикаментозный метод препаратами – ганцикловир, ацикловир, фоскарнет.
Чтобы исключить возможность инфицирования цитомегаловирусом пациентов при пересадке органов и тканей необходимо проводить тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Особую опасность цитомегаловирусная инфекция представляет для беременных женщин, так как может спровоцировать выкидыш, мертворождение или вызвать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с токсоплазмозом, герпесом и краснухой принадлежит к числу инфекций, обследоваться на которые женщины должны еще на этапе планирования беременности.
К каким докторам следует обращаться если у Вас Цитомегаловирусная инфекция у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Цитомегаловирусной инфекции у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .

Цитомегаловирус (CMV, ЦМВ) — вирус герпеса человека 5 типа. Серопозитивность у взрослого населения в мире колеблется в пределах от 25 % до 90 %, оставаясь почти повсеместной в развивающихся странах. Источником инфекции является больной человек или носитель.
У большинства иммунокомпетентных взрослых ЦМВИ протекает бессимптомно или с минимальными проявлениями в виде повышения температуры, утомляемости и т. д. Иногда ЦМВИ может протекать в виде синдрома мононуклеоза, который клинически неотличим от такового, вызванного вирусом Эпштейна-Барр. Поражение ЦНС, обычно в виде энцефалита, встречается редко и является прерогативой иммунокомпроментированных больных, особенно ВИЧ-инфицированных.
Выделяют врожденную и приобретенную ЦМВ-инфекцию. Первую можно установить при выделении вируса методом ПЦР в любой биологической жидкости (некоторые источники рекомендуют проверять наличие ЦМВ в моче, так как ЦМВ может присутствовать в молоке инфицированной матери — а значит, и в слюне ребенка; в любом случае, при взятии слюны нужно выдержать час после грудного кормления) у ребенка возрастом до трех недель (или у плода); первичную приобретенную ЦМВИ подтверждает сероконверсия анти-CMV IgG (отрицательный результат в первой пробе, положительный — во второй); чтобы получить представление о давности инфицирования, определяют авидность (условно говоря, крепкость связи) anti-CMV-IgG антител к возбудителю — чем выше последняя, тем, вероятно, больше времени прошло с момента инфицирования. Присутствие CMV IgM не может использоваться само по себе для диагностики первичной инфекции ЦМВ, поскольку IgM может также присутствовать при вторичной CMV-инфекции. Положительные результаты IgM в сочетании с низким показателем авидности IgG считаются надежным доказательством первичной инфекции. Напомним, что положительные результаты серологических тестов у ребенка до года не подтверждают факта инфицирования, а лишь говорят о наличии материнских антител.
Напомним, цитотмегаловирус относится к группе TORCH-инфекций, а внутриутробное инфицирование ими может приводить к развитию врожденных пороков развития; причем, в связи с широкой иммунизацией против краснухи, ведущая роль в структуре вирусных инфекций, формирующих пороки, переходит к врожденной цитомегаловирусной инфекции.
При инфицировании в первом и втором триместрах ЦМВ может привести к развитию у плода пахигирии, полимикрогирии, корковой дисплазии и гетеротопии, а также к аномалиям желудочно-кишечного тракта, сердечно-сосудистой и бронхо-легочной систем.
У беременных с латентной ЦМВ-инфекцией плод поражается далеко не всегда. Первичное инфицирование при беременности представляет значительно больший риск инфицирования плода (30–50 %), чем реактивация инфекции (до 2 %). Поздняя фетопатия (при инфицировании беременной на третьем триместре) не предполагает пороков развития и проявляется внутриутробной задержкой развития, желтухой, гепатоспленомегалией, уменьшением числа тромбоцитов (иногда до 50×10 9 /л), тромбогеморрагическим синдромом и ретикулоцитозом. Увеличение печени и селезенки сохраняются иногда до года, тогда как геморрагический синдром и тромбоцитопения исчезают через 2–3 недели. Интенсивность желтухи нарастает в течение первых 2 недель и затем медленно, иногда волнообразно снижается на протяжении 2–6 месяцев. Помимо желтухи и увеличения печени отмечается повышение активности сывороточных ферментов — АЛТ, АСТ, щелочной фосфатазы. В биоптате печени можно обнаружить характерные цитомегалические клетки. На этом фоне возможны воспалительные поражения различных органов и систем: пневмонит, адренелит, гепатит, энцефалит, хориоретинит и т. д.
Энцефалит при врожденной цитомегаловирусной инфекции
Врожденная ЦМВИ протекает в виде генерализованной формы. Симптомы появляются в течении первых нескольких недель (до нескольких месяцев) после рождения. На первый план обычно выходят желтуха, петехиальная сыпь, гепатоспленомегалия, отставание в развитии, плохой аппетит. Поражение ЦНС проявляет себя гипотонией при сохранных или оживленных рефлексах, выбуханием родничка (следствие повышения ВЧД из-за гиперпродукции ликвора), гиперкинезами и судорожным синдромом разной степени выраженности — вплоть до генерализованных судорожных приступов, иногда сенсоневральной глухотой и хориоретинитом.
Лучевые признаки
- поражения локализуются главным образом в субэпендимарных областях: здесь чаще всего имеют место воспаление и некроз паренхимы мозга, а также пролиферативный эпендимит; желудочки мозга расширены;
- некротические очаги, кроме субэпендимарной локализации, могут находиться в веществе полушарий мозга (височные, теменные, затылочные доли), его стволе, мозжечке. Для ЦМВ-энцефалита характерно наличие выраженного геморрагического компонента: кровоизлияния под эпендиму желудочков, массивные кровоизлияния в очагах некроза, иногда субарахноидальные кровоизлияния;
- при хроническом течении энцефалита наряду с острыми воспалительными изменениями можно увидеть кальцификаты и очаги кистозно-глиозной трансформации; для этих изменений также характерна перивентрикулярная локализация;
- нередко ЦМВ-энцефалит ассоциируется с пороками развития в виде пахигирии, полимикрогирии, корковой дисплазии и гетеротопии.

Кроме выраженной вентрикуломегалии, определяются множественные кальцификаты (стрелки), расположенные перивентрикулярно.

Рисунок 2 | Некрупные кальцификаты (стрелки) базальных ядер с двух сторон у ребенка с ЦВИ-энцефалитом.

Двустороннее расширение боковых желудочков, гиперинтенсивный очаг белого вещества правой лобной области (головка стрелки) и диффузная пахигирия — извилины мозга в указанной области выглядят широкими и уплощенными.
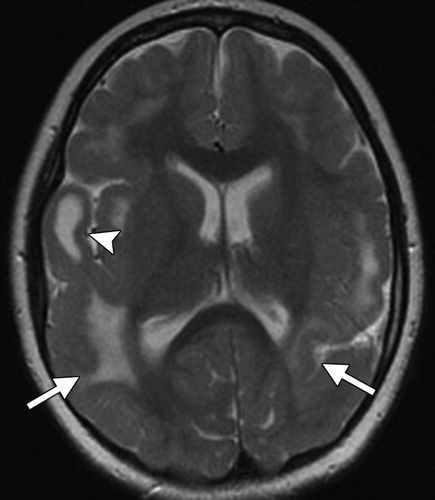
Видно множественные гиперинтенсивные субкортикально расположенные очаги воспаления паренхимы мозга (стрелки), а также участок кистозной трансформации в правой височной области (головка стрелки).
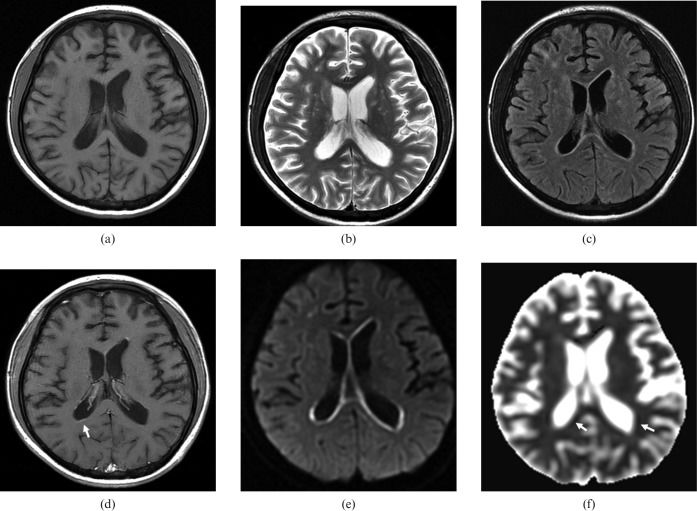
Т1ВИ (а): умеренная дилятация боковых желудочков;
Т2ВИ (b): небольшие округлые гиперинтенсивные очаги в области базальных ядер и субкортикальных отделов белого вещества правой лобной области;
FLAIR изображения (c) подтверждают наличие описанных очагов гиперинтенсивности;
на Т1ВИ после введения контрастного препарата (d) можно увидеть умеренное субэпендимальное контрастное усиление;
DWI и ACD (e,f) определили наличие субэпендимальных областей ограничения диффузии.

Вирусный энцефалит — это поражение паренхимы мозга вирусом, которое может сочетаться с воспалением мозговых оболочек (менингоэнцефалит) или с поражением спинного мозга (энцефаломиелит).
Лучевая диагностика критически важна в ведении пациентов с энцефалитом. Данные визуализационных методик помогают определить диагноз (и имеют особую ценность в ранней диагностике), обнаружить осложнения основного процесса (например, масс-эффект), предположить этиологию заболевания, отслеживать ответ на проведенную терапию и проводить динамическое наблюдение в случае перехода процесса в хроническую форму.
Энцефалит, вызванный герпесвирусами
В первую очередь подразумевается вызванный вирусом простого герпеса (ВПГ) герпетический энцефалит, однако позже мы поговорим в том числе и о цитомегаловирусном и варицелловирусном энцефалитах.
Серопревалентность (наличие антител) к вирусу простого герпеса первого и/или второго типов в разных странах мира оценивается в пределах 60–95 % у взрослых, однако энцефалит — редкий вариант инфекционного поражения ВПГ.
Попадание в ЦНС обеспечивает ретроаксональный путь передачи; данные, полученные с использованием экспериментальных моделей (кролики, мыши) показали возможность передачи по волокнам обонятельного пути. Считается также, что у взрослых ВПГ-1 энцефалиты вызываются реактивацией латентной инфекции в тройничном ганглии с распространением по ветвям V пары черепных нервов на оболочки передней и средней черепных ямок.
Герпетический энцефалит стал одним из первых инфекционных заболеваний, диагностируемых с использованием методов молекулярной биологии (ПЦР для обнаружения ДНК ВПГ в цереброспинальной жидкости) и одной из первых вирусных инфекций, в лечении которых была успешно применена противовирусная химиотерапия. В США ВПГ является наиболее распространенной причиной неэпидемического острого энцефалита.
Наиболее частые клинические признаки: высокая (более 38°С) температура, головная боль, дезориентация, афазия, угнетение сознания, судороги, нарушения поведения, тошнота и рвота.
Для данной патологии не характерна сезонность. Можно выделить два основных паттерна:
- герпетический энцефалит у детей и взрослых (чаще — ВПГ 1 типа);
- неонатальный герпетический энцефалит (в большинстве случаев обусловленный ВПГ 2 типа).
ВПГ-энцефалит у взрослых
Протекает с неспецифическими симптомами угнетения сознания, лихорадкой, головной болью и очаговой неврологической симптоматикой. Анализ ЦСЖ неспецифичен, часто удается выделить ДНК вируса методом ПЦР.
У иммунокомпетентных взрослых ВПГ обычно приводит к поражению:
- медиобазальных отделов полушарий: очаги некроза и кровоизлияний наблюдаются в височных областях, орбитальной поверхности лобных долей;
- островковых долей;
- могут поражаться также задние отделы затылочной коры;
- вовлечение теменных областей более характерно у детей, чем у взрослых;
- базальные ганглии обычно интактны (что при визуализации помогает дифференциировать энцефалит от ОНМК в бассейне средней мозговой артерии);
Иммуноскомпроментированные пациенты демонстрируют более диффузное поражение с распространением на стволовые структуры мозга.
Лучевые проявления
КТ
МРТ
Гораздо чувствительнее на ранней стадии как к непосредственным, так и к косвенным (отек мозга) признакам энцефалита.
Лучевые симптомы в разных МР-последовательностях:
Т1
- может демонстрировать неспецифические признаки отека в пораженном регионе в виде сглаженности извилин и признаков масс-эффекта;
- очаги острого/подострого кровоизлияния проявят себя областями повышенного сигнала.
Т2
DWI/ADC (ИКД)
- часто демонстрирует ограничение диффузии вследствие цитотоксического отека.
GRE/SWI

Рисунок 1 | Асимметричные области патологически повышенного МР сигнала в медиальных отделах обеих височных долей, больше выраженные в корковом веществе

Рисунок 2 | В последовательности DWI у того же пациента определяются области повышения сигнала в обоих лобно-височных областях. ИДК подтвердила ограничение диффузии

Т1-взвешенное корональное изображение после введения контраста демонстрирует асимметричное двустороннее гириформное и лептоменингальное контрастное усиление больше в области коры островка (большие стрелки) и поясной извилины (меньшая стрелка)
Неонатальный герпетический энцефалит
Как уже было сказано, чаще вызывается ВПГ 2 типа.
Развитие неонатального герпеса может происходить при контакте новорожденного с ВПГ в половых путях во время родов. Это заболевание является редким, составляя примерно 10 случаев на 100 000 деторождений в мире. Смертность при данной форме энцефалита достигает 50 %, также около 50 % выживших будут иметь тяжелые неврологические нарушения. Риск развития неонатального герпеса особенно высок, если первичное инфицирование матери ВПГ происходит на поздних сроках беременности. У женщин, перенесших генитальный герпес до беременности, риск передачи ВПГ детям крайне низок.
В клинической картине преобладают сонливость, лихорадка или гипотермия, судороги; менее частыми проявлениями являются апноэ, потеря веса, раздражительность, выпуклый передний родничок, везикулярная сыпь в области лба, фокальные клонические судороги конечностей.
Лучевые признаки
Герпетический энцефалит у младенцев характеризуется более диффузным поражением, причем эти изменения сложнее заметить на фоне незавершенной миелинизации; поражение типично затрагивает кору полушарий, глубокие слои белого вещества, включая перивентрикулярные области и таламусы. Медиальные области височных и нижние области лобных долей часто интактны. Геморрагии встречаются реже и появляются в более поздних стадиях.
КТ
- на ранней стадии изменения могут отсутствовать;
- в более поздних сроках определяются обширные зоны гиподенсивности (отвечающие отеку и/или некрозу) коры и белого вещества;
- при контрастировании чаще наблюдается гириформное контрастное усиление.
МРТ
Сигнальные характеристики аналогичны энцефалиту у взрослых:
В группе пациентов, у которых развился неонатальный герпетический энцефалит в течение 28 дней после рождения, основными признаками при использовании DWI-последовательности были кортикальные поражения. Двустороннее поражение глубоких слоев коры и белого вещества мозга, визуализируемые на 7-й день, были предикторами плохого прогноза и высокой вероятности развития двигательных и когнитивных расстройств.


Т1-взвешенная аксиальная томограмма: диффузная кистозная энцефаломаляция с компенсаторной вентрикуломегалией
Современные методики МРТ не ограничиваются классической томографией. Все чаще для диагностики герпетического энцефалита используется протонная МР-резонансная спектроскопия. Сообщается о снижении пика NAA (N-ацетиласпартата) по отношению к холину через 7–14 недель после первых симптомов заболевания; в некоторых случаях наблюдается повышенный пик холина. Иногда может быть повышен пик лактата. Считается, что уменьшение пика NAA отражает повреждение нейронов. Было отмечено, что восстановление нормальных значений NAA происходит одновременно с клинически значимым улучшением состояния пациента.
Диагностика приобретенной цитомегаловирусной инфекции ЦНС по МРТ
а) Терминология:
1. Сокращения:
• Цитомегаловирусная инфекция (ЦМВИ), цитомегаловирус (ЦМВ)
2. Определение:
• Приобретенное инфекционное поражение ЦНС: менингит, энцефалит, вентрикулит, ретинит, полирадикулопатия, миелит
• Первичная ЦМВИ: у здоровых взрослых обычно имеет бессимптомный характер
• Иммунокомпрометированные пациенты (СПИД, трансплантация органов) с повышенным риском → реактивация ранее латентной инфекции
б) Визуализация:
2. Рекомендации по визуализации:
• Лучший инструмент визуализации: МРТ с контрастным усилением
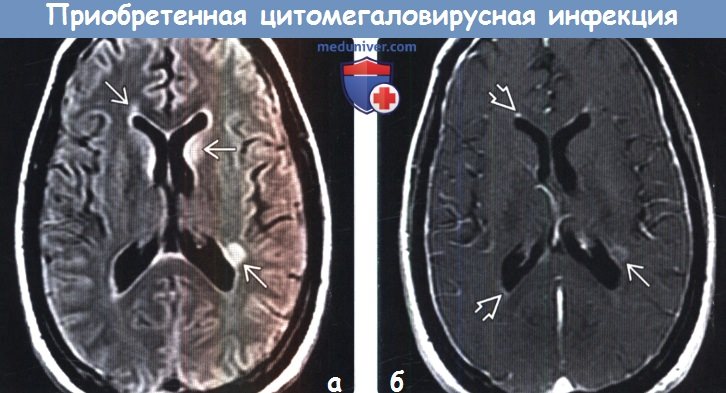
(а)МРТ, FLAIR, аксиальный срез: определяются легкая вентрикуломегалия и перивентрику-лярные очаги гиперинтенсивного сигнала, что обусловлено вентрикуло-энцефалитом.
(б) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у этого же пациента определяется контрастирование эпендимы и перивентри-кулярных очагов. У данного пациента был иммунодефицит, вентрикулит в сочетании с энцефалитом. ЦМВ-энцефалит обычно представляет собой вентрикуло-энцефалит с вовлечением перивентрикулярного белого вещества. Однако ЦМВ также может вызывать появление геморрагических или некротических поражений.
3. МРТ признаки приобретенной цитомегаловирусной инфекции (ЦМВИ):
• Т1-ВИ:
о Энцефалит: зона гипоинтенсивного сигнала с нечеткими контурами
о Вентрикулит: расширение желудочков с уровнем детрита
• Т2-ВИ:
о Энцефалит: неотчетливое перивентрикулярное повышение интенсивности сигнала
о Вентрикулит: расширение желудочков с повышением интенсивности сигнала вокруг них
• FLAIR:
о Энцефалит: неотчетливое перивентрикулярное повышение интенсивности сигнала
о Вентрикулит: расширение желудочков с повышением интенсивности сигнала вокруг них
о Возможно неспецифическое, мультифокальное, перивентрикулярное повышение интенсивности сигнала от БВ
• Постконтрастные Т1-ВИ:
о Энцефалит: обычно существенного контрастного усиления не наблюдается:
- При контрастировании возможно выявление некротического компонента
о Вентрикулит: эпендимальное и перивентрикулярное контрастное усиление
• MPT-спектроскопия: некротический энцефалит может характеризоваться ↑ холина, лактата и ↓ NAA
• ПВИ: более низкие значения rCBV, чем в опухоли
в) Дифференциальная диагностика:
1. ВИЧ-энцефалит:
• Перивентрикулярные фрагментарные участки гиперинтенсивного на Т2-ВИ сигнала в сочетании с атрофическими изменениями мозговой ткани; контрастное усиление отсутствует
2. ПМЛ:
• Гиперинтенсивные на Т2-ВИ поражения БВ с вовлечением субкортикальных U-волокон; часто поражаются лобные/теменно-затылочные области
• Субкортикальные U-волокна > перивентрикулярное БВ > серое вещество
3. Токсоплазмоз:
• Множественные поражения с кольцевым характером накопления контраста
• Глубокие ядра и большие полушария головного мозга
4. ОДЭМ:
• Перивентрикулярные фрагментарные участки гиперинтенсивного на Т2-ВИ сигнала, накапливающие контраст; 10-14 дней после инфекции/вакцинации
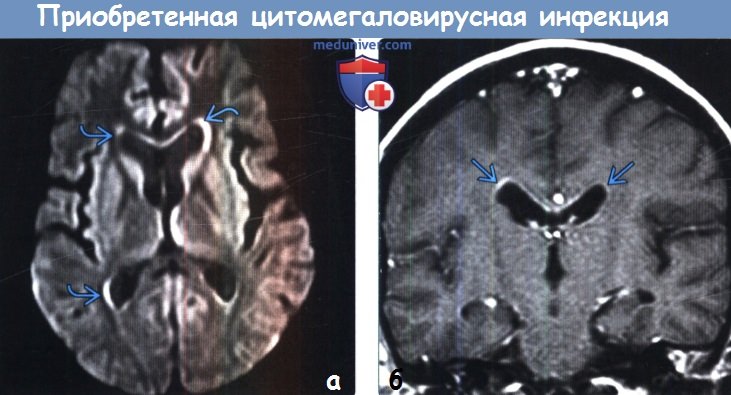
(а) МРТ, ДВИ, аксиальный срез: у 35- летнего ВИЧ-положительного пациента с очень низким числом CD4(+) клеток по ходу стенок боковых желудочков определяется тонкий гиперинтенсивный ободок. Кроме того, наблюдается легкое расширение желудочков и легкая атрофия коры.
(б) МРТ, постконтрастное Т1-ВИ, корональный срез: у того же пациента определяется слабовыраженное контрастирование эпендимы лобных рогов боковых желудочков. Данные изменения характерны для ЦМВ-вентрикулита.
г) Патология:
1. Общие характеристики приобретенной цитомегаловирусной инфекции (ЦМВИ):
• Этиология:
о Подавляющее большинство взрослых заражены ЦМВ
о Передача ЦМВ происходит преимущественно при контакте с инфицированными выделениями
о Поражение ЦНС происходит в основном у иммунокомпрометированных лиц:
- Вирус достигает головного мозга гематогенным путем
• Ассоциированные аномалии:
о Реактивация ВГЧ-6, связанная с ЦМВ-инфекцией у пациентов после трансплантации печени
о ЦМВ может вызывать трансактивацию вируса JC
д) Клиническая картина приобретенной цитомегаловирусной инфекции (ЦМВИ):
1. Проявления:
• Наиболее частые признаки/симптомы:
о ЦМВ-энцефалит: спутанность сознания, нарушение походки, невропатия черепных нервов, гиперрефлексия
2. Демография:
• Эпидемиология:
о Большинство детей заражаются ЦМВ в раннем возрасте, серопревалентность у взрослых приближается к 100%
о ЦМВ распространяется в ЦНС на поздних стадиях ВИЧ-инфекции, при низком количестве CD4(+) клеток
о До появления высокоактивной антиретровирусной терапии (ВА-АРТ) при ВИЧ цитомегаловирусный ретинит являлся наиболее частой причиной слепоты при СПИД (> 90%)
3. Течение и прогноз:
• Первичная инфекция обычно протекает бессимптомно; острое лихорадочное заболевание встречаются редко и называется цитомегаловирусный мононуклеоз
• Заражение может произойти вследствие реактивации латентной вирусной инфекции или инфекции, недавно приобретенной в результате трансплантации органа или костного мозга от серопозитивного донора
4. Лечение:
• Ганцикловир и другие противовирусные препараты при высокой степени тяжести заболевания
• ВААРТ: ↓ заболеваемости ЦМВ при СПИД
е) Список литературы:
1. Bilgrami М et al: Neurologic diseases in HIV-infected patients. Handb Clin Neurol. 121:1321-44, 2014
Читайте также:

