Что такое хромосомы и паразиты
Обновлено: 18.04.2024
Строение хромосом человека. Особенности организации
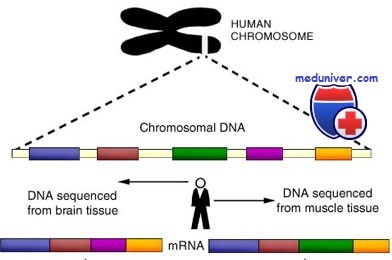
Все гены в геноме человека, а также детерминанты их экспрессии организованы в 46 хромосом, расположенных в ядре, плюс митохондриальная хромосома. Каждая хромосома состоит из единственной двойной спирали непрерывной ДНК; т.е. каждая хромосома в ядре — длинная, линейная спиральная двойная молекула ДНК, и ядерный геном состоит, следовательно, из 46 молекул, включающих более чем 6 млрд нуклеотидов.
Хромосомы, тем не менее, не просто двойная спираль ДНК. В каждой клетке геном упакован в виде хроматина, в котором ДНК объединена с несколькими классами хромосомных белков. За исключением фазы деления клетки, хроматин распределен по всему ядру и под микроскопом представляется сравнительно гомогенным. Когда клетка приступает к делению, геном конденсируется и появляются видимые под микроскопом хромосомы. Хромосомы, таким образом, видны как дискретные структуры только в ходе деления клеток, хотя они сохраняют свою целостность и между делениями.
В хромосоме молекула ДНК существует в виде хроматина, в комплексе с семейством основных хромосомных белков, называемых гистонами, и с разнородной группой негистоновых белков, значительно хуже охарактеризованных, но, как установлено, определяющих соответствующие условия для нормального поведения хромосом и влияющих на экспрессию генов.
В упаковке хроматина важнейшую роль играют пять основных типов гистонов. По две копии каждого из четырех основных гистонов — Н2А, Н2В, НЗ и Н4 — составляют октамер, вокруг которого, подобно нити вокруг катушки, обматывается сегмент двойной спирали ДНК. Вокруг каждого октамера гистоновых белков ДНК делает два оборота, что составляет приблизительно 140 пар оснований. После короткого (20-60 пар оснований) промежуточного участка ДНК вновь формируется виток и так далее, что придает хроматину вид бусинок, нанизанных на нитку.
Каждый комплекс ДНК с основными гистонами называется нуклеосомой, представляющей основную структурную единицу хроматина, и каждая из 46 хромосом человека содержит от нескольких сот тысяч до более миллиона нуклеосом. Пятый гистон, HI, как установлено, связывается с ДНК в ребре каждой нуклеосомы, в области межнуклеосомного промежутка. Объем ДНК, связываемой с нуклеосомой вместе с промежуточной областью, — почти 200 пар оснований.
Дополнительно к основным типам гистоновых белков множество специализированных гистонов могут заменять Н3 и Н2А, придавая при этом геномной ДНК специфические характеристики. Гистоны НЗ и Н4 также могут модифицироваться в закодированные белки. Эти так называемые посттрансляционные модификации могут изменять свойства нуклеосом. Набор основных и специализированных гистоновых белков и их модификаций часто называют гистоновым кодом, который может изменяться в разных типах клеток, вследствие чего полагают, что он определяет характер упаковки ДНК и доступность ее для регулирующих факторов, определяющих экспрессию генов или другие функции генома.
В течение клеточного цикла хромосомы проходят через последовательность конденсаций и деконденсаций. Тем не менее даже когда хромосомы находятся в наиболее деконденсированном состоянии, на этапе клеточного цикла, называемом интерфазой, ДНК упакована в хроматине в значительно большей степени, чем свободная от белков двойная спираль. Более того, длинные цепочки нуклеосом самоорганизуются во вторичную спиральную структуру хроматина, которая проявляется под электронным микроскопом как толстое волокно диаметром 30 нм, что почти в три раза толще, чем диаметр нуклеосом.
Огромный объем геномной ДНК, упакованной в хромосоме, можно оценить после специальной обработки хромосомы для того, чтобы освободить ДНК от белковой основы. При этом могут быть визуализированы длинные петли ДНК, а остатки белкового матрикса могут воспроизводить контуры типичной хромосомы.
Митохондриальная хромосома
Как упоминалось ранее, небольшое, но важное подмножество генов генома человека находится в цитоплазме в митохондриях. Митохондриальные гены наследуются строго по материнской линии. Клетки человека могут иметь сотни тысяч митохондрий, каждая из которых содержит множество копий небольшой циклической молекулы, митохондриальной хромосомы. Митохондриальная молекула ДНК всего 16 килобаз длиной (менее чем 0,03% длины наименьшей ядерной хромосомы!) и кодирует только 37 генов. Продукты этих генов функционируют в митохондриях, хотя большинство белков в митохондрии — фактически продукты ядерных генов.
Возможность мутаций в генах митохондрий продемонстрирована при нескольких заболеваниях с материнским типом наследования, а также как спорадическое нарушение.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Как происходит заражение?
До попадания в организм человека, гельминты и простейшие проходят цикл развития в других средах или живых организмах.
- В почве при определённых условиях температуры и влажности сохраняются яйца и личинки аскарид, стронгилоид, анкилостом Человек заражается при попадании зараженной почвы через грязные руки, воду, непромытые фрукты и овощи, непосредственно с землёй.
- В живых организмах проходят циклы развития следующие гельминты: описторхи (кошачья двуустка), клонорхи, трихинеллы, токсокары, эхинококки, свиной и бычий цепень. До достижения зрелости, чтобы паразитировать в человеке, возможна смена одного или двух промежуточных хозяев. Это моллюски, ракообразные, рыба, насекомые. Употребление термически недостаточно обработанной рыбы и мяса, сырой воды приводит к заражению.
Ещё один путь заражения - при непосредственном контакте людей через рукопожатия, общие предметы гигиены и быта или путем самозаражения. Речь идёт о контагиозных гельминтах: энтеробиоз, стронгилоидоз, цистицеркоз, лямблиоз.
Как можно заподозрить паразитарное заболевание?
Проявления могут быть разнообразными, течение от легкого до тяжёлого. Редко возникают типичные признаки, выдающие конкретного возбудителя. Зачастую признаков нет, или они маскируются под другие заболевания, или исчезают по мере окончания одного цикла развития паразита и начала другого. Например, личинки аскарид сначала попадают в лёгкие человека, где дозревают и мигрируют в кишечник. Ребёнка может беспокоить недолгий кашель (похоже на простуду), не настораживающий родителя.
Тем не менее, обычно выделяют острую и хроническую фазы течения паразитарного заболевания.
Острые проявления возникают вследствие общего воздействия на организм:
- Влияния токсинов – повышение температуры до 37 – 37,5 градусов, слабость, головные боли, снижение настроения и работоспособности, нарушения сна;
- Аллергических реакций – кожный зуд, крапивница, бронхоспазм, одышка, реже отёк Квинке;
- Активации иммунной системы– боли в мышцах и суставах; увеличение лимфоузлов, печени и селезенки
- Механического воздействия – если посмотреть под микроскопом, у каждого гельминта можно увидеть приспособления для закрепления в организме, травмирующие слизистую: зубья, крючья, присоски. В результате возникают боли в животе, частый стул, диспепсия.
Хроническая фаза характеризуется поражением определённых органов и систем. Чаще всего страдает кишечник, длительное механическое воздействие приводит к его воспалению, нарушениям всасывания и переваривания пищи. Развивается анемия, недостаток витаминов и микроэлементов, а у маленьких детей отмечается задержка роста и набора веса. Могут поражаться желчный пузырь и желчевыводящие пути (лямблиоз); сердечно-сосудистая система, лёгкие, нервная система (чаще трихинеллез); лёгкие и печень (эхинококкоз) и так далее. При длительном течении подавляется иммунитет и присоединяются вторичные инфекции.
Если Вы обнаружили любой из перечисленных признаков, сдайте клинический анализ крови с лейкоцитарной формулой. Повышение эозинофилов до 7-10% и более станет ещё одним подозрительным критерием.
Как выявить паразитарное заболевание?
-
, предпочтительнее обогащающий метод – PARASEP Определяет яйца всех видов гельминтов и простейших, обитающих в кишечнике
Следует обратить внимание на следующие моменты:
На что нужно обратить внимание?
- Наличие проявлений и одновременное обнаружение IgG могут свидетельствовать о хронической фазе гельминтоза
- В сомнительных случаях рекомендовано повторное исследование IgG через 2 недели. Нарастание уровня антител в 2 раза и более говорит об активности гельминта
- При трихинеллезе, эхинококкозе, цистицеркозе определение антител – единственный возможный метод лабораторной диагностики, поскольку человек – промежуточный хозяин для данных гельминтов.
Все же кое-какие закономерности ученым удалось выявить, несмотря на то что эта область науки постоянно преподносит новые сюрпризы
Я вся такая. внезапная, такая противоречивая!

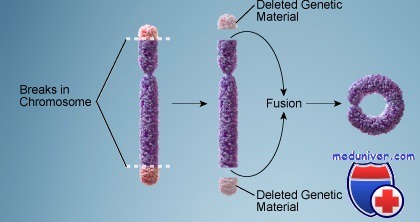
История теломерной биологии началась в 1930-е гг., когда Г. Мюллер и Б. Мак-Клинток описали теломеры как особые структуры хромосом, не позволяющие им слипаться друг с другом. Понятно, что во времена, когда еще не знали, как закодирована наследственная информация в клетке, установить природу теломер было невозможно. Период активного изучения теломер начался в 1980-х гг. и увенчался Нобелевской премией 2009 г. (Зверева и др., 2010).
Первым организмом, у которого определили последовательность нуклеотидов теломерной ДНК, была инфузория тетрахимена (Блекберн, 1978). Оказалось, что теломерная ДНК этого простейшего состоит из шести нуклеотидов TTGGGG, повторяющихся четыре-пять раз – такие структуры называют короткими повторами (мини- и микросателлитами). Затем структуру теломерных районов определили у других организмов из разных таксономических групп. Оказалось, что у большинства позвоночных это короткий повтор TTAGGG, у членистоногих (Arthropoda) – TTAGG, у круглых червей (Nematoda) – TTAGGC, у растений – TTTAGGG.
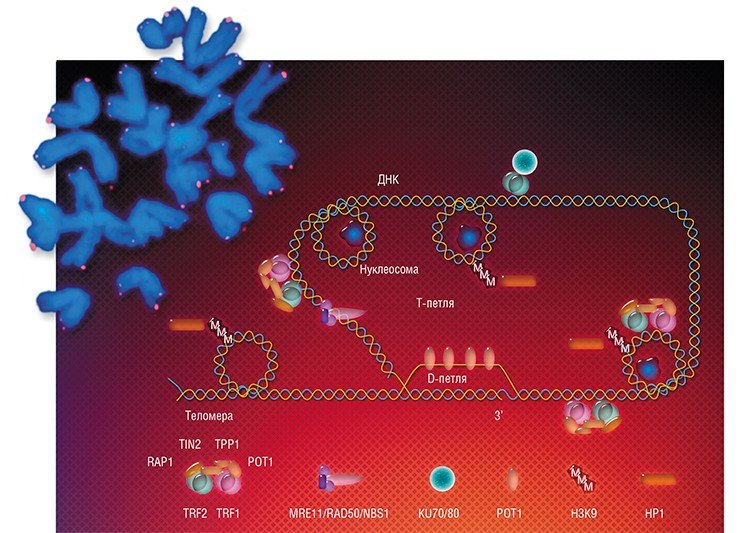
На путанице в названиях дело не закончилось. Достаточно обескураживающим открытием стало то, что не у всех организмов теломеры состоят из микросателлитов. Прежде считалось, что только короткие повторы ДНК консервативной структуры могут защищать концы хромосом, но у двукрылых насекомых и некоторых растений были выявлены теломерные структуры, значительно отличающиеся от типичных коротких повторов.
Так, у комаров рода Chironomus и Anopheles в роли теломер выступает сателлитная ДНК, представляющая собой повторы из нескольких сотен пар нуклеотидов, которые образуют теломерные области в несколько сотен тысяч пар нуклеотидов. У дрозофилы теломеры состоят из перемещающихся по геному мобильных элементов – ретротранспозонов HeT-A, TART и TAHRE. Один из них, TART, был также обнаружен на концах хромосом мухи Rhinchosciara americana. Возможно, нетипичные теломеры характерны для всех представителей многочисленного (более 150 тыс. видов) отряда двукрылых насекомых. Среди растений нетипичные теломеры найдены у некоторых видов подсемейств Alliaceae (луковые), Asphodelaceae (асфоделовые) и семейства Solonaceae (пасленовые): на концах их хромосом локализуются последовательности рибосомальной или сателлитной ДНК.
Более того, существуют промежуточные типы теломер: например, у тутового шелкопряда Bombyx mori теломерная ДНК состоит как из повторов TTAGG, так и из ретротранспозонов TRAS и SART – это говорит об эволюционной связи разных теломерных структур. У некоторых организмов определить структуру теломерных регионов пока не удалось: это тихоходки и поденки среди животных и, например, ульвовые и красные водоросли среди низших растений. Так что, возможно, существуют и другие варианты структуры теломерных районов.
Не только по структуре, но и по длине теломерные участки очень вариабельны. Размер теломер может отличаться на разных плечах одной хромосомы, у гомологичных и негомологичных хромосом, в разных клетках, тканях, органах, у близнецов, у разных индивидов, принадлежащих одному виду, у разных видов. С чем такая изменяемость связана и каково ее функциональное значение, до сих пор не понятно. При этом в исследованиях вариабельность обычно не учитывают, используя в анализе средние значения размера теломер, который определяют, расщепив ДНК изучаемой ткани ферментами рестриктазами, не трогающими теломерную ДНК. Оставшуюся ДНК метят, визуализируют и с помощью специального прибора определяют длину фрагмента самой многочисленной фракции – это и будет средний размер теломер.
Длина теломер всегда вызывала и продолжает вызывать много вопросов. Почему у слона она составляет всего 14 тыс. пар нуклеотидов, а у некоторых линий лабораторных мышей – в 10 раз больше? Есть ли какая-нибудь связь с размером тела? С продолжительностью жизни? С приспособленностью к меняющимся условиям окружающей среды? С болезнями? С наследственностью? Со скоростью старения? Это лишь небольшой перечень вопросов, возникающих в отношении размера теломер, правда на некоторые из них ученые уже нашли ответы.
Размер теломер, размер тела и продолжительность жизни – есть ли связь?
Как уже упоминалось выше, существует теория старения, согласно которой этот процесс происходит вследствие укорачивания теломер с возрастом из-за их неполного копирования в процессе удвоения ДНК. Теломеры называли (а некоторые до сих пор называют) митотическими часами клеток, хронометрами, счетчиками клеточных делений, потому что у человека в клетках тела они укорачиваются с возрастом. Рождается человек с длиной теломер 15—20 тыс. пар нуклеотидов, а умирает с длиной 5—7 тыс. Сейчас известно, что зависимость размера теломер от возрастных изменений не универсальна, длина теломерной ДНК у разных организмов (а иногда и у одного и того же организма) может со временем не только уменьшаться, но и расти, а у многих организмов такой зависимости вообще нет.

Какие теломеры считать длинными, а какие не очень? Все известные значения размеров теломер условно можно разделить на четыре группы. Очень короткие – десятки пар нуклеотидов, характерные для большинства простейших; короткие – меньше 20 тыс. пар нуклеотидов; длинные – больше 20 и меньше 100 тыс. пар нуклеотидов; экстрадлинные, или мегателомеры, – больше 100 тыс. пар нуклеотидов
Но все же объяснить различия в длине теломер у разных организмов разной продолжительностью их жизни – красиво и логично. Может быть, долгожители имеют необычайно длинные теломеры? К сожалению, по пальцам одной руки можно пересчитать организмы-долгожители с длинными теломерами. Это некоторые виды долгоживущих (сто и больше лет) черепах с теломерами длиной 50—60 тыс. пар нуклеотидов, аллигаторы, живущие больше полувека с теломерами размером около 30 тыс. пар нуклеотидов. Но у большинства других долгоживущих организмов теломеры довольно скромного размера. Например, у деревьев-долгожителей (более тысячи лет) сосны Pinus longaeva и гинкго Ginkgo biloba длина теломер составляет, соответственно, около 13 и 5 тыс. пар нуклеотидов. То есть длина теломер и продолжительность жизни не имеют явной связи. Другой вопрос, что эти организмы имеют активный механизм поддержания теломерных районов – фермент теломеразу, способную удлинять спонтанно укорачивающиеся при делении клетки теломерные участки ДНК, но это совсем другая история.

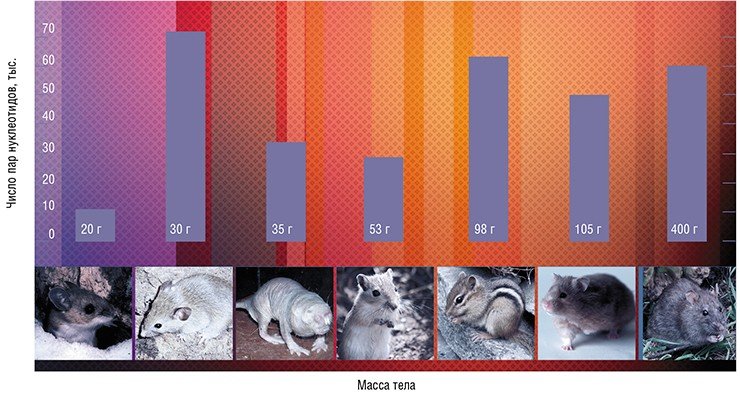
Больше повезло ученым, которые искали связь между размером теломер и размером организма. Сначала некоторая зависимость была обнаружена у грызунов: оказалось, что большинство крупных видов имеет короткие теломерные районы (10—18 тыс. пар нуклеотидов), а теломеры небольших грызунов могут достигать 72 тыс. пар (Seluanov et al., 2007). Возникла гипотеза, что эти данные отражают имеющийся у крупных организмов механизм защиты от рака в виде репликативного старения, когда клетки теряют способность делиться. Ведь чем больше в организме клеток, тем больше риск, что какая-то из них переродится в раковую. Тогда все логично: теломерная ДНК должна иметь достаточно небольшую длину, чтобы при постепенном укорочении вовремя запустилось репликативное старение, при этом теломераза, которая может поддерживать длину теломер (как в нормальных клетках, так и в раковых) должна быть неактивна.
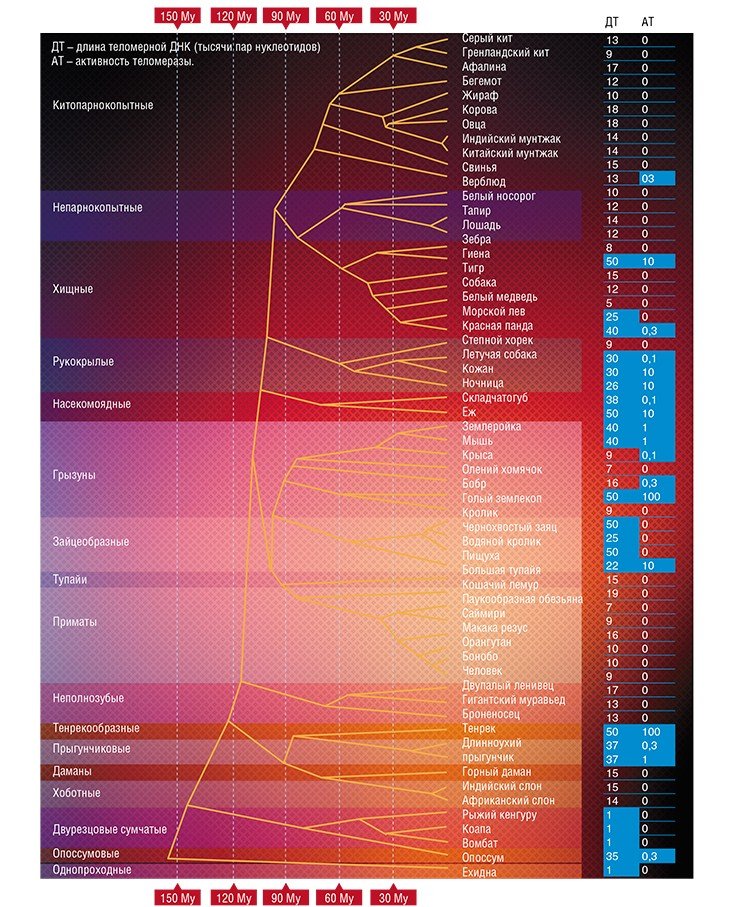
Исследования на других видах млекопитающих частично подтвердили данные, полученные на грызунах: длина теломерной ДНК действительно имеет отрицательную корреляцию с продолжительностью жизни и массой тела, и массивные животные с короткими теломерами не имеют активной теломеразы. Возможно, репрессия теломеразы и наличие более коротких теломер у крупных животных могут быть адаптацией к теплокровности, так как с увеличением температуры тела увеличивается частота мутаций и, следовательно, вероятность возникновения рака (Gomes et al., 2011). У небольших млекопитающих репликативного старения, видимо, нет, а физиологические процессы регулируются иным образом.
Конечно, предложенные объяснения имеют гипотетический характер, они не могут быть универсальными. Подтверждением этому служит, например, исследование длины теломер у байкальских планарий и моллюсков, при котором была обнаружена противоположная картина: более крупные животные имели более длинные теломеры, хотя не без исключений из правила.
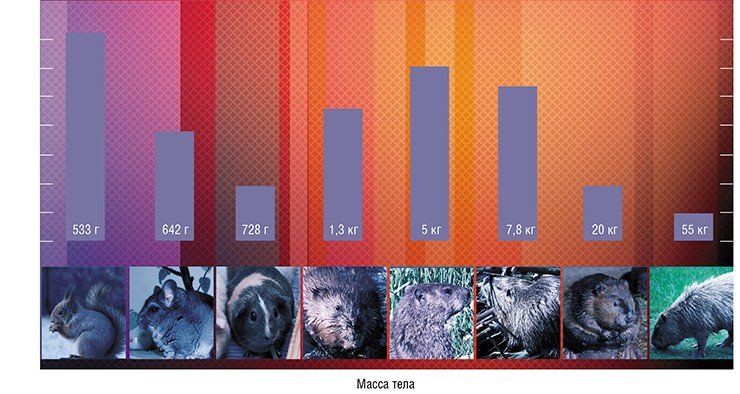
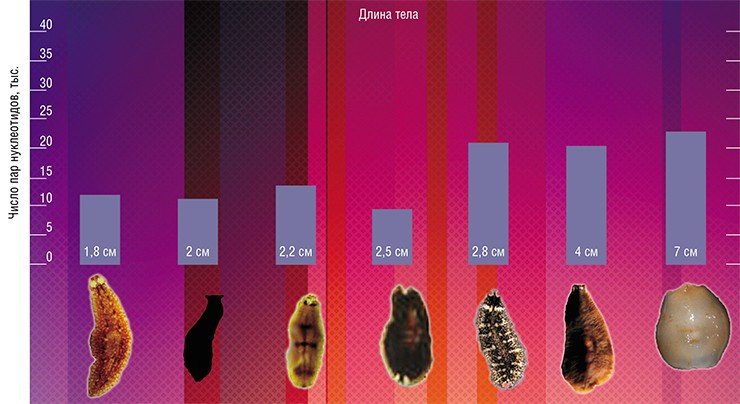
Наша работа в ЛИН СО РАН посвящена исследованию изменения длины теломерной ДНК и активности теломеразы у двух групп байкальских гидробионтов – планарий (плоских червей) и моллюсков. Эти организмы обитают в одинаковых условиях и подвергаются влиянию сходных факторов среды, демонстрируя такие свойственные байкальской фауне явления, как гигантизм и карликовость. Они имеют разную продолжительность жизни, которую у моллюсков, в отличие от планарий, можно точно определить, и различные стратегии выживания.
Анализ динамики теломерной ДНК с учетом особенностей этих животных поможет оценить влияние на нее внешних и внутренних факторов. По предварительным данным, во-первых, более крупные виды имеют более длинную теломерную ДНК. Во-вторых, длина теломерной ДНК с возрастом у разных видов животных меняется по-разному: у одних она увеличивается, а у других – уменьшается.
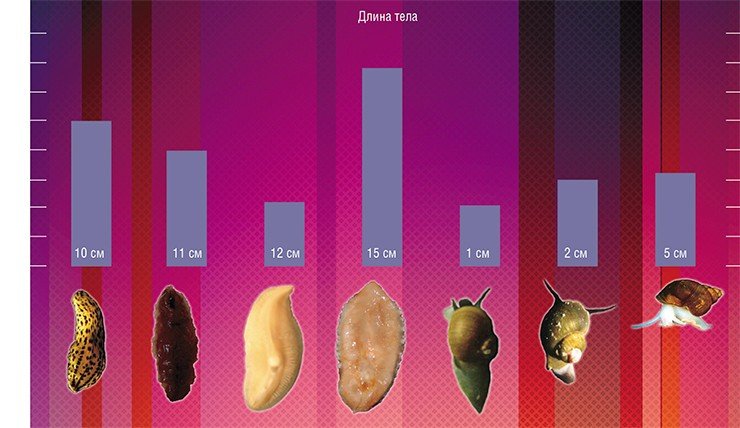
Такая видовая специфичность размера и динамики теломерной ДНК может иметь как адаптивный характер, так и наследственный, определяемый филогенетическим родством. А исследование активности теломеразы, которое тоже планируется осуществить, может пролить свет на внутреннюю причину различий в возрастной динамике теломерной ДНК у разных видов
Нет сомнений, что теломеры вовлечены во многие процессы в клетке, поэтому так трудно найти закономерность в распределении их размеров, и тем более предложить теорию, которая бы обладала предсказательными свойствами. Пока остается лишь перечислять те взаимосвязи, которые все же удалось обнаружить в разных исследованиях.
Одно из таких открытий относится к экстрадлинным (до 1 млн пар нуклеотидов) теломерным районам, которые были обнаружены у некоторых видов птиц. В кариотипах у них присутствуют микрохромосомы, и, возможно, такие аномально длинные теломеры нужны для их стабилизации.
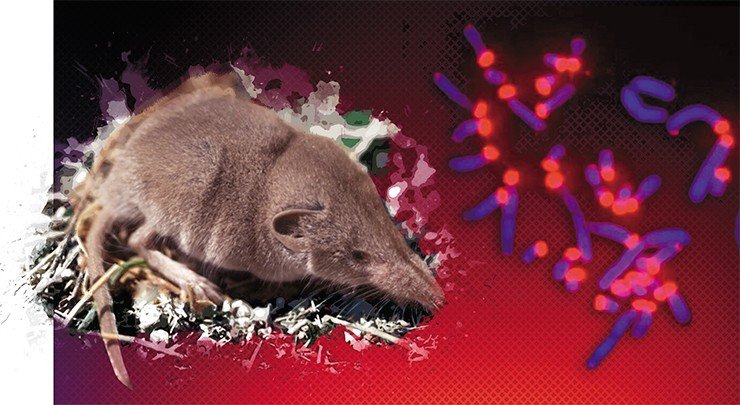
Выше мы затронули лишь некоторые возможные варианты объяснений изменчивости размеров теломер и роли их длины в жизни организма, не коснувшись внутривидовых отличий, связанных с полом, репродуктивным успехом, условиями обитания, образом жизни и т. п. Но даже то, что уже сказано, дает представление о всей сложности и многогранности этой актуальной области биологии.
Зверева М., Рубцова М. Нобелевская премия по физиологии и медицине 2009 года. Счетчик клеточного времени // Наука и жизнь. 2010. № 1. С. 2—5.
Bombarova M., Vitkova M., Spakulova M. et al. Telomere analysis of platyhelminths and acanthocephalans by FISH and Southern hybridization // Genomes. 2009. V. 52. P. 897—903.
Fulneckova J., Sevcikova, Fajkus J. et al. A broad phylogenetic survey unveils the diversity and evolution of telomeres in eukaryotes // Genome Biol. Evol. 2013. V. 5, N. 3. P. 468—483.
Gomes N., Ryder O., Houck M. et al. Comparative biology of mammalian telomeres: hypotheses on ancestral states and the roles of telomeres in longevity determination // Aging Cell. 2011. V. 10. P. 761—768.
Seluanov A., Chen Z., Hine C. et al. Telomerase activity coevolves with body mass, not lifespan // Aging Cell. 2007. V. 6(1). P. 45—52.
Zellinger B., Riha K. Composition of plant telomeres // Biochim. et Biophys. Acta. 2007. N 1769 (5–6). P. 399—409.
Zhdanova N., Minina J., Karamisheva T. et al. The very long telomeres in Sorex granarius (Soricidae, Eulipothyphla) contain ribosomal DNA // Chromosome Res. 2007. V. 15. P. 881—890

Согласно данным ВОЗ, ежегодно каждый второй человек на планете заражается гельминтами. Многие думают, что паразитические черви не наносят особого вреда здоровью. Однако не все так просто: гельминты способны поражать важные внутренние органы: сердце, легкие, головной мозг.
Гельминты — кто они?
Гельми́нты — паразитические черви, которые в качестве хозяина могут выбирать организм человека, животного, растения. Всего существует три класса гельминтов:
- ленточные черви. Данный класс насчитывает около 3,5 тыс. видов гельминтов. Длина паразитических червей варьируется от нескольких мм до 10-15 метров;
- сосальщики. Паразиты получили такое названия за счет наличия у них присосок, при помощи которых они получают питательные вещества. Человеческий организм может поражать около 4 десятков видов сосальщиков. Как правило, длина червей не превышает 5 см;
- круглые черви. Этот класс гельминтов насчитывает более 24 тыс. видов. Круглые черви имеют веретенообразную форму. Обычно их длина составляет не более 0,5 метра.
Заразиться гельминтами можно различными путями. Однако чаще всего паразитарная инвазия происходит по следующим причинам:
- Несоблюдение гигиены рук.
- Немытые овощи, фрукты; недожаренные или недоваренные мясо, рыба — употребление таких продуктов увеличивает риск паразитарной инвазии многократно.
- Хранение продуктов вне холодильника открытыми. Насекомые способны переносить яйца гельминтов на продукты, которые хранятся без упаковки.
- Контакт с домашними животными.
Основные симптомы наличия паразитов в организме:
- тошнота, рвота, диарея;
- снижение веса;
- аллергические высыпания;
- вздутие живота;
- зуд в заднем проходе;
- скрип зубами во сне.
Более подробно о признаках наличия паразитов в организме читайте в нашей статье.
Какие гельминты чаще всего встречаются в России? Рассмотрим самые распространенные виды паразитарных червей и заболевания, которые они вызывают.
Ленточные черви
Тело ленточного червя состоит из членников, общее число которых колеблется от 3 до 5000. Главный элемент фиксации гельминта — головка, дополнительные — присоски, крючья.
Наиболее часто ленточные черви становятся причиной следующих заболеваний:
Дифиллоботриоз
Возбудитель заболевания — лентец широкий, который поражает кишечник человека. Развитие яиц червя происходит в пресных водоемах. Схема попадания лентеца в человеческий организм выглядит следующим образом:
- Яйца червя заглатывают рачки, которые обитают в водоеме.
- Зараженных рачков поедают рыбы.
- Человек заражается паразитом, употребляя рыбу, прошедшую недостаточную тепловую обработку.
Симптоматика заболевания развивается через 1,5 месяца после заражения. Основной признак патологии — наличие в кале белесых фрагментов гельминта.
Прикрепляясь к слизистой кишечника, лентец поглощает в большом количестве витамин В12. По этой причине у людей с дифиллоботриозом часто развивается анемия. Кроме этого, лентец может вызывать увеличение печени, селезенки, непроходимость кишечника.
Тениаринхоз
Возбудитель заболевания — бычий цепень, который преимущественно обитает в тонкой кишке человека. За свой цикл развития гельминт сменяет двух хозяев: промежуточным является крупный рогатый скот, основным — человек. Бычий цепень может в течение 20 лет обитать в организме, размножаясь и нанося вред здоровью. Болезнь распространена во многих регионах РФ, однако чаще всего встречается в районах Северного Кавказа.
Как правило, люди заболевают тениаринхозом после употребления недожаренной или недоваренной говядины.
Болезнь часто протекает без выраженных симптомов и выявляется случайно, когда человек видит в своем кале элементы гельминта. У некоторых людей, кроме основных признаков заражения гельминтами, может возникать болевой синдром в правой части передней брюшной стенки.
Взрослые гельминты способны проникать в аппендикс, проток поджелудочной железы, желчевыводящие пути, провоцируя в них острые воспалительные процессы. При множественной паразитарной инвазии может развиться непроходимость кишечника.

Тениоз
Возбудитель заболевания — свиной цепень, который первоначально поражает тонкую кишку человека. В РФ наибольший рост заболеваемости среди населения наблюдается в районах, где распространено свиноводство. Это регионы, которые граничат с Украиной и Республикой Беларусь. Инфицирование человека происходит в результате потребления сырой или приготовленной ненадлежащим образом свинины.
Паразит может проникать в различные органы и ткани, вызывая болевой синдром в животе, спине, конечностях. Наиболее благоприятно патология протекает при локализации червя в подкожно-жировой клетчатке и скелетной мышечной ткани. При проникновении в глазные мышцы гельминты вызывают снижение остроты зрения, слезотечение, светобоязнь. Поражение свиным цепнем головного мозга может закончиться летальным исходом.
Сосальщики
Сосальщики имеют листовидную форму и отличаются высокой способностью к размножению в различные периоды жизненного цикла. Размножение червей возможно не только половым путем с оплодотворением, но и без него. Кроме присосок, черви имеют множество крючков и шипов, за счет которых они надежно прикрепляются к слизистым оболочкам органов.
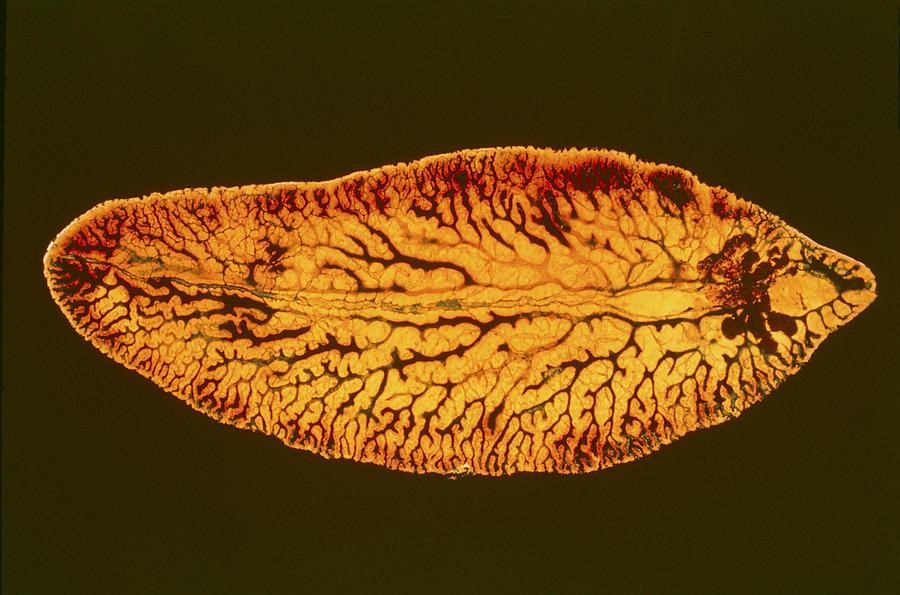
Распространенные патологии, вызываемые сосальщиками:
- фасциолез;
- описторхоз;
- парагонимоз.
Фасциолез
Фасциолез возникает при поражении печени или желчного пузыря печеночным сосальщиком. В основном заражение происходит при употреблении овощей, для полива которых использовали воду из открытых водоемов.
Кроме стандартных признаков заражения паразитами, у человека могут возникать астматические приступы, которые сопровождаются затрудненным дыханием, покраснением лица, расширением зрачков, тахикардией. Если взрослая особь вызвала непроходимость желчевыводящих протоков, то развивается механическая желтуха. Признаки патологии:
- схваткообразные боли в правом подреберье;
- пожелтение кожных покровов;
- лихорадка;
- бесцветные фекалии.
Описторхоз
Возбудитель болезни — кошачий сосальщик. Название паразита обусловлено тем, что кроме человека он часто поражает кошек и других млекопитающих, которые употребляют рыбу.
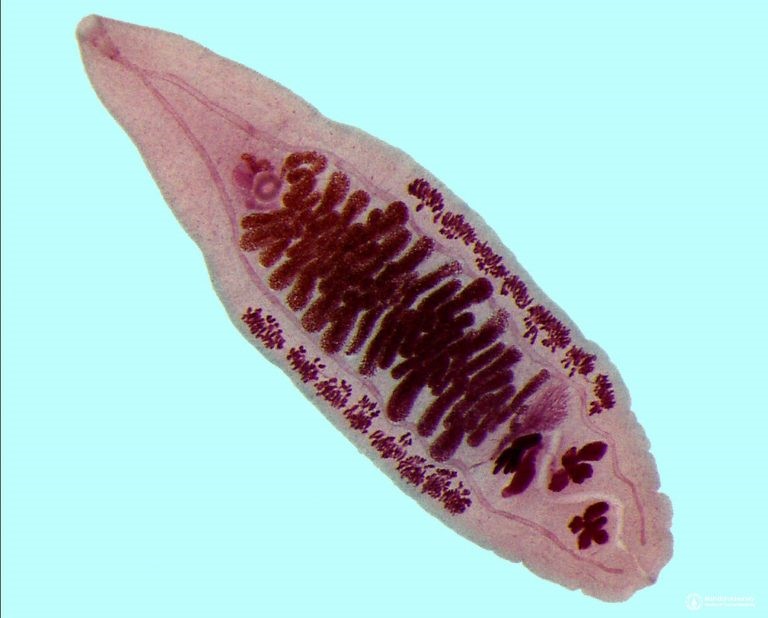
Как правило, кошачий сосальщик поражает печень и поджелудочную железу, вызывая в органах воспалительные процессы. Симптоматика разнообразна и зависит от количества паразитов. У больного могут наблюдаться:
- симптомы интоксикации;
- лихорадка,
- крапивница;
- зуд кожи;
- боли в мышцах, суставах, правом подреберье.
В отдельных случаях гельминты вызывают увеличение лимфатических узлов, развитие желтухи. Хроническая форма патологии нередко приводит к гепатиту, циррозу печени.
Парагонимоз
Виновник заболевания — легочный сосальщик, который проникает в организм человека с зараженными ракообразными. В России очаги парагонимоза — реки Дальнего Востока.
Сначала паразит проникает в кишечник человека, далее — в брюшную полость. Конечная точка его путешествия — ткань легких. Кроме этого, червь способен проникать в головной мозг и поражать центральную нервную систему.
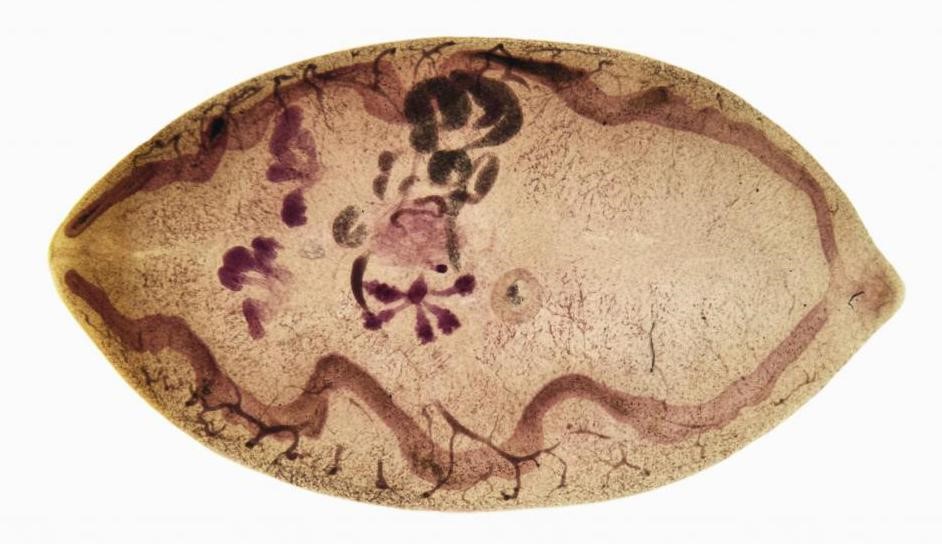
Специфические признаки паразитарной инвазии легких:
- болевой синдром в грудной клетке;
- кашель с мокротой, в которой могут присутствовать гной и кровь;
- лихорадка.
В отдельных случаях гельминты вызывают нарушение вентиляционной функции легких и газообмена при дыхании.
Круглые черви
Благодаря своему строению, круглые черви (нематоды) способны выживать даже в экстремальных условиях. Их тело покрыто трехслойным кожно-мускульным мешком, который надежно защищает паразитов от внешних воздействий.

Распространенные заболевания, вызываемые нематодами:
- аскаридоз;
- энтеробиоз;
- трихинеллез.
Аскаридоз
Развитие заболевания провоцирует аскарида, которая первоначально закрепляется в тонком кишечнике. Средняя длина взрослых особей составляет 40 см. Личинки паразита могут попасть в пищеварительную систему человека с немытыми овощами и фруктами, зараженной водой. Также нередко причиной аскаридоза становятся плохо вымытые перед едой руки.
Во время проникновения личинок в организм у человека могут наблюдаться субфебрильная температура, аллергические высыпания, кашель с выделением прозрачной мокроты. Признаки кишечной стадии аскаридоза (диарея, болевой синдром в животе) наблюдаются только при наличии нескольких паразитов. Как правило, обитание в кишечнике одного червя, протекает бессимптомно.
Осложнения при многочисленной паразитарной инвазии:
- закупорка желчного протока;
- гнойные воспалительные процессы в желчном пузыре, печени;
- воспаление аппендикса;
- кишечная непроходимость.
Энтеробиоз
Провокаторами заболевания являются острицы — небольшие черви длиной до 1 см. Гельминты проникают в пищеварительную систему человека также, как и аскариды.
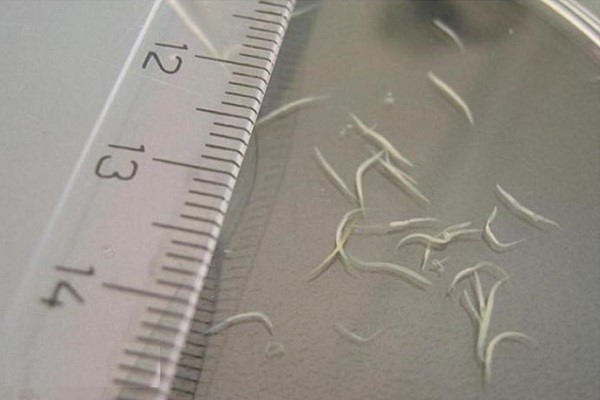
В настоящее время энтеробиоз является самой распространенной паразитарной патологией в мире. В основном заболевание диагностируется у детей в возрасте до 10 лет.
Симптоматика, как и в предыдущих случаях, развивается только при многочисленной паразитарной инвазии. У детей часто наблюдаются диарея, наличие в кале слизи, затрудненное и болезненное пищеварение, зуд в области ануса, тошнота. При тяжелом течении болезни могут возникать судороги конечностей. Кроме этого, острицы способны проникать в половые органы, вызывая в них острые воспаления.
Трихинеллез
Данное заболевание провоцирует трихинелла — один из самых маленьких паразитарных червей. Длина паразита редко превышает 4 мм. В личиночной стадии черви могут поражать скелетные мышцы. Исключением является миокард — мышечная ткань сердца. Взрослые особи паразитируют в тонкой кишке.
Как правило, заражение человека происходит при употреблении полусырой свинины. При этом для развития болезни достаточно употребить всего 30 г мяса, пораженного паразитами.
Патология проявляется стандартными симптомами паразитарной инвазии. В запущенной стадии могут возникнуть отечность век, лица, рук и ног, болевой синдром в пояснице, жевательных мышцах. Возможные осложнения — полное или частичная потеря подвижности, паралич дыхательных путей.
Как избежать заражения гельминтами?
Чтобы снизить риск заражения паразитическими червями, важно соблюдать следующие правила:
Гены и хромосомы человека. Строение
Неудивительно, что при часто встречающихся аномалиях (трисомиях) хромосом 13, 18 и 21 плод доживает до родов, поскольку эти хромосомы имеют наименьшее количество генов.
Гены могут изменяться и становиться причиной заболеваний человека за счет нескольких механизмов. Точечные мутации, при которых происходит замена одного основания ДНК в последовательности, могут оказывать влияние на многие функции гена. Миссенс-мутация — замещение одного основания в последовательности ДНК, из-за которого в синтезируемом протеине одна исходная аминокислота заменяется на другую. Такие мутации могут практически не повлиять на функции протеина, если замещающая аминокислота близка к исходной.
Эти изменения приводят к нисходящему сдвигу рамки считывания, что часто вызывает усечение белка. В целом такие мутации становятся причиной потери функций протеина и, соответственно, изменяют фенотип за счет снижения активности этого белка.
Со времен опытов Грегора Менделя с горохом, раскрывших механизмы наследования, генетика уделяет огромное внимание генным дефектам. Сегодня типы наследования определены для многих патологических состояний.
Как правило, акушер-гинеколог сталкивается с хромосомными аномалиями в двух клинических аспектах. Во-первых, это беременность в позднем репродуктивном возрасте матери, при которой риск хромосомных аномалий возрастает. Во-вторых, существует связь между невынашиванием беременности и хромосомными аномалиями: более половины спорадических выкидышей вызвано хромосомными аномалиями. Кроме того, акушеры-гинекологи занимаются лечением пациенток с привычными выкидышами и бесплодием в анамнезе, причиной которых тоже могут быть хромосомные аномалии.
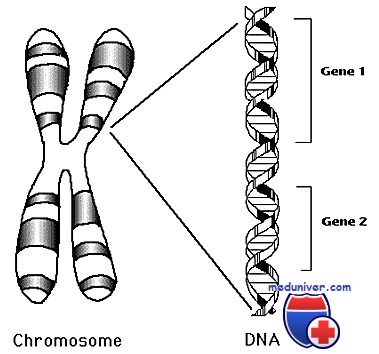
В клетках человека содержится 23 пары хромосом, из них 22 пары — аутосомы, общие для мужчин и женщин, и 1 пара — половые хромосомы (XX и XY). Упорядоченное расположение хромосом называют ка-риотипом. Рутинный хромосомный анализ производят путем взятия крови и стимулирования ускоренного деления лимфоцитов в культуре. После этого деление клеток ингибируют в метафазе и фиксируют хромосомы на предметном стекле. Затем хромосомы окрашивают и фотографируют для анализа.
Читайте также:

