Что такое мутированный вич
Обновлено: 25.04.2024
ВИЧ-инфекция — один из факторов, который во много раз повышает вероятность развития рака. Выяснили, какие именно онкозаболевания чаще всего могут возникать при положительном ВИЧ-статусе, как их вовремя обнаружить, и на какие факторы риска еще нужно обратить внимание людям, живущим с ВИЧ.
Мишень вируса
Главная мишень вируса — CD4-Т-лимфоциты. Они передают сигнал другим клеткам, которые защищают организм от рака. В результате вмешательства вируса количество CD4-T-лимфоцитов постепенно уменьшается. Критически низкий уровень этих клеток - одна из причин отсутствия согласованной работы между звеньями иммунитета и главный механизм, приводящий к развитию СПИДа.
СПИД-индикаторные опухоли
Иммунитет человека с ВИЧ-инфекцией перестает контролировать процессы избыточного клеточного деления и злокачественной трансформации клеток. Вместе с уменьшением количества CD4-T-лимфоцитов происходит накопление раковых клеток. В результате у человека развиваются несколько видов опухолей, которые называют СПИД-индикаторными: появление такого вида рака с очень большой вероятностью означает наличие у человека СПИДа.
Однако повышается риск появления не только СПИД-индикаторных опухолей, но и тех видов рака, которые развиваются из-за потери иммунного контроля над несколькими онкогенными инфекциями: вирусом герпеса человека 8 типа (ВГЧ-8), вирусом папилломы человека (ВПЧ), вирусами гепатита В и С (ВГВ, ВГС), вирусом Эпштейна-Барр (ВЭБ) и другими.
Все эти состояния развиваются у людей с ВИЧ-инфекцией преимущественно на фоне снижения количества CD4-T-лимфоцитов до уровня менее 200 клеток/мкл (при разбросе в норме от 500 до 1100 клеток), но также могут возникать при нормальном или близком к нормальному уровню CD4-T-лимфоцитов.
Саркома Капоши
Саркома Капоши (СК) — СПИД-индикаторная опухоль, при которой происходит злокачественная трансформация клеток лимфатических и кровеносных сосудов. Риск развития СК у пациентов с ВИЧ-инфекцией увеличивается в несколько сотен раз. Различные белки ВИЧ-1 способны усиливать воспаление и нарушать регуляцию в эндотелиальных клетках. Это приводит к тому, что саркома Капоши может развиться до того, как уровень CD4-T-лимфоцитов упадет ниже 200 клеток/мкл. Еще одно обязательное условие для возникновения СК — наличие в организме вируса герпеса человека 8 типа.
Саркома Капоши развивается в виде папулы, пятна, узелка, бляшки коричневого, розового, красного или темно-красного цвета от нескольких миллиметров до нескольких сантиметров в диаметре. Обычно высыпания концентрируются на ногах, голове, шее, на слизистой оболочке — в области неба, десен, конъюнктивы.
До эры внедрения лекарств от ВИЧ — антиретровирусной терапии (АРТ) 5-летняя выживаемость (с момента диагностики опухоли) пациентов с саркомой Капоши составляла менее 10%. Применение АРТ значительно улучшило ситуацию — сейчас речь идет о 74%, — а также позволило снизить риск развития СК.
Более половины случаев СК (56%) диагностируются сейчас в локальной форме — до того, как опухоль распространится на лимфатические узлы, слизистую ЖКТ, печень, селезенку и другие органы. Прием антиретровирусной терапии помогает значительно замедлить прогрессию болезни и предотвратить распространение СК по всему организму.
Однако, человеку с ВИЧ и его амбулаторному врачу-инфекционисту необходимо учитывать несколько факторов риска развития этой опухоли:
- Этническая принадлежность: люди еврейского или средиземноморского происхождения, а также экваториальные африканцы;
- Мужской пол;
- Иммунодефицит: Люди с уровнем CD4-клеток менее 200 кл/мкл, те, кто перенес трансплантацию органов или костного мозга или постоянно принимает глюкокортикостероиды;
- Сексуальная ориентация: мужчины, имеющие секс с мужчинами(МСМ), подвержены более высокому риску развития СК.
Опухоли, связанные с ВПЧ
К онкологическим заболеваниям, ассоциированным с вирусом папилломы человека, относятся инвазивный рак шейки матки (ИРШМ), сквамозный (чешуйчатый) рак головы/шеи, рак анального канала, вульвы и влагалища. СПИД-индикаторной из них является только ИРШМ.
Распространенность генитальной онкогенной инфекции ВПЧ среди женщин, живущих с ВИЧ, в целом выше, чем у остального населения.
Вирус папилломы человека способен к самопроизвольной элиминации — исчезновению из организма. У ВИЧ-положительных женщин этот процесс занимает больше времени, что увеличивает вероятность появления патологических изменений в шейке матки.
Продолжительный прием АРТ приводит к более низкой распространенности ВПЧ высокого риска и поражений шейки матки и даже предотвращает новые случаи ИРШМ.
Раннее начало антиретровирусной терапии, приверженность лечению обеспечивают снижение вирусной нагрузки — количества вируса в крови. Эти меры очень эффективны в отношении местного иммунитета слизистой оболочки и профилактики ИРШМ.
Скрининг ИРШМ заключается в проведении ПАП-теста и ВПЧ-теста (ПЦР). Женщины с ВИЧ-инфекцией в возрасте от 21 до 29 лет должны пройти ПАП-тест во время первичной диагностики ВИЧ, затем — через 12 месяцев, если анализ не показал патологии. Некоторые эксперты рекомендуют делать следующий ПАП-тест через 6 месяцев после первого. Если результаты трех последовательных мазков без отклонений, повторные тесты следует проводить каждые 3 года. ВПЧ-тест не рекомендуется подключать к ПАП-тесту до 30 лет — высока вероятность положительного результата, при этом оснований для активных действий нет. Лечения ВПЧ не существует, а для развития РШМ требуется, как правило, от 10 лет.
Также для предотвращения ИРШМ девочкам с сопутствующей ВИЧ-инфекцией старше 9 лет и до 26 лет крайне рекомендуется вакцинация от ВПЧ-инфекции (вакцины: 2-валентный Церварикс, 4-валентный Гардасил, в Европе/США - 9-валентный Гардасил-9). Кроме ИРШМ и дисплазии вульвы и влагалища у женщин, вакцинация предотвращает развитие рака анального канала. У ВИЧ+ гетеросексуальных мужчин и МСМ риск этого вида рака возрастает в 19 раз.
О чем еще нужно знать
У пациентов с ВИЧ-инфекцией повышается риск развития:
Гепатоцеллюлярная карцинома
К факторам риска развития ГЦК у пациентов с ВИЧ относятся: цирроз печени, ожирение, диабет, возраст старше 60 лет, мужской пол.
Скрининг ГЦК проводится с помощью анализа крови на альфа-фетопротеин (АФП), который может продуцироваться раковыми клетками, или инструментальных методик диагностики — УЗИ, КТ, МРТ.
В последние годы всё чаще используется фиброскан для оценки стадии фиброза и близости к циррозу, независимому фактору риска ГЦК.
Предотвратить появление гепатоцеллюлярной карциномы можно с помощью своевременной вакцинации и ревакцинации от вирусного гепатита В и контроля вирусной нагрузки.
Неходжкинские лимфомы (НХЛ)
Несмотря на появление АРТ, НХЛ остаются актуальной проблемой для людей, длительное время живущих с ВИЧ. Хотя в большом количестве случаев неходжкинские лимфомы являются СПИД-индикаторными, они способны развиваться при нормальном уровне CD4-клеток и являются одной из наиболее частых причин смерти среди ВИЧ-положительных.
Общая выживаемость у пациентов с этим диагнозом низкая: более половины умирают в течение пяти лет от момента постановки диагноза
Отсюда возникают факторы риска развития НХЛ при ВИЧ-инфекции:
- наличие ко-инфекции вирусными гепатитами В, C, H.pylori;
- наличие вирусной нагрузки вируса Эпштейна-Барр или цитомегаловируса;
- наличие аутоиммунных заболеваний до постановки диагноза ВИЧ-инфекция;
- наличие специфических изменений в протеинограмме до или во время ВИЧ-инфекции;
- наличие минимальной вирусной нагрузки ВИЧ, несмотря на АРТ;
- снижение CD4-Т-лимфоцитов.
К скринингу неходжкинских лимфом относятся мониторинг вирусной нагрузки ВЭБ, ВГС, ВГВ и проведение инструментальной диагностики (КТ, МРТ, УЗИ, ФГДС).
С помощью контроля факторов риска и своевременного скрининга можно не только найти опухоль на ранней стадии, но и предотвратить заболевание.
Если рак все же обнаружили, ни в коем случае нельзя прерывать антиретровирусную терапию — она проводится по жизненным показаниям, что означает высокую вероятность неблагоприятного исхода противоопухолевой терапии без сопутствующего противовирусного лечения.
ВИЧ обладает огромной вариабельностью генома – способностью очень быстро мутировать – намного быстрее, чем, например, вирус гриппа. Именно поэтому с ВИЧ так сложно бороться: разработка вакцин и эффективной терапии упирается в то, что вирус опережает ученых.
Для решения этих задач необходимо, прежде всего, знать, с кем мы имеем дело – то есть знать обо всем разнообразии вируса, и о том, как он меняется.
Это важно понимать и для целей практической медицины: если, например, появилась новая группа, подтип или вариант ВИЧ, необходимы диагностические системы, которые могут их определять.
О том, как происходит изучение мутаций ВИЧ, его эволюции и о новых диагностических системах, которые позволяют улавливать малейшие изменения в геноме вируса, рассказал вице-президент отдела прикладных исследований и технологий компании Abbott доктор Джон Хэкет (John Hacket). Кстати, Abbott была первой компаний, создавшей в 1985 году тест на определение антител к ВИЧ, то есть тест, позволявший диагностировать вирус в крови.
Быстрее гриппа
В настоящее время известно о существовании двух типов - ВИЧ 1 и ВИЧ 2. ВИЧ 1 является наиболее распространенным типом и делится на группы – М (эта группа самая распространенная), N,O и P. Группа Р была обнаружена совсем недавно – в 2009 году у женщины из Камеруна, которая приехала во Францию. В группе М существует еще и множество подтипов. При этом постоянно происходит образование новых вариантов. Не исключено, что скоро возникнут новые группы и подтипы вируса.
Во-вторых, ВИЧ реплицируется (размножается) необыкновенно быстро: в больном, который не получает лечение, образуется до десяти миллиардов вирусных частиц в день.
В-третьих, вирус обладает способностью к рекомбинации: например, если человек инфицирован разными суб-типами ВИЧ, они рекомбинируют между собой в организме человека, что и приводит к образованию нового варианта вируса.
Когда медикам и ученым стало понятно, что разнообразие ВИЧ столь велико, появилась необходимость в создании диагностических систем, которые могли бы не только определять все типы, группы и подтипы, известные на данный момент, но и выявлять новые. Ведь иначе можно получить ложноотрицательный результат, пропустив в образце варианты вируса, которых диагностическая система просто не знает.
На данный момент в рамках программы уже собрано более 25 тысяч образцов ВИЧ и гепатита В из 16-ти стран. Особое внимание удаляется очагам в Африке – поскольку именно там наблюдается максимальное разнообразие вариантов ВИЧ. В программе участвовали также 10 медицинских центров из России.
Для обнаружения новых вариантов ВИЧ используются самые современные научные методы, такие как секвенирование генома, включая глубокое секвенирование.
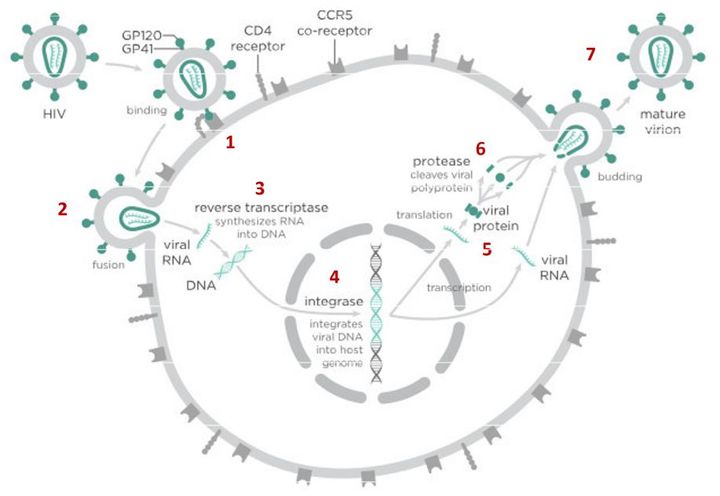
Вирусы могут размножаться только внутри клетки-хозяина, перестраивая ее работу так, что клетка начинает производить новые вирусные частицы. Это серьезно нарушает работу самой клетки и в большинстве случаев ведет к ее гибели. Процесс проникновения и размножения вируса в ней сложный и содержит много стадий, а значит, специальные лекарства могут тормозить его на различных этапах.
В случае с ВИЧ это выглядит так.
по теме

Лечение
Лучшие научпоп-статьи 2018 года
После того как вирусная частица приклеилась к рецепторам CD4 и CCR5/CXCR4 и закрепилась на поверхности клетки, другой специальный белок вируса gp41 соединяет оболочку вируса с мембраной клетки-мишени и помогает вирусу проникнуть внутрь клетки (цифра 2 на схеме). На этом этапе остановить вирус может другая группа препаратов — ингибиторы слияния, например, энфувиртид. Препарат связывается с вирусным белком gp41 и нарушает его работу.
На этом этапе размножение вируса блокирует очень большое количество препаратов из двух классов — нуклеозидные ингибиторы обратной транскриптазы (НИОТ — ламивудин, абакавир, тенофовир) и ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ — эфавиренз, рилпивирин). Принцип действия у веществ из обеих групп похожий: молекула лекарства связывается с обратной транскриптазой вируса, нарушает ее работу и так блокирует перенос генов вируса из РНК в ДНК. Это не позволяет генам вируса встроиться в ДНК клетки-хозяина и начать производство новых вирусных частиц.
На следующем этапе инфицирования (цифра 4 на схеме) готовая вирусная ДНК проникает в ядро и встраивается в ДНК клетки-хозяина с помощью специального вирусного фермента — интегразы. Работу этого фермента блокируют ингибиторы интегразы, например, долутегравир, не позволяя ДНК вируса встроиться в наши гены.
После того как вирусная ДНК встраивается в ДНК клетки-хозяина, клетка получает неправильную программу и начинает производить вирусные белки и РНК, необходимые для сборки новых частиц вируса (цифра 5 на схеме), используя для этого структуры, которые в норме производят собственные белки клетки. Такая перенастройка производства белка сильно нарушает работу клетки и через некоторое время вызывает ее гибель. Лекарств, которые бы влияли на этот этап размножения вируса, нет, так как здесь вирус использует собственные ферментные системы клетки-хозяина и блокирование их работы какими-то веществами навредит здоровым клеткам.
по теме

Лечение
Ошибка системы. Почему в регионах опять не хватает таблеток от ВИЧ
После синтеза вирусных белков клеткой-хозяином в работу вступает еще один фермент вируса — протеаза (цифра 6 на схеме). Дело в том, что белки ВИЧ синтезируются в виде длинных цепочек белков-предшественников, но они неактивные. Протеаза разрезает эти цепочки на более короткие фрагменты, которые становятся активными белками вируса: из одних собирается вирусная оболочка, другие выполняют функции ферментов (обратная транскриптаза, интеграза, протеаза, о которых мы говорили выше). Класс лекарств, нарушающих работу вирусной протеазы, включает большое количество препаратов от достаточно старого лопинавира до современного дарунавира. Основной недостаток препаратов этого класса — высокая степень перекрестной устойчивости: если вирус приобретает устойчивость к одному препарату, скорее всего, на него не подействует ни один другой препарат из этого класса.
На последнем этапе (цифра 7 на схеме) вирусные частицы собираются из готовых компонентов (синтезированных клеткой вирусных белков и РНК), как конструктор, и покидают клетку-хозяина. Лекарств, которые бы тормозили эти процессы, пока не существует.
ВИЧ имеет высокую склонность к мутациям, что позволяет ему быстро приобретать устойчивость к лекарствам. Мутации изменяют форму молекул ферментов вируса. Если при этом форма изменится существенно, то фермент не сможет нормально работать и такой вирус размножаться перестанет — это вредная для вируса мутация. Однако в некоторых случаях — при полезных мутациях — форма молекулы фермента меняется не сильно, а так, что сам фермент продолжает нормально работать, но молекула лекарства уже не может с ним связаться.
Поэтому для эффективного подавления размножения ВИЧ обычно назначают три разных препарата из разных групп, влияющих на разные ферменты вируса, блокируя его воспроизводство на разных этапах. Исключением является группа ингибиторов обратной транскриптазы (НИОТ и ННИОТ) — эти лекарства связываются с разными участками молекулы вирусного фермента, поэтому могут назначаться вместе, несмотря на то, что относятся к одной группе. В условиях такой терапии вирусу очень трудно выработать устойчивость, потому что одновременно должно произойти несколько полезных мутаций в разных генах вируса, а это бывает крайне редко.
Есть несколько перспективных технологий, например, CRISPR/Cas9, которые могут позволить полностью удалить вирусную ДНК из организма человека, но пока ни одна из них не прошла все необходимые исследования для подтверждения эффективности и безопасности. Исследования продолжаются.
На этой неделе китайский учёный сообщил о рождении генетически отредактированных близнецов. В их геном были внесены изменения, позволяющие почти полностью исключить риск развития хронической ВИЧ инфекции. 1% европейцев обладают такой устойчивостью с рождения. Рассказываем о появлении и механизме резистентности к ВИЧ.
Более 40 миллионов человек по всему миру заражены вирусом иммунодефицита человека (ВИЧ). Если сразу после заражения иммунная система не успевает уничтожить все вирусные частицы, они могут проникнуть внутрь клеток и встроиться в их геном. В результате этого человек становится носителем инфекции. Хроническая ВИЧ инфекция на сегодняшний день неизлечима, однако поддается контролю и в случае своевременной терапии не оказывает сильного влияния на самочувствие человека.
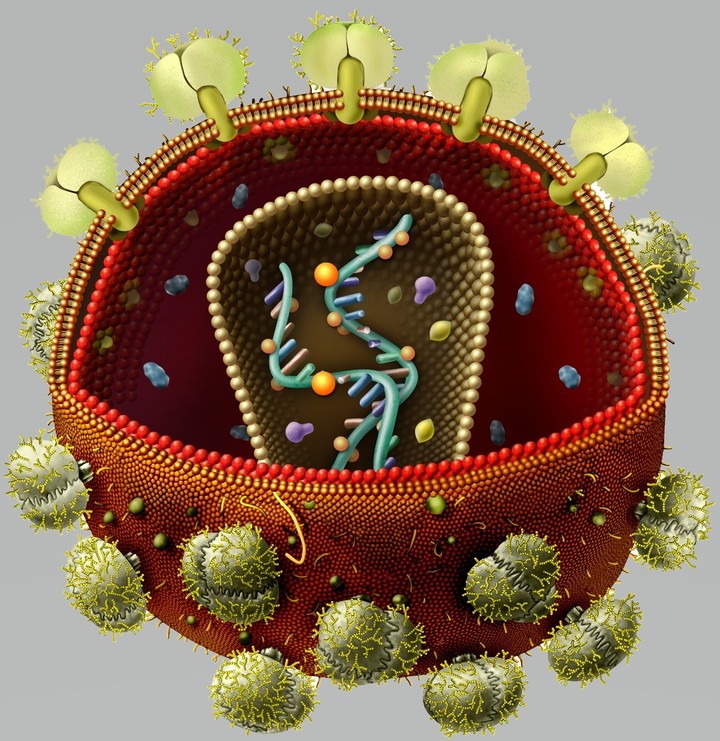
Для проникновения в клетку ВИЧ должен связаться с двумя рецепторами на ее поверхности. Один из рецепторов – CD4, присутствует на поверхности T-лимфоцитов и отвечает за распознавание чужеродных агентов. Второй рецептор, необходимый для слияния оболочки вируса и клетки, - CCR5. Его роль в иммунной реакции до конца не изучена, предполагается, что он участвует в развитии воспалительной реакции.

У некоторых людей с рождения есть защита от ВИЧ, обусловленная наличием в их геноме мутаций. Это снижает риск развития хронической инфекции даже в случае заражения. Одной из них является мутация в гене рецептора CCR5, представляющая собой потерю части гена (32 нуклеотида) - ССR5Δ32. В результате вирус не может связаться с рецептором и проникнуть в клетку.
При этом риск развития хронической инфекции низкий только у гомозиготных носителей мутации - у тех, кому мутантный ген достался от обоих родителей. Существуют противоречивые данные о влиянии мутации только в одной копии гена CCR5 на риск развития ВИЧ: от наличия защиты до отсутствия какого-либо влияния на течение заболевания.

Предполагается, что мутация ССR5Δ32 возникла около 1000 лет назад в Северной Европе среди викингов. Распространение мутации в Европе обычно связывают с набегами викингов на соседние народы. Длительное время было непонятно, что способствовало распространению и закреплению мутации среди народов Европы, ведь ВИЧ — сравнительно молодая инфекция, и носители этой мутации не получали какого-либо преимущества. Однако впоследствие было обнаружено, что кроме ВИЧ эта мутация также снижает вероятность заразиться черной оспой, многочисленные эпидемии которой в свое время привели к массовой гибели людей по всему миру.
В настоящее время частота встречаемости этой мутации в странах Европы составляет около 10%. Частота мутации среди клиентов Genotek оказалась равной 9,7%. При этом только 1,1% людей оказались носителями мутации в двух копиях гена CCR5, они имеет низкий риск развития хронической инфекции даже в случае заражения.
Гомозиготное носительство делеции в гене CCR5 не является абсолютной защитой от заражения ВИЧ и поводом не использовать до- и пост-контактную профилактику при угрозе заражения. Известны единичные случаи, когда у людей с таким генотипом развивалось хроническое носительство ВИЧ после заражения. Возможно, это связано с тем, что кроме CCR5, вирус может использовать другие рецепторы для проникновения в клетки (например, рецептор СXCR4).

Один известный случай излечения человека от хронической ВИЧ инфекции связан с этой мутацией. Тимоти Браун, или Берлинский пациент, был заражен ВИЧ и болен лейкемией. Ему требовалась пересадка костного мозга. Врач смог подобрать донора, гомозиготного по мутации в CCR5. Через 20 месяцев после операции, несмотря на отсутствие терапии, ВИЧ перестал обнаруживаться в крови, костном мозге и слизистой оболочке кишечника пациента.
А совсем недавно российским ученым удалось получить человеческие эмбрионы с измененным геном CCR5, используя 16 оплодотворенных яйцеклеток не пригодных для программ ЭКО. Из 16 модифицированных яйцеклеток, только 8 продолжили развитие, причем в 5 из них модификация прошла успешно и обе копии гена были изменены.
А в ноябре 2018 года было распространено заявление ученого из Китая, которому якобы удалось провести аналогичный эксперимент, в результате которого родились девочки-близнецы, у одной из которых мутация в CCR5 присутствует в двух генах, а другой - только в одном. Родители близнецов приняли решение не раскрывать своих имен и места жительства, никаких других доказательств, кроме заявления врача, также нет.
Несмотря на огромное количество статей и исследований о ВИЧ, в обществе до сих пор гуляет множество мифов и заблуждений об этом заболевании, а люди, столкнувшиеся с ВИЧ, — стигматизируются. Добавляет масла в огонь новость о всемирной ВИЧ-эпидемии. В результате — общество в неведении и панике. Резидент Высшей школы онкологии и химиотерапевт Татьяна Бобровицкая помогает нам снизить накал страстей и рассказывает, что современная медицина уже знает о ВИЧ-инфекции.
Неутешительная статистика: 1 млн россиян болеет ВИЧ
На первом месте в списке регионов-лидеров по количеству смертей от ВИЧ находится Кемеровская область: с 2018 года коэффициент смертности здесь вырос на 11% и составил 65,1. На втором месте находится Иркутская область с коэффициентом 42,4, что на 1% ниже показателей прошлого года (за год снизился на 1%). Третье место заняла Свердловская область, где коэффициент смертности вырос на 10% и составил 38,1.
АРТ снижает смертность от ВИЧ и СПИДа на 38%
К концу 2017 года 21,7 млн человек с ВИЧ-инфекцией получали пожизненную АРТ по всему миру. По оценкам экспертов, только 75% носителей этого заболевания знают свой статус.
- 90 % всех людей с ВИЧ должны знать о своем статусе;
- 90 % ВИЧ-инфицированных должны стабильно получать АРТ;
- у 90 % людей, получающих АРТ, должна наблюдаться вирусная супрессия (ограничение или полное подавление любой физиологической активности вируса — прим. ред.)

АРТ способна уничтожить ВИЧ в крови
ВИЧ невозможно вылечить, но благодаря использованию антиретровирусных препаратов (АРВ) его можно контролировать и, следовательно, предотвращать передачу. АРТ блокирует выработку новых вирусов в активных клетках CD4, инфицированных ВИЧ. Если терапия подошла пациенту, вирусная нагрузка снижается на 90% через несколько недель после начала терапии, а через несколько месяцев — уже на 99%.
Люди с ВИЧ, принимая терапию, могут иметь здоровых детей
АРТ охватывает порядка 80% беременных и кормящих грудью женщин по всему миру. По данным исследования Роланда Тубиана, Джерома Ле Шенадек Кристины Розиу и др. риск передачи ВИЧ типа 1 от матери к ребенку составляет всего 0,5% у не кормящих матерей, которые родили в срок, получая АРТ. Методология и результаты исследования опубликованы в журнале Clinical Infectious Diseases в феврале 2010 года.
Ученые пришли к выводу, что непрерывный контроль вирусной нагрузки на ранних стадиях уменьшает остаточный риск передачи ВИЧ-инфекции от матери к ребенку. При этом, для принятия решения о времени начала АРТ во время беременности важно учитывать не только количество CD4 (+) Т-клеток и риск преждевременных родов, но и также ВИЧ-нагрузку.
Сегодня существует множество доказательств влияния АРТ на распространение ВИЧ-инфекции. Инфицированный человек с неопределяемым уровнем вирусной нагрузки не может передавать заболевание. С 2007 по 2016 годы ученые провели три крупных исследования передачи ВИЧ половым путем при участии пар (как гомо-, так и гетеросексуальных), в которых один из партнеров — с ВИЧ-положительным статусом, принимающий АРТ.
В ходе исследований авторы не зафиксировали ни одного случая передачи вируса. Тем не менее, авторы UNAIDS Explainer настаивают на проведении тестов для уверенности в том, что у носителя подавлена вирусная нагрузка.
Как правило, человек с ВИЧ-положительным статусом, не принимающий АРВ-препараты, живет не более 10 лет. Продолжительность жизни при этом сильно зависит от ряда факторов: образа жизни, иммунитета и т. д. — некоторые не проживают и 3 лет с момента заражения. При этом, человек умирает не от СПИДа, а от оппортунистических (сопутствующих) заболеваний.
Препараты, созданные для борьбы с ВИЧ, уже объединены в отдельный класс. Они снижают вирусную нагрузку и блокируют распространение вируса. Благодаря этому, уровень лимфоцитов в крови повышается, поддерживая нормальный уровень иммунной защиты.
Если человек принимает терапию, то продолжительность жизни приближается к средней в популяции. В развитых странах ожидаемая продолжительность жизни — 60 лет с момента постановки диагноза.
Туберкулез — главная причина смерти людей с ВИЧ
Ежедневно от туберкулеза умирает около 4,4 тыс людей с инфекционными заболеваниями. Количество смертей от этой болезни среди ВИЧ-инфицированных людей в 2017 году составило 300 тыс. человек.
Страны-участники ООН в Политической декларации ООН об искоренении СПИДа взяли на себя обязательство к 2020 году снизить уровень смертности от туберкулеза среди носителей ВИЧ-инфекции на 75 %.
Риск развития онкологии при ВИЧ без АРТ увеличивается до 20 раз
У ВИЧ-инфицированных женщин переход нелеченной эрозии шейки матки в рак шейки матки (РШМ) происходит намного быстрее, чем у здоровых из-за поражения иммунной системы: при отсутствии терапии риск развития РШМ увеличивается в 5 раз, а по некоторым данным — в 13 раз.
Так, женщина с ВИЧ должна проходить цитологический скрининг не реже 1 раза полгода, а также тестирование на вирус папилломы человека (ВПЧ).
Важно знать, что, наряду с риском РШМ, увеличивается риск развития лимфом, злокачественного опухолевого заболевания лимфатической системы, в 20 раз, а также саркомы Капоши — множественных злокачественные новообразований кожи, которые в 95% случаев встречаются только людей с ВИЧ.

Как не заболеть?
Уже есть схемы терапии, позволяющие предотвратить инфицирование. Это доконтактная и постконтактная профилактика для пар с разным или неизвестным ВИЧ-статусом, а также для людей, практикующих частую смену половых партнеров.
В результате исследователи выявили несколько побочных эффектов: боли в месте инъекции (88% у активной группы и 49% — в группе плацебо), боли в животе и диарея, повышение уровня аспартат-аминотрансферазы (АсАт, молекулы белка, способствующей активизации биохимических процессов в организме), головокружение и общее недомогание.
Чтобы проверить иммуногенность вакцины (способность антигена вызывать иммунный ответ), ученые вакцинировали обезьян, а затем инфицировали их комбинированным вирусом SHIV (simian-human immunodeficiency virus). Выяснилось, что Ad26.Mos.HIV с gp140 защищает от инфекции лучше всего: даже после шестикратного введения вируса ⅔ животных остались здоровы. Сейчас проект находится в фазе испытаний 2b для оценки эффективности вакцины на 2600 женщинах с высоким риском заражения в Южной Африке.
Безусловно, ВИЧ-инфекция — серьезное и опасное заболевание, от которого никто не застрахован. Однако, благодаря труду врачей и ученых по всему миру, оно больше не приравнивается к смертному приговору. Для человека с ВИЧ-положительным статусом существует лишь одно ограничение — необходимость АРТ. В остальном носитель вируса сегодня может жить полноценной жизнью: ходить на работу, получать медицинскую помощь, иметь детей, с любовью и ответственностью относиться к себе, своему здоровью и здоровью своих близких.
Читайте также:

