Что такое нематодозах токсокароз токсаскаридоз унцинариоз
Обновлено: 18.04.2024
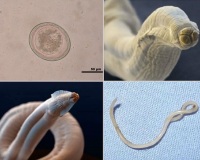
Тохосага canis – светложелтая нематода, на головном конце располагаются три губы и широкие боковые крылья. Длина самца 5-10 см, самки – 9-18 см. Хвост самки прямой, хвостовой конец самца загнут, на вершине находятся две равные спикулы и конусовидный придаток.
Toxascaris leonina – светложелтая нематода, на головном конце располагаются узкие боковые крылья. Длина самца 4-6 см, самки 6,5-10 см. Хвост самца постепенно утолщается, имеет 2 равные спикулы.
Яйца покрыты гладкой оболочкой, округлые, 0,075-0,085 мм в диаметре.
Токсокарозом болеют щенки до 3-месячного возраста, токсаскаридозом – более взрослые собаки. Возбудители – Тохосага canis и Toxascaris leonina попадают в организм собаки в виде инвазионных яиц. В яйце личинки созревают не менее 10 и 3 суток соответственно, поэтому свежий кал не может быть причиной заражения.
Вылупившиеся в кишечнике личинки проникают в кровь, на ранней стадии развития мигрируют через печень и легкие собак, повреждая эти органы и вызывая воспалительные процессы, отхаркиваются и проглатываются вместе с бронхиальной слизью. Снова попав в кишечник, достигают там половой зрелости. Вместе с аскаридами переносятся бактерии и вирусы, проникая даже в головной мозг.
Черви конкурируют с хозяином в отношении питательных веществ, отравляют организм продуктами своего обмена. Нематоды перфорируют стенку кишечника, открывая путь вирусам и бактериям. Клубок паразитов способен закупорить просвет кишечника и вызвать его разрыв. Нематоды могут заползать в поджелудочную железу и желчные протоки. Возможно внутриутробное заражение щенков токсокарами.
Личинки токсаскарисов развиваются в стенках тонкого отдела. Затем, проникнув в просвет кишечника, они достигают половой зрелости.
Рвота после приема корма, икота, исхудание, поносы и запоры, анемия. При пальпации – уплотнения в тонком отделе кишечника. Живот вздут.
Токсокароз может сопровождаться бронхитом. Это проявляется хрипами и кашлем.
Симптомокомплекс токсокароза щенков: бронхит + периодическая рвота + икота. Необходимо провести анализ кала на яйца гельминтов.
¦ РЕКОМЕНДОВАННЫЙ СПОСОБ ЛЕЧЕНИЯ
Лечение заключается в изгнании паразитов с помощью одного из антигельминтиков: левамизол (декарис) – 3-5 мг/кг внутрь или подкожно; пирантел (тивидин) – 15-20 мг/кг внутрь; мебендазол (медамин, вермокс, мебенвет) – 15-20 мг/кг внутрь; альбендазол (атазол) – 25 мг/кг внутрь.
Осторожно: превышение дозировки может вызвать отравление!
Для профилактики токсикоза вследствие массовой гибели и разложения паразитов в кишечнике назначают очистительные клизмы.
При паразитарном бронхите, осложненном бактериальной инфекцией, показано применение антимикробных средств.
Паразитарный бронхит, заболевания печени, желчевыводящих путей.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРес
Токсокароз и токсаскаридоз
Токсокароз и токсаскаридоз ¦ ОПИСАНИЕ ВОЗБУДИТЕЛЯТохосага canis – светложелтая нематода, на головном конце располагаются три губы и широкие боковые крылья. Длина самца 5-10 см, самки – 9-18 см. Хвост самки прямой, хвостовой конец самца загнут, на вершине находятся две равные
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
- Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
- Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
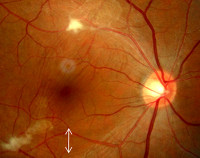
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
В статье представлены современные данные о ларвальных гельминтозах у детей, самым распространенным и трудно диагностируемым из которых является токсокароз, имеющий тяжелое хроническое течение с выраженным иммуносупрессивным эффектом и полиорганными пораже
The article represents the modern data on larva migrans in children, toxocariasis being the most widespread and difficultly diagnosed among them, with severe clinical course, pronounced immunosuppressing effect and multiple affections of organs. Pathogenesis, therapy and prevention of the disease are discussed.
Распространенность гельминтозов среди жителей различных континентов Земли огромна: на каждого жителя Африки приходится более двух видов гельминтов, в Азии и Латинской Америке более одного вида, в Европе поражен каждый третий житель. В России практически каждый человек в течение жизни переносит паразитарное заболевание, причем чаще страдают дети [1]. По величине ущерба, наносимого здоровью людей, гельминтозы занимают 4-е место после диареи, туберкулеза и ишемической болезни сердца. Ежегодно в мире от гельминтозов погибают 135 тыс. человек, причем число это неуклонно растет [2].
- санитарно-гигиенические — высокий уровень контаминации окружающей среды яйцами гельминтов в результате сброса необезвреженных сточных вод и стоков животноводческих комплексов; недостаточные гигиенические навыки населения, привычка удобрять почву экскрементами;
- миграционными — усилением миграции населения и завозом паразитарных болезней из эндемических стран, вторжением городского населения в сельскую местность (работа на садовых участках, дачах, личных фермах), рост числа бродячих животных;
- информационными — малая информированность населения, а порой и врачей о гельминтозах и путях их заражения, профилактика гельминтозов ограничена лишь лечением вновь выявленных случаев заболевания;
- этническими — особенности питания населения, а именно употребление сырой или слабообработанной продукции;
- экономическими — обеднение населения, удорожание лекарственных препаратов;
- экологическими — снижение общей иммунной реактивности.
В настоящее время известно около 270 видов гельминтов, паразитирующих в организме человека, из которых 30 широко распространены на территории России. Гельминты, паразитирующие у человека, относятся к типу плоских червей, среди которых различают два класса: Cestoidea — ленточные черви и Trematoda — сосальщики, и типу круглых червей (класс Nematoda — собственно круглые черви). В зависимости от места паразитирования в организме человека, гельминты подразделяются на просветные, к которым относится большинство патогенных для человека гельминтов, и тканевые. В тканях в свою очередь могут обитать как взрослые особи, так и личинки.
Гельминтозы, при которых основным патогеном являются личинки, мигрирующие или покоящиеся, называют личиночными или ларвальными [3]. Особенностью ларвальных гельминтозов является то, что человек в данной ситуации является промежуточным или случайным хозяином, а жизненный цикл паразита не завершается, личинка не превращается в половозрелую особь и не может дать потомство [4]. Следовательно, такой вид паразитирования является биологическим тупиком. К числу таких гельминтозов относят многие филяриозы, трихинеллез, гнатостомоз, капилляриоз, спарганоз, эхинококкозы, токсокароз и др.
В отсутствие этиологического диагноза, который поставить удается не всегда, этот вид гельминтозов обозначают обобщенным термином Larva migrans, под которым понимают симптомокомплекс, обусловленный паразитированием личинок гельминтов, для которых человек не является естественным хозяином [5–7]. В зависимости от пути проникновения и места паразитирования условно выделяют перкутанные, или кожные, и висцеральные формы. Возбудителями кожной формы являются шистосомы, анкилостомы, некоторые виды филярий. При этом личинки гельминтов проникают в неповрежденную кожу при контакте с водой или почвой, паразитируют в эпидермисе, дерме или гиподерме, а после самопроизвольной гибели личинки, через 1–6 месяцев, наступает полное выздоровление [8]. Это условно доброкачественные гельминтозы. Висцеральная форма, возбудителями которой являются эхинококки, токсокары, цистицерки и др., возникает при проглатывании человеком яиц гельминтов с водой, продуктами питания, частичками почвы и протекает зачастую тяжело, длительно, порой годами и, как правило, не заканчивается спонтанным выздоровлением. Прогноз у данной группы гельминтозов серьезный, вплоть до летального исхода [9].
Наиболее тяжело протекают ларвальные (личиночные) гельминтозы вследствие множественного поражения печени, легких, сердца, почек, головного мозга, органа зрения и др. (токсокароз, однокамерный эхинококкоз, цистицеркоз) или агрессивного роста и метастазов зародышей или яиц паразита (многокамерный эхинококкоз, парагонимоз). Кроме этого, обладая значительной антигенной чужеродностью, мигрирующие личинки вызывают тяжелую общую и местную аллергическую реакцию, вплоть до формирования в тканях эозинофильных гранулем, оказывают механическое и токсическое повреждение [10].
Для гельминтозов характерен широкий диапазон клинических симптомов: от слабовыраженных до генерализованных реакций с множественными поражениями. Именно такая неспецифичность, малоинформативность стандартных методик гельминтологического исследования на яйца глистов, в совокупности с традиционным отсутствием настороженности у городских практических врачей, побудили нас еще раз обратить внимание на эту проблему. Часто правильный диагноз скрывается за самыми разнообразными масками и распознается поздно (рис. 1).
.jpg)
Токсокароз является самым распространенным из ларвальных гельминтозов у детей, пораженность токсокарозом в странах умеренного пояса составляет от 2% до 37%, достигая 92,8% в тропических странах [11–14]. Токсокароз — это зоогельминтоз, имеющий тяжелое хроническое течение с выраженным иммуносупрессирующим эффектом и полиорганными поражениями. Возбудителем токсокароза является нематода из рода Toksokara. Наиболее известны Toksokara catis, паразитирующая в организме кошек, и Toksokara canis, паразитирующая в организме собак, волков, лисиц, песцов и других представителей семейства псовых [15, 16]. Самка Toksokara canis имеет длину 9–18 см, самец — 5–10 см. Взрослые паразиты локализуются в желудке и тонкой кишке окончательных хозяев. Средняя продолжительность жизни половозрелых особей составляет 4–6 мес, и каждая самка Toksokara canis откладывает более 200 тыс. яиц в сутки. Яйца выделяются незрелыми и через 5–8 дней инкубации в почве становятся инвазионными, сохраняя жизнеспособность и инвазивность до 10 лет. Кроме этого, широкому распространению токсокароза среди животных способствует совершенный механизм передачи возбудителя, при котором сочетаются прямой (заражение яйцами из окружающей среды), внутриутробный (заражение плода личинками через плаценту), трансмаммарный (передача личинок с молоком) пути передачи и заражение через резервуарных (паратенических) хозяев.
Основной источник опасности для человека — это домашние и бродячие собаки разного возраста. В настоящее время в Москве численность собак превышает 1 млн особей, которые ежедневно оставляют на ее территории около 270 тонн экскрементов, содержащих более 40 тысяч яиц токсокар в каждом грамме! Поэтому каждая вторая проба почвы детских площадок, скверов, парков и территорий вокруг жилых домов содержит яйца этих паразитов [17–20]. У детей заражению может способствовать геофагия, именно поэтому токсокарозом чаще болеют дети дошкольного возраста. Прямой контакт с собакой также может привести к заражению через шерсть, загрязненную почвой, содержащей зрелые яйца токсокар. Ребенок может заражаться круглогодично через загрязненные яйцами почву, продукты питания, воду, руки. Установлена роль тараканов в распространении токсокароза: они поедают значительное количество яиц токсокар и до 25% их выделяют в жизнеспособном состоянии в окружающую среду [21]. Группу риска составляют люди, по роду деятельности контактирующие с животными и почвой.
Человек служит паратеническим (резервуарным) хозяином, являясь для паразита биологическим тупиком, так как токсокары паразитируют у него только в личиночной стадии, не выделяясь в окружающую среду. После проглатывания человеком зрелых яиц, в проксимальном отделе тонкого кишечника из них выходят личинки, которые через слизистую оболочку проникают в кровоток, затем заносятся в печень и правую половину сердца. Попав в легочную артерию, личинки продолжают миграцию и переходят из капилляров в легочную вену, достигают левой половины сердца и затем разносятся кровью по разным органам и тканям. Мигрируя, они достигают места, где диаметр сосуда меньше размера самой личинки, и покидают кровяное русло. Личинки токсокар могут оседать абсолютно во всех органах и тканях, сохраняя жизнеспособность в течение длительного времени, периодически активизируясь и возобновляя миграцию. С течением времени часть личинок инкапсулируется и постепенно разрушается внутри капсулы.
Токсокароз имеет длительное, рецидивирующее течение [22]. Клинические проявления определяются интенсивностью инвазии, распределением личинок в органах и тканях, частотой реинвазии и особенностями иммунного ответа человека [23, 24]. В зависимости от преимущественной локализации личинок выделяют висцеральную и глазную формы токсокароза.
Висцеральный токсокароз встречается чаще как у детей, так и у взрослых и возникает в результате заражения большим числом личинок [25]. Клинические проявления острого токсокароза разнообразны (рис. 2).
Для больных токсокарозом наиболее характерна субфебрильная, реже — фебрильная лихорадка с пиком во второй половине дня, сопровождающаяся недомоганием и ознобом. Как правило, одновременно с лихорадкой выявляется синдром поражения легких, варьирующий в широких пределах: от катаральных явлений до тяжелых астмоидных состояний. Могут наблюдаться рецидивирующие бронхиты, бронхопневмонии вплоть до летального исхода. При рентгенологическом исследовании в этот период выявляются множественные или единичные эозинофильные инфильтраты, так называемый синдром Леффлера. Наряду с синдромом поражения легких часто отмечается увеличение размеров печени, а иногда и селезенки, сопровождающееся болями в животе, тошнотой, рвотой и диарей. Практически у всех больных выявляется лимфаденопатия. В отдельных случаях токсокароз сопровождается развитием аллергического миокардита, панкреатита, поражением почек [26]. Поражение кожи при токсокарозе встречается реже и отличается полиморфностью высыпаний: от эритем до пятнисто-папулезных и уртикарных элементов. Все чаще стали выявлять и поражение центральной нервной системы, которое может протекать в виде эписиндрома, гиперактивности, аффективной неустойчивости, трудностей в учебе. В тяжелых случаях регистрируется менингоэнцефалит, парезы, параличи, нарушения психики. Увязать такие явления непосредственно с токсокарозом весьма проблематично, однако в одном из сероэпидемиологических исследований, проведенном в 1984 г., показана связь затруднений при чтении, невозможности сосредоточиться и низкого уровня интеллекта с заболеванием дошкольников токсокарозом.
Золотым стандартом диагностики любого гельминтоза является паразитологический метод. Однако прижизненный паразитологический диагноз токсокароза практически невозможен, поскольку обнаружить мигрирующие личинки трудно, а идентифицировать их по гистологическим срезам весьма непросто [29].
Клиническо-анамнестическая диагностика токсокароза также затруднительна ввиду полиморфизма и неопределенности клинических проявлений. В повседневной клинической практике своевременная постановка диагноза и назначение специфической терапии — скорее исключение, чем правило. Для облегчения задачи в 1978 г. был предложен диагностический алгоритм (табл.).
При сочетании симптомов и признаков на сумму более 12 баллов целесообразно назначение иммунологической диагностики. В диагностике глазного токсокароза может помочь офтальмологическое обследование с обнаружением личинки в области диска зрительного нерва или в макулярной части.
Диагностика токсокароза на сегодняшний день основывается на лабораторных методах исследования [30]. Одним из постоянных проявлений висцеральной формы токсокароза является лейкоцитоз и стойкая длительная эозинофилия до 30–90%. Наблюдается также умеренная анемия, гиперпротеинемия, гипергаммаглобулинемия, высокий уровень IgE. При поражении печени отмечаются нарушения ее функции.
Наиболее информативными в диагностике токсокароза являются иммунологические методы, а именно определение титра специфических IgG-антител к Toksokara canis методом иммуноферментного анализа (ИФА), обладающим высокой чувствительностью и достаточной специфичностью при висцеральной локализации гельминта — 93,7% и 89,3% соответственно [31]. Установлена корреляция между клиническими проявлениями, тяжестью процесса и титpами антител. Титp специфических антител 1:800 и выше с большой степенью вероятности свидетельствует о заболевании, а титpы 1:200–1:400 — о носительстве токсокаp при висцеральном токсокаpозе и патологическом процессе пpи токсокаpозе глаза. За лицами с низкими титрами противотоксокарозных антител устанавливается диспансерное наблюдение и пpи появлении клинических признаков болезни рекомендуется проведение специфической терапии. Однако необходимо помнить, что не всегда имеется прямая корреляция между титром антител и тяжестью заболевания, так как токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного. Кроме того, возможны и ложные результаты исследования: ложноположительные могут наблюдаться у больных эхинококкозами, описторхозом (в острой фазе заболевания), миграционной фазой аскаридоза; ложноотрицательные — при токсокарозе глаз, первичном иммунодефиците, длительном течении гельминтоза.
До настоящего времени нет единой схемы специфической терапии токсокароза, базирующейся на научных данных. Обычно применяют противонематодозные препараты, действующие на личиночную стадию гельминтов — альбендазол и мебендазол; ивермектин и диэтилкарбамазин [32]. Все препараты активны в отношении мигрирующих личинок и недостаточно активны в отношении тканевых форм, находящихся в гранулемах. Самым часто используемым является мебендазол, назначаемый в дозе 200–300 мг/сут в 2–3 приема, внутрь, в течение 10–14 дней. Повторный курс проводят через 2 недели. Диэтилкарбамазин назначают в дозе 3–4 мг/кг/сут в 2 приема, внутрь, в течение 21 дня. Однако наиболее широким спектром действия обладает альбендазол, эффективный в отношении большинства кишечных нематодозов и ларвальных цестодозов. Механизм действия альбендазола связан с избирательным подавлением полимеризации бета-тубулина, что ведет к деструкции цитоплазматических микроканальцев клеток кишечного тракта гельминтов. Назначается альбендазол в дозе 10 мг/кг/сут в два приема, внутрь, после еды в течение 10–14 дней. Необходимость повторного курса устанавливается после клинико-лабораторного обследования больного. Побочные явления, возникающие при применении вышеуказанных препаратов, могут быть связаны не только с токсическим действием антигельминтных препаратов, но и с реакцией организма на массовую гибель личинок токсокар. Поэтому в процессе лечения целесообразно назначать антигистаминные препараты, а в ряде случаев и кортикостероиды.
При глазном токсокарозе гранулемы удаляют микрохирургическими методами, для разрушения личинок в средах глаза применяют лазерокоагуляцию [33]. При бессимптомном течении с низкими титрами специфических антител лечение не проводится, а за больными устанавливается динамическое наблюдение.
Критериями эффективности лечения считают постепенное снижение и ликвидацию клинических проявлений токсокароза, уменьшение уровня эозинофилов и специфических антител. Вместе с тем исследования показывают, что в результате лечения процесс снижения уровня специфических антител идет медленно и не охватывает всех пациентов. Клинический эффект от лечения опережает гематологический и иммунологический. При рецидивах симптоматики, сохранении стойкой эозинофилии или повышении титра специфических антител проводят повторные курсы, иногда до 4–5.
Диспансерное наблюдение за переболевшими проводит врач-инфекционист или педиатр на протяжении не менее 6 месяцев. Больные подлежат осмотру 1 раз в 2 месяца и снимаются с учета после 2-кратного отрицательного результата на антитела методом ИФА с интервалом в 3–4 месяца. Прогноз в большинстве случаев благоприятный.
Основную роль в контроле заболеваемости токсокарозом играет традиционная профилактика, которая включает в себя соблюдение правил личной гигиены, обязательное обучение детей санитарным навыкам, своевременную дегельминтизацию собак, оборудование мест выгула собак, повышение культурного уровня владельцев собак [34].
Литература
А. С. Боткина 1 , кандидат медицинских наук
М. И. Дубровская, доктор медицинских наук, профессор
ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Токсокароз – это хроническое инфекционное заболевание, вызываемое личинками круглого червя токсокары. Для инвазии характерна лихорадка, рецидивирующие высыпания и увеличение размеров печени. Патология сопровождается поражением глазных яблок и внутренних органов: сердца, головного мозга, легких. Диагностика заключается в обнаружении специфических антител к возбудителю. Лечение этиотропное (антигельминтные препараты), также применяются средства симптоматической терапии, в некоторых случаях производятся хирургические вмешательства.
МКБ-10
B83.0 Висцеральная форма заболеваний, вызываемых миграцией личинок гельминтов [висцеральная Larva migrans]
Общие сведения

Причины токсокароза
Возбудитель – круглый червь Toxocara, наиболее часто встречаются инвазии видами Т. сanis (собачий) и T. сati (кошачий). Основной цикл развития паразита не включает в себя человеческий организм, поэтому люди оказываются случайными хозяевами гельминта, который в подобных условиях неспособен достигать половозрелой формы. Источником инфекции является больное животное (чаще собака), больной человек эпидемиологически не опасен. Считается, что доля зараженных токсокарозом среди взрослых собак варьирует от 15 до 50%, щенков – до 80%.
Больные животные выделяют яйца гельминтов с фекалиями, сами паразиты в половозрелой форме находятся у постоянного хозяина в пищеварительном тракте. Наиболее опасными считаются дворы, детские площадки, парки, поскольку контаминация земли яйцами паразита встречается в 10-40% почвенных проб. Инфицирование людей происходит контактным и пищевым путем – при поглаживании, играх со зверями, особенно бродячими, употреблении в пищу немытых ягод, фруктов и овощей. Отмечено, что тараканы могут поглощать яйца токсокар с последующим выделением до 25% потенциально жизнеспособных особей, что играет важную роль в распространении инфекции в быту.
Патогенез
После попадания яиц токсокары в тонкий кишечник человека (преимущественно двенадцатиперстную кишку) высвобождаются личинки, проникающие в системный кровоток через слизистую оболочку. Сначала токсокары заносятся в печень и правую половину сердца, затем в легочную артерию и левый желудочек, откуда выходят в большой круг кровообращения. Распространяясь по организму, личинки оседают в различных органах и тканях, вызывая геморрагические и некротические изменения, образование воспалительных очагов в виде гранулем, в центре которых находится некротизированная ткань и личинка, вокруг – воспалительный инфильтрат.
При попадании в кровеносное русло продуктов жизнедеятельности возникают аллергические реакции. Часть личинок гибнет, оставшиеся гельминты выделяют особую маскирующую субстанцию, которая позволяет им персистировать в организме до 10 лет, периодически мигрируя по кровеносной системе и поражая новые ткани. Характерной особенностью токсокар является формирование гранулем в поджелудочной железе, головном мозге, печени, легких, миокарде и мезентериальных лимфатических узлах. Патогенез поражения глаз до конца не изучен, имеются гипотезы о низкой активности инвазии и малой выраженности иммунного ответа.
Патогенез эпилепсии при токсокарозе окончательно не ясен. Предполагается, что поражение головного мозга может привести к формированию волокнистых рубцов после острого воспаления или хронических гранулем. Другая теория объясняет появление эпилептических припадков при повреждении нейронов усиленным образованием провоспалительных цитокинов из-за повышения проницаемости гематоэнцефалического барьера, вызываемого паразитами, а также аутоантителами к нейрональным элементам, которые нередко обнаруживаются у больных токсокарозом.
Классификация
Классификация токсокароза у человека основывается на глубине инвазии в организм человека. Гельминтоз практически всегда протекает с минимальной либо неспецифической клиникой (субклинически), бессимптомная форма встречается в 13% случаев заболевания, органные поражения более характерны для детей. Выделяют следующие виды токсокароза:
- Глазной.Типичен для детей старше 8 лет, подростков и молодых взрослых. Поражение зрительного аппарата обычно одностороннее, протекает в виде хронического эндофтальмита, увеита, абсцессов стекловидного тела, папиллитов, кератитов и косоглазия. При длительном течении возможна слепота.
- Висцеральный.Протекает остро или хронически с вовлечением дыхательной системы, сердца, кожи, лимфатических узлов, селезенки, печени, суставов и мышц. Часто наблюдается диарея, тошнота и рвота. Описаны поражения головного мозга: рецидивирующие головные боли, менингоэнцефалит, эпилептические припадки.
Симптомы токсокароза
Инкубационный период определить сложно, считается, что он может занимать несколько лет. При остром начале наблюдается лихорадка до 38,5°C и выше, поражения дыхательной системы – от заложенности носа, сухого кашля и першения в горле до тяжелой одышки и астматического статуса. На коже появляется зудящая сыпь в виде волдырей и пятен, при подкожном расположении личинок видны приподнятые над поверхностью прямые или извилистые красновато-коричневые ходы. У детей нередко выявляются увеличенные плотноэластические безболезненные лимфоузлы. Пациенты с токсокарозом часто предъявляют жалобы на боли в животе, тошноту, иногда – рвоту и срывы стула.
Осложнения
Наиболее частые осложнения висцерального токсокароза – бронхиальная астма, хронический бронхит и эпилепсия, глазного – отслойка сетчатки и односторонняя слепота. Подкожное расположение личинок токсокар приводит к присоединению вторичной бактериальной инфекции, образованию инфильтраов, абсцессов и флегмон, поражение легких – к тяжелым пневмониям смешанной этиологии с нарастающей дыхательной недостаточностью. Массивная инвазия гельминтов, полиорганное поражение могут стать причиной летального исхода. У беременных женщин токсокароз часто выявляется невынашивание, задержка внутриутробного развития плода.
Диагностика
Диагноз токсокароза подтверждается врачом-инфекционистом. Для исключения сочетания висцерального и глазного гельминтоза обязательным является осмотр офтальмолога, по показаниям назначаются консультации других специалистов. Диагностические методы, необходимые для верификации токсокарозного поражения, включают следующие методики:
Дифференциальную диагностику проводят с аскаридозом, при котором нередко наблюдаются кишечная непроходимость, острая обструкционная дыхательная недостаточность. Необходимо исключить описторхоз и стронгилоидоз, которые протекают с желтухой, болями в правом подреберье и срывами стула. Глазную форму токсокароза дифференцируют от ретинобластомы, проявляющейся лейкокорией, косоглазием, слезотечением, светобоязнью, вторичной глаукомой. Кожные проявления могут быть следствием укусов насекомых, воздействия аллергенов.
Лечение токсокароза
Показанием для стационарного лечения являются висцеральные формы болезни. Постельный режим назначается только при наличии лихорадки и рекомендуется до 2-4 дней устойчивого отсутствия высоких цифр температуры тела. Специальной диеты нет, однако, учитывая некоторые побочные эффекты применяемых препаратов, рекомендуется воздержаться от приема жирной, жареной пищи, алкоголя, специй, маринадов, сладостей. Важно соблюдение питьевого режима, исключение контакта с возможными пищевыми и бытовыми аллергенами. Недопустимо самовольное прекращение начатого медикаментозного лечения.
- Антигельминтная терапия. Высокоэффективными антигельминтными средствами для разрушения мигрирующих личинок считаются албендазол, мебендазол, диэтилкарбамазин, которые применяются в таблетированных формах. В отношении токсокар, находящихся в гранулемах, данные препараты не обладают выраженным нейтрализующим эффектом.
- Хирургические методы лечения применяются при глазном токсокарозе и включают в себя микрохирургическое удаление гранулем, лазерную коагуляцию для расщепления личинок в средах глаза и коррекции отслойки сетчатки.
- Симптоматическая терапия проводится по показаниям. Включает жаропонижающие (парацетамол, целекоксиб), дезинтоксикационные (хлосоль, глюкозо-солевые растворы), десенсибилизирующие (глюконат, хлорид кальция), антигистаминные (хлорапирамин, дезлоратадин), отхаркивающие (ацетилцистеин, мукалтин), ферментативные (панкреатин) и другие средства.
Прогноз и профилактика
Прогноз при неосложненных формах благоприятный, летальных случаев не описано. Длительность приема лекарственных средств может составлять до 3-4 недель и более, иногда требуются несколько курсов с перерывами в 2-4 месяца. Критериями эффективности считаются исчезновение клиники, снижение уровня антител и эозинофилии крови. Описаны случаи диссеминированного токсокароза среди ВИЧ-инфицированных лиц в стадии СПИДа, а также пациентов, длительно принимающих системные глюкокортикостероиды или проходящих лучевую терапию по поводу онкологических болезней.
Профилактические вакцины на основе ДНК показали положительный эффект в экспериментах на мышах, исследования в настоящее время продолжаются. Рекомендуется осуществлять контроль за популяцией бродячих животных, проводить выгул собак на специально отведенных территориях. Важными мерами неспецифической борьбы с заболеваемостью являются отучение детей от поедания земли, привитие навыков личной гигиены после игр на улице, песочнице, общения с животными; тщательное мытье ягод, зелени, овощей и фруктов перед едой; назначение антигельминтных препаратов беременным собакам, новорожденным щенкам.
2. Токсокароз. Клиника. Диагностика. Лечение. Профилактика. Информационно¬методическое пособие. – 2004.
4. Токсокароз у детей/ Глазунова Л.В., Артамонов Р.Г., Бекташянц Е.Г., Куйбышева Е.В., Шиц О.Л., Кирнус Н.И., Иванова Е.Ю. // Лечебное дело. – 2008.
Токсокароз у детей — это тканевой гельминтоз, который вызван паразитами рода Toxocara. Заболевание имеет полиморфную клиническую картину. Типичные признаки висцеральной формы: легочной синдром, субфебрильная лихорадка, нарушения пищеварения. При глазном токсокарозе возникают отек и гиперемия век, болезненность, экзофтальм. Диагностика гельминтоза включает серологические и гистологические анализы, методы визуализации (рентгенография грудной клетки, УЗИ органов живота, ЭКГ, ЭхоКГ). Лечение проводится этиотропными противопаразитарными препаратами, гормонами и антигистаминными средствами, пробиотиками и ферментами.
МКБ-10
Общие сведения
Токсокароз — самое распространенное на территории России паразитарное заболевание, интенсивный показатель которого составляет 380 случаев на 100 тыс. населения. Наиболее подвержены дети дошкольного возраста. Среди возрастной группы до 4 лет половых различий заболеваемости не выявлено, в категории 5-14 лет паразиты чаще поражают мальчиков, а среди подростков 14-18 лет больше заражаются девочки. Несмотря на высокую частоту встречаемости, диагностика и лечение токсокароза затруднены, что связано с полиморфностью клинической картины.

Причины
Основной фактор риска инфицирования токсокарами — несоблюдение детьми санитарно-гигиенических норм, поэтому чаще всего болезнь поражает дошкольников, которые играют в песочнице, а потом берут все грязными руками. В группу риска относят семьи, у которых есть домашние животные, жители пригородов и сельской местности. Высокий риск заражения токсокарозом и другими гельминтозами у детей, которые страдают геофагией — патологической тягой к поеданию земли и песка.
Патогенез
Инкубационный период составляет несколько дней, но не исключено латентное течение гельминтоза. Передача инфекции ребенку происходит преимущественно 3 путями: контактно-бытовым — при играх с домашними или бродячими животными, алиментарным — при поедании овощей, зелени, которые загрязнены землей с цистами токсокар, водным — при употреблении зараженной некипяченой воды. Редкий путь инфицирования — гео-оральный, который наблюдается у детей с геофагией.
Жизненный цикл возбудителя достаточно сложен, он проходит в организме животных и частично в почве. В ЖКТ человека поступают зрелые цисты, из которых образуются личинки токсокар. Через стенку кишечника они проникают в кровоток: сначала по венозной системе достигают правых отделов сердца, затем попадают в легочные сосуды, оттуда — в левую половину сердца и далее разносятся по всем внутренним органам.
Личинки могут длительное время сохраняться в тканях в латентном состоянии, а их активация происходит при снижении иммунитета. Паразиты выделяют антигены, которые провоцируют аллергические реакции немедленного и замедленного типов, образование эозинофильных гранулем. Специфические для токсокароза тканевые элементы в центре имеют зону некроза, вокруг нее расположены эозинофилы, фагоциты и лимфоидные клетки.
Классификация
В литературе по детским инфекционным болезням существует несколько вариантов систематизации токсокароза:
- по течению: типичные и атипичные (стертые, бессимптомные) варианты;
- по локализации поражения: висцеральная и глазная формы;
- по тяжести: легкое, среднетяжелое и тяжелое течение.
По длительности токсокароз у детей бывает острым (до 3 месяцев) и хроническим, который подразделяется на непрерывный и рецидивирующий вариант.
Симптомы токсокароза у детей
Висцеральная форма
Клинические признаки гельминтоза зависят от объема поглощенных цист токсокары, степени распространения личинок по организму и уровня иммунной защиты. У детей чаще встречается висцеральная форма, которая ассоциирована с одновременным проникновением большого количества гельминтов в организм. Вначале токсокароз проявляется неспецифическими признаками: повышением температуры до субфебрильных цифр, небольшим ознобом, слабостью, вялостью.
У 65% детей первично выявляются симптомы поражения легких. Пациенты жалуются на кашель, который усиливается по ночам, одышку при физических нагрузках. Возможны катаральные явления в виде насморка и заложенности носа, отхаркивания слизистой мокроты при кашле. Хронический вариант токсокароза иногда протекает под маской рецидивирующих бронхитов или персистирующей бронхиальной астмы, классическое лечение которых не дает должного эффекта.
Помимо легочного синдрома, при гельминтозе наблюдается увеличение и болезненность нескольких групп лимфатических узлов. У ребенка возможна асимметрия живота и тяжесть в правом подреберье, вызванные увеличением размеров печени. Типичным проявлением считается рецидивирующая лихорадка неясного генеза. На коже ребенка образуются зудящие волдыри, на ладонях и ступнях формируются безболезненные узелки.
Глазная форма
Глазная форма токсокароза начинается с умеренной отечности и покраснения верхнего века, которые сохраняются не более 5 дней. Симптомы повторяются на протяжении полугода с промежутками от нескольких дней до 2-3 недель. Постепенно отек становится более выраженным, заметен экзофтальм, ребенок жалуется на боли при движениях глазом. Поражение при токсокарозе чаще одностороннее.
Осложнения
Если лечение гельминтоза не проводится вовремя, происходят паразитарные и аутоиммунные повреждения внутренних органов. Зачастую у ребенка формируется тяжелая персистирующая бронхиальная астма, которая сопровождается бронхообструктивным синдромом и дыхательной недостаточностью. Нарушения вентиляции и снижение местного иммунитета — предрасполагающие факторы развития у зараженных детей затяжных пневмоний, легочных абсцессов.
Поражение органов ЖКТ проявляется панкреатитом, гепатитом, синдромом мальабсорбции и мальдигестии. Также встречаются осложнения со стороны ЦНС (парезы, параличи, нарушения чувствительности), опорно-двигательного аппарата (синовиты, артриты). При токсокарозе возможен летальный исход, если личинки паразита мигрируют в миокард и жизненно важные центры головного мозга. Смерть наступает от острой сердечной недостаточности, остановки дыхания.
Диагностика
Обследованием ребенка занимается педиатр, который при подозрении на заражение гельминтами дает направление на консультацию детского инфекциониста. При физикальном исследовании органов дыхания обращают внимание на хрипы и ослабленное дыхание, при пальпации живота врач обнаруживает гепатомегалию, при внешнем осмотре выявляется аллергическая сыпь. В план диагностики включаются:
- Рентгенография ОГК. Обзорную рентгенограмму в двух проекциях делают для исследования степени поражения легочной ткани. На снимках заметны множественные очаги инфильтрации, усиление бронхиального рисунка, могут быть признаки эмфиземы. Для детальной диагностики проводится спирометрия (школьникам), тест на бронхиальную обструкцию.
- Биопсия. Обнаружение личинок токсокары в биоптатах — наиболее достоверный способ диагностики паразитарного процесса. Детям наиболее часто делают чрескожную пункционную биопсию печени. Если на кожных покровах есть характерные узелки, их биоптаты также используют для гистологической верификации диагноза.
- Дополнительные инструментальные методы. Для оценки состояния гепатобилиарной системы, поджелудочной железы и кишечника ребенка назначается УЗИ брюшной полости. При перебоях в работе сердца показана ЭКГ и эхокардиография. При затруднениях в диагностике выполняют КТ легких, брюшных органов.
- Серологические реакции. ИФА обладает высокой чувствительностью (93,7%) и специфичностью (89,3%) при висцеральной форме токсокароза. При титре антител 1:200 или 1:400 говорят о бессимптомном носительстве, а значение 1:800 и выше указывает на активный процесс, лечение которого нужно начинать незамедлительно.
- Общеклинические анализы. В гемограмме детей с токсокарозом обнаруживают эозинофилию, лейкоцитоз, повышение СОЭ. При биохимическом исследовании крови определяют гипергаммаглобулинемию, возрастание IgE, в печеночных пробах — синдром цитолиза. Обязательно исследуют кал на яйца глист, чтобы исключить другие гельминтозы.
Лечение токсокароза у детей
Этиотропное лечение проводится противогельминтными препаратами группы бензимидазолов. Они назначаются короткими курсами в возрастных дозировках. Спустя 3 месяца выполняется иммунологический контроль терапии и при негативной динамике подбирается новый курс противопаразитарных средств. Патогенетическое и симптоматическое лечение гельминтоза предполагает прием препаратов следующих групп:
- Кортикостероиды. Рекомендованы для купирования аллергических и аутоиммунных реакций при тяжелых формах токсокароза. Уменьшают активность воспалительного процесса, предотвращают системные осложнения.
- Антигистаминные средства. Используются при кожных аллергических проявлениях — зудящих дерматозах, отеке Квинке. Быстро устраняют субъективный дискомфорт, уменьшают отечность и покраснение кожи ребенка.
- Пробиотики. Применяются для нормализации пищеварительной функции, восстановления микробиоты кишечника. При мальбасорбции обычно терапия дополняется пищеварительными ферментами. Детям, страдающим диарейным синдромом, показаны энтеросорбенты.
Прогноз и профилактика
В большинстве случаев противопаразитарное лечение эффективно уничтожает личинок гельминтов и предупреждает необратимые поражения внутренних органов. Иногда токсокароз протекает в бессимптомной форме, что коррелирует с хорошей активностью иммунной системы. Неблагоприятный прогноз устанавливают при массивной инвазии, наличии у ребенка первичного или вторичного иммунодефицита.
В отношении больного и его окружения противоэпидемические меры и изоляция не проводятся. Профилактика токсокароза предполагает обучение ребенка правилам личной гигиены, тщательное мытье овощей и зелени, использование бутилированной или кипяченой водопроводной воды. Важную роль отводят лечению бездомных животных, организации приютов, что уменьшает количество естественных резервуаров инфекции.
1. Особенности течения токсокароза у детей/ Т.В. Сорокман, И.И. Перкас// Актуальная инфектология. — 2018.
4. Токсокароз у детей/ Л.В. Глазунова, Р.Г. Артамонов, Е.Г. Бекташянц, Е.В. Куйбышева// Лечебное дело. — 2008.
Читайте также:

