Что такое пневмоцистная инфекция
Обновлено: 24.04.2024
Пневмоцистоз - оппортунистическая инфекция с преимущественным поражением легких, у больных с иммунодефицитом способная к генерализации. Относится к числу наиболее распространенных СПИД-индикаторных болезней.
Возбудитель пневмоцистоза - Pneumocystis carina (Delanoe M., Delanoe P., 1912) - одноклеточный микроорганизм. По морфологическим признакам и чувствительности к антипротозойным препаратам их длительное время относили к типу простейших. Постепенно у пневмоцист начали выявлять черты, характерные для грибов. Попытки отнести их к грибам или простейшим наталкивались на нечеткость систематических критериев. По некоторым показателям они близки к Protozoa: по морфологии, наличию мейоза, присутствию в составе клеточной оболочки холестерола (а не эргостерола, как у грибов, что делает их чувствительными к антипаразитарным препаратам и нечувствительными к противогрибковому средству амфотерицину В), невозможности их культивирования на питательных средах для грибов. С грибами их сближает то, что пневмоцисты содержат структуры, подобные аскоспорам у грибов, а также фитостеролы, которых лишены животные клетки.
Метаболизм у P. carinii (синтез ароматических аминокислот, тимидина и др.) происходит, как у грибов; кроме того, у пневмоцист отсутствует спорогония, характерная для простейших. В 1988 г. Edman и Stringer, применив методы молекулярной генетики, показали, что последовательность нуклеотидов в т-РНК пневмоцист имеет высоую степень гомологии с последовательностью нуклеотидов т-РНК грибов, относящихся к дрожжам ( Saccharomycetes serevisiae). Для сравненения - аналогичные последовательности изучались также у разных видов простейших: токсоплазм, плазмодиев, акантамеб и др. По генетическим признакам пневмоцисты были ближе всего к грибам. Но это грибы, которые имеют ряд черт, сближающих их с простейшими. Так, м-ДНК P. carinii содержит гены дегидрогеназы и цитохромоксидазы, которые на 60% подобны генам грибов и только на 20% генам простейших. Аналогичные свойства были установлены и у других видое грибов.
По последним данным пневмоцисты относят к грибам возможно, к актиномицетам или высшим грибам - аско- или базидомицетам. Одновременно некоторые исследователи считают P. carinii филогенетически древним возбудителем неопределенного систематического положения, который в процессе эволюции утратил характерные таксономические признаки (Т. В. Бейер, 1989 г.). Современный молекулярно-биологический и молекулярно-генетический анализ не может окончательно определить их видовую принадлежность. Для решения этого вопроса необходимо ультраструктурное исследование возбудителя, изучение его филогенеза и усовершенствование техники культивирования пневмоцист.
P. carinii - внеклеточный паразит, тропный к легочной ткани. В цикле развития пневмоцисты выделяют вегетативную форму (трофозоит), предцисту и цисту с внутрицистными тельцами.
Трофозоиты - клетки размером 1-8 мкм, покрытые тонкой оболочкой. Их форма разнообразная и мобильная (овальная, амебоподобная и др.). Она зависит от формы структур, к которым они прилегают. От поверхности трофозоита отходят микровыросты и длинные отростки в виде филоподий. За их счет пневмоцисты соединяются между собой и прикрепляются к клеткам хозяина. Ядро ограничено двумя мембранами. В цитоплазме выявляются митохондрии, свободные рибосомы, мелкие и крупные вакуоли, полисахариды, капли липидов. Иногда встречаются сдвоенные клетки, что может свидетельствовать о делении или копуляции. По данным электронно-микроскопических исследований, трофозоиты плотно прилегают к альвеолоцитам первого порядка. Филоподий могут углубляться в клетку легкого хозяина, не разрывая ее оболочку. Одновременно мембрана альвеолоцита может входить в тело трофозоита, не повреждая его. Физиологический контакт возбудителя с хозяином осуществляется через систему микропиноцитарных пузырьков.
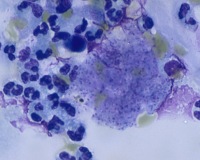
Предцисты - овальные клетки диаметром 2-5 мкм, лишенные пелликулярных выростов. В них происходит деление ядер. Цисты P. carinii округлой или овальной формы размером 3,5 - 10 мкм, иногда до 30 мкм (рис. 20). Они покрыты плотной трехслойной оболочкой и внешней мембраной. В цитоплазме содержится от 1 до 8 внутрицистных телец, которые выходят в просвет альвеолы после разрыва оболочки цисты. Пустые цисты имеют неправильную форму, чаще в виде полумесяца, иногда в них выявляются внутрицистные тельца. Размер последних 1-2 мкм. Пелликула внутрицистных телец вновь образуется после выхода из разрушенной цисты. Они становятся внеклеточными трофозоитами и начинают новый раунд жизненного цикла.
Патогенез пневмоцистоза определяется биологическими свойствами возбудителя и состоянием иммунной системы хозяина. Пропагативные формы пневмоцист, которые до настоящего времени не описаны, минуют верхние дыхательные пути, достигают альвеол и начинают жизненный цикл в организме нового хозяина. Прикрепление трофозоитов к альвеолоцитам первого порядка опосредуется многими механизмами, в частности большим количеством поверхностных гликопротеинов у P. carinii, которые взаимодействуют с протеинами легочной ткани через маннозные рецепторы на клетках хозяина, особенно макрофагах. Поверхностные гликопротеины пневмоцист высоко иммунногенные. Прикрепление пневмоцист сопровождается пролиферацией возбудителя, его взаимодействием с сурфактантом, освобождением токсических метаболитов. Защиту организма хозяина от P. carinii осуществляют Т-лимфоциты, альвеолярные макрофаги, специфические AT. Взаимодействие микро- и макроорганизма остается на субклиническом уровне, пока иммунная система не нарушена. Компроментация иммунной системы стимулирует рост численности пневмоцист.
При СПИДе число паразитов в альвеолах и бронхах настолько большое, что нарушается альвеолярная вентиляция, и больной умирает от нарастающей легочной недостаточности. Разрушение альвеолярно-капиллярной мембраны может приводить к диссеминации пневмоцист с основного места локализации.
На гистологических срезах легких, пораженных пневмоцистами, возникает картина, характерная только для пневмоцистоза. Расширенные бронхиолы, альвеолы и мелкие бронхи заполнены эозинофильной пенистой массой. Альвеолярный эпителий, контактирующий с возбудителем, гипертрофирован, стенки альвеол утолщены за счет расширения капилляров и инфильтрации лимфоидно-гистиоцитарными элементами. Вокруг сосудов наблюдаются обильные скопления плазмоцитов. На стенках бронхов и альвеол видны отдельные круглые формы и пласты пневмоцист, стелящиеся по стенкам альвеол. Выявляются разорванные цисты P. carinii с выбросом в окружающее пространство внутрицистных телец, которые наращивают цитоплазму и превращаются в трофозоиты, а потом дозревают до цист. Гистологическая картина легких напоминает альвеолярный липопротеиноз с явлениями экссудации, лейкоцитоза и сетчатого склероза. Заполненные пенистой массой группы альвеол и альвеолярные ходы чередуются с участками компресионного ателектаза и эмфиземы.
Для построения собственной клеточной оболочки P. carinii использует фосфолипиды (ненасыщенный фосфатидилхолин) сурфактанта хозяина. Это приводит к общему повреждению сурфактантного обмена: дисбалансу в уровнях сурфактантных фосфолипидов и протеинов, гиперсекреции сурфактанта. Выраженное размножение и созревание P. carinii прямо коррелирует с пиком активности сурфактантной системы. Гиперпродукция сурфактанта на фоне развивающейся дисфункции альвеолярных макрофагов приводит к заполнению альвеол относительно гомогенной пенистой массой. Механическое разрушение и инактивация сурфактанта белками экссудата усугубляют гипоксическое состояние тканей, активируют фиброзирование межальвеолярных перегородок. Происходит снижение секреторной функции альвеолоцитов второго порядка и возрастание их пролиферативной активности. Плоский альвеолярный эпителий замещается кубическим. У больных СПИДом размножение в альвеолах P.carinii часто происходит в составе смешанной инфекции (бактериальная флора, грибы). Это создает патоморфологическую картину пневмоцистоза.
После проведенного лечения и выздоровления полного восстановления сурфактантной системы легких не происходит. Это является причиной колонизации дыхательной системы больных СПИДом нозокомиальными, стойкими к антибиотикам широкого спектра действия штаммами микроорганизмов. Поэтому рецидивирующие пневмонии у больных СПИДом - нередкое явление.
Пневмоцистная пневмония – это тяжелая форма интерстициального легочного воспаления, вызываемая пневмоцистами и развивающаяся на фоне выраженных иммунодефицитных состояний. Клиническое течение характеризуется нарастающей одышкой, непродуктивным кашлем, фебрильной лихорадкой, болями в груди, развитием сердечно-легочной недостаточности. Диагноз ставится на основании рентгенологических признаков, состояния иммунного статуса, лабораторной идентификации патогена в крови, БАЛ, мокроте, биоптате (ПЦР, серологические тесты, РНИФ). Для этиотропной терапии используются сульфаниламидные, противопротозойные, иммуномодулирующие средства.
МКБ-10


Общие сведения
Пневмоцистная пневмония (ПП) относится к оппортунистическим инфекциям, поражающим лиц с иммунодефицитом и иммуносупрессией. При этом большинство людей с нормальным уровнем иммунитета переносит пневмоцистную инфекцию в виде ОРВИ. Антитела к возбудителю имеют около 90% взрослого населения, около 10% являются бессимптомными носителями пневмоцист – именно они представляют наибольшую угрозу для иммунокомпрометированных пациентов. Пневмоцистная пневмония является самой тяжелой клинической формой пневмоцистоза.

Причины
Характеристика возбудителя
Pneumocystis jirovecii – микроорганизм, вызывающий пневмоцистную пневмонию и другие виды пневмоцистоза у человека. До недавнего времени пневмоцисты считались простейшими, однако в 1988 г. на основании ряда характерных генетических, морфологических и биохимических признаков были отнесены к грибам семейства актиномицетов. Пневмоцисты обладают тропизмом к легочной ткани, весь их жизненный цикл протекает внутри альвеол и проходит 4 стадии:
- Трофозоит. Представляет собой вегетативную стадию P. Jirovecii. Имеет амебоидную форму, диаметр 1-5 мкм, одно ядро и тонкую двухслойную мембрану. Прикрепляется к альвеолоцитам, где увеличивается в размерах и делится.
- Прециста. Имеет овальную форму, диаметр 5 мкм. В ранней стадии содержит одно ядро, окруженное митохондриями, на поздней – 2-6 ядер с мембранами.
- Циста. Зрелая циста округлой формы, с 3-слойной стенкой, диаметром 7-8 мкм. Внутри цисты содержится четное количество (обычно 8 шт.) внутрицистных телец ‒ спорозоитов.
- Спорозоит. При разрыве зрелых цист из них высвобождаются спорозоиты, часть которых обладает одинарным набором хромосом (являются гаплоидными). Сливаясь, они вновь образуют трофозоиты, и жизненный цикл патогена повторяется.
В описанном цикле различают две фазы: неполовую, или асексуальную (деление трофозоита), и половую, или сексуальную (спорозоит-трофозоит-прециста-циста).
Пути передачи
Источниками P. jirovecii являются носители (бессимптомные или больные ОРЗ) и больные пневмоцистной инфекцией. В 30% случаев выявляется вовлеченность в эпидемический процесс медицинских работников. При кашле и чихании носители выделяют мелкодисперсный аэрозоль, содержащий патогены. Заражение восприимчивого макроорганизма происходит при вдыхании контаминированного воздуха (воздушно-капельным, воздушно-пылевым путем). Воротами для входящей инфекции служат дыхательные пути. Редко реализуется трансплацентарный путь передачи.
Характерны внутрисемейные и внутрибольничные эпидемические вспышки пневмоцистной пневмонии. Последние чаще происходят в отделениях недоношенных, домах престарелых, инфекционных стационарах. Пик детской заболеваемости пневмоцистной пневмонией приходится на конец лета – начало осени, взрослые болеют круглогодично.
Группы риска
Пневмоцисты являются типичными оппортунистами, поскольку вызывают манифестную инфекцию только при выраженном дефиците клеточного и гуморального иммунитета у определенного контингента пациентов. К группам риска по заболеваемости пневмоцистной пневмонией относятся:
- ВИЧ-инфицированные и больные СПИДом;
- пациенты с ЦМВ-инфекцией;
- недоношенные дети и младенцы с ЗВУР;
- дети, страдающие гипотрофией, рахитом;
- больные, получающие иммуносупрессивную терапию (по поводу лейкозов, миеломной болезни, других видов рака, трансплантации органов, коллагенозов);
- пациенты с первичными иммунодефицитами, болезнями крови (анемией, полицитемией), туберкулезом, патологией почек.

Патогенез
Пневмоцисты присутствуют в дыхательных путях здоровых людей, но вызывают пневмоцистную пневмонию только у лиц с нарушением гуморального и клеточного звена иммунитета. Экспериментально доказано, что ведущую роль в механизме пневмоцистоза играет снижение Т-хелперов (критическим является снижение СД4+ лимфоцитов ˂300-200 клеток/мкл), увеличение количества цитотоксических лимфоцитов СД8+.
P. Jirovecii с помощью особых выростов – филоподий – прикрепляется к альвеолоцитам первого порядка и альвеолярным макрофагам. Клеточной адгезии также способствуют гликопротеины пневмоцистов, которые взаимодействуют с фосфолипидами, апопротеинами, мукополисахаридами, сурфактантом альвеолярного эпителия. В условиях иммунокомпрометации цисты размножаются, используя сурфактант-ассоциированные белки, выделяют токсические метаболиты.
Происходит разрушение альвеолоцитов, заполнение альвеол пенистым экссудатом, содержащим большое количество пневмоцист на разных стадиях развития, воспалительные клетки, детрит. Интерстициальная ткань инфильтрируется плазматическими клетками. Развивается интерстициальная плазмоклеточная пневмония. Межальвеолярные перегородки гипертрофируются, что приводит к резкому снижению диффузии газов (альвеолярно-капиллярный блок), формированию дыхательной недостаточности и тяжелой гипоксии.
Классификация
В соответствии с патоморфологическими критериями в современной пульмонологии выделяют три стадии пневмоцистной пневмонии:
- I стадия. Происходит прикрепление пневмоцист к альвеолярной стенке. Воспалительная реакция и клинические проявления отсутствуют.
- II стадия. Отмечается десквамация альвеолоцитов, увеличение числа возбудителей в форме цист в макрофагах. В эту стадию появляются начальные клинические проявления пневмоцистной пневмонии.
- III стадия. Развивается альвеолит, плазмоцитарная инфильтрация интерстиция, гигантские скопления пневмоцист в макрофагах и альвеолах. Соответствует разгару заболевания.
Этапы развития пневмоцистной пневмонии:
- отечная фаза ‒ длится 7-10 дней, характеризуется нарастанием симптоматики;
- ателектатическая фаза ‒ продолжается в течение 4-х недель, сопровождается выраженной легочной недостаточностью;
- эмфизематозная фаза – имеет различную длительность, знаменуется обратным развитием симптоматики.
Симптомы пневмоцистной пневмонии
Инкубационный период вариабелен – от 7-10 дней до 2-4 недель (у больных СПИДом – до 10 недель). В отечную стадию клинические признаки пневмоцистной пневмонии легко спутать с обычной респираторной инфекцией. Симптомы нарастают постепенно: вначале беспокоит слабость, недомогание, субфебрилитет. Затем появляется одышка при умеренной нагрузке, боли в грудной клетке, сухой кашель.
В ателектатической стадии лихорадка принимает фебрильный характер, усиливается интоксикационный синдром (отсутствие аппетита, снижение веса, потливость по ночам). Кашель становится коклюшеподобным, постоянным, особенно беспокоит в ночное время суток. Одышка до 30-50 дыхательных движений в минуту выражена в покое. Отмечаются бледность кожных покровов с носогубным цианозом, тахикардия. В этот период пациент может погибнуть от сердечно-легочной недостаточности (СЛН).
У выживших пациентов наступает эмфизематозная стадия. Температура тела снижается, дыхательные расстройства исчезают. В исходе пневмоцистной пневмонии формируется эмфизема легких, легочное сердце. Пневмоцистная пневмония часто протекает в ассоциации с туберкулезом легких.
Четкая стадийность при пневмоцистозе прослеживается в основном у детей раннего возраста. У ВИЧ-инфицированных болезнь имеет стертое затяжное течение, у ВИЧ-негативных лиц с иммунодефицитом – более активное, с быстрым нарастанием СЛН.
Осложнения
Типичными осложнениями, развивающимися в разгар болезни, являются пневмоторакс, подкожная эмфизема, пневмомедиастинум, возникающие вследствие разрыва мелких кистозных образований. Возможно развитие абсцедирующей пневмонии. Эти состояния еще более усугубляют дыхательную недостаточность, повышают летальность. При значительном подавлении иммунитета может произойти генерализация пневмоцистной инфекции с мультиорганным поражением печени, селезенки, ЖКТ, щитовидной железы, органов зрения и слуха, лимфоузлов, костного мозга.

Диагностика
Из-за неспецифичности и стертости симптоматики существенной проблемой является гиподиагностика пневмоцистной пневмонии. Иногда патология диагностируется только посмертно. Все больные с подозрением на ПП должны быть в срочном порядке проконсультированы врачом-пульмонологом, инфекционистом. При выставлении диагноза опираются на следующие данные:
Дифференциальная диагностика
Комплексное клинико-лабораторное, рентгенологическое и бронхологическое обследование позволяет отличить пневмоцистную пневмонию от других поражений легких:
- легочного кандидоза;
- криптококковой пневмонии;
- цитомегаловирусной пневмонии;
- микоплазменной пневмонии;
- хламидийной пневмонии;
- туберкулеза легких;
- респираторного криптоспоридиоза;
- саркомы Капоши;
- бактериальной пневмонии.
Лечение пневмоцистной пневмонии
Стандартные антибактериальные средства при ПП неэффективны. В настоящее время препаратами первой линии считаются комбинированные сульфаниламиды, оказывающие противомикробное, бактерицидное и противопротозойное действие. Могут назначаться как перорально, так и внутривенно. Курс лечения составляет 1-3 недели.
При выраженных токсических эффектах и резистентности подбираются другие антибиотики, активные в отношении пневмоцист (линкозамиды, противолепрозные, противомалярийные, антипротозойные препараты). Из-за массовой гибели патогенов в первые дни терапии состояние пациентов с пневмоцистной пневмонией может ухудшиться, в связи с чем целесообразно назначение кортикостероидов.
Прогноз и профилактика
Смертность от пневмоцистной пневмонии достигает 50% среди недоношенных детей, 25-40% ‒ среди больных СПИДом. У 10-30% иммунокомпрометированных пациентов через несколько месяцев после излечения возникают рецидивы ПП. При отсутствии лечения летальность 100%.
Профилактическая работа реализуется в двух направлениях: эпидемиологическом и медикаментозном. Первый аспект предполагает широкое тестирование на пневмоцистную инфекцию представителей групп риска: пациентов с ВИЧ, онкопатологией, иммунодефицитами, недоношенных детей, сотрудников роддомов и стационаров. Второе направление – это фармакопрофилактика пневмоцистной пневмонии у лиц с количеством СД4+ клеток ˂200. Она заключается в приеме сульфаниламидов в профилактических дозах длительными курсами.
1. Пневмоцистная пневмония. Этиология, патогенез, клиника, дифференциальная диагностика, лечение (лекция)/ Боровицкий В.С.// Проблемы медицинской микологии. – 2012.
2. Пневмоцистная пневмония: исторические, эпидемиологические, клинико-морфологические аспекты/ Марковский В. Д., Плитень О. Н., Мирошниченко М. С., Мирошниченко А. А.// Annals of Mechnikov Institute, - 2012. - №3.
3. Особенности пневмоцистной пневмонии у ВИЧ-инфицированных лиц/ Пузырёва Л.В., Сафонов А.Д., Мордык А.В.// Медицинский вестник Северного Кавказа. – 2016. – Т.11, №3.
4. Пневмоцистоз. Современное состояние проблемы/ Каражас Н.В.// Альманах клинической медицины. – 2010.
Пневмоцистоз – оппортунистическая инфекция дыхательных путей, чаще поражающая детей раннего возраста, а также лиц с ослабленным иммунитетом. Пневмоцистоз может протекать в форме ОРЗ, ларингита, обструктивного бронхита, обострения ХЗЛ, интерстициальной пневмонии. Диагностика пневмоцистоза основана на обнаружении пневмоцист в мокроте и бронхиальном секрете с помощью микроскопии и ПЦР; данных гистологического исследования биоптатов бронхов; рентгенографии и КТ легких, сцинтиграфии, спирографии. Для проведения противопневмоцистной терапии используются препараты сульфаметоксазол+триметоприм, пентамидин, комбинация триметоприма с дапсоном и другие схемы лечения.
МКБ-10
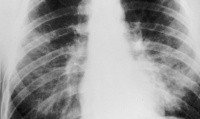
Общие сведения
Пневмоцистоз – легочная инвазия, вызываемая пневмоцистами и протекающая преимущественно в виде пневмоцистной пневмонии. Пневмоцистоз является иммунодефицит-ассоциированным инфекционным заболеванием, которым чаще всего болеют недоношенные дети, а также пациенты с первичными и вторичными иммунодефицитами. Смертельную опасность пневмоцистоз представляет для больных ВИЧ/СПИДом: при отсутствии лечения заболевание неизбежно заканчивается летальным исходом. Пневмоцистоз может возникать как спорадическая или внутрибольничная инфекция в отделениях педиатрии, гемобластозов, пульмонологии, противотуберкулезных инфекционных стационарах.

Причины пневмоцистоза
На сегодняшний день вопрос с видовой принадлежностью возбудителя пневмоцистоза окончательно не решен. В течение длительного времени микроорганизм Pneumocystis Carinii относили к простейшим класса споровиков. Однако в настоящее время доминирует точка зрения, что пневмоцисты занимают промежуточное положение между низшими и высшими грибами. В своем развитии пневмоцисты претерпевают 4 стадии: трофозоита, предцисты, цисты и спорозоита, протекающие на альвеоцитах. При разрыве оболочки созревшей цисты из нее выходят спорозоиты, которые проникают в легочные альвеолы, запуская очередной цикл стадийного развития пневмоцист новой генерации.
Источником эпидемиологической опасности выступает инвазированный человек (больной или носитель), выделяющий спорозоиты с частицами слизи во внешнюю среду при кашле или чихании. Передача возбудителей пневмоцистоза происходит по аспирационному механизму, воздушно-капельным, воздушно-пылевым, ингаляционным или аэрогенным путями. Считается, что среди клинически здоровых лиц до 10% являются носителями пневмоцист, однако у людей с нормально функционирующей иммунной системой инвазия протекает бессимптомно. Риску заболеваемости манифестными формами пневмоцистоза, главным образом, подвержены недоношенные новорожденные; дети с гипогаммаглобулинемией, гипотрофией, рахитом; больные ВИЧ/СПИДом и туберкулезом; пациенты, получающие иммуносупрессивную терапию по поводу коллагенозов, злокачественных новообразований, гематологических и лимфопролиферативных заболеваний, трансплантации органов и пр.
Пневмоцистоз развивается при снижении количества СД4+ клеток (Т-хелперов) в 4 и более раз по сравнению с нормой и достижении уровня менее 200 клеток в 1 мкл. При нарушении клеточного и гуморального иммунитета пневмоцисты начинают активно размножаться в альвеолах, вызывая развитие реактивного альвеолита, образование пенистого альвеолярного экссудата, содержащего пневмоцисты, лейкоциты, клеточный детрит и фибрин. При прогрессировании патологического процесса возникают участки ателектазов в легких, буллезное вздутии легочной ткани, что сопровождается нарушением вентиляции и газообмена, развитием дыхательной недостаточности.
Симптомы пневмоцистоза
В клиническом течении пневмоцистоза выделяют отечную (1-7 недель), ателектатическую (около 4-х недель) и эмфизематозную стадии. У части больных пневмоцистоз может протекать в виде ларингита, обструктивного или астматического бронхита, бронхиолита; в остальных случаях развивается пневмоцистная пневмония.
Инкубационный период пневмоцистоза занимает от 10 дней до 2-5 недель. Проявления отечной стадии развиваются постепенно и на ранних этапах включают в себя субфебрилитет, слабость, вялость. В конце первого периода присоединяется сухой кашель, тахипноэ, одышка. Признаками развивающегося пневмоцистоза у грудных детей может служить вялое сосание, отказ от кормления, плохая прибавка в массе тела, цианоз носогубного треугольника. Рентгенологические изменения в легких в отечной стадии пневмоцистоза отсутствуют; аускультативно определяется жестковатое дыхание, мелко- и среднепузырчатые хрипы; перкуторно - тимпанит в верхних отделах грудной клетки.
В ателектатической стадии пневмоцистоз может осложниться развитием пневмоторакса, экссудативного плеврита, легочного сердца, отека легких, а в случае присоединения бактериальной или грибковой инфекции – абсцессом легких. Летальные исходы в этот период обычно обусловлены дыхательной и сердечной недостаточностью. Третья, эмфизематозная стадия пневмоцистоза характеризуется уменьшением одышки и улучшением общего состояния больных. В исходе пневмоцистоза развивается эмфизема легких, сопровождающаяся значительным снижением показателей функции внешнего дыхания.
Диагностика
Клинические, физикальные и рентгенологические данные при пневмоцистозе не являются патогномоничными, что затрудняет своевременную диагностику заболевания. Между тем, пневмоцистную пневмонию всегда следует исключать у иммунокомпрометированных пациентов. С целью верификации пневмоцистоза проводится комплекс лабораторных и инструментальных исследований.
Для подтверждения диагноза пневмоцистоза выполняется бронхоскопия с забором бронхиального секрета, трансбронхиальная биопсия легкого, сцинтиграфия легких с галлием-67. Для лабораторной детекции P.carinii микроскопически исследуются окрашенные мазки мокроты, бронхиальный и трахеальный аспират; выполняется гистологическое исследование биоптатов, исследование мокроты методом ПЦР. Проводится иммунологическая диагностика: определение титра противопневмоцистных IgG и IgM в сыворотке крови с помощью РИФ и ИФА. Дифференциальную диагностику пневмоцистоза необходимо проводить с цитомегаловирусной, хламидийной, уреаплазменной, бактериальной пневмонией, туберкулезом легких, саркомой Капоши и др.
Лечение пневмоцистоза
Лечение пневмоцистоза проводится в стационаре. Лица с иммунодефицитом и недоношенные дети должны быть помещены в отдельные стерильные палаты с ламинарным воздушным потоком. В большинстве случаев для проведения специфической фармакотерапии пневмоцистоза используется комбинированные препараты (сульфаметоксазол+триметоприм, триметоприм+дапсон), пентамидин, эфлорнитин, атоваквон в течение 2-3 недель. Для устранения побочных эффектов терапии назначают фолиевую кислоту, глюкокортикоиды. Проводится инфузионная терапия (введение гамма-глобулина, солевых растворов, глюкозы, плазмы крови, альбумина и др.), кислородотерапия. У больных ВИЧ-инфекцией этиотропная терапия пневмоцистной пневмонии сочетается с высокоактивной антиретровирусной терапией.
Прогноз
Выживаемость при пневмоцистозе составляет 75-90%, а при повторном развитии пневмоцистной пневмонии – 60%. У 25-60% ВИЧ-инфицированных в течение года отмечаются рецидивы заболевания, поэтому больные нуждаются в проведении противорецидивного курса химиотерапии.
Грибковая пневмония – это микотическое поражение легких, возбудителями которого выступают различные виды грибов. Заболевание проявляется повышением температуры, слабостью, кашлем со слизисто-гнойной мокротой и кровохарканьем, одышкой, болью в груди, миалгией. Диагноз грибковой пневмонии ставится по данным анамнеза, симптоматики, рентгенографии легких, микробиологического, серологического и молекулярно-генетического исследований. Лечение грибковой пневмонии включает назначение антимикотических препаратов, иммунокорректоров, поливитаминов, детоксикационных и десенсибилизирующих средств.
МКБ-10
Общие сведения
Грибковая пневмония (пневмомикоз) - воспалительный процесс, развивающийся в альвеолах и паренхиме легких при внедрении и бесконтрольном размножении патогенных или условно-патогенных штаммов грибов. Грибковая пневмония может возникать как самостоятельное (первичное) заболевание при непосредственном инфицировании ткани легких или вторично, как осложнение другой фоновой, в т. ч. респираторной патологии (бронхоэктатической болезни, обструктивного бронхита, абсцесса легкого).
Грибковую пневмонию считают одной из тяжелейших форм воспаления легких, количество случаев которой в последнее время увеличивается, несмотря на использование в пульмонологии новейших антимикотических препаратов. Специфичность возбудителей и торпидное течение пневмомикозов представляют большие трудности для точной постановки диагноза и затягивают своевременное начало терапии, усугубляя воспалительные изменения.
Причины
Причиной развития грибковой пневмонии является колонизация слизистой нижних отделов респираторного тракта штаммами грибов, многие из которых - представители условно-патогенной микрофлоры. Возбудителями заболевания могут выступать грибы различных видов - плесневые (Aspergillus, Mucor), дрожжеподобные (Candida), эндемичные диморфные (Blastomyces, Coccidioides, Histoplasma), пневмоцисты (Pneumocystis). Наиболее часто при грибковой пневмонии выявляются грибы кандида (C. albicans), аспергиллы и пневмоцисты (P. carinii), обладающие преимущественным тропизмом к легочной ткани.
В зависимости от возбудителя пневмомикозы разделяют на:
Патогенные грибы - возбудители экзогенных пневмомикозов (Aspergillus, Mucor, Blastomyces, Coccidioides, Histoplasma) могут присутствовать в почве, воде, производственной и бытовой пыли, во влажных помещениях, на гнилой древесине, недостаточно обработанном медицинском оборудовании и проникать в легкие человека преимущественно при вдыхании воздуха, загрязненного мицелием и спорами (воздушно-капельно-пылевым путем). Возбудитель пневмоцистной пневмонии передается только от человека к человеку. Сначала формируется временное, а затем - стойкое носительство с развитием грибковой пневмонии.
Грибковая пневмония может проявляться как микст-инфекция (смешанная, вызванная различными типами грибов - дрожжеподобными и плесневыми) и сочетанная, обусловленная грибами и другими микроорганизмами (например, аспергиллами с грамнегативной микрофлорой). Торакальный актиномикоз является псевдомикозом, так как вызывается анаэробными бактериями рода Actinomyces и сопровождается образованием инфекционной гранулемы (актиномикомы) с прорастанием в окружающие ткани и появлением гнойных свищей.
Возбудители эндогенной грибковой пневмонии попадают в легкие из других очагов микоза, имеющихся в организме: путем аспирации (например, при кандидозе полости рта, трахеи, бронхов) или гематогенным и лимфогенным путем - при распространенном поражении. Грибы кандида, присутствующие в составе микробиоценоза кожи и слизистых дыхательного тракта, при определенных условиях активизируются, приобретают патогенность и вызывают пневмомикоз.
Факторы риска
Грибковая пневмония часто развивается у пациентов со злокачественными заболеваниями крови (острый лейкоз) и лимфопролиферативными опухолями, получающих длительную лучевую или системную химиотерапию (иммунодепресантами и глюкокортикоидами); как осложнение ВИЧ-инфекции и СПИДа, сахарного диабета, апластической анемии, туберкулеза, состояния после трансплантации органов, искусственной вентиляции легких. Возникновению грибковой пневмонии способствует нарушение нормальной микрофлоры (дисбактериоз респираторного тракта), связанное с продолжительным и нерациональным приемом антибиотиков. Среди основных факторов развития и реактивации грибковой пневмонии у 50% больных выступает агранулоцитоз. Грибковая пневмония часто сочетается с микозным поражением слизистых оболочек, кожи, ногтей.
Патогенез
Реализации патогенного потенциала грибов всегда способствует угнетение факторов специфической и неспецифической общей и местной резистентности организма с развитием иммунодефицитного состояния. Заселяя просветы бронхиол и альвеол, грибы начинают активно размножаться, вызывая миграцию лейкоцитов и скопление серозной жидкости. В период обострения микозные повреждения ткани легких характеризуются наличием зон распада в виде полостей, иногда - образованием абсцессов, в которых обнаруживаются скопления гриба; в период выздоровления на их месте появляются участки плотной грануляционной ткани.
Симптомы грибковой пневмонии
В большинстве случаев начало пневмомикоза характеризуется нечеткой клинической картиной, с незначительными, иногда атипичными симптомами и проявляется эпизодами повышения температуры, слабостью, сухим кашлем, миалгией. Интоксикация связана с действием микотоксинов. Появление гнойной мокроты при разрыве абсцессов, образованных скоплением грибов в ткани легких, делает картину заболевания более выраженной.
Массивное однократное заражение экзогенными грибками провоцирует острый процесс, в случае многократно повторяющихся поступлений небольших доз патогенов и у ослабленных пациентов пневмомикоз принимает хроническое течение с рецидивами. Избыточное развитие соединительной ткани приводит к появлению одышки, прожилок крови в мокроте (иногда, профузным легочным кровотечениям). Микст-формы пневмомикозов протекают тяжелее, чем моноинфекция. Грибковая пневмония может осложниться экссудативным или фибринозным плевритом при вскрытии абсцесса в плевральную полость или прорастании грибка в плевру; развитием дыхательной (в т. ч., острой) и сердечно-сосудистой недостаточности. Течение пневмомикозов различной этиологии имеет определенные клинические особенности.
Аспергиллез легких
Аспергиллезные пневмонии могут быть острыми и хроническими, включать тяжелые молниеносные формы. Для них часто характерны признаки абсцедирующей пневмонии, возможное вовлечение плевры и лимфоузлов, а также образование специфических нагнаивающихся гранулем. Беспокоят почти постоянные приступы кашля с обильными слизисто-гнойными или гнойными выделениями (в виде плотных комочков) и примесью крови, боли и тяжесть в груди, одышка, переходящая в удушье, длительный субфебрилитет с температурными скачками, ознобами и ночным потоотделением. Наблюдается тяжелое общее состояние, сильная слабость, анорексия и кахексия.
Возможно прорастание грибами стенок сосудов с формированием тромбозов и геморрагических инфарктов. Хроническая аспергиллезная пневмония вторично наслаивается на различные поражения легких, проявляясь симптомами основного заболевания и грибкового поражения. Локализованная форма - аспергиллома легких возникает при инфицировании грибами уже имеющейся полости в ткани легких и часто протекает бессимптомно. При грибковой пневмонии абсцедирование может стать хроническим процессом.
Кандидоз легких
Первичная кандидозная пневмония может сопровождаться признаками интоксикации при нормальной температуре тела, иногда может начинаться остро с лихорадки, одышки, кашля со скудной мокротой, охриплости голоса, боли в груди, повышенной потливости. Типично двустороннее поражение, у детей раннего возраста возможно рецидивирующее течение с переходом в хронический гранулематозный генерализованный кандидоз. Вторичная кандидозная пневмония протекает тяжело с удушающим кашлем, гнойно-кровянистой мокротой, рвотой, дегидратацией. Нередко она приобретает характер прогрессирующего деструктивного процесса с образованием в легких крупных тонкостенных кист, развитием ателектаза легкого, милиарной диссеминации или септического состояния.
Пневмоцистоз
Пневмоцистная пневмония протекает как моно- или микст-инфекция, часто асимптомно или со стертой клиникой, может латентно протекать уже в первые годы жизни. Нередка вероятность последующего реинфицирования. Характеризуется постепенным нарастанием гипоксемии и дыхательных расстройств, длительным непродуктивным кашлем на фоне скудных физикальных и рентгенографических данных. У недоношенных детей отмечается манифестная форма пневмоцистной пневмонии с длительной, резко выраженной дыхательной недостаточностью. Возникая первой из оппортунистических инфекций у иммунокомпрометированных больных, пневмоцистоз имеет достаточно длительное вялое течение, осложняясь спонтанным пневмотораксом, присоединением суперинфекции. В отсутствие специфического лечения возможен летальный исход.
Диагностика
Определение генеза грибковой пневмонии часто затруднено из-за своеобразия микотической инфекции, поэтому необходим комплексный подход с разбором анамнеза, клинических симптомов, результатов рентгенографии легких, микроскопического, культурального, серологического (ИФА, РСК, РПГА, РНИФ) и молекулярно - генетического (ПЦР) исследования мокроты, крови, лаважной и плевральной жидкости, аспирата легочной ткани.
При аспергиллезе выявляется картина абсцедирующей пневмонии и явления гнойного бронхита. При наличии данных за предшествующее лечение антибиотиками и отсутствие ответа на терапию можно изначально заподозрить грибковую пневмонию. Присутствие очага микоза в виде молочницы полости рта дает повод думать о кандидозной природе заболевания. Необходимо учитывать, что при наличии иммунодефицитного состояния риск развития грибковой пневмонии намного выше.
При грибковой пневмонии терапевт или пульмонолог аускультирует в легких множественные сначала сухие, затем влажные разнокалиберные хрипы. В крови больного выявляется эозинофильный лейкоцитоз со сдвигом влево и повышение СОЭ. На рентгенограмме определяется усиление легочного рисунка, инфильтративные тени незначительных или огромных размеров с неровными краями; при появлении абсцессов видны хаотично расположенные полости с уровнем жидкости.
При пневмомикозах споры и мицелий грибов можно выявить при микроскопии мазка мокроты и бронхоальвеолярной жидкости. Бакпосев мокроты важно провести до начала лечения, что повышает вероятность выделения и идентификации возбудителя грибковой пневмонии и проведения его количественной оценки. Прямое обнаружение ДНК и установление штамма грибов в мокроте методом ПЦР должно соотноситься с наличием клинических проявлений заболевания. Один факт колонизации грибами дыхательного тракта в отсутствие симптомов инфекционного поражения для постановки диагноза грибковой пневмонии недостаточен. ПЦР исследование крови на грибы позволяет дифференцировать диссеминированную и локальную формы микоза.
Материал из дистальных отделов бронхов получают методом бронхоскопии с бронхоальвеолярным лаважем. В смыве возбудитель пневмоцистной пневмонии выявляется в 89–98% случаев. При необходимости показано получение аспирата (биоптата) методом пункционной или открытой биопсии легкого. ПЦР при грибковой пневмонии информативна и после начала антибиотикотерапии и позволяет провести одновременное определение ДНК разных возбудителей при микст-инфекции. При серодиагностике показателен анализ динамики выявления антител к потенциальным возбудителям грибковой пневмонии.
Лечение грибковой пневмонии
Поскольку при грибковой пневмонии применение антибиотиков приведет к усугублению течения заболевания, требуется назначение или специфических антимикотических препаратов (итраконазола, амфотерицина В, флуконазола, кетоконазола и др.), или ингибиторов фолиевой кислоты и клиндамицина при пневмоцистозе.
При грибковой пневмонии для устранения дефицита иммунитета применяются иммунокорригирующие препараты, поливитамины, детоксикационные и стимулирующие средства, рациональный режим и питание. В случае грибково-бактериальной природы пневмонии показан короткий курс антибиотиков, а при сочетании с аллергической симптоматикой применяют десенсибилизирующие препараты, кортикостероиды. При осложнении пневмомикоза экссудативным плевритом выполняют плевральную пункцию и промывание плевральной полости.
Прогноз и профилактика
Точная оперативная диагностика и терапия делают прогноз грибковой пневмонии обнадеживающим. В случае несвоевременного и неадекватного лечении высок риск тяжелых осложнений. Грибковая пневмония является одной из самых частых причин летального исхода больных СПИДом. При благоприятном прогнозе первичного аспергиллеза и кандидоза может сохраняться склонность к воспалительным заболеваниям респираторного тракта и грибковая сенсибилизация; а легочные осложнения (пневмосклероз) могут приводить к инвалидности больного. При вторичной грибковой пневмонии прогноз зависит от тяжести основного фонового заболевания.
Предупреждение грибковой пневмонии включает профилактику на производстве и в сельском хозяйстве (герметизацию технологических процессов, связанных с выделением пыли; применение респираторов, микробиологический контроль окружающей среды); в медицине и пищевой промышленности (соблюдение правил дезинфекции и стерилизации). Индивидуальная профилактика подразумевает укрепление иммунитета, устранение дисбактериоза и хронической патологии, проведение рациональной антибиотикотерапии.
3. Внебольничная пневмония у взрослых: практическое пособие по диагностике, лечению и профилактике/ Чучалин А.Г., Синопальников А.И. и др. – 2010.
Легионеллёз - бактериальная инфекция, проявляющаяся тяжёлой пневмонией, выраженной интоксикацией, а также нарушениями функций ЦНС и почек.
Что провоцирует / Причины Легионеллёза (Болезни легионеров):
Возбудители - грамотрицательные аэробные подвижные бактерии рода Legionella семейства Legionellaceae. В настоящее время известно более 40 видов легионелл; для человека патогенно 22 вида. Наиболее частый возбудитель (более 90%) - L. pneumophila. Выделяют 18 сероваров бактерий; чаще всего заболевания вызывают бактерии 1 серовара. L. pneumophila культивируют на клеточных средах (куриные эмбрионы, морские свинки). Для роста на искусственных питательных средах бактерии нуждаются в цистеине и железе. Факторы патогенности легионелл включают липополисахаридный комплекс (эндотоксин) и сильнодействующий экзотоксин. Возбудитель устойчив во внешней среде: в жидкой среде при температуре 25 °С может сохраняться 112 дней, при 4 °С - 150 сут. Под действием 1% раствора формалина, 70° этилового спирта, 0,002% раствора фенола погибает за 1 мин, в 3% растворе хлорамина - в течение 10 мин. Колонизируя соединительные узлы, резиновые прокладки резервуаров для воды, бактерии интенсивно размножаются в них.
Механизм передачи - аэрозольный, заражение происходит чаще всего при вдыхании водного аэрозоля. Большинство вспышек связано с водными системами охлаждения, технологическими циклами, при функционировании которых образуется мелкодисперсный аэрозоль, содержащий бактерии. Возможен и воздушно-пылевой (почвенный) путь заражения при строительных и земляных работах. Накопившийся в почве, кондиционерах и головках душевых установок возбудитель вдыхается в виде водного или пылевого аэрозоля. В условиях лечебно-профилактических учреждений возможен артифициальный способ заражения, связанный с лечебными процедурами: вихревыми ваннами, терапией ультразвуковыми дезинтеграторами, интубацией и др.
Основные эпидемиологические признаки. Легионеллёз распространён повсеместно; заболеваемость выше в экономически развитых странах. Чаще возникает среди проживающих в гостиницах, медицинских работников и больных гериатрических и психиатрических стационаров. Показана возможность заражения лиц из групп риска при респираторной терапии или алиментарным путём (через питьевую воду). Вспышки среди населения возникают чаще в летне-осенние месяцы.
Случаи заболеваний, связанные с нозокомиальными вспышками, отмечают в течение всего года. Болеют преимущественно лица пожилого возраста, причём мужчины в 2-3 раза чаще, чем женщины. Известны внутрибольничные вспышки легионеллёза. Удельный вес пневмоний, вызванных легионеллами, составляет 0,5-5%, в то время как острое респираторное заболевание легионеллёзной природы (лихорадка Понтиак) возникает у 95% от общего числа лиц, подвергшихся заражению.
Патогенез (что происходит?) во время Легионеллёза (Болезни легионеров):
Основные входные ворота инфекции - различные отделы дыхательной системы, включая лёгочную ткань. Избирательное первичное поражение эпителиальных клеток верхних или более глубоких отделов респираторного тракта и лёгких зависит от инфицирующей дозы, размеров частиц аэрозолей, особенностей внешнего дыхания. Кроме того, возбудитель может проникать в организм человека, находясь внутри клеток различных простейших (амёб и др.), а также при проведении медицинских манипуляций и хирургических вмешательств у иммуносупрессивных лиц. В известной степени характер входных ворот определяет форму и тяжесть инфекционного процесса.
Высвобождение липополисахаридного комплекса (эндотоксина) после гибели бактерий и прогрессирующая эндотоксинемия обусловливают клинические проявления интоксикации вплоть до токсической энцефалопатии и инфекционно-токсического шока. С воздействием токсических факторов связывают возможность угнетения процессов кроветворения в костном мозге, некроза печёночных клеток, эпителия почечных канальцев, что наряду с микроциркуляторными нарушениями в почках ведёт к развитию острой почечной недостаточностью.
Симптомы Легионеллёза (Болезни легионеров):
Инкубационный период. При различных клинических формах заболевания варьирует от 2 до 10 дней, в среднем составляя 4-7 сут.
Течение пневмонии бурное, трудно поддающееся терапии. Заболевание могут осложнить развитие абсцессов, экссудативных плевритов, инфекционно-токсического шока. Часто несмотря на проводимое лечение прогрессирует дыхательная и сердечно-сосудистая недостаточность, требующая перевода больных на ИВЛ.
Поражения сердечно-сосудистой системы проявляются гипотонией, относительной брадикардией, сменяющейся тахикардией. Довольно часто (около 30% случаев) возникают продолжительная диарея с болями в животе и урчанием кишечника, гепатиты с желтухой и изменениями биохимических показателей крови. Возможны нарушения функции почек вплоть до почечной недостаточности, сохраняющейся впоследствии месяцами. При выздоровлении астенический синдром (слабость, головокружение, снижение памяти, раздражительность), рентгенологически определяемые инфильтраты в лёгких и плевральные изменения сохраняются в течение многих недель.
Острый альвеолит. Характерно появление с первых дней болезни сухого кашля на фоне высокой лихорадки и других проявлений интоксикации (головная боль, миалгии и т.д.). В дальнейшем кашель становится влажным с отхождением слизистой или слизисто-гнойной мокроты, нарастает одышка. В лёгких при аускультации с обеих сторон выслушивают обильную диффузную, длительно сохраняющуюся крепитацию. Процесс проходит с пропотеванием в альвеолы эритроцитов, фибрина, отёком альвеолярных перегородок. В некоторых случаях заболевание приобретает затяжное прогрессирующее течение с развитием фиброза.
Острое респираторное заболевание (лихорадка Понтиак). Легионеллёзная инфекция, протекающая без лёгочных поражений. На фоне температуры, быстро повышающейся до -40 °С, появляются озноб, головная боль, диффузные миалгии. Развивается респираторный синдром в виде ринитов, трахеобронхитов и бронхитов; нередко он сочетается с болями в животе и рвотой. Часто выявляют неврологические нарушения: головокружение, бессонницу, расстройства сознания и координации различной степени. Течение болезни благоприятное, длительность основных клинических проявлений составляет в среднем несколько дней; остаточный астеновегетативный синдром сохраняется значительно дольше.
Острое лихорадочное заболевание с экзантемой (лихорадка Форта Брэгг) . Более редкая форма легионеллёза. На фоне умеренных общетоксических и респираторных явлений (чаще в виде бронхита) возникает экзантема крупнопятнистого, кореподобного, скарлатиноподобного или петехиального характера. Элементы сыпи не имеют определённой характерной локализации, после их исчезновения шелушение кожи, как правило, не наблюдают.
В значительно более редких случаях заболевание может протекать в других формах: от субклинической до тяжёлых генерализованных форм с полиорганными поражениями и сепсиса.
Осложнения
Наиболее грозное осложнение - инфекционно-токсический шок, возникающий при легионеллёзной пневмонии. По данным ВОЗ, в этих случаях частота летальных исходов заболевания достигает 20%.
Диагностика Легионеллёза (Болезни легионеров):
Легионеллёзы следует отличать от пневмоний различной этиологии - стафилококковой, пневмококковой, микоплазменной, клебсиеллёзной, вызванной синегнойной палочкой и др., а также от ОРВИ, Ку-лихорадки, орнитоза и других заболеваний с поражением лёгких. Пневмонию легионеллёзной этиологии отличают выраженная интоксикация с развитием токсической энцефалопатии, обширный характер поражения лёгких, склонность к осложнениям (дыхательной и сердечно-сосудистой недостаточности, гепатитам, нарушениям функции почек).
Лабораторная диагностика
В гемограмме выявляют лейкоцитоз со сдвигом формулы влево, значительное повышение СОЭ (более 60 мм/ч).
Выделение возбудителя из крови, мокроты, плевральной жидкости, промывных вод бронхов сложно и на практике применяется редко, хотя бактериологический метод является наиболее точным подтверждением этиологии легионеллёзной инфекции. Бактерии можно выделить посевом исследуемого материала на специальные питательные среды либо после заражения лабораторных животных (морских свинок). Более доступна индикация антиген легионелл в исследуемом материале методами РИФ и И ФА.
В широкой практике распространены методы определения антител в реакциях микроагглютинации и РНИФ. Диагностически значимыми их результатами считают 4-кратное нарастание титров антител в парных сыворотках или диагностический титр 1:128 и выше при однократном исследовании. Иммуноферментный метод позволяет выявлять растворимый антиген легионелл в моче в острый период заболевания (3-10-й день болезни). Метод разработан только для выявления антигенов первой серогруппы L. pneumophila. ПЦР применяют для исследования материала нижней части респираторного тракта в острую фазу заболевания. Специфичность метода 95-99%, чувствительность 80-85%.
Лечение Легионеллёза (Болезни легионеров):
Основа этиотропной терапии легионеллёза - применение макролидов. В частности, эритромицин назначают внутрь в дозе 2-4 г/сут, в тяжёлых случаях вводят внутривенно капельно (эритромицин фосфат по 1 г/сут, максимально до 2-3 г/сут). При отсутствии или малой выраженности клинического эффекта антибиотикотерапию дополняют назначением рифампицина в дозе 0,6-1,2 г/сут. Курс лечения составляет 2-3 нед. Хороший клинический эффект также даёт назначение фторхинолонов (пефлоксацин).
Патогенетическое лечение, направленное на борьбу с интоксикацией, кровотечениями, развитием дыхательной и почечной недостаточности, шоковыми состояниями, проводят по общепринятым правилам. Необходима оксигенотерапия, довольно часто применяют ИВЛ.
Профилактика Легионеллёза (Болезни легионеров):
Эпидемиологический надзор включает контроль за санитарно-гигиеническим состоянием систем кондиционирования и охлаждения воды, душевых установок, аппаратов ИВЛ и др. Особое значение имеют своевременное обнаружение водного резервуара возбудителя и проведение дезинфекции.
Профилактические мероприятия проводят контроль за работой системы кондиционирования, качеством воды, используемой для лечебных и гигиенических процедур, и вентиляционной системой. Профилактические мероприятия направлены на снижение концентрации или элиминацию возбудителя в водных системах. Основные способы дезинфекции - термический (прогрев воды при температуре не ниже 80 °С) и химический (применение хлора). Эти методы или их сочетание применяют в зависимости от типа водного объекта, подлежащего дезинфекции. На промышленных предприятиях, электростанциях, в больницах и гостиницах замкнутые водные системы необходимо чистить и промывать не реже 2 раз в год. При обнаружении в системах легионелл ежеквартально проводят дезинфекционные мероприятия с последующим обязательным бактериологическим исследованием воды. На смену хлорированию и термообработке, часто негативно действующих на эксплуатацию водных систем и приборов, активно внедряют дезинфектанты, не содержащие хлора, ультрафиолетовое облучение или приспособления, обогащающие воду ионами серебра и меди. Средства специфической профилактики легионеллёза не разработаны.
Мероприятия в эпидемическом очаге
Проводят выявление больных среди лиц, находившихся в условиях, сходных с таковыми при заражении легионеллами. Госпитализацию больных проводят только по клиническим показаниям. Диспансерное наблюдение за переболевшими не регламентировано. В связи с тем, что нет достоверных данных о возможности передачи легионелл от человека к человеку, разобщение и экстренную профилактику контактных лиц не проводят. Дезинфекцию в очаге не проводят.
К каким докторам следует обращаться если у Вас Легионеллёз (Болезнь легионеров):
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Легионеллёза (Болезни легионеров), ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Читайте также:

