Что такое послеоперационная инфекция
Обновлено: 15.04.2024
Возбудители послеоперационных инфекций. Этиология нозокомиальных инфекций (НКИ)
S. aureus — основной возбудитель поверхностных и глубоких абсцессов и послеоперационных РИ как в виде моноинфекции, так и в сочетании с другими возбудителями. Циркуляция MRSA делает золотистый стафилококк наиболее значимым возбудителем НКИ.
В последние годы 17-22% всех нозокомиальных инфекций (НКИ) в отечественных клиниках были обусловлены S. aureus. Носителями данного возбудителя оказались 11,3% персонала клиники, причем наиболее часто S. aureus колонизировал слизистую оболочку преддверия носа.
При проведении локального микробиологического мониторинга в отечественных больницах в 2003-2005 гг. у пациентов с поверхностными раневыми инфекциями в 44% случаев были выделены штаммы S. aureus, в том числе у 10% больных с инфекцией мочевых путей и у 36% больных с инфекцией дыхательных путей. Представляет интерес частота выделения S. aureus в различных микробных ассоциациях, при этом установлено, что моновариант S. aureus встречался только в 37,8% случаев.
В отечественных клиниках S. aureus был причиной более половины всех осложнений после операций на молочной железе, 11,2% урологических операций и 12,5% операций в области кожи и подкожной клетчатки.
Наряду с этим отмечается увеличение количества полирезистентных штаммов стафилококков и энтеробактерий. Доля MRSA в 2006 г. составила 62%, а продуцентов БЛРС среди штаммов кишечной палочки и клебсиелл-29%.
Частота инфекций, вызванных антибиотикорезистентными бактериями возрастает во всем мире с каждым днем. Такие инфекции повышают заболеваемость и смертность, а следовательно, и расходы на здравоохранение. Существует множество причин, объясняющих эту тенденцию, но главным фактором повышения числа антибиотикоустойчивых бактерий служит возрастание применения антимикробных препаратов, в особенности антибиотиков широкого спектра действия. Многие исследования показали, что приблизительно в 50% случаев применение антибиотиков нерационально.
Несмотря на то, что многочисленные многоцентровые исследования, проведенные в Европе, США, Канаде, показали, что ведущими возбудителями ИОХВ и РИ остаются штаммы золотистого стафилококка (частота выделения превышает 40%), кишечной палочки (> 10%), синегнойной палочки (> 12%) и энтерококков (> 4-6%), все больше специалистов сообщают о госпитальных грибковых инфекциях.
В отделениях сердечно-сосудистой хирургии США диагностируют более 10 грибковых осложнений на каждую тысячу госпитализированных больных, причем в этиологии нозокомиальных микозов на долю грибов рода Candida приходится 80-90%, Aspergillu sspp. — 1,3-2,5%; в единичных случаях обнаруживали редкие грибы Malassezia, Trichasporon, Mucor, Rhizopus, Fusarium, Acremonium, Alternaria и др.
Все чаще и чаще в биоматериалах пациентов в стационарах обнаруживают не Candida albicans, а более вирулентные и антибиотикорезистентные виды Candida non-albicans. По обобщенным данным США, Канады, Европы, Индии, Тайваня (всего 26 стран мира) сделан вывод о возрастающей роли грибов Candida поп-albicans в развитии кандидемии и других заболеваний. Среди 14 368 штаммов грибов рода Candida, выделенных от больных с системными микозами в 40 больничных лабораториях, получены следующие виды: С. albicans — 69%, С. glabrata — 10%, С. tropicalis — 4,2%, С. parapsilosis — 3,6%, С. krusei— 1,7%.
В Санкт-Петербурге у 50% больных с кандидемией в крови обнаружены С. albicans, у остальных - С. parapsilosis, С. tropicalis, С. glabrata, С. rugosa и др..
Кроме дрожжевых грибов Candida велика проблема заражения грибами рода Aspergillus в больницах, особенно в период проведения ремонтных и строительных работ.
Еще в 1993 г. французскими учеными описано 96 пациентов с аспергиллезом. Все эти больные относились к группам риска: трансплантация костного мозга и внутренних органов, СПИД, другие виды иммунодефицита. Среди всех больных после трансплантационных операций в 5-10% случаев возникал легочный аспергиллез, а смертность среди них составляла 62-82%.
Известно, что плесневыми грибами A. fumigatus, A. flavus, Penicillium spp. и другими могут быть загрязнены кондиционеры, воздух, вода, стены, пол, окна, цветы, занавески, мягкие игрушки и другие предметы в помещениях, стационаров что служит опасным фактором развития НКИ. При вдыхании контаминированного воздуха споры грибов попадают в легкие, а из них могут проникать в мозг, печень, селезенку, почки, щитовидную железу, сердце, кровеносные сосуды, кости, суставы, синусы, гениталии, кожу и другие органы. В результате может развиться инвазивный аспергиллез, летальность при котором составляет 60-70%.
В одной из волгоградских больниц брали пробы воздуха различных помещений и смывы с предметов с целью определить связь между нозокомиальной средой и микрофлорой пациентов. Более чем в 25 % всех смывов с объектов внешней среды обнаружены грибы Penicillium, Mucor, Aspergillus и др. — типичные обитатели почвы. В 28,6% проб воздуха высеяны мицелиальные грибы. При этом взаимосвязь между микрофлорой, выделенной от больных и из окружающей среды, в этом конкретном случае не выявлена.
В другом исследовании вспышек аспергиллеза в стационарах Санкт-Петербурга обнаружили концентрацию грибов A. fumigatus и A. flavus в воздухе больниц до нескольких сотен спор в 1 м3 воздуха. В кардиологических стационарах после операций по протезированию клапанов констатировали циркуляцию зигомицет в воздухе.
В Екатеринбурге проводили микологический мониторинг воздуха нозокомиальных помещений в соответствии с требованиями СанПиН 2.1.3. 1375-03 и благодаря противогрибковой дезинфекции снизили концентрацию грибов в воздухе с 150-240 до 70 КОЕ/м3.
Таким образом, достаточно актуальной остается проблема распространения грибов в окружающей среде и контаминация ими медицинских работников.
Во всем мире признано, что гигиена рук персонала в здравоохранении - основное условие борьбы с НКИ, т. к. при оказании медицинской помощи через руки могут быть переданы условно-патогенные микроорганизмы, в т. ч. и грибы.
Исследованиями в рамках NNIS показано, что с помощью ДНК-типирования подтверждена возможность передачи грибов Candida от пациента к пациенту и от медработника к пациенту.
Около 40% здоровых лиц из обслуживающего персонала в хирургических отделениях имеют колонизацию кожи рук грибами Candida. Через загрязненные руки может быть передана кандидозная инфекция, способствующая развитию системных микозов вплоть до кандидемии. При обследовании сотрудников различных ОРИТ в 1-54% случаев и более на коже рук обслуживающего персонала выделялись штаммы грибов Candida, идентичные таковым у пациентов.
Следует отметить, что в настоящее время имеются серьезные разработки по дезинфекции рук персонала, однако важно добиться обязательного выполнения этих правил.
Существуют также нормативные документы по санитарно-эпидемиологическому состоянию лечебных учреждений, но, к сожалению, обязательными признаны только методы определения грибов при контроле воздуха. Это еще раз подтверждает, что грибы Candida и Aspergillus не рассматриваются как равноправные возбудители НКИ.
Обращает на себя внимание полиэтиологичность нозокомиальных инфекций (НКИ). Обнаружение возбудителей НКИ создает дополнительные трудности диагностики, эпидемиологического исследования и лечения больных НКИ.
Следует отметить, что количественные параметры контаминации биологического материала микроорганизмами не всегда принимаются во внимание в связи с трудностью соблюдения оптимальных условий взятия материала и усложнением проведения анализа и идентификации выделенных культур микроорганизмов. Вместе с тем количественная характеристика принципиально важна, т. к. дает представление об интенсивности эпидемического процесса.
Чрезвычайно важным представляется изучение характеристик выделенных штаммов возбудителя. Необходимы поиски продуцентов БЛРС, MRSA, KHC, VRE как вариантов возбудителей НКИ с маркерами лекарственной устойчивости. Количество содержащих эти маркеры штаммов микроорганизмов в различных подразделениях колеблется: для MRSA — от 68 до 84%, для КНС - от 61 до 77 %, для VRE - от 0 до 37 %, для БЛРС - от 20 до 30%.
Изучение эпидемиологической ситуации и мониторинг локальной структуры антибиотикорезистентности возбудителей НКИ необходимо проводить в условиях конкретного стационара. Эти данные нельзя экстраполировать на другие лечебные учреждения и отделения, поэтому мониторинг антибиотикорезистентности возбудителей при разных формах НКИ — важный аспект деятельности лаборатории клинической микробиологии в каждой конкретной клинике.
При этом желателен компьютерный мониторинг возбудителей нозокомиальных инфекций (НКИ) с использованием адекватных методов статистической обработки результатов лабораторных исследований.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Советы при раневой инфекции - нагноении раны после операции
1. Что такое хирургические раневые инфекции и какова их классификация?
Хирургические раневые инфекции (ХРИ) развиваются в течение 30 дней после хирургического вмешательства, за исключением тех случаев, когда в ране остается инородное тело. В случае имплантации инородного материала, опасность раневой инфекции сохраняется в течение года.
В зависимости от глубины поражения тканей раневые инфекции делятся на три клинически значимые категории:
а) Поверхностные ХРИ.
б) Глубокие ХРИ (вовлекающие фасции и мышцы).
в) Полостные ХРИ (распространение инфекции на любые анатомические образования, затронутые хирургическими манипуляциями).
2. Каковы классические признаки поверхностной, глубокой и полостной хирургической раневой инфекции (ХРИ)?
Поверхностные и глубокие хирургические раневые инфекции (ХРИ):
• Calor (жар)
• Tumor (отечность)
• Rubor (покраснение)
• Dolor (боль)
На полостную хирургическую раневую инфекцию (ХРИ) указывают общие симптомы: лихорадка, кишечная непроходимость и/или шок. Для уточнения диагноза могут потребоваться дополнительные исследования.
3. Можно ли предвидеть дальнейшее развитие ХРИ на основании типа раны?
Да. Исходя из степени загрязнения, раны можно отнести к одной из четырех категорий: чистые, чистые-контаминированные, контаминированные и грязные инфицированные. Чистые раны — атравматичные раны без признаков воспаления, с полным соблюдением правил асептики и без вскрытия полых органов. Чистые-контаминированные раны идентичны предыдущим, за исключением того, что вскрывался полый орган.
Контаминированные раны причинены чистым предметом, при минимальном контакте с инфицированным материалом. Грязные инфицированные раны развиваются в результате травмы загрязненным предметом или при значительном попадании инфицированного материала в разрез. По литературным данным, частота нагноения для каждой категории ран составляет 2,1%; 3,3%; 6,4% и 7,1% соответственно.
4. Какие другие факторы, кроме типа раны, позволяют прогнозировать развитие раневой инфекции?
Физическое состояние (но классификации Американского Общества Анестезиологов), результаты интраоперационных бактериальных посевов и продолжительность пребывания в стационаре до операции являются важными прогностическими факторами послеоперационных ХРИ. Важное значение имеет также адекватное регионарное кровоснабжение, что подтверждается низкой частотой нагноения ран в лицевой области.

5. Какие факторы может контролировать хирург для снижения частоты ХРИ?
Снизить частоту послеоперационной инфекции помогает сокращение продолжительности операции, облитерация мертвого пространства, тщательный гемостаз, максимальное уменьшение присутствия чужеродных материалов (включая лишние швы) и бережное обращение с тканями. Применение электрокоагуляции для гемостаза не повышает частоту раневых инфекций.
6. Снижает ли профилактическое назначение системных антибиотиков вероятность инфекции?
Применение антибиотиков при контаминированных и грязных инфицированных ранах абсолютно показано и является скорее лечением, чем профилактикой. При любых чистых контаминированных ранах рекомендуется назначение антибиотиков в качестве профилактики. Первоначально профилактическое лечение антибиотиками при чистых ранах проводилось только в случае имплантации синтетического материала. Общее мнение сводилось к тому, что любая польза от профилактического применения антибиотиков в чистой хирургии превышает потенциальный риск побочных эффектов от неправильного использования.
Однако, строго говоря, после любой операции в ране остается некоторое количество чужеродного материала (например, швы), и даже единственный шов может привести к нагноению за счет занесенных в рапу бактерий, которые сами по себе не вызовут инфекции. Кроме того, крупное проспективное рандомизированное исследование, посвященное профилактическому применению антибиотиков в чистой хирургии, показало очевидное значение профилактики для уменьшения количества ХРИ.
7. Когда нужно проводить антибактериальную профилактику?
Максимально положительный результат достигается при наличии терапевтической концентрации антибиотиков в тканях на момент контаминации. Следовательно, эффективность профилактики повышается, если антибиотики назначаются непосредственно перед хирургическим разрезом; более позднее профилактическое введение антибиотиков бессмысленно. Схемы многократного введения антибиотиков не имеют преимуществ перед однократной дозой. Беспорядочный выбор антибиотиков (не соответствующий больничным рекомендациям) может даже повысить частоту ХРИ.
8. Нужно ли проводить в операционной пульс-гидропрессивную обработку раны?
Да. Было проведено всестороннее исследование результатов пульс-гидропрессивной обработки раны при контаминации мягких тканей. При этом было продемонстрировано, что она в семь раз эффективнее снижает бактериальное загрязнение, чем промывание резиновой грушей. Эластические свойства мягких тканей способствуют удалению микрочастиц в промежутках между подачей жидкости. Оптимальное давление и частота импульсов должны составлять соответственно 4-5 кг на см2 и 800 импульсов в минуту.
9. Позволяют ли антибиотики и гидропрессивная обработка чаще закрывать грязные или контаминированные раны первичным натяжением?
Несмотря на эти эффективные методы терапии, решение о первичном закрытии раны для хирурга остается непростым, требует опыта и врачебной интуиции. Первичное закрытие рапы всегда предпочтительно, поскольку сокращает сроки заболеваемости и улучшает косметический результат. Однако при развитии инфекции последствия достаточно серьезны, и рапу необходимо снова раскрыть. Решение о первичном закрытии рапы принимается с учетом степени контаминации, количества некротической ткани или размеров оставленного мертвого пространства, адекватности кровоснабжения, эффективности дренажей, времени, прошедшего с момента повреждения и имплантации инородного материала.
В целом безопаснее оставить сомнительную рану открытой и предоставить ей возможность заживать вторичным натяжением или выполнить отсроченное закрытие рапы через 3-5 дней. Отсроченные швы являются тем компромиссом, который часто отличает опытного хирурга от восторженного дилетанта.
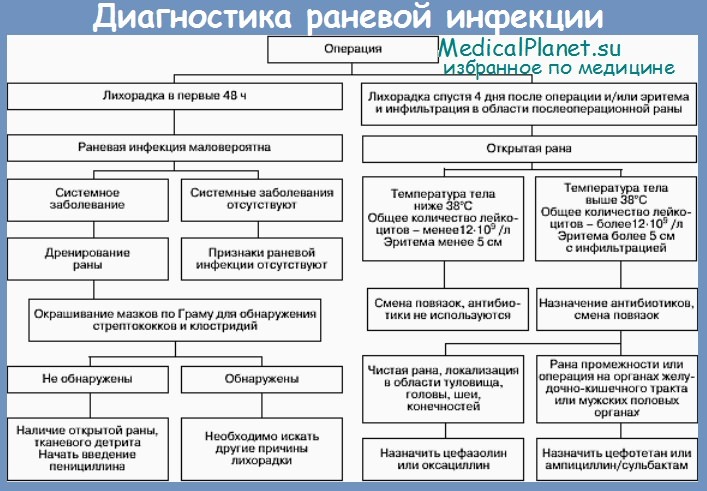
10. Обычная частота нагноения при типичных операциях.
Холецистэктомия 3%
Паховое грыжесечение 2%
Аппендэктомия 5%
Торакотомия 6%
Колэктомия 12%
11. Какие микроорганизмы чаще всего являются возбудителями раневой инфекции?
Поскольку стафилококк относится к наиболее распространенному на коже микроорганизму, он также чаще всего вызывает ХРИ. Однако ХРИ в ряде зон ассоциируются с другими микроорганизмами. Если была вскрыта кишка, возбудителями инфекции обычно являются представители семейства Enterobacteriaceae и анаэробы; при рассечении желчных путей и пищевода инфекционными возбудителями, помимо названных микробов, становятся энтерококки. Другие зоны, например мочевыводящие пути или влагалище, содержат такие микроорганизмы как стрептококки группы D, Pseudomonas и Proteus.
12. Как раневая инфекция связана с операцией по времени?
В типичных случаях раневая инфекция развивается на 5-7 день после операции; однако может развиться и молниеносная форма. Инфекции, вызванные клостридиями, развиваются при большом количестве нежизнеспособных тканей в закрытом пространстве и являются классическим примером молниеносной формы ХРИ.
13. Каковы первостепенные лечебные мероприятия при развитии ХРИ?
Первостепенное значение имеет дренирование раны. Дренаж ставится путем раскрытия раны или, в случае глубокой инфекции, под контролем компьютерной томографии (КТ) или ультразвукового исследования (УЗИ). Для лечения флегмоны и генерализованного сепсиса также применяется антибактериальная терапия.
14. Что может произойти, если не лечить поверхностную или глубокую ХРИ?
Местно состояние раны ухудшается, инфекция проникает в глубь тканей и продолжает распространяться. Если инфекция быстро прогрессирует, может развиться некротизирующий фасциит. В конечном итоге края рапы расходятся.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Раневая инфекция – это комплекс общих и местных патологических проявлений, возникающих при развитии инфекции в случайных или операционных ранах. Патология проявляется болью, ознобом, лихорадкой, увеличением регионарных лимфатических узлов и лейкоцитозом. Края раны отечные, гиперемированные. Наблюдается выделение серозного или гнойного отделяемого, в отдельных случаях образуются участки некроза. Диагноз выставляется на основании анамнеза, клинических признаков и результатов анализов. Лечение комплексное: вскрытие, перевязки, антибиотикотерапия.
МКБ-10
Общие сведения
Раневая инфекция – осложнение раневого процесса, обусловленное развитием патогенной микрофлоры в полости раны. Все раны, в том числе и операционные, как в гнойной хирургии, так и в травматологии считаются первично загрязненными, поскольку какое-то количество микробов попадает на раневую поверхность из воздуха даже при безукоризненном соблюдении правил асептики и антисептики. Случайные раны загрязнены сильнее, поэтому в таких случаях источником инфекции обычно является первичное микробное загрязнение. При операционных ранах на первый план выступает эндогенное (из внутренней среды организма) или внутригоспитальное (вторичное) инфицирование.

Причины
В большинстве случаев возбудителем инфекции в случайных ранах становится стафилококк. Редко в качестве основного возбудителя выступает протей, кишечная и синегнойная палочка. В 0,1% случаев встречается анаэробная инфекция. Через несколько дней пребывания в стационаре флора меняется, в ране начинают преобладать устойчивые к антибактериальной терапии грамотрицательные бактерии, которые обычно становятся причиной развития раневой инфекции при вторичном инфицировании как случайных, так и операционных ран.
Раневая инфекция развивается в случае, когда количество микробов в ране превышает некий критический уровень. При свежих травматических повреждениях у ранее здорового человека этот уровень составляет 100 тыс. микроорганизмов на 1 г ткани. При ухудшении общего состояния организма и определенных особенностях раны этот порог может существенно снижаться.
К числу местных факторов, повышающих вероятность развития раневой инфекции, относится присутствие в ране инородных тел, сгустков крови и некротических тканей. Также имеет значение плохая иммобилизация при транспортировке (становится причиной дополнительной травмы мягких тканей, вызывает ухудшение микроциркуляции, увеличение гематом и расширение зоны некроза), недостаточное кровоснабжение поврежденных тканей, большая глубина раны при малом диаметре раневого канала, наличие слепых карманов и боковых ходов.
Общее состояние организма может провоцировать развитие раневой инфекции при грубых расстройствах микроциркуляции (централизация кровообращения при травматическом шоке, гиповолемические расстройства), нарушениях иммунитета вследствие недостаточного питания, нервного истощения, химических и радиационных поражений, а также хронических соматических заболеваний. Особенно значимы в таких случаях злокачественные новообразования, лейкемия, уремия, цирроз, сахарный диабет и ожирение. Кроме того, снижение сопротивляемости инфекции наблюдается при проведении лучевой терапии и при приеме ряда лекарственных средств, в том числе – иммунодепрессантов, стероидов и больших доз антибиотиков.
Классификация
В зависимости от преобладания тех или иных клинических проявлений гнойные хирурги выделяют две общие формы раневой инфекции (сепсис без метастазов и сепсис с метастазами) и несколько местных. Общие формы протекают тяжелее местных, вероятность летального исхода при них повышается. Самой тяжелой формой раневой инфекции является сепсис с метастазами, который обычно развивается при резком снижении сопротивляемости организма и раневом истощении вследствие потери больших количеств белка.
К числу местных форм относятся:
- Инфекция раны. Является локализованным процессом, развивается в поврежденных тканях с пониженной сопротивляемостью. Зона инфицирования ограничена стенками раневого канала, между ней и нормальными живыми тканями есть четкая демаркационная линия.
- Околораневой абсцесс. Обычно соединен с раневым каналом, окружен соединительнотканной капсулой, отделяющей участок инфекции от здоровых тканей.
- Раневая флегмона. Возникает в случаях, когда инфекция выходит за пределы раны. Демаркационная линия исчезает, процесс захватывает прилежащие здоровые ткани и проявляет выраженную тенденцию к распространению.
- Гнойный затек. Развивается при недостаточном оттоке гноя вследствие неадекватного дренирования или зашивании раны наглухо без использования дренажа. В подобных случаях гной не может выйти наружу и начинает пассивно распространяться в ткани, образуя полости в межмышечных, межфасциальных и околокостных пространствах, а также в пространствах вокруг сосудов и нервов.
- Свищ. Образуется на поздних стадиях раневого процесса, в случаях, когда на поверхности рана закрывается грануляциями, а в глубине сохраняется очаг инфекции.
- Тромбофлебит. Развивается через 1-2 мес. после повреждения. Является опасным осложнением, обусловлен инфицированием тромба с последующим распространением инфекции по стенке вены.
- Лимфангит и лимфаденит. Возникают вследствие других раневых осложнений, исчезают после адекватной санации основного гнойного очага.
Симптомы раневой инфекции
Как правило, патология развивается спустя 3-7 дней с момента ранения. К числу общих признаков относится повышение температуры тела, учащение пульса, ознобы и признаки общей интоксикации (слабость, разбитость, головная боль, тошнота). В числе местных признаков – пять классических симптомов, которые были описаны еще во времена Древнего Рима врачом Аулусом Корнелиусом Сельсусом: боль (dolor), местное повышение температуры (calor), местное покраснение (rubor), отек, припухлость (tumor) и нарушение функции (functio laesa).
Характерной особенностью болей является их распирающий, пульсирующий характер. Края раны отечны, гиперемированы, в полости раны иногда имеются фибринозно-гнойные сгустки. Пальпация пораженной области болезненна. В остальном симптоматика может варьироваться в зависимости от формы раневой инфекции. При околораневом абсцессе отделяемое из раны нередко незначительное, наблюдается выраженная гиперемия краев раны, резкое напряжение тканей и увеличение окружности конечности. Образование абсцесса сопровождается снижением аппетита и гектической лихорадкой.
При раневых флегмонах выявляется существенное повышение местной температуры и резкое ухудшение состояния больного, однако рана выглядит относительно благополучно. Формирование гнойного затека также сопровождается значительным ухудшением состояния пациента при относительном благополучии в области раны. Температура повышается до 40 градусов и более, отмечаются ознобы, вялость, адинамия и снижение аппетита. Гнойное отделяемое отсутствует или незначительное, гной выделяется только при надавливании на окружающие ткани, иногда – удаленные от основного очага инфекции. При свищах общее состояние остается удовлетворительным или близким к удовлетворительному, на коже формируется свищевой ход, по которому оттекает гнойное отделяемое.
Осложнения
Осложнения обусловлены распространением инфекции. При гнойных тромбофлебитах общее состояние ухудшается, в зоне поражения определяются умеренные признаки воспаления, при расплавлении стенки вены возможно формирование флегмоны или абсцесса. Лимфангит и лимфаденит проявляются болезненностью, отечностью мягких тканей и гиперемией кожи в проекции лимфатических узлов и по ходу лимфатических сосудов. Отмечается ухудшение общего состояния, ознобы, гипертермия и повышенное потоотделение. При сепсисе состояние тяжелое, кожа бледная, наблюдается снижение АД, выраженная тахикардия, бессонница и нарастающая анемия.
Лечение раневой инфекции
Лечение заключается в широком вскрытии и дренировании гнойных очагов, а также промывании раны антисептиками. В последующем при перевязках используются сорбенты и протеолитические ферменты. В фазе регенерации основное внимание уделяется стимуляции иммунитета и защите нежных грануляций от случайного повреждения. В фазе эпителизации и рубцевания при больших, длительно незаживающих ранах выполняют кожную пластику.
Прогноз и профилактика
Прогноз определяется тяжестью патологии. При небольших ранах исход благоприятный, наблюдается полное заживление. При обширных глубоких ранах, развитии осложнений требуется длительное лечение, в ряде случаев возникает угроза для жизни. Профилактика раневой инфекции включает в себя раннее наложение асептической повязки и строгое соблюдение правил асептики и антисептики в ходе операций и перевязок. Необходима тщательная санация раневой полости с иссечением нежизнеспособных тканей, адекватным промыванием и дренированием. Пациентам назначают антибиотики, проводят борьбу с шоком, алиментарными нарушениями и белково-электролитными сдвигами.
Парапротезная инфекция – это инфекционный процесс в области сустава, возникающий после эндопротезирования и патогенетически связанный с наличием имплантата. Проявляется локальными признаками воспаления: отеком, болезненностью, местной гиперемией и гипертермией, нарушением функции конечности в сочетании с симптомами общей интоксикации. Нередко протекает со стертой клинической симптоматикой. Диагностируется с учетом анамнеза, лабораторных анализов, рентгенологических методик, МРТ, УЗИ. В зависимости от вида параэндопротезной инфекции выполняются ревизии с сохранением эндопротеза либо удаление имплантата с реэндопротезированием, артродезом, костно-мышечной пластикой.
МКБ-10
Общие сведения
Парапротезная инфекция – актуальная проблема современной травматологии и ортопедии. Последние десятилетия ознаменовались широким распространением эндопротезирования. Увеличилось не только общее количество операций, но и количество протезируемых суставов. Если раньше замене, в основном, подвергали тазобедренный сустав, то в наши дни рутинной практикой стало протезирование коленного, плечевого, других средних и мелких суставов конечностей. Соответственно, возросло число случаев развития инфекционного процесса в области оперативного вмешательства. Распространенность патологии при первичном эндопротезировании составляет 0,3-1%. Частота осложнения при повторной установке искусственного сустава, по различным данным, колеблется от 9 до 40%. В большинстве случаев осложнение возникает в первые два года после операции.

Причины
Непосредственной причиной парапротезной инфекции становятся болезнетворные бактерии, при этом существует определенная связь между типом возбудителя и видом протеза, обусловленная склонностью микробов к адгезии к тем или иным инородным материалам, находящимся в организме пациента. Так, в области металлических частей имплантата инфекция чаще вызывается золотистым стафилококком, в зоне полимерных – эпидермальным стафилококком. Наряду со стафилококковой флорой воспаление могут провоцировать стрептококки, кишечная палочка и некоторые другие микроорганизмы. Обстоятельствами, способствующими возникновению воспалительного процесса, считаются:
- Особенности вмешательства. Установлено, что при длительности операции более 3 часов вероятность осложнения увеличивается, что связано с продолжительным контактом тканей с внешней средой, нарушениями кровообращения, локальными обменными расстройствами и общей реакцией организма на стресс. Большое значение имеют интраоперационные осложнения, технические трудности и значительная кровопотеря, усугубляющие действие перечисленных факторов.
- Особенности установки эндопротеза. Риск развития инфекции в зоне искусственного сустава повышается при применении дополнительных биологических и синтетических материалов, нестабильности имплантата. В первом случае имеет значение реакция организма на наличие чужеродных элементов, во втором появляется постоянный источник травматизации окружающих тканей, создаются благоприятные условия для внедрения инфекционных агентов.
К числу особенностей организма пациента, способствующих появлению данного осложнения, относят пожилой возраст, наличие тяжелой соматической патологии и иммунные нарушения различного генеза. Негативную роль играет многократное или длительное применение антибиотиков перед операцией, обуславливающее устойчивость микроорганизмов к антибактериальной терапии, нарушение рекомендаций врача относительно режима активности и реабилитационных мероприятий в послеоперационном периоде.
Патогенез
Парапротезная инфекция – разновидность имплантат-ассоциированной инфекции, которая возникает после эндопротезирования вследствие способности патогенных микробов к колонизации имплантатов. Бактерии, вызывающие это осложнение, обладают свойством формировать биофильмы (биологические пленки) на поверхностях чужеродных материалов в организме больного. Выделяют два механизма возникновения биопленок. Первый – неспецифическое взаимодействие непосредственно между поверхностью протеза и микроорганизмами за счет сил поверхностного натяжения, водородных связей, гидрофобности, электростатического поля и т. д.
Второй – контакт бактерий с белками, располагающимися на поверхности искусственной конструкции. После установки части эндопротеза очень быстро покрываются слоем белков, среди которых преобладают альбумины. При адгезии микробов к этим белкам формируются микроколонии. Вначале имплантат колонизируется аэробными микроорганизмами, в последующем в глубоких слоях биофильма создается благоприятная среда для развития анаэробной микрофлоры. При увеличении биопленки или под влиянием внешних воздействий ее части отрываются от поверхности имплантата, происходит диссеминация процесса. Исследование перечисленных механизмов позволило объяснить устойчивость инфекции и неэффективность консервативной терапии этого осложнения.
Классификация
Существует много вариантов классификации параэндопротезной инфекции, однако общепризнанная международная систематизация этого осложнения пока отсутствует. Обычно травматологи-ортопеды используют классификацию Ковентри-Фитцджеральда, в основе которой лежит временной период между операцией и манифестацией инфекционного процесса. Различают четыре типа парапротезной инфекции:
- Острая послеоперационная. Признаки инфицирования определяются в течение месяца после вмешательства.
- Поздняя хроническая. Осложнение диагностируется во временном промежутке от 1 месяца до 1 года с момента операции.
- Острая гематогенная. Симптомы патологии возникают через 1 и более год после установки искусственного сустава.
- Положительная интраоперационная культура. Характеризуется бессимптомным течением при выявлении бактерий в 2-х и более интраоперационных образцах ткани.
В российской клинической практике также применяют систематизацию инфекций в области хирургических вмешательств, разработанную сотрудниками Новосибирского НИИТО. Согласно этой классификации различают три вида послеоперационных инфекционных процессов: ранний острый (возникший в первые 3 месяца), поздний острый (развившийся в течение 3-12 месяцев), хронический (диагностированный спустя 1 год и более после операции). При постановке диагноза отмечают наличие или отсутствие нестабильности эндопротеза.
С учетом формы выделяют флегмоноподобную, свищевую, латентную и атипичную инфекции, с учетом глубины – поверхностную и глубокую. Несмотря на то, что поверхностная инфекция протекает без вовлечения эндопротеза (то есть, имеет другой патогенез), поражает только кожные покровы и подкожную клетчатку, поддается консервативной терапии, специалисты рассматривают ее в рамках параэндопротезной инфекции, поскольку такой подход позволяет учесть все возможные варианты инфекционных осложнений эндопротезирования.
Симптомы парапротезной инфекции
Проявления патологии зависят от времени возникновения и глубины процесса. Поверхностная инфекция развивается в период восстановления после операции, сопровождается воспалением мягких тканей при интактности оперированного сустава. Характеризуется гиперемией, локальной припухлостью, повышением местной температуры, незначительными или умеренными болями, нарушением заживления раны, расхождением ее краев, наличием гнойного отделяемого. Возможно образование участков поверхностного некроза, формирование лигатурных свищей. Выраженность общей интоксикации определяется распространенностью поражения кожи и жировой клетчатки.
Глубокая парапротезная инфекция может манифестировать как в раннем послеоперационном периоде, так и спустя продолжительное время после вмешательства. Поражает мышцы и фасции. Проявляется отечностью мягких тканей, болью в проекции сустава, ограничением функции конечности, общими интоксикационными симптомами: повышением температуры тела до 38 °С и выше, ознобами, слабостью, разбитостью, тахикардией, тахипноэ. Возможно сочетание глубокого и поверхностного процесса, рассматриваемое специалистами как разновидность глубокой инфекции. Из-за распространенности иммунологических нарушений в популяции патология часто протекает со сглаженной симптоматикой. Снижение иммунитета усугубляют переливания крови, лекарственная терапия и другие лечебные мероприятия, проводимые на пред- и послеоперационном этапе.
Осложнения
Наиболее частые осложнения параэндопротезной инфекции обусловлены распространением гнойного процесса. Наблюдается образование абсцессов и флегмон. Особенно опасны глубокие затеки в полость таза, иногда формирующиеся при поражении оперированного тазобедренного сустава. В тяжелых случаях возможно развитие сепсиса. При часто рецидивирующей патологии снижается или утрачивается трудоспособность, ухудшается качество жизни больных, персистирующий очаг инфекции оказывает негативное влияние на деятельность внутренних органов.
Диагностика
Диагноз обычно выставляют специалисты в области ортопедии, наблюдающие пациентов, перенесших эндопротезирование сустава. Из-за часто встречающихся стертых форм и неспецифичности результатов дополнительных методик распознавание парапротезной инфекции может представлять определенные затруднения. Программа обследования обычно включает следующие методы:
- Опрос, осмотр. Признаком, указывающим на вероятность возникновения данной патологии, является замена сустава в анамнезе. Ортопед уточняет жалобы, время появления и динамику развития симптомов, оценивает внешний вид и функцию сустава, выявляет признаки воспаления, участки некроза, свищевые ходы и пр.
- Ультразвуковое сканирование. УЗИ сустава применяется в качестве скринингового метода, позволяет обнаружить абсцессы или гематомы, выполнить прицельную пункцию гнойного очага для последующего изучения содержимого в процессе бактериологического исследования.
- Рентгенологические методики. Результаты обычной рентгенографии часто неоднозначны. О наличии заболевания могут свидетельствовать остеолиз и периостальная реакция, без видимых причин возникшие после успешного вмешательства. Для оценки динамики процесса обязательно выполняют контрольные снимки. При свищах производят рентгенофистулографию для определения локализации свищевых ходов и затеков.
- Магнитно-резонансная томография. Является уточняющим методом, назначается на этапе предоперационного обследования для оценки размеров и расположения глубоких (в том числе – внутритазовых) абсцессов, уточнения объема хирургического вмешательства.
- Лабораторные анализы. При острой патологии в ОАК обнаруживаются признаки воспаления: лейкоцитоз, нейтрофилез, лимфоцитопения, сдвиг формулы влево, повышение СОЭ. При хронических формах изменения крови могут быть выражены незначительно. Более специфичны результаты исследования на С-реактивный белок, отражающие динамику воспалительного процесса, а также данные бакпосева раневого отделяемого. Микробиологический анализ синовиальной жидкости часто отрицательный из-за формирования биопленок.
Лечение парапротезной инфекции
В случаях поверхностного инфекционного процесса тактика такая же, как при других инфицированных ранах. Осуществляется санация поверхностного гнойного очага на фоне антибиотикотерапии, операции на суставе не требуются. При глубокой инфекции тактика определяется типом патологии с учетом времени ее возникновения, наличием либо отсутствием нестабильности сустава, расположением и размером гнойных затеков, состоянием костей и мягких тканей, устойчивостью флоры к антибактериальным препаратам и некоторыми другими факторами. Лечение только хирургическое. Существуют следующие варианты вмешательств:
- Ревизия с сохранением имплантата. Проводится при раннем инфицировании, сохранении стабильности сустава, незначительном поражении элементов эндопротеза. Сустав вскрывают, исследуют его поверхности. Инфицированные окружающие ткани иссекают, полиэтиленовый вкладыш заменяют (при необходимости – вместе с головкой протеза), рану ушивают, дренируют.
- Ревизионное эндопротезирование. Рекомендуется при поздней хронической и иногда – острой гематогенной парапротезной инфекции, предполагает одно- двух- или трехэтапную замену имплантата. Чаще всего используют двухэтапное реэндопротезирование, на первом этапе выполняют ревизию раны, затем после курса антибиотикотерапии устанавливают новый протез. При трехэтапном вмешательстве на втором этапе производят костную пластику.
- Артродез сустава. Показан при рецидивирующей инфекции, резистентности патогенной флоры к антибиотикам. Предусматривает удаление эндопротеза и наложение аппарата внешней фиксации для создания неподвижного соединения между концами костей.
- Ампутация или экзартикуляция. Осуществляется редко, в качестве показаний рассматривается наличие упорно рецидивирующего очага инфекции, представляющего угрозу для жизни больного, при одновременной утрате функции конечности.
Прогноз и профилактика
1. Медицинские и социальные проблемы эндопротезирования суставов конечностей/ Москалев В.П., Корнилов Н.В., Шапиро. К.И. - 2001
2. Инфекционные осложнения после эндопротезирования крупных суставов как актуальная проблема современной ортопедии/ Муконин А.А.// Новые медицинские технологии - 2006 -№ 8
3. Лечение параэндопротезной инфекции тазобедренного сустава: клинические рекомендации/ Министерство здравоохранения РФ - 2013
Читайте также:

