Что такое сепсис от укола
Обновлено: 15.04.2024
Сепсис — это самая тяжелая, генерализованная форма инфекционного процесса, которая развивается либо при высокой патогенности возбудителя, либо при недостаточном ответе защитных систем организма. Международным консенсусом рекомендовано использовать следующее определение: сепсис — это опасная для жизни дисфункция внутренних органов, вызванная нарушением регуляции ответа организма на инфекцию. При сепсисе наблюдается общий интоксикационный синдром, тромбогеморрагический синдром (кровоизлияния) и поражение внутренних органов.
Причины возникновения сепсиса
Сепсис может быть вызван большинством известных в эпидемиологии микроорганизмов, среди которых бактерии, вирусы (в том числе сезонные вирусы гриппа), грибы, паразиты. Обычно возбудитель инфекции попадает в организм из внешней среды. При определенных условиях, например, при иммунодефицитах, заболевание может развиться от естественной, условно-патогенной флоры организма, которая в норме присутствует у каждого человека. [1]
Само по себе наличие инфекции еще не является гарантией развития сепсиса. Необходимы дополнительные условия, которые приведут к генерализации процесса и патологическому ответу организма. Вероятность таких событий увеличивается в следующих случаях:
- Возраст больного старше 75 лет.
- Выполнение операций или инвазивных процедур.
- Наличие травм и ожогов.
- Нарушения иммунной системы — СПИД, онкологические заболевания, проведение химиотерапии, необходимость применения иммуносупрессивной терапии (например, после трансплантации органов), необходимость приема высоких доз глюкокортикостероидов.
- Долгое лечение в условиях стационара.
- Наличие катетеров, канюль, зондов и других инвазивных устройств.
- Беременность и роды.
- Наличие химической зависимости — алкоголизм, наркомания.
- Наличие хронических заболеваний — хроническая почечная недостаточность, дыхательная недостаточность, сахарный диабет и многое другое.
Виды сепсиса
В зависимости от расположения первичного очага инфекции, выделяют первичный (криптогенный) и вторичный сепсис. При первичном, очаг инфекции установить не удается. При вторичном сепсисе таковой очаг имеется. В зависимости от его локализации, выделяют:
- Чрескожный сепсис. Первичный очаг находится на коже, это могут быть раны, ожоги, гнойные заболевания кожи (гнойные абсцессы, фурункулы и др).
- Одонтогенный сепсис. Причиной его развития может стать кариес, пульпит, периодонтит, челюстной остеомиелит и другие заболевания зубочелюстной системы.
- Отогенный сепсис. Первичным очагом является воспалительный процесс в ухе. Как правило, это гнойные отиты среднего уха.
- Гинекологический сепсис — первичный очаг располагается в половых органах женщины.
- Хирургический сепсис — развивается в результате инфицирования хирургической раны или при инфицировании во время проведения инвазивных процедур. 2
Первые признаки и симптомы сепсиса
Определить первые признаки сепсиса бывает непросто, даже для специалистов. Это связано с тем, что, во-первых, этот синдром развивается уже на фоне существующей патологии, которая может иметь самую разнообразную симптоматику, а во-вторых, при наличии иммунодефицита, клиническая картина может быть стертой. Тем не менее, есть некоторые симптомы, которые позволяют заподозрить начало сепсиса:
- Повышение или понижение температуры тела — выше 38 и ниже 36 градусов.
- Снижение давления ниже рабочего значения.
- Увеличение частоты пульса.
- Увеличение частоты дыхательных движений (одышка).
- Снижение количества выделенной мочи.
- Общая слабость, изможденность.
- Нарушение сознания или поведения.
Особое внимание возникновению этих признаков уделяют у хронических больных, при наличии лейкопении, онкологических заболеваний и у пациентов, перенесших травмы или хирургические вмешательства. При возникновении хотя бы 2-3 таких симптомов, следует немедленно связаться с врачом.
Диагностика сепсиса
Своевременная диагностика сепсиса имеет решающее значение для выздоровления больного. Чем раньше начато лечение, тем больше шансов на успех. Диагноз выставляется на основании данных клинического осмотра и лабораторно-инструментального обследования.

Клинические критерии:
- Температура тела более 38 градусов или менее 36 градусов.
- Частота сердечных сокращений более 90 или превышает возрастную норму.
- Частота дыхания более 20 раз в минуту.
- Наличие отеков.
- Спутанность сознания.
- Повышение уровня глюкозы в крови более 7,7 мкмоль/л при отсутствии диабета.
- Нарушение гемодинамических процессов — снижение систолического артериального давления менее 90 мм.рт.ст, либо его снижение более чем на 40 мм.рт.ст. от привычного значения. [5,6]
Лабораторные критерии
Проводят общий анализ крови с подсчетом лейкоцитарной формулы и определением количества тромбоцитов. При сепсисе определяется лейкоцитоз более 12*109/л или лейкопения, когда количество лейкоцитов ниже 4*109/л. Также отмечается выход в кровяное русло незрелых форм гранулоцитов и уменьшение количества тромбоцитов.
В биохимическом анализе крови отмечается увеличение С-реактивного белка, креатинина, билирубина. Но это неспецифичные признаки, которые могут наблюдаться и при других заболеваниях. Поэтому продолжается поиск более информативных методов диагностики.
На сегодняшний день главными таким маркерами являются прокальцитонин, пресепсин, СРБ. По данным этого лабораторного показателя устанавливают диагноз и отслеживают динамику заболевания.
Бактериологический посев
Обнаружение в крови микроорганизмов является важным, но не обязательным проявлением сепсиса. Даже при использовании самых современных диагностических систем и при тщательном соблюдении техники забора материала, выделить возбудитель из крови удается менее, чем в половине случаев. Поэтому отрицательный результат бакпосева при наличии клинической симптоматики не должен расцениваться как отсутствие сепсиса, и, наоборот, выделение микроорганизмов из крови при отсутствии симптоматики, должно расцениваться как транзиторная бактериемия или вирусемия, но не как сепсис.
Тем не менее, биологические исследования в любом случае должны присутствовать, как один из этапов диагностики сепсиса по следующим причинам:
- Возможность определения этиологии возбудителя.
- Подбор или смена режимов антибиотикотерапии.
- Контроль эффективности лечения.
- В некоторых случаях позволяет определить источник инфекции, например, катетер-связанная инфекция, эндокардиты и др.
Стадии развития сепсиса
Развитие и течение септического процесса индивидуально и зависит как от свойств возбудителя, так и от особенностей организма больного. Тем не менее, можно выделить несколько фаз течения данного заболевания:
Что касается продолжительности заболевания, то здесь все опять же индивидуально. У одних, более сильных пациентов, сепсис купируется в течение 3-4 недель, у других он может протекать годами, периодически стихая и вспыхивая.
Кроме того, при диагностике сепсиса выделяют следующие состояния.
Токсико-резорбтивная лихорадка
Токсико-резорбтивная лихорадка — состояние, которое развивается при всасывании бактериальных токсинов или продуктов тканевого распада из первичного патологического очага. Как правило, это характерно для бактериальных инфекций ран, катетеров и др. Характерны общие типовые синдромы, которые сопровождают инфекционные процессы — лихорадка, изменения в общем анализе крови и мочи (лейкоцитоз, протеинурия). При ликвидации первичного очага, состояние пациента стабилизируется.
Септицемия
Септицемия — форма сепсиса, при которой наблюдается выраженный интоксикационный синдром, гиперэргия (повышенная реакционность организма) и быстрое течение. Септические очаги либо выражены минимально, либо отсутствуют. Такая форма сепсиса больше характерна для детей первых лет жизни. Для клинической картины больше характерны общие проявления:
- Гемолитическая желтуха, сопровождающаяся пожелтением кожных покровов и склер.
- Сыпь. Сначала она проявляется в виде мелких розовых точек, которые разрастаются и сливаются между собой, образуя бледно-розовые или пурпурные пятна.
- У некоторых пациентов элементы сыпи могут покрываться пузырями или язвами. При глубоких поражениях может затрагиваться подкожная жировая клетчатка с развитием флегмонозного воспаления.
- Геморрагический синдром — кровоизлияния во внутренние органы.
Септикопиемия
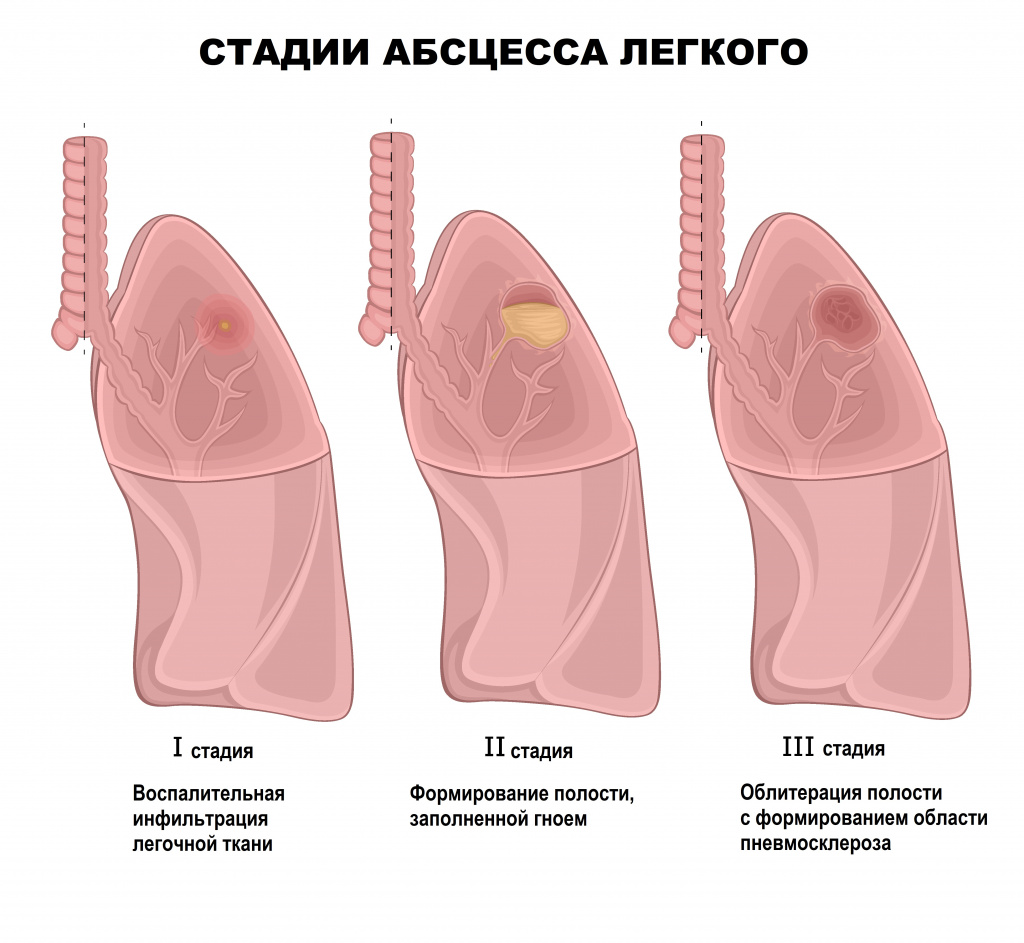
Септикопиемия — это форма сепсиса, при которой в организме, помимо общей интоксикации, начинают возникать метастатические абсцессы в органах и тканях, которые являются результатом бактериальной эмболии. Чаще всего первые абсцессы обнаруживаются в легких, а затем процесс распространяется на другие органы: печень, печень, сердце, менингиальные оболочки, синовиальные оболочки. Абсцессы могут прорваться и вызвать развитие эмпиемы плевры, флегмоны, перитонита и др.
Клиническая классификация сепсиса по стадиям
Клиническое стадирование сепсиса играет важную роль, так как оно помогает врачам выбирать оптимальную тактику и добиваться наилучших из возможных в каждом конкретном случае результатов лечения. Выделяют следующие стадии:
- Сепсис диагностируют, когда внутренняя температура (измеряется на слизистых оболочках) тела поднимается больше 38 градусов или опускается ниже 36 градусов, частота сердечных сокращений 90 в минуту и более, частота дыхания 20 в минуту и более, либо парциальное давление углекислого газа в артериальной крови (PaCO2) опускается ниже 32 мм. рт. ст. При этом уровень лейкоцитов в крови поднимается более 12000/мкл или опускается ниже ≤4000/мкл, либо среди них появляется более 10% незрелых форм.
- Тяжелый сепсис – сепсис, который сочетается с острой органной дисфункцией.
- Септический шок диагностируют, когда у пациента имеется стойкая гипотензия (снижение артериального давления) или гипоперфузия (недостаточное кровоснабжение) тканей, несмотря на адекватную инфузионную терапию.
- Синдром полиорганной дисфункции – состояние, при котором у больного имеется органная дисфункция (нарушение работы внутренних органов), и его гомеостаз не удается поддерживать без медикаментозного вмешательства.
Лечение сепсиса
Лечение сепсиса базируется на трех принципах:
Санация первичного очага. Это может быть достигнуто с помощью хирургического вмешательства и/или адекватной антибактериальной терапии. При обнаружении первичного очага, который можно санировать хирургически, необходимо провести это как можно скорее. Это может быть вскрытие и дренирование абсцессов, удаление инфицированных инвазивных устройств (катетеры, имплантаты и др.), дренирование и лаваж брюшной полости, и др.
Антимикробная терапия является еще одним краеугольным камнем лечения сепсиса, при этом важна ее своевременность и адекватность. Например, при развитии септического шока, препараты должны быть введены в течение часа от начала симптомов. При этом препарат должен охватывать весь спектр предполагаемых возбудителей и, что немаловажно, проникать в первичный инфекционный очаг. При необходимости назначения комбинированной терапии из нескольких препаратов, их применяют не более 5 дней, после чего должны быть получены данные биологических методов исследования и произведена коррекция схемы лечения. [7]
Обеспечение транспорта кислорода — все клинические проявления сепсиса усугубляются в условиях недостатка кислорода, поэтому очень важно контролировать этот процесс. Для этого проводят:
- Гемодинамическую поддержку — вливание растворов, которые обеспечивают восполнение водно-электролитного баланса, назначаются препараты, поддерживающие артериальное давление и др.
- Респираторную поддержку — искусственную вентиляцию легких, кислородные маски и др.
Коррекция метаболических нарушений
Одним из эффективных способов лечения сепсиса является селективная сорбция на колонках TORAYMYXIN. Данная методика успешно применяется во многих странах мира. В настоящее время такое лечение прошли более 200 тысяч пациентов с септическим шоком и тяжелыми формами сепсиса. Эффективность и безопасность технологии подтверждена в ходе клинических исследований. [11,12]

Осложнения при сепсисе
- Осложнения со стороны дыхательной системы. Нарушение вентиляции легких приводит к повышению аэрогематического барьера и, как следствие, пропотеванию жидкости в альвеолы. Это еще больше нарушает газообмен и приводит к развитию шокового легкого и респираторного дистресс-синдрома, который усугубляется усталостью дыхательных мышц.
- Осложнения со стороны почек. Наблюдается снижение фильтрационной функции почек из-за повреждения канальцев, развившееся в результате снижения давления. Сопровождается резким уменьшением выделяемой мочи, протеинурией, азотемией.
- Нарушение свертывания крови из-за падения уровня тромбоцитов и развития ДВС-синдрома — грозного состояния, при котором сначала происходит массовое образование тромбов в кровеносном русле, а затем массивные кровотечения из-за недостаточности кровесвертывающих факторов.
- Неврологические осложнения. Длительно протекающий сепсис может привести к развитию полинейропатии, которая, в частности, приводит к ослаблению дыхательной мускулатуры и невозможности самостоятельного дыхания.
- Септический шок — самое тяжелое проявление сепсиса, сопровождающееся стойким снижением кровяного давления, которое сложно восстановить даже с применением инфузионной терапии и вазопрессоров. Он развивается из-за выхода жидкости из кровеносных сосудов и из-за общего обезвоживания. При этом, нарушения настолько тяжелые, что могут привести к гибели пациента от полиорганной недостаточности.[13]
Прогноз при сепсисе
Прогноз при сепсисе очень осторожный. На возможность выздоровления оказывают влияние особенности этиологической микрофлоры, общее состояние пациента в начале заболевания, а также своевременность и адекватность проводимого лечения. Наиболее неблагоприятно сепсис протекает у людей старческого возраста и у ослабленных пациентов, имеющих сопутствующие заболевания.
В целом в крупных клиниках летальность при данном состоянии составляет 30-40%. При развитии септического шока, ситуация усугубляется и согласно некоторым данным, в таком случае от него погибает до 90% больных.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Абсцесс: причины появления, симптомы, диагностика и способы лечения.
Определение
Абсцесс - это ограниченное скопление гноя, окруженное оболочкой (пиогенной капсулой).
Причины появления абсцессов
Абсцессы могут быть асептическими и септическими. Асептические абсцессы развиваются после подкожного введения некоторых раздражающих химических веществ (скипидара, керосина, хлоралгидрата, хлористого кальция), которые вызывают некроз тканей. При этом некротизированные ткани растворяются лейкоцитами с образованием гноя, не содержащего микробов. Септические абсцессы чаще всего формируются в результате внедрения в ткани микроорганизмов (стафилококков, стрептококков, кишечной палочки, синегнойной палочки и т.д.), вызывающих гнойное воспаление.
Инфекционные агенты (бактерии, грибы) могут проникать в организм экзогенно через поврежденный эпителий кожи или слизистые оболочки (входные ворота) или эндогенно (из очага инфекции в самом организме).
Открытые повреждения кожи, инородные тела, медицинские манипуляции (инъекции, блокады, пункции), гематомы, серомы, а также гнойно-воспалительные процессы в организме (сепсис, гнойный лимфаденит, гнойный лимфангит, гнойный тромбофлебит, фурункул, карбункул и др.) могут приводить к развитию абсцесса.
На месте внедрения инфекции и воспаления ткани отмирают, и формируется гнойная полость, вокруг которой на границе со здоровой тканью начинает образовываться пиогенная капсула. Эта капсула служит своеобразным биологическим барьером, препятствующим распространению инфекции по организму. Чем дольше существует абсцесс, тем толще становится пиогенная капсула.
По распространенности самым частым считается абсцесс кожи, подкожной жировой клетчатки и мышечной ткани, хотя возникнуть он может в любом органе и ткани.
При прогрессировании гнойного процесса повышается риск разрыва пиогенной капсулы, в результате чего инфекционный процесс распространяется за ее пределы.
Классификация абсцессов
По причине возникновения:
а) стафилококковые;
б) стрептококковые;
в) пневмококковые;
г) колибациллярные;
д) гонококковые;
е) анаэробные неспорообразующие;
ж) клостридиальные анаэробные;
з) смешанные;
и) грибковые и др.
По происхождению и путям проникновения инфекции:
- метастатические (гематогенные) абсцессы, возникающие из отдаленных гнойных очагов;
- контактные абсцессы, происходящие из близлежащих очагов воспаления;
- травматические абсцессы, являющиеся следствием открытых и проникающих повреждений;
- криптогенные абсцессы, происхождение которых и пути проникновения инфекции установить не представляется возможным.
- поверхностные (поражение кожи и подкожной клетчатки);
- глубокие (в органах и тканях):
- острые абсцессы;
- хронические абсцессы.
Симптомы абсцессов
В начальной стадии формирования поверхностного абсцесса определяется отграниченная болезненная припухлость, горячая на ощупь. Через 3-4 дня в центре появляется размягчение, кожа в центре инфильтрата становится более тонкой и темной, а границы абсцесса - более четкими. На 4-7 сутки абсцесс вскрывается и из него выходит гнойное содержимое. При этом болезненность воспаленного участка уменьшается.
Абсцесс печени чаще всего возникает в результате распространения инфекции по сосудистому руслу из воспалительных очагов других органов или тканей брюшной полости (аппендицит, холангит, язвенный колит). Абсцессы могут быть одиночными или множественными. Для заболевания характерна высокая температура, озноб, боль и тяжесть в области печени, увеличение ее размеров.
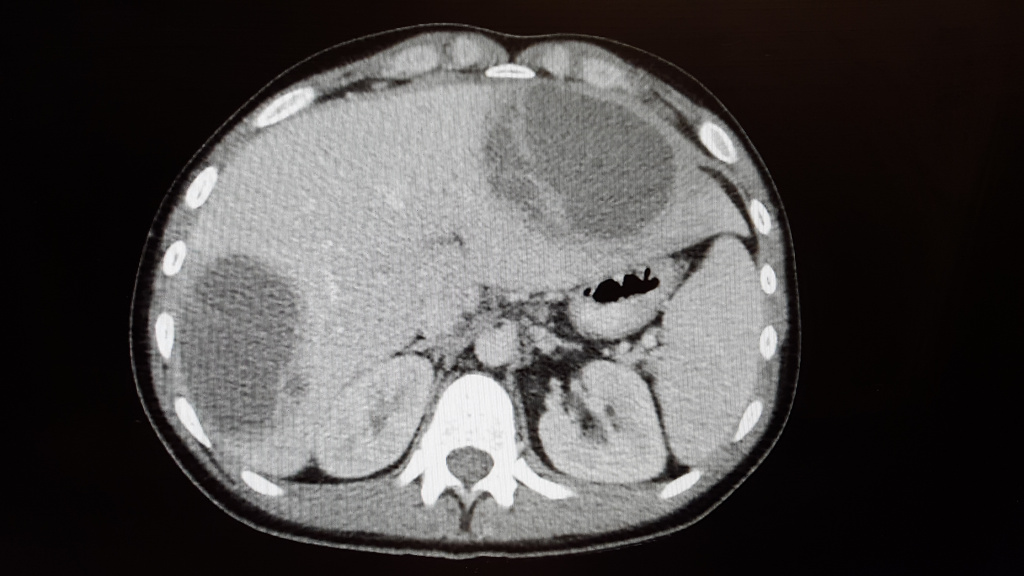
Абсцесс в печени
Абсцесс головного мозга может сформироваться в результате проникновения инфекции из среднего или внутреннего уха, придаточных пазух носа, из гнойных очагов мягких тканей головы. Абсцессы могут быть одиночными или множественными. Заболевание начинается с интоксикации, симптомов повышения внутричерепного давления (головной боли, тошноты и рвоты, сонливости, недомогания, нарушения памяти, расстройства внимания, нарушения зрения). Затем присоединяются общемозговые (головокружение, психомоторное возбуждение, галлюцинации) и очаговые симптомы (неврологические симптомы, свойственные местному поражению определенных структур центральной или периферической нервной системы).
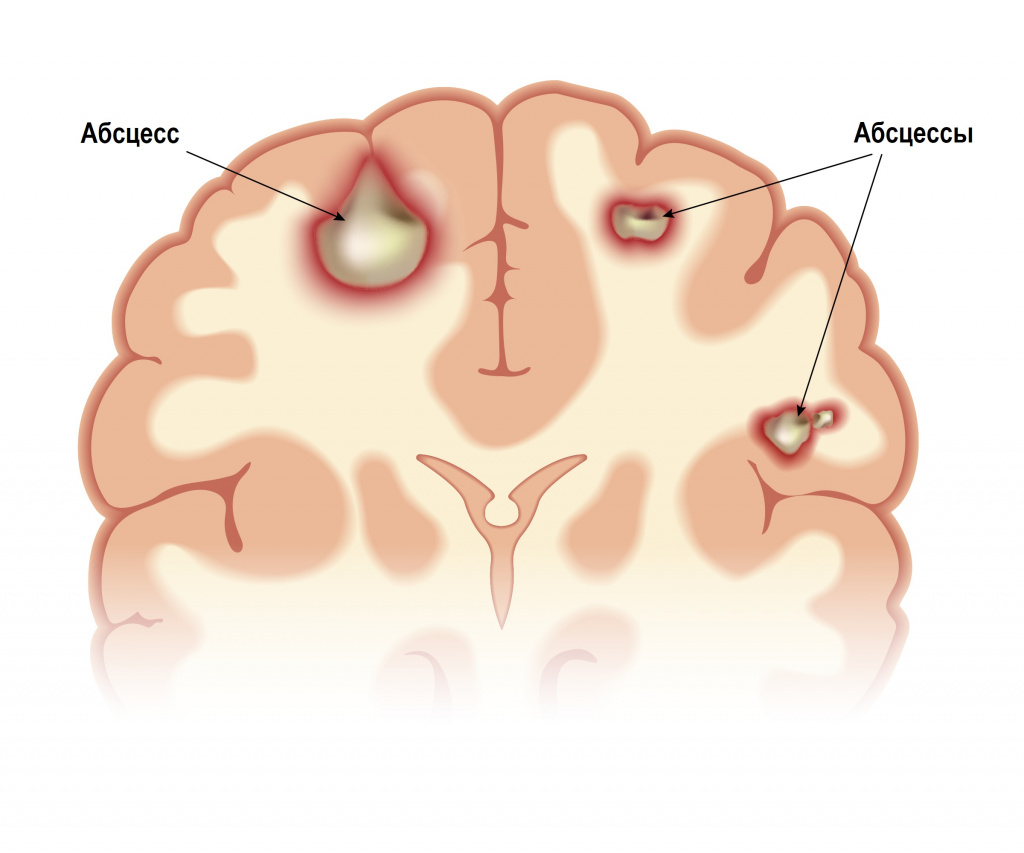
Внутримозговой абсцесс
Абсцессы брюшной полости встречаются в 30-35% у больных гнойным перитонитом. Обычно они располагаются в отлогих областях живота: подпеченочном, поддиафрагмальном пространстве, в подвздошных ямках и т.п. Клинике формирования абсцесса соответствует ухудшение состояния после небольшого светлого промежутка на фоне воспалительного заболевания брюшной полости (аппендицита, холецистита), наблюдается усиление интоксикации и боль в животе.
Внутрикостный абсцесс Броди – это отграниченный некроз губчатого вещества кости с преследующим расплавлением и образованием полости. Локализуется обычно в проксимальном отделе большеберцовой кости. Заболевание начинается с чувствительности к надавливанию. Нередко очаги ничем не проявляются, и боль носит эпизодический характер. Повышение температуры, озноб и другие симптомы интоксикации, как правило, отсутствуют, процесс может длиться годами.
Диагностика абсцессов
Диагностика поверхностного абсцесса не представляет трудностей. Диагноз устанавливается по совокупности жалоб и осмотра. Диагностика глубоких абсцессов может быть основана на результатах дополнительных лабораторных и инструментальных методов исследования.
-
Клинический анализ крови: общий анализ, лейкоформула, СОЭ (с микроскопией мазка крови при наличии патологических сдвигов) покажет присутствие в организме воспалительного процесса.
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
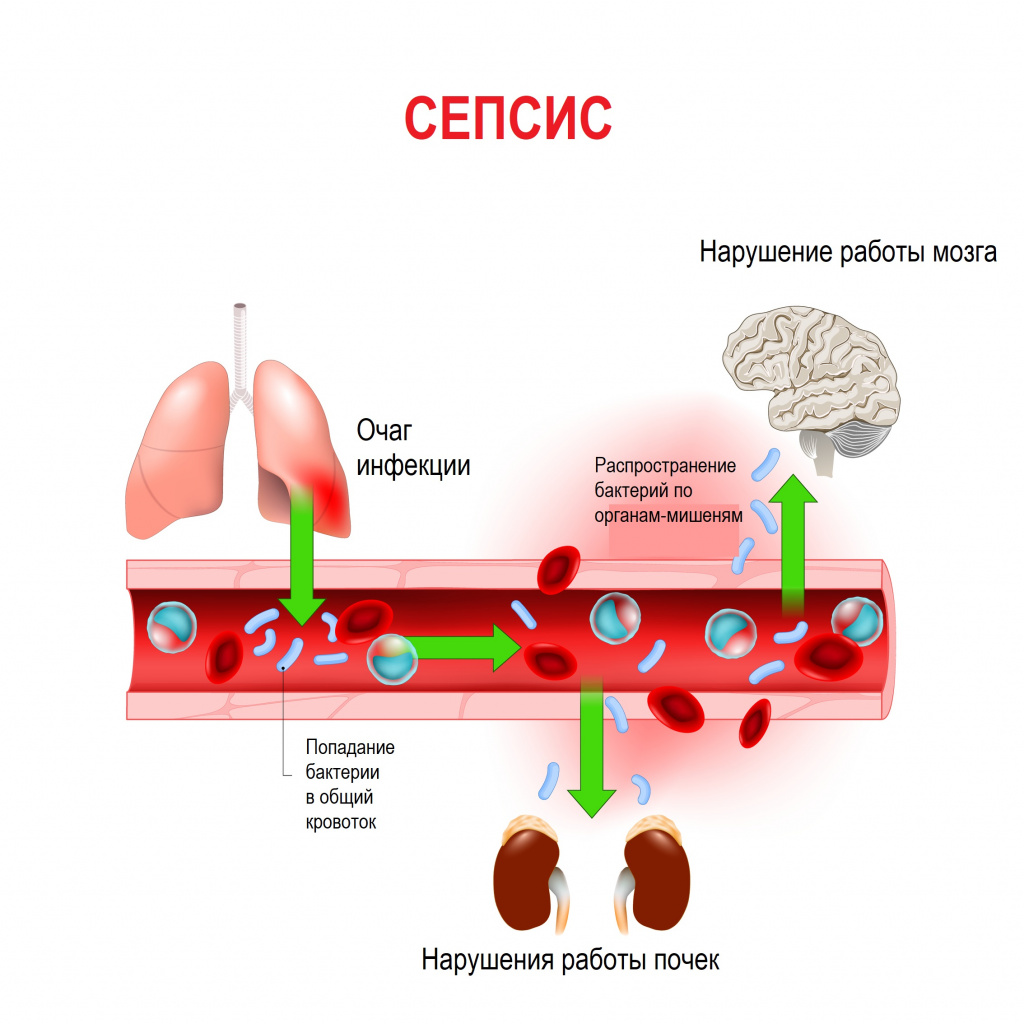
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
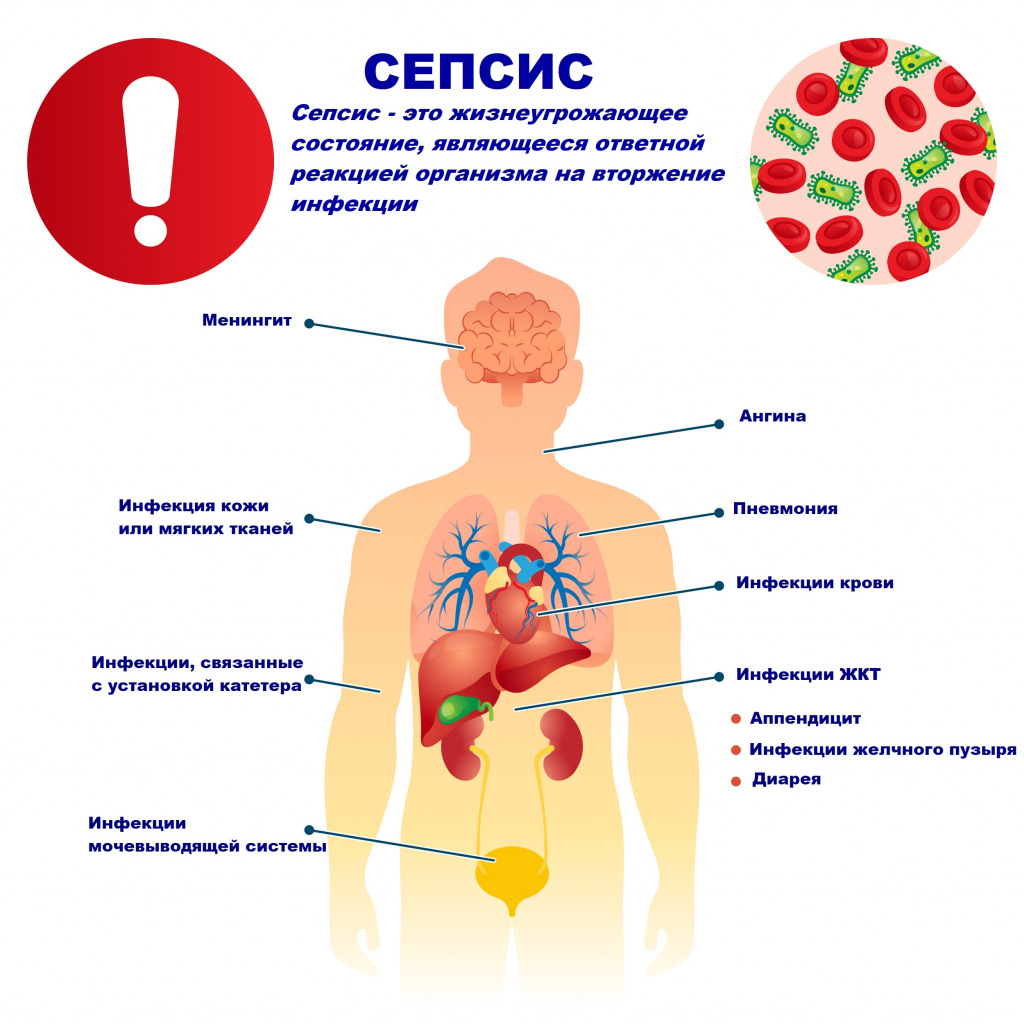
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Флегмона: причины появления, симптомы, диагностика и способы лечения.
Определение
Флегмона – это острое разлитое гнойное воспаление жировой клетчатки с тенденцией к быстрому распространению по клетчаточным пространствам и вовлечением в гнойный процесс мышц, сухожилий. Заболевание возникает в результате проникновения в мягкие ткани патогенных микроорганизмов, чаще золотистого стафилококка и стрептококка.
В отличие от абсцесса флегмона не имеет четких границ, поэтому гнойный экссудат может быстро распространяясь в окружающие ткани, постепенно приводя к их разрушению и некрозу.
Флегмона может образоваться на лице, шее, в полостях тела, на конечностях, в зоне переломов, раневых поверхностей, в местах укусов животных.
Причины появления флегмоны
Гнойную флегмону вызывают гноеродные микробы (стафилококки, стрептококки, синегнойная палочка и др.). При проникновении в ткани кишечной палочки, вульгарного протея, гнилостного стрептококка развивается гнилостная флегмона. Наиболее тяжелые формы флегмоны вызывают облигатные анаэробы, размножающиеся в условиях отсутствия кислорода. Так как микроорганизмы являются достаточно агрессивными, то и развитие воспаления происходит очень быстро.
Флегмона в большинстве случаев связана с проникновением в ткани патогенных микроорганизмов гематогенным путем (при повреждениях кожи и слизистых оболочек) и ятрогенным путем (инъекции) при несоблюдении правил асептики или техники введения препаратов.
Причиной флегмоны может стать попадание под кожу различных химических веществ (скипидара, керосина и др.).
Сильное и быстрое распространение процесса воспаления по клеточному пространству имеет связь со сниженным иммунитетом организма, его истощением, хроническими заболеваниями (туберкулезом, болезнями крови, сахарным диабетом и др.), регулярными интоксикациями (например, алкогольной) и иммунодефицитными состояниями.
Флегмоны могут стать осложнением других гнойных заболеваний (карбункула, абсцесса, сепсиса).
Другие причины формирования флегмоны:
- негнойное воспаление подкожной клетчатки (целлюлит), обычно распространяющееся по ходу соединительной ткани в межклеточном пространстве;
- осложнения остеомиелита, тромбофлебита, лимфаденита;
- в последние годы в связи с развитием эстетической хирургии участились случаи возникновения флегмон после операций по коррекции фигуры и введения филлеров.
Флегмона может быть первичной (возникшей в результате непосредственного внедрения микроорганизмов) или вторичной (развившейся при переходе воспаления с окружающих тканей), острой или хронической, поверхностной (поражение ткани до мышечного слоя) или глубокой, прогрессирующей или отграниченной.
С учетом локализации флегмоны подразделяют на подкожные, межмышечные, подфасциальные, забрюшинные, межорганные, флегмоны клетчатки средостения, флегмоны шеи, кисти, стопы.
Согласно медицинской классификации, флегмона подразделяется на следующие виды:
Клинические проявления флегмоны почти всегда протекают бурно и характеризуются внезапным началом и быстрым распространением. Среди ключевых признаков флегмоны выделяют:
- резкое повышение температуры до крайне высоких значений (39-40°С);
- общую интоксикацию со слабостью, бледностью, недомоганием, снижением аппетита, тошнотой, потливостью;
- озноб, головную боль, жажду;
- красноту и резкий отек тканей в месте поражения (если это подкожный процесс);
- увеличение лимфоузлов;
- нарушение функции пораженной части тела;
- формирование плотного, горячего, болезненного инфильтрата, не имеющего четкой границы;
- постепенное формирование участка размягченных тканей (гнойной полости).
Хроническая флегмона характеризуется появлением инфильтрата, кожа над которым приобретает синюшный оттенок.
Одним из видов хронической флегмоны является деревянистая флегмона (флегмона Реклю) – результат инфицирования микроорганизмами ротоглотки.
При серозной флегмоне клетчатка имеет студенистый вид, пропитана мутной водянистой жидкостью, по периферии воспалительный процесс без четкой границы переходит в неизмененную ткань. При прогрессировании процесса пропитывание мягких тканей резко увеличивается, жидкость становится гнойной. Процесс может распространяться на мышцы, сухожилия, кости.
Гнилостная флегмона характеризуется развитием в клетчатке множественных участков некроза, расплавлением тканей, обильным гнойным отделяемым со зловонным запахом.
Для анаэробной флегмоны характерны распространенное серозное воспаление мягких тканей, обширные участки некроза и образование в тканях множественных пузырьков газа.
Диагностика флегмоны
Как правило, для диагностики флегмоны назначают:
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Постинъекционный абсцесс – это ограниченный гнойно-воспалительный очаг в месте инъекционного введения лекарственного препарата. Для абсцесса характерно появление локального отека и покраснения кожи, постепенно увеличивающегося в объеме уплотнения, нарастание болей распирающего характера, флюктуация. Диагноз ставится на основании анамнеза и клинической картины (появление гнойно-воспалительного очага в месте проведения внутримышечных и внутривенных инъекций), данных УЗИ, МРТ мягких тканей. На стадии инфильтрации эффективно консервативное лечение. Сформировавшийся абсцесс вскрывают хирургическим путем и дренируют.
МКБ-10
Общие сведения
Случаи постинъекционного абсцедирования мягких тканей встречаются у лиц всех возрастов, чаще у тучных, полных пациентов. Большая часть постинъекционных гнойников развивается в области ягодиц, так как для парентерального введения лекарственных средств ягодичную мышцу используют чаще всего. У детей велика доля абсцессов плеча как следствие проведения прививок. Внутривенное введение наркотиков – наиболее частая причина формирования очага нагноения в области локтевой ямки. Постинъекционные абсцессы этой локализации составляют 69% всех случаев гнойно-воспалительных процессов мягких тканей у наркозависимых.

Причины
- Высокая патогенность микроорганизмов. Разные виды бактерий имеют различную скорость деления клеток и способность противостоять иммунной системе. Золотистый стафилококк или синегнойная палочка чаще вызывают формирование постинъекционного абсцесса, чем условно-патогенные виды, составляющие микрофлору кожи.
- Ослабление иммунитета. Может быть следствием банального сезонного ОРВИ или серьезного сопутствующего заболевания. Вероятность развития абсцессов выше у больных сахарным диабетом, тяжелыми сердечно-сосудистыми, эндокринными, инфекционными заболеваниями.
- Локальное нарушение кровообращения. Этому способствует одномоментное введение значительных объемов раствора в мышцу (более 5 мл), одновременное введение нескольких препаратов в одну ягодицу. Первым признаком абсцедирования является значительное уплотнение в месте уколов. Риск постинъекционного нагноения повышается у лежачих больных, пациентов с пролежнями.
- Местнораздражающее действие лекарств. Спровоцировать гнойное расплавление тканей способны не только бактерии, но и химические вещества. Ошибочное внутримышечное введение препаратов, предназначенных для внутривенных или подкожных вливаний, может вызвать некроз и воспаление. Индивидуальную реакцию может дать препарат, который разрешен для внутримышечного применения, но не подходит конкретному пациенту.
- Нарушение техники инъекций. Факторами развития постинъекционных осложнений служат несоблюдение правил асептики и антисептики, использование неправильного растворителя, слишком быстрое введение растворов, несовместимость разных лекарственных средств. Одним из последствий неправильной техники может стать повреждение сосудов различного диаметра иглой. Сгустки крови являются субстратом для размножения микроорганизмов и формирования постинъекционного абсцесса.
Патогенез
В основе развития воспалительной реакции лежит выход из поврежденных и погибших клеток во внеклеточную среду большого количества лизосомальных ферментов, которые изменяют обмен веществ в патологическом очаге. В зоне некроза обмен веществ замедляется, а в прилегающих к нему областях резко усиливается, что приводит к повышению потребления кислорода и питательных веществ, развитию ацидоза вследствие накопления недоокисленных продуктов: молочной, пировиноградной и других кислот.
Кровоснабжение патологического очага изменяется: усиливается приток крови и замедляется отток. Этим объясняется покраснение пораженной области. Кровеносные сосуды расширяются, повышается проницаемость капилляров для плазмы крови и клеток. В ткани выходят лейкоциты, макрофаги. Локальный приток жидкости приводит к формированию отека. Сдавливание нервных окончаний провоцирует болевые ощущения. Это этап инфильтрата, когда в очаге воспаления гноя еще нет. При благоприятных условиях на этапе инфильтрации изменения обратимы.
На этапе абсцедирования отмершие ткани и погибшие клетки иммунной системы образуют гной. Постинъекционный абсцесс располагается в центре очага воспаления. Сгустки гноя отграничены от здоровых тканей грануляционным валом. Гной не рассасывается. Устранить воспаление можно лишь в том случае, если создать условия для оттока содержимого абсцесса.
Симптомы постинъекционного абсцесса
Патологический очаг формируется в течение нескольких дней. Начало заболевания может пройти незамеченным для пациента в связи с незначительной степенью выраженности симптомов. Замаскировать первые проявления развивающегося гнойного воспаления могут боли и припухлость мест инъекции, обусловленные физиологической реакцией на введение лекарств. Разграничить формирование воспалительного инфильтрата и нормальную для внутримышечных инъекций реакцию можно при внимательном отношении к своим ощущениям.
Боль после укола сразу резкая распирающая, затем ноющая. Интенсивность ее достаточно быстро уменьшается. Боль при зреющем абсцессе постоянно усиливается. В норме уплотнение после уколов достаточно равномерное, температура его не отличается от температуры окружающих областей, кожа над уплотнением обычного цвета. Присоединение воспалительной реакции знаменуется заметным локальным повышением температуры. Нарастание отека и болей в ягодице приводит к тому, что на пораженной стороне невозможно сидеть. Неприятные ощущения усиливаются при ходьбе и выполнении других движений. Надавливание на область абсцесса резко болезненно, тогда как обычное уплотнение можно ощупать, не провоцируя у пациента выраженных неприятных ощущений.
Для постинъекционного абсцесса характерна лихорадка с повышением температуры тела до 39-40 о С. Однако ориентироваться только на этот симптом не стоит. Если воспалительный очаг развивается на фоне продолжающихся инъекций нестероидных противовоспалительных средств, обладающих обезболивающим и жаропонижающим действием, то гипертермия отсутствует.
Осложнения
Бурное развитие инфекции в очаге может спровоцировать образование затеков гноя в межмышечные пространства. Распространение бактерий в тканях вызывает развитие обширных флегмон ягодицы, бедра, плеча. Существует опасность формированием длительно незаживающих свищей мягких тканей и прямокишечных фистул. Прорыв гноя в кровеносное русло становится причиной сепсиса, перикардита, остеомиелита, ДВС-синдрома - в этих случаях даже при назначении адекватного лечения исход для пациента может быть неблагоприятным.
Диагностика
Постановка диагноза не вызывает у консультирующего хирурга сложностей. Характерная пентада признаков воспаления (покраснение, отек, боли, повышение температуры, нарушение функции) в месте выполнения инъекций позволяет быстро определиться с характером патологического процесса. Положительный симптом флюктуации свидетельствует о наличии жидкости в очаге, что является показанием к проведению хирургической операции. Для подтверждения диагноза постинъекционного абсцесса в сомнительных случаях проводят:
Лечение постинъекционного абсцесса
Подходы к лечению абсцессов на этапах инфильтрации и нагноения кардинально различаются. В первом случае показана консервативная терапия, во втором - хирургическая операция. Основные принципы консервативного местного лечения инфильтратов могут быть с успехом применены для быстрого рассасывания постинъекционных уплотнений, не имеющих признаков воспаления.
- Общее лечение. Его объем определяется врачом исходя из клинической картины. Противовоспалительные препараты и антибиотики нацелены на разрешение воспалительного процесса. Дополнительно может быть назначена инфузионная терапия для борьбы с интоксикацией.
- Местная терапия. Предполагает нанесение на пораженную область мази Вишневского или использование компрессов с димексидом. На начальных этапах допускается выполнение йодной сетки. Если улучшения состояния не наступает в течение суток, целесообразно использовать более эффективные препараты.
- Физиотерапия. Все тепловые воздействия под запретом. Эффективны электрофорез противовоспалительных средств, диадинамические токи. Физиотерапевтические процедуры назначаются одновременно с местным и общим противовоспалительным лечением.
- Хирургическая операция.Вскрытие и дренирование гнойной полости проводится под местным обезболиванием. Под общим наркозом операция выполняется при расположении постинъекционного абсцесса глубоко в тканях. В послеоперационном периоде проводится общее и местное консервативное лечение, назначаются физиотерапевтические процедуры.
Прогноз и профилактика
Прогноз постинъекционного нагноения благоприятный при условии своевременного обращения за медицинской помощью. В противном случае возможно развитие осложнений заболевания. Самопроизвольное вскрытие и опорожнение глубокого абсцесса невозможно, а без эвакуации гноя из полости выздоровление не наступает. Хирургическое вскрытие гнойника позволяет решить проблему за один день.
Профилактика постинъекционных осложнений предполагает введение лекарств парентерально в условиях лечебных учреждений медицинским персоналом, отказ от самолечения. Места введения растворов при курсовом назначении целесообразно менять: если на ягодицах уже сформировались уплотнения, можно вводить лекарства в мышцы передней поверхности бедра. Нельзя вводить средства для в/в инфузий в мышцы, даже если вены тонкие и ломкие. Инъекционный курс желательно сделать максимально коротким, продолжив лечение приемом таблеток.
1. Хирургическое лечение постинъекционных абсцессов мягких тканей и фармакологические возможности в повышении эффективности и безопасности инъекций: Автореферат диссертации/ Елхов И.В. - 2007.
2. Постинъекционные кровоподтеки, инфильтраты, некрозы и абсцессы/ Ураков А.Л., Уракова Н.А.// Современные проблемы науки и образования. - 2012 - №5.
3. Локальные постинъекционные осложнения или медикаментозноеятрогенное заболевание - инъекционная болезнь/ Уракова Н.А., Ураков А.Л.// Проблемы экспертизы в медицине. - 2014.
4. Лечение постинъекционных инфильтратов, абсцессов и флегмон/ Колб Л.И.// Военная медицина. - 2009 - №1.
Читайте также:

