Что такое синдром опухолевой интоксикации
Обновлено: 13.05.2024
Опухолевая интоксикация констатирует отравление организма продуктами жизнедеятельности злокачественной опухоли. Патологическое состояние не удостоилось отдельного места в классификациях, но его не минует ни один пациент с генерализованным процессом, эпизоды возможны и во время лекарственного лечения.
Причины опухолевой интоксикации
Главная причина — наличие клеток, выделяющих биологически активные вещества. Некоторые новообразования вырабатывают вредные субстанции, но после удаления первичной опухоли все признаки отравления бесследно исчезают. Такого рода интоксикация возникает ещё до обнаружения опухоли, так бывает при аденокарциноме легкого, когда вырабатываемые клетками вещества вызывают боли в суставах, при злокачественных лимфомах токсины инициируют слабость с потливостью и высокой температурой.
Интенсивность проявлений зависит от биологических особенностей клеток и их общей массы, при прогрессировании с увеличением объема опухоли усиливаются и симптомы хронического отравления. Особенно выраженные признаки наблюдаются при распаде опухоли, аналогичное по проявлениям, но гораздо более тяжелое состояние может развиться при массированной гибели злокачественных клеток в результате химиотерапии. При лечении высокочувствительных к цитостатикам новообразований лимфатической ткани и крови проводится профилактика синдрома лизиса опухоли.
Симптомы интоксикации характерны для множественных метастазов в костях, когда к токсичным клеточным продуктам присоединяется негативное действие выходящего из распадающейся костной ткани кальция — гиперкальциемия.

Симптомы опухолевой интоксикации
Интоксикация — это отравление, но не острое, а хроническое, то есть признаки его нарастают постепенно. Исключение составляет только синдром лизиса опухоли во время химиотерапии, когда клинические проявления нарастают стремительно вплоть до острой почечной недостаточности.
Типичны для интоксикации слабость и быстрая утомляемость, доводящие пациента до постоянного пребывания в постели. Возможно повышение температуры — от субфебрилитета при генерализованном процессе до 40°С при распаде крупного опухолевого конгломерата с образованием некротической полости диаметром в несколько сантиметров.
У всех пациентов изменяется цвет кожи — от бледного до землистого, всё индивидуально, но заметно окружающим. Присоединяется небольшая отечность поверхностных тканей — пастозность, повышается потливость, особенно ночная.
Продукты ракового метаболизма циркулируют в крови, оседая в органах и нарушая их функционирование. Повреждение сердечно-сосудистой системы проявляется изменением ритма сердца и учащением дыхания, нервной системы — депрессией с дневной сонливостью при нарушениях ночного сна. Почечные канальцы забиваются продуктами метаболизма, снижая выделительную функцию.
Частично токсичные продукты выводятся слизистой оболочкой желудочно-кишечного тракта, что приводит к её сухости и, как следствие, нарушению аппетита. Печень активно борется с токсинами, но и она перестает справляться, изменяя содержание в плазме микроэлементов и вязкость крови. При тяжелой опухолевой интоксикации постоянная тошнота сменяется не приносящей облегчения рвотой.
Диагностика и лечение опухолевой интоксикации
В первую очередь об интоксикационном синдроме свидетельствует совокупность жалоб пациента и его внешний вид, начиная с нездоровой окраски кожи.
В общем анализе крови интоксикацию заметить непросто, но в биохимическом может повыситься концентрация печеночных трансаминаз, креатинина, мочевой кислоты, калия и фосфатов.
Стимуляция аппетита заключается не только в приеме противорвотных и даче стимуляторов аппетита, необходима тщательная коррекция микроэлементов и макронутриентов — белков, жиров и углеводов. Недостаточно вызвать аппетит, надо предоставить питание, не усугубляющее опухолевую интоксикацию и помогающее восстановлению.
Длительность и интенсивность медикаментозной терапии зависит от степени выраженности интоксикации. В тяжелых случаях может потребоваться гемосорбция — очищение крови специальной аппаратной системой, или только очищение плазмы при плазмаферезе.
Адекватная терапия опухолевой интоксикации не только улучшит состояние пациента, но и увеличит продолжительность его жизни, сделав её качественней и спокойнее.
Не всегда при злокачественном заболевании возможно остановить протекание болезни, но необходимо стремиться сделать жизнь онкобольного достойной. В нашей клинике помогают всем онкологическим пациентам и в любой период развития опухоли.
Синдром распада опухоли – симптомокомплекс, обусловленный быстрым разрушением большого количества клеток злокачественной неоплазии. Обычно возникает при лечении болезней системы крови, реже – при терапии других онкологических заболеваний. Сопровождается метаболическими расстройствами, которые становятся причиной развития аритмии, брадикардии, судорог, расстройств сознания, острой почечной недостаточности, поноса или запора, тошноты, рвоты, кишечной непроходимости и других нарушений деятельности различных органов и систем. Диагностируется на основании симптомов и данных лабораторных анализов. Лечение – инфузионная терапия, симптоматическая терапия, гемодиализ.

Общие сведения
Синдром распада опухоли – ургентное состояние, возникающее в процессе консервативного лечения онкологических заболеваний. Чаще всего диагностируется при острых лимфобластных лейкозах и лимфомах, реже – при хронических лейкозах и солидных новообразованиях различной локализации. Синдром распада опухоли обычно выявляется на фоне приема химиопрепаратов или после завершения химиотерапии, реже наблюдается при проведении лучевой терапии, в отдельных случаях развивается спонтанно. Сопровождается возникновением острой почечной недостаточности, обусловленной гиперурикемией. Представляет угрозу для жизни больного, требует неотложной коррекции. Лечение осуществляют специалисты в сфере онкологии, урологии и реаниматологии.

Причины
Обычно синдром распада опухоли развивается в процессе лечения злокачественных новообразований, что обусловлено интенсивным разрушением клеток опухоли под действием химиопрепаратов либо лучевой терапии. Лейкозы и лимфомы, особенно – лимфома Беркитта имеют изначальную склонность к такому распаду, усугубляющуюся после начала лечения. Риск развития синдрома распада опухоли увеличивается при новообразованиях больших размеров. Из-за относительно медленного роста сосудов, не успевающих за быстрой пролиферацией опухолевых клеток, в крупных опухолях часто образуются участки с недостаточным кровоснабжением. Эти участки могут некротизироваться как спонтанно, так и при проведении терапии, травматизации неоплазии или ухудшении кровообращения, обусловленном различными факторами (изменением состояния больного, сдавлением крупного питающего сосуда и т. д.).
При синдроме распада опухоли в течение короткого периода времени разрушается большое количество злокачественных клеток, содержащих фосфаты и пуриновые нуклеотиды. Нуклеотиды метаболизируются в печени с образованием мочевой кислоты. В крови резко возрастает уровень мочевой кислоты, фосфора, калия и некоторых других веществ. Наряду с перечисленными расстройствами при синдроме распада опухоли развивается лактацидоз, обусловленный нарушением функций печени вследствие поражения отдаленными метастазами и/или токсического воздействия продуктов распада неоплазии на клетки органа.
Возникают характерные для синдрома распада опухоли расстройства кислотно-щелочного и водно-солевого обмена, оказывающие негативное влияние на деятельность всех органов и систем. Все это происходит на фоне истощения, метастатического поражения лимфоузлов и отдаленных органов, лейкоцитоза, анемии, расстройств иммунитета и предшествующего накопления токсичных метаболитов в крови, что еще больше ухудшает ситуацию и может стать причиной резкой декомпенсации состояния пациента с синдромом распада опухоли.
Из-за закисления крови снижается pH мочи. Кристаллы мочевой кислоты осаждаются в мозговом веществе, собирательных трубочках и почечных канальцах, препятствуя фильтрации и выведению мочи. Отмечается снижение почечного клиренса и уменьшение скорости фильтрации почек. Дополнительным фактором, усугубляющим нарушения функции почек при синдроме распада опухоли, является гиперфосфатемия, сочетающаяся с гипокальциемией. Из-за снижения уровня кальция в крови повышается уровень паратиреоидного гормона, стимулирующего выведение фосфатов из организма.
В результате действия этого гормона в ткани почек пациентов с синдромом распада опухоли откладываются соли кальция, также препятствующие фильтрации и выведению мочи. Возникают азотемия, олиго- или анурия, сопровождающиеся накоплением токсичных продуктов обмена в организме. Развивается острая почечная недостаточность, представляющая угрозу для жизни больного синдромом распада опухоли. Гипокальциемия и гиперкалиемия становятся причиной нарушений деятельности сердечно-сосудистой системы. Расстройства обмена влекут за собой нарушения функций центральной нервной системы и системы пищеварения.
Выделение распадающимися клетками ферментов, образование очагов некроза и снижение иммунитета способствуют развитию воспаления, присоединению инфекции и последующему нагноению в зоне распада новообразования и прилегающих тканей. Инфекционные осложнения еще больше ухудшают состояние больного с синдромом распада опухоли, затрудняют процесс лечения и могут становиться причиной развития сепсиса. Еще одним опасным осложнением данного состояния является расплавление крупного сосуда, сопровождающееся обильным кровотечением.
Симптомы синдрома распада опухоли
Развитие синдрома распада опухоли сопровождается ухудшением состояния больного. Возникают прогрессирующая слабость и гипертермия. Отмечаются диспепсические расстройства: боли в животе, тошнота, рвота, отсутствие аппетита, запоры или диарея. При поражении ЦНС наблюдаются судороги, парестезии и нарушения сознания. Поражение сердечно-сосудистой системы при синдроме распада опухоли проявляется брадикардией, аритмией и артериальной гипотонией. О развитии почечной недостаточности свидетельствуют олигоурия или анурия. У пациентов с синдромом распада опухоли нередко возникает желтушность кожных покровов вследствие нарушения функций печени.
Наряду с общей симптоматикой наблюдаются проявления, обусловленные локализацией новообразования. При распаде рака молочной железы образуются крупные язвы. Синдром распада опухоли желудка и кишечника может осложняться расплавлением сосуда с последующим кровотечением или перфорацией стенки органа и развитием перитонита. При распаде рака легкого возможны кровотечения, возникновение пневмоторакса и отхождение обильной гнилостной мокроты.
Диагностика
Диагноз выставляют на основании клинических проявлений, данных лабораторных анализов и инструментальных исследований. Первым настораживающим признаком обычно становится уменьшение количества выделяемой мочи. Для выявления синдрома распада опухоли определяют уровень креатинина, мочевой кислоты, фосфатов и кальция в сыворотке крови. Оценивают состояние печени с учетом результатов печеночных проб. При необходимости назначают ЭКГ, КТ и УЗИ почек.
Лечение синдрома распада опухоли
Незначительные обменные нарушения корректируют в амбулаторных условиях. При появлении признаков развернутого синдрома распада опухоли пациентов госпитализируют в отделение онкологии или реанимации (в зависимости от тяжести состояния и выраженности нарушений). При тошноте и рвоте назначают противорвотные средства. При запорах применяют слабительные и клизмы. При аритмии используют антиаритмические препараты. Для коррекции водно-солевых и кислотно-щелочных нарушений больным с синдромом распада опухоли проводят инфузионную терапию. Осуществляют контроль диуреза и коррекцию питьевого режима. В тяжелых случаях пациентов направляют на гемодиализ. При необходимости назначают анальгетики и противовоспалительные средства.
Прогноз и профилактика
При своевременном начале лечения прогноз при синдроме распада опухоли обычно благоприятный. После коррекции метаболических нарушений наблюдается восстановление функции почек. При отсутствии либо позднем начале терапии синдрома распада опухоли возможен летальный исход вследствие острой почечной недостаточности, остановки сердца или осложнений, обусловленных распадом новообразования (внутреннего кровотечения, перитонита вследствие перфорации стенки полого органа либо тяжелых инфекционных осложнений).
Меры по предотвращению развития синдрома распада опухоли включают в себя обильное питье за 1-2 дня до начала приема химиопрепаратов, а также регулярный контроль уровня креатинина, мочевой кислоты, фосфатов и кальция в сыворотке крови. В первую неделю лечения анализы осуществляют ежедневно. При появлении клинических или лабораторных признаков синдрома распада опухоли лабораторные тесты проводят несколько раз в день.
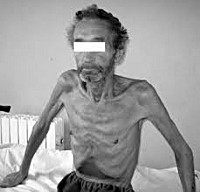
Раковая кахексия – крайнее истощение, возникающее при онкологических заболеваниях. Проявляется резким снижением массы тела, мышечной слабостью, нарушением трудоспособности, расстройствами сна, бледностью и дряблостью кожи, трофическими изменениями волос и ногтей, гипотонией, снижением иммунитета, отеками, психическими расстройствами, аменореей у женщин и утратой либидо у мужчин. Раковая кахексия сопровождается нарушениями всех видов обмена. Нередко становится прямой или косвенной причиной смерти больного. Диагностируется на основании анамнеза, данных внешнего осмотра и объективных исследований. Лечение медикаментозное.
Общие сведения
Раковая кахексия – прогрессирующая потеря массы тела, возникающая при злокачественных новообразованиях и сопровождающаяся нервно-мышечной слабостью, нарушением аппетита, расстройствами белкового, жирового, углеводного и водно-электролитного обмена. Кахексия оказывает выраженное негативное влияние на работу всех органов и систем. Со временем становится причиной несовместимых с жизнью нарушений гомеостаза. По различным данным, является причиной смерти 20-50% пациентов, страдающих онкологическими заболеваниями. Может возникать при опухолях любой локализации, однако чаще диагностируется при поражениях дыхательной и пищеварительной системы. Лечение раковой кахексии осуществляют специалисты в сфере онкологии, диетологии, гастроэнтерологии, пульмонологии и других областей медицины (в зависимости от локализации новообразования).

Патогенез раковой кахексии
Патогенез данного состояния пока недостаточно изучен. Предполагается, что основную роль в развитии раковой кахексии играет интоксикация организма продуктами распада злокачественного новообразования. Некоторые специалисты указывают, что фактором, провоцирующим и/или усугубляющим данный синдром, является вторичная инфекция в зоне распадающейся опухоли. Установлено, что раковая кахексия по ряду признаков отличается от истощения, обусловленного недостаточным поступлением питательных веществ в организм. При кахексии, вызванной голоданием, отмечается уменьшение количества жировой ткани. Уровень обмена веществ снижается, печень атрофируется, распад белка замедляется. При раковой кахексии больной теряет как жировую, так и мышечную ткань. Уровень обмена веществ остается в норме или повышается, печень увеличивается, распад белка становится более интенсивным.
Кроме того, раковая кахексия сопровождается расстройством всех видов обмена. Нарушения углеводного обмена проявляются снижением уровня глюкозы, уменьшением запасов гликогена, усилением глюконеогенеза и снижением чувствительности к инсулину. Нарушения жирового обмена при раковой кахексии заключаются в уменьшении количества жиров, усилении липолиза, снижении активности липопротеидлипазы, повышении уровня триглицеридов и распаде глицерина. О нарушении белкового обмена свидетельствуют отрицательный азотистый баланс и усиление распада белков, в том числе – за счет поперечно-полосатых мышц.
Раковая кахексия протекает на фоне уменьшения количества поступающих питательных веществ и увеличения энергетических затрат. Постоянным признаком раковой кахексии является расстройство аппетита, обусловленное целым рядом факторов, в том числе – болевым синдромом, вкусовыми и обонятельными нарушениями, химиотерапией, радиотерапией и стоматитом, часто развивающимся у онкологических больных. Другими причинами развития раковой кахексии являются депрессивное расстройство, нарушение функций различных органов, тошнота, рвота, рост опухолей желудочно-кишечного тракта, сдавление желудка и кишечника новообразованиями, расположенными в близлежащих органах.
Увеличение энергетических потерь при раковой кахексии обусловлено синдромом нарушенного всасывания и диареей, которые часто возникают на фоне лучевой терапии, химиотерапии, хирургического удаления значительных участков желудочно-кишечного тракта, новообразований поджелудочной железы, карциноидного синдрома, рака щитовидной железы и гастриномы. Из-за значительных потерь белка у больных раковой кахексией возникают анемия, гипертрансферринемия и гипоальбуминемия. Трофические изменения кожи, снижение иммунитета и ограничение подвижности, обусловленное резкой слабостью, становятся причиной развития пролежней и пневмонии.
Классификация раковой кахексии
Выделяют три стадии раковой кахексии:
- Прекахексия. Сопровождается нарушениями аппетита, снижением толерантности к глюкозе и другими признаками истощения при отсутствии значительной потери веса.
- Раковая кахексия. Диагностируется при потере 5 или более процентов массы тела за последние полгода, при потере 2 или более процентов массы тела в сочетании с саркопенией либо при снижении массы тела на 2 или более процентов, если индекс массы тела составляет менее 20 кг/м2.
- Рефрактерная раковая кахексия. Сопровождается выраженным ухудшением состояния пациента, отсутствием реакции на химио- и радиотерапию и неэффективностью лечебных мероприятий по увеличению массы тела.
Симптомы раковой кахексии
Пациенты предъявляют жалобы на резкую слабость, вялость, повышенную утомляемость, лихорадку, запоры или поносы. Нарушается суточный ритм сна-бодрствования: по ночам больные раковой кахексией страдают от бессонницы, в дневное время чувствуют сонливость. У женщин возникает аменорея, у мужчин отмечается отсутствие либидо. Развиваются психические расстройства. Многие пациенты с раковой кахексией страдают от депрессии. Наблюдаются слезливость, раздражительность и эмоциональная лабильность, сменяющиеся апатией и безразличием. При прогрессировании основного заболевания возможны нарушения сознания.
При внешнем осмотре больных раковой кахексией выявляется истощение различной степени выраженности. Иногда (как правило – при опухолях яичников, матки или молочной железы, сопровождающихся гормональными нарушениями) больные имеют нормальную или повышенную массу тела. Кожа пациентов с раковой кахексией сухая, дряблая, сероватого или желтоватого цвета с землистым оттенком. Отмечается углубление морщин, выраженный дефицит подкожной жировой клетчатки, ломкость волос и ногтей, повышенное выпадение волос. Могут наблюдаться безбелковые отеки, асцит или гидроторакс. Определяются гипотония и тахикардия. Развивается стоматит, возможно расшатывание и выпадение зубов. По анализам крови определяется анемия.
Диагностика раковой кахексии
Для оценки уровня анемии, функционального состояния печени и почек проводят общий анализ крови, биохимический анализ крови и общий анализ мочи. При подозрении на септические осложнения назначают анализ мочи на бакпосев. При отсутствии диагноза основного онкологического заболевания пациентов с раковой кахексией направляют на рентгенографию грудной клетки, УЗИ органов брюшной полости, колоноскопию, гастроскопию, гистероскопию, МРТ головного мозга и другие исследования (в зависимости от предполагаемой локализации новообразования). Назначают консультации различных специалистов: терапевта, кардиолога, гастроэнтеролога, невролога, эндокринолога, уролога, гинеколога и т. д.
Лечение раковой кахексии
Лечение симптоматическое. Пациентам с раковой кахексией назначают диету, предусматривающую употребление легкоусвояемых продуктов с большим количеством белков, жиров, микроэлементов и витаминов. Используют препараты для повышения аппетита и противорвотные средства. При необходимости (при выраженном истощении, нарушении глотании, тяжелых инфекционных осложнениях) осуществляют парентеральное введение глюкозы, аминокислотных смесей, витаминов и электролитных растворов. Параллельно проводят терапию основного заболевания.
Прогноз в большинстве случаев неблагоприятный, особенно при рефрактерной раковой кахексии. Состояние пациентов постепенно ухудшается. Расстройства гомеостаза усугубляются из-за нарушения деятельности различных органов и систем и присоединяющихся инфекционных осложнений. При потере 30-50% белка наступает летальный исход. Непосредственной причиной смерти становятся тяжелое общее истощение, пневмонии и обширные пролежни. От раковой кахексии погибает от 20 до 50% больных, страдающих онкологическими заболеваниями.
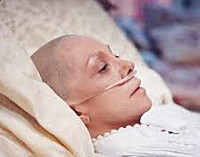
Раковая интоксикация – патологическое состояние, обусловленное распространенным онкологическим процессом и распадом злокачественной опухоли. Возникает на поздних стадиях онкологического заболевания. Может провоцироваться активной противораковой терапией. Проявляется слабостью, утомляемостью, бледностью кожи, сухостью слизистых, тошнотой, рвотой, потерей веса и аппетита, потливостью, гипертермией, костно-суставными болями, нарушениями сна, психическими расстройствами, анемией и снижением иммунитета. Диагноз выставляется на основании анамнеза, клинической симптоматики, результатов анализов и инструментальных исследований. Лечение симптоматическое.
Общие сведения
Раковая интоксикация – комплекс расстройств, возникающих у онкологических больных при отравлении организма продуктами распада злокачественной опухоли. Выявляется преимущественно на терминальных стадиях заболевания, рассматривается как одна из основных причин гибели пациентов. Кроме того, раковая интоксикация часто наблюдается при проведении химиотерапии, является закономерным следствием активного противоракового лечения, вызывающего разрушение опухоли.
Раковая интоксикация может провоцировать нарушения деятельности различных органов и систем, в том числе – почечную и печеночную недостаточность, сепсис и другие тяжелые инфекционные осложнения, что обуславливает важность продуманного подбора дозировок и видов лекарственных препаратов с учетом общего состояния больного, а также наличия тех или иных хронических заболеваний. Лечение осуществляют специалисты в области онкологии.

Причины раковой интоксикации
Одной из отличительных особенностей злокачественной опухоли является ее способность к быстрому неконтролируемому росту. Как правило, темпы роста сосудов, обеспечивающих кровоснабжение новообразования, отстают от скорости роста опухолевой ткани. Злокачественные клетки достаточно устойчивы к гипоксии и могут некоторое время существовать в условиях недостаточного кровоснабжения, однако рано или поздно умирают. Обычно этот процесс наблюдается при опухолях достаточно большого размера. Массовая гибель клеток становится причиной распада новообразования и вызывает раковую интоксикацию.
В организм попадает большое количество продуктов распада, которые провоцируют расстройства всех видов обмена веществ и нарушения деятельности различных органов и систем. Раковая интоксикация становится причиной повышения уровня мочевины. Кристаллы мочевины оседают в почечных канальцах, вызывая развитие почечной недостаточности, которая еще больше усугубляет обменные нарушения. Из-за увеличения количества фосфатов возникает дефицит ионов кальция, следствием которого становятся нарушения работы нервной системы. Повышение уровня кальция негативно влияет на работу сердца. У пациентов с раковой интоксикацией возникают аритмии, в тяжелых случаях возможно прекращение сердечной деятельности. Увеличение количества свободных радикалов стимулирует распад эритроцитов и развитие анемии.
Проявления раковой интоксикации весьма вариабельны. Формирование клинической картины определяется тяжестью состояния пациента, скоростью разрушения новообразования, количеством токсических веществ, попадающих в основной кровоток, особенностями локализации и течения онкологического процесса, масштабом хирургического вмешательства, наличием и объемом кровопотери (как возникшей в ходе операции и послеоперационном периоде, так и связанной с распадом опухоли), присоединением воспалительных осложнений, дозой химиопрепарата и другими факторами.
Симптомы раковой интоксикации
Наиболее постоянными признаками раковой интоксикации являются прогрессирующая слабость и беспричинная утомляемость. Наблюдаются характерные изменения внешнего вида: дефицит массы тела (в тяжелых случаях – вплоть до кахексии), бледный, землистый или желтоватый оттенок кожи, сухость кожи и слизистых оболочек. Возможен цианоз дистальных отделов конечностей. У больных с нарушениями функции печени выявляется иктеричность склер. Пациенты с раковой интоксикацией предъявляют жалобы на усиленное потоотделение. Как правило, потливость более выражена в ночное время.
В ходе опроса врач устанавливает, что резкое снижение веса произошло в течение короткого промежутка времени и сопровождалось нарушениями аппетита: отвращением к еде (особенно – к мясным продуктам), извращением вкуса и т. д. Кроме того, при раковой интоксикации наблюдаются диспепсические расстройства: тошнота, рвота и нарушения стула. Возможны запоры, поносы или чередование запоров и поносов. Отмечается длительное повышение температуры до субфебрильных (при некоторых заболеваниях – до фебрильных) цифр. Возникают боли в костях и суставах.
Больные с раковой интоксикацией могут сообщать о периодических мигренях и приступах головокружения. Расспрос пациентов и их родственников позволяет выявить изменения психического и эмоционального статуса. Могут наблюдаться апатия, раздражительность и эмоциональная лабильность. Раковая интоксикация нередко сопровождается депрессивными расстройствами. Возможны нарушения сна: бессонница, поверхностный сон, трудности при засыпании, ночные и ранние пробуждения. Часто обнаруживаются нарушения сердечного ритма. При раковой интоксикации существует высокая вероятность развития тромбозов и склонность к возникновению инфекционных осложнений. В анализе крови обнаруживаются признаки анемии (обычно – умеренной нормохромной).
Диагностика раковой интоксикации
Диагноз выставляется с учетом анамнеза, жалоб, данных объективного осмотра и результатов дополнительных исследований. Решающую роль в определении причины раковой интоксикации играет выявление основной патологии. При характерной клинической картине и отсутствии установленного диагноза онкологического заболевания пациентам с подозрением на раковую интоксикацию назначают комплексное обследование, которое включает в себя общие анализы крови и мочи, биохимический анализ крови, анализ крови на онкомаркеры, рентгенографию грудной клетки, сцинтиграфию костей скелета, УЗИ брюшной полости, УЗИ малого таза, гинекологический осмотр и другие исследования. План обследования определяется индивидуально.
При уже диагностированном онкологическом заболевании требуется оценка выраженности раковой интоксикации для определения тактики лечения (составления плана химиотерапии, принятия решения об оперативном вмешательстве, подбора симптоматических препаратов и т. д.). Для оценки тяжести раковой интоксикации используются стандартные показатели крови: уровень мочевины, креатинина и С-реактивного белка, реактивный ответ нейтрофилов, лейкоцитарный индекс интоксикации и т. д. Наряду с перечисленными показателями могут потребоваться данные о состоянии различных органов и систем больного с раковой интоксикацией, полученные при проведении ЭКГ, анализов мочи, анализов крови на гормоны и других исследований.
Лечение раковой интоксикации
Лечение симптоматическое, включает в себя мероприятия по детоксикации, устранению или смягчению клинических проявлений и коррекции нарушений деятельности различных органов и систем. Осуществляют энтеросорбцию, гемосорбцию и аппликационную сорбцию. Пациентам выписывают сорбенты для приема внутрь. При тяжелой раковой интоксикации применяют гемодиализ или плазмаферез. При наличии открытых ран в области распада опухоли проводят перевязки с сорбентами местного действия.
При рвоте больным с раковой интоксикацией назначают противорвотные средства (домперидон, метоклопрамид), при запорах – слабительные для перорального приема и ректальные свечи (макрогол, препараты сены, бисакодил, касторовое масло и пр.). При анемии используют препараты железа внутрь и парентерально, применяют эритропоэтин. Выбор медикаментов при раковой интоксикации, сопровождающейся психическими расстройствами, зависит от вида и тяжести расстройств. При эмоциональной лабильности назначают мягкие седативные средства, при нарушениях сна – снотворные, при депрессии – транквилизаторы и антидепрессанты.
Прогноз определяется причинами раковой интоксикации, тяжестью основного процесса, возрастом и общим состоянием больного, наличием и тяжестью сопутствующей соматической патологии. Состояния, возникающие при распаде крупных распространенных опухолей в запущенных стадиях заболевания, являются прогностически неблагоприятными. Больные с раковой интоксикацией погибают от кровотечений, нарушений деятельности органов, пораженных первичной опухолью или гематогенными метастазами, а также от истощения, инфекционных осложнений, почечной недостаточности, тромбозов, нарушений сердечной деятельности или полиорганной недостаточности, обусловленной обменными расстройствами и ослаблением организма. При раковой интоксикации, возникшей в процессе химиотерапии, прогноз может быть благоприятным. При приеме химиопрепаратов это – временное состояние, являющееся частью лечебного процесса.
Распад опухоли — это закономерное следствие слишком активного роста ракового узла по периферии или осложнение избыточно высокой реакции распространённого злокачественного процесса на химиотерапию.
Не каждому пациенту доводится столкнуться с тяжелой проблемой распада ракового процесса, но при любой интенсивности клинических проявлений инициируемое распадом злокачественной опухоли состояние непосредственно угрожает жизни и радикально меняет терапевтическую стратегию.

Распад опухоли: что это такое?
Распад — это разрушение злокачественного новообразования, казалось бы, что именно к распаду необходимо стремиться в процессе противоопухолевой терапии. В действительности при химиотерапии происходит уничтожение раковых клеток, только убийство органичное и не массовое, а единичных клеток и небольших клеточных колоний — без гибели большого массива ткани с выбросами в кровь из распадающихся клеток токсичного содержимого.
Под действием химиотерапии клетки рака приходят не к распаду, а к процессу апоптоза — программной смерти. Останки раковых клеток активно утилизируются фагоцитами и уносятся прочь от материнского образования, а на месте погибших возникает нормальная рубцовая ткань, очень часто визуально не определяющаяся.
Регрессия злокачественного новообразования в форме апоптоза происходит медленно, если наблюдать за новообразованием с перерывами в несколько дней, то заметно, как по периферии раковый узел замещается совершенно нормальной тканью и сжимается в размере.
При распаде раковый конгломерат не замещается здоровыми клетками соединительной ткани, мертвые клеточные пласты формируются в очаг некроза, отграничивающийся от остальной раковой опухоли мощным воспалительным валом. Внутри злокачественного новообразования некроз не способен организоваться и заместиться рубцом, он только увеличивается, захватывая новые участки ракового узла, походя разрушая опухолевую сосудистую сеть. Из мертвого очага в кровь поступают продукты клеточного гниения, вызывая интоксикацию.
Массированный выброс клеточного субстрата становится причиной тяжелейшей интоксикации, способной привести к смерти.
Причины распада злокачественной опухоли
Инициируют распад ракового образования всего только две причины: сама жизнедеятельность клеток злокачественной опухоли и химиотерапия.
Первая причина спонтанного — самопроизвольного распада характерна для солидных новообразований, то есть рака, сарком, злокачественных опухолей головного мозга и меланомы. Вторая причина распада типична для онкогематологических заболеваний — лейкозов и лимфом, при онкологических процессах встречается чрезвычайно редко.

Второй вариант распада, типичный для онкогематологических заболеваний, можно констатировать по клиническим симптомам тяжелейшей интоксикации с осложнениями — тумор-лизис-синдрому (СОЛ) и биохимическим анализам крови, где резко повышена концентрация мочевой кислоты, калия и фосфора, но существенно снижен кальций. Конкретная побудительная причина для развития СОЛ — обширное злокачественное поражение с очень высокой чувствительностью к химиотерапии.
При онкологических процессах — раках, саркомах, меланоме реакция на цитостатики преимущественно умеренная и не столь стремительная, поэтому СОЛ принципиально возможен только в исключительных случаях мелкоклеточного, недифференцированного или анаплазированного злокачественного процесса.
Симптомы распада злокачественной опухоли
Клиническим итогом спонтанного распада раковой опухоли становится хроническая интоксикация, нередко сочетающаяся с симптомами генерализованного воспаления вследствие образования гнойного очага. Симптомы разнообразны, но у большинства отмечается прогрессивно нарастающая слабость, повышение температуры от субфебрильной до лихорадки, сердцебиение и даже аритмии, изменение сознания — оглушенность, нарушение аппетита и быстрая потеря веса.
Локальные проявления спонтанного разрушения раковой опухоли определяются её локализацией:
- рак молочной железы, меланома и карцинома кожи, опухоли ротовой полости — гнойная, обильно секретирующая открытая язва с грубыми подрытыми краями, часто источающая гнилостный запах;
- распадающаяся карцинома легкого — при прободении некротической полости в крупный бронх возникает приступообразный кашель с гнойной мокротой, нередко с прожилками крови, иногда случается обильное легочное кровотечение;
- разрушение новообразования органов желудочно-кишечного тракта — развитие локального перитонита при прободении ракового конгломерата в брюшную полость, кровотечение с чёрным стулом и рвотой кофейной гущей;
- распадающаяся карцинома матки — интенсивные боли внизу живота, нарушение мочеиспускания и дефекации при образование гнойных свищей.
Синдром опухолевого лизиса при лейкозах и лимфомах потенциально смертельное состояние, приводящее:
- в первую, очередь к осаждению кристаллов мочевой кислоты в почечных канальцах с выключением функции и острой почечной недостаточностью;
- дополнительно повреждает почки быстрое закисление крови — лактатацидоз;
- снижение уровня кальция и повышение фосфатов инициирует судорожный синдром, дополняемый неврологическими проявлениями вследствие выброса цитокинов;
- повышения калия негативно отражается на сердечной деятельности;
- выброс биологически-активных веществ из клеток приводит к повышению проницаемости мелких кровеносных сосудов, что снижает уровень белков и натрия крови, уменьшает объем циркулирующей плазмы, клинические проявляется падением давления и усугублением поражения почек;
- обширные и глубокие нарушения метаболизма во всех системах органов с исходом в полиорганную недостаточность.
Лечение распада опухоли
Формально при распадающейся опухоли невозможна радикальная операция, зачастую заболевание считается неоперабельным, но химиотерапия и облучение исключаются из программы, потому что способны усугубить некроз. Отчаянное положение пациента и вероятность массированного кровотечения из изъеденного раком крупного сосуда оправдывает выполнение паллиативной операции, основная цель которой — удаление очага хронического воспаления и интоксикации.
Синдром лизиса опухоли лечится многочасовыми капельными вливаниями при усиленном диурезе — выведении мочи, связыванием мочевой кислоты специальными лекарствами. Одновременно поддерживается работа сердечно-сосудистой системы, купируется интоксикация и воспаление. При развитии острой почечной недостаточности проводится гемодиализ.
Синдром лизиса опухоли сложно лечить, но можно предотвратить или хотя бы уменьшить его проявления. Профилактика начинается за несколько дней до курса химиотерапии и продолжается не менее трёх суток после завершения цикла. Кроме специальных препаратов, выводящих мочевую кислоту, назначаются продолжительные капельницы, вводятся недостающие микроэлементы, а избыточные выводятся или связываются другими лекарствами.
Профилактика лизиса опухоли стала стандартом лечения онкогематологических больных, чего нельзя сказать об онкологических пациентах с распадающимися злокачественными процессами, которым очень сложно найти хирурга, готового выполнить паллиативную операцию. Во вмешательстве по санитарным показаниям отказывают из-за сложности выхаживания тяжелого больного после обширного хирургического вмешательства. В нашей клинике никому не отказывают в помощи.
Читайте также:

