Что такое uti инфекция
Обновлено: 19.04.2024
Категории МКБ: Интерстициальный цистит (хронический) (N30.1), Инфекция мочевыводящих путей без установленной локализации (N39.0), Острый тубулоинтерстициальный нефрит (N10), Острый цистит (N30.0), Пионефроз (N13.6), Хронический тубулоинтерстициальный нефрит (N11)
Общая информация
Краткое описание
Союз педиатров России
Клинические рекомендации: Инфекция мочевыводящих путей у детей
N10/ N11/ N13.6/ N30.0/ N30.1/ N39.0
Бактериурия – присутствие бактерий в моче (более 105 колоний-образующих единиц (КОЕ) в 1 мл мочи), выделенной из мочевого пузыря.
Асимптоматической бактериурией называют бактериурию, обнаруженную при диспансерном или целенаправленном обследовании у ребенка без каких- либо жалоб и клинических симптомов заболевания мочевой системы.
Острый пиелонефрит – воспалительное заболевание почечной паренхимы и лоханки, возникшее вследствие бактериальной инфекции.
Хронический пиелонефрит – повреждение почек, проявляющееся фиброзом и деформацией чашечно-лоханочной системы, в результате повторных атак инфекции МВП. Как правило, возникает на фоне анатомических аномалий мочевыводящего тракта или обструкции.
Рефлюкс-нефропатия - фокальный или диффузный склероз почечной паренхимы, первопричиной которого является пузырно-мочеточниковый рефлюкс, приводящий к внутрипочечному рефлюксу, повторным атакам пиелонефрита и склерозированию почечной ткани.
Уросепсис - генерализованное неспецифическое инфекционное заболевание, развивающееся в результате проникновения из органов мочевой системы в кровеносное русло различных микроорганизмов и их токсинов.
Классификация
Этиология и патогенез
Среди возбудителей инфекций мочевыводящих путей у детей преобладает грам-отрицательная флора, при этом около 90% приходится на инфицирование бактериями Escherichia coli. Грамположительные микроорганизмы представлены, в основном, энтерококками и стафилококками (5-7%). Кроме того, выделяют внутрибольничные инфекции штаммами Klebsiella, Serratia и Pseudomonas spp. У новорождённых детей относительно частой причиной инфекций мочевыводящих путей являются стрептококки групп А и В. В последнее время отмечен рост выявления Staphylococcus saprophyticus, хотя его роль остается спорной.
В настоящее время более половины штаммов E. coli при ИМВП у детей приобрели устойчивость к амоксициллину, однако сохраняют умеренную чувствительность к амоксициллину/клавуланату.
Среди многочисленных факторов, обуславливающих развитие инфекции МВП, приоритетное значение имеют биологические свойства микроорганизмов, колонизирующих почечную ткань, и нарушения уродинамики (пузырно-мочеточниковый рефлюкс, обструктивная уропатия, нейрогенная дисфункция мочевого пузыря).
Наиболее частым путем распространения инфекции считается восходящий. Резервуаром уропатогенных бактерий являются прямая кишка, промежность, нижние отделы мочевыводящих путей.
Анатомические особенности женских мочевыводящих путей (короткая широкая уретра, близость аноректальной области) обуславливают большую частоту встречаемости и рецидивирования ИМВП у девочек и девушек.
При восходящем пути распространения инфекции МВП после преодоления бактериями везикоуретерального барьера происходит их быстрое размножение с выделением эндотоксинов. В ответ происходит активация местного иммунитета макроорганизма: активация макрофагов, лимфоцитов, клеток эндотелия, приводящая к выработке воспалительных цитокинов (ИЛ 1, ИЛ 2, ИЛ 6, фактора некроза опухоли), лизосомальных ферментов, медиаторов воспаления; происходит активация перекисного окисления липидов, что приводит к повреждению почечной ткани, в первую очередь, канальцев.
Гематогенный путь развития инфекции мочевых путей встречается редко, характерен преимущественно для периода новорожденности при развитии септицемии и у детей грудного возраста, особенно при наличии иммунных дефектов. Этот путь также встречается при инфицировании Actinomyces species, Brucella spp., Mycobacterium tuberculosis.
Эпидемиология
Распространенность ИМВП в детском возрасте составляет около 18 случаев на 1000 детского населения. Частота развития ИМВП зависит от возраста и пола, при этом чаще страдают дети первого года жизни. У детей грудного и раннего возраста ИМВП – самая частая тяжелая бактериальная инфекция, она наблюдаются у 10-15% госпитализируемых лихорадящих больных этого возраста. До 3-х месячного возраста ИМВП чаще встречается у мальчиков, в более старшем возрасте – у девочек. В младшем школьном возрасте: 7.8% у девочек и 1.6% у мальчиков. С возрастом после первого перенесенного эпизода ИМВП возрастает относительный риск развития рецидива.

Ученые из Школы медицины Вашингтонского университета, заявили, что некоторые условно-патогенные бактерии, обнаруженные во влагалище, провоцируют рецидивы инфекций мочевых путей (ИМП), несмотря на лечение. Вот почему половые инфекции часто дают осложнения на мочевой пузырь и почки. Например, очень опасна Гарднерелла.

Результаты исследования, опубликованные в PLOS Pathogens, объясняют, почему сексуальная активность тесно связана с ИМП. Когда бактерия Gardnerella vaginalis из влагалища попадает в мочевой пузырь, она активизирует дремлющую кишечную палочку, сохранившуюся от предыдущей инфекции. Кишечная палочка снова начать размножаться, вызывая рецидив. Исследование Gardnerella может также способствовать более серьезным инфекциям почек.
Как связаны бактериальный вагиноз и цистит

Согласно данным нового исследования Вашингтонского университета (Сент-Луис), рецидивирующие ИМП грозят всем женщинам, в составе влагалищной флоры которых присутствует гарднерелла. На изображении клетка мочевого пузыря (синяя), подвергнувшаяся воздействию G. vaginalis. Под влиянием гарднереллы она умирает и отделяется от соседних клеток, обнаруживая незрелые клетки (фиолетовые).
Выводы исследования также могут объяснить, почему некоторые женщины испытывают рецидивирующие ИМП после полового контакта: в этот момент гарднерелла может легко попасть в мочевые пути.
Как проходило исследование: опыты и результаты
В рамках исследования, ученые заразили мочевые пузыри у мышей-самцов кишечной палочкой, инициируя мочевую инфекцию, а затем позволили им выздороветь. Через месяц после заражения в моче животных не было обнаружено бактерий E.coli. Однако предыдущие исследования показали, что небольшая популяция кишечной палочки может сохраняться в мочевом пузыре на уровнях, не обнаруживаемых в моче.
Затем исследователи вводили в мочевые пузыри мышей либо лактобактерии Lactobacillus crispatus — полезные бактерии, населяющие влагалище и защищающие женскую половую флору и G. vaginalis, вызывающую бактериальный вагиноз. Оба вида вагинальных бактерий удалялись из мочевого пузыря в течение 12 часов, но этого короткого пребывания в органе было достаточно, чтобы E. coli снова появлялась в моче более половины мышей, подвергшихся воздействию G. vaginalis. Это указывает на рецидив инфекции. У мышей, получавших нормальные вагинальные бактерии или стерильную соленую воду, было в пять раз меньше шансов на повторение цистита.
Более того, у некоторых мышей с гарднереллой бактерии выходили из мочевого пузыря и поднимались вверх по мочевому тракту в почки, вызывая инфекцию уже там.
Все мыши, с кишечной палочкой или гарднереллой в мочевых путях, показали некоторую степень повреждения почек. Но мыши, имеющие оба вида бактерий, в 6% случаев проявляли тяжелое повреждение почек. Они имели высокий уровень E. coli в почках и признаки того, что E. coli переместилась из почки в кровоток, что является смертельной формой ИМВП.
Ранее версия о том, что гарднерелла может влиять на почки не рассматривалась. Теперь же понятно, что бактериальный вагиноз гораздо опаснее, чем считалось. Поэтому ученые рекомендуют гинекологам и урологам, к которым приходят пациентки с циститом и другими признаками инфекций мочеполовых путей, обследовать этих женщин на наличие гарднереллы. При этом обращается внимание на то, что вылечить бактериальный вагиноз без подбора специальных антибиотиков не получится — бактерия слишком коварна и чрезвычайно устойчива к многим лекарствам.

Скрытые инфекции — это заболевания, передающиеся половым путём, протекающие бессимптомно на протяжении длительного времени. Они медленно разрушают организм, в итоге став причиной серьёзных проблем со здоровьем. Анализы на скрытые инфекции — единственный метод выявления таких состояний.
Прием гинеколога, уролога — 1000 руб. Консультация по результатам УЗИ, анализов (по желанию) — 500 руб.
Причины появления скрытых инфекций у мужчин и женщин
Основной способ заражения ИППП — незащищённый половой контакт, хотя некоторые заболевания (например, вирус папилломы человека) могут передаться и при использовании презерватива.

Важно понимать, что заражение происходит не через семенную жидкость, а посредством контакта со слизистыми. Это значит, что даже если половой акт был прерван, и семяизвержение произошло не во влагалище женщины, обмен микрофлорой все-равно состоялся. Состав флоры у каждого человека индивидуален и далеко не всегда безобиден.
Заражённый партнёр может и не знать о наличии у себя ЗППП. Мало того, что болезнь долго не дает симптомов, ее тяжело выявить и с помощью обычных анализов типа мазка на флору или бактериальный посев. Также человек может быть просто носителем: его иммунитет не дает размножаться патогенному микроорганизму, но и не убивает его. При попадании на слизистые партнера с ослабленным местным иммунитетом, бактерия или вирус моментально образуют колонии.
Какие инфекции относятся к скрытым
Под скрытой инфекцией понимается возбудитель, поселившийся на слизистой поверхности органа (уретре, шейке матки, кишечнике) и паразитирующий за его счёт. Он не может самостоятельно продуцировать белки, необходимые для поддержания жизнедеятельности, поэтому некоторое время ведёт себя тихо и не проявляет симптомов. В 60% случаев носитель инфекции узнаёт о том, что болен, только когда происходит резкое ухудшение самочувствия, и симптомы проявляются бурно и активно.
К скрытым инфекциям относятся:
-
: инкубационный период 4 недели. Путь передачи — половой. Ребёнок заражается от матери при родах. : причина №1 возникновения воспалительных процессов в мочеполовой системе. /уреплазмоз : половой путь и инфекция передаётся от матери ребёнку.
- Токсоплазмоз: половой путь и инфекция передаётся от матери ребёнку. : в острой форме мешает зачатию, способствует проникновению других инфекций.
- ВПЧ : является причиной рака шейки матки в 99,9% случаев. : часто развивается во время беременности по причине ослабления иммунитета, вызывает патологические изменения в строении плода. (бактериальный вагиноз): убивает молочнокислые полезные бактерии на поверхности влагалища и создают питательную среду для развития патогенной микрофлоры.
- Пиелонефрит: воспаление почек.
- Бактериурия: наличие бактерий в моче, которых быть не должно, указывает на заболевания мочеполовой системы. (неспособные оказать влияние на взрослого, но угрожающие жизни и здоровью плода).
В настоящее время существует 31 возбудитель скрытой инфекции. Каждый из них по-своему опасен.
Как развиваются скрытые инфекции
Проявления у женщин
Проявления у мужчин
Поражается поверхность влагалища и шейки матки, образуется эрозия
Поражается мочеиспускательный канал, головка пениса
Инфекция переходит на придатки и матку
Инфекция переходит на предстательную железу и почки
Инфекция охватывает весь организм, пациент жалуется на воспалительные процессы в слизистых оболочках — стоматиты, конъюнктивиты, язву желудка
Скрытые инфекции опасны тем, что приводят к хроническому воспалению. Например, у женщин эндометрий уже не может удерживать плодное яйцо, что приводит к выкидышу или воспалённые яичники не продуцируют яйцеклеток. А у мужчин в сперме содержится большое число неподвижных или ослабленных сперматозоидов. Именно скрытые инфекции являются причиной бесплодия у многих пар.
Группа риска
Человек может всю жизнь быть носителем инфекции, но не знать об этом. Лавинообразное распространение возбудителей провоцируют процессы, происходящие в организме. К ним относятся:
- изменения гормонального фона;
- ослабление иммунитета;
- беременность.
Часто ИППП проявляют себя параллельно с другой болезнью (гриппом, ангиной, воспалением лёгких). Особую опасность они представляют для беременных женщин. Их иммунитет ослаблен присутствием в организме новой жизни, поэтому возбудитель действует в организме беспрепятственно. Наибольшую опасность представляют TORCH-инфекции, получившие аббревиатуру от первых букв латинского написания болезней.
К ним относятся:
- T — toxoplasmosis (токсоплазмоз). Особенно опасно проникновение инфекции в первом триместре беременности. Женщине в таком случае предлагают сделать аборт . На последнем триместре заражение не так опасно.
- O — other, это общие заболевания, передающиеся бытовым и контактным путём (гепатит, микоплазмоз, хламидиоз, уреплазмоз, ветрянка, гонорея). . Если мама малыша переболела краснухой в детстве, у неё уже выработаны антитела. В противном случае есть большая угроза рождения ребёнка с полной глухотой, слепотой и параличом.
- C — citomegalia (цитомегаловирус). Инфекция убивает плод, а также повреждает его головной и спинной мозг. Малыш рождается с глубокой инвалидностью.
- H — herpes (генитальный герпес ). Малыш рождается слепым, глухим, с ДЦП, эпилепсией, если не произойдёт выкидыш на ранних сроках.
Все вышеперечисленные заболевания убивают плод либо приводят к врождённым патологиям и уродствам. Проникновение в организм на 2-12 неделе приводит к замиранию развития плода , 12-26 неделе — к аномальному развитию органов малыша, от 26 недели — к поражению ЦНС плода.
Что показывают анализы на скрытые TORCH-инфекции
При обнаружении TORCH-инфекции у женщины, ожидающей малыша, ей предлагают сделать аборт, потому что высока вероятность выкидыша или рождения ребёнка с серьёзными пороками развития. Вот почему анализы на TORCH-инфекции сдают на стадии планирования беременности за 2-3 месяца до наступления зачатия. В случае положительного результата будущая мама позаботится о своём здоровье и устранит проблемы, у неё хватит времени вылечиться и забеременеть будучи здоровой. TORCH-анализы — обязательная процедура при постановке в женской консультации на учёт.
TORCH-диагностика — это определение иммуноглобулинов (антител), способных противостоять ряду инфекций.
- IgM-антитела вырабатываются при проникновении инородных микроорганизмов первыми, и достигают пика концентрации в конце 3-го месяца инфицирования. Говорят об острой форме заболевания. После 4-го месяца они не определяются. Чтобы определить, как долго женщина заражена, у неё определяют IgG-антитела.
- IgG-антитела вырабатываются на повторное проникновение инфекции или на обострение хронической фазы. Эти иммуноглобулины защищают плод от болезней. Их наличие говорит о длительном нахождении инфекции в организме.
Женщина сдаёт 8 тестов на определение количества и качества антител IgM и IgG. При этом Ig — это международное обозначение чужеродного тела (инфекции).
Инфекции мочевыводящих путей — частое заболевание в повседневной урологической практике. Значительный прогресс в лечении инфекций мочевыводящих путей наблюдается за последние двадцать лет. В статье затрагиваются такие важные проблемы, как этиология, патогенез и лечение инфекций мочевыводящих путей у взрослых.
Инфекции мочевыводящих путей (ИМП) представляют собой серьезную проблему из-за их распространенности и связанной с ними заболеваемости. По статистике на них приходится примерно 20% всех внебольничных и примерно 50% нозокомиальных инфекций. Достижения последних десятилетий способствовали лучшему пониманию патогенеза инфекций мочевыводящих путей и выяснили важную роль как бактериальных, так и зависимых от пациентов факторов в развитии или предотвращении инфекции.
Динамичное развитие антибактериальной терапии значительно облегчило правильное лечение ИМП, но неправильное и широкое злоупотребление антибактериальными препаратами привело к увеличению лекарственной устойчивости микроорганизмов.
Эпидемиология ИМП
Инфекции мочевыводящих путей — одно из самых распространенных инфекционных заболеваний человека.
Частота возникновения ИМП зависит от пола и возраста обследуемых, а также от конкретных характеристик исследуемой популяции.
Риск ИМП возрастает, когда существует препятствие для оттока мочи или когда обстоятельства способствуют колонизации и росту бактерий. К физиологическим факторам, предрасполагающим к ИМП, относятся беременность, пожилой возраст и такие заболевания, как диабет и мочекаменная болезнь.
Этиология и патогенез ИМП
Наиболее частыми факторами, вызывающими ИМП, являются бактерии, реже вирусы, грибки или паразиты. Распространенность определенных типов бактерий, выделенных из мочи пациентов, во многом зависит от изучаемой популяции. Совершенно иначе обстоит дело у пациентов, находящихся на амбулаторном лечении, чем в больницах.
В физиологических условиях мочевыводящие пути стерильны, за исключением конца уретры. Первый эпизод ИМП в амбулаторных условиях в 80% случаев вызывается Escherichia coli, в 10-15% — Staphylococcus saprophyticus (кроме группы молодых сексуально активных женщин, в которой он составляет около 30%), другими грамотрицательными бактериями (Proteus mirabilis, Klebsiella spp.) или грамположительными (стафилококки, стрептококки, энтерококки). 70% рецидивов внебольничных инфекций вызваны к ишечной палочкой . Также наиболее частые нозокомиальные инфекции вызываются кишечной палочкой (около 50%), Enterobacter spp., Pseudomonas spp., Serratia marcescens, а также стафилококками, энтерококками и грибками.

Кишечная палочка
У 95% пациентов ИМП является результатом заражения одним штаммом бактерий. Заражение несколькими штаммами наблюдается у 5% пациентов, преимущественно у катетеризованных больных, с ослабленным иммунитетом, нейрогенными нарушениями мочевого пузыря или дефектами мочевыделительной системы.
Инфекция мочевыделительной системы может происходить восходящим путем (урогенные инфекции), кровотоком (гематогенные инфекции — очень редко вызваны, главным образом, золотистым стафилококком), лимфатическим путем или непрерывно (при наличии урогенитального или урогенитального свища).
ИМП почти всегда вызывается попаданием бактерий через уретру. В физиологических условиях бактерии часто попадают в мочевыводящие пути, однако из-за защитных механизмов организма развитие ИМП происходит редко.
Наиболее важные естественные механизмы защиты от ИМП:
- длина уретры у мужчин;
- перистальтика мочеточника, нормальная функция пузырно-мочеточниковых клапанов;
- подкисление и концентрация мочи;
- правильная бактериальная флора влагалища и области вокруг уретры;
- антибактериальные свойства секрета простаты;
- механизмы предотвращения бактериальной адгезии в мочевыводящих путях: механическое воздействие струи мочи, мукополисахариды стенки мочевого пузыря, антитела IgG и IgA.
Инфекции мочевыводящих путей редко возникают у здоровых людей с нормальной анатомической структурой и физиологической функцией мочевыводящих путей. В случае затрудненного оттока мочи или ослабления организма из-за системных заболеваний (диабет, подагра , опухолевый процесс) мы часто сталкиваемся с воспалительными изменениями мочевыделительной системы.

Подагра
К наиболее частым факторам, способствующим развитию инфекции мочевыводящих путей, относятся:
- 1-я беременность,
- старый возраст,
- препятствие оттоку мочи — мочекаменная болезнь, аденома простаты,
- атрогенные факторы — инструментарий мочевыводящих путей (цистоскопия, катетеризация мочевого пузыря, восходящая пиелография),
- врожденные пороки мочевыводящих путей — двойная чашечно-тазовая система, ретроградный пузырно-мочеточниковый отток,
- диабет, подагра,
- неврогенный мочевой пузырь,
- конечная стадия почечной недостаточности (диализ),
- половые отношения,
- длительная иммобилизация в постели.
Моча в мочевыводящих путях здорового человека стерильна. Наличие в нем бактерий свидетельствует об инфицировании.
Основным симптомом, позволяющим диагностировать ИМП, является так называемая значительная бактериурия, когда количество бактерий в 1 мл свежей, собранной в асептических условиях мочи превышает 100000.
Возникновение значительной бактериурии по полу и возрасту представлено ниже:
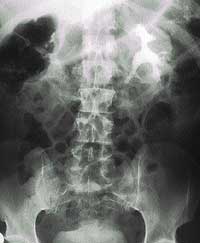
Инфекции мочевыводящих путей (ИМП) в большинстве стран мира — одна из наиболее актуальных проблем. Так, в США ИМП становятся причиной обращения к врачу 7 миллионов пациентов в год, а для миллиона пациентов являются причиной госпитализации [9]. Особую категорию ИМП составляют осложненные инфекции. Согласно современной классификации, к осложненным инфекциям мочевыводящих путей (ОИМП) относятся заболевания, объединенные наличием функциональных или анатомических аномалий верхних или нижних мочевых путей или протекающие на фоне заболеваний, снижающих общий иммунный статус.
Необходимо отметить, что группа ОИМП представлена крайне разнородными заболеваниями: от тяжелого пиелонефрита с явлениями обструкции и угрозой развития уросепсиса до катетер-ассоциированных инфекций МВП, которые могут исчезнуть самостоятельно после извлечения катетера.
Причины возникновения осложненных ИМП
Наиболее часто встречающиеся причины возникновения ОИМП приведены в табл. 1 [5].
Нарушения уродинамики вследствие обструкции МВП
На основании данных можно сделать вывод, что в большинстве случаев причиной осложненного течения ИМП становятся нарушения уродинамики по обструктивному типу при камнях различной локализации, стриктурах мочеточника и лоханочно-мочеточникового сегмента, инфравезикальной обструкции. Восстановление нормальной уродинамики является краеугольным камнем лечения любой мочевой инфекции. В тех случаях, когда причина возникновения обструкции не может быть ликвидирована немедленно, следует прибегать к дренированию верхних мочевых путей нефростомическим дренажем, а в случае инфравезикальной обструкции — к дренированию мочевого пузыря цистостомическим дренажем. Обе операции предпочтительно выполнять чрезкожно под ультразвуковым контролем.
Инородные тела МВП
Часто причиной осложнений при ИМП становятся инородные тела в мочевыводящих путях: конкременты почек и мочевого пузыря, различные дренажи. Лечение подобных инфекций длительное и подчас малоэффективное. Причина кроется в образовании на поверхности инородных тел микробной пленки, которая состоит из связанных между собой и с какой-либо поверхностью микроорганизмов, находящихся в различных фазах роста, их внеклеточных продуктов, соматических клеток, органического и неорганического материала [1].
Биопленка может быть ассоциирована не только с поверхностью дренажных трубок и конкрементов, но и с рубцово-измененными и некротизированными тканями, присутствующими в просвете мочевыводящих путей после предшествующих оперативных вмешательств. Так или иначе, но большинство осложняющих факторов благоприятствуют образованию биопленок. Бактерии, формирующие биопленку, значительно отличаются от планктонных свободно плавающих микробных клеток, не говоря уже о культуре микроорганизмов, использующейся для лабораторных тестов. Доза антибиотика, бактерицидная в отношении возбудителя в лабораторных условиях, зачастую не оказывает на биопленку никакого воздействия; кроме того, бактерии в биопленке более устойчивы к факторам окружающей среды. Вышесказанное свидетельствует о том, что именно биопленка в итоге является основной причиной возникновения трудностей, которые часто сопровождают лечение осложненной хронической персистирующей инфекции мочевыводящих путей.
Нейрогенные нарушения мочеиспускания
К заболеваниям, нарушающим нормальную уродинамику и осложняющим течение ИМП, относятся и нейрогенные нарушения мочеиспускания. Рассчитывать на успех лечения ИМП можно только после коррекции нейрогенных нарушений и восстановления нормальной уродинамики.
Сопутствующие заболевания
Особую группу составляют осложняющие факторы, связанные с наличием сопутствующих тяжелых заболеваний. Список этих заболеваний является предметом обсуждения, однако некоторые нозологии могут быть внесены в него без колебаний. Это заболевания, обусловливающие общее снижение иммунологической реактивности организма: сахарный диабет, иммунодефицитные состояния. К фоновым заболеваниям, значительно осложняющим течение ИМП, относятся также серповидно-клеточная анемия, почечная и печеночно-почечная недостаточность.
Катетер-ассоциированные ИМП
Факторы риска развития ОИМП
Помимо причин, обусловливающих возникновение ОИМП, существует ряд факторов риска развития этого состояния (табл. 3) [5].
Серьезную проблему для выбора эффективной терапии представляет сочетание ОИМП с хроническим простатитом. Хронический простатит — одно из самых трудных для диагностики и лечения заболеваний в урологии. Любое повышение внутриуретрального давления приводит к рефлюксу мочи и содержащихся в ней микроорганизмов в протоки периферической зоны в обход протоков центральной зоны предстательной железы, соустье которых с уретрой по своей природе почти клапанное. При несостоятельности внутреннего сфинктера нейрогенного происхождения или резекции шейки мочевого пузыря ткань простаты подвергается постоянному риску инфицирования и реинфицирования. Хронический бактериальный простатит характеризуется персистированием преимущественно грамотрицательных бактерий в секрете простаты и рецидивирующими ИМП [1, 3].
Этиология ОИМП
В табл. 2 приведены возбудители, наиболее часто являющиеся причиной возникновения ИМП [7]. Обращает на себя внимание, что на втором и третьем местах после наиболее распространенного возбудителя ИМП — кишечной палочки — при осложненных ИМП находятся Enterococcus spp. и Pseudomonas spp., а при катетер-ассоциированных инфекциях — дрожжевые грибки, отсутствующие при неосложненных ИМП.
Микробиологические особенности осложненных ИМП учитываются при выборе препарата для их лечения.
Лечение ОИМП
Лечение инфекции мочевых путей подразумевает проведение эффективной антибактериальной терапии при условии восстановления нормальной уродинамики и направлено на профилактику уросепсиса и возникновения рецидивов. Исключения составляют катетер-ассоциированные инфекции, в большинстве случаев исчезающие после удаления катетера. Открытым остается вопрос о необходимости антибактериальной терапии у пациентов с асимптоматической бактериурией. Большинство урологов считают, что лечение в подобных ситуациях не показано.
Дополнительной проблемой, значительно усложняющей лечение ОИМП, является высокая устойчивость микроорганизмов к большинству антибактериальных препаратов, длительно применяющихся в урологической практике. Госпитализация, неадекватные по длительности курсы лечения и некорректное назначение лекарственных препаратов приводят зачастую к возникновению антибиотико-устойчивых штаммов.
В нашей клинике в случае тяжелых инфекций мочевыводящих путей, а также в послеоперационном периоде после масштабных оперативных вмешательств мы в последнее время применяем новый антимикробный препарат группы фторхинолонов — L-изомер офлоксацина — левофлоксацин (таваник). Подобный выбор при назначении антибактериальной терапии объясняется доказанной способностью препаратов этой группы лучше проникать в биопленку [2, 9].
Поскольку на левофлоксацин приходится практически вся противомикробная активность в рацемической смеси изомеров, его активность in vitro в два раза превышает активность офлоксацина. Биодоступность препарата равняется 99 %, а особенности его фармакокинетики таковы, что 87 % препарата экскретируется с мочой в неизмененном виде [4]. Несмотря на наличие перекрестной устойчивости между левофлоксацином и другими фторхинолонами, некоторые микроорганизмы, устойчивые к хинолонам, могут проявлять чувствительность к левофлоксацину.
В исследованиях in vitro левофлоксацин доказал свою эффективность в отношении E.coli, Enterobacter, Klebsiella, Proteus Mirabilis, Pseudomonas aurugenosa, являющихся наиболее частыми возбудителями осложненной и неосложеннной форм урогенитальной инфекции (табл. 2).
Курс лечения таваником в дозе 250 мг однократно в течение суток на протяжении 10 дней проведен нами у 20 больных. Согласно полученным данным, эффективность и безопасность лечения были признаны хорошими и очень хорошими у 95% пациентов. Сходные результаты приводят в своих работах G. Richard, C. DeAbate et al., применявшие препарат по аналогичной схеме и добившиеся клинического эффекта у 98,1% пациентов [8]. Столь высокие показатели объясняются непродолжительностью применения левофлоксацина в урологической практике, чем и обусловлено отсутствие устойчивых к его действию штаммов микроорганизмов. Надо отметить, что устойчивость к препаратам этой фармакологической группы, связанная со спонтанными мутациями in vitro, встречается крайне редко [9].
Наряду с фторхинолонами в лечении ИМП широко применяются цефалоспорины II поколения (цефуроксим) и особенно III поколения (цефотаксим, цефтазидим и др.), а также карбапенемные антибиотики (имипенем/циластатин, меропенем).
При осложненных инфекциях МВП иногда назначают полусинтетические пенициллины (ампициллин, пиперациллин) и их комбинации с ингибиторами b-лактамаз (ампициллин/сульбактам, пиперациллин/тазобактам), ко-тримоксазол, аминогликозиды (обычно в комбинации с b-лактамами). Однако эффективность этих препаратов при ОИМП прогнозировать достаточно сложно из-за существенных различий в чувствительности возбудителей в зависимости от региона, стационара и источника развития инфекции (внебольничные или госпитальные). Таким образом, при назначении указанных препаратов в ходе терапии ОИМП следует опираться на данные бактериологического исследования мочи и учитывать чувствительность выделенных микроорганизмов.
Препараты нитрофуранового ряда — нефторированные хинолоны (налидиксовая кислота), оксихинолины (5-НОК) — не должны применяться для терапии ОИМП, так как они являются уроантисептиками, то есть создают терапевтическую концентрацию в моче, но не в паренхиме почек.
Длительность курса антибактериальной терапии ОИМП должна составлять не менее 14 дней. Более короткие курсы (7-10 дней) допустимы при назначении фторхинолоновых антибиотиков, выделении высокочувствительного возбудителя и устранении факторов, осложняющих течение ИМП [5].
В заключение хочется подчеркнуть, что лечение инфекций мочевыводящих путей — процесс сложный, длительный и зачастую малоэффективный, поскольку из всего многообразия существующих на сегодня антибактериальных препаратов ни один не обладает достаточно высокой эффективностью в отношении биопленок. Поэтому усилия врачей должны быть направлены преимущественно на профилактику возникновения подобных инфекций.
Читайте также:

