Что такое вэд инфекции
Обновлено: 26.04.2024
Герпесвирусы широко распространены в человеческой популяции. После первичного инфицирования вирусы герпесгруппы переходят в латентное состояние и пожизненно персистируют в организме. При неблагоприятных условиях и снижении местного или системного иммунитета может происходить реактивация инфекции, что обусловливает развитие воспаления чаще всего на местном уровне. Разнообразие клинических форм герпесвирусных инфекций постоянно поддерживает научный интерес как в области изучения их патофизиологии, так и в области поиска эффективной противовирусной терапии. Особенно актуально это для β- и γ-герпесвирусов, т. к. группа α-герпесвирусов изучена достаточно хорошо.
Цель исследования: определить эффективность валацикловира в отношении репликации вируса Эпштейна – Барр (ВЭБ), вируса герпеса человека 6 типа (ВГЧ-6), цитомегаловируса (ЦМВ) в ротоглотке у часто болеющих взрослых с хроническими воспалительными заболеваниями верхних дыхательных путей (ВДП).
Материал и методы: нами амбулаторно обследованы 80 пациентов с частыми рецидивами хронических воспалительных заболеваний ВДП. Всем пациентам проводились микробиологическое исследование мазков из ротоглотки и оценка вирусной нагрузки в смешанной слюне и цельной крови вне периода обострения. Пациенты получали терапию валацикловиром по схеме 500 мг 3 р./сут в течение 14 дней. Контроль вирусной нагрузки в биоматериале проводился после окончания лечения.
Результаты и обсуждение: микробный пейзаж ротоглотки часто болеющих взрослых вне периода обострения представлен преимущественно нормальной или условно-патогенной микрофлорой. В смешанной слюне обнаруживалась ДНК ВЭБ, ВГЧ-6, но не ЦМВ. При этом в образцах крови указанных пациентов ДНК вирусов герпесгруппы не выявлялась. Применение валацикловира в дозе 500 мг 3 р./сут достоверно снижает репликацию ВЭБ в ротоглотке у часто болеющих взрослых.
Выводы: целесообразно провести дальнейшие исследования по определению режима дозирования и оценке клинической эффективности ациклических нуклеозидов в лечении ВЭБ-инфекции.
Ключевые слова: герпесвирусы, вирус Эпштейна – Барр, вирус герпеса человека, цитомегаловирус, часто болеющие взрослые, вирусная нагрузка, валацикловир.
Human herpesviruses infections: clinical features and opportunities of therapy
R.V. Shubelko 1 , I.N. Zuykova 2 , A.E. Shulzhenko 2
1 JSC "K+31", Moscow
2 “National Research Center — Institute of Immunology” Federal Medical-Biological Agency of Russia, Moscow
Herpesviruses are widely spread among the human population. After the primary infection, the herpesviruses become latent and persistent in the human body for life. Adverse conditions and a low local or systemic immunity may reactivate the infection, which causes the inflammation, usually at the local level. The variety of clinical forms of herpesviruses infections constantly supports scientific interest both in the field of studying their pathophysiology and in the search for effective antiviral therapy. This is especially important for β- and γ-herpesviruses, since the α-herpesvirus group has been studied rather well.
Aim: to determine the efficacy of valacyclovir for replication of the Epstein-Barr virus (EBV), human herpesvirus type 6 (HHV-6), cytomegalovirus (CMV) in the oropharynx in frequently ill adults with chronic inflammatory diseases of the upper respiratory tract.
Patients and Methods: 80 patients with frequent recurrences of chronic inflammatory diseases of the upper respiratory tract were examined outpatiently. All patients underwent microbiological examination of swabs from the oropharynx and the viral load in mixed saliva and whole blood not in exacerbation period was assessed. Patients received valacyclovir therapy according to the scheme 500 mg x 3 times a day for 14 days. Control of viral load in the biomaterial was carried out after the end of treatment.
Results and Discussion: out of the period of exacerbation the oropharynx microflora in frequently ill adults is represented mainly by a normal or conditionally pathogenic microflora. EBV DNA, HHV-6, but not CMV DNA, were detected in the mixed saliva. The DNA of the herpesvirus was not detected in the blood samples of these patients. The use of valacyclovir in a dose
of 500 mg 3 times a day significantly reduces the replication of EBV in the oropharynx in frequently ill adults.
Conclusions: it is advisable to conduct further studies to determine the dosage regimen and evaluate the clinical efficacy of acyclic nucleosides in the treatment of EBV infection.
В статье рассмотрены клинические особенности и возможности терапии герпесвирусных инфекции человека. Определена эффективность валацикловира в отношении репликации вируса Эпштейна – Барр, вируса герпеса человека 6 типа, цитомегаловируса.
Введение
Герпесвирусы широко распространены в человеческой популяции и обладают большим разнообразием клинических проявлений, поражая различные органы и ткани. В настоящее время известно 8 видов герпесвирусов человека, разделенных на 3 группы: α-герпесвирусы — вирусы простого герпеса 1 и 2 типа (ВПГ-1, -2), вирус ветряной оспы (ВВО), β-герпесвирусы: цитомегаловирус (ЦМВ), вирус герпеса человека 6 типа (ВГЧ-6), ВГЧ-7 и γ-герпесвирусы: вирус Эпштейна – Барр (ВЭБ) и ВГЧ-8 [1, 2].
По данным ВОЗ, около 90% населения земного шара инфицированы одним или несколькими видами герпесвирусов. Первичное инфицирование, как правило, происходит в детском возрасте, после чего вирусы герпесгруппы переходят в латентное состояние, которое характеризуется отсутствием вирусной репликации и экспрессией вирусных белков. Реактивация герпесвирусов из латентной формы происходит на фоне транзиторных (инфекция, неблагоприятные факторы внешней среды, психоэмоциональные перегрузки, эндокринные нарушения и др.) или стойких (первичные или вторичные иммунодефициты, иммуносупрессивная терапия) иммунодефицитных состояний.
Распространенность герпесвирусов в мире и широкий клинический полиморфизм потенцируют проведение большого количества исследований в области изучения патофизиологии и иммунобиологии этой инфекции, а также поиск эффективной противовирусной терапии [1–3].
В своей практической деятельности врачи многих специальностей, в т. ч. и иммунологи, встречаются с заболеваниями, вызванными ВПГ 1 и 2 типа (лабиальный и генитальный герпес), ВВО (ветряная оспа, опоясывающий лишай), для которых разработаны и стандартизированы методы диагностики и терапии. Однако патофизиология и патоморфология хронических герпесвирусных инфекций, обусловленных β- и γ-герпесвирусами, недостаточно изучены, не разработаны четкие методы и стандарты их лечения, что создает определенные трудности в ведении таких пациентов.
Вирус Эпштейна – Барр
Цитомегаловирус
ЦМВ относится к семейству β-герпесвирусов. Для постнатальной цитомегаловирусной инфекции (ЦМВИ) входными воротами служат чаще всего слизистые оболочки ротоглотки и слюнные железы, где и происходит первичная репродукция вируса. Первичное инфицирование ЦМВ иммунокомпетентных лиц обычно протекает бессимптомно, лишь в 5% случаев — в виде мононуклеозоподобного синдрома (цитомегаловирусный мононуклеоз). Отличительными признаками острого процесса являются высокая лихорадка, интоксикационный синдром, сиалоаденит (чаще околоушных слюнных желез), фарингит, гепатомегалия, спленомегалия, выраженный и длительный астенический синдром. При этом для острого процесса поражение миндалин нехарактерно, увеличение регионарных лимфатических узлов отмечается редко. После разрешения первичной ЦМВИ вирус персистирует в латентном состоянии в моноцитах, эпителиальных клетках и клетках слюнных желез, которые являются резервуаром вирусных частиц.
ЦМВИ у взрослых протекает в латентной (локализованной) и генерализованной формах. Латентная форма обычно не проявляется четкими клиническими симптомами. Иногда наблюдаются легкие гриппоподобные состояния, субфебрилитет. У женщин латентно протекающая ЦМВИ может проявляться в виде повторного невынашивания беременности и мертворождения, а также в виде вульвовагинита, кольпита, цервицита, эндометрита, сальпингоофорита.
Генерализованная форма приобретенной ЦМВИ у взрослых наблюдается редко, чаще на фоне иммуносупрессии, и, безусловно, является прерогативой наблюдения инфекционистов. При этом могут поражаться желудочно-кишечный тракт (гепатит, сиалоаденит, эзофагит, гастрит, энтероколит), надпочечники (адреналит), бронхолегочная система (интерстициальная пневмония, бронхит, фиброзирующий бронхиолит, альвеолит), нервная система (энцефаловентрикулит, миелит, полирадикулопатия, полинейропатия), почки, глаза, миокард [1–3].
У иммунокомпетентных взрослых ЦМВ не поражает лимфоидную ткань, а его локальная реактивация проявляется репликацией в клетках эпителия слюнных желез, поэтому, вероятнее всего, он не играет какой-либо роли в развитии хронических воспалительных заболеваний ВДП у взрослых, характеризующихся в первую очередь поражением лимфоидных структур ротоглотки.
Вирус герпеса человека 6 типа
Еще один представитель семейства β-герпесвирусов — ВГЧ-6. Ведущий путь передачи герпесвирусной инфекции, вызванной ВГЧ-6, — воздушно-капельный. В таких случаях первичная репликация происходит в слюнных железах, лимфоидной ткани ротоглотки и шейных лимфатических узлах. Генерализация инфекции может происходить гематогенным или лимфогенным путем. Около 90% инфицированных клеток представлено Т-лимфоцитами (преимущественно CD4+), оставшаяся часть включает В-лимфоциты, моноцитарно-макрофагальные, глиальные клетки и мегакариоциты. Первичная ВГЧ-6-инфекция может протекать бессимптомно, в виде внезапной экзантемы, фебрильных или нефебрильных судорог.
На сегодняшний день считается доказанной роль ВГЧ-6 в формировании инфекционного мононуклеоза (или мононуклеозоподобного синдрома), который характеризуется непродолжительной фебрильной лихорадкой, умеренно выраженными симптомами интоксикации, умеренной лимфоаденопатией, поражением лимфоидной ткани ротоглотки (острый тонзиллит), умеренной гепатомегалией и, в половине случаев, спленомегалией, розеолоподобными высыпаниями (внезапная экзантема). В дальнейшем ВГЧ-6 переходит в латентную или персистирующую форму. Системная реактивация ВГЧ-6 чаще наблюдается у иммунокомпрометированных лиц и может приводить к развитию тяжелых органных поражений (энцефалит, пневмонит, миокардит и др.) и потенциально летальных системных поражений (вирусный сепсис) [1–3, 5].
К числу основных зон персистенции ВГЧ-6 относятся моноциты слюнных желез и лимфоидная ткань ротоглотки [2, 3, 5], поэтому реактивация хронической инфекции у иммунокомпетентных взрослых может происходить по типу мононуклеозоподобного синдрома, с воспалением слизистых оболочек и лимфоидных структур ротоглотки (тонзиллит, фарингиты). Не исключено также, что ВГЧ-6 играет определенную роль в снижении мукозального иммунитета ротоглотки и поддержании хронического воспалительного процесса на местном уровне.
Лечение герпесвирусных инфекций
Материал и методы
Результаты
Первичная герпесвирусная инфекция, обусловленная ВЭБ, ЦМВ, ВГЧ-6, протекает в большинстве случаев в виде инфекционного мононуклеоза. В дальнейшем герпесвирусы пожизненно персистируют в макроорганизме, в т. ч. и в области входных ворот инфекции (лимфоидная ткань ротоглотки). При неблагоприятных условиях и снижении местного или системного иммунитета может происходить локальная реактивация герпесвирусов, провоцируя развитие воспаления на местном уровне.
Микробный пейзаж ротоглотки у часто болеющих взрослых вне периода обострения представлен преимущественно нормальной или условно-патогенной микрофлорой.
В смешанной слюне часто болеющих взрослых вне периода обострения с высокой частотой достоверности обнаруживается ДНК ВЭБ, ВГЧ-6, и не обнаруживается ДНК ЦМВ. При этом в образцах крови указанных пациентов ДНК вирусов герпесгруппы не выявлена, что свидетельствует не о системной, а о преимущественно местной реактивации герпесвирусной инфекции. Учитывая, что титры вирусной нагрузки ВЭБ при микст-инфекции выше (4,47 Lg, копий/10 5 клеток), чем при моноинфекции
(3,99 Lg, копий/105 клеток), можно предположить стимулирующее влияние ВГЧ-6 на активность ВЭБ.
Стандартная антибактериальная терапия без учета вирусной репликации зачастую неэффективна или недостаточно эффективна. Применение противовирусной терапии ациклическими нуклеозидами в комплексном лечении пациентов с частыми рецидивами хронических воспалительных заболеваний ВДП позволяет повысить целенаправленность этиотропной терапии текущего воспалительного процесса.
Из ациклических нуклеозидов наиболее оптимальным и исследованным в лечении герпесвирусов является валацикловир, обладающий высокой биодоступностью и хорошим профилем безопасности. В нашей работе мы применяли дозу валацикловира в 2 раза меньшую, чем та, которая ранее апробировалась разными исследователями, главным образом потому, что мы воздействовали не на острый системный процесс, а на локальную реактивацию герпесвирусной инфекции. Выяснилось, что применение валацикловира в дозе 500 мг 3 р./сут достоверно снижает репликацию ВЭБ в ротоглотке у пациентов с микст-инфекцией (ВЭБ + ВГЧ-6) — на 75%, в большей степени у пациентов с моноинфекцией (ДНК ВЭБ) — на 86%. В отношении инфекции, вызванной ВГЧ-6, не получено достоверных данных о снижении вирусной нагрузки.
Выводы
У часто болеющих взрослых микробный пейзаж вне периода обострения представлен сочетанной бактериально-вирусной микрофлорой: нормальной и/или условно-патогенной бактериальной флорой и представителями герпесгруппы (ВЭБ, ВГЧ-6), что может играть роль в хронизации воспаления в ротоглотке, способствовать снижению местного иммунитета и приводить к частым обострениям патологии ВДП.
Применение валацикловира в дозе 500 мг 3 р./сут в течение 14 дней оказалось эффективным в отношении ВЭБ — на фоне терапии вирусная нагрузка снижалась до нулевых или клинически незначимых титров.
Валацикловир обладает хорошей переносимостью и безопасностью как у молодых пациентов, так и у пациентов старшего возраста.
Дальнейшие исследования должны быть направлены на оценку клинической эффективности валацикловира в лечении реактивации ВЭБ-инфекции у часто болеющих взрослых.
1. Human Herpesviruses: Biology, Therapy, and Immunoprophylaxis / Eds A. Arvin, G. Campadelli-Fiume et al. Cambridge: Cambridge University Press, 2007. 1432 p.
2. Исаков В. А., Архипова Е. И., Исаков Д. В. Герпесвирусные инфекции человека. СПб.: СпецЛит., 2013. 670 с. [Isakov V.A., Arkhipova Ye.I., Isakov D. V. Gerpesvirusnyye infektsii cheloveka. SPb.: SpetsLit., 2013. 670 s. (in Russian)].
3. Иммунотерапия: Руководство для врачей / под ред. Хаитова Р. М., Атауллаханова Р. И., Шульженко А. Е. 2-е изд., перераб. и доп. М.: ГЭОТАР-Медиа, 2018. 768 с. [Immunoterapiya: Rukovodstvo dlya vrachey / pod red. Khaitova R. M., Ataullakhanova R. I., Shul’zhenko A. Ye. 2-ye izd., pererab. i dop. M.: GEOTAR-Media, 2018. 768 s. (in Russian)].
4. Lennon P., Crotty M., Fenton J. E. Infectious mononucleosis // British Medical Journal. 2015. Vol. 350. P. 1–7.
5. Agut H., Bonnafous P., Gautheret-Dejean A. Laboratory and Clinical Aspects of Human Herpesvirus 6 Infection // Clinical Microbiology Reviews. 2015. Vol. 28 (2).
P. 313–335. doi: 10.1128/CMR.00122–14.
6. Andersson J., Britton S., Ernberg I. et al. Effect of acyclovir on infectious mononucleosis: a double-blind, placebo-controlled study // J Infect Dis. 1986. Vol. 153. P. 283–290.
7. Andersson J., Sköldenberg B., Henle W. et al. Acyclovir treatment in infectious mononucleosis: a clinical and virological study // Infection. 1987. Vol. 15. P. 14–20.
8. Pagano J. S., Sixbey J. W., Lin J. C. Acyclovir and Epstein-Barr virus infection // J Antimicrob Chemother. 1983. Vol. 12 (Suppl B). P. 113–121.
9. Tynell E., Aurelius E., Brandell A. et al. Acyclovir and prednisolone treatment of acute infectious mononucleosis: a multicenter, double-blind, placebo-controlled study // J Infect Dis. 1996. Vol. 174. P. 324–331.
10. Van der Horst C., Joncas J., Ahronheim G. et al. Lack of effect of peroral acyclovir for the treatment of acute infectious mononucleosis // J Infect Dis. 1991. Vol. 164. P. 788–792.
11. Vouloumanou E. K., Rafailidis P. I., Falagas M. E. Current diagnosis and management of infectious mononucleosis // Current Opinion in Hematology. 2012. Vol. 19 (1). P. 14–20. doi: 10.1097/MOH.0b013e32834daa08.
12. Balfour Jr.H., Hokanson K. M., Schacherer R. M. et al. A virologic pilot study of valacyclovir in infectious mononucleosis // Journal of Clinical Virology. 2007. Vol. 39. P. 16–21.
13. Walling D. M., Flaitz C. M., Nichols C. M. Epstein-Barr Virus Replication in Oral Hairy Leukoplakia: Response, Persistence, and Resistance to Treatment with Valacyclovir // Journal of Infectious Diseases. 2003. Vol. 188. P. 883–890.
14. Cox A. J., Gleeson M., Pyne D. B. et al. Valtrex therapy for Epstein-Barr virus reactivation and upper respiratory symptoms in elite runners // Med. Sci. Sports Exerc. 2004. Vol. 36 (7). P. 1104–1110.
15. Vezina H. E., Balfour Jr. H., Weller D. R. et al. Valacyclovir pharmacokinetics and exploratory pharmacodynamics in young adults with Epstein-Barr virus infectious mononucleosis // J Clin Pharmacol. 2010. Vol. 50. P. 734–742.
16. Hoshino Y., Katano H., Zou P. et al. Long-Term Administration of Valacyclovir Reduces the Number of Epstein-Barr Virus (EBV) -Infected B Cells but Not the Number of EBV DNA Copies per B Cell in Healthy Volunteers // Journal of virology. 2009. Vol. 83 (22). P. 11857–11861.
17. De Paor M., O’Brien K., Fahey T., Smith S. M. Antiviral agents for infectious mononucleosis (glandular fever) // The Cochrane Database of Systematic Reviews. 2016. Issue 12. CD011487. doi: 10.1002/14651858.
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ).
Одной из актуальных проблем современной медицины является высокая инфицированность населения одним из представителей оппортунистических возбудителей — вирусом Эпштейна–Барр (ВЭБ). Практикующие врачи в своей повседневной практике чаще сталкиваются с клинически манифестными формами первичной Эпштейна–Барр-вирусной инфекции (ЭБВИ) в виде острой, как правило, не верифицированной респираторной инфекцией (более 40% случаев) или инфекционным мононуклеозом (около 18% всех заболеваний) [1, 2]. В большинстве случаев эти заболевания протекают доброкачественно и заканчиваются выздоровлением, но с пожизненной персистенцией ВЭБ в организме переболевшего [1, 3–5].
Однако в 10–25% случаев первичное инфицирование ВЭБ, протекающее бессимптомно, и острая ЭБВИ могут иметь неблагоприятные последствия [6–9] с формированием лимфопролиферативных и онкологических заболеваний, синдрома хронической усталости, ВЭБ-ассоциированного гемофагоцитарного синдрома и др. [7, 9, 11–14].
До настоящего времени нет четких критериев, позволяющих прогнозировать исход первичного инфицирования ВЭБ. Перед врачом, к которому обращается пациент с острой ЭБВИ, всегда встает вопрос: что предпринять в каждом конкретном случае, чтобы максимально снизить риск развития хронической ЭБВИ и ВЭБ-ассоциированных патологических состояний Этот вопрос не праздный, и ответить на него действительно очень трудно, т. к. до сих пор нет четкой патогенетически обоснованной схемы лечения больных, а имеющиеся рекомендации часто противоречат друг другу.
По мнению многих исследователей, лечение ЭБВИ-мононуклеоза (ЭБВИМ) не требует назначения специфической терапии [15–17]. Лечение больных, как правило, проводится в амбулаторных условиях, изоляция пациента не требуется. Показаниями к госпитализации следует считать длительную лихорадку, выраженный синдром тонзиллита и/или синдром ангины, полилимфаденопатию, желтуху, анемию, обструкцию дыхательных путей, боли в животе и развитие осложнений (хирургических, неврологических, гематологических, со стороны сердечно-сосудистой и дыхательной системы, синдром Рейе).
При легком и среднетяжелом течении ЭБВ ИМ больным целесообразно рекомендовать палатный или общий режим с возвращением к обычной деятельности на адекватном для каждого конкретного больного физическом и энергетическом уровне. Проведенное многоцентровое исследование показало, что необоснованно рекомендуемый строгий постельный режим удлиняет период выздоровления и сопровождается длительным астеническим синдромом, требующим нередко медикаментозного лечения [18].
При легком течении ЭБВ ИМ лечение больных ограничивается поддерживающей терапией, включающей адекватную гидратацию, полоскание ротоглотки раствором антисептиков (с добавлением 2% раствора лидокаина (ксилокаина) при выраженном дискомфорте в глотке), нестероидные противовоспалительные препараты, такие как парацетамол (Ацетаминофен, Тайленол). По мнению ряда авторов назначение блокаторов Н2 рецепторов, витаминов, гепатопротекторов и местная обработка миндалин различными антисептиками являются малоэффективными и необоснованными способами лечения [19, 20]. Из экзотических методов лечения следует упомянуть рекомендуемое Ф. Г. Боковым и соавт. (2006) применение мегадоз бифидобактерий при лечении больных острым мононуклеозом [21].
Мнения о целесообразности назначения антибактериальных препаратов при лечении ЭБВИМ весьма противоречивы. По мнению Gershburg E. (2005) тонзиллит при ИМ часто асептический и назначение антибактериальной терапии не оправдано. Также нет смысла в применении антибактериальных средств при катаральной ангине [4]. Показанием для назначения антибактериальных препаратов является присоединение вторичной бактериальной инфекции (развитие у больного лакунарной или некротической ангины, таких осложнений, как пневмония, плеврит и др.), о чем свидетельствуют сохраняющиеся более трех суток выраженные воспалительные изменения показателей крови и фебрильная лихорадка. Выбор препарата зависит от чувствительности микрофлоры на миндалинах больного к антибиотикам и возможных побочных реакций со стороны органов и систем.
По данным H. Fota-Markowcka et al. (2002) у больных чаще выделяют гемофильную палочку, стафилококк и пиогенный стрептококк, реже — грибы рода Candida [22], поэтому следует признать обоснованным назначение этим больным препаратов из группы цефалоспоринов 2–3 поколения, линкосамидов, макролидов и противогрибковых средств (флуконазол) в терапевтических дозах на 5–7 дней (реже — 10 дней) [4]. Некоторые авторы при наличии некротической ангины и гнилостном запахе изо рта, вызванных, вероятно, ассоциированной анаэробной флорой, рекомендуют использовать метронидазол по 0,75 г/сут, разделенных на 3 приема, в течение 7–10 дней.
Противопоказаны препараты из группы аминопенициллинов (ампициллин, амоксициллин (Флемоксин Солютаб, Хиконцил), амоксициллин с клавуланатом (Амоксиклав, Моксиклав, Аугментин)) из-за возможности развития аллергической реакции в виде экзантемы. Появление сыпи на аминопенициллины не является IgE-зависимой реакцией, поэтому применение блокаторов Н1 гистаминовых рецепторов не имеет ни профилактического, ни лечебного эффекта [19].
По мнению ряда авторов до настоящего времени сохраняется эмпирический подход к назначению глюкокортикостероидов больным с ЭБВИ [23]. Глюкокортикостероиды (преднизолон, преднизон (Делтазон, Метикортен, Оразон, Ликвид Пред), Солу Кортеф (гидрокортизон), дексаметазон) рекомендуются больным с тяжелым течением ЭБВИМ, с обструкцией дыхательных путей, неврологическими и гематологическими осложнениями (тяжелая тромбоцитопения, гемолитическая анемия) [4, 24]. Суточная доза преднизолона составляет 60–80 мг в течение 3–5 дней (реже 7 дней) с последующей быстрой отменой препарата. Одинаковой точки зрения на назначение этим больным глюкокортикостероидов при развитии миокардита, перикардита и поражениях ЦНС нет.
При тяжелом течении ЭБВИМ показана внутривенная дезинтоксикационная терапия, при разрыве селезенки — хирургическое лечение.
Наиболее дискуссионным остается вопрос о назначении противовирусной терапии больным с ЭБВИ. В настоящее время известен большой перечень препаратов, являющихся ингибиторами ВЭБ репликации в культуре клеток [4, 25–27].
I. Подавляющие активность ДНК-полимеразы ВЭБ:
- ациклические аналоги нуклеозидов (ацикловир, ганцикловир, пенцикловир, валацикловир, валганцикловир, фамцикловир);
- ациклические аналоги нуклеотидов (цидофовир, адефовир);
- аналоги пирофосфатов (Фоскарнет (фоскавир), фосфоноацетиловая кислота);
- 4 оксо-дигидрохинолины (возможно).
II. Различные соединения, не ингибирующие вирусной ДНК-полимеразы (механизм изучается): марибавир, бета-L-5 урацил йододиоксолан, индолокарбазол.
Однако проведенный метаанализ пяти рандомизированных контролируемых испытаний с участием 339 больных ЭБВИМ, принимавших ацикловир (Зовиракс), показал неэффективность препарата [28, 29].
Одна из возможных причин кроется в цикле развития ВЭБ, в котором ДНК вируса имеет линейную либо циркулярную (эписома) структуру и размножается в ядре клетки хозяина. Активная репликация вируса происходит при продуктивной (литической) стадии инфекционного процесса (ДНК ВЭБ линейной формы). При острой ЭБВИ и активации хронической ЭБВИ происходит цитолитический цикл развития вируса, при котором он запускает экспрессию собственных ранних антигенов и активирует некоторые гены клеток макроорганизма, продукты которых участвуют в репликации ВЭБ. При латентной ЭБВИ ДНК вируса имеет вид эписомы (круговой суперспиральный геном), находящейся в ядре. Циркулярный геном ДНК ВЭБ характерен для CD21+ лимфоцитов, в которых даже при первичном инфицировании вирусом практически не наблюдается литической стадии инфекционного процесса, а ДНК воспроизводится в виде эписомы синхронно с клеточным делением инфицированных клеток. Гибель пораженных ВЭБ В лимфоцитов связана не с опосредованным вирусом цитолизом, а с действием цитотоксических лимфоцитов [4].
При назначении противовирусных препаратов при ЭБВИ врач должен помнить, что их клиническая эффективность зависит от правильной трактовки клинических проявлений болезни, стадии инфекционного процесса и цикла развития вируса на этой стадии. Однако не менее важным является и тот факт, что большинство симптомов ЭБВИ связаны не с прямым цитопатическим действием вируса в инфицированных тканях, а с опосредованным иммунопатологическим ответом ВЭБ-инфицированных В лимфоцитов, циркулирующих в крови и находящихся в клетках пораженных органов. Именно поэтому аналоги нуклеозидов (ацикловир, ганцикловир и др.) и ингибиторы полимеразы (Фоскарнет), подавляющие репликацию ВЭБ и уменьшающие содержание вируса в слюне (но не санирующие ее полностью [4], не оказывают клинического эффекта на тяжесть и продолжительность симптомов ЭБВИМ.
Показаниями для лечения ЭБВИМ противовирусными препаратами являются: тяжелое, осложненное течение болезни, необходимость профилактики ВЭБ-ассоциированной В-клеточной лимфопролиферации у иммунокомпрометированных пациентов, ВЭБ-ассоциированная лейкоплакия. Bannett N. J., Domachowske J. (2010) рекомендуют применять ацикловир (Зовиракс) внутрь в дозе 800 мг внутрь 5 раз в сутки в течение 10 дней (или 10 мг/кг каждые 8 часов в течение 7–10 дней). При поражениях нервной системы предпочтителен внутривенный способ введения препарата в дозе 30 мг/кг/сут 3 раза в сутки в течение 7–10 дней.
По мнению E. Gershburg, J. S. Pagano (2005), если под действием каких-либо факторов (например, иммуномодуляторов, при ВЭБ-ассоциированных злокачественных опухолях — применение лучевой терапии, гемцитабина, доксорубицина, аргинина бутирата и др.) удается перевести ДНК ВЭБ из эписомы в активную репликативную форму, т. е. активировать литический цикл вируса, то в этом случае можно ожидать клинический эффект от противовирусной терапии.
В комплексной терапии рекомендуется внутривенное введение иммуноглобулинов (Гаммар-П, Полигам, Сандоглобулин, Альфаглобин и др.) 400 мг/кг/сут, № 4–5.
В последние годы все чаще для лечения ЭБВИ стали применять рекомбинантные альфа-интерфероны (Интрон А, Роферон-А, Реаферон-ЕС) по 1 млн ME в/м в течение 5–7 дней или через день; при хронической активной ЭБВИ — 3 млн ME в/м 3 раза в неделю, курс 12–36 недель.
Медикаментозная коррекция астенического синдрома при хронической ЭБВИ включает назначение адаптогенов, высоких доз витаминов группы В, ноотропных препаратов, антидепрессантов, психостимуляторов, препаратов с прохолинергическим механизмом действия и корректоров клеточного метаболизма [30–32].
Залогом успешного лечения больного с ЭБВИ являются комплексная терапия и строго индивидуальная тактика ведения как в стационаре, так и во время диспансерного наблюдения.
Литература
И. В. Шестакова, доктор медицинских наук, доцент
Н. Д. Ющук, доктор медицинских наук, профессор, академик РАМН
МГМСУ, Москва
Считается, что вирус Эпштейна-Барр человеческие организмы поражает чаще всего. И большинство исследований эту теорию действительно подтверждают – многие люди являются носителями микроорганизма, сами о том не подозревая. И чтобы лечение вируса Эпштейна-Барр началось вовремя, нужно знать симптоматику недуга. Конечно же, в разных организмах болезнь проявляет себя по-своему. Но как правило, эти отличия несущественны.
Особенности развития и симптоматика вируса Эпштейна-Барр
Этот микроорганизм относится к знаменитому семейству герпесвирусов. Это лимфотропный вирус, приводящий к разладам в работе иммунной системы. Он передается воздушно-капельным, контактно-бытовым и половым путем. Медицине известны и такие случаи, когда заражение происходило еще в младенческом возрасте при родах. Перенеся первичную инфекцию, многие пациенты до конца жизни остаются ее носителями.
Распознать симптоматику и вовремя начать лечение вируса Эпштейна-Барр очень важно, поскольку он представляет серьезную опасность для организма. Вот лишь небольшой список недугов, к которым ВЭБ может привести:
- герпес;
- заболевания нервной системы;
- нарушения в работе желудочно-кишечного тракта;
- добро- и злокачественные опухоли кишечника и желудка;
- гепатит;
- рассеянный склероз;
- синдром хронической усталости;
- инфекционный мононуклеоз;
- лимфомы;
- болезнь Ходжкина;
- злокачественное новообразование в области носоглотки;
- грибковые заболевания.
Главным признаком вируса Эпштейна-Барр считается увеличение лимфатических узлов. Они могут достигать пары сантиметров в диаметре. Зачастую припухлости не доставляют слишком много дискомфорта, но некоторым пациентам приходится сталкиваться с достаточно сильными болями. Начинается поражение с шейных, но впоследствии может переходить и на локтевые, подмышечные, бедренные и паховые лимфоузлы.
Зная эти симптомы, вы сможете вовремя начать лечение вируса Эпштейна-Барр и предотвратить переход недуга в хроническую форму:
- слабость;
- боль в горле; ;
- повышение температуры до 39-40°C;
- увеличение печени и селезенки;
- высыпания (притом сыпь может быть разного вида: точки, язвы, пятна папулы);
- быстрая утомляемость;
- общая слабость;
- боль в мышцах;
- поносы;
- тошнота;
- рвота;
- изменение тембра голоса;
- появление гнойного налета на задней стенке глотки.
Носители ВЭД могут страдать от частых грибковых поражений. Все из-за того, что иммунитет не может оказывать должного сопротивления инфекции.
Лечение вируса Эпштейна-Барр
Единой схемы, подходящей для лечения всех, без исключения, пациентов, не существует. Выбирать оздоровительный курс может либо инфекционист, либо онколог – все зависит от того, насколько сильно вирус успел развиться.
Бороться с вредоносным микроорганизмом нужно в условиях стационара. Чаще всего для лечения вируса Эпштейн-Барр применяют такие препараты:
- Виферон;
- Альфаинтерферон; ;
- Арбидол;
- Тетрациклин;
- Изопринозин;
- Валтрекс;
- Ганцикловир;
- Лейкинферон и другие.
Кроме противовирусных медикаментов и антибиотиков, обязательно принимать витамины и препараты для укрепления иммунитета.

Продолжительность лечения также зависит от стадии заболевания и может варьироваться в пределах от двух недель до нескольких месяцев.
Полагаться исключительно на лечение народными средствами при вирусе Эпштейна-Барр не стоит. Но в качестве дополнительной терапии использовать их можно вполне. Чрезвычайно полезными считаются травы. Наиболее эффективными при ВЭБ являются:
- женьшень;
- мята;
- ромашка;
- календула;
- мать-и-мачеха.
Герпес – известный и достаточно распространенный вирус. Сталкиваться с разными его видами и формами приходится практически всем представительницам прекрасного пола. Что представляет собой герпес второго типа, и как с ним бороться, расскажем в статье.
Саркоидоз легких – заболевание, при котором в органе образуются небольшие сгустки – гранулемы. Это доброкачественные новообразования. Многие пациенты даже не догадываются о своей болезни – саркоидоз может никак не проявлять себя. Лечение же недуга требуется при появлении симптомов.
Кашель может доставлять массу дискомфорта в течение дня. Представьте, насколько неприятно бывает просыпаться из-за утреннего приступа. Провоцировать появление его могут абсолютно разные факторы. Есть среди них и безобидные, и те, что представляют серьезную опасность для здоровья.
Что такое вегето-сосудистая дистония (ВСД)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Патриной А.В., невролога со стажем в 17 лет.
Над статьей доктора Патриной А.В. работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Вегетососудистая дистония (ВСД) — это синдром, представленный в виде разнообразных нарушений вегетативных функций, связанных с расстройством нейрогенной регуляции и возникающих по причине нарушения баланса тонической активности симпатического и парасимпатич еского отдела в егетативной нервной системы [3] . Проявляется функциональными нарушениями, но обусловлены они субклеточными нарушениями [5] .
Краткое содержание статьи — в видео:
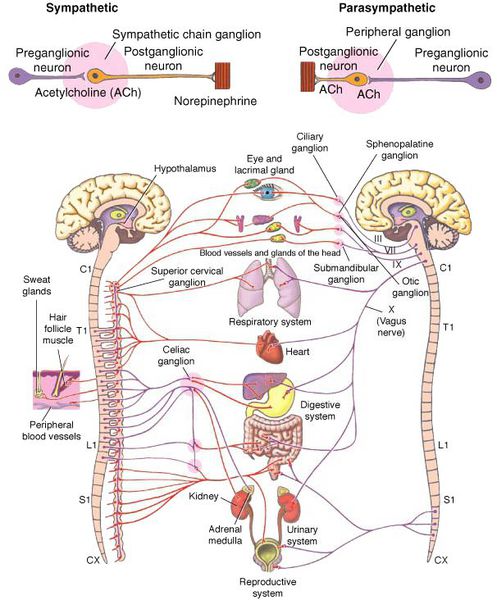
Что такое вегетативная нервная система (ВНС)
Вегетативная (автономная) нервная система (ВСН) является частью нервной системы организма, контролирующей деятельность внутренних органов и обмен веществ во всём организме. Она располагается в коре и стволе головного мозга, области гипоталамуса, спинном мозге, и состоит из периферических отделов. Любая патология этих структур, а также нарушение взаимосвязи с ВСН могут стать причиной возникновения вегетативных расстройств [1] .
Вегетососудистая дистония может возникнуть в разном возрасте, но преимущественно она встречается у молодых [5] .
Особенности проявления заболевания
- У мужчин и женщин. Женщины страдают от ВСД в два раза чаще мужчин, но различий в проявлениях болезни нет [3] .
- У подростков. ВСД распространена у подростков из-за активной гормональной перестройки организма.
- У беременных. ВСД у беременных также возникает в связи с гормональными изменениями. Опасные последствия: при гипотоническом типе ВСД — плацентарная недостаточность, гипоксия плода; при гипертоническом — гестозы, преэклампсия, эклампсия; отслойка плаценты; гипертонус матки, преждевременные роды.
Причины ВСД
ВСД — многопричинное расстройство, которое может выступать в качестве отдельного первичного заболевания, но чаще оно является вторичной патологией, проявляющейся на фоне имеющихся соматических и неврологических заболеваний [15] .
Факторы риска развития вегето-сосудистой дистонии подразделяются на предрасполагающие и вызывающие.
Вызывающие факторы:
- Психогенные[5] — острые и хронические психо-эмоциональные стрессы и другие психические и невротические расстройства [3] , которые являются основными предвестниками (предикторами) заболевания [10] . ВСД — это, в сущности, избыточная вегетативная реакция на стресс [9] . Часто психические расстройства — тревожный синдром депрессия — параллельно с психическими симптомами сопровождаются вегетативными: у одних пациентов преобладают психические, у других на первый план выходят соматические жалобы, что затрудняет диагностику [10] .
- Физические — переутомление, солнечный удар (гиперинсоляция), ионизирующая радиация, воздействие повышенной температуры, вибрация. Часто воздействие физических факторов связано с осуществлением профессиональных обязанностей, тогда они позиционируются как факторы профессиональной вредности [1] , которые могут вызывать или усугубить клиническую картину вегетососудистой дистонии. В таком случае имеются ограничения по допуску к работе с указанными факторами (приказ Минздрава РФ от 2021 года № 29).
- Химические — хронические интоксикации, злоупотребление алкоголем, никотином, спайсами и другими психоактивными веществами [5] . Проявления ВСД также могут быть связаны с побочными действиями некоторых лекарственных препаратов: антидепрессантов с активирующим действием, бронходилататоров, леводопы и препаратов, содержащих эфедрин и кофеин [10] . После их отмены происходит регресс симптомов ВСД.
- Дисгормональные — этапы гормональной перестройки: пубертат, климакс [3] , беременность, дизовариальные расстройства [5] , приём противозачаточных средств с периодами отмены [10] .
- Инфекционные — острые и хронические инфекции верхних дыхательных путей, мочеполовой системы, инфекционные заболевания нервной системы (менингиты, энцефалиты и другое) [5] .
- Иные заболевания головного мозга — болезнь Паркинсона, дисциркуляторная энцефалопатия (ДЭП), последствия черепно-мозговой травмы и другие [3] .
- Иные соматические заболевания — гастрит, панкреатит, гипертоническая болезнь, сахарный диабет, тиреотоксикоз [1] .
Предрасполагающие факторы:
- Наследственно-конституциональные особенности организма — заболевание возникает в детстве или в подростковом возрасте, со временем расстройство компенсируется, но восстановление нарушенных функций нестойкое, поэтому ситуация легко дестабилизируется под воздействием неблагоприятных факторов [10] .
- Особенности личности[5] — усиленная концентрация внимания на соматических (телесных) ощущениях, которые воспринимаются как проявление болезни, что, в свою очередь, запускает патологический механизм психо-вегетативной реакции [6] .
- Неблагоприятные социально-экономические условия — состояние экологии в целом, низкий уровень жизни, экономический кризис в стране, жилищные условия отдельных людей, культура питания (приверженность фастфуду, удешевление производства продуктов питания за счёт использования ненатурального сырья), культура спорта (несмотря на активное строительство спортивных комплексов, всё-таки полноценная интеграция спорта в повседневную жизнь населения не происходит) [5] . Также речь идёт об особенности климата в центральной части России с дефицитом ультрафиолетового излучения в холодное время года, что приводит к обострению многих хронических заболеваний в осенне-весенний период, в том числе и ВСД [1] .
- Патологии перинатального (дородового) периода — внутриутробные инфекции и интоксикации, резусконфликты, внутриутробная гипоксия (кислородное голодание), гестозы матери, фетоплацентарная недостаточность и другие [6] .
Мясищев В.Н., выдающийся отечественный психотерапевт, полагает, что ВСД развивается в результате влияния психо-эмоциональных нарушений на имеющиеся вегетативные аномалии [13] .
Также заболевание может возникать и у здоровых людей как транзиторная (временная) психофизиологическая реакция на какие-либо чрезвычайные, экстремальные ситуации [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы вегето-сосудистой дистонии
ВСД характеризуется проявлением симпатических, парасимпатических или смешанных симптомокомплексов [1] . Преобладание тонуса симпатической части ВСН (симпатикотония) выражается в тахикардии, бледности кожи, повышении артериального давления, ослаблении сокращений стенок кишечника (перистальтике), расширении зрачка, ознобе, ощущении страха и тревоги [2] . Гиперфункция парасимпатического отдела (ваготония) сопровождается замедлением сердцебиения (брадикардией), затруднением дыхания, покраснением кожи лица, потливостью, повышенным слюноотделением, снижением артериального давления, раздражением (дискинезией) кишечника [2] .
Энтеровирусная инфекция – что это?
Энтеровирусные (неполио) инфекции - группа острых инфекционных заболеваний, вызываемых различными представителями энтеровирусов.

Основные возбудители:
- Коксаки A (24 серотипа),
- Коксаки B (6 серотипов),
- ECHO (34 серотипа)
- неклассифицированные энтеровирусы человека 68 - 71 типов.
Энтеровирус – это опасно?

Большинство энтеровирусных инфекций протекают легко. Но некоторые штаммы могут вызывать более тяжелые заболевания, особенно у маленьких детей.
Как происходит заражение?

Источник инфекции – человек (больной или носитель).
Заражение происходит воздушно-капельным путем, через пыль, а также водным, пищевым и контактно-бытовым путями.
Вода открытых водоемов, загрязненная сточными водами, как в качестве источников питьевого водоснабжения, так и используемая в качестве зон для купания населения - наиболее опасна в плане передачи инфекции.
Инкубационный период 1-10 дней.
Кто может заразиться?

Энтеровирусами может заразиться любой Чаще всего заражаются и заболевают дети, младенцы и подростки, т.к они еще не обладают иммунитетом (защитой) от предыдущих воздействий этих вирусов.
Имеет ли заболевание сезонность?
Вспышки энтеровирусной инфекции преимущественно возникают в летне-осенний период, но отдельные случаи встречаются в течение всего года.
Как протекает инфекция?

Энтеровирусная инфекция характеризуется разнообразием клинических проявлений и множественными поражениями органов и систем: серозный менингит, геморрагический конъюнктивит, синдром острого вялого паралича, заболевания с респираторным синдромом и другие.
Один и тот же серотип энтеровируса способен вызывать развитие нескольких клинических синдромов и, наоборот, различные серотипы энтеровирусов могут вызвать сходные клинические проявления болезни. Наибольшую опасность представляют тяжелые формы инфекции с поражением нервной системы.
Как защититься?

Соблюдение правил личной гигиены имеет жизненно важное значение для предотвращения распространения энтеровирусных инфекций.
- мытье рук с мылом
- тщательное мытье овощей и фруктов перед употреблением
- приобретение продуктов питания только в санкционированных местах
- термическая обработка продуктов
- купание только в разрешенных местах
- соблюдение гигиены во время купания (не заглатывать воду)
- недопущение контактов с инфицированными людьми, особенно с сыпью
- пить только бутилированную воду
При подозрении на инфекционное заболевание – немедленно обратитесь к врачу.
Читайте также:

