Что такое волчанка осложнения почек
Обновлено: 17.04.2024
Сотрудники Кыргызской государственной медицинской академии им. И.К. Ахунбаева, Первого МГМУ им. И.М. Сеченова и Витебского государственного ордена Дружбы народов медицинского университета представили обзор, целью которого стал – анализ данных литературы последних лет, касающийся распространенности и патогенетических механизмов развития поражения почек (волчаночного нефрита) при СКВ.
В последние годы обсуждается вопрос о причине более раннего и частого развития хронической болезни почек (ХБП) при системной красной волчанке (СКВ). В основе СКВ лежит сложное взаимодействие генетических и экзогенных факторов, приводящее к сложным нарушениям системы врожденного и приобретенного иммунитета; гиперпродукции провоспалительных цитокинов; патологической активации В-клеток; нарушению внутриклеточной сигнализации Т-клеток; дефекту клиренса клеток, подвергнутых апоптозу и некрозу. Среди аутоиммунных заболеваний человека, СКВ распространена преимущественно среди лиц женского пола, соотношение женщин и мужчин составляет примерно 10:1. Причем, в 90% случаев заболевание поражает молодых женщин детородного возраста (20 – 40 лет), хотя может развиваться как в детском, так и в пожилом возрасте у лиц обоих полов. Здесь стоит отметить, что у лиц старших возрастных групп наблюдается относительно спокойное течение как волчаночной нефропатии, так и СКВ. Примерно у 20% больных СКВ развивается в возрасте до 16 лет. Вовлечение почек в патологический процесс при СКВ, чаще всего формируется вследствие отложения в клубочках иммунных комплексов, что приводит к развитию воспалительной реакции в клубочках и, при прогрессировании, к вовлечению в процесс почечного интерстиция. Кроме того, повреждение почек может поддерживаться за счет других механизмов, таких как тромботическая микроангиопатия. Как отмечают исследователи, СКВ является классическим проявлением V типа кардиоренального синдрома, когда поражение сердца и почек развивается одновременно. ХБП оказывает важнейшее влияние на жизненный прогноз у больных СКВ.
Распространенность хронической болезни почек при системной красной волчанке
Поражения почек при СКВ (волчаночный нефрит, люпус-нефрит, волчаночная нефропатия) развиваются при остром и подостром течении СКВ с высокой иммунологической активностью, реже – при её хроническом течении. Большинство почечных нарушений появляются обычно в течение первых 6-36 месяцев после постановки диагноза СКВ. Имеются сведения, что риск развития волчаночного нефрита у больных СКВ спустя 5 лет и более после дебюта заболевания относительно невелик. Многие исследователи утверждают, что у детей с СКВ волчаночный нефрит встречается чаще (клинически диагностируется у 70–75%) и протекает тяжелее, чем у взрослых. А.В. Александров, Л.Н. Шилова, и соавторы проанализировали данные 60 больных с достоверным диагнозом СКВ с различными клиническими проявлениями. Как отмечают исследователи, поражение почек носило крайне разнообразный характер и выявлялось у 24 (40%) больных СКВ. У подавляющего большинства (15 человек) волчаночный нефрит развился в течение первых 6 лет от начала заболевания, у 12% больных поражение почек было первым проявлением СКВ. Клинико-лабораторные проявления поражения почек при СКВ отмечаются в 30-80% случаев, а морфологические изменения в почечной ткани встречаются практически у каждого пациента. В ряде работ наличие ХБП на основании классификации K/DOQI, Kidney Disease Outcomes Quality Initiative, 2007 установлено у 83% больных СКВ. Причем у 50% больных СКВ, имеющих ХБП, выявлялась С2 градация заболевания. В одном из исследований, среди 64 больных СКВ клинические и лабораторные проявления поражения почек отмечены у 48 человек в 75% случаев. Т.П. Макарова с соавторами провели ретроспективный анализ 60 случаев СКВ с оценкой клинических проявлений заболевания и вариантов волчаночного нефрита у детей в Республике Беларусь и Республике Татарстан. Так, среди участников исследования у 35 больных диагноз волчаночного нефрита верифицирован морфологически.
Распространенность признаков ХБП при СКВ имеет некоторые расовые, климато — географические отличия. По отчетам международных регистров США, общая распространенность волчаночного нефрита зависела от расовой принадлежности. Например, за период 1996-2004 гг. показатель частоты возникновения терминальной хронической почечной недостаточности, обусловленной волчаночным нефритом, составил 4,5 случая на 1 млн. взрослого населения в общей популяции и был значительно выше у представителей негроидной расы (17-20 на 1 млн. населения) и латиноамериканцев (6 на 1 млн. населения), чем у лиц европеоидной расы (2,5 на 1 млн. населения). В ретроспективном когортном исследовании Великобритании у 12% представителей европеоидной и 62% лиц негроидной рас с волчаночным нефритом в итоге формировалась терминальная хроническая почечная недостаточность. Кроме того, вероятность возникновения поражения почек была меньше у лиц белой расы (европейцев, американцев европейского происхождения; 12-33%), чем у представителей негроидной расы (афроамериканцев, жителей стран Карибского бассейна; 40-69%), латиноамериканцев (36-61%) или пациентов азиатского происхождения (индейцы, китайцы; 47-53%).
Волчаночный нефрит. Волчаночный нефрит отмечается у 60% взрослых и 80% детей и реже регистрируется при хроническом течении СКВ. У больных СКВ поражения почек могут протекать в форме хронического гломерулонефрита, быстропрогрессирующего гломерулонефрита, острого повреждения почек, нефротического синдрома, интерстициального нефрита или (реже) дистального тубулярного ацидоза, прогрессирующего снижения скорости клубочковой фильтрации, часто с гиперкалиемией. Волчаночный нефрит – это модель иммунокомплексного воспаления, механизм развития которого отражает патогенез СКВ. Выраженная активация В-лимфоцитов, играющих важную роль в обеспечении гуморального иммунитета, сопровождается продукцией аутоантител, прежде всего, к ядерным и цитоплазматическим белкам с последующим образованием циркулирующих иммунных комплексов (ЦИК). С патофизиологической точки зрения при встрече с антигеном или стимуляции со стороны T-лимфоцитов некоторые B-лимфоциты трансформируются в плазматические клетки, способные к продукции антител. Активированные В-лимфоциты начинают усиленно продуцировать цитокины, которые от клетки к клетке передают сигнал воспаления на уровне дезоксирибонуклеиновой кислоты (ДНК). У больных с СКВ аутоантитела к двуспиральной ДНК тесно связаны с активностью волчаночного нефрита и выявляются в составе иммунных комплексов в клубочках почек. Отложение ЦИК на почечных структурах сопровождается активацией моноцитов и макрофагов, в результате усиливается повреждение эндотелия сосудов клубочков, апоптоз и расстройства кровотока в микроциркуляторном русле. Макрофаги передают Т-лимфоцитам одновременно с переработанным антигеном и интерлейкин-1, который подготавливает поверхностные рецепторы на Т-хелперах к связыванию передаваемого антигена.
На скорость клиренса ЦИК большое влияние оказывают половые гормоны, в частности, эстрогены, замедляющие их элиминацию. Это одна из причин более частого выявления у женщин аутоиммунных заболеваний и СКВ. В трудах В.А. Насоновой, среди важных механизмов развития СКВ и волчаночного нефрита, особое место занимает замедление элиминации ЦИК из кровотока с удлинением времени их циркуляции, что связано с несостоятельностью макрофагов и моноцитов. Кроме того, элиминацию ЦИК обеспечивают также эритроциты периферической крови (через связывание их с рецепторами комплемента С3). При взаимодействии с рецепторами комплемента иммунные комплексы теряют способность фиксироваться в тканях органов-мишеней, в частности, почек. При СКВ регистрируется генетический дефект нарушения рецепторного звена связывания иммунных комплексов, что ведет к удлинению времени циркуляции и депонированию. У некоторых больных с СКВ обнаружен генетический дефицит комплемента С4, маркер которого входит в состав HLA/ Human Leukocyte Antigens и часто выявляется при носительстве HLA В8. Часто развитие волчаночного нефрита в дебюте и обострение СКВ (при остром и подостром течении заболевания) объясняются стабильно повышенным уровнем иммунных комплексов, свойством аутоантител (малый размер и легкая растворимость), которые определяют повреждающую активность ЦИК. Малые по размеру и растворимые иммунные комплексы плохо фагоцитируются и дольше циркулируют в кровотоке.
С другой стороны, более частому развитию волчаночного нефрита в некоторой степени способствует и уровень органного кровотока в почках. Так, о высокой функциональной активности почек свидетельствует тот факт, что в почку поступает примерно 25% всего объема сердечного выброса и эквивалентное количество кислорода. А объем кровотока в почке в несколько раз превышает такой в миокарде, головном мозге и печени. Важно, что наличие дуговых и сегментарных разветвлений сосудов почек, где наиболее активны кровоток и завихрения крови определяют локализацию и контакт ЦИК с базальной мембраной клубочков.
Нарушения активности В-лимфоцитов и их апоптоз при ревматических заболеваниях, в том числе при СКВ, активно изучается отечественными исследователями. При СКВ связывание антител к ДНК и других аутоантител с базальной мембраной клубочков ведет к активации комплемента.
Система комплемента – это группа белков, последовательно реагирующих друг с другом. При СКВ активация системы комплемента происходит классическими путями – формированием комплекса антиген – антитело. При волчаночном нефрите происходит последовательная активация компонентов комплемента (С1-С4-С2-С3-С3a-С3b), что приводит к формированию мембраноатакующего комплекса, вызывающего повреждение и лизис клетки. Непосредственное участие системы комплемента в развитии и прогрессировании волчаночного нефрита подтверждает тот факт, что комплементы обнаруживаются в очаге повреждения ткани почек (при иммуногистохимическом исследовании в клубочках выявляются отложения комплемента С3 и С1q), повышается их активность в крови и потребление отдельных компонентов комплемента (С1-С3-С4-С5). В частности, при СКВ дефицит ранних компонентов системы комплемента играет роль в возникновении волчаночного нефрита. Тогда как, повышенные титры антител к ДНК и низкие уровни комплемента C3 и C4 в крови часто указывают на активную волчанку. Наряду с ЦИК, поражению клубочков способствуют также повреждение эндотелия антифосфолипидными антителами, нарушение продукции и биологического действия оксида азота и формирование микротромбозов. В совокупности, нарушение целостности базальной мембраны клубочков, изменение заряд-селективности и колебание внутриклубочкового давления провоцируют протеинурию и нередко повышение артериального давления.
- Минимальные мезангиальные изменения;
- Мезангиальные пролиферативные измене-ния с отложениями в мезангии;
III. Очаговые пролиферативные изменения в клубочках;
- Диффузные (≥50% клубочков) пролифера-тивные изменения; диффузный сегментарный пролиферативный (IV-S, > 50% пораженных клубочков) с сегментар-ными изменениями; диффузный глобальный пролиферативный (IV-G, >50% пораженных клубочков) с глобаль-ными изменениями;
- Мембранозный гломерулонефрит;
- Запущенный гломерулосклероз:
- Активный нефрит: быстропрогрессирующий волчаночный нефрит; медленно прогрессирующий волчаночный нефрит; с нефротическим синдромом; с выраженным мочевым синдромом;
- Неактивный нефрит с минимальным мочевым синдромом или субклиническая протеинурия.
Заключение. Подытоживая литературные данные, следует отметить, что при СКВ поражение почек является одним из наиболее распространенных, тяжелых и прогностически неблагоприятных форм заболевания. Именно вовлечение в патологический процесс почек предопределяет в дальней-шем прогноз этих больных в отношении заболевания, а осложнения, связанные с волчаночным нефритом, являются основной причиной летальности у данной категории больных.
Муркамилов И.Т., Айтбаев К.А., Фомин В.В., Счастливенко А.И., Юсупов Ф.А.
Волчаночный нефрит — это деструкция гломерулярного аппарата почек вследствие аутоиммунного воспаления при системной красной волчанке. Проявляется отеками, уменьшением диуреза, макрогематурией, повышением АД, нарастающей интоксикацией, которые обычно усугубляют основную симптоматику СКВ, реже являются самостоятельными симптомами волчанки. Диагностируется с помощью общего анализа мочи, определения уровней сывороточного креатинина, аутоантител, волчаночного антикоагулянта, пункционной биопсии почек с гистологическим исследованием биоптата. Для лечения применяют цитостатики, кортикостероиды, ингибиторы рецепторов ангиотензина, проводят ЗПТ, трансплантацию почки.
МКБ-10
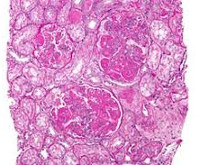
Общие сведения
Клинические признаки волчаночного гломерулонефрита определяются почти у половины больных с установленным диагнозом СКВ. Судя по результатам биопсий, распространенность почечной патологии при волчанке может превышать 90%. Заболевание одинаково часто поражает женщин и мужчин, страдающих волчанкой, однако у пациентов мужского пола волчаночный нефрит отличается более ранним началом, тяжелым и агрессивным течением. При возникновении в возрасте старше 40 лет гломерулонефрит имеет меньшую активность и протекает благоприятнее. Актуальность своевременной диагностики нефрологической патологии у больных СКВ обусловлена ухудшением общего прогноза при аутоиммунном поражении почек. Активный люпус-нефрит остается второй по частоте причиной смерти от волчанки и составляет до 23% в структуре летальности при этом заболевании.

Причины
Поражение почек при СКВ обусловлено характерными нарушениями иммунитета. Непосредственной причиной нефрита становится повреждение паренхимы и интерстиция вследствие специфической аутоиммунной деструкции тканей. Специалистами в сфере клинической урологии, нефрологии и ревматологии выявлено два этиологических фактора развития почечной патологии у пациентов, страдающих системной красной волчанкой:
- Иммунные комплексы. При СКВ неконтролируемо усиливается образование антител к собственным клеткам организма. Осаждение циркулирующих иммунных комплексов (ЦИК) в почках потенцирует возникновение специфического воспалительного процесса (гломерулонефрита).
- Волчаночный антикоагулянт. Антифосфолипидные антитела, вытесняя фосфолипид-связывающие протеины, провоцируют усиление коагуляции. Возникающие артериальные и венозные микротромбозы приводят к ишемии и атрофии почечной паренхимы, усугубляя течение нефрита.
Патогенез
Ключевым звеном в развитии волчаночного нефрита является повреждение почечных тканей вследствие аутоиммунной деструкции. В результате поликлональной активации B-лимфоцитов, недостаточной активности T-супрессоров, низкой толерантности к аутоантигенам в организме больного в большом количестве образуются антитела к ДНК, нуклеосомам, кардиолипину, некоторым фракциям комплемента. Первыми в гломерулах обычно осаждаются иммунные комплексы, антигеном в которых являются нуклеосомы, тропные к анионным участкам базальных мембран. В дальнейшем происходит осаждение ЦИК с другими антигенами.
Классификация
В качестве основного критерия систематизации вариантов люпус-нефрита использованы морфологические изменения почечных структур, их распространенность и клинические проявления. Такой подход позволяет максимально точно спрогнозировать течение заболевания и подобрать оптимальную схему лечения. Эксперты ВОЗ различают 6 классов волчаночного нефрита:
- КлассI – мезангиальный нефрит с нормальными клубочками. Морфологические изменения мезангия не выражены, при электронной или иммунофлуоресцентной микроскопии в нем определяются иммунные комплексы. Клиническая симптоматика отсутствует. Наиболее прогностически благоприятный вариант патологии. Пациенты нуждаются в динамическом наблюдении и скрининговых исследованиях для контроля над состоянием почек.
- КлассII – пролиферативный мезангиальный нефрит. Отмечается расширение мезангия, увеличение количества мезангиальных клеток, наличие осажденных ЦИК. В осадке мочи могут выявляться эритроциты, суточная протеинурия не превышает 500 мг. Клинические симптомы поражения почек отсутствуют. Прогноз благоприятный. Базисная терапия предполагает прием блокаторов ангиотензиновых рецепторов, глюкокортикостероидов в низких и средних дозировках.
- КлассIII – пролиферативный очаговый гломерулонефрит. До половины гломерул подверглись эндо- и экстракапиллярной клеточной пролиферации. Участки воспаления сегментарно распределены в паренхиме. Определяется протеинурия и гематурия. Гипертензия, нефротический синдром, повышение концентрации сывороточного креатинина наблюдаются редко. Кроме кортикостероидов назначают цитостатические препараты. Прогноз различный.
- КлассIV – пролиферативный диффузный гломерулонефрит. Иммуновоспалительному некрозу и склерозированию подверглось больше половины гломерул. В клинической картине кроме лабораторных изменений часто выявляется повышение давления, нефротический синдром. Уровень сывороточного креатинина обычно увеличен. Необходима комплексная терапия цитостатиками и стероидами. Прогноз серьезный.
- КлассV – мембранозный гломерулонефрит. Гломерулярная мембрана утолщена. Обнаруживается субэпителиальное и интрамембранозное отложение иммунных комплексов. Преобладает клиника нефротического синдрома, у некоторых больных возможно увеличение АД, появление эритроцитов в моче, изредка повышается уровень креатинина. Рекомендована иммуносупрессорная терапия разными препаратами и ЗПТ. Прогноз сомнительный.
- КлассVI – склерозирующий гломерулонефрит. Склерозировано более 90% клубочковых капилляров. Быстро возникает и нарастает хроническая почечная недостаточность при минимальных изменениях мочевого осадка. Прогноз неблагоприятный. Пациентам требуется раннее назначение заместительной почечной терапии и пересадка почек. Без радикального лечения заболевание переходит в терминальную стадию.
Отечественными специалистами предложена классификация люпус-нефрита с учетом тяжести, особенностей течения и исходов патологического процесса. Быстропрогрессирующую форму аутоиммунного воспаления почек с нефротическим синдромом, злокачественной гипертензией, ранним возникновением ХПН, плохим прогнозом выявляют у 10-12% больных СКВ. Активный нефрит с признаками волчаночного нефротического синдрома обнаруживают у 30-40% пациентов. В 30-33% случаев определяется активный гломерулонефрит, в картине которого преобладает мочевой синдром. У 15-30% больных нефрит протекает латентно и диагностируется только лабораторно.
Симптомы волчаночного нефрита
Заболевание развивается в среднем через год после постановки диагноза СКВ, хотя может быть и единственным висцеральным проявлением волчанки. В 40% люпус-нефрит имеет бессимптомное течение и выявляется лабораторно. В клинике обычно преобладают признаки основной патологии (поражения суставов, характерная эритема, серозиты), к которым присоединяются отеки, локализованные на лице и наиболее выраженные по утрам, уменьшение суточного количества мочи. 2-5% больных отмечают появление видимой примеси крови в моче. При прогрессировании процесса у 60-70% пациентов возникает стойкая артериальная гипертензия с высокими значениями диастолического давления, рефрактерная к традиционным гипотензивным препаратам. Общее состояние зависит от выраженности морфологических изменений, при нефрите легкой степени нарушения отсутствуют, при тяжелом течении нарастают симптомы интоксикации, появляется кожный зуд, сильные головные боли.
Осложнения
Заболевание часто приводит к формированию или обострению сердечно-сосудистой патологии. Наиболее распространенными осложнениями волчаночного нефрита, развивающимися вследствие поражения сосудов при симптоматической артериальной гипертензии с дислипидемией, являются ишемическая болезнь сердца, инсульты. У пациентов могут возникать тяжелые инфекционные процессы (сепсис, некурабельные пневмонии, туберкулез), связанные с резким снижением иммунитета при длительном лечении кортикостероидами и цитостатиками. Нефрит при волчанке повышает риск злокачественной трансформации клеток, в частности – лейкоцитов с развитием В-клеточных лимфом. Почечная недостаточность как исход волчаночного гломерулонефрита обнаруживается у 10-15% больных. У 36% пациентов с быстропрогрессирующим заболеванием наблюдается ДВС-синдром.
Диагностика
Постановка диагноза волчаночного нефрита обычно не представляет сложностей при наличии характерной симптоматики заболевания. Диагностика может быть затруднена, если гломерулонефрит является единственным органным проявлением СКВ. При подозрении на волчаночный генез поражения почек рекомендованы следующие методы исследований:
- Общий анализ мочи. Соответственно клиническому варианту люпус-нефрита в осадке могут определяться эритроциты, лейкоциты, цилиндры. Для всех форм волчаночного гломерулонефрита кроме I класса характерна протеинурия от 200 до 3000-3500 мг белка/сут и более.
- Содержание креатинина в крови. Обычно показатель повышен у пациентов с диффузным пролиферативным люпус-нефритом, реже — при очаговом, мембранозном поражении, склерозирующей форме заболевания. Высокий креатинин служит прогностически неблагоприятным признаком.
- Исследование крови на антитела. Обнаруживается наличие антинуклеарного фактора, антинуклеарных антител, антител к ds-ДНК, нуклеосомам, гистонам. С1q. При проведении анализа применяют иммунофлуоресцентные и иммуногистохимические методы.
- Волчаночный антикоагулянт(LA). Умеренные и высокие показатели теста характерны для сочетания нефрита с антифосфолипидным синдромом. Положительные результаты свидетельствуют о повышенном риске усугубления аутоиммунного воспаления тромботическими процессами.
- Пункционная биопсия почек. Гистологическое исследование биоптата позволяет выявить патогномоничные морфологические изменения тканей. Проводится всем больным с подозрением на люпус-нефрит при измененном общем анализе мочи или повышенном сывороточном креатинине.
В общем анализе крови часто определяется снижение уровня лейкоцитов, эритроцитов, тромбоцитов, ускорение СОЭ. В качестве вспомогательных методов, позволяющих оценить выраженность структурных изменений и функциональную состоятельность почечной паренхимы, могут выполняться УЗИ, КТ, МСКТ, МРТ почек, экскреторная урография, нефросцинтиграфия, комплексное биохимическое исследование крови, нефрологический комплекс, оценка системы гемостаза. Дифференциальная диагностика люпус-нефрита проводится с быстропрогрессирующим и хроническим гломерулонефритом, лекарственной нефропатией, поражениями почек при ревматоидном артрите, других системных заболеваниях соединительной ткани, миеломной болезни, аутоиммунном гепатите, геморрагическом васкулите, первичном и наследственном амилоидозе. По показаниям пациента кроме уролога, нефролога и ревматолога консультирует терапевт, гепатолог, гематолог, онколог, онкогематолог, токсиколог.
Лечение волчаночного нефрита
Основными терапевтическими задачами при ведении пациентов с СКВ, у которых диагностирован специфический гломерулонефрит, являются индукция ремиссии, максимально долгое сохранение функциональной состоятельности паренхимы, профилактика рецидивов и осложнений, улучшение качества жизни и показателей выживаемости. При выборе схемы лечения учитывают активность аутоиммунного процесса, потенциальную обратимость деструктивных изменений, выраженность почечной недостаточности. Больным с неактивным процессом (I класс люпус-нефрита) рекомендован периодический скрининг состояния почек и назначение препаратов для коррекции других клинических проявлений СКВ.
При волчаночном гломерулонефрите II класса терапию начинают с ингибиторов АПФ, оказывающих антигипертензивный и нефропротективный эффекты за счет снижения системного артериального давления без ущерба ренальному кровотоку. Терапевтическая резистентность состояния, нарастание протеинурии, появление признаков гематурии является основанием для дополнительного применения глюкокортикостероидов и имидазольных цитостатиков. Больным с активным люпусным воспалением гломерул III-V класса в качестве базисных назначают иммуносупрессивные лекарственные средства:
- Цитостатические препараты. Являются обязательным элементом индукционного и поддерживающего лечения. При агрессивном течении заболевания предпочтительна пульс-терапия сверхвысокими дозами алкилирующих производных диамидофосфата, которые ингибируют активность B-лимфоцитов. В последующем больных переводят на поддерживающие дозировки имидазольных цитостатиков или селективных производных микофеноловой кислоты.
- Глюкокортикостероиды. В качестве монопрепаратов в настоящее время практически не используются. Эффективно дополняют цитостатическую терапию, обеспечивая более длительное сохранение почечных функций и лучшие показатели выживаемости. Обычно назначаются в низких дозировках и альтернирующих режимах приема. На начальных этапах лечения возможно проведение активной пульс-терапии высокими дозами.
Альтернативными методами ведения больных с терапевтически резистентными вариантами волчаночного гломерулонефрита являются применение ингибиторов кальциневрина, синтетических моноклональных антител к CD20 и CD22-антигенам мембран B-лимфоцитов, антицитокиновых препаратов, молекулярных блокаторов иммунной реакции. Апробируются и внедряются технологии тотального облучения лимфоидной ткани, костного мозга с последующей трансплантацией стволовых клеток.
Симптоматическая терапия люпус-нефрита направлена на коррекцию отдельных клинических проявлений заболевания. При развитии артериальной гипертензии и значительной протеинурии рекомендован прием ингибиторов АПФ или селективных блокаторов рецепторов ангиотензина II. Для устранения возможной дислипидемии используются статины. Пациентам с признаками антифосфолипидного синдрома показаны антикоагулянты и антиагреганты. Нарастание признаков почечной недостаточности, особенно при волчаночных гломерулонефритах V-VI класса, служит основанием для проведения ЗПТ (гемодиализа, перитонеального диализа, гемофильтрации, гемодиафильтрации и др.), а затем трансплантации почки после 3-6-месячного снижения активности аутоиммунного воспаления.
Прогноз и профилактика
Хотя развитие почечной патологии в целом ухудшает прогноз СКВ, при своевременной диагностике и адекватной терапии пятилетняя выживаемость наблюдается у 80-85% больных с тяжелыми формами гломерулонефрита и у 95% с процессами средней тяжести. Первичная профилактика волчаночного нефрита заключается в скрининговых обследованиях пациентов из группы риска по СКВ с целью раннего выявления и назначения комплексного лечения основной патологии, что позволяет снизить вероятность развития поражения почек. Для предупреждения прогрессирования уже имеющегося нефрита необходимо проведение длительной поддерживающей терапии.
1. Лечение волчаночного нефрита с позиций доказательной медицины/ Сущук Е.Л., Торгашина Л.В.// Научно-практическая ревматология. - №6.
2. Патогенез волчаночного нефрита/ Р.М. Стернер, С.П. Хартоно, Д.П. Гранде// Журнал клинической и клеточной иммунологии. – 2004.
3. Волчаночный нефрит: подходы к диагностике и лечению/ Макарова Т. П., Сенек С.А., Фирсова Н.Н., Мрасова В.К., Осипова Н.В., Садыкова Д.И., Ашрафуллина Ч.И.// Практическая медицина. – 2008.
4. Особенности современного течения волчаночного нефрита и факторы риска его прогрессирования: Автореферат диссертации/ Самокишина Н.А. – 2008.
Системная красная волчанка – хроническое системное заболевание, с наиболее выраженными проявлениями на коже; этиология красной волчанки не известна, но ее патогенез связан с нарушением аутоиммунных процессов, в результате чего вырабатываются антитела к здоровым клеткам организма. Заболеванию в большей степени подвержены женщины среднего возраста. Заболеваемость красной волчанкой не велика – 2-3 случая на тысячу человек населения. Лечение и диагностика системной красной волчанки осуществляются совместными усилиями ревматолога и дерматолога. Диагноз СКВ устанавливается на основании типичных клинических признаков, результатов лабораторных анализов.




Общие сведения
Системная красная волчанка – хроническое системное заболевание, с наиболее выраженными проявлениями на коже; этиология красной волчанки не известна, но ее патогенез связан с нарушением аутоиммунных процессов, в результате чего вырабатываются антитела к здоровым клеткам организма. Заболеванию в большей степени подвержены женщины среднего возраста. Заболеваемость красной волчанкой не велика – 2-3 случая на тысячу человек населения.
Развитие и предполагаемые причины системной красной волчанки
Точная этиология красной волчанки не установлена, но у большей части пациентов обнаружены антитела к вирусу Эпштейна-Барр, что подтверждает возможную вирусную природу заболевания. Особенности организма, вследствие которых вырабатываются аутоантитела, также наблюдаются почти у всех больных.
Гормональная природа красной волчанки не подтверждена, но гормональные нарушения ухудшают течение заболевания, хотя спровоцировать его возникновение не могут. Женщинам с диагностированной красной волчанкой не рекомендован прием пероральных контрацептивов. У людей, имеющих генетическую предрасположенность и у однояйцевых близнецов заболеваемость красной волчанкой выше, чем в остальных группах.
В основе патогенеза системной красной волчанки лежит нарушение иммунорегуляции, когда в качестве аутоантигенов выступают белковые компоненты клетки, прежде всего ДНК и в результате адгезии мишенью становятся даже те клетки, которые изначально были свободны от иммунных комплексов.
Клиническая картина системной красной волчанки

При красной волчанке поражается соединительная ткань, кожа и эпителий. Важным диагностическим признаком является симметричное поражение крупных суставов, и, если возникает деформация суставов, то за счет вовлечения связок и сухожилий, а не вследствие поражений эрозивного характера. Наблюдаются миалгии, плевриты, пневмониты.
Но наиболее яркие симптомы красной волчанки отмечаются на коже и именно по этим проявлениям в первую очередь и ставят диагноз.

На начальных стадиях заболевания красная волчанка характеризуется непрерывным течением с периодическими ремиссиями, но почти всегда переходит в системную форму. Чаще отмечается эритематозный дерматит на лице по типу бабочки – эритема на щеках, скулах и обязательно на спинке носа. Появляется гиперчувствительность к солнечному излучению – фотодерматозы обычно округлой формы, носят множественный характер. При красной волчанке особенностью фотодерматозов является наличие гиперемированного венчика, участка атрофии в центре и депигментации пораженной области. Отрубевидные чешуйки, которыми покрывается поверхность эритемы, плотно спаяны с кожей и попытки их отделить, очень болезненны. На стадии атрофии пораженных кожных покровов наблюдается формирование гладкой нежной алебастрово-белой поверхности, которая постепенно замещает эритематозные участки, начиная с середины и двигаясь к периферии.
У некоторых пациентов с красной волчанкой поражения распространяются на волосистую часть головы, вызывая полную или частичную алопецию. Если поражения затрагивают красную кайму губ и слизистую оболочку рта, то очаги поражения представляют собой синюшно-красные плотные бляшки, иногда с отрубевидными чешуйками сверху, их контуры имеют четкие границы, бляшки склонны к изъязвлениям и причиняют боль во время еды.
Красная волчанка имеет сезонное течение, и в осенне-летние периоды состояние кожи резко ухудшается из-за более интенсивного воздействия солнечного излучения.

При подостром течении красной волчанки наблюдаются псориазоподобные очаги по всему телу, ярко выражены телеангиэктазии, на коже нижних конечностей появляется сетчатое ливедио (древоподобный рисунок). Генерализованная или очаговая алопеция, крапивница и кожный зуд наблюдаются у всех пациентов с системной красной волчанкой.
Во всех органах, где имеется соединительная ткань, со временем начинаются патологические изменения. При красной волчанке поражаются все оболочки сердца, лоханки почек, желудочно-кишечный тракт и центральная нервная система.
Если помимо кожных проявлений пациентов мучают периодические головные боли, суставные боли без связи с травмами и погодными условиями, наблюдаются нарушения со стороны работы сердца и почек, то уже на основании опроса можно предположить о более глубоких и системных нарушениях и обследовать пациента на наличие красной волчанки. Резкая смена настроения от эйфоричного состояния до состояния агрессии тоже является характерным проявлением красной волчанки.
У больных красной волчанкой пожилого возраста кожные проявления, почечный и артралгический синдромы менее выражены, но чаще наблюдается синдром Шегрена – это аутоиммунное поражение соединительной ткани, проявляющееся гипосекрецией слюнных желез, сухостью и резью в глазах, светобоязнью.
Дети, с неонатальной формой красной волчанки, родившиеся от больных матерей, уже в младенческом периоде имеют эритематозную сыпь и анемию, поэтому следует проводить дифференциальный диагноз с атопическим дерматитом.
Диагностика системной красной волчанки
Реакция Вассермана может быть ложноположительной, как и другие серологические исследования, что порой приводит к назначению неадекватного лечения. При развитии пневмонии проводят рентгенографию легких, при подозрении на плеврит - плевральную пункцию. Для диагностики состояния сердца - ЭКГ и эхокардиографию.
Лечение системной красной волчанки

Как правило, первоначальное лечение красной волчанки бывает неадекватным, так как ставятся ошибочные диагнозы фотодерматозов, экземы, себореи и сифилиса. И только при отсутствии эффективности назначенной терапии проводятся дополнительные обследования, в ходе которых и диагностируется красная волчанка. Полного излечения от этого заболевания добиться невозможно, но своевременная и корректно подобранная терапия позволяет добиться улучшения качества жизни пациента и избежать инвалидизации.
Пациентам с красной волчанкой нужно избегать прямых солнечных лучей, носить одежду, прикрывающую все тело, а на отрытые участки наносить крема с высоким защитным фильтром от ультрафиолета. На пораженные участки кожи наносят кортикостероидные мази, так как использование негормональных препаратов не приносит эффекта. Лечение необходимо проводить с перерывами, чтобы не развился гормонообусловленный дерматит.
В при неосложненных формах красной волчанки для устранения болевых ощущений в мышцах и суставах назначаются нестероидные противовоспалительные препараты, но с осторожностью следует принимать аспирин, так как он замедляет процесс свертывания крови. Обязателен прием глюкокортикостероидов, при этом дозы препаратов подбираются таким образом, чтобы при минимизации побочных эффектов защитить внутренние органы от поражений.
Метод, когда у пациента делают забор стволовых клеток, а потом проводят иммунодепрессивную терапию, после чего для восстановления иммунной системы вновь вводят стволовые клетки, эффективен даже в тяжелых и безнадежных формах красной волчанки. При такой терапии аутоиммунная агрессия в большинстве случаев прекращается, и состояние пациента с красной волчанкой улучшается.
Здоровый образ жизни, отказ от алкоголя и курения, адекватная физическая нагрузка, сбалансированное питание и психологический комфорт позволяют пациентам с красной волчанкой контролировать свое состояние и не допустить инвалидизации.
Системная красная волчанка (СКВ) – аутоиммунное заболевание, этиология которого остается неизвестной. Кожный синдром при СКВ зачастую имеет первостепенное диагностическое значение – поражение кожи в 20-30% случаев является самым ранним симптомом, а у 60-
Systemic lupus erythematosus: alertness in the practice of a dermatologist / M. M. Tlish, Zh. Yu. Naatyzh1, T. G. Kuznetsova, E. A. Chernenko /State Budgetary educational institution of higher professional education Kuban State Medical University of the Ministry of Healthcare of the Russian Federation, Krasnodar, Russia
Abstract. Systemic lupus erythematosus (SLE) is an autoimmune disease, the etiology of which remains unknown. Skin syndrome in SLE is often of paramount diagnostic value – skin lesion is the earliest symptom in 20-30% of cases, and in 60-70% it manifests itself at various stages of the course of the disease, which leads to the patient's primary referral to a dermatologist. Frequent diagnostic errors are due to the absence of clinical symptoms of systemic lesions in the presence of cutaneous manifestations of lupus erythematosus (LE). In this case, laboratory tests are an integral part of the algorithm for managing patients with LE at the stage of contacting a dermatologist. The most specific laboratory test is the determination of antinuclear antibodies by an indirect immunofluorescence reaction, referred to as antinuclear factor (ANF). An elevated ANF titer is included in the list of diagnostic criteria for SLE, its detection allows one to suggest a diagnosis of SLE and determine a further algorithm for the provision of medical care. The article presents two clinical cases illustrating that against the background of an isolated skin lesion and the absence of visible somatic pathology, abnormalities in immunological tests were identified. This made it possible to suspect the systemic course of the process at an early stage and refer patients to a rheumatologist's consultation, where the diagnosis of SLE was confirmed. For citation: Tlish M. M., Naatyzh Zh. Yu., Kuznetsova T. G., Chernenko E. A. Systemic lupus erythematosus: alertness in the practice of a dermatologist // Lechaschy Vrach. 2020; vol. 23 (11): 23-26. DOI: 110.26295/OS.2020.35.78.005
Согласно современным представлениям, системная красная волчанка (СКВ) – аутоиммунное заболевание неустановленной этиологии, характеризующееся гиперпродукцией органонеспецифических аутоантител с развитием иммуновоспалительного повреждения тканей внутренних органов [1]. Широкий ряд вырабатываемых аутоантител и их прямое или опосредованное воздействие на клеточные мишени обуславливают многообразие клинических проявлений при красной волчанке (КВ) [2]. СКВ может проявляться изолированным или сочетанным поражением систем и органов, включающим поражение кожи и слизистых оболочек (волчаночная бабочка, дискоидная эритема, фотосенсибилизация, алопеция, телеангиэктазии, сетчатое ливедо, язвы в полости рта), сердечно-сосудистой системы (перикардит, миокардит, эндокардит, коронарит), почек (волчаночный нефрит), центральной нервной системы (судороги, психоз), опорно-двигательного аппарата (артралгии, артриты), легких (плеврит, волчаночный пневмонит), гематологическими нарушениями (гемолитическая анемия, лейкопения, тромбоцитопения) и т. д. [3].
Ключевую роль в диагностике СКВ играет обнаружение клинических проявлений заболевания и данные лабораторной диагностики [3]. Кожный синдром при СКВ зачастую имеет первостепенное диагностическое значение – поражение кожи в 20-30% случаев является самым ранним симптомом, а у 60-70% проявляется на различных этапах течения болезни, что приводит к первичному обращению больного именно к дерматологу [4]. Поражения кожи при СКВ полиморфны и представлены различными изменениями – от незначительных телеангиэктазий до буллезных поражений [2]. Выделяют волчаночно-специфичные и волчаночно-неспецифичные поражения кожи, последние встречаются в несколько раз чаще. К волчаночно-специ-фичным относят различные проявления хронической, подострой и острой КВ [5]. Группа неспецифических поражений включает: фотосенсибилизацию, лейкоцитокластический и уртикарный васкулит, телеангиэктазии, сетчатое ливедо, злокачественный атрофический папулез и синдром Рейно [5]. Широкая вариабельность клинических проявлений кожного синдрома обуславливает необходимость проведения тщательного дифференциального диагноза [1].
Важным инструментом ранней диагностики системных заболеваний является обнаружение аутоантител с помощью лабораторных тестов [3]. Наиболее специ-фичными для СКВ являются антинуклеарные антитела (АНА) – это гетерогенная группа аутоантител к компонентам клеточного ядра, среди которых выделяют антитела к двуспиральной дезоксирибонуклеиновой кислоте (ДНК), гистонам, нуклеосомам, экстрагируемым ядерным антигенам, ядрышковым антигенам и другим клеточным структурам [6]. Стандартным методом обнаружения группы АНА является непрямая реакция иммунофлюоресценции (НРИФ) с использованием линии эпителиальных клеток аденокарциномы гортани человека (HЕp-2) [7]. Определение АНА методом НРИФ принято обозначать как антинуклеарный фактор (АНФ), содержание которого оценивается по максимальному выявленному титру в сыворотке крови, с указанием интенсивности и типа флюоресценции [8]. Количественное увеличение титра свыше 1:160 входит в перечень диагностических критериев СКВ согласно рекомендациям Американской коллегии ревматологов (American College of Rheumatology, ACR) и Европейской лиги борьбы с ревматизмом (European League Against Rheumatism, ULAR) и используется для оценки активности процесса, прогноза, так как является предиктором развития СКВ на доклинической стадии [8].
Длительное формирование патогномоничного клинического симптомокомплекса СКВ, отсутствие проведения необходимых лабораторных исследований и междисциплинарного взаимодействия являются причиной частых диагностических ошибок, приводящих к отсутствию своевременной противовоспалительной и иммуносупрессивной терапии у врача-ревматолога. Учитывая вышесказанное, считаем целесообразным привести собственные клинические наблюдения.
Клиническое наблюдение № 1
Данные со стороны других органов и систем: предъявляет жалобы на ноющие боли в мелких суставах кистей и коленных суставах, чувство утренней скованности. Соматически не обследована.
Объективно: кожный патологический процесс носит ограниченный симметричный характер, локализуется на коже крыльев носа, щек, подбородка. Представлен: эритематозные пятна, чешуйки, телеангиэктазии.
На коже лица (в области крыльев носа, щек, подбородка) расположены ярко-розовые эритематозные очаги, с четкими границами, слегка инфильтрированные, правильной округлой формы, диаметром 3-4 см, покрытые небольшим шелушением в центре очагов; в периферической зоне очагов визуализируются телеангиэктазии (рис. 1). Удаление чешуек сопровождается болезненностью (симптом Бенье–Мещерского).
.jpg)
Определена биодоза 20 секунд.
Результаты гистоморфологического исследования кожи из патологического очага на правой щеке: фолликулярный гиперкератоз; эпидермис с тенденцией к атрофии; вакуольная дистрофия клеток базального слоя. Под эпидермисом сосуды расширены. Во всех отделах дермы – густые диффузные и периваскулярные лимфогистиоцитарные инфильтраты с примесью нейтрофилов и плазмоцитов. Вокруг сально-волосяных фолликулов – густой лимфогистиоцитарный инфильтрат с примесью нейтрофилов, тучных клеток и фибробластов, проникающий в наружное эпителиальное влагалище. В дерме – участки мукоидного набухания коллагеновых волокон. Заключение: морфологическая картина может соответствовать красной волчанке.
Данные общеклинических исследований: общий и биохимический анализ крови – показатели в пределах нормы; общий анализ мочи – показатели в пределах нормы.
Настораживающими факторами в плане трансформации кожной формы в системный процесс у пациентки М. явились: дебют заболевания в молодом возрасте, длительная инсоляция в анамнезе, II фототип кожи, биодоза 20 секунд, наличие выраженного суставного синдрома.
Для исключения диагноза СКВ было проведено иммунологическое исследование:
- Антинуклеарный фактор на НЕр-2 клетках: 1:320 титр (норма менее 160); мелкогранулярный тип свечения.
- Антитела к двуспиральной ДНК (a-dsDNA) – 53 МЕ/мл (норма – менее 25 МЕ/мл).
- Анализ крови на антитела к фосфолипидам класса IgG (скрининг) – 10,13 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
- Анализ крови на антитела к фосфолипидам класса IgM (скрининг) – 12,68 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
С полученными данными больная направлена к ревматологу в Краевую клиническую больницу № 2, где был подтвержден диагноз СКВ. Больная взята на диспансерный учет ревматологом для определения дальнейшей тактики ведения и лечения.
Клиническое наблюдение № 2
Объективно: кожный патологический процесс носит распространенный характер, локализован на коже лица, шеи. Представлен: пятна, телеангиэктазии, чешуйки.
На коже лица в области щек, левой околоушной области и шеи расположены отечные эритематозные очаги розовато-красного цвета, диаметром 2–3 см, преимущественно правильно-округлой формы с небольшим шелушением, визуализируются единичные телеангиэктазии. Удаление чешуек сопровождается болезненностью (симптом Бенье–Мещерского) (рис. 2).
.jpg)
Результаты гистоморфологического исследования кожи из патологического очага: на коже левой щеки – фолликулярный гиперкератоз; участки паракератоза; эпидермис местами атрофичен; вакуольная дистрофия клеток базального слоя эпидермиса; подэпидермальные пузыри. В сосочковом слое – отек, стенки сосудов утолщены. В дерме – густые очаговые и периваскулярные лимфогистиоцитарные инфильтраты с примесью нейтрофилов. Вокруг сально-волосяных фолликулов – густой лимфогистиоцитарный инфильтрат с примесью нейтрофилов, тучных клеток и фибробластов, проникающий в наружное эпителиальное влагалище. В дерме – участки мукоидного набухания коллагеновых волокон. Заключение: морфологическая картина больше соответствует красной волчанке.
Данные общеклинических исследований: в общем и биохимическом анализах крови выявлены следующие отклонения – лейкоциты 3,7 × 10 9 /л; холестерин 8,7 ммоль/л.
Учитывая длительность течения кожного патологического процесса, отсутствие результатов обследования смежных специалистов, для исключения диагноза СКВ было проведено иммунологическое исследование:
- Антинуклеарный фактор на НЕр-2 клетках: 12 560 титр (норма менее 160); крупногранулярный тип свечения.
- Антитела к двуспиральной ДНК (a-dsDNA) – 0,5 МЕ/мл (норма – менее 25 МЕ/мл).
- Анализ крови на антитела к фосфолипидам класса IgG (скрининг) 16,65 МЕ/мл (референсные значения: до 10 МЕ/мл – не обнаружено).
- Анализ крови на антитела к фосфолипидам класса IgM (скрининг) – 14,68 МЕ/мл (референсные значения до 10 МЕ/мл – не обнаружено).
Таким образом, иммунологические исследования и их комплексный анализ являются неотъемлемой составляющей алгоритма ведения больных с КВ уже на этапе обращения к врачу-дерматологу и способствуют высокому качеству оказания медицинской помощи данному контингенту больных.
Литература/References
М. М. Тлиш, доктор медицинских наук, профессор
Ж. Ю. Наатыж 1 , кандидат медицинских наук
Т. Г. Кузнецова, кандидат медицинских наук
Е. А. Черненко
ФГБОУ ВО КубГМУ Минздрава России, Краснодар, Россия
Системная красная волчанка: настороженность в практике дерматолога/ М. М. Тлиш, Ж. Ю. Наатыж, Т. Г. Кузнецова, Е. А. Черненко
Для цитирования: Тлиш М. М., Наатыж Ж. Ю., Кузнецова Т. Г., Черненко Е. А. Системная красная волчанка: настороженность в практике дерматолога // Лечащий Врач. 2020; т. 23 (11), 23-26. DOI: 110.26295/OS.2020.35.78.005
Теги: аутоиммунное заболевание, кожный синдром, алгоритм лечения
Диагноз системной красной волчанки (СКВ) в последние десятилетия стал все чаще встречаться в нефрологическом стационаре. Судить о том, насколько актуальна проблема СКВ, можно хотя бы на основании того, что статья
Системная красная волчанка — аутоимунное заболевание, характеризующееся изменениями со стороны клеточного и гуморального иммунного ответа. Фундаментальным нарушением в иммунной системе у больных с СКВ в настоящее время принято считать генетически обусловленный дефект апоптоза (программированной смерти) аутореактивных клонов Т- и В-клеток. В индукции заболевания помимо генетических факторов важную роль играет уровень половых гормонов. Отрицательное влияние эстрогенов подтверждается развитием заболевания преимущественно у женщин детородного возраста, высокой частотой дебюта и/или обострения заболевания после родов и абортов, а также низким уровнем тестостерона и повышенным — эстрадиола у мужчин с СКВ. Среди экзогенных факторов большое значение придается ультрафиолетовому облучению, бактериальным липополисахаридам и различным группам вирусов, активирующих В-клетки, и применению некоторых лекарственных препаратов, в особенности гормональных контрацептивов.
Потеря иммунной толерантности к собственным, в первую очередь ядерным, антигенам приводит к продукции множества комплемент-связывающих аутоантител к компонентам клеточного ядра, цитоплазмы и мембран, в частности к двухцепочечной ДНК и нуклеосомам. Аутоантитела оказывают как прямое повреждающее действие на различные органы и ткани, так и опосредованное — через формирование иммунных комплексов и активацию системы комплемента. Характерно также не только иммунокомплексное, но и тромботическое поражение сосудов, последнее обусловлено наличием антител к кардиолипину, а также развитием антифосфолипидного синдрома (АФС) и вторичного ДВС. Таким образом, системные повреждения имеют смешанный (цитотоксический, иммунокомплексный и тромботический) генез.
Прогрессирующее поражение жизненно важных органов — почек, центральной нервной системы, сердца, легких, системы крови — определяет тяжесть и прогноз заболевания. Поражаются также и другие органы, суставы, серозные оболочки, кожа. Характерной особенностью СКВ является тот факт, что даже через много лет после начала заболевания процесс сохраняет свою активность.
Диагноз устанавливается при наличии четырех и более из следующих клинических и серологических критериев (критерии Американской ревматологической ассоциации, 1982):
Системный характер заболевания и вовлечение почек в патологический процесс именно в период его максимальной активности приводят к тому, что в большинстве случаев в нефрологической клинике приходится сталкиваться с разнообразными экстраренальными проявлениями СКВ (см. таблицу 1). К ним относятся легочные инфильтраты и альвеолярные кровотечения, цереброваскулит и поперечная миелопатия, тромботические поражения сосудов легких, конечностей, кишечника, головного мозга, эндо-, мио- и перикардит, поражения печени, суставов, тромбоцитопения, анемия, лимфоаденопатия, серозиты, разнообразные кожные проявления и другие симптомы. Наибольшее прогностическое значение имеют поражения ЦНС и легких.
Вовлечение центральной и периферической нервной системы при СКВ встречается довольно часто — до 50% случаев. Отмечаются цереброваскулит, двигательные нарушения, моно- и полинейропатия, асептический менингит, острые психозы, цефалгии, дисфория, судороги. Поперечная миелопатия представляет собой хотя и довольно редкое — 1—3%, но прогностически неблагоприятное и плохо поддающееся терапии проявление заболевания.
Поражение легких чаще всего отмечается в виде пульмонита и тромбоэмболии легочной артерии (ТЭЛА). Диффузные альвеолярные кровотечения развиваются менее чем у 2% больных с СКВ, смертность при этой патологии составляет 70—90%.
Большое значение придается в настоящее время антифосфолипидному синдрому. В рамках АФС рассматриваются такие проявления заболевания, как поражения клапанов сердца, тромбозы коронарных артерий, тромботическая легочная гипертензия, пурпура и язвы голеней, синдром Эванса (сочетание гемолитической анемии с тромбоцитопенией), синдром Снеддона (артериальная гипертензия, рецидивирующие тромбозы мозговых артерий и мраморный рисунок кожи).
Среди поражений сердца наиболее часто встречается перикардит (до трети случаев), причем среди пациентов с активной стадией заболевания распространенность перикардита еще выше — он отмечается более чем у половины больных. У некоторых из них перикардит оказывается первым проявлением СКВ. Грозным осложнением является тампонада сердца, встречающаяся, однако, достаточно редко — примерно 1% случаев.
Волчаночный гломерулонефрит (ВГН) представляет собой одно из наиболее серьезных и прогностически значимых проявлений СКВ. Механизм развития люпус-нефрита иммунокомплексный. Связывание антител к ДНК и других аутоантител с базальной мембраной почечных клубочков ведет к активации комплемента и рекрутированию клеток воспаления в гломерулы.
Клинически почечная патология выявляется, по данным разных авторов, у 50—70% больных, а морфологические изменения — еще чаще. Изучение почечных биоптатов больших групп пациентов показало, что вовлечение почек имеет место практически во всех случаях СКВ. Даже при отсутствии мочевого синдрома в биопсийном материале крайне редко не обнаруживаются изменения, особенно при использовании методов иммунофлюоресценции и электронной микроскопии. Помимо собственно ВГН могут развиваться также почечная тромботическая микроангиопатия, тромбозы почечных артерий и вен, обусловленные наличием антифосфолипидных аутоантител, и иммунокомплексные тубулоинтерстициальные повреждения.
Клиническая картина гломерулонефрита (ГН) при СКВ многообразна (см. таблицу 2) и включает в себя практически все выделяемые в настоящее время варианты: минимальный мочевой синдром; выраженный мочевой синдром в комбинации с гипертонией; нефротический синдром (НС), часто сочетающийся с гематурией и гипертонией, и быстро прогрессирующий гломерулонефрит. При этом каких-либо специфических клинических признаков, характерных именно для люпус-нефрита и позволяющих только на основании симптомов поражения почек диагностировать СКВ, нет.
Доминирующим симптомом является протеинурия — до 100% случаев, НС развивается примерно у половины больных. Микрогематурия присутствует почти всегда, но не бывает изолированной; макрогематурия встречается достаточно редко. Преобладают тяжелые формы заболевания, распространенность которых достигает 63%. Артериальная гипертензия зафиксирована в 50% случаев, более чем у половины больных отмечается снижение скорости клубочковой фильтрации, нарушаются также канальцевые функции. Поражение почек часто развивается в начале заболевания, на фоне высокой активности процесса, иногда становится его первым проявлением или возникает в период обострения.
Разнообразны также и морфологические изменения. Имеются характерные для ВГН признаки (фибриноидный некроз капиллярных петель, гиалиновые тромбы, проволочные петли), что в некоторых случаях позволяет поставить диагноз СКВ на основании результатов биопсии почки, но могут обнаруживаться и изменения, свойственные ГН в целом. Согласно отечественной классификации В. В. Серова (1980), выделяют очаговый пролиферативный волчаночный нефрит, диффузный пролиферативный волчаночный нефрит, мембранозный ГН, мезангиопролиферативный ГН, мезангиокапиллярный и фибропластический ГН. Классификация ВОЗ (1995), базирующаяся на данных световой, иммунофлюоресцентной и электронной микроскопии, позволяет выделить шесть классов изменений.
При сопоставлении этих двух классификаций (см. таблицу 3) можно отметить параллели между мезангиопролиферативным гломерулонефритом и II классом и, отчасти, между очаговым пролиферативным волчаночным нефритом и III классом. Класс IV включает в себя диффузный пролиферативный волчаночный нефрит, а также случаи мезангиокапиллярного гломерулонефрита. Класс V соответствует мембранозному нефриту, а VI — фибропластическому.
Частота обнаружения различных морфологических классов варьирует, чаще всего — до 60% случаев — выявляются изменения IV класса, считающегося, по мнению большинства исследователей, прогностически наиболее неблагоприятным. Помимо морфологического типа отрицательное прогностическое значение имеют нарушение функции почек, артериальная гипертензия, выраженная гематурия, а также мужской пол, высокие титры антител к ДНК, низкий уровень комплемента, анемия, тромбоцитопения и наличие полисерозита.
Течение заболевания и прогноз при СКВ вообще и при ВГН в частности в настоящее время не могут рассматриваться вне связи с результатами лечения. За последние 40 лет прогноз заболевания существенно улучшился (см. таблицу 4). Пятилетняя актуариальная выживаемость увеличилась почти в два раза как при СКВ в целом, так и при ВГН. При ВГН с изменениями IV класса динамика еще более яркая. Если 30 и более лет назад выживаемость пациентов с ВГН IV класса редко превышала один-два года, то в последующем пятилетняя актуариальная выживаемость возросла более чем в четыре раза.
Эффективность терапии высокими дозами КС в сочетании с ЦС при ВГН, в том числе с изменениями IV класса, показана во множестве работ и контролированных исследований. Преимущества терапии комбинацией ЦФ с преднизолоном, по сравнению с монотерапией ПЗ у больных с пролиферативным ВГН, наглядно подтверждены показателями почечной выживаемости.
В заключение хочется еще раз подчеркнуть, что проблема диагностики и лечения СКВ весьма актуальна не только для ревматологии и нефрологии, но и для других, на первый взгляд далеких от нее областей медицины. Пациентов с СКВ нередко длительное время обследуют и лечат с различными диагнозами амбулаторно или госпитализируют в инфекционные, неврологические, гинекологические, туберкулезные и другие стационары, из-за чего больные не получают своевременно адекватного лечения. Между тем современная иммуносупрессивная терапия может радикально изменить их судьбу. В связи с этим необходимо еще раз напомнить врачам различных специальностей, что системная красная волчанка — это не так уж редко встречающееся, грозное, опасное для жизни заболевание, требующее своевременной диагностики и лечения.
Е. В. Захарова
ГКБ им. С. П. Боткина, Москва
Читайте также:

