Что такое врожденный кандидоз
Обновлено: 12.05.2024
Кандидозные вульвовагиниты у девочек. Кандидозный сепсис и внутриутробный кандидоз
Кандидозные вульвовагиниты у девочек встречаются нередко, особенно в грудном возрасте, и характеризуются появлением творожистоподобных налетов на отечной слизистой оболочке преддверия, малых половых губ и около клитора. При восходящей инфекции в первую очередь возникают уретриты, в ряде случаев возможно развитие кандидозного цистита и пиелонефрита. При этом в содержимом мочевых путей и в гнойно-некротических очагах поражения выявляется псевдомицелий гриба.
В результате попадания элементов гриба в кровяное русло при различных изолированных системных кандидозах может возникнуть генерализация кандидоинфекции с образованием метастазов в различных органах, т. е. развивается кандидозный сепсис. При этом может развиться поражение головного мозга в виде кандидозного менингоэнцефалита, возникают метастатические абсцессы в почках, печени, селезенке, легких и других органах. Описаны кандидозные эндокардиты, миокардиты и перикардиты. При гистологическом исследовании в центре метастатических очагов, как правило, имеется разной степени выраженности некроз ткани с радиарно располагающимися нитями псевдомицелия и дрожжеподобными клетками, по периферии этого очага определяются нейтрофильные лейкоциты.
Другой формой генерализованного кандидоза у детей является хронический гранулематозпый кандидоз, характеризующийся образованием туберкулоподобных гранулем во внутренних органах. В основе этого заболевания лежит генетически обусловленная дисфункция фагоцитарных клеток. Установлено, что у больных хроническим кандидозом иейтрофилы обладают нормальной фагоцитарной активностью, по не способны уничтожить С. albicans, при этом выявлено отсутствие мислопероксидазы в лейкоцитах. В. Е. Пигаревский (1975) высказывает предположение, что развитие хронического кандидоза может быть обусловлено дефицитом другого важного противогрибкового и антибактериального фактора в лейкоцитах — катионных гранулярных белков. Снижение переваривающей способности отмечается также и у моноцитов. В макрофагах, эпителиоидных и гигантских многоядерных клетках отмечается вегетация С. albicans.
Внутриутробный кандидоз
Инфицирование плода грибами рода Candida может происходить трансплацентарным или восходящим путем при наличии у беременной женщины влагалищного кандидоза. В эксперименте показано, что грибы могут попадать в околоплодную жидкость, прорастая хорион. Гематогенным путем грибы попадают в организм плода из крови матери через плаценту.
Внутриутробный кандидоз может проявляться изолированным поражением органов дыхания, желудочно-кишечного тракта, головного мозга в связи с тропностью грибов рода Candida к богатой гликогеном мозговой ткани плода. Результатом гематогенной диссеминации возбудителя являются генерализованные формы внутриутробного кандидоза, при которых наблюдается преждевременное прерывание беременности и возможна внутриутробная гибель плода.
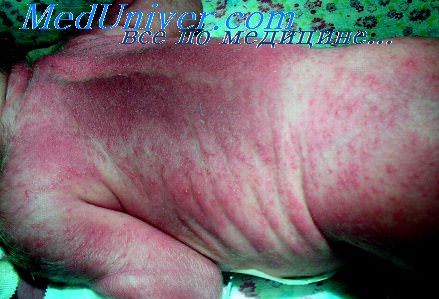
Для внутриутробного генерализованного кандидоза характерным является поражение кожи, ЦНС и внутренних органов (легких, слизистой оболочки пищевода, печени, селезенки, почек, надпочечников) с образованием специфических продуктивно-некротических гранулем.
Особенно тяжелые изменения возникают при внутриутробном поражении головного мозга. В этих случаях мягкие мозговые оболочки мутные, белесоватые. Периваскулярно определяются милиарные беловато-желтые очажки — гранулемы, в центре которых имеются дрожжеподобные клетки и псевдомицелий гриба. В веществе мозга вблизи сосудов также обнаруживаются гранулемы, состоящие из элементов гриба и пролиферирующих клеток глии. В артериях и венах мягких мозговых оболочек и головного мозга выявляются элементы гриба. Периваскулярно обнаруживаются макрофагальные инфильтраты в виде муфт.
Характерным для внутриутробного кандидоза является поражение субэпендимарных отделов желудочков головного мозга, особенно боковых. Эпендима желудочков тусклая, шероховатая, с беловато-желтыми или грязно-серыми подушковидными наложениями. При гистологическом исследовании в этих участках определяются некроз, элементы гриба и гранулематозная ткань. Типичны перифокальные изменения в виде резко выраженной дилатации сосудов и кровоизлияний. В результате кровоизлияний и очагового некроза может развиться ложная порэнцефалия.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Инвазивный кандидоз – тяжелая грибковая инфекция, вызванная грибами рода Candida, которая может проявляться кандидемией и/или вовлечением в процесс любых органов и систем ребенка [14, 29].
Этиология и патогенез
Candida spp. – одноклеточные дрожжеподобные грибы. Образуют псевдомицелий и мицелий. В настоящее время известно более 150 видов грибов рода Candida, среди которых основное значение, как возбудители кандидоза, имеют не более 10 видов (C.albicans, C.parapsilosis, C. lusitaniae, C. tropicalis и др.)[1, 35, 36].
Candida spp. – естественные обитатели кожи и слизистых оболочек человека. Грибковая инфекция возникает при локальных и системных нарушениях противоинфекционной защиты организма человека [26].
При эндогенном пути инфицирования происходит адгезия грибов на поверхности кожи и/или слизистых оболочках, которая сопровождается инвазией в поверхностные слои покровных тканей с поражением стенки лимфатических и кровеносных сосудов, что приводит к гематогенному (при иммунодефицитных состояниях - и лимфогенному) распространению микроорганизмов с последующей генерализацией инфекционного процесса и диссеминацией в ткани внутренних органов [1, 5, 21, 26, 28]. Может быть и негематогенный путь распространения, например, через слизистую оболочку ЖКТ в брюшную полость.
Экзогенный путь передачи грибов - через контаминированный хирургический инструментарий, внутрисосудистые катетеры, дренажи, при нарушении техники проведения парентерального питания [35]. В последние годы у недоношенных детей, получающих лечение в условиях ОРИТ, наряду с кандидозом стали выявлять случаи инфекций, связанных с оказанием медицинской помощи, вызванных другими дрожжеподобными грибами (Malassezia spp., Rhodotorula spp. и др.) [9, 13, 25].
Эпидемиология
По данным экспертной группы Российской ассоциации специалистов перинатальной медицины (РАСПМ) частота инвазивного кандидоза (ИК) у новорожденных в структуре инфекционно-воспалительных заболеваний составляет от 15 до 30%.
Частота возникновения ИК у новорожденных обратно пропорциональна сроку гестации и массе тела при рождении и составляет от 2,6% до 3,1% у новорожденных с очень низкой массой тела (ОНМТ) и от 10% до 16% у новорожденных с экстремально низкой массой тела (ЭНМТ) [7, 9, 19, 27]. В 10% случаев грибы рода Candida являются причиной нозокомиального сепсиса у детей с ЭНМТ при рождении, находящихся на лечении в условиях отделения реанимации и интенсивной терапии новорожденных (ОРИТН) [23].
Среди пациентов с ЭНМТ при рождении летальность на фоне ИК составляет 34% в сравнении с 14% у данной категории пациентов без ИК [38].
Показатель летальности при кандидемии составляет 20-40%, кандидозном менингите – 50%, а при поражении двух и более органов и/или систем данный показатель может увеличиваться до 57% [13, 15, 31, 38].
По данным литературы, кандидемию выявляют у 37-50% детей в сочетании с кандидозным менингитом [29, 31]. Частота изолированного кандидозного менингита при развитии инвазивного кандидоза у новорожденных достигает 10-20% [29].
Поражение почек диагностируют у 10-35% новорожденных на фоне кандидемии. Поражение почек как правило сопровождается кандидурией и, в ряде случаев, развитием почечной недостаточности [13, 17, 29].
Клиническая картина
Cимптомы, течение
Основными факторами риска развития инвазивных микозов у новорожденных являются [1, 9, 14, 21, 22, 28, 29, 30]:
1. Недоношенность (малый вес при рождении (менее 1000г) и малый гестационный возраст (менее 27 недель)
4. Терапия антимикробными препаратами широкого спектра действия, особенно цефалоспоринами третьего поколения и карбапенемами
9. Наличие кандидозной инфекции у матери во время настоящей беременности и родов.
К поверхностным кандидозам относят: кандидоз желудочно-кишечного тракта (ЖКТ) - кандидозный стоматит, глоссит, хейлит, гингивит, кандидоз верхних дыхательных путей, интертригинозный (пеленочный дерматит).
Клинические проявления поверхностного кандидоза зависят от локализации очага поражения. Поражение кожи может выглядеть как интертригинозный или пеленочный дерматит, наиболее характерный для новорожденных. Поражение слизистой оболочки наиболее часто происходит в ротовой полости (молочница). Клиническая картина развивается чаще всего на 5-14 день жизни. Помимо молочницы возможно развитие стоматита, глоссита, хейлита и гингивита [6, 16, 17].
Диагностика
- использования антибактериальных, гормональных, цитостатических препаратов. Необходимой также является информация о том, выполнялись ли бактериологические посевы матери во время беременности и о полученных результатах.
При подозрении на грибковую инфекцию необходимо проводить осмотр новорожденного в родильном блоке и в неонатальных отделениях (реанимация и интенсивная терапия, патология новорожденных, хирургия новорожденных) на наличие клинических проявлений кандидоза в виде поражений кожи и слизистых оболочек, признаков инфекционного токсикоза (бледность, сероватый колорит кожных покровов, и др.), диспептических расстройств (вздутие живота, ослабление перистальтики, нарушение усвоения энтерального питания), признаков нарушения мочеотделения (олиго - и/или анурия), дыхательных нарушений (бради - и/или тахипноэ, апноэ, лабильность сатурации, нарастания потребности в кислороде, потребности в проведении респираторной терапии) и гемодинамических расстройств (тахи - и/или брадикардия, артериальная гипотензия), наличие желтухи, гепатоспленомегалии.
б) При подозрении на развитие кандидоза мочевыделительной системы необходимо осуществить посев мочи, собранной через стерильный мочевой катетер.
г) При выявлении кандидемии следует исключить поражение почек и ЦНС. При подозрении на развитие инвазивного кандидоза ЦНС – необходимо проведение люмбальной пункции с последующим культуральным исследованием СМЖ.
Посевы крови, СМЖ, асцитической и плевральной жидкостей производят с использованием флаконов с жидкой питательной средой для культивирования в автоматических гематологических анализаторах. При наличии в лаборатории масс-спектрометра рекомендуется проведение прямой идентификации грибов из положительной гемокультуры методом MALDI-TOF-MS анализа, при отрицательном результате осуществление высева на плотные питательные среды с последующей биохимической или MALDI-TOF-MS идентификацией выросших колоний грибов [11, 12, 14]. Для видовой дифференцировки видов грибов допускается использование хромогенных сред (различные виды грибов образуют на поверхности питательного агара колонии различных цветов). Окраска колоний зависит от производителя питательной среды, оценку видовой принадлежности грибов проводят в соответствии с инструкцией производителя.
Колонизация нескольких локусов (3-х и более) – является независимым фактором риска и предиктором прогрессирования для грибкового сепсиса (Manzoni P. 2006).
д) При выявлении кандидемии следует исключить поражение почек и ЦНС. При подозрении на развитие инвазивного кандидоза ЦНС – необходимо проведение люмбальной пункции с последующим культуральным исследованием СМЖ [37]. Посевы крови, СМЖ, асцитической и плевральной жидкостей производят с использованием флаконов с жидкой питательной средой для культивирования в автоматических гематологических анализаторах. При наличии в лаборатории масс-спектрометра рекомендуется проведение прямой идентификации грибов из положительной гемокультуры методом MALDI-TOF-MS анализа, при отрицательном результате осуществление высева на плотные питательные среды с последующей биохимической или MALDI-TOF-MS идентификацией выросших колоний грибов [11, 12, 13, 14].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
б) Методики определения 1,3 –b-D-глюкана и антител против ростовых трубок C. albicans (CAGTA) в настоящее время проходят процесс регистрации в РФ и не могут быть использованы в клинической практике [1].
а) Компьютерная томография головного мозга, легких и/или органов брюшной полости высокого разрешения.
Н.В. БЕЛОБОРОДОВА, доктор медицинских наук, профессор, главный научный сотрудник академической группы академика РАМН Ю.Ф. Исакова.
При участии Ж.И. АРХИПОВОЙ, кандидата медицинских наук, НИИ детской гематологии. Серьезные экологических изменения, происходящие на планете в последние десятилетия, не могли не сказаться на состоянии микроэкологии и иммунореактивности современного человека.
В этом - одна из глобальных причин роста грибковых заболеваний, которыми сегодня, по данным Всемирной организации здравоохранения, страдает каждый пятый житель планеты. Чаще проявлениями грибковых заболеваний являются различные локальные поражения кожи, ногтей, слизистых оболочек полости рта, кишечника, уретры и влагалища, однако при серьезных нарушениях иммунореактивности организма может наступить генерализация процесса, и тогда грибковые заболевания приобретают жизнеугрожающий характер.
На фоне достижений современной медицины, увеличения продолжительности жизни наиболее ослабленных больных (глубоконедоношенные дети, пациенты с опухолями и иммунодефицитами) в лечебных учреждениях наблюдается широкое распространение инвазивных микозов, которые составляют до 12% в этиологической структуре внутрибольничных инфекций и до 40% в структуре инфекционной летальности. Ученые из Центра контроля заболеваемости (Атланта, США) называют кандидоз внутрибольничной эпидемией последнего десятилетия, так как заболеваемость им иммунокомпрометированных больных возросла в 11 раз.
Колонизация слизистых грибами Candida у практически здоровых людей колеблется от 15 до 40% и может возрасти до 80% на фоне какой-либо патологии в условиях длительной госпитализации, но инвазивный микоз у них не развивается благодаря большому количеству защитных механизмов против грибковой инфекции. Защитные механизмы, не связанные с иммунной системой, включают барьеры в виде кожи и слизистых, а также конкурентные взаимодействия с нормальными бактериями, которые обеспечивают защиту от кандидоза и других микозов посредством соревнования за пищу и, возможно, посредством локальной продукции веществ с антифунгальной активностью. Само по себе разрушение барьеров химической травмой, ожогом или операцией, как и нарушение нормального биоценоза кишечника после длительного применения антибиотиков широкого спектра действия, крайне редко приводит к развитию системного микоза, но вызывает предпосылки для этого в виде локального избыточного накопления грибов в тех местах, где действие физиологических барьеров нарушено.
Общеизвестными факторами риска возникновения грибковой инфекции являются длительная антибиотикотерапия и снижение защитных сил организма. В нормальном организме нейтрофилы, макрофаги и эозинофилы фагоцитируют и убивают бластоспоры кандид, а альвеолярные макрофаги и нейтрофилы способны блокировать прорастание спор аспергилл. Нейтрофилы и моноциты уничтожают также псевдогифы Candida и гифы Aspergillus. Поэтому первыми кандидатами на развитие диссеминированного кандидоза и аспергиллеза являются больные с количественными и функциональными дефектами нейтрофилов, особенно в условиях депрессии Т-клеточного звена иммунной сиcтемы. К специфическим условиям относится лекарственная нейтропения на фоне лечения цитостатиками, особенно глубокая (14 дней нейтрофилы
У пациентов с онкогематологическими заболеваниями к появлению специфических факторов риска инвазивного микоза приводит терапия. На современном этапе она обязательно включает мощные цитостатики, глюкокортикоиды и антибиотики широкого спектра действия. Помимо возникновения нейтропении цитостатики приводят к разрушению кожных и слизистых барьеров, глюкокортикоиды угнетают Т-лимфоциты и макрофаги, антибиотики нарушают биоценоз кишечника. Неудивительно, что в онкогематологических стационарах инвазивные микозы становятся все возрастающей проблемой.
Барьер №1 - конкурентное взаимодействие грибов с бактериями нормальной микрофлоры хозяина
Барьер №2 - целостность кожи и слизистых
Барьер №3 - фагоцитоз и иммунологические реакции
Основные факторы, способствующие разрушению барьеров
№1 - неадекватная (избыточная) антибиотикотерапия
№2 - повреждение эпителия (механическое, токсическое, воспалительное), замедление регенерации, авитаминоз
№3 - снижение иммунореактивности под влиянием цитостатиков, стероидных гормонов
Еще в 80-е годы грибковые инфекции возникали в основном на фоне длительной госпитализации, продолжительной антибиотикотерапии и повторных курсов химиотерапии. Средняя продолжительность периода от момента установления диагноза онкогематологического заболевания до развития грибкового осложнения составляла 19 месяцев. В настоящее время все чаще грибковые инфекции стали наблюдаться на ранних этапах лечения цитостатиками. Это связано как с агрессивностью режимов полихимиотерапии, так и с широким применением современных супермощных антибиотиков.
Важно отметить, что инвазивные грибковые поражения могут развиваться не только у больных при явнымх дефектах иммунореактивности, но и у пациентов с любыми хирургическими заболеваниями в случае осложненного течения послеоперационного периода, реанимационных мероприятий, интенсивной терапии, длительной искусственной вентиляции легких. Мы наблюдали таких пациентов после тяжелых комбинированных травм, после повторных операций по поводу абдоминального сепсиса, после кардиохирургических, нейрохирургических операций и др. В этих случаях предрасполагающим моментом является совокупность факторов, снижающих барьерную функцию слизистых оболочек (стресс, нарушения гемодинамики, гипоксия, длительная невозможность энтерального питания и др.) в сочетании с массивной комбинированной антибиотикотерапией, к сожалению, необходимой у больных высокого риска по жизненным показаниям. Забегая вперед, следует отметить, что даже при выделении грибов из крови или очагов инфекции при проведении целенаправленной противогрибковой терапии у таких пациентов не представляется возможным отказаться от одновременного введения антибиотиков в связи с высокой опасностью септического шока.
Самым частым видом микоза является кандидоз. В списке возбудителей кандидоза лидирующее место занимает Candida albicans. Этим видом грибов вызывается более 80% кандидозов. Однако инфекция может быть вызвана и другими видами: С. tropicalis, С. parapsilosis, С. krusei, С. lusitaniae, Torulopsis glabrata.
Кандидоз в зависимости от степени поражения может быть классифицирован как поверхностный и глубокий. Поверхностный кандидоз включает кожный, орофарингеальный, мочеполовой и характеризуется поражением соответствующих слизистых. Наиболее опасен глубокий кандидоз, составляющий основной спектр кандидозных инфекций у иммунокомпрометированных больных, который может быть классифицирован как фунгемия, диссеминированный кандидоз и кандидоз отдельных органов.
Инвазивное кандидозное поражение желудочно-кишечного тракта (ЖКТ). Считается общепризнанным, что ЖКТ является основным эндогенным резервуаром Candida, откуда происходит проникновение грибов в кровь (феномен транслокации) и последующее распространение инфекции по организму. Однако у больного с агранулоцитозом локальное поражение ЖКТ грибами рода Candida не ограничивается хорошо описанной в литературе ролью "ворот" для диссеминации, а само по себе может вызвать жизнеугрожающие состояния: прогрессирование поражения быстро приводит к множественной инфильтрации или некрозам всей толщи стенки пищеварительного канала, вызывая такие тяжелые осложнения, как кишечная непроходимость, перитонит, желудочно-кишечное кровотечение, вплоть до летального исхода.
Поражение легких. Грибы рода Candida часто высеваются из респираторных секретов, однако клиническое значение таких высевов в большинстве случаев невелико, так как колонизация ротовой полости и верхних дыхательных путей приводит к контаминации мокроты. Более того, легочная инфекция грибами Candida обычно возникает в результате гематогенного распространения, и мокрота у таких больных не отделяется вовсе. Симптомы кандидозной пневмонии схожи с клиническими проявлениями бактериальной пневмонии, но носят более непостоянный характер. Обращает на себя внимание несоответствие выраженных нарушений дыхания скудным аускультативным и рентгенологическим признакам. Рентгенологические нарушения могут ограничиваться изменениями корня и усилением сосудистого рисунка, почти в половине случаев наблюдается рентгенонегативная кандидозная пневмония. В финале заболевания может развиться диссеминация по обоим легочным полям. Рентгенологически этот процесс характеризуется появлением множественных "мигрирующих" облаковидных теней. Сегодня для диагностики поражения легких у иммунокомпрометированных больных наиболее широко используется бронхоальвеолярный лаваж с последующим микробиологическим исследованием.
Поражение кожи встречается в 5-10% случаев острого диссеминированного кандидоза. Классически оно имеет вид плотных, приподнимающихся над поверхностью узлов 0,5-1 см в диаметре, розово-красного цвета, не исчезающих при надавливании. Однако у большинства больных изменения на коже представляют собой просто папулезную или пятнисто-папулезную сыпь, часто неотличимую от медикаментозной.
Изменения на коже и инфильтраты мягких тканей часто становятся информативным материалом для идентификации возбудителя, так как поверхностное расположение делает их удобными для биопсии. Сочетание посева с гистологическим исследованием значительно увеличивает этот показатель. Следует иметь в виду, что поражения кожи при кандидозе затрагивают дерму, в то время как поверхностный слой эпидермиса остается интактным, поэтому клиницист должен быть очень внимателен при заборе материала. При гистологическом исследовании обычно находят псевдомицелий грибов, фибрин и небольшие геморрагии в сочетании с отеком стенки сосудов и периваскулярной ткани.
Поражение ЦНС. Кандидозный менингит встречается относительно редко, наиболее характерен для новорожденных и недоношенных детей, а также как вторичное осложнение при шунтирующих нейрохирургических вмешательствах. В случае развития у имунокомпрометированных больных имеет исключительно агрессивное течение. Поражение оболочек головного мозга характеризуется достаточно ярко выраженными общемозговыми и менингеальными симптомами, а также нейтрофильным или лимфоцитарным плеоцитозом в ликворе - в зависимости от степени нейтропении. Candida имеет низкую высеваемость из ликвора, при морфологическом исследовании ликвора друзы гриба или псевдомицелий обнаружить, как правило, не удается, клинические симптомы (лихорадка, головная боль) не специфичны, поэтому грибковая природа менингита у больных с нейтропенией редко распознается при жизни. Внутримозговые абсцессы, связанные с Candida, могут вызывать очаговую неврологическую симптоматику, соответствующую их локализации.
Поражение сердца. Клиника кандидозного эндокардита не отличается от клиники бактериального, сопровождается длительной лихорадкой и формированием вегетаций на клапанах сердца. Особенностью этой локализации является частое сочетание с фунгемией: хотя бы однократный высев Candida из крови имеют до 80% больных кандидозным эндокардитом. На фоне иммунодефицита могут развиваться грибковые микроабсцессы в миокарде, что иногда проявляется аритмиями. Возможна закупорка грибковыми тромбоэмболами кардиальных артерий с развитием ишемии и сердечной недостаточности.
Хронический диссеминированный кандидоз (ХДК). Наиболее важный маркер ХДК - поражение печени и селезенки. Именно микроабсцессы в этих органах определяют хронический характер течения болезни. Термины "ХДК" и "гепатолиенальный кандидоз" в литературе являются синонимами. Клинически ХДК проявляется увеличением печени и селезенки на фоне длительной лихорадки. Иногда заболевание сопровождается желтухой или болями в правом подреберье. В крови отмечаются высокий лейкоцитоз и выраженная гипербилирубинемия (в основном за счет прямой фракции) в среднем у половины больных. Уровень трансаминаз повышается непостоянно и не более, чем в 3 раза. Наблюдения позволяют сказать, что в целом у большинства больных поражение печени грибами выглядит как холестатический гепатит. Такая особенность приводит к тому, что ХДК часто ошибочно принимается за токсическое поражение цитостатиками, особенно при отсутствии характерных изменений на УЗИ. Кандидозные микроабсцессы в паренхиматозных органах выглядят при ультразвуковом исследовании и компьютерной томографии как гипоэхогенные очаги, поэтому многие клиницисты считают обнаружение этих характерных изменений диагностическим критерием, подтверждающим инвазивную грибковую инфекцию.
Кандидемия. Многие авторы утверждают, что Candida spp., высеянная из крови, редко является контаминантом и должна быть принята во внимание как патоген практически во всех случаях. Фунгемия обнаруживается примерно в 30% случаев диссеминированного кандидоза и имеет важное диагностическое значение, так как служит основным прижизненным доказательством инвазивного кандидоза. Повторная (стойкая) кандидемия может быть результатом инфицирования центрального венозного катетера или проявлением деструктивного поражения глубоких тканей.
С момента возникновения проблемы грибковых инфекций в 60-70-е гг. огромные усилия медиков всего мира были направлены на разработку методов диагностики этих опасных осложнений, так как ранняя диагностика остается основным критическим моментом, определяющим успех в ведении больного с инвазивной инфекцией. Однако до настоящего времени от 20 до 75% случаев инвазивных микозов диагностируется лишь на аутопсии.
Кроме классических микробиологических методов серьезным подспорьем в лабораторной диагностике сегодня является определение маркеров кандидоза - Д-арабинитола и маннозы - методом газовой хроматографии. Даже при трудной локализации очага, недоступного для биопсии и посева, обнаружение высокого уровня маркеров в крови или спинномозговой жидкости позволяет подтвердить диагноз кандидоза, кроме того, в динамике объективно оценить эффект противогрибковой терапии.
Профилактика и лечение. Широко распространено мнение о необходимости одновременно с антибиотиками принимать нистатин, что гарантирует от грибковых осложнений. Действительно, нистатин препятствует массивному размножению кандид на слизистых ЖКТ. Однако крайне важно учитывать, что этот препарат не всасывается при приеме внутрь, то есть не способен воздействовать на клетки грибов, находящиеся вне просвета кишечника. Поистине революционным событием в этиотропной терапии кандидоза следует считать появление препарата флуконазола, наиболее известного под торговым названием дифлюкан. Хорошая биодоступность препарата обеспечивает высокую эффективность практически при любой локализации процесса - от распространенных кожных поражений до менингита. Почти всегда рекомендуется прием препарата внутрь за исключением редких случаев крайне тяжелого состояния больного, когда препарат вводят внутривенно. Благодаря отсутствию токсичности и низкой частоте побочных реакций флуконазол применяется даже у недоношенных детей. Очень важно правильно соблюдать режимы дозирования (см. табл.).
| Пациенты | Показания и дозы флуконазола | ||
| Новорожденные и дети раннего возраста | кандидоз кожи и слизистых 5-6 мг/кг 1 раз в день 5 дней | грибковый сепсис 10 мг/кг 1 раз в день 10-14 дней | грибковый менингит 15 мг/кг 1 раз в день 10-14 дней |
| Взрослые | кандидоз кожи и слизистых 50 мг 1 раз в день 5 дней | вагинальный кандидоз 150 мг однократно (!) | кандидемия, диссеминированный кандидоз 200-400 мг 1 раз в день 2-4 недели |
Когда терапия флуконазолом не дает эффекта, следует думать о кандидозе, вызванном природно резистентными видами кандид, например C.krusei. В этих случаях рекомендуется противогрибковая терапия эффективным, но потенциально токсичным препаратом амфотерицин В (относительно менее высокой токсичностью характеризуется препарат с торговым названием фунгизон). Лечение проводится только в стационаре под тщательным лабораторным контролем. Дозы амфотерицина В из-за опасности нефротоксических реакций не должны превышать 0,5-1 мг/кг в сутки внутривенно один раз в день или через день. При наличии микроабсцессов в печени, головном мозге и других органах наиболее эффективными являются липосомальные формы амфотерицина В (амфоцил и др.), которые, однако, малодоступны из-за высокой стоимости.
Таким образом, в настоящее время актуальность своевременной диагностики и раннего лечения кандидоза чрезвычайно высока.
Что такое вагинальный кандидоз (молочница)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Соснина А. С., гинеколога со стажем в 15 лет.
Над статьей доктора Соснина А. С. работали литературный редактор Вера Васина , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Вагинальный кандидоз (кандидозный вагинит) — поражение слизистой оболочки влагалища дрожжеподобными грибами рода Candida. В быту эту болезнь называют молочницей .
Краткое содержание статьи — в видео:
Candida — это условно-патогенные микроорганизмы, факультативные анаэробы (организмы, способные жить как в присутствии кислорода, так и без него). Они обладают тропизмом — направлением роста на клетки богатые гликогеном, в частности клетки слизистой оболочки влагалища. Самый распространённый вид возбудителя, который встречается в 70—90 % случаев, — Candida albicans.
В последние годы растёт заболеваемость кандидозом, вызванным другими представителями рода Candida. Наиболее часто выявляются:
- С. glabrata (15 %);
- C. dubliniensis (6 %);
- C. tropicalis (3—5 %);
- C. parapsilosis (3 %);
- C. krucei (1—3 %).
Распространение новых видов микроорганизмов связано в первую очередь с бесконтрольным самолечением пациенток, приводящем к возрастающей устойчивости грибов к препаратам [3] [4] .
Частота кандидозного вагинита среди инфекционных заболеваний влагалища и вульвы составляет 30—45 %. Патология занимает второе место среди всех инфекционных заболеваний влагалища и является крайне распространённым поводом для обращения женщин за медицинской помощью. По данным J. S. Bingham (1999):
- к 25 годам около 50 % женщин репродуктивного возраста сталкивались с хотя бы одним диагностированным врачом эпизодом вагинального кандидоза;
- к началу периода менопаузы — около 75 % [17] .
Кандидозный вагинит редко наблюдается в постменопаузе, за исключением тех пациенток, которые получают гормональную заместительную терапию.
Предрасполагающими факторами заболевания являются:
- Механические — ношение синтетического белья, первый половой контакт, травматическое повреждение тканей влагалища, длительное применение внутриматочной спирали.
- Физиологические — беременность, менструация.
- Эндокринные — гипотиреоз, сахарный диабет.
- Иммунодефицитные состояния.
- Ятрогенные (приём антибиотиков, кортикостероидов, иммуносупрессоров, лучевая терапия, химиотерапия, онкологические заболевания, оральные контрацептивы).
- Прочие (авитаминоз, аллергические заболевания, хронические патологии гениталий и желудочно-кишечного тракта).
Заболевание, как правило, не передаётся половым путём, но установлено, что оно связано с характером половых контактов: анально-вагинальным и орогенитальным. Также не исключается вероятность развития кандидозного баланопостита у половых партнёров пациенток с вагинальным кандидозом.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы вагинального кандидоза
Основные симптомы при вагинальном кандидозе:
- жжение и зуд в области влагалища и вульвы;
- творожистые выделения из влагалища;
- расстройства мочеиспускания;
- боль при половом акте.
Зуд может усиливаться после водных процедур, полового акта, ночью во время сна и в период менструации [1] .
В целом симптомы вагинального кандидоза нарастают перед менструацией. При беременности проявление болезни также усугубляется, это связано со снижением иммунитета у беременных женщин.
Объективные признаки вагинального кандидоза:
- отёк и гипермия слизистой оболочки влагалища и наружных половых органов;
- белые или зеленовато-белые наложения на стенках влагалища;
- покраснение слизистой влагалища.
При осложнённом кандидозе на коже наружных половых органов появляются везикулы — пузырьки, возвышающиеся над уровнем кожи или слизистой и заполненные прозрачным или мутным содержимым, которые могут вскрываться и образовывать эрозии. При вагинальном кандидозе также могут наблюдаться трещины слизистой вульвы, задней спайки и перианальной области [2] .
Патогенез вагинального кандидоза
Грибы рода Candida относятся к условно-патогенной микрофлоре, которая присутствует как в окружающей среде, так и на поверхности кожных покровов и слизистых оболочках здорового человека (в полости рта, кишечнике, влагалище). При снижении защитных сил организма возможно повышение адгезивных свойств (способности прилипать) грибов с прикреплением их к клеткам эпителия влагалища, колонизацией слизистой оболочки и развитием воспалительной реакции [7] .
Вагинальный кандидоз зачастую затрагивает только поверхностные слои эпителия влагалища без проникновения возбудителя в более глубокие слои слизистой оболочки. Однако в редких случаях эпителиальный барьер преодолевается и происходит инвазия в подлежащую ткань с последующей гематогенной диссеминацией (распространением возбудителя инфекции из первичного очага заболевания по всему органу или организму посредством кровотока) [8] [9] .
Основные этапы патогенеза:
- Адгезия (прилипание) грибов на слизистой и колонизация.
- Инвазия (проникновение) в эпителий.
- Преодоление эпителиального барьера.
- Проникновение в соединительную ткань.
- Преодоление защитных механизмов ткани.
- Попадание в сосуды.
- Гематогенная диссеминация.
При вагинальном кандидозе воспаление происходит в верхних слоях эпителия влагалища. Причина состоит в том, что поддерживается динамическое равновесие между грибом, который не может проникнуть в более глубокие слои, и организмом, который сдерживает его распространение. Соответственно инфекция может долго развиваться в одном месте, проявляясь творожистыми выделениями из влагалища. Обострение заболевания происходит при сдвиге равновесия между развитием грибов и защитными силами организма.
Классификация и стадии развития вагинального кандидоза
Согласно национальным клиническим рекомендациям [18] , выделяют две формы вагинального кандидоза:
- острую — до трёх обострений в год;
- хроническую (рецидивирующую) — не менее четырёх обострений в год.
По классификации, предложенной D.A. Eschenbach, вагинальный кандидоз подразделяют на два типа:
У женщин различают три формы заболевания:
- вагинит (воспаление влагалища); (воспаление влагалища и вульвы); (воспаление шейки матки).
У мужчин выделяют:
- баланит (воспаление головки полового члена);
- баланопостит (воспаление крайней плоти и головки полового члена); (воспаление мочеиспускательного канала).
Для острой формы вагинального кандидоза характерны выраженные симптомы: обильные выделения из влагалища, жжение и зуд во влагалище и наружных половых органах. На фоне таких симптомов нередко снижается трудоспособность пациентки и развиваются неврозы. Острая форма вагинального кандидоза встречается наиболее часто и формируется в результате увеличения количества грибов рода Candida во влагалище на фоне снижения иммунитета пациентки.
Рецидивирующий вагинальный кандидоз — встречается у 10—15 % женщин репродуктивного возраста и проявляется четырьмя и более обострениями за год [11] .
Неосложнённая форма заболевания предполагает впервые выявленный или возникающий менее четырёх раз в год вагинальный кандидоз с умеренными проявлениями вагинита у пациенток без сопутствующих факторов риска (сахарный диабет, приём глюкокортикоидов, цитостатиков и др.).
При осложнённом вагинальном кандидозе наблюдаются яркие объективные симптомы: покраснение, отёк, образование язв, трещин слизистых оболочек и кожи перианальной области. Также характерны рецидивы четыре и более раз в год. Заболевание часто возникает на фоне сахарного диабета, ВИЧ-инфекции, терапии глюкокортикоидами и цитостатиками. Возбудителем заболевания в данном случае являются как C. albicans, так и другие грибы рода Candida.
Осложнения вагинального кандидоза
К осложнениям вагинального кандидоза у женщин относятся:
- стеноз влагалища;
- воспалительные патологии органов малого таза — сальпингит, оофорит и другие;
- заболевания мочевыделительной системы — цистит, уретрит[2] .
Стеноз влагалища развивается при воспалении стенок влагалища. При этом просвет влагалища сужается, а стенки влагалища становятся плохо растяжимы. Пациентки испытывают боль при половом акте.
Сальпингит — инфекционно-воспалительное заболевание фаллопиевой (маточной) трубы. Возникает при переходе инфекции восходящим путем из влагалища, не исключен также и гематогенный путь передачи. Сальпингит чаще всего протекает в сочетании с оофоритом — воспалением яичника. Поражение может быть как односторонним, так и двусторонним. Пациентки испытывают боль в области придатков, внизу живота слева или справа, повышается температура тела, возникает общее недомогание, слабость, а иногда и тошнота со рвотой. При несвоевременном лечении данного осложнения высок риск бесплодия, наступления внематочной беременности, возникновения спаечного процесса, приводящего к оперативному вмешательству, инфицированию органов брюшины и малого таза. Сальпингит особенно опасен в случаях, когда с кандидозом сочетаются другие инфекции [1] .
Уретрит — воспаление слизистой мочеиспускательного канала. Проявляется болезненным мочеиспусканием, чувством жжения в области уретры, выделением с мочой крови или гноя, дискомфортом при соприкосновении с бельём, слипанием краёв уретры, покраснением области вокруг мочеиспускательного канала.
Цистит — воспаление мочевого пузыря. Патология возникает при попадании возбудителя восходящим путём через уретру в мочевой пузырь. Симптомы цистита схожи с симптомами уретрита, однако есть некоторые отличия: частые позывы к мочеиспусканию при небольшом количестве мочи, чувство неполного опорожнения мочевого пузыря, боль, резь в конце мочеиспускания, помутнение мочи, повышение температуры тела, боли внизу живота.
На фоне вагинального кандидоза возрастает частота осложнений при беременности, а также увеличивается риск инфицирования плода.
Кандидоз плода может вызвать его внутриутробную гибель или приводить к преждевременным родам. После родов у женщин возможно развитие кандидозного эндометрита — воспалительного процесса в тканях, выстилающих внутреннюю полость матки.
Диагностика вагинального кандидоза
Диагностика вагинального кандидоза основывается на характерных жалобах пациентки, данных анамнеза, клинических проявлениях, выявленных при гинекологическом осмотре. В зеркалах видна гиперемия, отёк слизистой, белые налёты на стенках влагалища.
Независимо от этих признаков, подтверждение диагноза должно основываться на лабораторных данных:
- Микроскопия мазков вагинального отделяемого — позволяет выявить споры и мицелий гриба.
- Культуральный метод — посев влагалищного содержимого на искусственные питательные среды. Метод определяет количество, видовую принадлежность, чувствительность к противогрибковым препаратам, а также характер и степень заселения другими микроорганизмами. Культуральный метод дополняет микроскопию.
- Серологическая диагностика (РСК). Определяет антитела против антигенов грибов рода Candida. Такая диагностика имеет значение при генерализации процесса.
- Молекулярно-биологические методы. Направлены на обнаружение специфических фрагментов ДНК Candida spp. Применяют метод полимеразной цепной реакции (ПЦР).
- Иммунофлюоресцентная диагностика (Candida Sure Test) проводится в случае рецидивирующего течения вагинального кандидоза [15] .
К дополнительным методам диагностики относятся: изучение микробиоценоза кишечника, обследование на инфекции, передаваемые половым путём, внутривенный тест на толерантность к глюкозе [16] .
Дифференциальную диагностику проводят со следующими заболеваниями:
- генитальным герпесом; ;
- аэробным вагинитом;
- кожными заболеваниями (экземой, красным плоским лишаём, склеродермией, болезнью Бехчета и др.).
Лечение вагинального кандидоза
Показаниями к назначению терапии вагинального кандидоза являются жалобы пациентки, клинические проявления и лабораторное подтверждение наличия грибов рода Candida. Лечение не требуется при обнаружении грибов без каких-либо клинических проявлений (кандидозоносительство). Это правило обусловлено тем, что грибы рода Candida могут содержаться в небольшом количестве во влагалище и являются частью нормальной микрофлоры, если их количество не превышает пороговое значение 10 4 .
Механизм действия противогрибковых препаратов — нарушение синтеза эргостерола (вещества в составе клеточных мембран грибов), что приводит к образованию дефектов в мембране микроорганизма. В зависимости от дозы антимикотики проявляют фунгистатическое (замедление роста) или фунгицидное (полное уничтожение) действие [15] .
Существуют различные группы препаратов для лечения вагинального кандидоза:
- антибиотики (пимафуцин, амфотерицин В, нистатин, леворин);
- имидазолы (клотримазол, сертаконазол, кетоконазол, гино-певарил, миконазол);
- триазолы (итраконазол, флуконазол);
- комбинированные препараты ("Тержинан", "Полижинакс", "Пимафукорт", "Клион Д", "Макмирор комплекс");
- препараты разных групп (флуцитозин, гризеофульвин, дафнеджин, нитрофунгин, йодат поливинилпирролидон).
Лечение подбирается гинекологом индивидуально для каждой пациентки, учитывая клиническую картину, форму заболевания и степень выраженности симптомов. Но важно отметить, что при лечении молочницы при беременности флуконазол противопоказан, так как он может негативно повлиять на развитие плода [19] [20] .
При лечении острых форм вагинального кандидоза назначают местное лечение. Препарат не всасывается в системный кровоток, а действует в области влагалища и слизистой. Примеры схем лечения:
-
150 мг в виде вагинальных свечей один раз в сутки в течение трёх дней; один аппликатор крема на ночь вагинально в течение трёх дней; одна свеча на ночь один раз в сутки в течение восьми дней; одна таблетка на ночь в течение 10 дней.
При хроническом кандидозе наряду с местным лечением применяют системные антимикотики:
-
150 мг один раз внутрь; 200 мг внутрь два раза с интервалом 12 часов в течение одного дня или 200 мг в сутки в течение трёх дней.
При рецидивирующей форме заболевания (более четырёх эпизодов в год) применяют схему:
-
150 мг внутрь три раза с интервалом 72 часа в 1,4 и 7 день лечения.
Для купирования рецидивов препарат применяют в дозировке 150 мг один раз в неделю в течение шести месяцев.
В последние годы всё больше исследуется способность C. albicans формировать биоплёнки — вещества на поверхности колонии микроорганизмов, которые служат барьером для проникновения лекарственных средств и обеспечивают выживание. Основным полисахаридом, определяющим развитие резистентности к антибиотикам, является глюкан. Его рассматривают как одну из причин формирования резистентности к антимикотическим препаратам. Этим объясняется отсутствие эффекта при лечении у некоторых больных. Таким пациенткам можно порекомендовать препарат фентиконазол 600 мг в сутки с интервалом в три дня. Лекарство отличается от других способностью преодолевать биоплёнки, тем самым повышая эффективность лечения при резистентности к другим препаратам.
Прогноз. Профилактика
При своевременном обращении пациентки к врачу, лабораторном обследовании и отсутствии самолечения прогноз благоприятный. Самолечение опасно из-за риска рецидива заболевания, его хронизации и возникновения резистентности к препарату, неверно выбранному пациенткой или при неадекватной дозе.
Чтобы повысить эффективность терапии пациентки должны следовать схеме лечения, индивидуально назначенной гинекологом. Во время лечения и диспансерного наблюдения необходимо соблюдать половой покой или применять барьерные методы контрацепции. Повторно обратиться к врачу для контроля анализов следует через 7-10 дней [12] .
Кандидоз у детей и его причины
Совершенствование технологии выхаживания, реанимации и интенсивной терапии новорожденных детей и, прежде всего, глубоконедоношенных новорожденных привело к существенному увеличению контингента пациентов, особо чувствительных к развитию микозов в силу особенностей их противоинфекционной защиты, а именно - недостаточность и несовершенство защитных барьеров кожи и слизистых, а также особенности клеточного звена противоинфекционной защиты, их интерферонового статуса и иммунного реагирования в ответ на инфекционный процесс. Всё это создаёт благоприятные условия для развития микотического процесса.
Среди факторов риска развития диссеминированного кандидоза у новорожденных и грудных детей Г. Н. Буслаева выделяет увеличение частоты кандидоза мочеполовой сферы матери. Частота врождённого кандидоза колеблется от 0,1 до 1% всех случаев микоза. До сих пор основным считалось постнатальное инфицирование. На самом деле, по мнению Г. А. Самсыгиной, преимущественно встречается интранатальное инфицирование при заболевании беременной кандидозом половых органов.
Уже в 1-е сутки жизни у 4,6% новорожденных в меконии выявляется Candida, к 4-5-му дню, к моменту выписки из родильного дома, - у 46,2% здоровых детей; без клинических проявлений кандидоза они становятся кандиданосителями. К концу 1-го года жизни эта цифра достигает уже 54,6%.
Существенное значение имеют недоношенность, морфофункциональная незрелость, критические ситуации, требующие проведения реанимационных мероприятий, интенсивная антибактериальная и иммуносупрессивная терапия, повышенная пролиферация кишечника, первичный и вторичный иммунодефицит. Возможно внутриутробное инфицирование грибами. Основными путями инфицирования новорожденных грибом Candida авторы считают внутриутробный (анте- и интранатальный) и постнатальный (экзогенный и эндогенный). По их данным, 60-80%) беременных страдают кандидозом, который особенно проявляется в поздние сроки беременности (у 75-94% - это Candida albicans). У 20% новорожденных гриб Candida albicans выделен в пуповинной крови.
Г. Н. Буслаева также выделяет интранатальное и постнатальное кандидозное инфицирование новорожденных. Автор указывает, что. кандидоз развивается вследствие внутриутробного или постнатального инфицирования (контаминации). Внутриутробное инфицирование может возникнуть анте- или интранатально. В свою очередь антенатальное инфицирование может осуществляется трансплацентарным или восходящим путем передачи инфекции. Трансплацентарный путь встречается крайне редко, только при генерализованном кандидозе или кандидозном плацентите у матери. Более часто отмечается восходящий путь, особенно на фоне генитального кандидоза у беременной женщины.
Это связано с тем, что в конце беременности значительно повышается проницаемость плодных оболочек и снижается антимикотическая активность околоплодных вод. Интранатальная контаминация происходит во время прохождения плода по родовым путям. Особенно высока вероятность значительного инфицирования при наличии генитального кандидоза у роженицы.
Постнатальное инфицирование может произойти в любом возрасте. Оно возникает эндо- или экзогенно. Эндогенное развитие кандидоза отмечается у кандиданосителей при воздействии провоцирующих факторов, таких, как использование иммуносупрессивной и антибактериальной терапии, развитие иммунодефицитных состояний, онкологические и эндокринные заболевания. При экзогенном инфицировании можно говорить о нозокомиальной инфекции.
При этом кандидоз развивается на фоне хирургических вмешательств, пребывания в палатах интенсивной терапии, длительного парентерального питания, катетеризации, интубации. Таким образом, экзогенное инфицирование чаще реализуется у недоношенных детей, больных, пребывающих в ОТИ и других отделениях стационаров.
Многие авторы подчеркивают роль дискинетических явлений желудочно-кишечного тракта в патогенезе кандидоза слизистой оболочки полости рта, глотки и гортани, считая кишечник источником аутоинфекции дрожжеподобными грибами (Кашкин П. Н., Ариевич А. М., Степанищева З. Г.). По данным этих авторов, хроническими заболеваниями желудочно-кишечного тракта страдало от 6,4 до 12% больных. У них диагностированы хронический холецистит, язвенная болезнь желудка и хронический колит.
Читайте также:

