Что такое золотистый стафилококк биология
Обновлено: 18.04.2024
Золотистый стафилококк (Staphylococcus aureus) представляет собой шарообразную, неподвижную и аэробную (способную существовать в воздухе) бактерию, положительно окрашиваемую по Грамму, которая вызывает различные заболевания у детей и реже у взрослых.
Высокая патогенность золотистого стафилококка связана с тремя факторами.
И, конечно, следует отметить, что иммунитет к золотистому стафилококку отсутствует, и человек, переболевший стафилококковой инфекцией, может заразиться ею вновь.
Особую опасность золотистый стафилококк представляет для грудных детей, находящихся в роддоме. Именно в больницах высока концентрация данного микроба в окружающей среде, чему немаловажное значение придает нарушение правил асептики и стерилизации инструментов и носительства стафилококка среди мед. персонала.
Бесспорно, что причиной стафилококковой инфекции является, как правило, золотистый стафилококк. Заражение происходит при снижении иммунитета, чему способствует ряд факторов:
- прием антибиотиков и гормональных препаратов;
- стрессы;
- неправильное питание;
- гипо- и авитаминозы;
- инфекции;
- дисбактериоз кишечника;
- несоблюдение правил личной гигиены; ;
- незрелость ребенка при рождении;
- искусственное вскармливание;
- позднее прикладывание к груди.
Различают генерализованные и локальные формы стафилококковой инфекции.
К генерализованным формам относится сепсис (септикопиемия и септикоцемия).
К локальным формам относятся заболевания кожи, слизистых оболочек, внутренних органов, костей, суставов, молочных желез и пупочного канатика. Также отдельной графой стоит выделить пищевые отравления эндотоксином стафилококка.
Кроме того, стафилококковая инфекция может быть первичной и вторичной (при наличии первичного очага). По течению выделяют острые, затяжные и хронические формы, а по тяжести стафилококковой инфекции легкой, средней и тяжелой степени.
Симптомы стафилококковой инфекции зависят от места локализации стафилококк в организме ребенка и от степени снижения защитных сил организма. К основным признакам стафилококковой инфекции относятся
- повышение температуры тела
- выраженный интоксикационный синдром (вялость, слабость, отсутствие аппетита, тошнота).
Омфалит
Поражение микробом пупочной ранки, которое сопровождается отеком пупочного кольца, гнойным отделяемым из раны. При вовлечении в процесс пупочной вены прощупывается уплотненная и утолщенная вена. Также наблюдается гиперемия, которая распространяется вверх, в сторону грудины.
Поражение кожных покровов
Поражение глаз
При поражении слизистой глаз развивается конъюнктивит (светобоязнь, слезотечение, отек век, гнойное отделяемое из глаз).
Поражение дыхательных путей
Ринит – покраснение слизистой с обильным гнойным отделяемым из носа. При проникновении инфекции ниже развивается ангина, характеризующаяся болью в горле, фарингит, трахеит с сухим и болезненным кашлем.
Инфицирование бронхов и легких приводит к бронхитам и пневмониям. Как правило, бронхиты и пневмонии протекают сочетано с фарингитами, ринитами, трахеитами.
Отмечается значительное повышение температуры (до 39-40°C), сухой кашель, одышка.
Возможно развитие стеноза дыхательных путей.
Поражение центральной нервной системы
Проникновение золотистого стафилококка в головной мозг ведет к развитию менингита и абсцесса головного мозга. Заболевания у детей протекают тяжело, с высокой температурой и явлениями интоксикации.
Поражение мочевыводящих путей
Развиваются уретрит, цистит, пиелонефрит. Характерные симптомы: учащенное и болезненное мочеиспускание, боли в поясничной области, высокая температура. В анализах мочи определяются белок, большое количество лейкоцитов, высевается золотистый стафилококк.
Поражение костей и суставов
При инфицировании костей и суставов развиваются артриты и остеомиелит.
Пищевая токсикоинфекция
Развивается при употреблении зараженной или испорченной пищи и протекает с явлениями острого энтероколита. Характерны повышение температуры, тошнота, рвота до 10 и более раз в сутки, жидкий стул с примесью зелени.
Сепсис
Заражение крови или сепсис, возникает при выраженном иммунодефиците. Течение заболевание тяжелое, с очень высокой температурой, выраженными симптомами интоксикации, нарушением сознания (от возбуждения до вялости).
При развитии инфекционно-токсического шока резко падает артериальное давление, больной теряет сознание и может впасть в кому.
Септикопиемия – циркулирование золотистого стафилококка в крови с формированием гнойных очагов, как на коже ребенка, так и во внутренних органах.
При септицемии характерно развитие инфекционного токсикоза. Септицемию может осложнять присоединение пневмонии, развитие ДВС-синдрома и прочее.
Дифференциальную диагностику стафилококковой инфекции следует проводить со стрептококковой инфекцией. В диагностике заболеваний стафилококковой этиологии используют следующие серологические методы, отличающиеся быстротой и высокой точностью:
- Стандартный коагулазный тест в пробирке, который продолжается 4 часа, но при отрицательном результате продляется на сутки.
- Латекс-агглютинация, при которой используются коммерческие наборы частиц латекса, связанных с антителами к стафилококку (А-протеину, фактору слипания и ряду поверхностных антигенов), что делает ее также полезной для видовой и штаммовой идентификации возбудителя
- Общие анализы крови и мочи (в крови определяется лейкоцитоз, нейтрофилез, повышенное СОЭ, а в моче белок, лейкоциты, стафилококки).
- Посев биологического материала на питательные среды.
Посев на питательные среды проводится с целью идентификации возбудителя заболевания и определения его чувствительности и устойчивости к антибиотикам.
Посев кала должен производиться не позднее чем через 3 часа после дефекации, мазки со слизистых рта и носоглотки должны браться натощак, до чистки зубов и до приема лекарств.
Мазок при стафилококковом конъюнктивите берется с нижнего века стерильным тампоном, смоченным в дистиллированной воде и до умывания.
При кожных заболеваниях мазки берутся после предварительно обработки кожи вокруг раны раствором антисептика и удаления некротизированных участков (корочек) из раны.
Позволяет определить динамику заболевания и эффективность лечения. Проводится 2 и более раз с перерывами в 7-10 дней. Нарастание титра антител в крови более 1:100 свидетельствует о прогрессировании инфекции.
Позволяет определить чувствительность микроба к фагам-вирусам для назначения соответствующего лечения.
Одни и те же симптомы могут быть признаками разных заболеваний, а болезнь может протекать не по учебнику. Не пытайтесь лечиться сами — посоветуйтесь с врачом.
При легких формах стафилококковой инфекции назначение антибиотиков не требуется.
При среднетяжелых и тяжелых формах назначаются полусинтетические пенициллины (амоксиклав), которые эффективны при устойчивости микроорганизма к пенициллинам и цефалоспорины (кефзол, цефтриаксон).
Сроки лечения зависят от тяжести заболевания и инфицирования кожи или внутренних органов (от 7 дней до нескольких месяцев).
При гнойно-воспалительных заболеваниях кожи (фурункулез, карбункул, импетиго) назначается местное лечение - мупироцин или производные плевромутилина. При их отсутствии может быть произведена обработка ран растворами антисептиков: бриллиантовой зеленью, перекисью водорода, перманганатом калия и антибактериальными мазями (синтомициновая, олеандомициновая мази, бактробан).
При конъюнктивите ежедневно промываются глаза слабым раствором марганцовки, и закапывается 30% раствор альбуцида 4-5 раз в сутки.
При гнойных поражениях кожи (абсцессы, флегмоны) производится хирургическое вскрытие гнойников для оттока гноя.
Кроме того, показано назначение антистафилококкового бактериофага, антистафилококковой плазмы и иммуноглобулина (при сепсисе и тяжелом течении заболеваний).
При стафилококковой пищевой токсикоинфекции антибиотики не назначаются, используется антистафилококковый анатоксин. Проводят промывание желудка и восполнение объема циркулирующей крови внутривенными инфузиями солевых растворов (физ. раствор, раствор глюкозы, регидрон и прочие).
Лечением стафилококковой инфекции у детей занимается детский врач-инфекционист.
Методы лечения подбираются в зависимости от поражения тех или иных органов. Ребенок госпитализируется в отдельную палату-бокс, где производится ежедневная смена постельного и нательного белья и ежедневный душ больного.
Особенно опасен золотистый стафилококк для детей грудного возраста. Возможные осложнения:
- сепсис;
- инфекционно-токсический шок;
- кома;
- летальный исход.
Прогноз зависит от тяжести заболевания и эффективности лечения.
При легких поражениях кожи и слизистых оболочек прогноз благоприятный. Массивное инфицирование золотистым стафилококком, особенно при развитии сепсиса в 50% заканчивается летальным исходом.

Новость
Структурная формула нового пептидного антибиотика.
Автор
Редакторы
- Антибиотики
- Биомолекулы
- Биотехнологии
- Здравоохранение
- Микробиология
- Фармакология
Немецкие ученые обнаружили новое оружие для борьбы с больничным монстром — мультирезистентным золотистым стафилококком. Долгие годы оно скрывалось не в вечной мерзлоте или Марианской впадине, а прямо под нашим носом. Вернее — в нём.
В последние годы во всем мире увеличилось количество инфекционных заболеваний, вызванных устойчивыми к антибиотикам бактериями. Организмы с множественной лекарственной резистентностью (multidrug-resistant organisms, MDRO), такие как метициллин-резистентный золотистый стафилококк, нечувствительные к ванкомицину энтерококки или резистентные к цефалоспоринам третьего поколения грамотрицательные бактерии, в ближайшие десятилетия могут стать более частыми причинами смерти, чем рак [1].
Несколько лет назад удалось обнаружить, что представители человеческой микробиоты способны производить бактериоцины, поражающие близкородственных бактерий [2]. Например, в 2014 году из человеческого комменсала Lactobacillus gasseri выделили и описали новый синтезируемый рибосомами тиопептидный антибиотик — лактоциллин [3].
Семейные разборки
Немецкий исследователь Александр Ципперер со своими сотрудниками в июле 2016 года сообщил о том, что обнаружил в человеческом носу бактерию Staphylococcus lugdunensis IVK28, которая подавляет рост метициллин-резистентного золотистого стафилококка (methicillin-resistant Staphylococcus aureus, MRSA) [1].
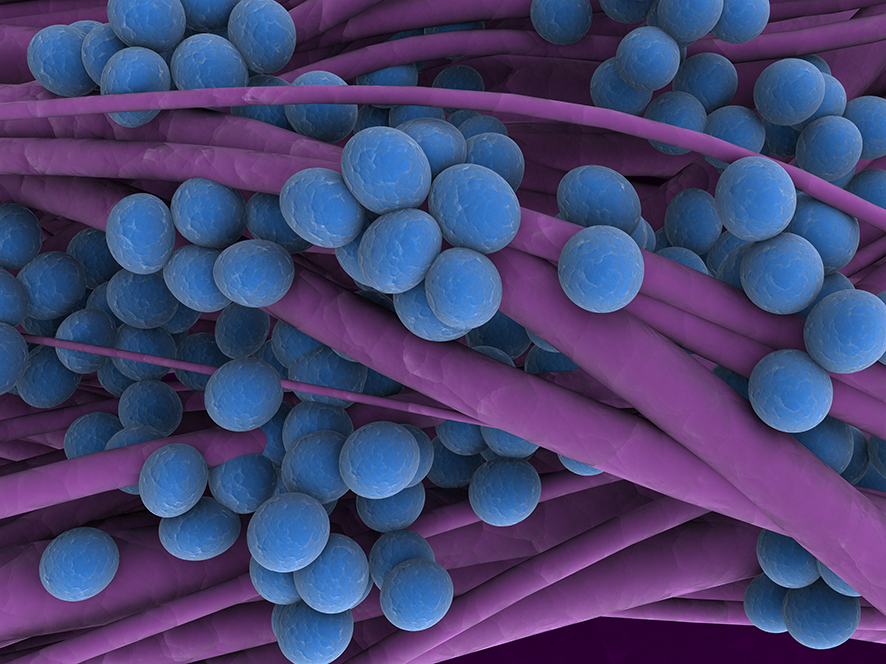
Золотистый стафилококк
Стафилококки относятся к типичным бактериям-комменсалам, колонизирующим кожу и поверхности слизистых оболочек. Staphylococcus aureus — шаровидные грамположительные бактерии, вырабатывающие каротиноидный пигмент, который придает их клеткам золотистый цвет (рис. 1). Эти микроорганизмы чрезвычайно устойчивы к внешним воздействиям и выживают в воздухе, пыли, почве, продуктах питания, на оборудовании пищевых производств и предметах быта [6], [7].

Рисунок 1. Staphylococcus aureus и лейкоциты.

Рисунок 2. Метициллин-резистентные золотистые стафилококки.
Staphylococcus aureus — бактерия условно-патогенная, проявляющая свои патологические свойства только в благоприятных условиях, а создает их, как правило, ослабление иммунитета носителя. Активная жизнедеятельность стафилококка может привести к разнообразным заболеваниям [5], [7], [8]:
- кожи (прыщи, фурункулы, синдром ошпаренной кожи);
- органов дыхания (плеврит, пневмония);
- костной и соединительной тканей (артрит, остеомиелит);
- нервной системы и органов чувств (отит, менингит);
- сердечно-сосудистой системы (эндокардит, флебит, стафилококковая бактериемия).
Факторы патогенности S. aureus — это микрокапсула, компоненты клеточной стенки, ферменты агрессии и токсины. Микрокапсулы защищают клетки бактерий от фагоцитоза, способствуют их адгезии и распространению по организму хозяина. Составляющие клеточной стенки (например пептидогликан, тейхоевые кислоты и белок А) вызывают развитие воспаления, обездвиживают фагоциты и нейтрализуют иммуноглобулины. Коагулаза, главный фермент агрессии, вызывает свертывание плазмы крови [7], [9].
Наиболее опасны метициллин-резистентные стафилококки (methicillin-resistant S. aureus, MRSA) (рис. 2). Метициллин — это модифицированный пенициллин, с помощью которого еще недавно успешно боролись со стафилококковой инфекцией. MRSA устойчивы не только к метициллину, но и к другим антибиотикам пенициллиновой группы (диклоксациллину, оксациллину, нафциллину и др.), а также к цефалоспоринам. В последнее время выявлены штаммы и с более широким спектром устойчивости: ванкомицин-резистентные (VRSA) и гликопептид-резистентные (GISA) [6], [9], [10].
Штамм S. lugdunensis IVK28 эффективно боролся со своим вредоносным родственником лишь в условиях недостатка железа и только на твердых агаризованных средах (рис. 3, слева). Механизм противостояния был неясен, а потому Ципперер провел транспозонный мутагенез клеток выделенного штамма — чтобы выявить ген, ответственный за синтез смертельного для S. aureus вещества.

В итоге удалось получить мутанта IVK28, который не мог подавлять рост MRSA. Анализ места встройки транспозона показал, что тот нарушил структуру гена предполагаемой нерибосомной пептидсинтетазы (НРПС). Оказалось, что этот ген вместе с другими последовательностями, связанными с биосинтезом антибиотиков, входит в состав оперона размером 30 т.п.н. Это указывало на то, что предполагаемая молекула ингибитора может быть комплексом нерибосомных пептидов.
Оперон методом ПЦР обнаружили во всех культурах S. lugdunensis, а значит, он характерен для всего вида, а не только для штамма IVK28. Однако GC-состав оперона (26,9%) отличался от GC-состава остального генома S. lugdunensis (33,8%), что свидетельствовало о возможном заимствовании этого полезного генетического кластера у других видов бактерий — путем горизонтального переноса .
Оперон состоит из генов lugA, B, C и D, кодирующих пептидсинтетазные белки (см. врезку ниже), а также из других генов, чьи продукты необходимы для синтеза и транспорта нерибосомного пептида.
Чтобы окончательно вменить оперону участие в антибактериальной деятельности S. lugdunensis, наименьший ген (lugD) удалили. Мутант ΔlugD, как и ожидалось, не мог подавлять рост золотистого стафилококка, но когда в него ввели плазмиду с работающим геном lugD, агрессивный фенотип восстановился (рис. 3, в центре и справа).
Секретное оружие
Выделенный Ципперером продукт lug-оперона оказался нерибосомным циклическим пептидом, состоящим из пяти аминокислот (двух D-валинов, L-валина, D-лейцина и L-триптофана) и тиазолидинового гетероцикла (рис. 4). Назвали антибиотик лугдунином.

Химическим синтезом удалось получить продукт с идентичными природному лугдунину химическими свойствами и антибактериальным эффектом. Ученые предположили, что этот антибиотик ингибирует синтез бактериальных биополимеров — белков, ДНК и пептидогликанов [5].
Нерибосомные пептиды
Этот класс пептидов синтезируется в клетках низших грибов и бактерий без участия рибосом. Нерибосомные пептиды (НРП) также встречаются и у высших организмов, которые имеют бактерий-комменсалов [12].
НРП подразделяются на несколько функциональных групп [13]:
- антибиотики (ванкомицин);
- предшественники антибиотиков (ACV-трипептид — предшественник пенициллина и цефалоспорина);
- иммуносупрессоры (циклоспорин);
- противоопухолевые пептиды (блеомицин);
- сидерофоры (пиовердин);
- токсины (HC-токсин);
- сурфактанты (сурфактин).
Строение
Синтез
Каждый модуль состоит как минимум из трех доменов:
- конденсирующего (принимающего пептидную цепь из предыдущего модуля);
- аденилирующего (выбирающего нужную аминокислоту);
- пептидильного (образующего пептидную связь).
Нередко модули включают и другие домены, в том числе эпимеризующий, который преобразует L-аминокислоты в D-формы [14].
По аналогии с триплетным рибосомным кодом для синтеза белка существует и нерибосомный, код НРПС, определяемый 10 остатками аминокислот в субстрат-связывающем кармане аденилирующего домена. От комбинации этих остатков зависит то, какая аминокислота будет встроена в пептид конкретным модулем НРПС. Зная этот код, можно предсказывать субстратную специфичность аденилирующих доменов и даже произвольно изменять ее посредством замены аминокислот в домене [14].
В экспериментах немецких ученых лугдунин действовал не только на метициллин-резистентных стафилококков, но и на гликопротеин-резистентных, и даже на других грамположительных бактерий типа листерии и ванкомицин-резистентного энтерококка (табл. 1). Минимальная ингибирующая концентрация (МИК) нового бактериоцина — 1,5–12 мкг × мл −1 , что говорит о высокой активности вещества. При этом такие концентрации никак не влияли на человеческую сыворотку, не вызывали лизис нейтрофилов или эритроцитов и не ингибировали метаболическую активность моноцитов. Бактериальные же клетки под действием лугдунина в концентрации даже ниже МИК прекращали синтезировать ДНК, РНК, белки и компоненты клеточной стенки. В этом отношении лугдунин напоминает даптомицин, дающий такой же эффект, но способ действия которого пока не изучен. Не было отмечено возникновения резистентности клеток S. aureus к лугдунину даже после их месячного выращивания на малых концентрациях.
| Виды и штаммы | Резистентность | МИК лугдунина (мкг × мл −1 ) |
|---|---|---|
| Staphylococcus aureus USA300 (LAC) | MRSA | 1,5 |
| + 50% человеческой сыворотки крови | 1,5 | |
| Staphylococcus aureus USA300 (NRS384) | MRSA | 1,5 |
| Staphylococcus aureus Mu50 | GISA | 3 |
| Staphylococcus aureus SA113 | 3 | |
| Staphylococcus aureus RN4220 | 3 | |
| Enterococcus faecium BK463 | VRE | 3 |
| Enterococcus faecalis VRE366 | VRE | 12 |
| Listeria monocytogenes ATCC19118 | 6 | |
| Streptococcus pneumoniae ATCC49619 | 1,5 | |
| Bacillus subtilis 168 (trpC2) | 4 | |
| Pseudomonas aeruginosa PAO1 | >50 | |
| Escherichia coli DH5α | >50 | |
| Условные обозначения: MRSA — метициллин-резистентные S. aureus; GISA — устойчивые к гликопротеинам S. aureus; VRE — ванкомицин-резистентные Enterococcus. Таблица из [1]. | ||
Испытания в боевых условиях
Как и полагается, способность лугдунина лечить стафилококковые инфекции продемонстрировали in vivo на мышиной модели (рис. 5). У шести мышей сбрили шерсть на спине и, повредив кожу многократным приклеиванием/отклеиванием пластыря, нанесли на это место золотистого стафилококка. Затем кожу обработали мазью, содержащей 1,5 мкг лугдунина, и спустя шесть часов оценили результат. Обработка новым антибиотиком сильно сокращала или даже полностью уничтожала популяцию S. aureus. Причем не только на поверхности кожи, но и в более глубоких ее слоях.

Рисунок 5. Общая схема подхода к идентификации природного антибиотика. Из бактериальных популяций человеческого тела отбирают представителей, которые не могут сосуществовать с интересующими патогенными бактериями. Этих возможных конкурентов тестируют по отдельности на средах с инфекционным агентом. Из культуры, успешно подавляющей рост патогенов, выделяют антибиотик, действие которого проверяют на животных моделях.
[5], рисунок модифицирован и адаптирован
Чтобы понять, может ли S. lugdunensis помешать колонизации носовой полости позвоночных животных золотистым стафилококком в естественных условиях, ученые провели следующий эксперимент. В носы хлопковых хомяков ввели два вида смешанных культур (S. aureus + S. lugdunensis IVK28 и S. aureus + S. lugdunensis IVK28ΔlugD) и каждую по отдельности. В контрольных случаях, когда вводили по одному штамму, все три культуры стабильно колонизировали носовую полость. Однако при введении смеси S. aureus + S. lugdunensis IVK28 количество золотистого стафилококка через 5 дней значительно уменьшилось по сравнению со смесью S. aureus + S. lugdunensis IVK28ΔlugD. Этот эксперимент показал, что продукция лугдунина позволяет штамму IVK28 эффективно конкурировать с золотистым стафилококком in vivo.
Оставалось разобраться, предотвращает ли присутствие S. lugdunensis в носу человека колонизацию бактериями S. aureus. Ципперер и его коллеги исследовали мазки из носовых ходов 187 госпитализированных больных. Из них у 60 человек (32,1%) обнаружили золотистого стафилококка и у 17 человек (9,1%) — S. lugdunensis. И только у одного пациента с S. lugdunensis в носу обитал S. aureus. У всех выделенных штаммов S. lugdunensis ПЦР-анализ продемонстрировал наличие lug-оперона, а все обнаруженные штаммы S. aureus оказались восприимчивы к лугдунину.
Перспективы
Лугдунин оказался первым обнаруженным бактериоцином нового класса — макроциклических тиазолидиновых пептидных антибиотиков. Все проверенные штаммы S. aureus (как природные, так и лабораторные) не смогли выработать резистентности к нему. Это дает надежду на то, что лугдунин в будущем станет коммерческим препаратом для борьбы с золотистым стафилококком.
И наконец, сам факт обнаружения нового антибиотика у представителя человеческой микробиоты должен послужить стимулом для активизации поиска других продуцентов бактериоцинов в составе именно таких сообществ. В дальнейшем это поможет медикам успешнее сдерживать наступление мультирезистентных патогенов.

Обзор
Автор
Редакторы

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Немного о VR
В видео есть часть, где представлена VR-работа. Чтобы лучше понять, что где находится — прочитайте, пожалуйста, описание ниже:
- Для удобства рассмотрения внутренних процессов, происходящих в бактериальной клетке, клеточная стенка и цитоплазматическая мембрана сделаны прозрачными.
- В цикле репродукции вируса рассматривается один вид бактериофага. Это стафилококковый бактериофаг 80α (альфа).
- Процессы репликации, трансляции и транскрипции упрощены, и для лучшего ви́дения этих процессов они немного разнесены в пространстве.
Золотистый стафилококк
Стафилококки — грамположительные и не спорообразующие кокки, которые образуют пары, короткие цепочки или гроздья. Род Staphylococcus содержит много видов, которые отделяются друг от друга на основе продукции фермента коагулазы [1].
Золотистый стафилококк (Staphylococcus aureus) — коагулазоположительный вид, является одним из самых вирулентных видов.
Золотистый стафилококк — часто безвредный обитатель эпителия кожи и слизистых оболочек человека, но также связан с серьезными системными и местными инфекциями [2] и является одной из наиболее распространенных причин пищевых инфекций во всем мире. S. aureus производит 15 энтеротоксинов.
Энтеротоксины бактериальные токсины, которые вызывают секрецию жидкости из клеток кишечника.
Борьба с золотистым стафилококком
Борьба с бактериями велась издавна. Люди пробовали лечить раны растениями. И методом проб и ошибок подбирали нужные противомикробные лекарства [3].
Уже в 1940 году появились первые сведения об устойчивости бактерий к пенициллину.
Бактериофаг
В 1919 году, еще до обнаружения пенициллина, Феликс Д’Эрелль открыл совершенно другой метод борьбы с бактериями. Но потом он так и не смог конкурировать с антибиотиками. Речь идет о бактериофаговой терапии.
Бактериофаги (фаги) — это вирусы, которые используют для размножения только прокариотические клетки. Эти вирусы встречаются в природе повсеместно [6]. S. aureus был одним из первых организмов, использованных для демонстрации существования бактериофага [2].
В 1920–1940-е годы проводили множество исследований по клиническому применению бактериофагов, но стабильных результатов получено не было. На Западе от бактериофаговой терапии начали отказываться [7].
Борьба золотистого стафилококка и бактериофага
Сейчас фаговые препараты представляют собой смеси нескольких бактериофагов. Мы остановимся на одном из стафилококковых фагов.
Фаг 80α — умеренный бактериофаг лямбда семейства Siphoviridae с геномом в виде двухцепочечной ДНК. 80α способен к генерализованной трансдукции, а также может выступать в качестве помощника для мобилизации островков патогенности SaPI [2], которые, как было показано, кодируют такие факторы вирулентности, как токсины синдрома токсического шока и коагулаза [1].
Как и у других бактериофагов, капсид 80α собирается в виде пустого предшественника — прокапсида. Горсти фаговой ДНК упаковываются в прокапсиды через портальную вершину в АТФ-зависимом процессе, который требует малых и больших субъединиц фермента терминазы. Упаковка ДНК сопровождается расширением капсида и структурной перестройкой оболочки.
Для бактериофаговой терапии рекомендуется использовать те бактериофаги, которые идут по литическому пути развития (с разрывом клетки).
Бактериофаговые препараты
Сейчас с развитием современных методов генной инженерии и молекулярной биологии бактериофаговая терапия оживает в новых исследованиях. И на данный момент бактериофаговая терапия применяется очень осторожно и строго контролируемо, во избежание повторения истории с антибиотиками.
Однако не везде соблюдаются такие строгие стандарты. В Западной Европе после открытия антибиотиков от использования бактериофагов довольно быстро отказались. В Восточной Европе, несмотря на отсутствие крупных и контролируемых клинических испытаний, они оставались относительно популярным лечением в XX веке [8].
Приглашение от авторов проекта
Мы хотим, чтобы у всех была возможность окунуться в микромир. Поэтому приглашаем жителей Санкт-Петербурга лично посетить виртуальную реальность. Чтобы сделать это, напишите Надежде в Instagram (irreal.art) или Ярославе в VK.
Золотистый стафилококк обитает везде – в воздухе, почве, на коже, на слизистых оболочках носа и ротоглотки, откуда в небольших количествах попадает в кишечник. Это и послужило причиной отнесения Staphylococcus aureus к условно-патогенным микроорганизмам (УПМ).
К слову, предельно допустимое количество золотистого стафилококка в составе микрофлоры ЖКТ (желудочно-кишечного тракта) до сих пор остается спорным. Одни исследователи считают, что в анализах кала численность этого микроорганизма не должна превышать 10 клеток на1 гкала, другие же полагают, что неопасной является даже более высокая доза – до 1000 клеток в грамме. Так или иначе, все ученые и врачи сходятся во мнении, что патогенность золотистого стафилококка неоспорима.
Если у человека иммунитет находится в норме, то восприимчивость к патогенному воздействию у организма низкая. Но если состояние микрофлоры, которая первая встает на пути борьбы с патогенными микроорганизмами, ухудшается, то стафилококки приобретают способность преодолевать тканевые барьеры и мигрировать по всему организму. Затем они осваивают новую среду обитания, которая была стерильной, а следовательно и не имела микробов-конкурентов. Выделяя в эту среду, то есть в ткани человека, продукты обмена веществ, стафилококки вызывают воспалительный процесс.
Staphylococcus aureus обладает целым набором болезнетворных факторов. Сюда входят ферменты фибринолизин и лецитовителлаза, разрушающие белки человеческого организма фибрин и лецитин; вещества, свертывающие плазму крови (плазмокоагулаза); растворяющие эритроциты гемолизины; разрушающие лейкоциты (лейкоцидин); энтеротоксины А, В, С, Д, Е и F– вещества, вызывающие диарею; эксфолиатины, которые поражают кожу.
Пути передачи возбудителя стафилококковой инфекции разнообразны. Staphylococcus aureus может передаваться как воздушно-капельным путем, так и контактно-бытовым, попадать в организм с пищей и питьем. Поскольку стафилококк способен длительно сохраняться в пыли, он с легкостью переносится с воздушными потоками по системам вентиляции.
Обладая повышенной устойчивостью к антибиотикам, эта бактерия вызывает внутрибольничные инфекции (ВБИ) разного рода. По данным Всемирной Ассоциации Здравоохранения (ВОЗ), золотистому стафилококку, как возбудителю ВБИ, отводится первое место.
Какие заболевания способен вызывать стафилококк?
- Болезни кожи и подкожной клетчатки, такие как: пиодермия, эксфолиативный дерматит (пузырчатка новорожденных), синдром ошпаренной кожи, везикулопустуллез, гидроаденит, абсцесс, панариции, фурункулы.
- Заболевания органов дыхания: ангина, пневмония, плеврит.
- Болезни нервной системы и органов чувств: отит, конъюнктивит, менингит.
- Болезни органов пищеварения: парапроктит, энтерит, энтероколит, стоматит, парапроктит, острая пищевая интоксикация.
- Заболевания костно-мышечной системы и соединительной ткани: артрит, остеомиелит, периостит.
- Болезни мочеполовой системы: пиелит, цистит, уретрит, мастит, эндометрит, орхит.
- Заболевания сердечно-сосудистой системы: эндокардит, перикардит, флебит.
Этот список можно продолжать, ведь стафилококк, как и любой другой микроорганизм способен мутировать. Так в 1980 году появилось новое заболевание, виновником которого стал стафилококк. Эта болезнь получила название синдром токсического шока. Первые случаи инфицирования новым штаммом золотистого стафилококка были связаны с женскими гигиеническими тампонами. Сейчас уже известны случаи заражения этим синдромом при родах и как осложнение после хирургических вмешательств (в первую очередь – после операций в области носа).
Если микроорганизм проникает через поврежденную кожу, слизистые оболочки желудочно-кишечного тракта, дыхательных путей или мочеполовых органов, то начинает развиваться гнойно-воспалительный процесс по типу абсцесса. Когда защитная реакция организма слабая, то местное воспаление переходит в генерализованный патологический процесс, то есть затрагивается весь орган или даже организм целиком.

staphilococcus Aureus
Токсины стафилококка нарушают деятельность клеток иммунной системы (лейкоцитов, нейтрофилов и макрофагов) и подавляют, то есть ингибируют ответ иммунитета на стафилококковые антигены. Токсины разносятся с лимфой и кровью в другие ткани и органы, вызывая воспалительные реакции и там. В месте локализации золотистого стафилококка образуются фибринные сгустки, происходит некроз (отмирание) тканей и гибель иммунных клеток. Таким образом формируется гнойный очаг, содержащий клетки золотистого стафилококка.
Часто стафилококковые инфекции развиваются на фоне вирусных заболеваний, а аткже у лиц с пониженным иммунитетом. В значительной степени иммунный ответ организма на агрессора зависит от состояния микрофлоры, в которой немаловажную роль играет нормальная бактериальная флора кишечника. Подавление нормофлоры посредством антибиотиков, гормонов, иммунодепрессантов (например, перед трансплантацией), рентгеновским облучением влечет за собой инфицирование стафилококком. У таких людей наблюдается склонность к рецидивам заболевания, то есть к его повторному возникновению.
У новорожденных детей есть врожденный иммунитет к Staphylococcus aureus. Дети более старшего возраста, равно как и взрослые, вырабатывают собственные антитела к стафилококковым антигенам в результате частого столкновения кожных покровов с этими микроорганизмами. Но риск заражения все равно присутствует, особенно при нахождении в условиях стационаров. Формы золотистого стафилококка, которые курсируют в больничных заведениях, обладают выработанной поколениями устойчивостью к антибиотикам (полирезистентностью). Поэтому вспышки стафилококковых внутрибольничных инфекций отмечаются регулярно, о чем уже упоминалось выше.
Пищевые интоксикации (отравления), вызванные Staphylococcus aureus встречаются повсеместно. Впервые роль этих бактерий в отравлениях тортами с кремом отметил Лащенков П.Н. еще в 1901 году.
Наилучшая температура для размножения золотистого стафилококка находится в пределах от 25 до 37 °С. Но при этом отдельные штаммы способны выдерживать температуру в 100°С в течение получаса, а внутри замороженных продуктов эти кокки сохраняются до 4 месяцев. Для большинства патогенных бактерий высокие концентрации сахара и соли являются губительными (на этом основаны принципы консервации некоторых продуктов). В то же время для золотистого стафилококка вполне приемлема концентрация сахара до 60%, а соли – до 12%.
Исход заболеваний, вызванных золотистым стафилококком, как правило, — выздоровление. Исключение составляют стафилококковые инфекции, перешедшие в генерализованную форму, возникшие у детей первого года жизни. В этом случае количество смертельных случаев достигает 30%.
В качестве профилактических мероприятий применяется термическая обработка продуктов. Также во избежание заражения необходимо воздерживаться от контактов с больными, особенно это касается маленьких детей. Больной родственник с банальной ангиной может стать причиной серьезного заболевания у ребенка. Ни в коем случае нельзя без контроля врача принимать самим и давать детям антибиотики! А вот различные меры по укреплению иммунитета, в том числе и поддержание микрофлоры в нормальном состоянии посредством приема препаратов, содержащих лакто- и бифидобактерии наоборот, приветствуется. Но, опять же, в разумных пределах.

Staphylococcus aureus – патогенная разновидность стафилококков, вызывающий гнойно-воспалительные поражения органов и систем. Возбудитель диагностируется в подмышечной области, носовых ходах. Носителями патогенного микроорганизма считаются работники медицинских учреждений, больные некоторыми видами дерматита. У здоровых людей в норме золотистый стафилококк выявляется в носовых ходах, гортани, в промежности, на волосистой части головы, в ЖКТ.
Особенности носительства микроорганизма
Около 20% детей первых двух лет жизни являются носителями Staphylococcus aureus. Бактерия выявляется в носовой полости. С 4 лет патогенный микроорганизм выявляется у 50% детей.
Среди взрослых носителями является около 20% населения.
Среди медицинского персонала, число носителей достигает 30%.
После первой менструации, микроорганизм выявляется у 10% женщин. Во время менструального цикла, количество носителей среди женщин достигает 25%.
Штаммы золотистого стафилококка
Существует несколько видов штаммов золотистого стафилококка. Некоторые из них приобрели высокую устойчивость к некоторым группам антибактериальных препаратов. Такие штаммы получили название метициллин-резистентные. Они резистентны ко многим видам антибиотиков, в том числе к пенициллиновому ряду. В Америке ежегодно растет количество людей, зараженных этим видом микроорганизма.
Заразиться метициллин-резистентным штаммом можно в любом общественном месте. Смертность от него составляет порядка 30% — в США каждый год от инфекций, вызванных микроорганизмом, каждый год умирает до 20 тысяч человек.
Диагностика
Золотистый стафилококк выявляется при анализе биоматериала. Его могут обнаружить в кале при анализе на дисбактериоз. Метициллин-резистентный штамм обнаруживается в отделяемом носоглотки, околоносовых пазухах, в других видах отделяемого. Забор материала проводится при подозрении на носительство. В плановом порядке анализ на золотистый стафилококк делается при прохождении медицинского обследования медперсонала, работников сферы образования, общепита. В норме, микроорганизм должен отсутствовать.
Обнаружение бактерии возможно при проведении анализа на коагулазу.
Антибиотики против золотистого стафилококка
От золотистого стафилакокка применяют разные виды антибиотиков. Это могут быть:
Для борьбы с золотистым стафилококком применяют жирные кислоты, содержащие до16 атомов углерода. Противомикробная активность вещест обусловлена кислой средой, в которой микроорганизмы не выживают.
Читайте также:

