Что за режимы при лечении туберкулезе легких
Обновлено: 19.04.2024
Для цитирования: Мишин В.Ю., Степанян И.Э. Контролируемая химиотерапия туберкулеза органов дыхания в современных условиях. Проблема лекарственной устойчивости. РМЖ. 2000;12:496.
Центральный НИИ туберкулеза РАМН,
кафедра туберкулеза Московского государственного медико-стоматологического университета
Этиотропная химиотерапия играет приоритетную роль среди методов лечения туберкулеза, к которым относятся также лечебно-охранительный режим, рациональное питание, патогенетическая терапия, коллапсотерапия, оперативное и санаторно-курортное лечение. Лечебный эффект противотуберкулезных препаратов основан на их бактериостатическом или бактерицидном действии в отношении микобактерий туберкулеза (МБТ), которое приводит к уменьшению бактериальной популяции в организме больного.
Группа препаратов, применяемых для лечения туберкулеза, весьма немногочисленна и включает разнородные химические соединения – антибиотики и химиотерапевтические средства.
Основными противотуберкулезными средствами на сегодня являются изониазид, рифампицин, стрептомицин, пиразинамид, этамбутол, тиоацетазон. Первые два из перечисленных препаратов обладают бактерицидным действием и способны быстро убивать большое количество активно размножающихся МБТ [1].
Противотуберкулезные препараты “второго ряда” – канамицин, амикацин, капреомицин; этионамид (протионамид); офлоксацин, ципрофлоксацин; циклосерин (теризидон); ПАСК – назначают в случаях, когда по каким-либо причинам невозможно использовать основные средства [2].
Полвека назад, вскоре после появления первых противотуберкулезных препаратов, продолжительность лечения была сравнительно небольшой (1– 3 мес), химиотерапия оказывала фантастический эффект, что позволило необоснованно считать проблему лечения туберкулеза решенной. Однако опыт, накопленный фтизиатрией в последующие десятилетия, показал, что после того, как интенсивное размножение бактериальной популяции подавлено в результате химиотерапии, продолжается персистирование части микобактерий, которые сохраняются, главным образом, внутриклеточно (внутри фагоцитов). Подавить жизнедеятельность этой части МБТ очень трудно, так как большинство химиопрепаратов не действуют на внутриклеточно расположенные микобактерии. Оказалось также, что при монотерапии (лечение одним противотуберкулезным препаратом), нерегулярном приеме лекарств быстро формируется лекарственная устойчивость МБТ.
Таким образом, было обосновано одновременное назначение больным нескольких противотуберкулезных средств, созданы новые химиопрепараты, продолжительность лечения постепенно увеличивалась и достигла 12–18 мес, что не всегда было оправдано. Было установлено, что низкая эффективность лечения туберкулеза в большей степени обусловлена нерегулярным приемом препаратов, чем недостаточной длительностью его. В течение последнего десятилетия по рекомендации ВОЗ во многих странах внедрили методику контролируемой краткосрочной химиотерапии (ДОТС), которая оказалась эффективной и позволила сократить длительность лечения до 6–9 мес за счет использования рациональных режимов химиотерапии.
Режимы химиотерапии
Понятие “режим химиотерапии” включает определенную комбинацию химиопрепаратов, их дозировку, способ использования в виде однократной суточной дозы или разделенной на 2–3 приема, путь введения (внутрь, внутривенно, в виде аэрозолей, эндобронхиальных вливаний, ректально) и ритм приема (ежедневно или прерывисто).
Интенсивность и длительность химиотерапии больного туберкулезом определяется наличием или отсутствием бактериовыделения, тяжестью и распространенностью легочного процесса, сведениями о предшествующем лечении. Учет указанных факторов позволяет отнести каждый случай заболевания к определенной категории (табл. 1).
Курс противотуберкулезной химиотерапии состоит из двух фаз. Назначение первой фазы – интенсивной – подавить размножение бактериальной популяции, добиться ее количественного уменьшения. Главной задачей второй фазы является предупреждение размножения оставшихся микобактерий.
В первой фазе химиотерапии впервые выявленным бациллярным больным назначают 4 основных противотуберкулезных препарата. Интенсивную химиотерапию проводят 2 мес, а при сохранении бактериовыделения по данным микроскопии мазка – 3 мес. Во второй фазе химиотерапии у впервые выявленных больных используют 2 препарата в течение 4 мес ежедневно или через день.
Впервые выявленным больным, лечившимся нерегулярно или прервавшим лечение, а также больным с рецидивом туберкулеза, в интенсивной фазе рекомендуется назначение 5 химиопрепаратов в течение 2 мес, затем в течение еще 1 месяца применяют 4 химиопрепарата (отменяется стрептомицин). Вторую фазу химиотерапии у этой категории больных рекомендуется проводить 3 противотуберкулезными препаратами в течение последующих 5 мес ежедневно или через день.
Больным, у которых при первоначальном исследовании мокроты не были выявлены МБТ, интенсивную фазу химиотерапии проводят тремя основными противотуберкулезными препаратами, после чего переходят на прием двух препаратов в течение 4 мес (см. табл. 1).
Больные хроническими формами туберкулеза легких должны лечиться по индивидуальным схемам химиотерапии с учетом устойчивости микобактерий к химиопрепаратам (табл. 2).
Эффективность проводимой химиотерапии оценивают по динамике клинических проявлений, бактериовыделения, рентгенологически выявляемых изменений в легких (уменьшению инфильтративных изменений в легких и закрытию каверн).
Обеспечение регулярного приема больным назначенных химиопрепаратов является важной задачей в течение всего периода лечения. В стационаре прием назначенных химиопрепаратов осуществляется под контролем медицинского персонала с точным учетом принятых медикаментов. В амбулаторных условиях прием химиопрепаратов осуществляется под контролем медицинского персонала в противотуберкулезных диспансерах либо на дому у больного. Контроль облегчается при применении всей суточной дозы в один прием, при интермиттирующем лечении.
Удобство контролируемой химиотерапии обеспечивается также применением комбинированных таблетированных форм, содержащих 2–4 основных химиопрепарата. Майрин содержит этамбутол, изониазид и рифампицин, в майрин П дополнительно включен пиразинамид. Рифакомб плюс, рифатер и трикокс включают изониазид, пиразинамид и рифампицин; рифинаг и тибитекс - изониазид и рифампицин. Их применение значительно облегчает контроль за химиотерапией, особенно в амбулаторных условиях. Нерегулярный прием химиопрепаратов может привести к развитию лекарственной устойчивости МБТ и прогрессированию процесса.
Часть больных в процессе лечения нуждается в изменении режима химиотерапии вследствие возникновения неустранимых побочных реакций на препараты, либо обнаружения лекарственной устойчивости, либо отсутствия эффекта от проводимой терапии, что чаще всего выражается продолжающимся бактериовыделением и сохранением каверны в легком. Режим химиотерапии целесообразно менять не позже, чем через 2–3 мес после начала лечения, поскольку к концу 3-го месяца уже имеются результаты количественного исследования мокроты методом микроскопии до начала лечения и в процессе химиотерапии; результаты посева мокроты, сделанного до начала лечения, с данными о чувствительности МБТ к химиопрепаратам; динамика рентгенологических изменений в легких. Своевременная коррекция химиотерапии значительно повышает ее эффективность, способствует более быстрому заживлению деструктивных изменений в легких. Индивидуализация лечебной тактики осуществляется на основании информации, полученной на протяжении всего периода химиотерапии.
Причины неэффективности лечения
Положительных результатов лечения удается достичь не у всех больных. Среди важнейших причин неэффективности лечения больных туберкулезом можно назвать побочное действие противотуберкулезных препаратов; заметное увеличение частоты остропрогрессирующих форм туберкулеза, протекающих на фоне выраженного иммунодефицита с развитием необратимых изменений в легких; сопутствующие туберкулезу заболевания; плохое обеспечение противотуберкулезными химиопрепаратами, отсутствие контроля за приемом лекарств, недисциплинированность больных и др. Однако наиболее важной причиной недостаточной эффективности химиотерапии остается лекарственная резистентность МБТ.
Лекарственная резистентность МБТ
Больные туберкулезом, выделяющие лекарственно-устойчивые штаммы МБТ, длительное время остаются бактериовыделителями и могут заражать окружающих лекарственно-резистентными возбудителями. Чем больше число больных, выделяющих лекарственно-устойчивые МБТ, тем выше риск распространения инфекции среди здоровых лиц и появления новых случаев заболевания туберкулезом с первичной лекарственной устойчивостью.
По определению экспертов ВОЗ [2], лекарственно-устойчивый туберкулез – это случай туберкулеза легких с выделением МБТ, устойчивых к одному и более противотуберкулезным препаратам. В последние годы в связи с ухудшением эпидемической ситуации существенно увеличилось число больных, выделяющих МБТ, устойчивые к основным противотуберкулезным препаратам. По данным ЦНИИ туберкулеза РАМН, у 50% впервые выявленных и ранее не леченных противотуберкулезными препаратами больных в мокроте определялись лекарственно-устойчивые МБТ, из них у 27,7% имелась устойчивость к 2 основным противотуберкулезным препаратам – изониазиду и рифампицину. При хроническом фиброзно-кавернозном туберкулезе частота выявления лекарственно-уcтойчивых МБТ возрастает до 95,5% [3].
Феномен лекарственной устойчивости МБТ имеет важное клиническое значение. Существует тесная взаимосвязь количественных изменений микобактериальной популяции и изменения ряда биологических свойств МБТ, одним из которых является лекарственная устойчивость. В активно размножающейся бактериальной популяции всегда имеется некоторое количество лекарственно-устойчивых мутантов, которые практического значения не имеют, но по мере сокращения бактериальной популяции под влиянием химиотерапии изменяется соотношение между количеством лекарственно-чувствительных и устойчивых МБТ [4]. В этих условиях происходит размножение главным образом устойчивых МБТ, эта часть бактериальной популяции увеличивается. В клинической практике необходимо исследовать лекарственную чувствительность МБТ и результаты этого исследования сопоставлять с динамикой туберкулезного процесса в легких [3].
Методы обнаружения лекарственной устойчивости МБТ
Повышение эффективности лечения туберкулеза, вызванного лекарственно-устойчивыми МБТ, возможно за счет использования ускоренных методов обнаружения лекарственной устойчивости МБТ, что позволяет своевременно изменять режим химиотерапии, отменив препараты, к которым выявлена устойчивость МБТ, и назначить противотуберкулезные средства, к которым чувствительность сохранена.
Исследование лекарственной устойчивости МБТ непрямым методом осуществляют после получения культуры МБТ, выделенных от больного, что требует от 30 до 45 сут. Коррекция химиотерапии в таком случае носит отсроченный характер и проводится, как правило, уже на конечном этапе интенсивной фазы химиотерапии.
Лекарственную устойчивость МБТ в настоящее время определяют методом абсолютных концентраций, который основан на добавлении в плотную питательную среду Левенштейна–Йенсена стандартных концентраций противотуберкулезных препаратов, которые принято называть предельными. Для изониазида она составляет 1 мкг/мл, рифампицина – 40 мкг/мл, стрептомицина – 10 мкг/мл, этамбутола – 2 мкг/мл, канамицина – 30 мкг/мл, амикацина – 8 мкг/мл, протионамида (этионамида) – 30 мкг/мл, офлоксацина (таривида) – 5 мкг/мл, циклосерина – 30 мкг/мл и пиразинамида – 100 мкг/мл. Определение лекарственной устойчивости МБТ к пиразинамиду проводят на специально приготовленной яичной среде с рН 5,5–5,6. Культура МБТ считается устойчивой, если в пробирке выросло более 20 колоний.
В последнее время для ускоренного определения лекарственной устойчивости применялся радиометрический метод с использованием автоматической системы BACTEC – 460 TB (Becton Dickinson Diagnostic Systems, Sparks, MD), который позволяет выявлять лекарственную устойчивость МБТ на жидкой среде Middlebrook 7H10 через 8–10 дней.
Другая не менее важная задача – правильное лечение впервые выявленных больных туберкулезом легких с использованием комбинации из 4–5 основных противотуберкулезных препаратов до получения данных лекарственной устойчивости МБТ [1]. В этих случаях существенно повышается вероятность того, что даже при наличии первичной лекарственной устойчивости МБТ бактериостатическое действие окажут 2 или 3 химиопрепарата, к которым чувствительность сохранена. Именно несоблюдение фтизиатрами научно обоснованных комбинированных режимов химиотерапии при лечении впервые выявленных больных и назначение им в большинстве случаев только 3 химиопрепаратов является грубой врачебной ошибкой, что, в конечном счете, ведет к формированию вторичной лекарственной устойчивости МБТ.
Наличие у больного туберкулезом легких лекарственно-резистентных МБТ существенно снижает эффективность лечения, приводит к появлению хронических и неизлечимых форм, а в ряде случаев и к летальным исходам. Особенно тяжело протекают поражения легких, вызванные полирезистентными МБТ, которые устойчивы как минимум к изониазиду и рифампицину, т.е. к основным и самым активным противотуберкулезным препаратам [4]. Множественная лекарственная устойчивость МБТ является на сегодня наиболее тяжелой формой бактериальной устойчивости, а специфические поражения легких, вызванные такими микобактериями, называются полирезистентным туберкулезом легких [2]. Лекарственная устойчивость МБТ имеет не только клиническое и эпидемиологическое, но и экономическое значение, так как лечение таких больных обходится намного дороже, чем больных с МБТ, чувствительными к основным химиопрепаратам. Разработка лечения лекарственно-резистентного туберкулеза легких является одним из приоритетных направлений современной фтизиатрии.
Возможные режимы химиотерапии при выявлении лекарственной устойчивости МБТ больных с впервые выявленным деструктивным туберкулезом легких представлены в табл. 2.
Для проведения эффективной химиотерапии больных хроническими формами туберкулеза легких с множественной лекарственной устойчивостью МБТ используют комбинации резервных противотуберкулезных препаратов, включающие пиразинамид и этамбутол, к которым медленно и довольно редко формируется вторичная лекарственная устойчивость [4]. В табл. 2 представлены схемы химиотерапии для больных с множественной лекарственной устойчивостью МБТ, ранее длительно получавших противотуберкулезную терапию.
Все резервные препараты обладают довольно низкой бактериостатической активностью, поэтому общая длительность химиотерапии у больных с хроническим фиброзно-кавернозным туберкулезом легких и множественной лекарственной устойчивостью МБТ должна составлять не менее 21 мес.
При отсутствии эффекта от проводимой химиотерапии резервными противотуберкулезными препаратами возможно применение хирургических методов лечения, наложение лечебного искусственного пневмоторакса или пневмоперитонеума. Оперировать следует после максимально возможного сокращения микобактериальной популяции, что определяется с помощью микроскопии или культурального исследования мокроты. После операции следует продолжать применять тот же режим химиотерапии минимум 18–20 мес. Лечебный искусственный пневмоторакс должен продолжаться у больных полирезистентным туберкулезом легких не менее 12 мес.
Повышение эффективности лечения больных с лекарственно-устойчивым туберкулезом легких в значительной степени зависит от своевременной коррекции химиотерапии и применения противотуберкулезных препаратов, к которым сохранена чувствительность. Для лечения больных лекарственно-устойчивым и, особенно, полирезистентным туберкулезом легких необходимо использовать резервные препараты: протионамид (этионамид), амикацин (канамицин), офлоксацин. Эти препараты в отличие от основных (изониазид, рифампицин, пиразинамид, этамбутол, стрептомицин) намного более дорогостоящие, менее эффективные и имеют много побочных эффектов. Они должны быть доступны только для специализированных противотуберкулезных учреждений.
Эффективное лечение больных туберкулезом достигается за счет подавления микобактериальной популяции путем применения современных режимов контролируемой химиотерапии основными противотуберкулезными препаратами: изониазидом, рифампицином, пиразинамидом, стрептомицином, этамбутолом. Важнейшими факторами, снижающими эффективность химиотерапии, следует признать резистентность МБТ к противотуберкулезным препаратам, характер специфического процесса и побочные реакции на химиопрепараты.
Повышение эффективности лечения больных с лекарственно-устойчивым туберкулезом легких в значительной степени зависит от своевременной коррекции химиотерапии и применения противотуберкулезных препаратов, к которым сохранена чувствительность. Для лечения больных лекарственно-устойчивым и, особенно, полирезистентным туберкулезом легких необходимо использовать резервные препараты: протионамид (этионамид), амикацин (канамицин), офлоксацин.
1. Лечение туберкулеза: рекомендации для национальных программ.- ВОЗ - Женева, 1998. - Пер. с англ. 77.
2. Рекомендации по лечению резистентных форм туберкулеза. - ВОЗ. - Женева, 1998. - Пер. с англ. 47.
3. Чуканов В.И. Основные принципы лечения больных туберкулезом легких. //Русс. мед. журн. 1998; 17: 1138–42.
Повышение эффективности лечения больных туберкулезом – наиболее актуальная задача фтизиатрии. Основной путь для ее решения – подавление микобактериальной популяции путем применения контролируемой химиотерапии укороченной длительности с использованием наиболее активных противотуберкулезных препаратов и современных схем химиотерапии, а также усиление репаративных процессов в пораженных органах средствами и методами патогенетического воздействия на организм больного.
Среди наиболее неблагоприятных факторов, снижающих эффективность химиотерапии, следует признать резистентность МБТ туберкулеза к противотуберкулезным препаратам, характер специфического процесса и побочные реакции на противотуберкулезные препараты.
To enhance therapeutical efficiency in patients with tuberculosis is the most urgent task of phthisiologists. The main way of solving the problem is to eliminate a mycobacterial population by short-term controlled chemotherapy by using the most active antituberculous drugs and currently available drug treatment regimens and to enhance reparative processes in the involved organs by employing pathogenetic means and methods.
Drug-resistance of Mycobacterium tuberculosis, the pattern of the specific process, and side effects of antituberculous agents should be recognized to be one of the most poor factors that reduce the efficacy of drug therapy.
В.И. Чуканов — доктор мед. наук, профессор, руководитель отдела фтизиатрии Центрального НИИ туберкулеза РАМН, Москва
V.I. Chukanov — prof. MD, Head, Department of Phthisiology, Central Research Institute of Tuberculosis, Russian Academy of Medical Sciences, Moscow
Н еблагополучная эпидемиологическая ситуация по туберкулезу обусловливает актуальность разработки и внедрения в практику эффективных методов лечения больных туберкулезом. Важным в этой проблеме представляется комплексный (как медицинский, так и социально-экономический) подход к лечению туберкулеза, который позволит значительно уменьшить резервуар туберкулезной инфекции.
Излечение больных туберкулезом зависит от 2 взаимосвязанных факторов: подавления размножающейся микобактериальной популяции с помощью противотуберкулезных препаратов и регрессии туберкулезных изменений в пораженных органах с развитием репаративных процессов.
Среди комплекса лечебных мероприятий, направленных на излечение больных туберкулезом, этиотропная химиотерапия занимает ведущее место. И хотя в течение нескольких десятилетий накоплен значительный опыт по применению противотуберкулезных препаратов, в современных условиях возникает необходимость постоянного совершенствования режимов химиотерапии: выбора определенной комбинации противотуберкулезных препаратов, их дозировки, способа применения (в виде однократной суточной дозы или разделенной на 2 – 3 приема), пути введения (внутрь, внутривенно, в виде аэрозолей, эндобронхиальных вливаний, ректально) и ритма приема препаратов (ежедневного или интермиттирующего).
Клиническая эффективность противотуберкулезных препаратов определяется многими факторами, среди которых главными являются: массивность самой микобактериальной популяции, чувствительность или устойчивость находящихся в ней микобактерий туберкулеза (МБТ) к применяемым препаратам, способность отдельных особей к быстрому размножению; уровень создаваемой бактериостатической концентрации препарата в крови и степень проницаемости в очаги поражения; взаимодействие с другими лекарственными средствами; способность препаратов влиять на внутриклеточно расположенные (фагоцитированные) МБТ; свойство препаратов индуцировать лекарственную резистентность возбудителя, а также переносимость больными противотуберкулезных препаратов и их комбинаций.
В основе лечебного действия противотуберкулезных препаратов лежит их непосредственное бактериостатическое и бактерицидное влияние на микробную клетку. Препараты способствуют разрушению МБТ, подавляют их репликацию, что приводит к уменьшению бактериальной популяции в организме больного. Наиболее существенным для эффективного лечения является бактерицидное действие некоторых противотуберкулезных препаратов (в частности, изониазида и рифампицина), способных быстро убивать большое количество активно размножающихся МБТ. При уменьшении бактериальной популяции применение таких препаратов, как рифампицин и пиразинамид, позволяет добиться и стерилизующего эффекта, т.е. подавить и медленно размножающиеся МБТ.
Следует также иметь в виду, что противотуберкулезные препараты оказывают разное влияние на внутриклеточно и внеклеточно расположенные МБТ. Так, при прогрессировании процесса происходит интенсивное размножение МБТ в организме человека, их выход в ткани пораженных органов, распространение лимфо-бронхогенным и гематогенным путем, в результате чего появляются новые участки воспаления, развивается казеозный некроз. Большинство МБТ в этот период находится внеклеточно, а та часть бактериальной популяции, которая оказалась фагоцитированной в процессе воспалительной реакции, вследствие интенсивного внутриклеточного размножения обусловливает разрушение фагоцитов и вновь оказывается расположенной внеклеточно.
Таким образом, внутриклеточная локализация МБТ на этом этапе является сравнительно кратковременной. На активно размножающуюся бактериальную популяцию выраженное антибактериальное действие оказывают практически все противотуберкулезные препараты.
По мере затихания туберкулезного процесса величина бактериальной популяции уменьшается вследствие подавления размножения МБТ. В условиях продолжающейся химиотерапии и уменьшения бактериальной популяции в организме больного сохраняется часть МБТ, которые находятся в состоянии персистирования. Персистирующие МБТ нередко выявляются только микроскопическим методом, так как при посеве на питательные среды они не растут. Такие МБТ называют “спящими” или “дремлющими”, иногда – “убитыми”. В качестве одного из вариантов персистирования МБТ возможна их трансформация в L-формы или мелкозернистые формы.
На этапе, когда интенсивное размножение бактериальной популяции сменяется состоянием персистирования остающейся ее части, МБТ находятся главным образом внутриклеточно (внутри фагоцитов). Подавить жизнедеятельность внутриклеточно расположенных МБТ очень трудно, так как ряд препаратов оказывает бактериостатическое действие на внутриклеточно расположенные возбудители значительно слабее, чем на находящиеся вне макрофагов.
Еще несколько лет назад считали, что эффективность химиотерапии во многом зависит от ее длительности. В период появления первых противотуберкулезных препаратов продолжительность лечения была сравнительно небольшой (1 – 3 мес). По мере накопления опыта химиотерапии продолжительность ее постепенно увеличивалась и достигла 12 – 18 мес. В последние годы взгляды на необходимую продолжительность противотуберкулезной терапии были пересмотрены. Апробированная во многих странах методика контролируемой химиотерапии укороченной длительности (ДОТС) показала свою высокую эффективность и позволила значительно сократить длительность лечения (до 6 – 9 мес) за счет использования рациональных режимов химиотерапии, способствующих быстрому подавлению микобактериальной популяции и прекращению бактериовыделения, что имеет важное клиническое и эпидемиологическое значение. В связи с различным состоянием бактериальной популяции на разных этапах течения болезни в процессе химиотерапии в последние годы стало принятым делить весь период лечения химиопрепаратами на 2 этапа. Следует указать, что такое деление периодов химиотерапии отечественные фтизиатры использовали уже давно.
Первый этап характеризуется проведением интенсивной насыщенной химиотерапии; цель его – подавить размножение бактериальной популяции, добиться ее количественного уменьшения. Назначение второго этапа долечивания – воздействовать на оставшуюся бактериальную популяцию, в большинстве своем находящуюся внутриклеточно в виде персистирующих форм МБТ, предупредить размножение оставшихся МБТ.
Согласно современным представлениям (схема), на первом этапе химиотерапии, когда происходит быстрое размножение МБТ, впервые выявленным бациллярным больным назначают 4 противотуберкулезных препарата (изониазид, рифампицин, пиразинамид, стрептомицин или этамбутол). Такая интенсивная химиотерапия проводится в течение 2 мес, а при сохранении бактериовыделения, подтвержденном данными микроскопии мазка, – 3 мес. У впервые выявленных больных на втором этапе химиотерапии, когда основная масса микобактериальной популяции уже подавлена, используют 2 препарата (изониазид и рифампицин) в течение 4 мес ежедневно или через день. Впервые выявленным больным, лечившимся нерегулярно или прервавшим лечение, а также больным с рецидивом туберкулеза, в интенсивной фазе рекомендуется назначение 5 препаратов (изониазид, рифампицин, пиразинамид, стрептомицин и этамбутол) в течение 2 мес, затем в течение еще 1 мес применяют 4 препарата (отменяется стрептомицин). Второй этап химиотерапии у этой категории больных рекомендуется проводить 3 противотуберкулезными препаратами в течение последующих 5 мес ежедневно или через день.
Больным, у которых при первоначальном исследовании мокроты не были выявлены МБТ, интенсивный этап химиотерапии можно проводить 3 препаратами (изониазидом, рифампицином, пиразинамидом) в течение 2 мес, после чего продолжить прием 2 препаратов (изониазида и рифампицина или этамбутола) в течение 4 мес.
Больных хроническими формами туберкулеза органов дыхания следует лечить по индивидуальным схемам химиотерапии с учетом устойчивости МБТ к препаратам и дальнейшей модификацией режима химиотерапии в случаях обнаружения вторичной устойчивости к применяемым препаратам. Чаще всего таким больным, как и больным, у которых выявлена полирезистентность МБТ, применяют препараты резерва – канамицин, амикацин, протионамид, этамбутол, а также производные фторхинолонов (офлоксацин, ломефлоксацин, ципрофлоксацин).
Эффективность проводимой химиотерапии оценивается по нескольким параметрам: клиническим (уменьшение или исчезновение симптомов интоксикации и “грудных” жалоб); микробиологическим (уменьшение массивности бактериовыделения по данным количественной ее оценке); рентгенологическим (уменьшение инфильтративно-воспалительных изменений в легких и заживление каверн).
При проведении химиотерапии важной задачей является обеспечение регулярного приема больным назначенных противотуберкулезных препаратов в течение всего периода лечения. Методы, обеспечивающие регулярность химиотерапии, тесно связаны с организационными формами лечения в больничных (санаторных) и амбулаторных условиях. В больничных условиях прием назначенных противотуберкулезных препаратов осуществляется в присутствии медицинского персонала с точным учетом принятых медикаментов. Одним из видов контролируемой химиотерапии является парентеральное применение препаратов. В амбулаторных условиях практикуют несколько методов:
1. Прием противотуберкулезных препаратов в присутствии медицинского персонала, который осуществляется: а) в противотуберкулезных диспансерах; б) на дому у больного. Контроль за приемом противотуберкулезных препаратов облегчается при применении всей суточной дозы в один прием, а также интермиттирующем лечении.
2. Прием самим больным противотуберкулезных препаратов, выданных диспансером на определенный срок, чаще всего на 7 дней, с систематическим контролем за расходованием медикаментов.
В последнее время появились комбинированные таблетированные формы, содержащие 2 или 3 наиболее активных препарата. Например, рифатер или трикокс включают 3 препарата – изониазид, рифампицин, пиразинамид; рифанаг и тибинекс включают 2 препарата – изониазид и рифампицин. Их применение значительно облегчает контроль за химиотерапией, особенно в амбулаторных условиях. Нерегулярный прием противотуберкулезных препаратов может привести к развитию лекарственной устойчивости МБТ и прогрессированию процесса.
Изложенные положения составляют основную схему программированной химиотерапии. Вместе с тем по ходу лечения у части больных приходится вносить изменения в составленную после обследования программу химиотерапии. Необходимость смены препаратов вызвана рядом причин: во-первых, наличием неустранимых побочных реакций, вызванных теми или иными препаратами; во-вторых, обнаружением первичной лекарственной устойчивости МБТ туберкулеза к препаратам, данные о которой врач получает обычно через 2 – 3 мес после начала лечения; и, в-третьих, неэффективностью проводимой терапии, что чаще всего выражается продолжающимся бактериовыделением и сохранением каверны, а иногда медленным рассасыванием воспалительных изменений в легких. При недостаточном эффекте химиотерапии необходимо подобрать оптимальную методику лечения: изменить комбинацию препаратов, их дозы, способ введения лекарственных средств, дополнительно использовать патогенетические средства и физиотерапевтические методы лечения. В этих случаях целесообразнее всего менять режим химиотерапии не позже, чем через 2 – 3 мес после начала лечения. Чем позже меняется режим химиотерапии, тем длительнее оказывается период лечения. Следует учесть, что к концу третьего месяца уже имеются: а) результаты количественного исследования мокроты методом микроскопии до начала лечения и в процессе химиотерапии; б) результаты посева мокроты, сделанного до начала лечения, и определения лекарственной чувствительности МБТ; в) динамика рентгенологических изменений, в частности степень рассасывания воспалительных изменений в легких.
Индивидуализация лечебной тактики без достаточной информации, собранной в процессе лечения, невозможна, поэтому необходимо наблюдение за больными и на последующих этапах химиотерапии. Своевременно внесенная коррекция в процессе лечения значительно повышает эффективность химиотерапии, способствует более быстрому заживлению деструктивных изменений в легких.
Рекомендуемые схемы химиотерапии
Туберкулез легких – это инфекционная патология, вызываемая бациллой Коха, характеризующаяся различными в клинико-морфологическом отношении вариантами поражения легочной ткани. Многообразие форм туберкулеза легких обусловливает вариабельность симптоматики. Наиболее типичны для туберкулеза легких респираторные нарушения (кашель, кровохарканье, одышка) и симптомы интоксикации (длительный субфебрилитет, потливость, слабость). Для подтверждения диагноза используются лучевые, лабораторные исследования, туберкулинодиагностика. Химиотерапия туберкулеза легких проводится специальными туберкулостатическими препаратами; при деструктивных формах показано хирургическое лечение.
МКБ-10

Общие сведения
На сегодняшний день туберкулез легких представляет не только медико-биологическую, но и серьезную социально-экономическую проблему. По данным ВОЗ, туберкулезом инфицирован каждый третий житель планеты, смертность от инфекции превышает 3 млн. человек в год. Легочный туберкулез является самой частой формой туберкулезной инфекции. Удельный вес туберкулеза других локализаций (суставов, костей и позвоночника, гениталий, кишечника, серозных оболочек, ЦНС, глаз, кожи) в структуре заболеваемости значительно ниже.

Причины
Характеристика возбудителя
Отличительной чертой МБТ является их высокая устойчивость к внешним воздействиям (высоким и низким температурам, влажности, воздействию кислот, щелочей, дезинфектантов). Наименьшую стойкость возбудители туберкулеза легких демонстрируют к солнечному свету. Для человека опасность представляют туберкулезные бактерии человеческого и бычьего типа; случаи инфицирования птичьим типом микобактерий крайне редки.
Пути заражения
Основной путь заражения при первичном туберкулезе легких – аэрогенный: от больного открытой формой человека микобактерии распространяются с частичками слизи, выделяемыми в окружающую среду при разговоре, чихании, кашле; могут высыхать и разноситься с пылью на значительные расстояния. В дыхательные пути здорового человека инфекция чаще попадает воздушно-капельным или пылевым путем.
Меньшую роль в инфицировании играют алиментарный (при употреблении зараженных продуктов), контактный (при использовании общих предметов гигиены и посуды) и трансплацентарный (внутриутробный) пути. Причиной вторичного туберкулеза легких выступает повторная активация ранее перенесенной инфекции либо повторное заражение.
Факторы риска
Однако попадание МБТ в организм не всегда приводит к заболеванию. Факторами, на фоне которых туберкулез легких развивается особенно часто, считаются:
- неблагоприятные социально-бытовые условия
- курение и другие химические зависимости
- недостаточное питание
- иммуносупрессия (ВИЧ-инфекция, прием глюкокортикоидов, состояние после трансплантации органов)
- онкологические заболевания и др.
В группе риска по развитию туберкулеза легких находятся мигранты, заключенные, лица, страдающие наркотической и алкогольной зависимостью. Также имеет значение вирулентность инфекции и длительность контакта с больным человеком.
Патогенез
При снижении местных и общих факторов защиты микобактерии беспрепятственно проникают в бронхиолы, а затем в альвеолы, вызывая специфическое воспаление в виде отдельных или множественных туберкулезных бугорков или очагов творожистого некроза. В этот период появляется положительная реакция на туберкулин - вираж туберкулиновой пробы. Клинические проявления туберкулеза легких на этой стадии часто остаются нераспознанными. Небольшие очажки могут самостоятельно рассасываться, рубцеваться или обызвествляться, однако МБТ в них длительно сохраняются.
Классификация
Первичный туберкулез легких - это впервые развившаяся инфильтрация легочной ткани у лиц, не имеющих специфического иммунитета. Диагностируется преимущественно в детском и подростковом возрасте; реже возникает у лиц старшего и пожилого возраста, которые в прошлом перенесли первичную инфекцию, закончившуюся полным излечением. Первичный туберкулез легких может принимать форму:
- первичного туберкулезного комплекса (ПТК)
- туберкулеза внутригрудных лимфоузлов (ВГЛУ)
- хронически текущего туберкулеза.
Вторичный туберкулез легких развивается при повторном контакте с МБТ или в результате реактивации инфекции в первичном очаге. Основные вторичные клинические формы представлены:
Отдельно различают кониотуберкулез (туберкулез, развивающийся на фоне пневмокониозов), туберкулез верхних дыхательных путей, трахеи, бронхов; туберкулезный плеврит. При выделении больным МБТ в окружающую среду с мокротой говорят об открытой форме (ВК+) туберкулеза легких; при отсутствии бацилловыделения – о закрытой форме (ВК–). Также возможно периодическое бацилловыделение (ВК±).
Течение туберкулеза легких характеризуется последовательной сменной фаз развития:
- 1) инфильтративной
- 2) распада и обсеменения
- 3) рассасывания очага
- 4) уплотнения и обызвествления.
Симптомы туберкулеза легких
Первичный туберкулезный комплекс
Первичный туберкулезный комплекс сочетает в себе признаки специфического воспаления в легком и регионарный бронхоаденит. Может протекать бессимптомно или под маской простудных заболеваний, поэтому выявлению первичного туберкулеза легких способствуют массовые скрининги детей (проба Манту) и взрослых (профилактическая флюорография).
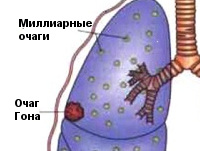
Чаще возникает подостро: больного беспокоит сухой кашель, субфебрилитет, утомляемость, потливость. При острой манифестации клиника напоминает неспецифическую пневмонию (высокая лихорадка, кашель, боль в груди, одышка). В результате лечения происходит рассасывание или обызвествление ПТК (очаг Гона). В неблагоприятных случаях может осложняться казеозной пневмонией, образованием каверн, туберкулезным плевритом, милиарным туберкулезом, диссеминацией микобактерий с поражением почек, костей, мозговых оболочек.
Туберкулез внутригрудных лимфоузлов
Признаки туберкулезной интоксикации включают отсутствие аппетита, снижение массы тела, утомляемость, бледность кожи, темные круги под глазами. На венозный застой в грудной полости может указывать расширение венозной сети на коже грудной клетки. Данная форма нередко осложняется туберкулезом бронхов, сегментарными или долевыми ателектазами легких, хронической пневмонией, экссудативным плевритом. При прорыве казеозных масс из лимфоузлов через стенку бронхов могут формироваться легочные очаги туберкулеза.
Очаговый туберкулез легких
Клиническая картина очагового туберкулеза малосимптомна. Кашель отсутствует или возникает редко, иногда сопровождается выделением скудной мокроты, болями в боку. В редких случаях отмечается кровохарканье. Чаще больные обращают внимание на симптомы интоксикации: непостоянный субфебрилитет, недомогание, апатию, пониженную работоспособность. В зависимости от давности туберкулезного процесса различают свежий и хронический очаговый туберкулез легких.
Течение очагового туберкулеза легких относительно доброкачественное. У больных с нарушенной иммунной реактивностью заболевание может прогрессировать в деструктивные формы туберкулеза легких.
Инфильтративный туберкулез легких
Клиническая картина инфильтративного туберкулеза легких зависит от величины инфильтрата и может варьировать от нерезко выраженных симптомов до острого лихорадочного состояния, напоминающего грипп или пневмонию. В последнем случае отмечается выраженная высокая температура тела, ознобы, ночная потливость, общая слабость. Со стороны органов дыхания беспокоит кашель с мокротой и прожилками крови.
В воспалительный процесс при инфильтративной форме туберкулеза легких часто вовлекается плевра, что обусловливает появление болей в боку, плеврального выпота, отставание пораженной половины грудной клетки при дыхании. Осложнениями инфильтративного туберкулеза легких могут стать казеозная пневмония, ателектаз легкого, легочное кровотечение и др.
Диссеминированный туберкулез легких
Может манифестировать в острой (милиарной), подострой и хронической форме. Тифоидная форма милиарного туберкулеза легких отличается преобладанием интоксикационного синдрома над бронхолегочной симптоматикой. Начинается остро, с нарастания температуры до 39-40 °С, головной боли, диспепсических расстройств, резкой слабости, тахикардии. При усилении токсикоза может возникать нарушение сознания, бред.
При легочной форме милиарного туберкулеза легких с самого начала более выражены дыхательные нарушения, включающие сухой кашель, одышку, цианоз. В тяжелых случаях развивается острая сердечно-легочная недостаточность. Менингеальной форме соответствуют симптомы поражения мозговых оболочек.
Подострое течение диссеминированного туберкулеза легких сопровождается умеренной слабостью, понижением работоспособности, ухудшением аппетита, похуданием. Эпизодически возникают подъемы температуры. Кашель продуктивный, не сильно беспокоит больного. Иногда первым признаком заболевания становится легочное кровотечение.
Хронический диссеминированный туберкулез легких при отсутствии обострения бессимптомен. Во время вспышки процесса клиническая картина близка к подострой форме. Диссеминированный туберкулеза легких опасен развитием внелегочного туберкулеза, спонтанного пневмоторакса, тяжелых легочных кровотечений, амилоидоза внутренних органов.
Кавернозный и фиброзно-кавернозный туберкулез легких
Характер течения кавернозного туберкулезного процесса волнообразный. В фазу распада нарастают интоксикационные симптомы, гипертермия, усиливается кашель и увеличивается количество мокроты, возникает кровохарканье. Часто присоединяется туберкулез бронхов и неспецифический бронхит.
Фиброзно-кавернозный туберкулез легких отличается формированием каверн с выраженным фиброзным слоем и фиброзными изменениями легочной ткани вокруг каверны. Протекает длительно, с периодическими обострениями общеинфекционной симптоматики. При частых вспышках развивается дыхательная недостаточность II-III степени.
Осложнениями, связанными с деструкцией легочной ткани, являются профузное легочное кровотечение, бронхоплевральный свищ, гнойный плеврит. Прогрессирование кавернозного туберкулеза легких сопровождается эндокринными расстройствами, кахексией, амилоидозом почек, туберкулезным менингитом, сердечно-легочной недостаточностью – в этом случае прогноз становится неблагоприятным.
Цирротический туберкулез легких
Является исходом различных форм туберкулеза легких при неполной инволюции специфического процесса и развитии на его месте фиброзно-склеротических изменений. При пневмоциррозе бронхи деформированы, легкое резко уменьшено в размерах, плевра утолщена и нередко обызвествлена.
Изменения, происходящие при цирротическом туберкулезе легких, обусловливают ведущие симптомы: выраженную одышку, тянущую боль в груди, кашель с гнойной мокротой, кровохарканье. При обострении присоединятся признаки туберкулезной интоксикации и бацилловыделение. Характерным внешним признаком пневмоцирроза служит уплощение грудной клетки на стороне поражения, сужение и втянутость межреберных промежутков. При прогрессирующем течении постепенно развивается легочное сердце. Цирротические изменения в легких необратимы.
Туберкулома легкого
Представляет собой инкапсулированный казеозный очаг, сформировавшийся в исходе инфильтративного, очагового или диссеминированного процесса. При стабильном течении симптомы не возникают, образование выявляется при рентгенографии легких случайно. В случае прогрессирующей туберкуломы легкого нарастает интоксикация, появляется субфебрилитет, боль в груди, кашель с отделением мокроты, возможно кровохарканье. При распаде очага туберкулома может трансформироваться в кавернозный или фиброзно-кавернозный туберкулез легких. Реже отмечается регрессирующее течение туберкуломы.
Диагностика
Диагноз той или иной формы туберкулеза легких выставляется врачом-фтизиатром на основании совокупности клинических, лучевых, лабораторных и иммунологических данных. Для распознавания вторичного туберкулеза большое значение имеет подробный сбор анамнеза. Для подтверждения диагноза проводится:
- Лучевая диагностика.Рентгенография легких является обязательным диагностической процедурой, позволяющей выявить характер изменений в легочной ткани (инфильтративный, очаговый, кавернозный, диссеминированный и т. д.), определить локализацию и распространенность патологического процесса. Выявление кальцинированных очагов указывает на ранее перенесенный туберкулезный процесс и требует уточнения данных с помощью КТ или МРТ легких.
- Анализы. Обнаружение МБТ достигается неоднократным исследованием мокроты (в т. ч. с помощью ПЦР), промывных вод бронхов, плеврального экссудата. Но сам по себе факт отсутствия бацилловыделения не является основанием для исключения туберкулеза легких. Современные иммунологические тесты позволяют выявить туберкулезную инфекцию почти со 100%-ной вероятностью. К ним относятся QuantiFERON и Т-спот. ТБ.
- Туберкулинодиагностика. К методам туберкулинодиагностики относятся диаскин-тест, пробы Пирке и Манту, однако сами по себе данные методы могут давать ложные результаты. Иногда для подтверждения туберкулеза легких приходится прибегать к пробному лечению противотуберкулезными препаратами с оценкой динамики рентгенологической картины.
По результатам проведенной диагностики туберкулез легких дифференцируют с пневмонией, саркоидозом легких, периферическим раком легкого, доброкачественными и метастатическими опухолями, пневмомикозами, кистами легких, абсцессом, силикозом, аномалиями развития легких и сосудов. Дополнительные методы диагностического поиска могут включать бронхоскопию, плевральную пункцию, биопсию легкого.

Лечение туберкулеза легких
Во фтизиатрической практике сформировался комплексный подход к лечению туберкулеза легких, включающий медикаментозную терапию, при необходимости - хирургическое вмешательство и реабилитационные мероприятия. Лечение проводится поэтапно: сначала в тубстационаре, затем в санаториях и, наконец, амбулаторно. Режимные моменты требуют организации лечебного питания, физического и эмоционального покоя.
- Противотуберкулезная терапия. Ведущая роль отводится специфической химиотерапии с помощью препаратов с противотуберкулезной активностью. Для терапии различных форм туберкулеза легких разработаны и применяются 3-х, 4-х и 5-тикомпонентные схемы (в зависимости от количества используемых препаратов). К туберкулостатикам первой линии (обязательным) относятся изониазид и его производные, пиразинамид, стрептомицин, рифампицин, этамбутол; средствами второго ряда (дополнительными) служат аминогликозиды, фторхинолоны, циклосерин, этионамид и др. Способы введения препаратов различны: перорально, внутримышечно, внутривенно, эндобронхиально, внутриплеврально, ингаляторно. Курсы противотуберкулезной терапии проводят длительно (в среднем 1 год и дольше).
- Патогенетическая терапия. При туберкулезе легких включает прием противовоспалительных средств, витаминов, гепатопротекторов, инфузионную терапию и пр. В случае лекарственной резистентности, непереносимости противотуберкулезных средств, при легочных кровотечениях используется коллапсотерапия.
- Хирургическое лечение. При соответствующих показаниях (деструктивных формах туберкулеза легких, эмпиеме, циррозе и ряде др.) применяются различные оперативные вмешательства: кавернотомию, торакопластику, плеврэктомию, резекцию легких.
Профилактика
Профилактика туберкулеза легких является важнейшей социальной проблемой и приоритетной государственной задачей. Первым шагом на этом пути является обязательная вакцинация новорожденных, детей и подростков. При массовых обследованиях в дошкольных и школьных учреждениях используется постановка внутрикожных туберкулиновых проб Манту. Скрининг взрослого населения осуществляется путем проведения профилактической флюорографии.
Очаговый туберкулез легких – форма вторичного туберкулеза, протекающая с формированием в легких очагов специфического воспаления не более 10 мм в диаметре. Протекает бессимптомно или малосимптомно. У части больных очаговый туберкулез легких может сопровождаться недомоганием, субфебрилитетом, болью в боку, сухим кашлем. В диагностике очагового туберкулеза наиболее информативны рентгенография легких, выявление МБТ в мокроте или бронхиальных смывах. В начальном периоде больным очаговым туберкулезом легких назначается комбинация из трех-четырех основных противотуберкулезных химиопрепаратов с последующим уменьшением до двух наименований.
МКБ-10

Общие сведения
Очаговый туберкулез легких – специфическое туберкулезное поражение, характеризующееся наличием в легких немногочисленных небольших (в пределах 1-2-х сегментов) фокусов продуктивного воспаления. Очаговый туберкулез относится к вторичной туберкулезной инфекции, т. е. обычно возникает через много лет после излечения первичного туберкулеза. Именно поэтому преобладающее большинство заболевших составляют взрослые пациенты. Среди других клинико-морфологических форм туберкулеза легких на долю очаговой формы приходится 15-20%. Отличительными особенностями очагового туберкулеза легких являются ограниченность зоны поражения одним-двумя сегментами, недеструктивный характер воспаления и латентное течение инфекции.
Причины
Очаговый туберкулез легких может возникнуть в результате экзогенной суперинфекции либо эндогенной активации инфекции в старых первичных очагах (кальцинатах). Экзогенное инфицирование возможно при тесном контакте с больными открытой формой туберкулеза в семье, противотуберкулезном диспансере, различных замкнутых коллективах. Заражение происходит аэрогенным путем. При этом вновь заболевшие выделяют микобактерии, устойчивые к тем же противотуберкулезным препаратам, что и источник инфекции. Роль экзогенной суперинфекции велика в районах с неблагополучной эпидемической ситуацией, неблагоприятными социально-бытовыми условиями проживания, при отсутствии специфической иммунизации населения.
Реактивация эндогенной инфекции происходит в старых туберкулезных очагах в легких (очаг Гона) или внутригрудных лимфатических узлах. В остаточных очагах микобактерии туберкулеза могут длительно персистировать в виде L-форм. Реверсия инфекции обычно происходит на фоне ослабления ранее сформированного противотуберкулезного иммунитета, чему способствуют:
- стрессы
- плохое питание
- переутомление
- лечение иммунодепрессантами
- сопутствующие заболевания (пневмокониозы, сахарный диабет, язвенная болезнь желудка и двенадцатиперстной кишки)
- вредные зависимости (алкоголизм, табакокурение, наркомания).
Патогенез
В патогенезе реактивации эндогенной инфекции, как причины очагового туберкулеза легких, определяющую роль играет лимфогематогенное рассеивание микобактерий по организму. Очаговый туберкулез легких имеет преимущественно верхнедолевую локализацию. Многочисленные исследования в области фтизиатрии и пульмонологии объясняют это различными факторами: ограниченной подвижностью верхушки легкого, ее слабой аэрацией, замедленным крово- и лимфотоком в этой области, вертикальным положением тела человека и даже гиперсенсибилизацией, способствующей избирательной фиксации микобактерий в верхушке легких.
Классификация
По давности течения очаговый туберкулез легких может быть свежим (мягкоочаговым) и хроническим (фиброзно-очаговым).
- Свежий туберкулез является начальной стадией вторичного процесса, развившегося у пациента, ранее инфицированного микобактериями и переболевшего первичной инфекцией. Морфологически характеризуется эндобронхитом и перибронхитом в области сегментарных бронхов, при вовлечении альвеол - лобулярной бронхопневмонией.
- Хронический очаговый туберкулез может развиваться как в результате рассасывания свежего очагового туберкулеза, так и в исходе других легочных форм – инфильтративной, диссеминированной, кавернозной. При этом воспалительные очаги инкапсулируются, замещаются соединительной тканью или обызвествляются. По сути, они представляют собой остаточные фиброзные очаги, однако при определенных условиях могут реактивироваться, вызывая обострение туберкулезного процесса и увеличение границ поражения. В свою очередь, при прогрессировании хронический очаговый процесс также может трансформироваться в инфильтративный, кавернозный или диссеминированный туберкулез легких.
В своем развитии очаговый туберкулез проходит фазы инфильтрации, распада и уплотнения. В зависимости от размеров различают мелкие (до 3 мм в диаметре), средние (до 6 мм), крупные (до 10 мм) очаги.
Симптомы очагового туберкулеза
Особенностью клинического течения туберкулеза легких является стертость или отсутствие симптоматики, поэтому большая часть случаев выявляется при профилактической флюорографии. Примерно у трети пациентов определяется слабо выраженный интоксикационный синдром и признаки поражения органов дыхания.
Признаки интоксикации включают в себя субфебрильную температуру по вечерам, ощущение жара, сменяющееся кратковременным познабливанием, потливость, недомогание, снижение аппетита, нарушение сна. Иногда при очаговом туберкулезе легких, как проявление специфической интоксикации, возникают признаки гипертиреоза: увеличение размеров щитовидной железы, тахикардия, блеск глаз, колебания веса, раздражительность. У женщин могут отмечаться нарушения менструального цикла по типу опсоменореи или пройоменореи.
Возможны жалобы на боль в боку, между лопатками, в плечах. Кашель обычно носит непостоянный характер, может быть сухим или сопровождаться скудным отделением мокроты. Изредка возникает кровохарканье.
Диагностика
Физикальные данные, выявляемые при объективном обследовании больного с подозрением на очаговый туберкулез легких, неспецифичны. Пальпация позволяет выявить небольшую болезненность и ригидность мышц плечевого пояса; лимфоузлы не увеличены. Перкуторный звук над очагом поражения приглушен, при аускультации прослушивается жесткое дыхание, во время покашливания больного определяются единичные мелкопузырчатые хрипы.
Туберкулиновые пробы при очаговом туберкулезе легких, как правило, нормергические, поэтому не играют существенной роли в диагностике. В редких случаях больные могут реагировать на подкожное введение туберкулина повышением температуры тела, увеличением количества мокроты, ускорением СОЭ и т. п. Методом скрининга также могут служить иммунологические реакции крови (Т-Спот.ТБ, квантиферон-тест), которые используются для подтверждения инфицированности.
Для определения активности туберкулеза исследуется мокрота на КУБ, производится бронхоскопия с забором бронхоальвеолярных смывов. Эндоскопическая картина при свежем очаговом туберкулезе легких характеризуется признаками эндобронхита.
Основную информацию о форме туберкулеза дает рентгенография легких, однако рентгенологическая картина может быть различной в зависимости от фазы и длительности процесса. При свежем очаговом туберкулезе обычно определяется 1-2 крупных очага и несколько средних или мелких; тени слабоконтурирующие, малоинтенсивные, округлой формы. Хронический очаговый туберкулез рентгенологически проявляется наличием плотных фокусов с очагами обызвествления и фиброзных тяжей; тени средней и высокой интенсивности, обычно малого и среднего размера. Дифференциальная диагностика проводится с неспецифической очаговой пневмонией, пневмомикозами, периферическим раком легкого.

КТ органов грудной клетки. Множественные очаговые изменения верхней доле правого легкого (верифицированный туберкулез)
При сомнительных данных прибегают к проведению тест-терапии: пациенту на 2-3 месяца назначают противотуберкулезные средства и отслеживают клинико-рентгенологическую и лабораторную динамику. При уменьшении или частичном рассасывании очагов диагноз очагового туберкулеза несомненен.
Лечение очагового туберкулеза легких
Лечение активного очагового туберкулеза легких проводится в противотуберкулезном стационаре, неактивного – в амбулаторных условиях под наблюдением фтизиатра. Стандартный режим химиотерапии предусматривает назначение не менее трех противотуберкулезных препаратов (рифампицин, изониазид, пиразинамид, этамбутол) на срок 2-3 месяца. В начальном периоде также может применяться стрептомицин. В фазе продолжения, которая длится 4-6 месяцев, оставляют прием двух препаратов (рифампицин+изониазид, изониазид+этамбутол). Общая длительность терапии очагового туберкулеза легких составляет 6-9 месяцев, а у отдельных пациентов – до одного года. Реабилитация после курса лечения осуществляется в условиях противотуберкулезного санатория.
Прогноз
Исход очаговой формы туберкулеза легких, как правило, благополучный. В результате полноценного лечения свежие очаги полностью рассасываются, наступает полное клиническое излечение. При хроническом течении очагового туберкулеза возможен переход в менее прогностически благоприятные формы (инфильтративную, кавернозную, диссеминированную). Чаще всего исходом служит пневмосклероз с формированием очагов фиброза или кальциноза. Такие пациенты в течение 1—2 лет нуждаются в проведении химиопрофилактики. Наибольшую сложность представляет лечение устойчивых к химиопрепаратам случаев. Профилактика очагового туберкулеза легких состоит в проведении рентгенологического обследования населения, санпросветработы, повышении неспецифической резистентности организма. В сокращении числа случаев вторичного туберкулеза легких большое значение имеет вакцинопрофилактика.
Читайте также:

