Что защищает ребенка от инфекций в утробе матери
Обновлено: 19.04.2024
В чем трудности диагностики ЦМВ? Каков механизм заражения ЦМВИ? В последние годы отмечена тенденция к увеличению среди беременных частоты вирусных инфекций и возросла их способность, при определенных условиях, к эпидемическому распространению.
В чем трудности диагностики ЦМВ?
Каков механизм заражения ЦМВИ?
В последние годы отмечена тенденция к увеличению среди беременных частоты вирусных инфекций и возросла их способность, при определенных условиях, к эпидемическому распространению.
Особое значение приобретает проблема цитомегаловирусной инфекции (ЦМВИ) при беременности, вследствие того что цитомегаловирус (ЦМВ) может явиться причиной акушерской патологии, эмбрио- и фетопатий, внутриутробной и перинатальной инфекции [1].
Наличие латентных форм ЦМВИ с атипичным течением, инаппарантными проявлениями и поражением тканей органов представляет большие трудности для своевременного распознавания инфекции и является причиной диагностических ошибок.
Среди родившихся живыми 0,2-2,2% детей внутриутробно инфицированы цитомегаловирусом. Внутриутробная ЦМВИ, вне зависимости от формы заболевания, может представлять опасность вследствие поражения ЦНС и привести к возникновению психомоторных нарушений, умственной отсталости детей даже через несколько лет после родов [2].
Беременным принадлежит значительный процент в эпидемиологии ЦМВИ, которая обнаруживается у них в два раза чаще, чем краснуха.
ЦМВИ может способствовать развитию осложнений во время беременности, родов и в послеродовом периоде. Акушерская патология наиболее часто проявляется в виде спонтанных выкидышей, мертворождений, рождения нежизнеспособных детей [3, 4, 11].
Проблема изучения цитомегаловирусной инфекции и ее влияния на течение и исход беременности, разработка основ комплексной профилактики и лечения крайне актуальны и особенно важны для практического здравоохранения.
Цитомегаловирус является крупным ДНК-геном со сравнительно низкой вирулентностью и особой способностью к резкому подавлению клеточного иммунитета.
Воздействия экзо- и эндогенных факторов приводят к снижению иммунитета и, соответственно, к активации хронической цитомегаловирусной инфекции.
Источниками инфекции могут являться носители ЦМВ, их биологические жидкости и выделения: кровь, моча, слезы, слюна, грудное молоко, спинномозговая жидкость, амниотическая жидкость, вагинальное отделяемое, слизь из носоглотки, сперма, фекалии и др.
Особый тропизм ЦМВ проявляет к слюнным железам. Отсюда реальная возможность передачи ЦМВ от матери к ребенку при поцелуях. Имеется прямая корреляционная зависимость между инфицированием цитомегаловирусом и сексуальной активностью партнеров.
С учетом возраста и интимности контактов между людьми выявляются две волны атаки ЦМВИ: первая достигается к трехлетнему возрасту, вторая — к периоду половой зрелости.
В большинстве случаев имеет место бессимптомное вирусоносительство или субклиническая, инаппарантная, хроническая инфекция, которая вне иммунодепрессии не вызывает никаких субъективных нарушений или объективных клинических проявлений. Длительной (нередко пожизненной) латенции способствует внутриклеточное сохранение ЦМВ в лимфоцитах, где он надежно защищен от действия специфических антител и интерферона.
Морфологические изменения проявляются в виде комплексов из цитомегалических клеток (ЦМК) и интерстициальной лимфогистиоцитарной инфильтрации [3].
Цитомегалические изменения наиболее часто наблюдаются в слюнных железах, легких, почках и головном мозге.
Описаны локальные цитомегалические повреждения глаз (хореоретиниты), кишечника (колиты), кожи (дерматиты), надпочечников, легких, почек, головного мозга [3].
Вопрос о влиянии срока беременности на передачу инфекции от матери к плоду остается открытым. Считается, что наибольшую угрозу для плода представляет развитие цитомегаловирусной инфекции в первой половине беременности.
Реактивация латентной инфекции ведет к передаче вируса от матери к плоду в 0,15%–0,36% случаев [5].
Возможно несколько путей передачи инфекции от матери к плоду:
- трансплацентарный;
- через инфицированные выделения в родовом канале;
- кормление инфицированным материнским молоком.
Трансплацентарная передача ЦМВИ наиболее часто приводит к инфицированию плода [7].
Цитомегаловирус от матери может проникать через плаценту в любом сроке беременности и вызывать поражение плода.
Цитомегаловирусная инфекция у беременных может быть первичной или рецидивирующей. Первичное материнское заражение ЦМВ, возникшее во время беременности, лучше всего диагностируется при изучении сероконверсии антител к ЦМВ. Присутствие антител IgG и IgM можно считать свидетельством первичной материнской инфекции. Рецидивирующая ЦМВ-инфекция во время беременности включает в себя как реактивацию собственного штамма ЦМВ, так и возможную реинфекцию новым штаммом вируса [9].
В большинстве случаев, в популяциях с высоким превалированием антител к ЦМВ, развитие ЦМВИ во время беременности скорее происходит в результате реинфицирования.
Врожденная ЦМВИ возникает либо после первичной инфекции, либо в результате обострения хронической. Более тяжелые последствия наблюдаются в период беременности при первичной инфекции.
При беременности в условиях иммунодефицита возникает неспецифическая депрессия иммунной системы. При ЦМВИ больше всего страдает клеточный иммунитет. Именно характер сдвигов в системе клеточного иммунитета во многом определяет течение и исход цитомегалии.
В ответ на внедрение вируса происходит выработка антител. При цитомегалии комплиментсвязывающие антитела сохраняются на протяжении всей жизни, что позволяет установить случаи имевшего в прошлом заболевания. Очевидно, что специфические антитела важны при защите против цитомегаловируса.
Антитела класса IgG свидетельствуют о том, что женщина ранее встречалась с инфекцией. Беременные имеют более интенсивную и длительную реакцию IgG. Высокие показатели титров антител свидетельствуют об активизации хронического процесса.
Отсутствие IgG в пуповинной сыворотке или сыворотке крови новорожденного исключает врожденную ЦМВИ, в то время как их присутствие может означать пассивный перенос от матери к плоду.
Значительно более высокий уровень IgG у новорожденного, чем у матери, может свидетельствовать о врожденной инфекции.
При исследовании в первые шесть месяцев жизни ребенка врожденная ЦМВИ исключается, если уровень IgG будет постепенно снижаться. Наличие IgМ в сыворотке крови характеризует первичную инфекцию. Антитела IgМ сохраняются в крови от 12 до 18 недель от начала первичной инфекции.
Антитела класса IgM через плаценту не переходят, их синтез осуществляется плодом и новорожденным в ответ на антигенное раздражение.
Механизм передачи ЦМВ предполагает тесный контакт между беременной (родильницей) и плодом (новорожденным). После беременности и родов ЦМВ можно найти почти во всех жидкостях тела, особенно в цервико-вагинальных выделениях и в грудном молоке, что может явиться источником пери- и постнатальной передачи ЦМВ от матери к новорожденному.
Передача инфекции может произойти с кровью при гемотрансфузиях и парентеральных манипуляциях, а также через поврежденную кожу и мацерированные слизистые. Установлено, что интранатальная или ранняя постнатальная передача ЦМВИ происходит в 10 раз чаще, чем трансплацентарная.
В послеродовом периоде эпидемиологическая опасность для новорожденного сохраняется в случаях нарушения женщиной гигиенических норм, а также вследствие передачи вируса с грудным молоком (20% серопозитивных матерей имеют ЦМВ в грудном молоке и 30% из них могут выделять вирус в молоко в течение года после родов) [8].
Перинатальные и постнатальные проявления ЦМВИ у детей почти всегда протекают в легкой форме и асимптоматично.
Многообразие вариантов течения ЦМВИ у беременных связано в большинстве случаев с бессимптомной латенцией и полиморфизмом клинических проявлений заболевания.
Варианты течения ЦМВИ и широкий спектр их проявлений обусловлены сложностью взаимоотношений между ЦМВ и клеткой хозяина.
Нередко клинические симптомы проявляются в виде субфебрильной температуры, ринофарингита, кашля, развития мононуклеозоподобного синдрома.
Диапазон клинических вариантов варьирует от слабо выраженного сиалоаденита и благоприятно текущего мононуклеозоподобного заболевания (лимфоцитоз, атипичные мононуклеары) до тяжелых поражений печени, легких и мозга.
У беременных симптоматическая ЦМВИ обычно проявляется в форме синдрома мононуклеоза, что подтверждается наличием лимфоцитоза, присутствием антител ЦМВ IgG и IgM в сыворотке и культуры ЦМВ в крови, моче, слюне, цервикальных выделениях.
Мононуклеозоподобный синдром характеризуется продолжительной лихорадкой, ознобами, быстрой утомляемостью, болями в мышцах, головными болями, встречается чаще у молодых людей [6].
У беременной женщины наиболее часто происходит обострение хронической ЦМВИ, которая, как правило, не имеет явных клинических проявлений. Однако у данной категории женщин в анамнезе нередко имеются указания на привычное невынашивание или неразвивающуюся беременность, мертворождения, рождение нежизнеспособных детей, а также детей-инвалидов с врожденными пороками развития [11].
Инфицирование возможно в любом триместре, тем не менее наиболее тяжелые последствия возникают при первичной инфекции, возникшей у матери в течение первых 20 недель беременности. Вместе с тем даже при развитии первичной ЦМВИ во время беременности 90-95% женщин имеют шанс родить здорового ребенка [12].
Внутриутробная цитомегаловирусная инфекция может приводить к рождению детей с тяжелыми неврологическими расстройствами, поражениями зрительного и слухового нервов.
Степень поражения плода зависит от срока инфицирования. Заражение на ранних сроках беременности чаще ведет к гибели плода и самопроизвольным выкидышам.
Дети с ЦМВИ (положительным IgM) от серопозитивных матерей имеют более низкий вес и рост при рождении, чем дети серонегативных матерей.
ЦМВ может инфицировать плаценту, плод, амниотическую жидкость. Вирусная культура и характерные цитомегалические клетки могут быть выявлены у плодов от женщин с активной первичной ЦМВИ. Однако наличие признаков или симптомов ЦМВ у плода не всегда является предвестником серьезного заболевания при рождении и в постнатальном периоде.
При выявлении симптомов болезни в течение первых трех недель жизни ребенка ЦМВИ может рассматриваться как врожденная, возникновение заболевания в более поздние сроки чаще характеризует приобретенную форму ЦМВИ (постнатальное инфицирование).
Врожденная ЦМВИ характеризуется, как правило, генерализованным поражением органов плода и целым комплексом клинических симптомов.
Для приобретенной формы ЦМВИ характерно латентное течение, преимущественно с локальным поражением слюнных желез.
У новорожденных, инфицированных внутриутробно, в 90% случаев не бывает симптомов при рождении, у 5-17% их них развиваются осложнения в более позднем периоде [6].
Развитие симптоматики у новорожденного с ЦМВИ коррелируется с симптомами, присутствующими при рождении.
Остальные дети с врожденной ЦМВИ совершенно асимптоматичны и выглядят при рождении здоровыми.
Клинические формы ЦМВИ могут иметь острое или хроническое течение.
По степени тяжести заболевания ЦМВИ выявляют:
- легкую (в том числе стертые и субклинические формы инфекции), при которой поражения внутренних органов незначительны и не сопровождаются функциональными нарушениями (компенсация);
- среднетяжелую, при которой имеется поражение внутренних органов, сопровождаемое функциональными нарушениями различной степени (субкомпенсация);
- тяжелую, при которой резко выражена интоксикация и поражение внутренних органов сопровождается тяжелыми функциональными нарушениями (декомпенсация);
При тяжелом течении врожденной ЦМВИ смерть ребенка чаще наступает в первые дни и недели жизни; при легком — болезнь принимает волнообразное течение.
Следует отметить, что дети с врожденной или перинатальной активной цитомегалией чрезвычайно предрасположены к развитию бактериальных суперинфекций, что обусловлено в первую очередь иммунной недостаточностью.
Симптомы врожденной ЦМВИ включают признаки замедления внутриутробного развития, внутриутробную гипотрофию, конъюгационную желтуху, гепатоспленомегалию, интерстициальную пневмонию, нарушения мозгового кровообращения. Осложнения со стороны ЦНС также очень часты и проявляются у новорожденных повышенной сонливостью, плохим сосательным рефлексом, макро- и микроцефалией, гидроцефалией, порэнцефалией, хориоретинитом, сенсоневральной глухотой [4, 11].
Врожденная ЦМВИ может также иметь необычные проявления, такие как вентрикуломегалия, перивентрикулит или образование кист, гемолитическая анемия, петехии, геморрагическая пурпура, тромбоцитопения, хронический гепатит и асцит [3, 8].
Однако, несмотря на очень большое количество симптомов и осложнений, ассоциируемых с врожденной ЦМВИ, трудно предсказать физическое и интеллектуальное развитие ребенка, основываясь на симптомах, присутствующих при рождении.
Каждое из перечисленных клинических проявлений ЦМВИ заслуживает отдельного рассмотрения.
Гепатомегалия вместе со спленомегалией и петехиями является самым убедительным подтверждением болезни у детей с врожденной ЦМВИ. Обычно присутствуют явления гепатита с нарушениями функции печени (желтуха, гипербилирубинемия).
Функция печени, как правило, нормализуются в первые недели жизни.
Спленомегалия нередко может явиться единственным показателем врожденной ЦМВИ при рождении.
Петехии обычно носят преходящий характер и наблюдаются в течение двух-трех суток после рождения. При врожденной ЦМВИ чаще встречается комбинация петехий с гепатоспленомегалией и тромбоцитопенией.
При исследовании крови выявляется картина гипохромной анемии, эритробластоз, тромбоцитопения.
Врожденная ЦМВИ приводит к ухудшению зрения у 20% детей. Чаще всего наблюдается хориоретинит (односторонний или двусторонний), который может привести к слепоте. Однако врожденная ЦМВИ обычно не вызывает микроофтальмию или катаркту.
Микроцефалия может быть частично причиной замедленного развития новорожденного и сочетаться с внутричерепными кальцификатами, которые локализуются в перивентрикулярной структуре и ликворе.
Компьютерная томография является наиболее чувствительным методом для их определения. Ультразвук и рентгенография черепа относятся к менее чувствительным методам.
Многие дети с микроцефалией и внутричерепными кальцификатами имеют неврологические проявления.
У 10% детей с асимптоматичными проявлениями инфекции могут наблюдаться осложнения, даже в возрасте пяти–семи лет, чаще в виде сенсорной потери слуха, неврологических расстройств или умственного отставания. Половина детей с врожденной ЦМВИ имеют сочетанную потерю слуха. Глухота носит двухсторонний сенсоневральный характер. Нередко также диагностируются врожденные сердечно-сосудистые, гастроинтестинальные, мышечно-скелетные аномалии развития органов [7].
Таким образом, для беременных с цитомегаловирусной инфекцией должен быть предусмотрен комплекс диагностических, профилактических и лечебных мероприятий, направленных на уменьшение случаев возникновения врожденной цитомегаловирусной инфекции, что должно быть обязательным условием создания эффективной системы профилактики и охраны здоровья матери и ребенка.
Что такое антенатальная гибель плода? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кондратенко Юлии Николаевны, гинеколога со стажем в 17 лет.
Над статьей доктора Кондратенко Юлии Николаевны работали литературный редактор Маргарита Тихонова , научный редактор Светлана Симанина и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Антенатальная гибель плода — это внутриутробная смерть плода, наступившая до начала родов, но после 21 недели беременности. Является причиной 39-42 % мертворождений. У таких детей отсутствует сердцебиение, дыхание, движения и пульсация сосудов пуповины [12] .
Согласно первым комплексным оценкам, каждый год на свет появляется более 7200 мертворождённых детей. Даже в высокоразвитых странах Европы и Северной Америки показатель мертворождения не опускается ниже 1,3 % [9] . Уровень мертворождения в России в 2018 году был равен 5,51 %. При этом доля антенатальной гибели плода составила 91,8 %. Однако за последние пять лет показатель перинатальной смертности (гибели ребёнка до и после родов) стал снижаться [13] .
Чаще внутриутробная гибель плода наблюдается у девочек-подростков в силу незрелости организма, а также у беременных 35 лет и старше. К этому возрасту у женщины , как правило, возникает ряд хронических заболеваний, снижается овариальный резерв — запас фолликулов в яичниках. Всё это является риском неразвивающейся беременности по причине хромосомной патологии плода.
Также риск антенатальной потери выше у женщин с более чем двумя родами в анамнезе, привычным невынашиванием беременности , искусственными абортами, многоплодными беременностями, наличием послеоперационного рубца на матке и при экстракорпоральном оплодотворении (ЭКО) [23] .
Существует множество причин внутриутробной гибели плода. Они могут быть как со стороны самого плода, так и стороны матери [8] .
Непосредственной причиной смерти является дистресс-синдром плода . Он подразумевает под собой все нарушения функционального состояния плода, в первую очередь, его движений и сердцебиения.
Опосредованные причины антенатальной гибели плода :
- Врождённые аномалии развития плода — синдром Дауна, синдром Патау, синдром Эдвардса и др. . Чаще всего это происходит при:
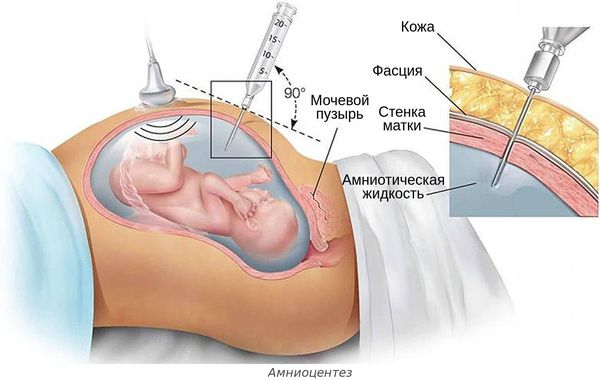
- инвазивной диагностике и лечении беременной — амниоцентезе (во время удаления излишков околоплодных вод, введения лекарств или пункции амниотической оболочки), пунктировании сосудов пуповины и др.;
- нарушении стерильности во время введения препаратов крови внутрь матки через сосуды пуповины (например, при переливании эритроцитарной массы плоду с гемолитической болезнью);
- преждевременном разрыве околоплодных оболочек в случае пролонгированной беременности;
- общих инфекциях беременной — TORCH-инфекциях, сифилисе , туберкулёзе, урогенитальном хламидиозе и ВИЧ-инфекции[13] .
- Экстрагенитальные заболевания матери — сахарный диабет, нарушения работы щитовидной железы, почек и надпочечников, травмы, злоупотребление алкоголем и курение , особенно при наличии воспалений урогенитального тракта.
- Особенности течения беременности :
- различные формы позднего токсикоза;
- угроза прерывания беременности;
- истмико-цервикальная и фетоплацентарная недостаточность ;
- инфекционные заболевания;
- нарушение кровотока в матке и плаценте;
- тазовое предлежании плода.
- Неустановленные причины .
Инфекция может быть вирусной (цитомегаловирусы, вирусы простого герпеса, краснухи, Коксаки, ВИЧ), бактериальной (хламидии, микоплазмы, уреаплазмы, стрептококки группы В, энтеробактерии, кишечная палочка) и грибковой (кандидоз).
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы антенатальной гибели плода
Процесс внутриутробной гибели плода далеко не всегда может сопровождаться изменениями в самочувствии женщины. Иногда беременная отмечает более частые шевеления плода, но позже происходит их полное прекращение. Это говорит об острой гипоксии плода — снижении содержания кислорода в организме [2] . Однако часто гибель малыша наступает незаметно для матери и врача, что приводит к поздней диагностике антенатальной смерти плода [4] .
В течение первых трёх дней гибели малыша пациентка может обратить внимание на изменения своего состояния:
- прекращаются шевеления плода;
- уменьшается размер молочных желёз, снижается их напряжение;
- живот перестаёт увеличиваться в объёме;
- возникает слабость, недомогание, тяжесть внизу живота.
Если с момента гибели плода в утробе матери прошло несколько недель, могут присоединяться признаки воспалительной реакции:
- повышение температуры до 38 ℃;
- сильные тянущие боли внизу живота;
- головная боль и головокружение;
- сонливость;
- нарушение сознания [16] .
Патогенез антенатальной гибели плода
Несмотря на то, что внутриутробная гибель плода является общемировой проблемой, вопросы её патогенеза остаются нерешёнными [5] [14] [21] [25] . В связи с этим проводится множество исследований, в частности исследования плаценты — предполагается, что её изменения являются основной или одной из главных причин смерти плода. Установить фактическую причину при аутопсии (вскрытии) мертворождённого довольно трудно [3] [6] [15] [22] [24] .
Суть патогенеза заключается в нарушении функции плаценты, развитии хронической плацентарной недостаточности, нарушении кровоснабжения плода, его росте и развитии. Поражаются внутренние органы плода — развивается внутриутробная пневмония, менингит и др. В какой-то момент происходит нарушение нормального функционирования плаценты, развивается острая плацентарная недостаточность и плод погибает.
Профессором И. В. Бариновой в 2015 году были представлены два типа плодовых потерь при внутриутробной гипоксии. Каждому из них характерно своеобразное сочетание патогенетических факторов, связанных с матерью, плацентой и плодом.
Патогенез первого типа отличается комплексом таких признаков, как ранняя тяжёлая преэклампсия и васкулопатия, т. е. патологическое изменение сосудов базальной пластинки плаценты (неполноценная перестройка спиральных артерий, необходимая для улучшения кровоснабжения плода, острый атероз, тромбоз и кровотечения). Всё это нарушает циркуляцию материнской крови в плаценте [1] .
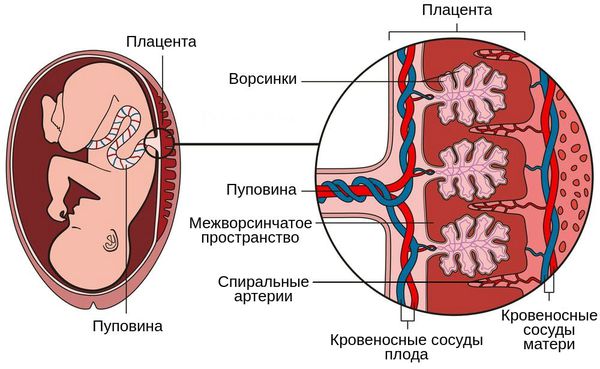
Патогенез второго типа обусловлен нарушением циркуляции в плодовой части плаценты, незрелостью ворсин относительно срока беременности, а также васкулопатией сосудов плода и тромбозом ворсин.
Эти основные звенья патогенеза антенатальной гибели позволяют своевременно профилактировать и назначать патогенетическую терапию фетоплацентарной недостаточности [1] .
Классификация и стадии развития антенатальной гибели плода
Пока не существует общепринятой классификации внутриутробной гибели плода. Однако изучение причин перинатальной смертности привело к появлению двух понятий:
- "Необъяснимое" мертворождение — внезапная гибель малыша наступает по неизвестным причинам. Установить их можно только после анатомического вскрытия плода и исследования плаценты. Зачастую выявляются аномалии опорно-двигательной и нервной системы, несовместимые с жизнью, а также поражения сердечно-сосудистой системы, в частности фатальная аритмия — нарушение сердечного ритма.
- Мертворождение, связанное с задержкой роста плода — гибель плода обусловлена нарушениями обмена веществ, поступления кислорода и кровоснабжения плода из-за материнских факторов, а также факторов, связанных с плодом и плацентой [8] .
Полноценное гистологическое исследование внутриутробно погибшего плода необходимо для установления причины его смерти. Некоторые матери отказываются от него, но это неправильно. Дело в том, что у многих женщин с гибелью плода в анамнезе повышается риск повторных потерь при следующих беременностях [26] . Поэтому исследование причин мертворождения позволит предотвратить повторение этой трагедии в будущем.
Осложнения антенатальной гибели плода
При своевременном обращении к доктору антенатальная гибель плода не приводит к осложнениям. Если же пациентка обратилась за медицинской помощью спустя больше двух недель после смерти ребёнка, то у неё с большой вероятностью могут развиваться такие осложнения, как:
- Кровотечение во время и после родов.
- Гнойно-септические осложнения:
- хориоамнионит — воспаление стенок плодного пузыря и заражение инфекцией околоплодных вод;
- послеродовой метроэндометрит — воспаление мышечной и слизистой оболочки стенки матки;
- инфекции послеоперационной раны — может возникнуть, если роды проходили путём кесарева сечения, например, при раннем отделении плаценты;
- послеродовой сепсис — заражение крови.
Чтобы избежать их, необходимо тщательно наблюдать за состоянием пациентки и выполнять профилактические мероприятия:
- плановое проведение родов при высоком риске кровотечения;
- профилактика анемии ;
- гемостатическая терапия;
- пережатие пуповины ребёнка не раньше первой минуты после рождения;
- строгое соблюдение стерильности при выполнении кесарева сечения и вагинальных исследований во время родов;
- использование индивидуальных комплектов при родоразрешении;
- отказ от катетеризации мочевого пузыря и эпизиотомии (рассечения задней стенки влагалища) без явной необходимости;
- профилактический приём антибиотиков после выполнения инвазивной диагностики или при длительном безводном периоде;
- ранняя выписка из родильного дома (на третьи сутки после родов) [16] .
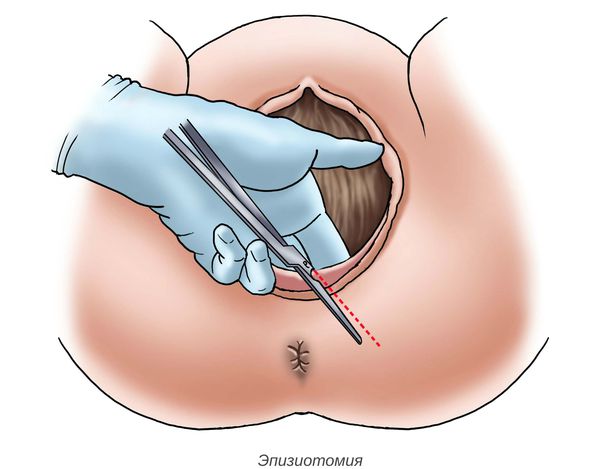
Антенатальная гибель плода является серьёзным состоянием при многоплодной беременности . В случае дихориальной беременности (когда малыши развиваются независимо друг от друга: каждый имеет свои жизненно важные структуры — плодный мешок и плаценту) гибель близнеца не влияет на другого ребёнка. При монохориальной беременности (когда у малышей одна плацента на двоих) риски повреждения второго плода существенно выше:
- в 12 % случаев происходит гибель второго ребёнка;
- в 18 % случаев у него диагностируются неврологические нарушения.
В связи с этим рекомендован контроль показателей эхокардиографии (УЗИ сердца), оценка мозгового кровотока (УЗИ головного мозга) и МРТ выжившего плода [18] .
Помимо прочих осложнений у женщины может возникнуть депрессия , тревожное и посттравматическое расстройство на почве пережитой трагедии или чувства вины. У неё может развиться страх перед будущей беременностью, желание избежать её [26] . В этих случаях пациентке требуется психотерапевтическая помощь.
Диагностика антенатальной гибели плода
После того как женщина обращается к врачу с жалобами на недомогание и отсутствие шевеления плода, врач направляет пациентку на диагностическое обследование. Оно позволяет поставить точный диагноз.
Постановка диагноза внутриутробной гибели плода включает следующие этапы обследования:
- Выслушивание сердечных сокращений плода специальным стетоскопом. Обычным медицинским стетоскопом в данном случае услышать сердцебиение невозможно. Для этого существует деревянный акушерский стетоскоп. Он отличается широкой воронкой, которая плотно прикладывается к животу беременной.
- Выслушивание сердечных сокращений фетальным аудиодопплером и/или монитором . Фетальный допплер можно использовать даже в домашних условиях, начиная с 12-ой недели беременности. Для этого женщине нужно лечь на спину и для чёткого сигнала нанести гель на те участки живота, которые будут соприкасаться с датчиком. Сам допплер нужно передвигать медленно, без резких движений. Длительность исследования — 3-7 минут.
- Ультразвуковое исследование плода (УЗИ). Этот метод является одним из самых достоверных для диагностики внутриутробной гибели плода. С его помощью доктор констатирует отсутствие сердцебиения у малыша [16] .

Анализы для диагностики внутриутробной гибели плода на позднем сроке беременности не так важны. Отсутствия шевелений плода в течение нескольких дней и сердцебиения по данным УЗИ достаточно для правильной постановки диагноза.
Лечение антенатальной гибели плода
При подтверждённом диагнозе антенатальной гибели плода показана экстренная госпитализация и принятие решения о методе и сроке родоразрешения. Чем меньше интервал между установленным диагнозом и родоразрешением, тем меньше риск возникновения осложнений во время и после родов.
Выбор метода определяется индивидуально, на основании клинических данных и особенностей акушерской ситуации. Оптимальным вариантом родоразрешения при антенатальной гибели плода являются роды через родовые пути. Но иногда выполняется кесарево сечение, например при раннем отделении плаценты от стенок матки, обильном или продолжающемся кровотечении из половых путей.
При родоразрешении беременных с антенатальной гибелью плода, осложнившейся септическим состоянием, показано экстренное оперативное вмешательство. Объём операции решается индивидуально, возможна удаление матки с плодом (экстирпация).
После родов важно тщательно наблюдать за состоянием роженицы, провести профилактику послеродового кровотечения и гнойно-септических осложнений. Необходимо обратить внимание на выделения из половых путей (гнойные или кровянистые ), температуру тела, появление озноба, слабости, тянущих болей внизу живота.
Во всех случаях внутриутробной гибели плода показано патологоанатомическое исследование плода и последа (его оболочки). Отказ от исследования по желанию родственников оформляется в соответствии с нормами действующего законодательства [19] .
Самым тяжёлым остаётся вопрос о том, когда же произошла гибель плода. Раньше считалось, что в основе определения времени гибели лежит оценка выраженности процессов мацерации — размягчения и разрыхления тканей плода [20] . Однако наличие признаков мацерации не всегда позволяет достоверно судить о давности наступления гибели, т. к. время её развития зависит от причин гибели малыша.
Прогноз. Профилактика
Потеря беременности является показанием к проведению медицинской, психологической и социальной реабилитации пациенток. Необходим полный комплекс диагностических исследований для выяснения причины гибели плода. Выбор алгоритма обследования базируется на данных анамнеза, особенностях течения беременности и результатах патологоанатомического исследования плода и последа.
Женщины с внутриутробной гибелью плода в анамнезе входят в группу риска данного осложнения при последующих беременностях. Поэтому наступление беременности у таких пациенток требует выполнения комплекса мероприятий по подготовке организма женщины к полноценному зачатию, вынашиванию и рождению здорового ребёнка [10] . Оптимальный интервал между беременностями должен составлять не менее 6 месяцев, чтобы минимизировать потенциальные сложности течения последующей беременности [26] .
При неустановленной причине гибели плода в анамнезе необходимо учитывать данный факт при выработке тактики родоразрешения последующих беременностей.
Профилактика антенатальной гибели плода предполагает:
- ведение здорового образа жизни;
- диагностику и адекватное лечение соматических и хронических инфекционных заболеваний;
- своевременное выявление генетической патологии;
- лечение высокого артериального давления;
- контроль уровня глюкозы в крови при сахарном диабете [26] ;
- предупреждение травм живота;
- прекращение контакта с бытовыми токсичными веществами;
- ликвидацию профессиональных вредностей (переход на другую работу);
- адекватное назначение лекарств в период беременности;
- приём фолиевой кислоты до зачатия;
- комплексное антенатальное наблюдение за состоянием плода [7] ;
- регистрацию шевелений плода на 28 неделе беременности;
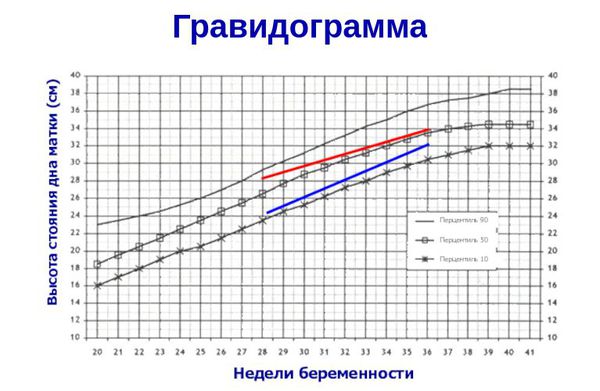
- ведение гравидограммы с 24 недели беременности (сводной таблицы данных, регистрирующей динамику течения беременности) — повышает качество диагностики задержки развития плода и снижает риск потери малыша в 1,8 раз [11] .
Курение увеличивает риск перинатальной смертности на 27 % [17] . Однако чаще антенатальная гибель плода наблюдается у беременных, употребляющих алкоголь — в 6,25 % случаев [8] . Поэтому отказ от вредных привычек значительно увеличивает шансы родить здорового ребёнка.
Рассмотрена проблема внутриутробного инфицирования и внутриутробной инфекции (ВУИ) плода, факторы риска внутриутробных инфекций, патогенетические механизмы возникновения, развития и воздействия ВУИ, подходы к диагностике и лечению.
The issue of fetal intrauterine infecting and intrauterine infection (IUI) was considered, as well as the risk factors of intrauterine infections, pathogenic mechanisms of their occurrence, development and effect of IUI, and approaches to the diagnostics and treatment.
Проблема внутриутробной инфекции особо актуальна в современных условиях в связи с распространенностью и тяжестью воспалительных процессов. Проблема внутриутробного инфицирования и внутриутробной инфекции (ВУИ) плода является одной из ведущих в акушерской практике и в перинатологии в связи с высоким уровнем инфицирования беременных, рожениц и родильниц, опасностью нарушения развития плода и рождения больного ребенка. Наличие инфекции у матери является фактором риска ВУИ плода, но не всегда означает его заболевание [1, 5–7, 13].
Внутриутробная инфекция — группа инфекционно-воспалительных заболеваний плода и детей раннего возраста, которые вызываются различными возбудителями, но характеризуются сходными эпидемиологическими параметрами и нередко имеют однотипные клинические проявления. Заболевания развиваются в результате внутриутробного (анте- и/или интранатального) инфицирования плода. При этом в подавляющем большинстве случаев источником инфекции для плода является мать. Истинная частота врожденных инфекций до настоящего времени не установлена, но, по данным ряда авторов, распространенность данной патологии в человеческой популяции может достигать 10%. В структуре перинатальной смертности ВУИ составляет более 30% [1, 5–7].
Кроме этого, ВУИ относятся к тяжелым заболеваниям и во многом определяют уровень младенческой смертности.
Согласно данным многих авторов, причиной внезапной смерти грудных детей является инфекционное заболевание, протекающее без ясной симптоматики. В числе причин или фоновых состояний скоропостижной смерти могут быть ВУИ [2].
Под внутриутробным инфицированием понимают процесс внутриутробного проникновения микроорганизмов к плоду, при котором отсутствуют признаки инфекционной болезни плода. Как правило, инфекционный процесс затрагивает плаценту, в которой развивается плацентит, хориоамнионит и т. д. Диагноз внутриутробного инфицирования у новорожденного устанавливается на основании выделения возбудителя из клеток крови, ликвора и других источников, выявления IgM и низкоавидных IgG в пуповинной крови, а также при морфологическом исследовании плаценты [1, 5–7].
Внутриутробное инфицирование не означает неизбежного развития инфекционного заболевания. Для выявления ВУИ необходимо наличие данных лабораторного исследования в сочетании с клинической картиной инфекционного заболевания. Под ВУИ подразумевают не только процесс распространения инфекционных агентов в организме плода, но и вызванные ими морфофункциональные нарушения различных органов и систем, характерные для инфекционной болезни (сепсис, пневмония, менингит, гепатит и т. д.), возникшей анте- или интранатально и выявляемой пренатально или после рождения [10, 11].
Инфекционно-воспалительные заболевания во время беременности имеют особенности: инфицирование плода и новорожденного может быть вызвано как острой инфекцией матери, так и активацией хронической, персистирующей инфекции во время беременности; большая часть заболеваний беременных, приводящих к внутриматочной инфекции, протекает в латентной или субклинической форме; активация персистирующей инфекции возможна при любом нарушении гомеостаза в организме беременной (стресс, острые респираторные вирусные инфекции, переохлаждение и др.) [1, 2].
Возможный спектр возбудителей внутриутробной инфекции весьма разнообразен и широк. Это бактерии (грамположительные и грамотрицательные; аэробные и анаэробные), грибы, простейшие, внутриклеточные микроорганизмы (микоплазмы, хламидии), вирусы. Чаще всего наблюдается сочетание возбудителей — бактериально-вирусная смешанная инфекция [3, 4, 10, 11].
Зачастую ВУИ ассоциируются с наличием инфекций TORCH — то есть синдромом комплекса. Данный термин образован первыми буквами латинских названий наиболее часто верифицируемых врожденных инфекций: T — токсоплазмоз (Тoxoplasmоsis), R — краснуха (Rubella), С — цитомегалия (Cytomegalia), Н — герпес (Herpes) и О — другие инфекции (Оther). К последним относят сифилис, листериоз, вирусные гепатиты, хламидиоз, ВИЧ-инфекцию, микоплазмоз и др. [9, 11].
Принимая во внимание, что источником инфекции для плода всегда является его мать, особое значение приобретают следующие факторы риска внутриутробных инфекций:
- хронические очаги инфекции в организме матери (в том числе наличие воспалительных заболеваний органов малого таза, урогенитальные инфекции);
- первичное инфицирование во время беременности, активация инфекционного процесса;
- патологическое снижение общего и местного иммунитета;
- наличие экстрагенитальной патологии (анемия, тромбофилии, аутоиммунные заболевания);
- повышение проницаемости плацентарного барьера во II и III триместрах беременности при невынашивании беременности и плацентарной недостаточности;
- отягощенный акушерско-гинекологический диагноз;
- неблагоприятные социально-бытовые факторы [1, 9, 11].
Патогенетические механизмы возникновения, развития и воздействия ВУИ разнообразны и зависят от многих факторов:
- срока беременности, при котором происходит инфицирование (чем раньше, тем прогноз будет более неблагоприятным);
- вида возбудителя, его вирулентности, массивности обсеменения;
- первичности или вторичности инфекционного процесса у беременной;
- путей проникновения инфекции к плоду (восходящий, нисходящий, гематогенный);
- степени распространенности и интенсивности воспалительного процесса;
- состояния организма матери, его иммунологической толерантности.
Влияние инфекции на эмбрион и плод заключается в воздействии комплекса следующих факторов:
- патологическое воздействие микроорганизмов и их токсинов (инфекционное заболевание, гипоксия плода, задержка развития плода);
- нарушение процесса имплантации и плацентации (низкая плацентация, предлежание плаценты);
- снижение метаболических процессов и иммунологической защиты плода [1, 9, 11].
Таким образом, реализуется ли внутриутробное инфицирование в ВУИ или нет, зависит от ряда факторов, которые мы представили выше.
Учитывая неспецифичность клинических проявлений ВУИ во время беременности, диагностика данной патологии в большинстве случаев затруднена и возможна лишь в результате сочетания клинических и лабораторно-диагностических методов обследования.
Клинический метод исследования позволяет выявить различные осложнения гестационного периода, такие как невынашивание беременности и синдром задержки роста плода (СЗРП). Кроме этого, немаловажное значение имеет наличие проявлений инфекции у матери (отит, гайморит, пиелонефрит, цистит и т. д.).
Методы, позволяющие оценить состояние фетоплацентарной системы:
- эхография (плацентометрия, поведенческая активность плода, его тонус, количество околоплодных вод, степень зрелости плаценты);
- допплерография (МПК, ФПК);
- кардиотокография (КТГ).
Микробиологические и серологические исследования:
- микроскопия влагалищных мазков (повышенное содержание лейкоцитов, кокковая флора, признаки дисбиоза, грибковая флора);
- бактериальный посев (наличие анаэробных и аэробных бактерий, грибковой флоры);
- ПЦР-диагностика (геномы ВПГ-1, ВПГ-2, ЦМВ, микоплазмы, уреаплазмы, хламидии);
- иммуноферментный анализ (ИФА): обнаружение в сыворотке специфических антител к возбудителям (IgM, IgG, IgA) в диагностически значимых титрах.
Исследование хориона (биопсия хориона): бактериологический метод, ПЦР-диагностика.
Исследование околоплодных вод (амниоцентез): бактериологический метод, ПЦР-диагностика.
Исследование пуповинной крови плода (кордоцентез): бактериологический метод, ПЦР-диагностика и специфический иммунный ответ (IgM) плода.
Морфологическое исследование плаценты, данные аутопсии.
Предположительный диагноз внутриутробного инфицирования и ВУИ помогают поставить косвенные методы:
- наличие у матери клиники инфекционного заболевания;
- наличие специфического иммунного ответа;
- результаты УЗИ, допплерометрии, КТГ.
К прямым методам диагностики внутриутробного инфицирования и ВУИ относятся: выявление возбудителя в материале, полученном при биопсии хориона, амниоцентезе (ПЦР, бактериологический метод), кордоцентезе (ПЦР, бактериологический метод и определение уровня специфических IgM).
Характер течения беременности при внутриутробной инфекции зависит от срока воздействия возбудителя.
На ранних этапах зародыша (1–3 недели беременности) из-за отсутствия механизмов взаимодействия инфекционного агента и плодного яйца реализации воспалительной реакции чаще всего не происходит. Контакт с инфекцией может закончиться альтернативным процессом и гибелью плодного яйца. Повреждение эмбриона инфекцией на 4–12 неделях беременности связано с вирусной инфекцией, проникновением микроорганизмов через хорион. Плод еще не имеет защитных механизмов. Нарушение закладки органов и систем вызывает тератогенный и эмбриотоксический эффект [13, 15].
В I триместре беременности специфических клинических признаков наличия ВУИ нет, косвенно о ней свидетельствуют некоторые эхографические признаки:
- повышенный локальный тонус матки;
- отслойка хориона;
- изменение формы плодного яйца (деформация);
- прогрессирование истмико-цервикальной недостаточности (функционального характера);
- гипоплазия хориона;
- увеличение или персистенция желточного мешка;
- несоответствие размеров эмбриона размерам полости плодного яйца (увеличение, уменьшение);
- отсутствие редукции хорионической полости.
Инфекционные фетопатии возникают с 16-й недели, когда происходит генерализация инфекции у плода. Могут возникать такие пороки развития, как фиброэластоз эндокарда, поликистоз легких, микро- и гидроцефалия (ранние фетопатии) [12–15].
В III триместре плод реагирует на внедрение возбудителя локальной реакцией. Могут возникнуть энцефалит, гепатит, пневмония, интерстициальный нефрит. Влияние вирусов чаще всего проявляется признаками незрелости, дисэмбриогенетическими стигмами, затяжным адаптационным периодом, значительной потерей массы тела в раннем постнатальном периоде. Данные эхографии во II и III триместрах беременности, указывающие на развитие инфекции у плода:
- СЗРП;
- гипоксия плода;
- фетоплацентарная недостаточность;
- многоводие или маловодие;
- неиммунная водянка плода;
- увеличение или уменьшение толщины плаценты, наличие патологических включений;
- контрастирование базальной мембраны;
- наличие взвеси в околоплодных водах;
- кальцификаты в печени и селезенке и головном мозге плода;
- поликистоз легких, почек плода;
- эхогенные фиброзные включения на папиллярных мышцах и створках клапанов сердца плода;
- расширение петель кишечника плода (гипоксия, энтерит) [12–15].
После верификации диагноза ВУИ лечебные мероприятии проводят с помощью этиотропной, антимикробной терапии: препараты пенициллинового ряда и макролиды. Целесообразность назначения антимикробных препаратов не вызывает сомнения, если ВУИ обусловлено наличием патогенных возбудителей (бледная спирохета, токсоплазма, хламидии, гонококк и т. д.) [8, 14].
В настоящее время одним из наиболее дискутабельных вопросов в акушерстве является выяснение истинной этиологической роли генитальных микоплазм (Mycoplasma hominis, Mycoplasma genitalis, Ureaplasma urealyticum) в развитии патологии матери и плода. Инфицирование плода генитальными микоплазмами происходит преимущественно интранатально: в 18–55% — у доношенных новорожденных и в 29–55% — у недоношенных [3, 16, 20].
Актуальность проблемы урогенитального микоплазмоза обусловлена не только значительным распространением этой инфекции в популяции, но и неоднозначностью ее оценки как эпидемиологами, так и клиницистами [16].
По данным различных исследователей, микоплазмы являются возможной причиной развития конъюнктивитов, врожденных пневмоний, респираторного дистресс-синдрома, хронических заболеваний легких, менингита и неонатального сепсиса. Вопрос о терапии микоплазменной инфекции до настоящего времени остается открытым. В схемах терапии предусматривается 7–10-дневные курсы макролидов [1, 3, 21, 22].
Во время беременности противовирусная терапия при генитальном герпесе, цитомегаловирусной инфекции, вирусе ветряной оспы проводится с помощью этиотропных препаратов (ацикловир) начиная со II триместра гестационного периода. Целью лечения является профилактика рецидивирования и антенатального инфицирования [14, 17, 19].
Трихомонадная инфекция относится к группе негонококковых воспалительных заболеваний мочеполовых органов. Лечение трихомониаза во время беременности осуществляется с помощью метронидазол-содержащих препаратов начиная со II триместра гестационного периода [8].
Появление новых методов диагностики, разработка и внедрение новых лекарственных средств не изменяют ситуацию с внутриутробными инфекциями, оставляя это по-прежнему актуальной проблемой в акушерстве. Все это обуславливает неуклонный рост инфекции в человеческой популяции, высокий процент рецидивов инфекции даже у пациентов, получавших курс антибиотикотерапии в соответствии с действующими инструкциями и схемами лечения. Проблема осложняется тем, что в настоящее время отсутствует единая концепция механизма рецидивирования, недостаточно изучена роль микст-инфекции в возникновении, течении и персистировании инфекции, не учитываются особенности гормонального и иммунного статуса больного, не сформированы диагностические критерии контроля излеченности патологического процесса. Это все вместе взятое является стимулом для продолжения исследований, направленных на решение данных проблем. Несмотря на то что роль вирусных и бактериальных инфекций в этиологии и патогенезе многих патологических процессов не вызывает сомнений, вопрос о значении инфекций в качестве моновозбудителя на сегодняшний день окончательно не решен. Актуальным по-прежнему остается вопрос разработки алгоритма лабораторной диагностики заболеваний.
Только совершенствование диагностических подходов, разработка оптимальных алгоритмов и методов обследования и предупреждение распространения резистентных штаммов путем адекватного отношения к каждому пациенту индивидуально (обязательное проведение посевов на определение чувствительности к антибиотикам до назначения терапии) может изменить данную ситуацию.
Исследование выполнено за счет гранта Российского научного фонда (проект № 15-15-00109).
Литература
В. Н. Кузьмин 1 , доктор медицинских наук, профессор
К. Н. Арсланян, кандидат медицинских наук
Э. И. Харченко, кандидат медицинских наук
ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва

Почему и откуда берутся внутриутробные инфекции (ВУИ), в чём опасность внутриутробных инфекций у новорождённых, как их выявить и как с ними бороться, как защитить будущего ребёнка от заражения внутриутробно и во время родов (в интранатальный период)? Это вопросы, которые чаще всего беспокоят женщин, планирующих стать мамами, а также в период вынашивания ребёнка. Постараюсь в доступной форме ответить на эти и другие вопросы, волнующие будущих мамочек.
Какие инфекционные заболевания при беременности могут повлиять на развитие ребёнка?
Внутриутробные инфекции представляют собой группу заболеваний эмбриона, плода и новорожденного, которые развиваются в результате заражения в дородовом периоде или в родах, т. е. в анте-или интранатальный период. Инфицирование матери в период беременности нередко приводит к выкидышам и врождённым порокам развития у новорождённого. Возбудителями внутриутробных инфекционных заболеваний могут быть вирусы, бактерии, а иногда и паразиты, вызывающие явные либо скрытые инфекции у матери. Поэтому ещё на этапе планирования беременности врачу и будущей матери нужно обратить внимание на:
- инфекции, которые передаются половым путём (ИППП);
- бактериальные инфекции;
- инфекции, передающиеся простейшими микроорганизмами, грибами;
- цитомегаловирусная инфекция;
- герпес;
- хламидии;
- микоплазмы.
Что покажет УЗИ плода?
Ультразвуковое исследование (УЗИ) плода в период его вынашивания помогает специалисту своевременно обнаружить наличие различных патологий в развитии будущего ребёнка. Это, к примеру, маловодие или многоводие, большой живот, увеличенные какие-то внутренние органы, например, печень, селезёнка. В ходе ультразвуковой диагностики также могут быть обнаружены отложения кальцинатов в кишечнике, в печени, в головном мозге. В нашем медицинском лечебно-диагностическом центре "Целитель" в Махачкале опытные специалисты ультразвуковой диагностики проведут качественное исследование, которое позволит подтвердить или исключить патологию с высокой достоверностью.

Обнаруженные в ходе исследования ультразвуковые маркеры внутриутробной инфекции являются реальным подспорьем в оценке состояния плода и прогнозирования дальнейшей тактики ведения беременности. Если возможно, то врачи примут на ранних этапах меры для устранения обнаруженных отклонений. Если же это состояние, которое не совместимо с жизнью, то принимается решение о том, что лучше прервать беременность.
Клинические проявления внутриутробной инфекции?
При наличии внутриутробной инфекции околоплодные воды, которые отходят при рождении младенца, мутного цвета, имеют неприятный запах. Могут быть при этом даже загрязнены меконием (первые выделения из кишечного тракта), что указывает на угрожающее состояние заражения плода. На это врачам обязательно нужно обращать внимание. После этого опытные детские врачи осматривают плаценту, её полнокровие, есть ли какие-то кровоизлияния.
А что касается самого ребёнка, то в первую очередь нужно посмотреть на сроки, на вес. Обратить внимание на цвет кожи. Имеет ли место затяжная, длительная желтушность кожных покровов или, наоборот, бледность кожи, которая может указывать на анемию. Могут быть какие-то кожные высыпания, характерные для пиодермии, стрептодермии. У малыша может быть врождённая пневмония, врождённый миокардит, врождённые менингиты и энцефалиты. Исследуются печень, селезёнка на предмет увеличения этих органов. Также проводится анализ крови, где тоже можно увидеть изменения клинической картины.
Если мы видим соответствующие факторы риска, к примеру, 2 или 3 признака из тех, что перечислены выше, то этот ребёнок уже должен попасть в "группу риска" по внутриутробным инфекциям и его надо тщательным образом обследовать.
Чем опасны внутриутробные инфекции?
Существуют, так называемые, персистирующие инфекции, т. е. хронические, длительно текущие. Но они не всегда передаются от матери ребёнку. Поэтому не нужно особо беспокоиться, что вот, если у мамы есть инфекционная болезнь, то она на 100% передастся плоду. Частота передачи инфекции ребёнку в данном случае не такая высокая, как в случае первичного внутриутробного инфицирования.
Наибольшую угрозу для будущего ребёнка представляет мать, впервые заболевшая во время беременности, особенно в первом его триместре. Вот этот период наиболее опасен. Поэтому хочется призвать всех женщин – прежде, чем планировать рождение ребёнка, сдайте анализы на наличие антител к таким инфекциям со сходными эпидемиологическими признаками, как:
- корь;
- эпидемический паротит;
- менингококковая инфекция;
- краснуха;
- ветряная оспа;
- гепатиты.
Почему? Потому что это группа инфекционно-воспалительных заболеваний, которую у будущей матери можно предотвратить, если она за 3 месяца до зачатия сделает вовремя вакцину.
Помимо этого, есть также ранние исходы инфекций. Это: миокардиты, пневмония, гипотрофия, анемия. Есть поздние, когда внутриутробная инфекция может проявиться позже. Бывает, что проходит 5-6 лет, и у малыша в этом возрасте может обнаружиться:
- задержка психомоторного развития;
- задержка речевого развития;
- снижение остроты зрения;
- снижение слуха;
- гидроцефалия;
- микроцефалия.
Об этом тоже нужно помнить и не забывать.
Диагностика и лечение внутриутробных инфекций?
В первую очередь опытный доктор в целях выявления у женщины инфекций, опасных для ребёнка, назначит общий анализ крови и общий анализ мочи. Также обязательно надо будет сделать УЗИ щитовидной железы и проверить гормональный статус женщины.
Общий принцип лечения внутриутробных инфекционных заболеваний в настоящее время включает в себя противовирусный, антибактериальный курс, проведение симптоматической и патогенетической терапии новорожденных. Если возникнут какие-то проблемы у вас или вашего ребёнка, лечащий врач должен будет подобрать индивидуальную схему лечения, наиболее эффективную в данном конкретном случае.
Профилактика ВУИ
Очень важно для женщины, планирующей беременность предпринять все возможные меры для исключения возможности врождённых инфекций у новорождённого. Прежде всего нужно встать на учёт у гинеколога в срок до 12 недель. Необходимо прислушаться к рекомендациям специалистов и провести полное обследование состояния здоровья будущей матери, включая сдачу следующих анализов:

- мазок на флору;
- ПЦР-исследование на наличие хламидий, микоплазмы, уреаплазмы, вирус простого герпеса, цитомегаловируса;
- серологическое исследование крови на токсоплазмоз, краснуху, ВИЧ, гепатиты и другие инфекции.
Нужно также провести лечение имеющихся хронических очагов инфекции (кариес, тонзиллит, мочеполовые инфекционные заболевания) и не забывать о плановой вакцинации – прививках от кори, краснухи, гриппа.
Помимо этого, чтобы исключить заражения инфекциями, передающимися половым путём, желательно обследоваться и половому партнёру, ну и конечно же не допускать случайных сексуальных связей.
"Желаю вам родить живого, здорового, ребёнка. Чтобы он дальше по жизни только радовал вас своими успехами сначала в учёбе, а потом и дальше по работе. А для этого мы должны быть, во-первых, готовы и, во-вторых, мы должны полностью обследоваться. Т. е. женщина, решившая стать матерью, априори должна быть здорова."
Улуханова Лала Уджаговна, доктор медицинских наук, профессор, врач-педиатр, гастроэнтеролог, инфекционист, нефролог, пульмонолог в Махачкале, специалист высшей квалификационной категории.
Читайте также:

