Цитомегаловирус что это такое глицирризиновая кислота
Обновлено: 24.04.2024
В работе освещены проблемы коморбидности псориаза и заболеваний гепатобилиарной системы. Приведенные эпидемиологические данные о поражении печени при псориазе подтверждены результатами собственных исследований. Несомненный интерес представляют препараты, оказывающие влияние не только на гепатобилиарную систему, но и на псориаз. В ходе биоинформационного анализа установлены белки и малые молекулы, задействованные в патогенезе как псориаза, так и заболеваний печени. Наиболее релевантным оказался белок HMGB1, на регуляцию которого можно влиять глицирризиновой кислотой.
- КЛЮЧЕВЫЕ СЛОВА: псориаз, гепатобилиарная система, биоинформационный анализ, глицирризиновая кислота
В работе освещены проблемы коморбидности псориаза и заболеваний гепатобилиарной системы. Приведенные эпидемиологические данные о поражении печени при псориазе подтверждены результатами собственных исследований. Несомненный интерес представляют препараты, оказывающие влияние не только на гепатобилиарную систему, но и на псориаз. В ходе биоинформационного анализа установлены белки и малые молекулы, задействованные в патогенезе как псориаза, так и заболеваний печени. Наиболее релевантным оказался белок HMGB1, на регуляцию которого можно влиять глицирризиновой кислотой.
Псориаз остается актуальной и сложной проблемой современной дерматологии, что обусловлено высокой распространенностью в популяции, значительной долей в структуре дерматологических заболеваний и отсутствием единой этиопатогенетической концепции.
Важное значение в поддержании и рецидивировании дерматоза отводят нарушениям гепатобилиарной системы, поскольку патология печени и желчевыводящих путей может инициировать и усилить выраженность эндотоксикоза, воспаления, иммунный дисбаланс, обусловить нарушение процессов регенерации в организме в целом и коже в частности [2, 3].
Однако данные о частоте нарушений гепатобилиарной системы при разных формах заболевания, клинических, лабораторных и инструментальных особенностях гепатопатий и о состоянии печени и желчевыводящих путей у пациентов с различными формами псориаза противоречивы, а унифицированные алгоритмы диагностики таких нарушений отсутствуют [4, 5].
Псориаз и заболевания печени: факторы развития и взаимообусловленность
Установлена общность факторов, обусловливающих риск развития псориаза и заболеваний печени. Так, у пациентов с псориазом чаще, чем у здоровых лиц, отмечаются ожирение, гиперлипидемия, метаболический синдром. Эти же факторы способствуют развитию неалкогольной жировой болезни печени (НАЖБП). Доказано также, что злоупотребление алкоголем повышает вероятность развития не только алкогольной болезни печени (АБП), но и псориаза, в частности его тяжелых форм [4, 6–8].
Кроме того, показано, что псориаз является независимым фактором развития НАЖБП, риск развития последней увеличивается на 70%, ее тяжелых форм – на 60% [9]. Псориаз также считается дополнительным фактором развития АБП [10].
При сочетанном течении псориаза и НАЖБП, АБП более быстро прогрессирует фиброз и заболевания печени чаще достигают стадии цирроза [10, 11]. Получены данные о повышении смертности среди больных псориазом от цирроза печени [12]. У пациентов с НАЖБП и псориазом чаще развивается псориатический артрит [13], а потребление алкоголя, обусловливающего развитие АБП, способствует более тяжелому течению и ухудшению прогноза псориаза [14].
Результаты исследований ферментативной активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), гамма-глутаминтранспептидазы (ГГТ), лактатдегидрогеназы, монооксигеназной системы не выявили каких-либо специфичных изменений у таких пациентов. Достоверные изменения функции печени наблюдались только при тяжелых, торпидных и осложненных формах псориаза [15, 16].
Патогенетическое обоснование коморбидности
Анализ литературы свидетельствует об общих звеньях патогенеза псориаза и НАЖБП/АБП. Ключевую роль играют воспалительный процесс и выработка провоспалительных цитокинов, в частности интерлейкинов (IL) 1 и 6, и фактора некроза опухоли альфа (TNF-α).
При псориазе IL-1 стимулирует экспрессию молекул адгезии на поверхности эндотелиальных клеток, пролиферацию кератиноцитов и выработку провоспалительных цитокинов [17]. IL-6 способствует миграции Т-клеток в эпидермис, росту и дифференцировке дермальных и эпидермальных клеток [18]. TNF-α стимулирует пролиферацию кератиноцитов, продукцию провоспалительных цитокинов, ангиогенез и экспрессию молекул адгезии [19].
IL-6 при НАЖБП участвует в формировании инсулинорезистентности [20], а IL-1 и TNF-α – в развитии и прогрессировании воспалительного процесса в паренхиме печени [21–23]. Указанные цитокины способствуют развитию воспаления и при АБП [24].
Еще одним аргументом в пользу единого патогенеза является повышенный уровень IL-1 и IL-6, TNF-α, выявляемый как при псориазе, так и при НАЖБП и АБП [11, 14].
Глицирризиновая кислота и псориаз
Сказанное выше свидетельствует о том, что комплексная терапия больных псориазом, имеющих признаки поражения гепатобилиарной системы, должна включать лекарственные препараты с гепатопротективным действием.
Учитывая проблему полипрагмазии, необходимо найти препарат, терапевтическими мишенями которого являются звенья патогенеза как псориаза, так и заболеваний печени. В этом отношении представляют интерес препараты глицирризиновой кислоты.
В экспериментальных исследованиях продемонстрирована способность глицирризиновой кислоты подавлять продукцию IL-1 [25], IL-6 [26] и TNF-α [27]. Кроме того, она характеризуется псевдоглюкокортикостероидной активностью, обусловленной ингибированием 11-бета-оксистероиддегидрогеназы [28], а топические глюкокортикостероиды – наиболее часто применяемый при псориазе класс препаратов.
Эффективность и благоприятный профиль безопасности глицирризиновой кислоты (препарата Фосфоглив (глицирризиновая кислота + фосфолипиды)) изучались в рандомизированных клинических исследованиях при НАЖБП [29], АБП [30], а также в качестве патогенетической терапии у пациентов с хроническим гепатитом С [31], которые не могли получать противовирусные препараты. Полученные результаты позволили включить данную фиксированную комбинацию в клинические рекомендации и стандарты оказания медицинской помощи.
Кроме того, было проведено несколько небольших исследований, доказавших положительное влияние Фосфоглива не только на состояние печени, но и на течение псориаза [32, 33].
Все это послужило основанием для более детального изучения потенциала препарата Фосфоглив у больных псориазом.
Результаты собственных исследований
Авторами проведено эпидемиологическое исследование распространенности заболеваний печени и их структуры у пациентов с псориазом и биоинформационное исследование влияния глицирризиновой кислоты на псориатический процесс.
В структуре установленных диагнозов заболеваний печени у пациентов с псориазом преобладали стеатоз и вирусные гепатиты, что отражает тенденцию, характерную для популяции (рис. 3).
Уровень АЛТ оказался повышенным у 119 (28,9%) мужчин и 73 (24,5%) женщин, АСТ – у 124 (30,1%) и 76 (25,6%), ГГТ – у 140 (34,06%) и 69 (23,2%), холестерин – у 93 (22,6%) и 86 (28,9%), билирубин – у 73 (17,76%) мужчин и 66 (22,22%) женщин соответственно. При этом у трети пациентов отмечались изменения по двум или трем показателям.
У 42,7% мужчин и 29,6% женщин с измененными биохимическими показателями диагноз в отношении заболевания печени поставлен не был.
Полученные результаты подтверждают целесообразность применения гепатопротекторов при псориазе.
В связи с актуальностью гепатопротекторов, способных воздействовать не только на гепатобилиарную систему, но и на воспалительные процессы при псориазе, представляется целесообразным применение препарата Фосфоглив. Действие его активных компонентов при поражении гепатоцитов хорошо изучено, в то время как влияние глицирризиновой кислоты на течение псориаза представляет несомненный научный и практический интерес.
С этой целью было проведено биоинформационное исследование с использованием реферативной базы данных ResNet и программы Pathway Studio (компания Ariadne Genomics Inc., США). База данных ResNet содержит аннотации биологических объектов, в том числе клеточных процессов и малых молекул, а также аннотации функциональных связей между ними, сформированные при обработке текстового массива полнотекстовых статей и абстрактов, индексированных в Medline.
Значимость объединенных общей функцией процессов и малых молекул оценивалась по тому, насколько пересечение их множества, приписанного к данной категории, превышало ожидаемый размер. Гипергеометрическое распределение использовали в качестве модели случайного пересечения множеств.
При помощи программы Pathway Studio производилось распределение процессов по приоритетам: чем меньше значение p, тем выше вероятность, что процессы, относящиеся к заболеванию, включены туда неслучайно.
Согласно анализу литературы, 164 белка достоверно регулируются глицирризиновой кислотой. Из них были отобраны белки с большим количеством ссылок. Наиболее релевантными по количеству связей являются только 42 белка (см. таблицу). Первое место среди них занимает HMGB1.
HMGB1 (амфотерин) – белок группы ядерных негистоновых белков HMG. Он взаимодействует с ДНК ядра клетки и играет важную роль в развитии воспаления. HMGB1 как цитокиновый медиатор секретируется активированными макрофагами и моноцитами и, будучи ядерным белком, может высвобождаться при некрозе клеток и тканей. После высвобождения HMGB1 может связываться с рецептором врожденного иммунитета TLR4, что приводит к секреции цитокинов макрофагами и последующей воспалительной реакции.
Помимо ингибирования HMGB1 глицирризиновая кислота угнетает продукцию провоспалительных цитокинов: TNF-α, IL-6, IL-8, IL-1 и др.
Подавляющее большинство белков (см. таблицу) играет важную роль в развитии псориаза. Учитывая, что HMGB1 наиболее представлен в связи с глицирризиновой кислотой, было решено использовать классический сигнальный каскад от этого белка с дальнейшим обогащением сигналинга другими наиболее представленными белками. В результате мы получили сигнальный путь, идущий от глицирризиновой кислоты через HMGB1, который может гипотетически ингибировать псориатический процесс: подавлять продукцию основных провоспалительных цитокинов и клеточные процессы, вовлеченные в развитие псориаза (рис. 4). Ингибирование HMGB1 глицирризиновой кислотой может приводить к снижению активности АКТ-1 и NF-kB, отвечающих за апоптотические процессы в клетке.
Таким образом, снижение ингибирования процесса апоптоза способно снизить псориатические проявления. Уменьшение экспрессии генов TNF-α, IL-17, IL-8, IL-1, IL-18 и ММР9 также должно существенно повлиять на уменьшение патологического процесса.
Результаты исследований подтвердили потенциальную возможность Фосфоглива влиять на патогенез псориаза. В связи с этим становится очевидным необходимость проведения исследований влияния Фосфоглива не только на процессы, протекающие в гепатобилиарной системе, но и на цитокиновый статус больных псориазом с целью ингибирования остроты псориатического процесса и, возможно, увеличения периода между рецидивами.
Цитомегалия – это инфекционное заболевание вирусного генеза, передающееся половым, трансплацентарным, бытовым, гемотрансфузионным путем. Симптоматически протекает в форме упорной простуды. Отмечается слабость, недомогание, головные и суставные боли, насморк, увеличение и воспаление слюнных желез, обильное слюноотделение. Часто протекает бессимптомно. Опасна цитомегалия беременных: она может вызывать самопроизвольный выкидыш, врожденные пороки развития, внутриутробную гибель плода, врожденную цитомегалию. Диагностика осуществляется лабораторными методами (ИФА, ПЦР). Лечение включает противовирусную и симптоматическую терапию.
МКБ-10
Общие сведения
Другие названия цитомегалии, встречающиеся в медицинских источниках, - цитомегаловирусная инфекция (ЦМВ), инклюзионная цитомегалия, вирусная болезнь слюнных желез, болезнь с включениями. Цитомегалия является широко распространенной инфекцией, и многие люди, являясь носителями цитомегаловируса, даже не подозревают об этом. Наличие антител к цитомегаловирусу выявляется у 10—15% населения в подростковом возрасте и у 50% взрослых людей. По некоторым источникам, носительство цитомегаловируса определяется у 80% женщин детородного периода. В первую очередь это относится к бессимптомному и малосимптомному течению цитомегаловирусной инфекции.

Причины
- воздушно-капельным: при чихании, кашле, разговоре, поцелуях и т.д.;
- половым путем: при сексуальных контактах через сперму, влагалищную и шеечную слизь;
- гемотрансфузионным: при переливании крови, лейкоцитарной массы, иногда - при пересадке органов и тканей;
- трансплацентарным: во время беременности от матери плоду.
Нередко цитомегаловирус находится в организме многие годы и может ни разу не проявить себя и не нанести вреда человеку. Проявление скрытой инфекции происходит, как правило, при ослаблении иммунитета. Угрожающую по своим последствиям опасность цитомегаловирус представляет у лиц со сниженным иммунитетом (ВИЧ-инфицированных, перенесших трансплантацию костного мозга или внутренних органов, принимающих иммунодепрессанты), при врожденной форме цитомегалии, у беременных.
Патогенез
Попадая в кровь, цитомегаловирус вызывает выраженную иммунную реакцию, проявляющуюся в выработке защитных белковых антител – иммуноглобулинов М и G (IgM и IgG) и противовирусной клеточной реакцией - образованием лимфоцитов CD 4 и CD 8. Угнетение клеточного иммунитета при ВИЧ-инфекции приводит к активному развитию цитомегаловируса и вызываемой им инфекции.
Даже при бессимптомном течении инфекции носитель цитомегаловируса является потенциально заразным для неинфицированных лиц. Исключение составляет внутриутробный путь передачи цитомегаловируса от беременной женщины плоду, который происходит в основном при активном течении процесса, и лишь в 5% случаев вызывает врожденную цитомегалию, в остальных же носит бессимптомный характер.
Симптомы цитомегалии
Врожденная цитомегалия
В 95% случаев внутриутробное инфицирование плода цитомегаловирусом не вызывает развития заболевания, а протекает бессимптомно. Врожденная цитомегаловирусная инфекция развивается у новорожденных, матери которых перенесли первичную цитомегалию. Врожденная цитомегалия может проявляться у новорожденных в различных формах:
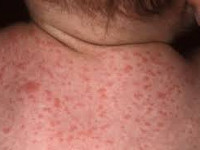
- петехиальная сыпь – мелкие кожные кровоизлияния - встречается у 60-80% новорожденных;
- недоношенность и задержка внутриутробного развития плода - встречается у 30% новорожденных;
- желтуха;
- хориоретинит – острый воспалительный процесс в сетчатке глаза, часто вызывающий снижение и полную потерю зрения.
Летальность при внутриутробном инфицировании цитомегаловирусом достигает 20-30%. Из выживших детей большая часть имеет отставание в умственном развитии или инвалидность по слуху и зрению.
Приобретенная цитомегалия у новорожденных
При инфицировании цитомегаловирусом в процессе родов (при прохождении плода по родовым путям) или в послеродовом периоде (при бытовом контакте с инфицированной матерью или грудном вскармливании) в большинстве случаев развивается бессимптомное течение цитомегаловирусной инфекции. Однако у недоношенных младенцев цитомегаловирус может вызывать затяжную пневмонию, к которой часто присоединяется сопутствующая бактериальная инфекция. Часто при поражении цитомегаловирусом у детей отмечается замедление в физическом развитии, увеличение лимфоузлов, гепатит, сыпь.
Мононуклеозоподобный синдром
У лиц, вышедших из периода новорожденности и имеющих нормальный иммунитет, цитомегаловирус может вызывать развитие мононуклеозоподобного синдрома. Течение мононуклеазоподобного синдрома по клинике не отличается от инфекционного мононуклеоза, вызываемого другой разновидностью герпесвируса – вирусом Эбштейна-Барр. Течение мононуклеозоподобного синдрома напоминает упорную простудную инфекцию. При этом отмечается:
- длительная (до 1 месяца и более) лихорадка с высокой температурой тела и ознобами;
- ломота в суставах и мышцах, головная боль;
- выраженные слабость, недомогание, утомляемость;
- боли в горле;
- увеличение лимфоузлов и слюнных желез;
- кожные высыпания, напоминающие сыпь при краснухе (обычно встречается при лечении ампициллином).
В отдельных случаях мононуклеозоподобный синдром сопровождается развитием гепатита – желтухой и повышением в крови печеночных ферментов. Еще реже (до 6% случаев) осложнением мононуклеозоподобного синдрома служит пневмония. Однако у лиц с нормальной иммунной реактивностью она протекает без клинических проявлений, выявляясь лишь при проведении рентгенографии легких.
Длительность течения мононуклеозоподобного синдрома составляет от 9 до 60 дней. Затем обычно наступает полное выздоровление, хотя на протяжении нескольких месяцев могут сохраняться остаточные явления в виде недомогания, слабости, увеличенных лимфоузлов. В редких случаях активизация цитомегаловируса вызывает рецидивы инфекции с лихорадкой, потливостью, приливами и недомоганием.
Цитомегаловирусная инфекция у лиц с ослабленным иммунитетом
Ослабление иммунитета наблюдается у лиц, страдающих синдромом врожденного и приобретенного (СПИД) иммунодефицита, а также у пациентов, перенесших пересадку внутренних органов и тканей: сердца, легкого, почки, печени, костного мозга. После пересадки органов пациенты вынуждены постоянно принимать иммунодепрессанты, ведущие к выраженному подавлению иммунных реакций, что вызывает активность цитомегаловируса в организме.
У пациентов, перенесших трансплантацию органов, цитомегаловирус вызывает поражение донорских тканей и органов (гепатит – при пересадке печени, пневмонию при пересадке легкого и т. д.). После трансплантации костного мозга у 15-20% пациентов цитомегаловирус может привести к развитию пневмонии с высокой летальностью (84-88%). Наибольшую опасность представляет ситуация, когда инфицированный цитомегаловирусом донорский материал пересажен неинфицированному реципиенту.
Цитомегаловирус поражает практически всех ВИЧ-инфицированных. В начале заболевания отмечаются недомогание, суставные и мышечные боли, лихорадка, ночная потливость. В дальнейшем к этим признакам могут присоединяться поражения цитомегаловирусом легких (пневмония), печени (гепатит), мозга (энцефалит), сетчатки глаза (ретинит), язвенные поражения и желудочно-кишечные кровотечения.
У мужчин цитомегаловирусом могут поражаться яички, простата, у женщин – шейка матки, внутренний слой матки, влагалище, яичники. Осложнениями цитомегаловирусной инфекции у ВИЧ-инфицированных могут стать внутренние кровотечения из пораженных органов, потеря зрения. Множественное поражение органов цитомегаловирусом может привести к их дисфункции и гибели пациента.
Диагностика
С целью диагностики цитомегаловирусной инфекции проводится лабораторное обследование. Постановка диагноза цитомегаловирусной инфекции основана на выделении цитомегаловируса в клиническом материале или при четырехкратном повышении титра антител.
- ИФА-диагностика. Включает определение в крови специфических антител к цитомегаловирусу - иммуноглобулинов М и G. Наличие иммуноглобулинов М может свидетельствовать о первичном заражении цитомегаловирусом либо о реактивации хронической ЦМВИ. Определение высоких титров IgМ у беременных может угрожать инфицированию плода. Повышение IgМ выявляется в крови спустя 4-7 недель после заражения цитомегаловирусом и наблюдается на протяжении 16-20 недель. Повышение иммуноглобулинов G развивается в период затухания активности цитомегаловирусной инфекции. Их наличие в крови говорит о присутствии цитомегаловируса в организме, но не отражает активности инфекционного процесса.
- ПЦР-диагностика. Для определения ДНК цитомегаловируса в клетках крови и слизистых (в материалах соскобов из уретры и цервикального канала, в мокроте, слюне и т. д.) используется метод ПЦР-диагностики (полимеразной цепной реакции). Особенно информативно проведение количественной ПЦР, дающей представление об активности цитомегаловируса и вызываемого им инфекционного процесса.
В зависимости от того, какой орган поражен цитомегаловирусной инфекцией, пациент нуждается в консультации гинеколога, андролога, гастроэнтеролога или других специалистов. Дополнительно по показаниям проводится УЗИ органов брюшной полости, кольпоскопия, гастроскопия, МРТ головного мозга и другие обследования.
Лечение цитомегаловирусной инфекции
Неосложненные формы мононуклеазоподобного синдрома не требует специфической терапии. Обычно проводятся мероприятия, идентичные лечению обычного простудного заболевания. Для снятия симптомов интоксикации, вызываемой цитомегаловирусом, рекомендуется пить достаточное количество жидкости.
Лечение цитомегаловирусной инфекции у лиц, входящих в группу риска, проводится противовирусным препаратом ганцикловиром. В случаях тяжелого течения цитомегалии ганцикловир вводится внутривенно, т. к. таблетированные формы препарата обладают лишь профилактическим эффектом в отношении цитомегаловируса. Поскольку ганцикловир обладает выраженными побочными эффектами (вызывает угнетение кроветворения - анемию, нейтропению, тромбоцитопению, кожные реакции, желудочно-кишечные расстройства, повышение температуры и ознобы и др.), его применение ограничено у беременных, детей и у людей, страдающих почечной недостаточностью (только по жизненным показаниям), он не используется у пациентов без нарушения иммунитета.
Для лечения цитомегаловируса у ВИЧ-инфицированных наиболее эффективен препарат фоскарнет, также обладающий рядом побочных эффектов. Фоскарнет может вызывать нарушение электролитного обмена (снижение в плазме крови магния и калия), изъязвление половых органов, нарушение мочеиспускания, тошноту, поражение почек. Данные побочные реакции требуют осторожного применения и своевременной корректировки дозы препарата.
Прогноз
Особую опасность цитомегаловирус представляет при беременности, так как может провоцировать выкидыш, мертворождение или вызывать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с герпесом, токсоплазмозом и краснухой, относится к числу тех инфекций, обследоваться на которые женщины должны профилактически, еще на этапе планирования беременности.
Профилактика
Особенно остро вопрос профилактики цитомегаловирусной инфекции стоит у лиц, входящих в группу риска. Наиболее подвержены инфицированию цитомегаловирусом и развитию заболевания ВИЧ-инфицированные (особенно больные СПИДом), пациенты после трансплантации органов и лица с иммунодефицитом иного генеза.
Неспецифические методы профилактики (например, соблюдение личной гигиены) неэффективны в отношении цитомегаловируса, так как заражение им возможно даже воздушно-капельным путем. Специфическая профилактика цитомегаловирусной инфекции проводится ганцикловиром, ацикловиром, фоскарнетом среди пациентов, входящих в группы риска. Также для исключения возможности инфицирования цитомегаловирусом реципиентов при пересадке органов и тканей необходим тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Цитомегаловирусная инфекция у детей — это инфекционное заболевание, которое вызвано цитомегаловирусом и поражает слюнные железы, внутренние органы, ЦНС. В детстве патология чаще возникает при трансплацентарном или интранатальном заражении. Локализованные формы проявляются сиаладенитом, гепатитом, нефритом и т. д., распространенный вариант инфекции характеризуется поражением головного мозга, легких, почек и органов ЖКТ. Диагностика предполагает идентификацию возбудителя цитологическими, гистологическими, серологическими и молекулярно-биологическими методами. Лечение цитомегаловирусной болезни проводится специфическим иммуноглобулином и противовирусными препаратами.
МКБ-10
Общие сведения
Заражение цитомегаловирусной инфекцией (ЦМВИ) наблюдается у 20%‒60% всего детского населения, но в большинстве случаев оно протекает бессимптомно. Внутриутробное инфицирование вирусом от больной матери происходит в 30-50% случаев, при этом до 18% младенцев после рождения имеют клинические симптомы. Учитывая полиморфизм клинической картины, ранняя диагностика и лечение у детей затруднены. Цитомегаловирусная инфекция представляет серьезную опасность, особенно для плода и новорожденного, у которых заболевание, как правило, вызывает необратимые осложнения.

Причины
Болезнь вызвана герпесвирусом 5 типа — Cytomegalovirus hominis. Он имеет 6 штаммов: Davis, AD 169, Kerr, C-87, Esp, Towne, причем ребенок может быть инфицирован сразу несколькими подтипами возбудителя. Цитомегаловирус (ЦМВ) имеет ДНК-геном, отличается медленной репликацией и сравнительно низкой вирулентностью. Он термолабилен, уничтожается при температуре более 56°С, но длительно сохраняет жизнеспособность в комнатных условиях.
При врожденной ЦВМИ передача вируса к плоду происходит трансплацентарно, при перинатальной инфекции — путем контакта с вагинальными выделениями матери, грудным молоком или препаратами крови. Риск заражения увеличивается, если мать с острой формой болезни не получает специфическое лечение. В постнатальном периоде ребенок чаще всего заражается от ближайших родственников и сверстников воздушно-капельным или контактно-бытовым путем.
Патогенез
Попадая в кровь, вирус реплицируется в лейкоцитах, моноцитах и макрофагах и в дальнейшем он пожизненно сохраняется в лимфоцитарных органах. Зачастую процесс выражается в виде латентной инфекции, при которой у ребенка нет симптомов, и ему не требуется лечение. Активность цитомегаловируса зависит от состояния иммунитета: при физиологической иммунной недостаточности, которая наблюдается у детей раннего возраста, риск манифестной цитомегаловирусной инфекции возрастает в разы.
Классификация
В детской инфектологии различают врожденную (внутриутробную) и приобретенную формы патологии. По течению инфекция бывает острой (до 3 месяцев), подострой (3-6 месяцев), затяжной (6-12 месяцев) и хронической (более 1 года). По клиническим признакам выделяют локализованный (сиаладенит, нефрит, гепатит, энцефалит) и генерализованный вариант. С учетом тяжести течения цитомегаловирусную болезнь делят на 3 степени:
- Легкая. Отличается незначительными патоморфологическими изменениями во внутренних органах, которые не сказываются на их функциональной активности.
- Среднетяжелая. Проявляется выраженными органическими поражениями в сочетании с клиническими симптомами и расстройством функции некоторых внутренних органов.
- Тяжелая. Манифестирует тяжелыми органическими патологиями, резко выраженной интоксикацией и генерализованным характером поражения.
Симптомы
Врожденная ЦМВИ
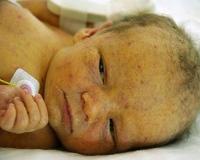
У пациентов с манифестной врожденной форме цитомегаловирусной болезни признаки наблюдаются с первых дней жизни. Типичный комплекс симптомов у новорожденных детей включает недоношенность и/или низкую массу тела, поражение гепатобилиарной системы (увеличение печени, желтуха, гепатиты и циррозы), лимфаденопатии и геморрагическую сыпь на коже. Если инфицирование произошло на ранних сроках беременности, ребенок рождается с аномалиями — микроцефалией, гипоплазией легких, атрезией пищевода.
Приобретенная ЦМВИ
Приобретенная цитомегаловирусная болезнь обычно протекает в субклинической или латентной форме, когда у ребенка возникают гриппоподобные симптомы, субфебрильная температура без видимой причины. После заражения инфекция может длительное время себя не проявлять и давать обострения при снижении иммунного статуса, действии неблагоприятных эндо- или экзогенных факторов.
Течение манифестной приобретенной формы напоминает инфекционный мононуклеоз. У ребенка внезапно появляется слабость, повышается температура, беспокоят недомогание, головные боли, отсутствует аппетит. Позже присоединяются сильные боли в горле, увеличиваются подчелюстные и шейные лимфоузлы. Если цитомегаловирусная инфекция проявляется сиаладенитом, наблюдается резкое увеличение и болезненность слюнных желез на фоне фебрильной лихорадки.
Генерализованная ЦМВИ
При генерализованном варианте течения инфекции у детей поражается бронхолегочная система (пневмонии, дыхательная недостаточность), ЖКТ (энтероколит, мальабсорбция), печень (желтуха, цитомегаловирусный гепатит, билиарный цирроз). Особенно опасно вовлечение в процесс нервной системы, что проявляется судорожным синдромом, парезами и параличами, задержкой психомоторного развития.
Осложнения
Поражение клеток при цитомегаловирусной болезни создает благоприятные условия для возникновения аутоиммунных поражений — системной красной волчанки, рассеянного склероза, гломерулонефрита. Иногда после малосимптомной врожденной цитомегаловирусной инфекции осложнения наблюдаются в отдаленном периоде (в возрасте ребенка 2-5 лет). В основном они проявляются неврологическими расстройствами и поражением органов чувств.
Диагностика
Цитомегаловирусная инфекция отличается многообразием клинических признаков и часто протекает под маской других патологий, что затрудняет работу детского инфекциониста. На первичном приеме, помимо стандартного физикального осмотра, врач собирает детальный акушерский анамнез, чтобы выявить факторы риска антенатального инфицирования. Диагноз ЦМВИ правомочен только при лабораторном подтверждении, для чего используют следующие методы:
Инструментальные методы подбираются соответственно форме заболевания. Для оценки структурно-функциональных особенностей печени и билиарного тракта назначают УЗИ органов брюшной полости. КТ и МРТ головного мозга информативны для выявления врожденных пороков и кальцификатов. Рентгенография ОГК необходима при симптомах дыхательных расстройств. По показаниям ребенка направляют на консультации к профильным специалистам— кардиологу, неврологу, отоларингологу.
Лечение цитомегаловирусной инфекции у детей
Препаратом выбора у новорожденных и детей первого года жизни является специфический антицитомегаловирусный иммуноглобулин, который имеет повышенную концентрацию IgG. Лечение начинают при манифестных формах заболевания и проводят по схеме: вначале вводится высокая доза препарата, а спустя 9-10 дней дозировку постепенно уменьшают, контролируя степень ответа на терапию и активность процесса.
В старшем возрасте перечень препаратов, применяемых при цитомегаловирусной инфекции, значительно расширяется. Лечение включает противовирусные средства из группы нуклеозидов и нуклеотидов (ганцикловир, валганцикловир), производные ортофосфорной кислоты (фоскарнет). При легкой и среднетяжелой формах назначают интерфероны, иммуностимуляторы.
Для купирования интоксикации показано обильное питье (при легких формах), при среднетяжелых и тяжелых клинических вариантах рекомендована инфузионная терапия. Патогенетическая терапия подбирается в соответствии с характером течения болезни и может включать пищеварительные ферменты, ингибиторы протеиназ, гемостатики. Для предупреждения вторичных бактериальных осложнений используют антибиотики (макролиды, цефалоспорины, гликопептиды).
Прогноз и профилактика
При малосимптомных приобретенных вариантах цитомегаловирусная болезнь протекает без осложнений, зачастую у ребенка выявляется только латентное носительство. Угрозу для жизни и здоровья представляют тяжелые генерализованные инфекции, которые в 50-60% случаев сопровождаются осложнениями, несмотря на проводимое лечение. Особо опасно поражение цитомегаловирусом для детей с иммунодефицитными состояниями.
Основу профилактики врожденной ЦМВИ составляет обязательное лабораторное обследование женщин на носительство цитомегаловируса, которое проводится при планировании зачатия и во время беременности. Если в семье есть пациент с цитомегаловирусной инфекцией, необходимо ограничить его общение с ребенком и обеспечить лечение. Карантинно-изоляционные мероприятия в отношении заболевших и контактных лиц не производятся.
2. Клинические рекомендации (протокол лечения) оказания медицинской помощи детям больным цитомегаловирусной инфекцией. — 2015.
Вирусные инфекции половых органов продолжают привлекать пристальное внимание исследователей и клиницистов вследствие роста заболеваемости, значительной контагиозности и потенциальной онкогенности.
- КЛЮЧЕВЫЕ СЛОВА: вирусы, инфекции, гистамин, фосфолипаза, герпес, Эпиген интим
Вирусные инфекции половых органов продолжают привлекать пристальное внимание исследователей и клиницистов вследствие роста заболеваемости, значительной контагиозности и потенциальной онкогенности.
Рисунок 1. Динамика уровня цитокинов в цервикальном канале после применения глицирризиновой кислоты/плацебо при генитальном герпесе
Рисунок 2. Динамика уровня ММР-1 и ТIМР-1 в цервикальном канале после применения глицирризиновой кислоты/плацебо при генитальном герпесе
Рисунок 3. Динамика уровня цитокинов в цервикальном канале после применения глицирризиновой кислоты/плацебо при папилломавирусной инфекции
Рисунок 4. Динамика уровня ММР-1 и ТIМР-1 в цервикальном канале после применения глицирризиновой кислоты/плацебо при папилломавирусной инфекции
Рисунок 5. Динамика уровня цитокинов в цервикальном канале после применения глицирризиновой кислоты/плацебо при цитомегаловирусной инфекции
Рисунок 6. Динамика уровня ММР-1 и ТIМР-1 в цервикальном канале после применения глицирризиновой кислоты/плацебо при цитомегаловирусной инфекции
Исследования последних лет показали, что вирусы способны поддерживать воспалительный процесс в зоне поражения с изменением структурно-функциональных характеристик ткани, вызывать изменения антигенной структуры инфицированных клеток, индуцируя появление аутоантител, могут быть индукторами неопластических трансформаций. Локальные изменения слизистых оболочек и кожи при вирусной инвазии проявляются появлением в ткани воспалительных инфильтратов, активацией клеток иммунной системы, изменением уровня цитокинов, факторов роста и протеолитических ферментов, активацией ангиогенеза, изменением экспрессии генов.
Препараты солодки обладают многосторонней биологической активностью и оказывают противовоспалительное, противовирусное и иммуномодулирующее действие. Противовоспалительное действие заключается в купировании воспалительных реакций, вызываемых гистамином, серотонином и брадикинином. Кислота ингибирует активность фосфолипазы А и образование простагландина Е2 в активированных макрофагах, ускоряет миграцию лейкоцитов в зону воспаления. При этом угнетается как экссудативная, так и пролиферативная фаза воспалительного процесса. Как показали исследования, глицирризиновая кислота обладает также выраженным противовирусным действием. Первое исследование антивирусных свойств глицирризиновой кислоты было проведено в 1979 году, а в 90-е годы было установлено, что она прерывает репликацию вирусов на ранних стадиях за счет ингибирования киназы Р.
В ряде исследований было показано, что мутантные штаммы вирусов, резистентные к ацикловиру, сохраняют чувствительность к глицирризиновой кислоте. При взаимодействии кислоты с вирионами изменяются различные фазы вирусного цикла, что сопровождается необратимой инактивацией вирусных частиц, находящихся в свободном состоянии вне клеток; блокируется внедрение активных вирусных частиц внутрь клетки, нарушается способность вируса к индукции синтеза новых вирусных частиц.
Глицирризиновая кислота обладает также выраженным иммуномодулирующим действием. Показана способность глицирризиновой кислоты индуцировать образование ИФН и активировать неспецифические факторы клеточного иммунитета.
Все пациентки были разделены на группы:
- I группа – 30 женщин с папилломавирусной инфекцией половых органов;
- II группа – 30 женщин с типичной формой генитального герпеса (легкой и средней степени тяжести);
- III группа – 30 женщин с цитомегаловирусной инфекцией половых органов;
- контрольная группа – 10 здоровых женщин репродуктивного возраста.
В исследовании с целью оценки механизма действия исследуемого препарата использовалась модель моноинфекции и монотерапии. В каждой группе пациенткам проводили местную терапию глицирризиновой кислотой (n = 20) или препаратом плацебо (n = 10) в течение 1 мес., препарат наносили ежедневно по 2-3 раза на слизистые оболочки половых органов путем распыления, при локализации поражений на шейке матки препарат применяли интравагинально с помощью специальной насадки. Назначение препарата или плацебо в группах проводили слепым методом. Во время исследования лечение другими противовирусными препаратами не проводилось. Клиническую эффективность терапии оценивали в ходе лечения, период последующего наблюдения составил 6 мес.
С целью оценки локального действия глицирризиновой кислоты (до лечения и сразу после его окончания) исследовали слизь цервикального канала на содержание провоспалительных Th1-цитокинов – IL-1b, IL-6, TNF-α и IFN-γ, противовоспалительных Th2-цитокинов – IL-4, IL-10, а также матриксных металлопротеиназ ММР-1 и тканевых ингибиторов матриксных металлопротеиназ ТIМР-1.
Анализ динамики клинических симптомов инфекции после применения глицирризиновой кислоты свидетельствует о высокой клинической эффективности препарата. При типичной форме генитального герпеса на фоне лечения длительность и клиническая выраженность рецидивов герпеса по субъективной оценке больных значительно уменьшилась, что позитивно повлияло на качество жизни пациенток. По сравнению с плацебо на фоне применения глицирризиновой кислоты отмечалось быстрое купирование симптомов вульводинии (зуда, жжения, дискомфорта в области герпетических высыпаний вульвы и влагалища); более быстрое заживление поражений (в среднем на 2 ± 0,78 дня по сравнению с плацебо); ускорение процессов эпителизации зон поражения; значительное сокращение зоны гиперемии вокруг герпетических элементов и реакции регионарных лимфатических узлов. Значительное снижение на фоне лечения местной воспалительной реакции, окружающей герпетические элементы, и ускорение процессов репарации ткани способствовало снижению риска присоединения вторичной бактериальной инфекции и развитию осложнений.
На фоне терапии глицирризиновой кислотой у пациенток с экзофитными формами папилломавирусной инфекции гениталий отмечалось купирование симптомов стойкого дискомфорта, зуда и жжения в области наружных половых органов через 4-6 дней от начала применения препарата. При наличии небольших и множественных кондилом вульвы и влагалища отмечено значительное уменьшение экзофитных образований в размере и общей площади поражения. При цитомегаловирусной инфекции исходно только у 6 пациенток отмечались симптомы вульводинии, которые были быстро купированы на фоне терапии глицирризиновой кислотой.
Основной задачей исследования была оценка влияния глицирризиновой кислоты на локальные молекулярно-биологические процессы в половом тракте при вирусных инфекциях. При анализе содержания провоспалительных цитокинов IL-1b, IL-6, TNF-α и IFN-γ в цервикальном канале до лечения во всех группах было выявлено, что персистенция вирусной инфекции сопровождалась значительным увеличением уровня Th1-цитокинов, что отражало интенсивность воспалительных реакций в ткани и являлось важным маркером фазы активации вирусной инфекции. При всех типах вирусной инфекции локальные уровни Th1-цитокинов достоверно превышали контрольные значения:
- при генитальном герпесе в I группе уровень IL-1b был повышен в 33,2 раза, IL-6 – в 3,5 раза, TNF-α – в 4,6 раза и IFN-γ – в 3,6 раза;
- при папилломавирусной инфекции во II группе уровень IL-1b был повышен в 62,4 раза, IL-6 – в 2,4 раза, TNF-α – в 13,6 раза и IFN-γ – в 3 раза;
- при цитомегаловирусной инфекции в III группе уровень IL-1b был повышен в 18,6 раза, IL-6 – в 1,3 раза, TNF-α – в 3,7 раза и IFN-γ – в 2,8 раз (во всех случаях p 0,05 (рисунки: 1, 3, 5).
При анализе системы тканевых протеолитических ферментов матриксных металлопротеиназ и их ингибиторов как ключевых эффекторов тканевого ремоделирования и важных маркеров воспалительного процесса во всех группах выявлено повышение локальной активности ММР-1 (рисунки: 2, 4, 6).
После курса терапии глицирризиновой кислотой локальные уровни Th1-цитокинов IL-1b, IL-6, TNF-α и IFN-γ в цервикальном канале достоверно снизились до контрольных значений, при этом динамика изменений была особенно показательна в I группе пациенток с генитальным герпесом, где исходная интенсивность воспалительных реакций была максимальной (рисунки 1, 3 и 5).
Терапия глицирризиновой кислотой привела к усилению защитного потенциала слизистой оболочки – к активации противовоспалительных Th2-цитокинов, при этом уровни IL-4 и IL-10 повысились, в ряде случаев превысив контрольные значения. При применении плацебо уровни провоспалительных Th1-цитокинов и регуляторных Th2-цитокинов незначительно колебались за счет волнообразности самого вирусного инфекционного процесса, но достоверно не изменились (p > 0,05 во всех группах по сравнению с исходными значениями и контролем).
При анализе действия глицирризиновой кислоты на уровень тканевых матриксных металлопротеиназ выявлено достоверное снижение после лечения активности протеолитических ферментов до контрольных значений:
Читайте также:

