Цитомегаловирус на слизистых оболочках
Обновлено: 24.04.2024
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
ГБОУ ВПО "Московский государственный медико-стоматологический университет им. А.И. Евдокимова"
Институт химической физики им. Н.Н. Семенова РАН, Москва
Совершенствование терапии цитомегаловирусной инфекции у мужчин
Журнал: Клиническая дерматология и венерология. 2016;15(3): 48‑52
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
Увеличилось количество сексуально активных мужчин с хроническими воспалительными заболеваниями органов малого таза (ВЗОМТ), при обследовании которых в соскобах из уретры выявлялись ДНК цитомегаловируса (ЦМВ). Цель исследования — совершенствование подходов к диагностике и терапии цитомегаловирусной инфекции урогенитального тракта. Материал и методы. Под наблюдением находились 56 пациентов с ВЗОМТ, обусловленными патогенной, условно-патогенной микрофлорой и ЦМВ. Назначали 0,004% раствор Панавира по 5 мл внутривенно, антибактериальные препараты. Результаты. Комплексная терапия с применением антибактериальных препаратов и 0,004% раствор Панавира по 5 мл внутривенно у пациентов с инфекцией ЦМВ в урогенитальном тракте показала эффективность в 84,61% случаев.
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
ГБОУ ВПО "Московский государственный медико-стоматологический университет им. А.И. Евдокимова"
Институт химической физики им. Н.Н. Семенова РАН, Москва
Выделяют два периода жизни человека, наиболее уязвимых для инфицирования, — детский возраст до 5—6 лет, когда передача инфекции происходит от матери к ребенку или от детей, выделяющих вирус. Вторым критическим периодом является возраст 16—30 лет: в данной группе лиц передача вируса осуществляется от лиц с латентным или субклиническим течением инфекции, главным образом половым путем как при гомо-, так и гетеросексуальных контактах.
Среди условий, способствующих реактивации ЦМВИ, выделяют: стрессы (психотравмы, длительные интеллектуальные и физические перегрузки, хронический дефицит сна); инфекции, имеющие повреждающее действие на иммунную систему; нарушения метаболизма вследствие заболевания органов эндокринной системы (гипотиреоз, тиреотоксикоз, недостаточность половых гормонов, сахарный диабет) или дефицита белков, микроэлементов, витаминов; истощение антиоксидантной системы в результате хронической инфекции, радиационных поражений, заболеваний внутренних органов, токсического действия продуктов свободнорадикального окисления; интоксикации различного генеза. К ятрогенным факторам относят длительный прием иммуносупрессантов, включая глюкокортикоиды и цитостатики.
По данным Е.А. Григорьевой и соавт. (2003), к ухудшению состояния больных ЦМВИ приводили интеркуррентные заболевания, хронические воспалительные заболевания гениталий. Вторичный иммунодефицит, проявляющийся резким угнетением фагоцитарной активности нейтрофилов крови, функциональной активности Т-лимфоцитов и недостаточностью иммунного ответа, способствует реактивации ЦМВ, способного в свою очередь вызывать депрессию практически всех звеньев иммунитета: угнетение клеток-киллеров, дисфункцию макрофагов, дефицит продукции интерлейкинов. Отмечено, что при ассоциации с другими возбудителями ЦМВ может приобретать цитопатические свойства, поддерживать воспалительную реакцию, снижать эффективность специфической терапии (Дерябин П.Г., 2003; Чернова Н.И., 2013). Полное выздоровление происходит лишь в том случае, если из организма удален возбудитель и выключены иммунопатологические механизмы, а временный дефект иммунологической реактивности ликвидирован. Следовательно, диагностика ЦМВИ заключается не только в детекции ЦМВ в организме пациента, но и в определении факторов, способствующих повышению вирусной активности, которая обусловливает патологические изменения в органах.
Решение этих задач зависит от мастерства врачей, чья недостаточная компетентность может приводить к диагностическим ошибкам, следовательно, к неправильному лечению. При назначении терапии следует учитывать, что наибольшую эффективность следует ожидать от препаратов, сочетающих этиотропный и иммуномодулирующий эффекты. Наряду с созданием новых химических средств идет интенсивный поиск среди соединений растительного происхождения. В данном аспекте определенный интерес представляет отечественный препарат Панавир — очищенный экстракт побегов растения Solanum tuberosum, биологически активный полисахарид, основное действующее вещество которого — гексозный гликозид, полученный методом ферментативного гидролиза с последующей газожидкостной хроматографией, состоящий из глюкозы, рамнозы, арабинозы, маннозы, ксилозы, галактозы, уроновых кислот, результат более чем десятилетних исследований ученых НИИ физико-химической медицины РАМН. Доклинические исследования на моделях вирусных инфекций на протяжении ряда лет проходили в основном в НИИ вирусологии им. Д.И. Ивановского и в НИИ физико-химической медицины РАМН. Так, под руководством проф. А.А. Кущ в лаборатории клеточной инженерии ГН НИИ вирусологии им. Д.И. Ивановского была показана высокая противовирусная активность Панавира в отношении ЦМВ. Препарат в определенном диапазоне доз полностью предотвращал вирус-индуцированное цитопатическое действие (ЦПД) в культурах клеток, обладал способностью тормозить развитие ЦПД в клетках, повышал жизнеспособность клеток в присутствии вирусов. В экспериментах in vitro было показано, что препарат обладает относительно низким цитотоксическим и антипролиферативным действием в отношении целого ряда клеточных культур (перевиваемые клетки линии Vero, диплоидные клетки фибробластов эмбрионов человека, клетки SW-13). В ходе токсикологических исследований было выявлено, что ЛД50 в несколько тысяч раз выше оптимальной терапевтической дозы, а также было показано, что Панавир не обладает тератогенными, мутагенными свойствами, не изменяет реологические показатели крови. Доклинические исследования in vitro и in vivo выявили противовирусные свойства препарата в отношении инфекций, вызываемых самыми разными вирусами, как ДНК-, так и РНК-содержащими, например, вирусами простого герпеса (ВПГ) 1-го и 2-го типов, ЦМВ, вирусом гепатита С, гриппа А, В, аденовирусами, что свидетельствует о поливалентном характере противовирусной активности нового препарата. Характерными особенностями механизма противовирусной активности Панавира являются его влияние на ингибирование синтеза вирусных белков и доказанное повышение жизнеспособности клеток в культуре в присутствии вирусов, снижение титров вирусов в культуре клеток и в эксперименте на животных, увеличение латентного периода развития экспериментальной инфекции in vitro и in vivo, митогенная активность в реакции бласттрансформации лимфоцитов, способность модулировать уровень лейкоцитарных интерферонов α и γ. Противовирусное действие Панавира включает несколько механизмов:
1) препятствие адгезии вируса на поверхности клетки;
2) блокада пенетрации вируса в клетку;
3) нарушение синтеза капсидных белков и заключительной сборки вируса.
В ходе исследований, проведенных в ЦНИКВИ Минздрава России, на кафедре кожных и венерических болезней МГМСУ, Уральском НИИ дерматовенерологии, МОНИКИ, Научном центре акушерства и гинекологии, показана высокая эффективность Панавира в терапии пациенток с генитальной герпетической, папилломавирусной, цитомегаловирусной инфекциями.
При ЦМВИ Панавир назначают в форме 0,004% раствора по 5 мл внутривенно по схеме: три инъекции через 48 ч в течение 1-й недели и две инъекции с интервалом 72 ч в течение 2-й недели (всего пять инъекций на курс).
Цель исследования — совершенствование терапии ЦМВИ у мужчин.
Материал и методы
Под наблюдением находились 56 мужчин в возрасте от 20 до 35 лет с ЦМВИ урогенитального тракта (УГТ).
Лабораторная диагностика
1. Микроскопическое исследование с целью определения эпителия, лейкоцитарной реакции, морфотипа биоты, внутриклеточных грамотрицательных диплококков (Neisseria gonorrhoeae), Trichomonas vaginalis.
2. Культуральное исследование с целью выявления роста N. gonorrhoeae, T. vaginalis, Ureaplasma urealyticum, Mycoplasma hominis, условно-патогенной микрофлоры.
3. Молекулярно-генетическое исследование с целью детекции ДНК Chlamydia trachomatis, N. gonorrhoeae, T. vaginalis, Mycoplasma genitalium, Ureaplasma spp., Gardnerella vaginalis, M. hominis, вируса папилломы человека (ВПЧ) и ВПГ (качественное и количественное).
4. Для детекции ЦМВИ использовали иммуноферментный анализ (ИФА) с выявлением в сыворотке крови специфических анти-ЦМВ классов IgM (качественный анализ) и IgG (количественный анализ). Вирусологическое выявление ЦМВ проводили на культуре фибробластов легких эмбриона человека, при исследовании крови, слюны, мочи, эякулята. ДНК ЦМВ в отделяемом из УГТ определяли посредством полимеразной цепной реакции (ПЦР). Всем пациентам проведено микроскопическое и бактериологическое исследование клинического материала из уретры.
На протяжении исследования проводилось четыре визита, включающих однократный осмотр во время лечения, далее через 30, 60 и 90 дней после лечения с лабораторным контролем на 30-й и 90-й день лечения.
Больные были разделены на две группы: в 1-ю вошли 14 мужчин без ИППП, во 2-ю — 42 человека с инфекционными заболеваниями УГТ. Антимикробная терапия определялась чувствительностью микрофлоры к антибиотикам, возможностью создания в очаге инфекции концентрации препаратов, подавляющих жизнедеятельность микроорганизмов, отсутствием или маловыраженным побочным действием на организм больного. Учитывая этиологию, патогенез, клиническую симптоматику, терапия проводилась в соответствии с клиническими рекомендациями: джозамицин по 500 мг 3 раза в сутки или доксициклина моногидрат по 100 мг в сутки. В зависимости от топического диагноза курс составлял 10—20 сут. Препараты применялись в комбинации с метронидазолом по 500 мг 2 раза в день 5—10 дней.
Всем больным с ИППП был назначен 0,004% раствор Панавира по 5 мл внутривенно — три инъекции через 48 ч в течение 1-й недели и две инъекции с интервалом 72 ч в течение 2-й недели.
Оценка эффективности терапии основывалась на данных динамики субъективных и объективных симптомов и результатов лабораторной диагностики.
На протяжении исследования проводилось четыре визита, включающих два осмотра до лечения, далее через 30 (с лабораторным контролем) и 90 дней после проведенной терапии.
Результаты
Средний возраст пациентов составил 29,15±4,18 года. Количество холостых и состоящих в браке оказалось одинаковым (по 50%). При анализе данных сексуального анамнеза мужчин, обратившихся за медицинской помощью, было констатировано, что 100% пациентов имели незащищенные орогенитальные контакты с новым партнером, при этом женатые мужчины имели связи вне брака, 12 человек отмечали случайные половые контакты.
Основные жалобы были представлены дискомфортом в уретре и промежности, наличием выделений, а также дизурическими расстройствами разной степени выраженности. Длительность перечисленных симптомов отмечалась в среднем от 3 мес до 2 лет. В результате проведенной терапии было установлено, что применение комплексной терапии способствовало купированию дискомфорта в области гениталий у большинства пациентов обоих групп.
У пациентов 2-й группы в отделяемом уретры отмечался лейкоцитоз от 10 до 80 в поле зрения. При культуральном исследовании рост T. vaginalis регистрировался у 22 обследованнных, условно-патогенной микрофлоры — у 100%. Через 30 и 90 дней после лечения нормализация лейкоцитоза отмечалась у 34 пациентов. При бактериологическом обследовании более высокие количественные показатели для таких возбудителей, как Streptococcus fаecalis, Staphylococcus epidermidis, Candida albicans, отмечены у 8 больных.
До лечения при помощи ПЦР выявлены С. trachomatis у 12 больных, а также ВПЧ, ВПГ у 33 пациентов 2-й группы (табл. 1).

Таблица 1. Результаты исследования ПЦР
В большинстве случаев была диагностирована микстинфекция, включающая 3—4 ассоцианта. Через 30 и 90 дней после проведенной терапии результаты были отрицательными у 42 (100%) больных.
При включении в исследование у всех мужчин (n=56, или 100%) были положительными анти-ЦМВ IgG и отрицательными IgМ. При обследовании крови, мочи, слюны, эякулята, соскобов из уретры с помощью молекулярно-генетического и вирусологического методов ЦМВ наиболее часто (78,69%) определялся в эякуляте и соскобах из уретры (60,66%) у пациентов с ИППП, тогда как у мужчин без патогенной микрофлоры в соскобах из уретры и в моче (14,29%) (табл. 2).

Таблица 2. Выявление маркеров CMV
Все пациенты переносили лечение хорошо, побочных эффектов или аллергических реакций отмечено не было.
Заключение
Результаты исследования демонстрируют высокую эффективность предложенного комплексного метода лечения генитальной бактериально-вирусной инфекции с использованием противовирусного препарата Панавир в форме 0,004% раствора по 5 мл внутривенно и антибактериальных препаратов.
Как показывает наблюдение за пролеченными больными в течение 90 дней, возникновение реактивации ЦМВИ после комплексной терапии с применением системного введения препарата Панавир в форме 0,004% раствора по 5 мл внутривенно произошло у 4 (9,52%) больных ИППП и у 4 (28,57%) — без ИППП.
Цитомегаловирусная инфекция (цитомегалия) – это обусловленные цитомегаловирусом определенные изменения в организме, возникающие в критические периоды жизни – при беременности, при иммунодефиците, в раннем младенческом возрасте.
Во взрослом возрасте у практически здоровых людей цитомегалия может длительно протекать в скрытой форме, а вирус может длительно находиться в организме, не проявляясь клинически.
Основа диагностики – лабораторное выявление цитомегаловируса или антител к нему в крови.
Обычно используется определение уровня антител класса IgМ и IgG (Anti-CMV-IgM и Anti-CMV-IgG) .
- Если в крови выявляются иммуноглобулины класса М (антитела класса IgM положительны), это говорит об активной инфекции и свежем заражении цитомегаловирусом, произошедшем в ближайшие 2-3 недели.
- Наличие только иммуноглобулинов G (антитела IgG положительны) в крови говорит о наличии цитомегаловируса в организме в неактивной фазе – это носительство без активации инфекции.
- Появление в крови нарастающего количества иммуноглобулина G (антитела класса IgG) говорит об активизации иммунитета и формировании иммунного ответа в организме.
- Если в крови есть оба класса иммуноглобулинов IgM и IgG – это инфекция, развившаяся около месяца назад или хроническая активная инфекция (по типу врожденной цитомегалии, инфекции у лиц с иммунодефицитом).
ЦМВ-инфекция у взрослых
Заражение цитомегаловирусом у взрослых может протекать под маской простуды упорного характера, при этом могут быть длительный насморк и недомогание, слабость, головные боли и боли в суставах, увеличение в области слюнных желез и лимфоузлов.
Чаще всего процесс заражения происходит практически незаметно для человека.
В целом тяжесть заболевания будет напрямую зависеть от состояния иммунной системы – течение может быть от полностью бессимптомного до тяжелой генерализованной инфекции.
Цитомегаловирус у детей
При врожденной ЦМВ-инфекции у новорожденных
- может возникать сыпь на коже в виде мелких кровоизлияний,
- может быть либо недоношенность, либо задержка внутриутробного развития малыша,
- может проявиться сильная желтуха сразу же после рождения,
- развитие хориоретинита (воспаление сетчатки и сосудистой оболочки глаза),
- состояние может быть тяжелым с летальностью до 30%.
У детей с врожденной цитомегалией возникает отставание в умственном развитии или возникают проблемы зрения и слуха.
У недоношенных младенцев приобретенная цитомегаловирусная инфекция дает симптоматику длительной пневмонии, из-за присоединения микробной инфекции. Может отмечаться замедление в физическом развитии, проявления гепатита, сыпи или увеличение лимфатических узлов.
Иногда у более старших детей ЦМВ-инфекция дает проявления, подобные мононуклеозу. Возникают проявления упорной простуды с болью в горле, длительной лихорадкой, ознобом и головными болями, болью в суставах и мышцах, увеличением лимфатических узлов и области слюнных желез. При этом могут быть высыпания на коже, похожие на краснуху. Иногда может возникать желтуха или изменение активности печеночных ферментов. Часто бывают осложнения с развитием пневмонии, но обычно она протекает нетяжело, иногда выявляясь только на рентгене.
Одни и те же симптомы могут быть признаками разных заболеваний, а болезнь может протекать не по учебнику. Не пытайтесь лечиться сами — посоветуйтесь с врачом.
Наличие вируса в крови не требует никакого лечения, так как в неактивном состоянии у здоровых людей он опасности не представляет.
Цитомегаловирусная инфекция у детей — это инфекционное заболевание, которое вызвано цитомегаловирусом и поражает слюнные железы, внутренние органы, ЦНС. В детстве патология чаще возникает при трансплацентарном или интранатальном заражении. Локализованные формы проявляются сиаладенитом, гепатитом, нефритом и т. д., распространенный вариант инфекции характеризуется поражением головного мозга, легких, почек и органов ЖКТ. Диагностика предполагает идентификацию возбудителя цитологическими, гистологическими, серологическими и молекулярно-биологическими методами. Лечение цитомегаловирусной болезни проводится специфическим иммуноглобулином и противовирусными препаратами.
МКБ-10
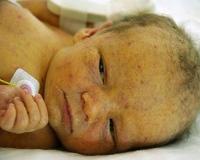
Общие сведения
Заражение цитомегаловирусной инфекцией (ЦМВИ) наблюдается у 20%‒60% всего детского населения, но в большинстве случаев оно протекает бессимптомно. Внутриутробное инфицирование вирусом от больной матери происходит в 30-50% случаев, при этом до 18% младенцев после рождения имеют клинические симптомы. Учитывая полиморфизм клинической картины, ранняя диагностика и лечение у детей затруднены. Цитомегаловирусная инфекция представляет серьезную опасность, особенно для плода и новорожденного, у которых заболевание, как правило, вызывает необратимые осложнения.

Причины
Болезнь вызвана герпесвирусом 5 типа — Cytomegalovirus hominis. Он имеет 6 штаммов: Davis, AD 169, Kerr, C-87, Esp, Towne, причем ребенок может быть инфицирован сразу несколькими подтипами возбудителя. Цитомегаловирус (ЦМВ) имеет ДНК-геном, отличается медленной репликацией и сравнительно низкой вирулентностью. Он термолабилен, уничтожается при температуре более 56°С, но длительно сохраняет жизнеспособность в комнатных условиях.
При врожденной ЦВМИ передача вируса к плоду происходит трансплацентарно, при перинатальной инфекции — путем контакта с вагинальными выделениями матери, грудным молоком или препаратами крови. Риск заражения увеличивается, если мать с острой формой болезни не получает специфическое лечение. В постнатальном периоде ребенок чаще всего заражается от ближайших родственников и сверстников воздушно-капельным или контактно-бытовым путем.
Патогенез
Попадая в кровь, вирус реплицируется в лейкоцитах, моноцитах и макрофагах и в дальнейшем он пожизненно сохраняется в лимфоцитарных органах. Зачастую процесс выражается в виде латентной инфекции, при которой у ребенка нет симптомов, и ему не требуется лечение. Активность цитомегаловируса зависит от состояния иммунитета: при физиологической иммунной недостаточности, которая наблюдается у детей раннего возраста, риск манифестной цитомегаловирусной инфекции возрастает в разы.
Классификация
В детской инфектологии различают врожденную (внутриутробную) и приобретенную формы патологии. По течению инфекция бывает острой (до 3 месяцев), подострой (3-6 месяцев), затяжной (6-12 месяцев) и хронической (более 1 года). По клиническим признакам выделяют локализованный (сиаладенит, нефрит, гепатит, энцефалит) и генерализованный вариант. С учетом тяжести течения цитомегаловирусную болезнь делят на 3 степени:
- Легкая. Отличается незначительными патоморфологическими изменениями во внутренних органах, которые не сказываются на их функциональной активности.
- Среднетяжелая. Проявляется выраженными органическими поражениями в сочетании с клиническими симптомами и расстройством функции некоторых внутренних органов.
- Тяжелая. Манифестирует тяжелыми органическими патологиями, резко выраженной интоксикацией и генерализованным характером поражения.
Симптомы
Врожденная ЦМВИ
У пациентов с манифестной врожденной форме цитомегаловирусной болезни признаки наблюдаются с первых дней жизни. Типичный комплекс симптомов у новорожденных детей включает недоношенность и/или низкую массу тела, поражение гепатобилиарной системы (увеличение печени, желтуха, гепатиты и циррозы), лимфаденопатии и геморрагическую сыпь на коже. Если инфицирование произошло на ранних сроках беременности, ребенок рождается с аномалиями — микроцефалией, гипоплазией легких, атрезией пищевода.
Приобретенная ЦМВИ
Приобретенная цитомегаловирусная болезнь обычно протекает в субклинической или латентной форме, когда у ребенка возникают гриппоподобные симптомы, субфебрильная температура без видимой причины. После заражения инфекция может длительное время себя не проявлять и давать обострения при снижении иммунного статуса, действии неблагоприятных эндо- или экзогенных факторов.
Течение манифестной приобретенной формы напоминает инфекционный мононуклеоз. У ребенка внезапно появляется слабость, повышается температура, беспокоят недомогание, головные боли, отсутствует аппетит. Позже присоединяются сильные боли в горле, увеличиваются подчелюстные и шейные лимфоузлы. Если цитомегаловирусная инфекция проявляется сиаладенитом, наблюдается резкое увеличение и болезненность слюнных желез на фоне фебрильной лихорадки.
Генерализованная ЦМВИ
При генерализованном варианте течения инфекции у детей поражается бронхолегочная система (пневмонии, дыхательная недостаточность), ЖКТ (энтероколит, мальабсорбция), печень (желтуха, цитомегаловирусный гепатит, билиарный цирроз). Особенно опасно вовлечение в процесс нервной системы, что проявляется судорожным синдромом, парезами и параличами, задержкой психомоторного развития.
Осложнения
Поражение клеток при цитомегаловирусной болезни создает благоприятные условия для возникновения аутоиммунных поражений — системной красной волчанки, рассеянного склероза, гломерулонефрита. Иногда после малосимптомной врожденной цитомегаловирусной инфекции осложнения наблюдаются в отдаленном периоде (в возрасте ребенка 2-5 лет). В основном они проявляются неврологическими расстройствами и поражением органов чувств.
Диагностика
Цитомегаловирусная инфекция отличается многообразием клинических признаков и часто протекает под маской других патологий, что затрудняет работу детского инфекциониста. На первичном приеме, помимо стандартного физикального осмотра, врач собирает детальный акушерский анамнез, чтобы выявить факторы риска антенатального инфицирования. Диагноз ЦМВИ правомочен только при лабораторном подтверждении, для чего используют следующие методы:
Инструментальные методы подбираются соответственно форме заболевания. Для оценки структурно-функциональных особенностей печени и билиарного тракта назначают УЗИ органов брюшной полости. КТ и МРТ головного мозга информативны для выявления врожденных пороков и кальцификатов. Рентгенография ОГК необходима при симптомах дыхательных расстройств. По показаниям ребенка направляют на консультации к профильным специалистам— кардиологу, неврологу, отоларингологу.
Лечение цитомегаловирусной инфекции у детей
Препаратом выбора у новорожденных и детей первого года жизни является специфический антицитомегаловирусный иммуноглобулин, который имеет повышенную концентрацию IgG. Лечение начинают при манифестных формах заболевания и проводят по схеме: вначале вводится высокая доза препарата, а спустя 9-10 дней дозировку постепенно уменьшают, контролируя степень ответа на терапию и активность процесса.
В старшем возрасте перечень препаратов, применяемых при цитомегаловирусной инфекции, значительно расширяется. Лечение включает противовирусные средства из группы нуклеозидов и нуклеотидов (ганцикловир, валганцикловир), производные ортофосфорной кислоты (фоскарнет). При легкой и среднетяжелой формах назначают интерфероны, иммуностимуляторы.
Для купирования интоксикации показано обильное питье (при легких формах), при среднетяжелых и тяжелых клинических вариантах рекомендована инфузионная терапия. Патогенетическая терапия подбирается в соответствии с характером течения болезни и может включать пищеварительные ферменты, ингибиторы протеиназ, гемостатики. Для предупреждения вторичных бактериальных осложнений используют антибиотики (макролиды, цефалоспорины, гликопептиды).
Прогноз и профилактика
При малосимптомных приобретенных вариантах цитомегаловирусная болезнь протекает без осложнений, зачастую у ребенка выявляется только латентное носительство. Угрозу для жизни и здоровья представляют тяжелые генерализованные инфекции, которые в 50-60% случаев сопровождаются осложнениями, несмотря на проводимое лечение. Особо опасно поражение цитомегаловирусом для детей с иммунодефицитными состояниями.
Основу профилактики врожденной ЦМВИ составляет обязательное лабораторное обследование женщин на носительство цитомегаловируса, которое проводится при планировании зачатия и во время беременности. Если в семье есть пациент с цитомегаловирусной инфекцией, необходимо ограничить его общение с ребенком и обеспечить лечение. Карантинно-изоляционные мероприятия в отношении заболевших и контактных лиц не производятся.
2. Клинические рекомендации (протокол лечения) оказания медицинской помощи детям больным цитомегаловирусной инфекцией. — 2015.
Цитомегалия – это инфекционное заболевание вирусного генеза, передающееся половым, трансплацентарным, бытовым, гемотрансфузионным путем. Симптоматически протекает в форме упорной простуды. Отмечается слабость, недомогание, головные и суставные боли, насморк, увеличение и воспаление слюнных желез, обильное слюноотделение. Часто протекает бессимптомно. Опасна цитомегалия беременных: она может вызывать самопроизвольный выкидыш, врожденные пороки развития, внутриутробную гибель плода, врожденную цитомегалию. Диагностика осуществляется лабораторными методами (ИФА, ПЦР). Лечение включает противовирусную и симптоматическую терапию.
МКБ-10
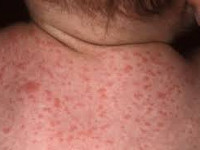
Общие сведения
Другие названия цитомегалии, встречающиеся в медицинских источниках, - цитомегаловирусная инфекция (ЦМВ), инклюзионная цитомегалия, вирусная болезнь слюнных желез, болезнь с включениями. Цитомегалия является широко распространенной инфекцией, и многие люди, являясь носителями цитомегаловируса, даже не подозревают об этом. Наличие антител к цитомегаловирусу выявляется у 10—15% населения в подростковом возрасте и у 50% взрослых людей. По некоторым источникам, носительство цитомегаловируса определяется у 80% женщин детородного периода. В первую очередь это относится к бессимптомному и малосимптомному течению цитомегаловирусной инфекции.

Причины
- воздушно-капельным: при чихании, кашле, разговоре, поцелуях и т.д.;
- половым путем: при сексуальных контактах через сперму, влагалищную и шеечную слизь;
- гемотрансфузионным: при переливании крови, лейкоцитарной массы, иногда - при пересадке органов и тканей;
- трансплацентарным: во время беременности от матери плоду.
Нередко цитомегаловирус находится в организме многие годы и может ни разу не проявить себя и не нанести вреда человеку. Проявление скрытой инфекции происходит, как правило, при ослаблении иммунитета. Угрожающую по своим последствиям опасность цитомегаловирус представляет у лиц со сниженным иммунитетом (ВИЧ-инфицированных, перенесших трансплантацию костного мозга или внутренних органов, принимающих иммунодепрессанты), при врожденной форме цитомегалии, у беременных.
Патогенез
Попадая в кровь, цитомегаловирус вызывает выраженную иммунную реакцию, проявляющуюся в выработке защитных белковых антител – иммуноглобулинов М и G (IgM и IgG) и противовирусной клеточной реакцией - образованием лимфоцитов CD 4 и CD 8. Угнетение клеточного иммунитета при ВИЧ-инфекции приводит к активному развитию цитомегаловируса и вызываемой им инфекции.
Даже при бессимптомном течении инфекции носитель цитомегаловируса является потенциально заразным для неинфицированных лиц. Исключение составляет внутриутробный путь передачи цитомегаловируса от беременной женщины плоду, который происходит в основном при активном течении процесса, и лишь в 5% случаев вызывает врожденную цитомегалию, в остальных же носит бессимптомный характер.
Симптомы цитомегалии
Врожденная цитомегалия
В 95% случаев внутриутробное инфицирование плода цитомегаловирусом не вызывает развития заболевания, а протекает бессимптомно. Врожденная цитомегаловирусная инфекция развивается у новорожденных, матери которых перенесли первичную цитомегалию. Врожденная цитомегалия может проявляться у новорожденных в различных формах:
- петехиальная сыпь – мелкие кожные кровоизлияния - встречается у 60-80% новорожденных;
- недоношенность и задержка внутриутробного развития плода - встречается у 30% новорожденных;
- желтуха;
- хориоретинит – острый воспалительный процесс в сетчатке глаза, часто вызывающий снижение и полную потерю зрения.
Летальность при внутриутробном инфицировании цитомегаловирусом достигает 20-30%. Из выживших детей большая часть имеет отставание в умственном развитии или инвалидность по слуху и зрению.
Приобретенная цитомегалия у новорожденных
При инфицировании цитомегаловирусом в процессе родов (при прохождении плода по родовым путям) или в послеродовом периоде (при бытовом контакте с инфицированной матерью или грудном вскармливании) в большинстве случаев развивается бессимптомное течение цитомегаловирусной инфекции. Однако у недоношенных младенцев цитомегаловирус может вызывать затяжную пневмонию, к которой часто присоединяется сопутствующая бактериальная инфекция. Часто при поражении цитомегаловирусом у детей отмечается замедление в физическом развитии, увеличение лимфоузлов, гепатит, сыпь.
Мононуклеозоподобный синдром
У лиц, вышедших из периода новорожденности и имеющих нормальный иммунитет, цитомегаловирус может вызывать развитие мононуклеозоподобного синдрома. Течение мононуклеазоподобного синдрома по клинике не отличается от инфекционного мононуклеоза, вызываемого другой разновидностью герпесвируса – вирусом Эбштейна-Барр. Течение мононуклеозоподобного синдрома напоминает упорную простудную инфекцию. При этом отмечается:
- длительная (до 1 месяца и более) лихорадка с высокой температурой тела и ознобами;
- ломота в суставах и мышцах, головная боль;
- выраженные слабость, недомогание, утомляемость;
- боли в горле;
- увеличение лимфоузлов и слюнных желез;
- кожные высыпания, напоминающие сыпь при краснухе (обычно встречается при лечении ампициллином).
В отдельных случаях мононуклеозоподобный синдром сопровождается развитием гепатита – желтухой и повышением в крови печеночных ферментов. Еще реже (до 6% случаев) осложнением мононуклеозоподобного синдрома служит пневмония. Однако у лиц с нормальной иммунной реактивностью она протекает без клинических проявлений, выявляясь лишь при проведении рентгенографии легких.
Длительность течения мононуклеозоподобного синдрома составляет от 9 до 60 дней. Затем обычно наступает полное выздоровление, хотя на протяжении нескольких месяцев могут сохраняться остаточные явления в виде недомогания, слабости, увеличенных лимфоузлов. В редких случаях активизация цитомегаловируса вызывает рецидивы инфекции с лихорадкой, потливостью, приливами и недомоганием.
Цитомегаловирусная инфекция у лиц с ослабленным иммунитетом
Ослабление иммунитета наблюдается у лиц, страдающих синдромом врожденного и приобретенного (СПИД) иммунодефицита, а также у пациентов, перенесших пересадку внутренних органов и тканей: сердца, легкого, почки, печени, костного мозга. После пересадки органов пациенты вынуждены постоянно принимать иммунодепрессанты, ведущие к выраженному подавлению иммунных реакций, что вызывает активность цитомегаловируса в организме.
У пациентов, перенесших трансплантацию органов, цитомегаловирус вызывает поражение донорских тканей и органов (гепатит – при пересадке печени, пневмонию при пересадке легкого и т. д.). После трансплантации костного мозга у 15-20% пациентов цитомегаловирус может привести к развитию пневмонии с высокой летальностью (84-88%). Наибольшую опасность представляет ситуация, когда инфицированный цитомегаловирусом донорский материал пересажен неинфицированному реципиенту.
Цитомегаловирус поражает практически всех ВИЧ-инфицированных. В начале заболевания отмечаются недомогание, суставные и мышечные боли, лихорадка, ночная потливость. В дальнейшем к этим признакам могут присоединяться поражения цитомегаловирусом легких (пневмония), печени (гепатит), мозга (энцефалит), сетчатки глаза (ретинит), язвенные поражения и желудочно-кишечные кровотечения.
У мужчин цитомегаловирусом могут поражаться яички, простата, у женщин – шейка матки, внутренний слой матки, влагалище, яичники. Осложнениями цитомегаловирусной инфекции у ВИЧ-инфицированных могут стать внутренние кровотечения из пораженных органов, потеря зрения. Множественное поражение органов цитомегаловирусом может привести к их дисфункции и гибели пациента.
Диагностика
С целью диагностики цитомегаловирусной инфекции проводится лабораторное обследование. Постановка диагноза цитомегаловирусной инфекции основана на выделении цитомегаловируса в клиническом материале или при четырехкратном повышении титра антител.
- ИФА-диагностика. Включает определение в крови специфических антител к цитомегаловирусу - иммуноглобулинов М и G. Наличие иммуноглобулинов М может свидетельствовать о первичном заражении цитомегаловирусом либо о реактивации хронической ЦМВИ. Определение высоких титров IgМ у беременных может угрожать инфицированию плода. Повышение IgМ выявляется в крови спустя 4-7 недель после заражения цитомегаловирусом и наблюдается на протяжении 16-20 недель. Повышение иммуноглобулинов G развивается в период затухания активности цитомегаловирусной инфекции. Их наличие в крови говорит о присутствии цитомегаловируса в организме, но не отражает активности инфекционного процесса.
- ПЦР-диагностика. Для определения ДНК цитомегаловируса в клетках крови и слизистых (в материалах соскобов из уретры и цервикального канала, в мокроте, слюне и т. д.) используется метод ПЦР-диагностики (полимеразной цепной реакции). Особенно информативно проведение количественной ПЦР, дающей представление об активности цитомегаловируса и вызываемого им инфекционного процесса.
В зависимости от того, какой орган поражен цитомегаловирусной инфекцией, пациент нуждается в консультации гинеколога, андролога, гастроэнтеролога или других специалистов. Дополнительно по показаниям проводится УЗИ органов брюшной полости, кольпоскопия, гастроскопия, МРТ головного мозга и другие обследования.
Лечение цитомегаловирусной инфекции
Неосложненные формы мононуклеазоподобного синдрома не требует специфической терапии. Обычно проводятся мероприятия, идентичные лечению обычного простудного заболевания. Для снятия симптомов интоксикации, вызываемой цитомегаловирусом, рекомендуется пить достаточное количество жидкости.
Лечение цитомегаловирусной инфекции у лиц, входящих в группу риска, проводится противовирусным препаратом ганцикловиром. В случаях тяжелого течения цитомегалии ганцикловир вводится внутривенно, т. к. таблетированные формы препарата обладают лишь профилактическим эффектом в отношении цитомегаловируса. Поскольку ганцикловир обладает выраженными побочными эффектами (вызывает угнетение кроветворения - анемию, нейтропению, тромбоцитопению, кожные реакции, желудочно-кишечные расстройства, повышение температуры и ознобы и др.), его применение ограничено у беременных, детей и у людей, страдающих почечной недостаточностью (только по жизненным показаниям), он не используется у пациентов без нарушения иммунитета.
Для лечения цитомегаловируса у ВИЧ-инфицированных наиболее эффективен препарат фоскарнет, также обладающий рядом побочных эффектов. Фоскарнет может вызывать нарушение электролитного обмена (снижение в плазме крови магния и калия), изъязвление половых органов, нарушение мочеиспускания, тошноту, поражение почек. Данные побочные реакции требуют осторожного применения и своевременной корректировки дозы препарата.
Прогноз
Особую опасность цитомегаловирус представляет при беременности, так как может провоцировать выкидыш, мертворождение или вызывать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с герпесом, токсоплазмозом и краснухой, относится к числу тех инфекций, обследоваться на которые женщины должны профилактически, еще на этапе планирования беременности.
Профилактика
Особенно остро вопрос профилактики цитомегаловирусной инфекции стоит у лиц, входящих в группу риска. Наиболее подвержены инфицированию цитомегаловирусом и развитию заболевания ВИЧ-инфицированные (особенно больные СПИДом), пациенты после трансплантации органов и лица с иммунодефицитом иного генеза.
Неспецифические методы профилактики (например, соблюдение личной гигиены) неэффективны в отношении цитомегаловируса, так как заражение им возможно даже воздушно-капельным путем. Специфическая профилактика цитомегаловирусной инфекции проводится ганцикловиром, ацикловиром, фоскарнетом среди пациентов, входящих в группы риска. Также для исключения возможности инфицирования цитомегаловирусом реципиентов при пересадке органов и тканей необходим тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
Особенности течения цитомегаловирусной инфекции урогенитального тракта у сексуально активных женщин
Журнал: Клиническая дерматология и венерология. 2013;11(3): 69‑75
Чернова Н.И. Особенности течения цитомегаловирусной инфекции урогенитального тракта у сексуально активных женщин. Клиническая дерматология и венерология. 2013;11(3):69‑75.
Chernova NI. Specific features of cytomegalovirus infection of the urogenital tract in sexually active women. Klinicheskaya Dermatologiya i Venerologiya. 2013;11(3):69‑75. (In Russ.).
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
Московский государственный медико-стоматологический университет им. А.И. Евдокимова
Цитомегаловирусная инфекция (ЦМВИ) — широко распространенное инфекционное заболевание человека, с вертикальным, половым, парентеральным, оральным путями передачи, реализующимися через кровь, цервикальный и вагинальный секреты, сперму и женское молоко. В большинстве случаев инфекция протекает без клинических проявлений. При иммуносупрессии, вызванной разными причинами, цитомегаловирус (ЦМВ) способен привести к развитию заболевания с многообразными симптомами, что обусловлено его способностью инфицировать практически все системы органов (ретинит, увеит, серонегативный мононуклеоз, пневмония, гепатит, болезни желудочно-кишечного тракта, центральной нервной системы, посттрансфузионный синдром) [1—5].
В среднем у 90—95% взрослого населения обнаруживаются антитела к ЦМВ. В литературе приводятся многочисленные данные об особенностях течения ЦМВИ у новорожденных, беременных и иммунонекомпетентных пациентов. В настоящий момент обследованию на ЦМВИ подлежат следующие категории граждан: женщины при подготовке к беременности, беременные и пациенты с выявленными иммунодефицитными состояниями. Изучению значимости ЦМВ в патологии взрослого населения уделяется особое внимание [6—9]. Однако не учитывается, что ЦМВ нередко способствует хроническому воспалительному поражению органов малого таза и гениталий, что обусловливает низкую эффективность терапии инфекций, передаваемых половым путем (ИППП), и снижение репродуктивной способности пациентов.
Цель настоящего исследования — определение форм течения ЦМВИ урогенитального тракта у сексуально активных женщин репродуктивного возраста.
Материал и методы
Под наблюдением находились 356 пациенток с ЦМВИ, которая характеризовалась наличием в крови анти-CMV IgG.
Для выявления достоверных триггерных клинических и лабораторных факторов, ассоциирующихся с ЦМВИ урогенитального тракта, данные опроса и обследования больных сравнивали с результатами аналогичных исследований, проведенных в контрольной группе, которая состояла из 120 женщин. Критериями отбора являлись: репродуктивный возраст, отсутствие беременности, лактации, системной и местной антибактериальной терапии в течение 1 месяца до начала данного обследования, нормальное состояние микрофлоры урогенитального тракта и исключенная ЦМВИ.
Результаты
Важное значение для выяснения характера ЦМВИ имеют сведения о перенесенных соматических и инфекционных заболеваниях. Частота экстрагенитальной патологии косвенно отражает состояние противоинфекционной защиты организма и иммунной системы в целом.

При анализе соматической патологии (табл. 2) наиболее часто в основной группе по сравнению с контрольной отмечались инфекционные вирусные заболевания (82,58% случаев), патология желудочно-кишечного тракта (55,9%) и заболевания органов дыхания (20,51%). У пациенток с ЦМВИ в 4,2 раза чаще отмечалась патология эндокринной системы (в 31,46% случаев; p<0,05).
Подробному анализу были подвергнуты данные о гинекологических заболеваниях, которые относятся к факторам, влияющим на состояние системного и локального иммунитета.

Среди перенесенных гинекологических заболеваний наиболее часто встречались патология шейки матки (44,10% случаев; p<0,05) и воспалительные заболевания органов малого таза (75%; p<0,05) по сравнению с контролем (табл. 3). Кроме того, у женщин с ЦМВИ чаще наблюдались ИППП (в 55,34% случаев; p<0,05) и бесплодие (28,65%; p<0,05).

При изучении особенностей сексуального анамнеза (табл. 4) выявлено, что у пациенток с ЦМВИ в 3 раза чаще (p<0,05) отмечалось раннее начало половой жизни. Соотношение женщин по количеству половых партнеров в обеих группах было сопоставимым. В ходе анализа особенностей сексуальных предпочтений установлено, что пациентки основной группы чаще практиковали аногенитальные контакты (p<0,05).
Незащищенные половые контакты (включая без использования презерватива с последующей обработкой раствором мирамистина) в анамнезе имели более 84% пациенток с ЦМВ и 70% женщин из группы контроля (p<0,05).
Таким образом, вероятным предрасполагающим фактором для ЦМВИ урогенитального тракта являлось раннее начало половой жизни и большое количество незащищенных аногенитальных контактов.
При клиническом обследовании анализировали особенности субъективных ощущений, проводили тщательный общий и гинекологический осмотр.
Таким образом, у пациенток с ЦМВИ при гинекологическом осмотре чаще выявлялся острый или хронический воспалительный процесс в малом тазу.

Результаты микроскопического исследования мазков отделяемого генитального тракта, окрашенных по Граму, представлены в табл. 6.

Анализ результатов культурального исследования отделяемого мочеполового тракта женщин выявил доминирование грибов Candida spp. (48,60%), G. vaginalis (30,62%), T. vaginalis (21,35%). У большинства женщин в биотопах влагалища имела место ассоциация ЦМВИ с условно-патогенными бактериями (Streptococcus, St. aureus, Ureaplasma spp., M. hominis) в высоком титре (более 10 5 КОЕ/мл; табл. 7).

Результаты комплексного обследования этих женщин представлены в табл. 8.
У 71 (19,9%) женщины состояние вагинальной микроэкологии было оценено как нормоценоз. Проанализировав полученные данные, можно было выделить его некоторые особенности, которые в ряде случаев позволили назвать указанное состояние нормоценозом только условно. Так, только у 22 (6,18%) женщин из 356 состояние микроэкологии полностью соответствовало всем критериям нормы репродуктивного возраста: при микроскопии вагинального отделяемого отсутствовала выраженная лейкоцитарная реакция (количество лейкоцитов не превышало 10 в поле зрения), эпителий был представлен клетками поверхностного и промежуточного слоев, количество микрофлоры было умеренным при абсолютном преобладании морфотипа лактобактерий. Морфотипы условно-патогенных микроорганизмов (УПМ) не определялись. При культуральном исследовании титр лактобацилл составлял 10 6-8 КОЕ/мл вагинального отделяемого, а концентрации УПМ были низкими (менее 10 3 КОЕ/мл).
Наиболее частой патологией среди 356 обследованных пациенток с ЦМВИ оказался кандидоз (57,30%), в большинстве случаев сопровождавшийся умеренным повышением титра УПМ (Streptococcus группы В в 10 6 КОЕ/мл и St. aureus более 10 6 КОЕ/мл).
Аэробный вагинит (1,12%) как вариант дисбиоза влагалища был обусловлен колонизацией вагинального биотопа высокими титрами E. coli (более 10 7 КОЕ/мл) и стрептококков группы В (10 6 КОЕ/мл). По данным микроскопии в этих случаях также отмечалась выраженная лейкоцитарная реакция (более 40 лейкоцитов в поле зрения).
У 21,06% женщин микроскопически был установлен бактериальный вагиноз, что сопровождалось высокой колонизацией факультативно-анаэробной и анаэробной флоры (более 10 6 КОЕ/мл).
В 0,56% случаев состояние вагинальной микроэкологии было оценено как другой вариант дисбиоза влагалища, когда при минимальном содержании микрофлоры (данные микроскопии) доминировали факультативно-анаэробные и аэробные УПМ (грамположительные кокки), а лактоморфотипы были единичными в поле зрения.
Таким образом, только у 19,9% пациенток с ЦМВИ имелся классический вариант микроценоза, в остальных случаях микрофлора влагалища претерпевала изменения, связанные с нарастанием титра факультативно-анаэробных УПМ. У 80,1% женщин выявлены нарушения микроценоза влагалища, в большинстве случаев связанные с увеличением количества Candida spp. При исследовании отделяемого из уретры с помощью ПЦР идентифицированы возбудители ИППП и УПМ. Наиболее часто выявлялись ДНК HPV (11,52%), T. vaginalis, M. hominis, HSV 1-го и 2-го типов (2,81 и 3,08% соответственно), С. trachomatis были идентифицированы в уретре у 5,34% больных.
В цервикальном канале в 5 раз чаще определялись УПМ и патогены. Так, наиболее часто у женщин с ЦМВИ были выделены вирус папилломы человека (42,13%), T. vaginalis (11,52%), M. hominis (21,63%), С. trachomatis (18,82%) и Ureaplasma spp. (24,44%).
В соскобах из влагалища также наиболее часто определялась ДНК вируса папилломы человека (43,25%), T. vaginalis (21,35%), M. hominis (14,89%), Ureaplasma spp. (19,38%), а также G. vaginalis (25%).
При исследовании проб из прямой кишки были идентифицированы ДНК ВПЧ (28,93%) и M. hominis (11,24%).

Для верификации диагноза ЦМВИ проводили расширенный анализ результатов, полученных разными методами исследования (табл. 9).
При анализе данных с целью выявления маркеров ЦМВИ установлена наибольшая частота обнаружения анти-CMV IgG — 356 (100%) случаев. Анти-CMV IgM были выявлены у 89 (25%) женщин. Обнаружение антител класса G к CMV свидетельствовало как об инфицированности, так и о наличии в большинстве случаев сформированного специфического противовирусного иммунитета. Выявление антител класса М совместно с IgG было одним из признаков реактивации данной вирусной инфекции.
При исследовании материала, полученного из урогенитального тракта с помощью ПЦР, ДНК CMV была обнаружена у 208 (58,43%) женщин.
ЦМВ на культуре фибробластов легких человека при исследовании крови выявлен у 93 (26,12%) женщин, мочи — у 199 (55,90%), слюны — у 204 (57,30%) больных, влагалищного отделяемого — у 225 (63,20%), из цервикального канала — в 268 (75,28%) случаях. В целом ЦМВ был обнаружен у 268 (75,28%) пациенток.
Учитывая этиологию, патогенез и клинические проявления ЦМВИ урогенитального тракта, пациенткам с реактивированной и латентной формой ЦМВИ проводилась комплексная терапия инфекционного процесса в соответствии с клиническими рекомендациями по ведению больных с ИППП. Противовирусное лечение включало использование препарата Панавир. Основное действующее вещество данного препарата — гексозный гликозид, полученный методом ферментативного гидролиза с последующей газожидкостной хроматографией, состоящий из глюкозы, рамнозы, арабинозы, маннозы, ксилозы, галактозы, уроновых кислот. В ряде экспериментальных и клинических исследований установлена противовирусная и иммуномодулирующая активность Панавира. Данный препарат повышает неспецифическую резистентность организма к разным инфекциям и способствует индукции интерферона, Панавир (5 мл 0,004% раствора) применялся парентерально (внутривенно струйно) 1 раз в сутки через 48 ч (3 инъекции в 1-ю неделю лечения), затем — через 72 ч (2 инъекции во 2-ю неделю терапии). Всего на курс пришлось 5 инъекций в течение 2 недель.
При контрольном исследовании, проведенном через 14 дней после лечения, лишь у 2 (8,0%) пациенток с латентной формой ЦМВИ выявлен CMV в культуре клеток отделяемого цервикального канала, ДНК CMV не определялась у 24 (96%) больных. В результате лечения при реактивированной форме ЦМВИ была констатирована негативация IgM анти-CMV в крови у 100% женщин. При исследовании CMV на культуре фибробластов эмбрионов человека вирурия установлена у 1 (5,56%) пациентки, выделение из цервикального канала отмечено у 3 (16,67%). Результаты вирусологического обследования крови, слюны, влагалищных выделений были отрицательными у всех женщин. При проведении ПЦР наличие ДНК CMV выявлено у 2 (11,11%) пациенток, получавших парентерально Панавир.
Таким образом, в ходе исследования определены основные диагностические клинико-лабораторные критерии разных форм ЦМВИ урогенитального тракта сексуально активных женщин репродуктивного возраста, на основании которых возможности определения данной инфекции существенно увеличились. Наличие клинических проявлений при реактивированной ЦМВИ и определение вирусов при подостром или хроническом течении воспалительных заболеваний органов малого таза способствовали определению значимости данной инфекции в развитии патологии гениталий. Применение препарата Панавир в комплексной терапии повышало эффективность лечения в 89,5% случаев, что позволяет рекомендовать препарат Панавир для комплексной терапии ЦМВИ.
Читайте также:

