Цитомегаловирус в желчном пузыре
Обновлено: 26.04.2024
Цитомегаловирусная инфекция – инфекционное заболевание, обусловленное высокораспространенным вирусом герпеса 5-го типа, характеризующаяся политропностью поражений органов и систем, сложными иммунологическими реакциями со стороны макроорганизма, с формиров
Резюме. Цитомегаловирусная инфекция – инфекционное заболевание, обусловленное высокораспространенным вирусом герпеса 5-го типа, характеризующаяся политропностью поражений органов и систем, сложными иммунологическими реакциями со стороны макроорганизма, с формированием длительной, нередко пожизненной персистенции вируса в организме. В настоящее время отмечается рост заболеваемости цитомегаловирусной инфекцией во всех странах мира. Согласно эпидемиологическим данным, большинство людей в течение своей жизни инфицируются цитомегаловирусом. Так, в Европе и США серопозитивны по цитомегаловирусу 40-60% взрослого населения, в развивающихся странах распространенность цитомегаловирусой инфекции еще более высока – 80% детей и почти все взрослое население. Среди беременных специфические антитела к цитомегаловирусу определяются от 40% в развитых до 100% в развивающихся странах. Частота внутриутробной передачи цитомегаловируса колеблется в пределах 0,2-2,2%, в среднем составляя 1% в популяции. Многообразие клинических форм, от субклинического течения до развития тяжелых жизнеугрожающих форм у особых, иммунокомпроментированных групп пациентов, делает цитомегаловирусную инфекцию сложной и актуальной проблемой современной медицины. Одним из основных органов-мишеней для цитомегаловируса является гепатобилиарная система. Малое число наблюдений, ограниченные данные о патогенезе развития поражения печени при цитомегаловирусной инфекции у детей, а также отсутствие единых регламентирующих документов по диагностике и лечению указанных состояний в педиатрической практике послужили причиной для написания данной статьи. В работе приведены актуальные данные о патогенезе, клинической картине, диагностике, а также подходах к терапии цитомегаловирусного гепатита у детей.
Цитомегаловирусная инфекция (ЦМВИ) – инфекционное заболевание, вызванное герпесвирусом 5-го типа (Cytomegalovirus). Характеризуется полиморфной клинической симптоматикой и специфичной морфологической картиной с присутствием цитомегалических клеток на фоне лимфогистиоцитарных инфильтратов. В настоящее время ЦМВИ является одной из наиболее актуальных вирусных проблем инфекционной патологии, что обусловлено ее широким распространением, многообразием путей передачи, чрезвычайно большим спектром клинических проявлений, а также частым развитием тяжелых форм инфекции в определенных группах пациентов. Европейским регионарным бюро Всемирной организации здравоохранения (ВОЗ) ЦМВИ отнесена к числу болезней, которые определяют будущее инфекционной патологии. Многие эксперты считают необходимым принципиально изменить отношение к цитомегаловирусу (ЦМВ) и усилить борьбу с его распространением [2, 3].
Общие сведения
У людей с эффективным иммунитетом ЦМВИ в большинстве случаев характеризуется латентным течением. Клиническая манифестация заболевания с возможным развитием крайне тяжелых форм происходит относительно редко и зачастую у пациентов с приобретенными или врожденными иммунодефицитными состояниями (ИДС) [4]. В настоящее время, учитывая развитие биомедицинских технологий, в частности разработку и широкое использование цитостатических препаратов, а также высокоактивной биологической терапии, перманентный рост заболеваемости ВИЧ-инфекцией, рост онкопатологии и числа тяжелых аутоиммунных патологий, актуальность ЦМВИ не вызывает сомнений. Это одна из наиболее частых причин самопроизвольных выкидышей, преждевременных родов, врожденных пороков развития и фетопатий [4, 5].
Сегодня отмечается рост заболеваемости ЦМВИ во всех странах мира, что связано как с улучшением качества диагностики, так и с указанными выше причинами [5]. Согласно эпидемиологическим данным, большинство людей в течение жизни инфицируются ЦМВ. Так, в Европе и США 40-60% взрослого населения серопозитивны по ЦМВ, в развивающихся странах распространенность ЦМВИ еще выше – 80% детей и почти все взрослое население. Среди беременных специфические антитела к ЦМВ определяются от 40% в развитых до 100% в развивающихся странах. Частота внутриутробной передачи ЦМВ колеблется в пределах 0,2-2,2%, в среднем составляя 1% в популяции [2].
Учитывая, что ЦМВ характеризуется политропностью, клиническая картина может включать различные синдромы, однако одним из наиболее частых проявлений является синдром поражения печени. Наиболее распространенным заболеванием печени, связанным с ЦМВ, является острый гепатит, тяжесть которого варьирует от бессимптомного повышения аланиновой аминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ), а также самоограничивающегося гепатита до тяжелого поражения печени с развитием острой печеночной недостаточности (ОПчН). Кроме того, могут наблюдаться и нетипичные проявления, такие как холестатические формы острого гепатита, развитие хронического гепатита, а также вероятный дебют аутоиммунного гепатита [6, 7].
В зависимости от времени инфицирования ЦМВ выделяют врожденный и приобретенный гепатит. Поражение печени – характерный признак врожденной ЦМВ-инфекции – встречается у 40-63,3% больных [8, 9]. Врожденный ЦМВ-гепатит (ЦМВГ) всегда развивается как первично-хронический процесс. Поражение печени часто сочетается с другими пороками развития: атрезией желчевыводящих путей, поражением нервной системы, легких, почек и др. [10, 11]. В этиологической структуре неонатальных гепатитов ЦМВ-этиология составляет до 40% [12]. К концу первого года жизни поражение печени при врожденной ЦМВИ отмечается редко – примерно в 2% случаев [13]. Приобретенный ЦМВГ может протекать в форме острой инфекции в рамках мононуклеозоподобного синдрома, а также как самостоятельное заболевание, заканчиваясь выздоровлением с полным восстановлением функционального состояния печени или первично-хроническим процессом 13.
Эпидемиология
Патогенез
ЦМВИ может протекать в виде первичной инфекции у ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни. При острой ЦМВИ могут поражаться практически все типы клеток человеческого организма – эндотелиальные, эпителиальные, гладкомышечные, фибробласты, нейроны, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и многие другие, то есть вирус не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения у различных групп пациентов [18].
Патогенез ЦМВГ до настоящего времени не до конца ясен. Традиционно считается, что ЦМВ поражает желчные протоки с развитием холестатического гепатита. Однако обнаружено, что вирус оказывает и прямое цитопатическое действие непосредственно на паренхиму печени, таким образом, ЦМВ является прямым гепатотропным агентом.
В формировании изолированного поражения гепатоцитов при ЦМВГ важную роль может играть непосредственное попадание возбудителя в кровь (парентеральный механизм инфицирования). Возбудитель сразу оказывается в системном кровотоке, откуда и попадает в паренхиму печени, где оказывает цитопатическое действие на клетки печени.
Образующиеся по ходу инфекции специфические антитела соединяются с вирусными антигенами и формируют иммунные комплексы, вовлекающие в патологический процесс другие органы и системы [21, 22].
Особое свойство ЦМВИ – способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [23]. Указанные изменения в иммунной системе приводят к формированию неэффективного иммунного ответа, что ухудшает течение основного патологического процесса, приводит к формированию предрасположенности к развитию вторичных вирусных и бактериальных инфекций.
Подходы к диагностике
Диагноз ЦМВГ устанавливают после тщательного анализа клинико-анамнестических данных, лабораторных и инструментальных методов обследования.
Ведущими методами этиологической диагностики являются определение антител (anti-CMV IgM, anti-CMV IgG + IEA IgG с определением авидности), а также качественная и количественная полимеразная цепная реакиця (ПЦР) для определения ДНК вируса в крови, слюне и моче и некоторых других средах [24].
Первым в сыворотке крови появляется IgM, сохраняющийся в среднем около 4 недель. В последующем возможно выявление IgG, для которых обязательно определение авидности. Данный показатель указывает на давность течения инфекционного процесса. Стоит отметить, что серодиагностика позволяет установить диагноз не во всех случаях [16]. При использовании серологических методик для диагностики острых ЦМВГ возможна перекрестная реакция с вирусом Эпштейна–Барр и гепатита Е [24].
У новорожденных серологические исследования редко информативны, особенно при манифестной клинике, так как врожденная иммунная система ко времени требуемого серологического ответа еще не эффективна. Отсутствие специфических фетальных IgM даже на фоне острой тяжелой ЦМВИ (серологическая ниша) – общая черта этого онтогенетического периода. Указанные маркеры начинают продуцироваться только через несколько месяцев [25].
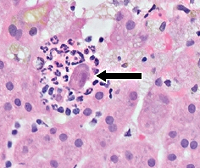
Если лабораторная диагностика не дала результата, методом выбора, как и при любом неуточненном гепатите, является биопсия печени. Гистологически ЦМВГ характеризуется классическим цитопатическим действием вируса на гепатоциты, эпителий билиарного тракта, эндотелиальные клетки и клетки Купфера. Инфицированные клетки имеют как цитоплазматическое, так и ядерное увеличение с цитоплазматическими и внутриядерными включениями. Другие неспецифические изменения предполагают умеренный лобулярный гепатит, гепатоцеллюлярный некроз, портальную мононуклеарную инфильтрацию и микроабсцессы [26]. Также в некоторых случаях возможно использование иммуногистохимического исследования. Следует отметить, что биопсия печени, как перкутанная, так и трансъюгулярная, на настоящем этапе считается малоинвазивной процедурой и не несет высоких рисков, что позволяет считать ее решающим методом обследования, особенно при неуточненных поражениях печени.
Подходы к лечению
Учитывая, что в основе патогенеза ЦМВГ лежит прямое вирусное поражение, ведущее значение принадлежит этиотропной терапии. Несмотря на токсичность противовирусных анти-ЦМВ-препаратов при развитии у ребенка угрожающей жизни манифестной ЦМВИ, в частности острого ЦМВГ, применение ганцикловира и валганцикловира показано и необходимо после обязательного предварительного анализа риска и пользы. Ганцикловир впервые применен у новорожденных в конце 1980-х гг., в последующем было многократно показано, что он хорошо переносится в том числе и детьми, а также эффективен при лечении манифестных форм ЦМВИ. Препарат назначают в дозе 5-6 мг/кг два раза в сутки в среднем в течение 6 недель. Стоит отметить, что препарат обладает выраженными токсическими свойствами, поэтому применяется при наличии строгих показаний. Ограничения применения ганцикловира также связаны с необходимостью реализации для его инфузии венозного доступа с массивным кровотоком, у детей зачастую – центрального венозного катетера.
Альтернативой к инвазивному использованию ганцикловира стало введение валганцикловира, рандомизированное исследование эффективности которого завершено в 2015 г. Препарат обладает менее выраженными токсическими свойствами. Согласно международному Консенсусу 2017 г., лечение валганцикловиром показано детям со среднетяжелой врожденной ЦМВИ – 16 мг/кг 2 раза в сутки до 6 месяцев.
С патогенетической точки зрения важна гепатопротективная терапия. Наиболее доказанным в этом отношении препаратом является урсодезоксихолевая кислота, которая назначается в дозе 10 мг/кг 1 раз в сутки, курс зависит от динамики холестатического и цитолитического синдрома, а также от течения основного заболевания в целом.
Учитывая иммунные нарушения, реализующиеся при ЦМВИ и проявляющиеся депрессией различных звеньев иммунитета, а особенно интерферонопродукции, рационально применение иммуномодулирующей терапии препаратами интерферона альфа-2 бета.
При реализации тяжелых форм ЦМВГ с развитием ОПчНв терапии рационально применять стероиды (2 мг/кг по преднизолону) для купирования мезенхимально-воспалительного синдрома в паренхиме печени. При развитии печеночной энцефалопатии показаны препараты лактулозы. При отсутствии эффекта от проводимой терапии, прогрессировании ОПчН, а также при формировании хронического гепатита с признаками развития цирроза печени показано проведение трансплантации органа при соответствии характеристик кандидата на трансплантацию. В свою очередь при лечении легких или бессимптомных форм ЦМВГ используется симптоматическая терапия [16, 28].
Заключение
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
Сведения об авторах:
Information about the authors:
Цитомегаловирусный гепатит у детей: современное состояние проблемы/ Г. С. Карпович, А. Е. Шестаков, М. А. Михайленко, Ю. С. Серова
Для цитирования: Карпович Г. С., Шестаков А. Е., Михайленко М. А., Серова Ю. С. Цитомегаловирусный гепатит у детей: современное состояние проблемы // Лечащий Врач. 2022; 1 (25): 25-29. DOI: 10.51793/OS.2022.25.1.004
Теги: дети, инфекция, гепатобилиарная система, гепатит
Цитомегаловирусный гепатит — это воспалительное поражение печеночной паренхимы и внутрипеченочных желчных путей, вызванное цитомегаловирусами. Обычно проявляется болью справа в подреберье, желтушностью, потемнением мочи, диспепсией, интоксикацией. Может протекать в безжелтушном варианте. Диагностируется с помощью ИФА, РИФ, РСК, УЗИ печени, фиброэластометрии, цитоморфологического анализа печеночного биоптата и биохимического исследования крови. Для лечения применяют рекомбинантные интерфероны, нуклеотиды и нуклеозиды, иммуноглобулины, холеретики, гепатопротекторы, иммуномодуляторы.
МКБ-10
Общие сведения
Гепатит — одна из локализованных форм цитомегаловирусной инфекции, при которой репликация вирионов происходит преимущественно в печеночной ткани. Устойчивость цитомегаловируса (ЦМВ) при комнатной температуре в сочетании с восприимчивостью к патогену обусловили высокую распространенность инфекции в популяции.
По данным исследований в сфере клинической гастроэнтерологии и инфекционных болезней, носителями вируса являются 40-95% взрослых и 20-60% детей, у которых при снижении иммунитета может возникнуть поражение печени. Особо опасно развитие цитомегаловирусного гепатита для новорожденных, заразившихся внутриутробно – летальность в таких случаях достигает 10%.

Причины
Возбудитель заболевания — ДНК-содержащий вирус цитомегаловирусной инфекции. Патоген принадлежит к семейству герпес-вирусов, отличается крупными размерами нуклеокапсидов генома, может реплицироваться, не повреждая пораженную клетку, присутствует во всех биологических жидкостях носителя или больного (крови, слюне, вагинальном секрете и др.). Персистенция вирионов в организме сопровождается резким угнетением клеточного иммунитета. Активацию возбудителя и манифестацию цитомегаловирусного гепатита провоцируют иммунодефицитные состояния:
- ВИЧ-инфекция. Поражение печени обычно наблюдается в фазе IIIB (СПИД) на фоне стойкого снижения количества Т-хелперов. Гепатит часто сочетается с цитомегаловирусным ретинитом, эрозивно-язвенным колитом, гастритом, повреждениями ЦНС и других органов.
- Прием иммуносупрессивных препаратов. Предпосылкой к развитию гепатита является длительный прием кортикостероидов, цитостатиков, других медикаментов, угнетающих иммунитет. В группу риска входят пациенты с онкопатологией и перенесшие трансплантацию органов.
- Беременность. Реактивации латентного вируса способствует естественное снижение иммунитета у беременных, предотвращающее отторжение генетически чужеродного плода. Иногда наблюдается повторное заражение женщины другими штаммами возбудителя.
- Период новорожденности. В 30-50% случаев инфицирование ребенка происходит внутриутробно, в родах или послеродовом периоде. При недостаточности иммунитета возможно проявление цитомегаловирусного процесса в форме острого либо хронического гепатита.
Патогенез
С учетом присутствия вируса во всех жидких средах и секретах заражение происходит разными путями — фекально-оральным, аэрогенным, контактным, вертикальным (трансплацентарным, при прохождении по родовым путям, грудном вскармливании), парентеральным (при переливании крови и пересадке органов). Обычно после попадания в организм возбудитель цитомегаловирусной инфекции быстро оказывается в крови, проникает в лейкоциты и мононуклеары, где реплицируется и длительное время персистирует. Зараженные клетки изменяются, но не погибают, оставаясь резервуаром вируса.
При реактивации на фоне иммунодефицита патоген распространяется по организму, проявляя высокую эпителиотропность. Внедрение вируса в эпителий желчных протоков, гепатоциты и сосудистый эндотелий вызывает цитомегалическую трансформацию клеток и образование мононуклеарных инфильтратов. В результате возникает внутрипеченочный холестаз, усугубляемый закупоркой желчных протоков слущенными пораженными клетками. Инфицированные гепатоциты при цитомегаловирусном гепатите подвергаются деструкции вплоть до цитолиза, что сопровождается процессами фиброза и склероза.
Классификация
При систематизации клинических форм заболевания учитывают особенности течения, тяжесть симптоматики и время инфицирования. Такой подход является оптимальным для выбора терапевтической тактики и прогнозирования вероятного исхода цитомегаловирусного гепатита. При выделении легкого, умеренного и редко встречающегося тяжелого вариантов патологии основываются на выраженности клинических симптомов и степени морфологических изменений. Критериями классификации являются:
- Динамика развития гепатита. Различают острое и хроническое поражение печени. Для острого гепатита цитомегаловирусного генеза характерна манифестация интоксикационным синдромом с быстрым развитием гепатомегалии, желтушности и боли, выраженными изменениями лабораторных показателей. Хронические варианты могут быть первичными или исходом острых, преобладают фиброзно-цирротические изменения.
- Время инфицирования. ЦМВ-гепатиты бывают врожденными и приобретенными. Значительное число случаев болезни у детей вызвано внутриутробным инфицированием. Практически у 100% больных врожденная патология представлена первично-хроническим процессом с риском исхода в цирроз печени. До 59% случаев приобретенных форм гепатита протекает в виде остро манифестировавшей инфекции с высокой вероятностью полного обратного развития.
Симптомы цитомегаловирусного гепатита
Безжелтушная хроническая форма цитомегаловирусного гепатита обнаруживается значительно реже, характеризуется медленным прогрессированием и скудной клинической картиной. На первый план выступают общие неспецифические симптомы поражения печени: периодический дискомфорт в эпигастральной области и правом подреберье, быстрая утомляемость, астенические состояния. У всех пациентов наблюдаются диспепсические расстройства — тошнота, горечь во рту, снижение аппетита.
Осложнения
Изолированное течение цитомегаловирусного гепатита встречается редко. Обычно он сочетается с поражениями других органов и систем. У больных со сниженной иммунной реактивностью вирус вызывает генерализованную инфекцию, которая характеризуется вялотекущей атипичной пневмонией, тотальным поражением ЖКТ, преобладанием в крови атипичных мононуклеаров. Инфекционный агент нередко поражает зрительный анализатор с развитием хориоретинитов, может проникать в головной мозг и вызывать подострый энцефалит.
Частым осложнением цитомегаловирусного типа гепатита является развитие облитерирующего холангита вследствие закупорки желчных протоков некротическими массами. В дальнейшем холангит может приводить к билиарному циррозу печени — опасному заболеванию с плохим прогнозом. Снижение дезинтоксикационной функции гепатоцитов и накопление в крови азотистых соединений потенцирует формирование печеночной энцефалопатии, проявляющейся нарушениями сознания, очаговой неврологической симптоматикой и типичными изменениями на ЭЭГ.
Диагностика
Верификация диагноза цитомегаловирусного гепатита представляет затруднения, поскольку зачастую трудно доказать связь между серологическими признаками вирусной инфекции и поражением печени. Диагностический поиск предусматривает комплексное лабораторно-инструментальное обследование пациента с целью исключения других этиологических факторов. Наиболее информативны:
В общем анализе крови в острой фазе гепатита определяется лейкоцитоз, большое количество мононуклеаров, при длительном течении заболевания наблюдается снижение уровня тромбоцитов. В биохимическом анализе крови выявляются маркеры цитолиза: повышение трансаминаз, преобладание АСТ над АЛТ, признаки холестаза (возрастание уровней щелочной фосфатазы и холестерина).
Дифференциальная диагностика
В первую очередь дифференциальную диагностику проводят между цитомегаловирусным поражением печени и типичными вирусными гепатитами типа В, С. Решающими в постановке диагноза становятся результаты серологических реакций (выявление антител к ЦМВ) и наличие патогномоничных признаков при микроскопическом исследовании образцов печеночной паренхимы. Также необходимо дифференцировать заболевание с токсическими гепатитами. Обследованием и лечением пациента занимаются гастроэнтеролог или гепатолог, инфекционист.
Лечение цитомегаловирусного гепатита
Выбор терапевтической тактики определяется возрастом пациента, клинической формой и тяжестью течения заболевания, наличием признаков генерализации инфекции. Новорожденным и пациентам с признаками острого печеночного воспаления показана срочная госпитализация для предотвращения угрожающих жизни осложнений. При легком течении рекомендован покой, диета с низким содержанием жиров, экстрактивных веществ и специй, исключением алкоголя. Проводится терапия, направленная на улучшение реологических свойств желчи и защиту гепатоцитов.
Больным с холестазом назначают препараты урсодезоксихолевой и дезоксихолевой кислот, которые снижают литогенность и вязкость желчи, оказывают иммуномодулирующее действие. Лечение цитомегаловирусного поражения печени дополняют растительными гепатопротекторами, стабилизирующими мембраны гепатоцитов, препятствующими разрушению клеточных структур и ускоряющими регенерационные процессы. Базовыми противовирусными средствами для терапии умеренно выраженных, тяжелых и хронических форм гепатита, вызванного цитомегаловирусами, являются:
- Рекомбинантные интерфероны. Терапевтический эффект медикаментов основан на угнетении репликации вирусной ДНК, усилении фагоцитоза, повышении специфической цитотоксичности Т-киллеров. Производные интерферона альфа-2b позволяют достичь стойкой ремиссии более чем у 80% пациентов с хроническим течением гепатита.
- Нуклеозиды и нуклеотиды. Являются препаратами выбора при тяжелом гепатите и его сочетании с иммунодефицитными состояниями. Средства этой группы не обеспечивают элиминацию вирусных частиц, но замедляют их репликацию. В качестве альтернативы могут применяться производные ортофосфорной кислоты.
- Иммунотерапия. Противоцитомегаловирусный гипериммунный человеческий иммуноглобулин содержит вирус-нейтрализирующие антитела (IgG). Кроме непосредственного воздействия на вирионы иммуноглобулины оказывают иммуностимулирующее действие и повышают неспецифическую резистентность организма.
Этиопатогенетическая терапия сочетается с симптоматическим лечением. По показаниям проводятся инфузии различных растворов для восстановления кислотно-основного и водно-электролитного баланса. При гипертермии, выраженной миалгии с осторожностью используются нестероидные противовоспалительные средства. Возможно назначение иммуностимуляторов (тимусных полипептидов, производных имидазотиазола). После выздоровления необходимо диспансерное наблюдение с контрольными обследованиями у гастроэнтеролога через 3, 6, 12 месяцев.
Прогноз и профилактика
Исход цитомегаловирусного гепатита зависит от степени распространенности процесса и своевременности диагностики. В большинстве случаев прогноз заболевания относительно неблагоприятный вследствие недостаточной эффективности существующих противовирусных медикаментозных средств. Для профилактики ЦМВ-гепатита нужно соблюдать правила личной гигиены, людям из группы риска (беременные, лица с иммунодефицитом) желательно избегать контактов с маленькими детьми.
1. О роли цитомегаловирусной инфекции при вирусных гепатитах. / Яковлев А.А., Власов Н.Н. и др.// Вирусные гепатиты и другие активные инфекции. Сборник научных трудов – 1997.
3. Роль герпесвирусов в этиологии хронических гепатитов / Коломиец А.Г., Ключарева А.А. и др.// Здравоохранение: Орган МЗ Республики Беларусь - 1998 - №9.
Цитомегалия – это инфекционное заболевание вирусного генеза, передающееся половым, трансплацентарным, бытовым, гемотрансфузионным путем. Симптоматически протекает в форме упорной простуды. Отмечается слабость, недомогание, головные и суставные боли, насморк, увеличение и воспаление слюнных желез, обильное слюноотделение. Часто протекает бессимптомно. Опасна цитомегалия беременных: она может вызывать самопроизвольный выкидыш, врожденные пороки развития, внутриутробную гибель плода, врожденную цитомегалию. Диагностика осуществляется лабораторными методами (ИФА, ПЦР). Лечение включает противовирусную и симптоматическую терапию.
МКБ-10
Общие сведения
Другие названия цитомегалии, встречающиеся в медицинских источниках, - цитомегаловирусная инфекция (ЦМВ), инклюзионная цитомегалия, вирусная болезнь слюнных желез, болезнь с включениями. Цитомегалия является широко распространенной инфекцией, и многие люди, являясь носителями цитомегаловируса, даже не подозревают об этом. Наличие антител к цитомегаловирусу выявляется у 10—15% населения в подростковом возрасте и у 50% взрослых людей. По некоторым источникам, носительство цитомегаловируса определяется у 80% женщин детородного периода. В первую очередь это относится к бессимптомному и малосимптомному течению цитомегаловирусной инфекции.

Причины
- воздушно-капельным: при чихании, кашле, разговоре, поцелуях и т.д.;
- половым путем: при сексуальных контактах через сперму, влагалищную и шеечную слизь;
- гемотрансфузионным: при переливании крови, лейкоцитарной массы, иногда - при пересадке органов и тканей;
- трансплацентарным: во время беременности от матери плоду.
Нередко цитомегаловирус находится в организме многие годы и может ни разу не проявить себя и не нанести вреда человеку. Проявление скрытой инфекции происходит, как правило, при ослаблении иммунитета. Угрожающую по своим последствиям опасность цитомегаловирус представляет у лиц со сниженным иммунитетом (ВИЧ-инфицированных, перенесших трансплантацию костного мозга или внутренних органов, принимающих иммунодепрессанты), при врожденной форме цитомегалии, у беременных.
Патогенез
Попадая в кровь, цитомегаловирус вызывает выраженную иммунную реакцию, проявляющуюся в выработке защитных белковых антител – иммуноглобулинов М и G (IgM и IgG) и противовирусной клеточной реакцией - образованием лимфоцитов CD 4 и CD 8. Угнетение клеточного иммунитета при ВИЧ-инфекции приводит к активному развитию цитомегаловируса и вызываемой им инфекции.
Даже при бессимптомном течении инфекции носитель цитомегаловируса является потенциально заразным для неинфицированных лиц. Исключение составляет внутриутробный путь передачи цитомегаловируса от беременной женщины плоду, который происходит в основном при активном течении процесса, и лишь в 5% случаев вызывает врожденную цитомегалию, в остальных же носит бессимптомный характер.
Симптомы цитомегалии
Врожденная цитомегалия
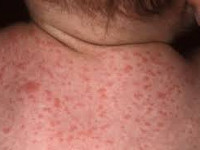
В 95% случаев внутриутробное инфицирование плода цитомегаловирусом не вызывает развития заболевания, а протекает бессимптомно. Врожденная цитомегаловирусная инфекция развивается у новорожденных, матери которых перенесли первичную цитомегалию. Врожденная цитомегалия может проявляться у новорожденных в различных формах:
- петехиальная сыпь – мелкие кожные кровоизлияния - встречается у 60-80% новорожденных;
- недоношенность и задержка внутриутробного развития плода - встречается у 30% новорожденных;
- желтуха;
- хориоретинит – острый воспалительный процесс в сетчатке глаза, часто вызывающий снижение и полную потерю зрения.
Летальность при внутриутробном инфицировании цитомегаловирусом достигает 20-30%. Из выживших детей большая часть имеет отставание в умственном развитии или инвалидность по слуху и зрению.
Приобретенная цитомегалия у новорожденных
При инфицировании цитомегаловирусом в процессе родов (при прохождении плода по родовым путям) или в послеродовом периоде (при бытовом контакте с инфицированной матерью или грудном вскармливании) в большинстве случаев развивается бессимптомное течение цитомегаловирусной инфекции. Однако у недоношенных младенцев цитомегаловирус может вызывать затяжную пневмонию, к которой часто присоединяется сопутствующая бактериальная инфекция. Часто при поражении цитомегаловирусом у детей отмечается замедление в физическом развитии, увеличение лимфоузлов, гепатит, сыпь.
Мононуклеозоподобный синдром
У лиц, вышедших из периода новорожденности и имеющих нормальный иммунитет, цитомегаловирус может вызывать развитие мононуклеозоподобного синдрома. Течение мононуклеазоподобного синдрома по клинике не отличается от инфекционного мононуклеоза, вызываемого другой разновидностью герпесвируса – вирусом Эбштейна-Барр. Течение мононуклеозоподобного синдрома напоминает упорную простудную инфекцию. При этом отмечается:
- длительная (до 1 месяца и более) лихорадка с высокой температурой тела и ознобами;
- ломота в суставах и мышцах, головная боль;
- выраженные слабость, недомогание, утомляемость;
- боли в горле;
- увеличение лимфоузлов и слюнных желез;
- кожные высыпания, напоминающие сыпь при краснухе (обычно встречается при лечении ампициллином).
В отдельных случаях мононуклеозоподобный синдром сопровождается развитием гепатита – желтухой и повышением в крови печеночных ферментов. Еще реже (до 6% случаев) осложнением мононуклеозоподобного синдрома служит пневмония. Однако у лиц с нормальной иммунной реактивностью она протекает без клинических проявлений, выявляясь лишь при проведении рентгенографии легких.
Длительность течения мононуклеозоподобного синдрома составляет от 9 до 60 дней. Затем обычно наступает полное выздоровление, хотя на протяжении нескольких месяцев могут сохраняться остаточные явления в виде недомогания, слабости, увеличенных лимфоузлов. В редких случаях активизация цитомегаловируса вызывает рецидивы инфекции с лихорадкой, потливостью, приливами и недомоганием.
Цитомегаловирусная инфекция у лиц с ослабленным иммунитетом
Ослабление иммунитета наблюдается у лиц, страдающих синдромом врожденного и приобретенного (СПИД) иммунодефицита, а также у пациентов, перенесших пересадку внутренних органов и тканей: сердца, легкого, почки, печени, костного мозга. После пересадки органов пациенты вынуждены постоянно принимать иммунодепрессанты, ведущие к выраженному подавлению иммунных реакций, что вызывает активность цитомегаловируса в организме.
У пациентов, перенесших трансплантацию органов, цитомегаловирус вызывает поражение донорских тканей и органов (гепатит – при пересадке печени, пневмонию при пересадке легкого и т. д.). После трансплантации костного мозга у 15-20% пациентов цитомегаловирус может привести к развитию пневмонии с высокой летальностью (84-88%). Наибольшую опасность представляет ситуация, когда инфицированный цитомегаловирусом донорский материал пересажен неинфицированному реципиенту.
Цитомегаловирус поражает практически всех ВИЧ-инфицированных. В начале заболевания отмечаются недомогание, суставные и мышечные боли, лихорадка, ночная потливость. В дальнейшем к этим признакам могут присоединяться поражения цитомегаловирусом легких (пневмония), печени (гепатит), мозга (энцефалит), сетчатки глаза (ретинит), язвенные поражения и желудочно-кишечные кровотечения.
У мужчин цитомегаловирусом могут поражаться яички, простата, у женщин – шейка матки, внутренний слой матки, влагалище, яичники. Осложнениями цитомегаловирусной инфекции у ВИЧ-инфицированных могут стать внутренние кровотечения из пораженных органов, потеря зрения. Множественное поражение органов цитомегаловирусом может привести к их дисфункции и гибели пациента.
Диагностика
С целью диагностики цитомегаловирусной инфекции проводится лабораторное обследование. Постановка диагноза цитомегаловирусной инфекции основана на выделении цитомегаловируса в клиническом материале или при четырехкратном повышении титра антител.
- ИФА-диагностика. Включает определение в крови специфических антител к цитомегаловирусу - иммуноглобулинов М и G. Наличие иммуноглобулинов М может свидетельствовать о первичном заражении цитомегаловирусом либо о реактивации хронической ЦМВИ. Определение высоких титров IgМ у беременных может угрожать инфицированию плода. Повышение IgМ выявляется в крови спустя 4-7 недель после заражения цитомегаловирусом и наблюдается на протяжении 16-20 недель. Повышение иммуноглобулинов G развивается в период затухания активности цитомегаловирусной инфекции. Их наличие в крови говорит о присутствии цитомегаловируса в организме, но не отражает активности инфекционного процесса.
- ПЦР-диагностика. Для определения ДНК цитомегаловируса в клетках крови и слизистых (в материалах соскобов из уретры и цервикального канала, в мокроте, слюне и т. д.) используется метод ПЦР-диагностики (полимеразной цепной реакции). Особенно информативно проведение количественной ПЦР, дающей представление об активности цитомегаловируса и вызываемого им инфекционного процесса.
В зависимости от того, какой орган поражен цитомегаловирусной инфекцией, пациент нуждается в консультации гинеколога, андролога, гастроэнтеролога или других специалистов. Дополнительно по показаниям проводится УЗИ органов брюшной полости, кольпоскопия, гастроскопия, МРТ головного мозга и другие обследования.
Лечение цитомегаловирусной инфекции
Неосложненные формы мононуклеазоподобного синдрома не требует специфической терапии. Обычно проводятся мероприятия, идентичные лечению обычного простудного заболевания. Для снятия симптомов интоксикации, вызываемой цитомегаловирусом, рекомендуется пить достаточное количество жидкости.
Лечение цитомегаловирусной инфекции у лиц, входящих в группу риска, проводится противовирусным препаратом ганцикловиром. В случаях тяжелого течения цитомегалии ганцикловир вводится внутривенно, т. к. таблетированные формы препарата обладают лишь профилактическим эффектом в отношении цитомегаловируса. Поскольку ганцикловир обладает выраженными побочными эффектами (вызывает угнетение кроветворения - анемию, нейтропению, тромбоцитопению, кожные реакции, желудочно-кишечные расстройства, повышение температуры и ознобы и др.), его применение ограничено у беременных, детей и у людей, страдающих почечной недостаточностью (только по жизненным показаниям), он не используется у пациентов без нарушения иммунитета.
Для лечения цитомегаловируса у ВИЧ-инфицированных наиболее эффективен препарат фоскарнет, также обладающий рядом побочных эффектов. Фоскарнет может вызывать нарушение электролитного обмена (снижение в плазме крови магния и калия), изъязвление половых органов, нарушение мочеиспускания, тошноту, поражение почек. Данные побочные реакции требуют осторожного применения и своевременной корректировки дозы препарата.
Прогноз
Особую опасность цитомегаловирус представляет при беременности, так как может провоцировать выкидыш, мертворождение или вызывать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с герпесом, токсоплазмозом и краснухой, относится к числу тех инфекций, обследоваться на которые женщины должны профилактически, еще на этапе планирования беременности.
Профилактика
Особенно остро вопрос профилактики цитомегаловирусной инфекции стоит у лиц, входящих в группу риска. Наиболее подвержены инфицированию цитомегаловирусом и развитию заболевания ВИЧ-инфицированные (особенно больные СПИДом), пациенты после трансплантации органов и лица с иммунодефицитом иного генеза.
Неспецифические методы профилактики (например, соблюдение личной гигиены) неэффективны в отношении цитомегаловируса, так как заражение им возможно даже воздушно-капельным путем. Специфическая профилактика цитомегаловирусной инфекции проводится ганцикловиром, ацикловиром, фоскарнетом среди пациентов, входящих в группы риска. Также для исключения возможности инфицирования цитомегаловирусом реципиентов при пересадке органов и тканей необходим тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Цитомегаловирусная инфекция у детей — это инфекционное заболевание, которое вызвано цитомегаловирусом и поражает слюнные железы, внутренние органы, ЦНС. В детстве патология чаще возникает при трансплацентарном или интранатальном заражении. Локализованные формы проявляются сиаладенитом, гепатитом, нефритом и т. д., распространенный вариант инфекции характеризуется поражением головного мозга, легких, почек и органов ЖКТ. Диагностика предполагает идентификацию возбудителя цитологическими, гистологическими, серологическими и молекулярно-биологическими методами. Лечение цитомегаловирусной болезни проводится специфическим иммуноглобулином и противовирусными препаратами.
МКБ-10
Общие сведения
Заражение цитомегаловирусной инфекцией (ЦМВИ) наблюдается у 20%‒60% всего детского населения, но в большинстве случаев оно протекает бессимптомно. Внутриутробное инфицирование вирусом от больной матери происходит в 30-50% случаев, при этом до 18% младенцев после рождения имеют клинические симптомы. Учитывая полиморфизм клинической картины, ранняя диагностика и лечение у детей затруднены. Цитомегаловирусная инфекция представляет серьезную опасность, особенно для плода и новорожденного, у которых заболевание, как правило, вызывает необратимые осложнения.

Причины
Болезнь вызвана герпесвирусом 5 типа — Cytomegalovirus hominis. Он имеет 6 штаммов: Davis, AD 169, Kerr, C-87, Esp, Towne, причем ребенок может быть инфицирован сразу несколькими подтипами возбудителя. Цитомегаловирус (ЦМВ) имеет ДНК-геном, отличается медленной репликацией и сравнительно низкой вирулентностью. Он термолабилен, уничтожается при температуре более 56°С, но длительно сохраняет жизнеспособность в комнатных условиях.
При врожденной ЦВМИ передача вируса к плоду происходит трансплацентарно, при перинатальной инфекции — путем контакта с вагинальными выделениями матери, грудным молоком или препаратами крови. Риск заражения увеличивается, если мать с острой формой болезни не получает специфическое лечение. В постнатальном периоде ребенок чаще всего заражается от ближайших родственников и сверстников воздушно-капельным или контактно-бытовым путем.
Патогенез
Попадая в кровь, вирус реплицируется в лейкоцитах, моноцитах и макрофагах и в дальнейшем он пожизненно сохраняется в лимфоцитарных органах. Зачастую процесс выражается в виде латентной инфекции, при которой у ребенка нет симптомов, и ему не требуется лечение. Активность цитомегаловируса зависит от состояния иммунитета: при физиологической иммунной недостаточности, которая наблюдается у детей раннего возраста, риск манифестной цитомегаловирусной инфекции возрастает в разы.
Классификация
В детской инфектологии различают врожденную (внутриутробную) и приобретенную формы патологии. По течению инфекция бывает острой (до 3 месяцев), подострой (3-6 месяцев), затяжной (6-12 месяцев) и хронической (более 1 года). По клиническим признакам выделяют локализованный (сиаладенит, нефрит, гепатит, энцефалит) и генерализованный вариант. С учетом тяжести течения цитомегаловирусную болезнь делят на 3 степени:
- Легкая. Отличается незначительными патоморфологическими изменениями во внутренних органах, которые не сказываются на их функциональной активности.
- Среднетяжелая. Проявляется выраженными органическими поражениями в сочетании с клиническими симптомами и расстройством функции некоторых внутренних органов.
- Тяжелая. Манифестирует тяжелыми органическими патологиями, резко выраженной интоксикацией и генерализованным характером поражения.
Симптомы
Врожденная ЦМВИ
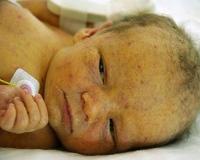
У пациентов с манифестной врожденной форме цитомегаловирусной болезни признаки наблюдаются с первых дней жизни. Типичный комплекс симптомов у новорожденных детей включает недоношенность и/или низкую массу тела, поражение гепатобилиарной системы (увеличение печени, желтуха, гепатиты и циррозы), лимфаденопатии и геморрагическую сыпь на коже. Если инфицирование произошло на ранних сроках беременности, ребенок рождается с аномалиями — микроцефалией, гипоплазией легких, атрезией пищевода.
Приобретенная ЦМВИ
Приобретенная цитомегаловирусная болезнь обычно протекает в субклинической или латентной форме, когда у ребенка возникают гриппоподобные симптомы, субфебрильная температура без видимой причины. После заражения инфекция может длительное время себя не проявлять и давать обострения при снижении иммунного статуса, действии неблагоприятных эндо- или экзогенных факторов.
Течение манифестной приобретенной формы напоминает инфекционный мононуклеоз. У ребенка внезапно появляется слабость, повышается температура, беспокоят недомогание, головные боли, отсутствует аппетит. Позже присоединяются сильные боли в горле, увеличиваются подчелюстные и шейные лимфоузлы. Если цитомегаловирусная инфекция проявляется сиаладенитом, наблюдается резкое увеличение и болезненность слюнных желез на фоне фебрильной лихорадки.
Генерализованная ЦМВИ
При генерализованном варианте течения инфекции у детей поражается бронхолегочная система (пневмонии, дыхательная недостаточность), ЖКТ (энтероколит, мальабсорбция), печень (желтуха, цитомегаловирусный гепатит, билиарный цирроз). Особенно опасно вовлечение в процесс нервной системы, что проявляется судорожным синдромом, парезами и параличами, задержкой психомоторного развития.
Осложнения
Поражение клеток при цитомегаловирусной болезни создает благоприятные условия для возникновения аутоиммунных поражений — системной красной волчанки, рассеянного склероза, гломерулонефрита. Иногда после малосимптомной врожденной цитомегаловирусной инфекции осложнения наблюдаются в отдаленном периоде (в возрасте ребенка 2-5 лет). В основном они проявляются неврологическими расстройствами и поражением органов чувств.
Диагностика
Цитомегаловирусная инфекция отличается многообразием клинических признаков и часто протекает под маской других патологий, что затрудняет работу детского инфекциониста. На первичном приеме, помимо стандартного физикального осмотра, врач собирает детальный акушерский анамнез, чтобы выявить факторы риска антенатального инфицирования. Диагноз ЦМВИ правомочен только при лабораторном подтверждении, для чего используют следующие методы:
Инструментальные методы подбираются соответственно форме заболевания. Для оценки структурно-функциональных особенностей печени и билиарного тракта назначают УЗИ органов брюшной полости. КТ и МРТ головного мозга информативны для выявления врожденных пороков и кальцификатов. Рентгенография ОГК необходима при симптомах дыхательных расстройств. По показаниям ребенка направляют на консультации к профильным специалистам— кардиологу, неврологу, отоларингологу.
Лечение цитомегаловирусной инфекции у детей
Препаратом выбора у новорожденных и детей первого года жизни является специфический антицитомегаловирусный иммуноглобулин, который имеет повышенную концентрацию IgG. Лечение начинают при манифестных формах заболевания и проводят по схеме: вначале вводится высокая доза препарата, а спустя 9-10 дней дозировку постепенно уменьшают, контролируя степень ответа на терапию и активность процесса.
В старшем возрасте перечень препаратов, применяемых при цитомегаловирусной инфекции, значительно расширяется. Лечение включает противовирусные средства из группы нуклеозидов и нуклеотидов (ганцикловир, валганцикловир), производные ортофосфорной кислоты (фоскарнет). При легкой и среднетяжелой формах назначают интерфероны, иммуностимуляторы.
Для купирования интоксикации показано обильное питье (при легких формах), при среднетяжелых и тяжелых клинических вариантах рекомендована инфузионная терапия. Патогенетическая терапия подбирается в соответствии с характером течения болезни и может включать пищеварительные ферменты, ингибиторы протеиназ, гемостатики. Для предупреждения вторичных бактериальных осложнений используют антибиотики (макролиды, цефалоспорины, гликопептиды).
Прогноз и профилактика
При малосимптомных приобретенных вариантах цитомегаловирусная болезнь протекает без осложнений, зачастую у ребенка выявляется только латентное носительство. Угрозу для жизни и здоровья представляют тяжелые генерализованные инфекции, которые в 50-60% случаев сопровождаются осложнениями, несмотря на проводимое лечение. Особо опасно поражение цитомегаловирусом для детей с иммунодефицитными состояниями.
Основу профилактики врожденной ЦМВИ составляет обязательное лабораторное обследование женщин на носительство цитомегаловируса, которое проводится при планировании зачатия и во время беременности. Если в семье есть пациент с цитомегаловирусной инфекцией, необходимо ограничить его общение с ребенком и обеспечить лечение. Карантинно-изоляционные мероприятия в отношении заболевших и контактных лиц не производятся.
2. Клинические рекомендации (протокол лечения) оказания медицинской помощи детям больным цитомегаловирусной инфекцией. — 2015.
В статье описано течение холестатического варианта врожденной цитомегаловирусной инфекции у детей с оценкой акушерско-гинекологического анамнеза матерей и особенностей неонатального периода у новорожденных. Беременность у женщин протекала с признаками фет
Abstract. The article describes the course of the cholestatic variant of congenital cytomegalovirus infection in children with an assessment of the obstetric and gynecological history of mothers and the characteristics of the newbornneonatal period. Pregnancy in women proceeded with signs of fetal-placental insufficiency, which led to the birth of children with a low gestational age, since cytomegalovirus infection developed in an acute form. The newborns had a low Apgar score and signs of hypotrophy of I-II degrees. The clinical picture of congenital cytomegalovirus hepatitis was characterized by a protracted course and had an undulating character, a complete recovery of mass-growth parameters, a symptom of jaundice took place within 3 months. It was revealed that a longer cholestasis syndrome was observed in children who had both congenital cytomegalovirus infection and impaired bilirubin uptake, in particular, Gilbert's syndrome. Ursodeoxycholic acid is the only generally accepted starting drug for the drug effect on cholestasis syndrome in children with liver disease. Complex therapy with the use of the drug Ursodeoxycholic acid at a dose of 15-20 mg/kg per day, at the early stages of treatment, this infectious pathology made it possible to stabilize the clinical and laboratory parameters. In the absence of complaints and clinical manifestations, the levels of ALT, AST and ALP were restored for a long period within 5-6 months, while the cholesterol values returned to normal by 3 months. The chosen scheme of therapy with Ursodeoxycholic acid at a dose of 15-20 mg/kg per day contributed to the prevention of severe complications from the biliary tract, such as chronic cholecystocholangitis, primary biliary cirrhosis. The use of therapeutic tactics, taking into account the individual characteristics of young children, was not accompanied by the presence of side effects. For citation: Pervishko O. V., Soboleva N. G., Baum T. G., Volik D. V., Kalinovskya D. Yu. Congenital cytomegalovirus hepatitis: cholestatic syndrome and its correction // Lechaschi Vrach. 2022; 2 (25): 20-24. DOI: 10.51793/OS.2022.25.2.003
Резюме. В статье описано течение холестатического варианта врожденной цитомегаловирусной инфекции у детей с оценкой акушерско-гинекологического анамнеза матерей и особенностей неонатального периода у новорожденных. Беременность у женщин протекала с признаками фетоплацентарной недостаточности, что обуславливало рождение детей с низким сроком гестации, так как цитомегаловирусная инфекция развивалась в острой форме. Новорожденные имели низкую оценку по шкале Апгар и признаки гипотрофии I-II степени. Клиническая картина врожденного цитомегаловирусного гепатита характеризовалась затяжным течением и носила волнообразный характер, полное восстановление весоростовых показателей, симптома желтухи проходило в течение 3 месяцев. Выявлено, что более длительный синдром холестаза отмечался у детей, которые имели одновременно врожденную цитомегаловирусную инфекцию и нарушение захвата билирубина, в частности синдром Жильбера. Единственным общепринятым стартовым препаратом для медикаментозного воздействия на синдром холестаза при заболеваниях печени у детей является урсодезоксихолевая кислота. Комплексная терапия с применением препарата урсодезоксихолевой кислоты в дозе 15-20 мг/кг в сутки на ранних этапах лечения данной инфекционной патологии позволила стабилизировать клинико-лабораторные показатели. При отсутствии жалоб и клинических проявлений уровни аланинаминотрансферазы, аспартатаминотрансферазы и щелочной фосфатазы восстанавливались в течение 5-6 месяцев, тогда как показатели холестерина нормализовались к 3 месяцам. Выбранная схема терапии препаратом урсодезоксихолевой кислоты в дозе 15-20 мг/кг в сутки способствовала профилактике тяжелых осложнений со стороны желчевыводящих путей, таких как хронические холецистохолангиты, первичный билиарный цирроз. Применение лечебной тактики с учетом индивидуальных особенностей детей раннего возраста не сопровождалось побочными эффектами.
В зарубежных и отечественных литературных источниках наиболее исследованной инфекцией раннего детского возраста была и остается одна из герпетических, а именно цитомегаловирусная (ЦМВИ). Влияние вирусного агента на различных этапах внутриутробного и внеутробного периода формирует основную клиническую картину. Вариантами течения заболевания являются:
- острый приобретенный ЦМВ-гепатит с полным выздоровлением;
- первично-хронический приобретенный ЦМВ-гепатит умеренной степени активности;
- врожденный ЦМВ-гепатит с формированием порока развития (атрезии) желчевыводящих путей;
- формирующийся билиарный цирроз печени 1.
Механизм формирования отличных друг от друга патологий печени при ЦМВИ до конца не изучен [5]. В то же время с помощью нецелевой газовой хроматографии – масс-спектрометрии активно исследуются изменения аминокислотного, азотного и энергетического обмена у детей с инфантильной холестатической гепатопатией и внепеченочной билиарной атрезией [6]. Современные клинические характеристики ЦМВ-гепатита связаны с синдромом длительной желтухи, гиперферментемией, холестазом, а также с формированием аплазии/гипоплазии желчных протоков 8.
Современная лабораторная диагностика позволяет установить причину заражения гепатотропным вирусом и определить вовлеченность паренхимы в патологический процесс [9]. Холестатический вариант течения болезни является наиболее распространенным. Он характеризуется наличием желтухи у 62% детей. Основным биохимическим показателем холестаза у новорожденных и детей раннего возраста является повышение в сыворотке крови щелочной фосфатазы (ЩФ), 5-нуклеотидазы (5-НТ), гаммаглутамилтранспептидазы (ГГТ) [10]. В этом случае показатели аланинаминотрансферазы (АЛТ)/аспартатаминотрансферазы (АСТ) повышаются одновременно в 1,5-2 раза, но с преобладанием уровня АСТ [11].
Длительное хроническое течение заболевания требует назначения гепатопротекторов комбинированного воздействия, в частности, обладающих желчегонным, цитопротективным, антифибринолитическим действием. Единственным общепринятым стартовым препаратом для медикаментозного воздействия на синдром холестаза при заболеваниях печени у детей является урсодезоксихолевая кислота (УДХК) [12]. В литературных источниках широко описаны области ее применения, в частности в составе комплексной терапии холестаза у новорожденных и детей раннего возраста 14, при вирусных гепатитах В и С, а также с целью проведения дифференциальной диагностики билиарной атрезии и неонатального гепатита у 101 ребенка [17]. Основное холеретическое действие УДХК обусловлено несколькими механизмами, в частности конкурентной борьбой с токсичными желчными кислотами за рецепторы в подвздошной кишке, влиянием на гидрофобные желчные кислоты с целью их выведения, активацией транспортных белков [18].
На основании вышесказанного целью нашей работы явилось изучение эффективности применения УДХК при врожденном ЦМВ-гепатите у детей с признаками холестатического синдрома.
Материалы и методы исследования
Под наблюдением находились 34 ребенка в возрасте от 28 дней до 12 месяцев с висцеральной формой врожденной ЦМВИ, протекавшей с синдромом холестаза. Среди них было 19 мальчиков и 15 девочек, выписанных из родильного дома или со второго этапа выхаживания. Ежемесячно при проведении объективного осмотра измеряли антропометрические параметры, оценивали динамику результатов лабораторно-инструментальных обследований.
При выявлении синдрома холестаза всем обследуемым назначали суспензию УДХК (Урсофальк) в вечернее время (19-22 часа) в дозе 15-20 мг/кг в сутки в 1 прием в течение первого месяца с последующим ежемесячным динамическим контролем.
Результаты и обсуждение
У большинства наших пациентов акушерско-гинекологический анамнез был отягощен. В частности, угроза прерывания беременности на ранних сроках отмечалась у 21 женщины; признаки хронической фетоплацентарности – у 67%.
Проведение скрининга на TORCH-инфекции показало, что ЦМВ выявлялся у 7 из 34 обследуемых женщин во время беременности с помощью метода ПЦР-диагностики в крови. После консультации инфекциониста женщины получали лечение интерфероном α-2b по схеме, с последующим динамическим контролем. Остальные беременные на герпетические инфекции не обследовались, 2 женщины на учете не состояли. При сборе акушерского анамнеза обращало на себя внимание наличие контактов внутри семьи с детьми, посещающими детский сад и школу, при этом 9 детей получали лечение по поводу приобретенной ЦМВИ.
Большинство детей родились в срок, но 6 из них имели низкий срок гестации от 32 до 36 недель. Путем кесарева сечения родились 11 детей, при этом отмечен длительный безводный период продолжительностью более 14 часов. При рождении большинство детей имели низкую оценку по шкале Апгар: 6-7 баллов – 21 ребенок; 5-7 баллов – 9 новорожденных; 3-5 баллов – 4 пациента. Оценка весоростовых показателей выявила у 19 новорожденных признаки гипотрофии I–II степени. Признаки врожденной пневмонии отмечались у 12 детей (35%), синдром дыхательных расстройств – у 11 пациентов (32%). Неврологическая симптоматика с момента рождения у 14 (41%) наблюдаемых была представлена синдромом двигательных нарушений, 18 (53%) имели признаки вегетовисцеральных нарушений, 2 (6%) – гипертензионно-гидроцефальный синдром.
Продолжительность лабораторных изменений в биохимических анализах и их показатели перед началом и после терапии представлены в табл. 2.
Прием Урсофалька позволил нормализовать уровень общего и прямого билирубина, содержание холестерина в течение первых 2-3 месяцев лечения, тогда как максимально долго сохранялись высокими уровни АЛТ, АСТ, ГГТ, ЩФ. Особенностями ОАК крови при висцеральной форме ЦМВИ были лейкоцитоз до 13,6 ± 3,1 × 10 9 г/л со сдвигом влево у 2/3 больных; увеличение лимфоцитов – у 55,8% детей; нейтропения – у 41,2%; гипохромная анемия – у 50% обследуемых. Стабилизация показателей тромбоцитов происходила в течение двух месяцев.
По данным ультразвукового обследования органов брюшной полости определялись увеличение печени у 2/3 детей, которое держалось более 6 месяцев, и спленомегалия – до 5 месяцев. Толщина стенки желчного пузыря нормализовалась на фоне применения препарата Урсофальк в течение 2 месяцев у большинства пациентов.
При проведении контроля ПЦР-диагностики на ЦМВ в крови, моче, слюне динамика отрицательных результатов выявилась следующая: в крови вирус перестал определяться в течение 2,5 месяцев. Вирус продолжал сохраняться в слюне (до 2000 копий/ мл) в течение 10 месяцев, в моче (до 1500 копий/ мл) – 9 месяцев при отсутствии клинических проявлений, переводя данное заболевание в стадию стабилизации.
Комплексное лечение позволило нормализовать показатели биохимического анализа крови, в частности показатели общего и прямого билирубина, уровней ферментов печени и холестерина (табл. 2). Применение препарата УДХК (Урсофальк) в дозировке 15-20 мг/кг в лечении синдрома холестаза показало высокую эффективность данной лекарственной формы, а также не позволило развиться осложнениям в виде холецистохолангитов, внутридолькового холестаза, холангита, цирроза печени.
Лечение холестатического варианта врожденной ЦМВИ с использованием препарата УДХК (Урсофальк) в суспензии проводилось длительно, за время наблюдения родители не отмечали побочных эффектов терапии, а ее эффективность оценивали положительно.
Выводы:
- Формирование холестатического варианта врожденной ЦМВИ происходило при первичном инфицировании женщины во время беременности.
- Источниками инфекции для женщины явилось эпидокружение, в частности, дети дошкольного и школьного возраста, посещающие организованные коллективы.
- Холестатический синдром при ЦМВ-гепатите протекает длительно и носит волнообразный характер.
- На формирование длительного синдрома холестаза также оказывали влияние наследственные заболевания, связанные с нарушением захвата билирубина (в частности, синдром Жильбера).
- Назначение препарата УДХК (Урсофальк) приводило к нормализации клинико-лабораторных и инструментальных показателей у детей с синдромом желтухи и холестаза при ЦМВ-гепатите.
- Длительность терапии препаратом УДХК (Урсофальк) определяется индивидуальными особенностями пациента.
- Антихолестатическая терапия препаратом Урсофальк при его длительном приеме направлена на профилактику осложнений при врожденном ЦМВ-гепатите.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
1 Федеральное государственное бюджетное образовательное учреждение высшего образования Кубанский государственный медицинский университет Министерства здравоохранения Российской Федерации; 350063, Россия, Краснодар, ул. Седина, 4
2 Клиника G8 Centre, 350062, Россия, Краснодар, ул. Совхозная, 1, корп. 7
Сведения об авторах:
Information about the authors:
Врожденный цитомегаловирусный гепатит: холестатический синдром и его коррекция/ О. В. Первишко, Н. Г. Соболева, Т. Г. Баум, Д. В. Волик, Д. Ю. Калиновская
Для цитирования: Первишко О. В., Соболева Н. Г., Баум Т. Г., Волик Д. В., Калиновская Д. Ю. Врожденный цитомегаловирус¬ный гепатит: холестатический синдром и его коррекция // Лечащий Врач. 2022; 2 (25): 20-24. DOI: 10.51793/OS.2022.25.2.003
Теги: новорожденные, цитомегаловирус, желтуха, холестаз
Читайте также:

