Цитомегаловирус вызывает рак шейки матки
Обновлено: 24.04.2024
В последнее десятилетие характер серьезной медико-социальной проблемы приобрели оппортунистические инфекции вследствие их широкого распространения и крайне неблагоприятного влияния на уровень общего и репродуктивного здоровья населения [1,2,6,7]. Результаты проведенных исследований свидетельствуют о росте ЦМВ-инфекции при патологии генитального тракта у женщин [5,7]. Генерализованная форма цитомегаловирусной инфекции у женщин может проявляться в виде воспаления и эрозии шейки матки, внутреннего слоя матки, влагалища и яичников, а у мужчин генерализованная форма цитомегаловирусной инфекции поражает яички, околоушные железы, вызывает воспаление мочеиспускательного канала и неприятные ощущения при мочеиспускании. Так, цитомегалические клетки были выявлены, в соскобах шейки матки, цервикального канала, эндометрия, что свидетельствует о возможности ЦМВ вызывать эрозии шейки матки, цервициты, эндометриты. Гигантские ядерные включения обнаруживались и при исследовании кондилом [1,7]. Наиболее часто ЦМВИ органов малого таза возникает на фоне иммуносупрессии, выражающейся в дисбалансе регуляции иммунной системы, в том числе цитокиновой [3,4,5,7]. Способность вируса реплицироваться в клетках иммунной системы и индуцировать ее недостаточность является фоном для развития рецидивирующих бактериальных, грибковых и вирусных заболеваний.
Эффективное лечение цитомегалии сопряжено с определенными трудностями в выборе медикаментов. В арсенале врачей сегодня имеется несколько терапевтических средств - противовирусные препараты и человеческие иммуноглобулины [6,7]. До настоящего времени для лечения ЦМВИ наиболее широко использовались ацикловир и ганцикловир[2,6]. Высоким профилем безопасности обладает ацикловир, однако его действие на ЦМВ в 100 раз ниже, чем на ВПГ1/2 типа. Ганцикловир - характеризуется большей активностью против ЦМВ (в 50 раз), но выраженным токсическим эффектом [2,5]. В экспериментальных исследованиях доказано, что ганцикловир может угнетать сперматогенез и не исключается его канцерогенное воздействие на организм[9]. Во многих медицинских центрах мира проводиться пассивная иммунопрофилактика ЦМВИ с помощью иммуноглобулинов. При этом имеется достаточное количество работ, в которых дискутируется эффективность профилактического назначения иммуноглобулина у разных групп больных[2].
Все вышеперечисленное определяет необходимость поиска новых безопасных высокоэффективных препаратов обладающих противовирусным и иммуномодулирующим действием. Именно поэтому представляет интерес отечественный противовирусный препарат растительного происхождения Панавир, эффективный в отношении инфекций вызываемых разными ДНК- и РНК- содержащими вирусами (ЦМВ, ВПГ, ВПЧ). Руководствуясь инструкцией препарат может назначаться врачом при цитомегаловирусной инфекции, в том числе у пациенток с привычным невынашиванием беременности. Может применяться у женщин с хронической вирусной инфекцией и интерферонодефицитным состоянием на этапе подготовки к беременности. Характерными особенностями противовирусной активности Панавира является ингибирование синтеза вирусных белков, повышение жизнеспособности клеток, а так же индуцирование продукции IFN-a и IFN-y лейкоцитами.
Целью исследования явилось определение эффективности ректальных суппозиторий Панавир в лечении пациентов с ЦМВИ органов малого таза.
Материалы и методы
Под наблюдением находилось 30 больных с реактивацией ЦМВИ в органах малого таза, в возрасте от 20 до 40 лет. Диагностику ЦМВИ проводили при помощи исследования соскобов из уретры, вагины и цервикального канала с выявлением ДНК ЦМВ методом ампфликации нуклеиновых кислот ПЦР. Интерфероновый статус определяли в крови больных полученной из кубитальной вены. Забор материала для лабораторных исследований проводился до и через месяц после окончания лечения. Изучение эффективности, переносимости препарата проводилось на основании изучения: динамики показателей интерферонового статуса, отсутствия ДНК вируса цитомегалии в соскобах из урогенитального тракта после лечения и длительности ремиссии.
Панавир назначали, по 1 суппозиторию ректально на ночь. Процедура повторялась через день, 5 свечей на курс.
Результаты
При исследовании соскобов из урогенитального тракта при помощи ПЦР и ПЦР real time у всех больных выделены ДНК ЦМВ в клинически значимом титре, что свидетельствовало реактивации инфекции в нижних отделах органов малого таза.
При оценке показателей интерферонового статуса до лечения выявлены нарушения у всех 30 больных с цитомегаловирусной инфекцией органов малого таза.
Динамика показателей интерферонового статуса после терапии больных суппозиториями панавир
| Показатели (Ме/мл) | До лечения (п=30) | После лечения (п=30) | Контрольная группа |
| сывороточный IFN | 16,8±3,1* | 6 ±2,0** | 4,8 ±0,5 |
| Продукция FN-a | 24,2 ±2,6* | 67,6 ±4,6** | 89 ±1,5 |
| Продукция IFN-y | 12,4 ±2,7* | 27,3 ± 2,66** | 32,4 ±5,9 |
Частота выделения ДНК ЦМВ из эпителия урогенитального тракта после терапии больных суппозиториями панавир
| Срок лечения | Число больных | ЦМВ не выявлен | ЦМВ выявлен |
| До лечения | 30 | 0 | 30 |
| После лечения | 30 | 27 | 3 |
Через месяц после терапии суппозиториями панавир ДНК ЦМВ в соскобах из урогенитального тракта не обнаруживалась у 27 пациентов из 30.
При наблюдении за больными в период 60 дней после проведенного лечения ремиссия наблюдалась у 29 пациентов.
Выводы:
Литература
1. Прозоровский СВ., Тартаковский И.С. Возбудители оппортунистических инфекций - роль в инфекционной патологии человека и методы лабораторной диагностики. Клин. лаб. диаг. 1998; 2: 24, 33-5.
2. Чешек Н.И. Методическое пособие для врачей. Цитомегаловирусная инфекция. Эпидемиология, клиника, диагностика, лечение и профилактика. М, 2001, 3-5.
3. Белокрицкая Т.Е., Витковский Ю.А., Пономарева Ю.Н. Роль цитокинов в патогенезе нарушений иммунитета и гемостаза у больных с тяжелыми дисплазиями и раком шейки матки. Вопр. онкол. 2003; 49 (1): 51-4.
4. Краснопольский В. И., Радзинский В.Е., Буянова С.Н. Патология влагалища и шейки матки. М.: Медицина, 1997.
5. Козлова В.И., Пухнер А.Ф. Вирусные, хламидийные и микоплазменные заболевания гениталий. М., 1997; с. 536.
6.0shiro ВТ. Cytomegalovirus Infection in Pregnancy. In Protocols for Infectious Diseases in Obstetrics and Gynecology, 2nd ed. Mead PB, Hager WD, Faro S, eds.: BlackwellScience, 2000; 157-70.
7. Sweet RL, Gibbbs RS (eds.). Infectious Diseases of the Female Genital Tract, 3d ed.: Williams and Wilkins, 2005; 469-79.
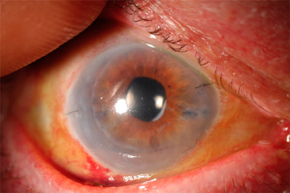
Генерализованная форма ЦМВИ (цитомегалии, цитомегаловирусной инфекции), как правило, возникает на фоне какого-либо другого заболевания, резко снижающего иммунитет (лейкозы, злокачественные опухоли, СПИД), или после тяжелых хирургических операций. Следствием цитомегалии в этом случае могут быть воспаление надпочечников, селезенки, поджелудочной железы, почек и других внутренних органов. ЦМВИ также может проявляться в виде гепатита. Доказано, что до 30% гепатитов неясной этиологии обусловлены поражением печени герпесвирусами, а именно цитомегаловирусом или вирусом простого герпеса.
Как сопутствующие явления возникают пневмонии, поражения сосудов глаза, стенок кишечника, головного мозга и периферических нервов. В составе крови уменьшается количество тромбоцитов. Кроме основного заболевания и ЦМВИ, ухудшение состояния больного может вызвать наслаивающаяся септическая бактериальная инфекция.
По статистике Всемирной Организации Здравоохранения генерализованная форма цитомегалии является причиной наибольшего количества летальных случаев в мире после гриппа и ОРВИ.
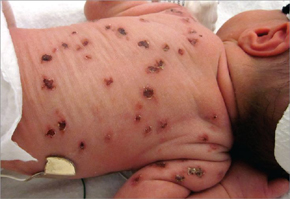
Внутриутробная ЦМВИ считается наиболее опасной, так как может вызвать серьезные поражения плода вплоть до его гибели или привести к рождению детей с тяжелыми неврологическими расстройствами, патологией зрительного и слухового нервов, различными соматическими повреждениями. Характер поражения зависит от сроков инфицирования плода ЦМВ. На ранних сроках (4–6 недель беременности) возможна его гибель или самопроизвольный выкидыш. При инфицировании цитомегаловирусом (ЦМВ) в поздние сроки беременности прогноз более благоприятен. Инфицирование ЦМВ плода во второй половине беременности может не приводить к клинически выраженной патологии при рождении, но быть причиной развития заболевания в первые недели - месяцы жизни ребенка.
Инфицирование в первые 3 месяца гестации может привести к тератогенному действию на плод, а в более поздние сроки – к врожденной цитомегалии, не сопровождающейся пороками развития. У части детей внутриутробное инфицирование ЦМВ проявляется лишь к 5–7 годам в виде нарушения зрения, ухудшения слуха, судорожных расстройств, или задержки физического и умственного развития.
В связи с этим крайне важно обследование женщин на ранних сроках беременности (оптимально – при ее планировании) с целью установления иммунного статуса в отношении ЦМВИ и выявления группы риска, требующей более серьезного и регулярного обследования вплоть до родов.
Возможность онкогенного действия вируса окончательно не изучена. Полагают, что выделение вируса цитомегалии из опухоли больных саркомой Капоши, карциномы простаты, злокачественной лимфомы, рака шейки матки, аденокарциномы толстой кишки и др. является косвенным свидетельством этиологической роли отдельных штаммов ЦМВ человека в развитии онкологических заболеваний.
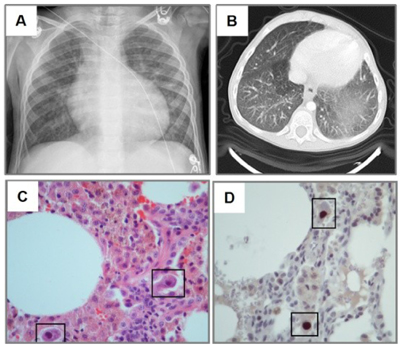
Цитомегаловирусная инфекция наиболее часто поражает реципиентов трансплантируемых органов. У 38–96% пациентов после трансплантации встречается активная форма ЦМВИ, при которой каждый орган может быть вовлечен в инфекционный процесс. Клинически выраженная ЦМВИ – одно из серьезных инфекционных осложнений при трансплантации солидных органов и костного мозга, являясь одной из частых причин длительной госпитализации больных и их смерти.
Имеются данные, подтвержденные при экспериментальной инфекции у животных, что у больных, перенесших пересадку сердца, ЦМВИ является одной из причин атеросклероза. Доказано, что сосудистые поражения почечного трансплантанта с дисфункцией почки обусловлены ЦМВИ.
Период максимального риска инфицирования приходится на 1–4-й мес. после трансплантации. Максимальный риск заболевания выше при первичном инфицировании. При первичном инфицировании заболевание протекает более тяжело, чем при активизации латентной ЦМВИ.
Основными проявлениями ЦМВИ у больных после трансплантации органов является гепатит, пневмония, ретинит, тяжелые поражения желудочно-кишечного тракта, лейкопения. Присоединение бактериальной, грибковой или протейной инфекции на фоне ЦМВИ могут приводить к угрожающим жизни последствиям. Так, у пациентов после трансплантации костного мозга самым тяжелым осложнением считается интерстициальная пневмония, которая диагностируется в 15–20% случаев. У 80–90% больных пневмония заканчивается летальным исходом.

Основным местом локализации первичной генитальной инфекции ВПГ у женщин является шейка матки. Чаще всего, герпетические поражения у женщин локализуются на больших и малых половых губах (68,6%), в области вульвы (41,8%), клитора (35,7%), влагалища и шейки матки (84,4%).
ВПГ был изолирован из шейки матки во время первичного заражения у 88—90 % женщин с первичной инфекцией ВПГ-2, которые имели везикулезную сыпь на наружных гениталиях, у 65 % — с повторным эпизодом инфекции ВПГ-2, и у 80 % женщин с ВПГ-1. Большинство (89 %) женщин, выделяющих вирус при первичном эпизоде заболевания, имели изменения на шейке матки.
Особенностью генитального герпеса (Herpes genitalis) женских половых органов является многоочаговость. В патологический процесс нередко вовлекаются нижний отдел мочеиспускательного канала, слизистая оболочка ануса и прямой кишки. Вовлечение в инфекционный процесс этих органов может происходить вторично, вслед за возникновением герпеса наружных гениталий, но может протекать и как изолированное поражение.
Рецидивирующая герпетическая инфекция (РГИ) может проявляться клиникой вульвовагинита и цервицита, вызывать поражения слизистой матки, труб и придатков. В 83,6 % случаев при стойких, не поддающихся терапии кольпитах, лейкоплакиях шейки матки выделяют вирус простого герпеса (ВПГ) как один из ведущих этиологических факторов заболевания.
По некоторым данным, в 66 % случаев у женщин герпетическая инфекция (ГИ) протекает атипично. Об имеющейся длительно текущей хронической ГИ можно говорить на основании особенностей клинического течения, наличия герпетического антигена в эпителиальных клетках вульвы, влагалища и периферической крови.
д) хронических часто рецидивирующих сальпингоофоритах (воспаление маточных труб и яичников) и эндометритах, не поддающихся стандартной антибактериальной терапии;
У 1–2% женщин, поступающих в гинекологическую клинику, независимо от основного заболевания, обнаруживают цитологические доказательства ВПГ-инфекции.
Герпес наружных половых органов у женщин
При рецидивирующем герпесе (РГ) наружных половых органов у женщин, очаг поражения находится в области наружных гениталий и перианальной области. Герпетические высыпания у женщин возникают на больших и малых половых губах, области лобка и промежности.
Типичная форма РГ наружных гениталий характеризуется ярко выраженными симптомами болезни, классическим развитием очага поражения (эритема, образование везикул, развитие эрозивно-язвенных элементов, эпителизация) и субъективными ощущениями (зуд, чувство жжения, болезненность, недомогание). проявляется повторяющимися пузырьковыми высыпаниями. Выраженная симптоматика позволяет врачам визуально поставить диагноз РГГ, своевременно назначить лечение и информировать больного об инфекционном характере заболевания и опасности заражения полового партнера.
Герпес нижнего отдела урогенитального тракта, анальной области и ампулы прямой кишки
Поражение слизистых оболочек входа во влагалище, влагалища, влагалищной части шейки матки, цервикального канала, уретры, мочевого пузыря, анальной области и ампулы прямой кишки проявляется в двух клинических формах:
- очаговой, характеризующейся появлением типичных для простого герпеса слизистых оболочек везикулезно-эрозивных элементов,
- диффузной, при которой патологический процесс протекает по типу неспецифического воспаления.
Герпес верхнего отдела полового тракта (поражение матки, маточных труб).
Типичная клиническая картина герпетических поражений органов верхнего отдела мочеполового тракта проявляется симптомами неспецифического воспаления. Неспецифические герпетические поражения внутренних половых органов проявляются эндоцервицитом, эрозией шейки матки, вагинитом. Ряд авторов цервициты без наружных язв также относят к атипичным проявлениям ГГ.
Клинические проявления герпетических поражений внутренних половых органов не имеют специфических особенностей по сравнению с воспалительными процессами невирусной этиологии. Обычно больные предъявляют жалобы на выделения из влагалища, периодически появляющиеся боли в малом тазу, области проекции матки, яичников.
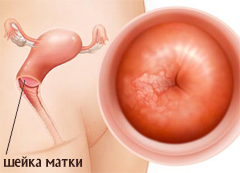
Герпетические поражения шейки матки
Герпетические поражения шейки матки могут носить типичный и нетипичный характер. В типичном варианте генитального герпеса – это всегда хорошо заметные множественные, довольно мелкие, с четкими границами округлые эрозии; высыпные элементы быстро минуют везикулярную стадию, в которой, кстати, эти элементы плохо различимы без применения кольпоскопии. Проблема причастности ВПГ к развитию нетипичных герпетических изменений слизистой шейки матки в настоящее время находится в стадии исследований.
При кольпоскопии в острый период герпетической инфекции шейки матки определяют изъязвление с неровными краями с сукровицей в области дна. Эволюция этого поражения идет от изъязвления с красным дном к простой эрозии до полного исчезновения в течение 3-х недель. К предшествующим изменениям относят маленькие буллезные образования, затем округлые микроэрозии с последующим формированием простых красных пятен, которые похожи на местный пятнистый кольпит.
Исследования показали, что выделение ДНК ВПГ с поверхности эрозии шейки матки в 60 % случаев сопровождается репликативной фазой ГИ (репликация и сборка вирусных частиц в инфицированных клетках). При эрозии и дисплазии шейки матки ВПГ-2 выявляется в 27,2% случаев непосредственно в соскобах со слизистой цервикального канала и сопровождается повышением титра специфических иммуноглобулинов в крови до диагностических уровней.
Особое значение влияние герпетической инфекции на состояние эпителия шейки матки имеет у женщин, длительно принимающих оральные гормональные контрацептивы. Известно, что длительный прием комбинированных стероидов в той или иной мере усиливает процессы плоскоклеточной метаплазии, а также может вызывать эффект эндоцервикальной гиперплазии, причем этот эффект в случае его развития наблюдается как в эпителии цервикального канала, так и в участках псевдоэрозии на фоне эктропиона, в полипах слизистой цервикального канала. В связи с этим прием оральных комбинированных контрацептивов может являться кофактором в развитии рака шейки матки, особенно в сочетании с герпетической инфекцией.
Герпетический цервицит
Герпетический цервицит – это воспалительный процесс, вызванный ВПГ. Для клинических проявлений герпетического цервицита характерно разнообразие проявлений — от легкой гиперемии с небольшим количеством эрозий до тяжелого некротического поражения (под эрозией шейки матки понимают дефект эпителия в результате воспаления). Цервицит диагностируется у 70-90% женщин с герпетическим поражением половых органов. Шейка матки при герпетическом эндоцервиците отечна, часто имеет эрозии, легко кровоточит при манипуляциях.
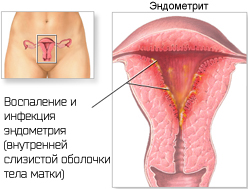
Герпетический эндометрит
Эндометрит — это воспаление внутренней (слизистой) оболочки матки (эндометрия) с поражением как функционального, так и базального слоя. Эндометрит, вызванный вирусом простого герпеса, является следствием длительной персистенции (существования) вируса в эндометрии. Герпетический эндометрит, как правило, возникает при атипичном или бессимптомном течении ГГ, типичная форма отмечается редко (~20% случаев). Клинические симптомы при вирусном поражении эндометрия чаще всего отсутствуют или проявляются нетипично, что приводит к ошибкам в диагностике и позднему началу лечения.
При герпетическомпоражении ткани нарушаются факторы местного и общего иммунитета, целостность поверхности эпителия, что приводит к созданию благоприятных условий для развития других инфекционных процессов .
Клинически герпетический эндометрит чаще проявляется во второй фазе менструального цикла или во время беременности, что, возможно, обусловлено повышением уровня простагландинов в этот период или супрессией Т-клеточного звена иммунитета, способствующих реактивации ВПГ, персистирующего в эндометрии. Субклиническая латентная внутриматочная герпетическая инфекция является важным фактором невынашивания беременности. Эндометриты ВПГ-этиологии встречаются нечасто, но эти заболевания очень опасны и могут вызвать гибель женщины и плода.
Герпес уретры и мочевого пузыря (герпетический уретрит)
Герпетический уретрит у женщин субъективно проявляется болями и резями в начале мочеиспускания, частыми позывами к мочеиспусканию. У 4,8% женщин имеет место очень болезненное мочеиспускание, или задержка мочеиспускания в результате инфекции уретры и слизистой оболочки мочевого пузыря. Нормализация функции мочевого пузыря у больных с задержкой мочеиспускания обычно происходит в течение 6–10 дней.
При осмотре наблюдаются гиперемия наружного отверстия уретры, наличие скудных слизистых выделений; при уретроскопии в передней части уретры иногда удается обнаружить мелкие поверхностные эрозии, катаральное воспаление.
Герпетический цистит
Ведущими симптомами герпетического цистита являются цисталгия, появление болей в конце мочеиспускания, дизурические явления. При герпетическом цистите появляются гематурия (кровь в моче), появление болей в конце мочеиспускания, боли в области мочевого пузыря. У женщины это может быть первым и единственным признаком ВПГ-инфицирования мочеполовой сферы. Он нередко возникает в первые 1-3 месяца после начала половой жизни или после смены полового партнера.
Герпес анальной области и прямой кишки
Очаг поражения в анальной области обычно представляет собой рецидивирующую трещину, что нередко является поводом для диагностических ошибок. Такие больные с ошибочным диагнозом "трещина заднего прохода" попадают к хирургам. Зудящая форма герпеса ануса и герпетическое поражение геморроидальных узлов, также трудны для диагностики.
Поражение анальной области может возникнуть первично как самостоятельное заболевание или вторично – в результате затекания отделяемого влагалища и мацерации слизистой оболочки ануса при наличии у пациентки герпетического кольпита, сопровождающегося обильной экссудацией.
При поражении сфинктера и слизистой оболочки ампулы прямой кишки (герпетический проктит) больных беспокоят зуд, чувство жжения и болезненность в очаге поражения, возникают мелкие эрозии в виде поверхностных трещин с фиксированной локализацией, кровоточащие при дефекации. При ректоскопии определяется катаральное воспаление, иногда эрозии.
Герпес внутренних гениталий - субклиническая и бессимптомная формы.
Для субклинической формы герпеса внутренних гениталий (влагалища, матки, яичников и т.д.) типично отсутствие у пациентки жалоб, иногда имеются указания на периодически появляющиеся необильные слизистые выделения из влагалища. При гинекологическом осмотре симптомы воспаления не выявляются. При динамическом лабораторном исследовании мазков отделяемого канала шейки матки, влагалища и уретры периодически выявляется повышенное количество лейкоцитов (до 200–250 и выше в поле зрения), свидетельствующее о наличии воспалительного процесса. При вирусологическом исследовании мазков методом иммунофлюоресценции в лейкоцитах определяется антиген ВПГ.
Бессимптомная форма герпеса внутренних гениталий характеризуется отсутствием у больных каких-либо жалоб на половую сферу, объективных клинических данных, подтверждающих воспаление. При лабораторном исследовании отделяемого урогенитального тракта выделяется ВПГ, в то время как в мазках признаков воспаления (лейкоцитоза) нет. Бессимптомная форма герпеса внутренних гениталий выявляется у 20–40% женщин, страдающих РГГ ягодицы и бедра. Это важное обстоятельство необходимо учитывать при планировании беременности у женщин с этой формой РГГ в связи с существующей вероятностью развития во время беременности осложнений ВПГ-инфекции.
Согласно данным литературы, у 83,6% женщин, страдающих не поддающимися терапии кольпитами и лейкоплакией шейки матки, ВПГ является одним из факторов заболевания. Доказано, что ВПГ может быть причиной развития эндометрита и сальпингоофорита.
Герпетический вульвовагинит
У женщин часто встречаются герпетический вульвовагинит, особенностью течения которого является нередкое присоединение отека пораженной области. Вирус герпеса могут изолированно поражать вульву и влагалище. Заражение происходит от больных. Герпетический вульвовагинит проявляется мелкими пузырьками на гиперемированной вульве. Пузырьки содержат прозрачную, а при присоединении вторичной инфекции — гнойную жидкость. Через 5—7 дней пузырьки вскрываются с образованием эрозий и язвочек, которые покрываются струпом. В начале заболевания выражены жжение, боли и зуд в области вульвы. Общие симптомы включают головную боль, озноб, повышение температуры тела.
Генитальный герпес во время беременности
Заболевание ВПГ женщин во время беременности может явиться причиной гибели плода, мертворождения, преждевременных родов. Герпесвирусы вызывают до 30% спонтанных абортов на ранних сроках беременности и свыше 50% поздних выкидышей, занимают второе место после вируса краснухи по тератогенности (развитие уродств плода).
Тяжелейшие формы неонатального герпеса развиваются при инфицировании новорожденного вирусом простого герпеса в родах. При первичном ГГ у матери инфицируется от 30% до 80% детей, при рецидивирующем герпесе – 3–5%. Инфицирование плода во время родоразрешения, если у матери в конце беременности имели место герпетические высыпания, происходит у 50% женщин, больных РГГ; при этом у 60–80% инфицированных детей развивается энцефалит.
Герпес менструальный
Менструальный герпес — это генитальный герпес (ГГ) с монотонным типом рецидивирования и тяжелым течением, характеризующийся ежемесячными обострениями инфекционного процесса до, во время или после менструации. Такое течение заболевания может стать для женщины сильнейшим психотравмирующим фактором, ограничивающим ее социальную активность и снижающим качество жизни.
Этот вариант ГИ является сложным для лечения. Поэтому разработка адекватных и эффективных способов лечения и профилактики рецидивов у больных с данными формами ГГ остается актуальной. Европейские стандарты лечения пациенток предусматривают длительную (годами) супрессивную терапию противовирусными препаратами , что не исключает повторного рецидирования ГГ и бессимптомного вирусовыделения, появления побочных эффектов и резистентности вирусов герпеса к лекарственной терапии.
Герпетические заболевания органов мочеполовой системы все чаще наблюдаются у пациентов с микст-инфекцией. Генитальный герпес в 80% случаев протекает в виде микробной ассоциации, в сочетании с хламидиями, уреа- и микоплазмой, стрепто-, стафилококками, грибковой флорой. Не исключено сочетанное поражение гениталий ВПГ, гонококком, бледной трепонемой, другими вирусами, передающимися при половом контакте. При выявлении бактериально-вирусных ассоциаций необходимо учитывать синергическое действие (взаимодействие) различных возбудителей в развитии воспалительного процесса гениталий
Вследствие сочетания инфекций и общего влияния возбудителей на организм развивается более тяжелое, иногда с атипической симптоматикой, заболевание. В этом случае необходимо тщательного обследовать пациентов для постановки точного диагноза и исключения ВИЧ-инфекции.
Рецидивирующий генитальный герпес также чаще протекает не как самостоятельное заболевание, а сопровождает другую патологию мочеполовой системы. Накапливаются данные о том, что гонококковая, хламидийная, трихомонадная инфекции могут активизировать герпетическую инфекцию, предопределяя возникновение рецидивов герпетического заболевания гениталий.
Иммунодефицитные состояния
ВПГ угнетает иммунную систему (иммуносупрессия). Клинически это выражается в частых простудах, сниженной работоспособности, быстрой утомляемости, низкой устойчивости к стрессам, апатии. Температура может повышаться до субфебрильной. По мере прогрессирования иммуносупрессии увеличивается частота возникновения рецидивов герпетической инфекции, увеличивается распространенность очагов поражения кожи и слизистой оболочки.
Психоэмоциональные осложнения

При длительно протекающей, часто рецидивирующей герпетической инфекции для больных характерно развитие психоэмоциональных нарушений, в большой степени связанных с астеническим синдромом. У некоторой части больных герпетическая инфекция вызывает диагностически значимую личностную дисгармонию, с риском развития тяжелых невротических и депрессивных состояний.
Генитальный герпес (ГГ) у женщин сопряжен с большей степенью психоэмоциональных осложнений, чем у мужчин. Так, у 48% женщин с генитальным герпесом специализированное обследование позволило установить отклонение личности, а у 11% – неврастенические, депрессивные синдромы.
Часто рецидивирующее и длительное течение генитального герпеса вызывает тяжелые физические страдания. Бичом для женщин и мужчин являются генитальный герпес с яркими высыпаниями, жжением, выделениями различного характера из половых органов.
Еще одним психологическим аспектом проблемы герпеса является социальная, т.к. инфекция нарушает нормальную половую жизнь пациентов, способствует возникновению фобий, порождает страх социальной оценки и приводит к семейным неурядицам.
ГГ как причина рака. Онкогенное влияние герпетической инфекции.
Важное значение вируса простого герпеса (ВПГ) в патологии человека – это его возможная ассоциация с некоторыми формами рака у людей.
Следует отметить возможную роль ВПГ-2 (в ассоциации с паповавирусами, ЦМВ, хламидиями и микоплазмами) в развитии опухолевых процессов у человека, в частности рака шейки матки и рака предстательной железы. Считают, что в этом случае ВПГ-2 может поддерживать канцерогенез, инициируя развитие дисплазии и поддерживая ее в состоянии стабилизации.
Накапливается число клинико-экспериментальных наблюдений, подтверждающих этиологическую роль биотипов ВПГ в развитии дисплазии, карциномы in situ, рака шейки матки у женщин. Так, при эрозии и дисплазии шейки матки, ВПГ-2 выявляется в 27,2% случаев непосредственно в соскобах со слизистой цервикального канала и сопровождается повышением титра специфических иммуноглобулинов в крови до диагностических уровней.
Герпетическая инфекция (ГИ) с большей вероятностью может приводить к онкологическому заболеванию при смешанных формах инфекции. Например при наличии ассоциации ВПГ-2 с вирусами папилломы человека регистрируется значительно более высокая степень риска развития онкопоражений, когда происходит направленная индукция процессов малигнизации эпителиальных клеток.
Хроническая ГИ повышает риск развития онкозаболеваний при воздействии химических канцерогенов и мутагенов. Это происходит потому, что геномы клеток, хронически инфицированных ВПГ-2, становятся уязвимыми к действию химических канцерогенов. Как пример — курение увеличивает риск развития рака шейки матки у женщин с хронической герпетической инфекцией эндоцервикса.
Еще одним фактором в инициации и поддержании механизмов канцерогенеза у человека, может стать иммуносупрессивный эффект хронической рецидивирующей ГИ. Из-за подавления ряда звеньев клеточного (противоопухолевого) иммунитета развивается ВПГ-индуцированный иммунодефицит. Он может послужить благоприятным фоном для развития неопластического процесса из единичных мутировавших (стареющих) потенциально раковых клеток.
ГГ и ВИЧ-инфекция
Генитальный герпес способствует распространению ВИЧ-инфекции, а также других инфекций, передающихся половым путем (эпидемиологический синергизм).
• в кожных герпетических изъязвлениях содержится большое количество CD4+ лимфоцитов, которые являются идеальной мишенью для ВИЧ, вследствие чего даже при очень низкой концентрации ВИЧ возрастает вероятность инфицирования полового партнера;
• герпесвирусы способствуют экспрессии генов ВИЧ, что создает дополнительные условия для эффективной репродукции вируса
Вирусы герпеса могут активировать ВИЧ, находящийся в стадии про-вируса, и являются кофактором прогрессирования ВИЧ-инфекции и СПИДа. В этой связи герпетическая инфекция является одним из важных СПИД-индикаторных заболеваний.
Атеросклероз
Ассоциация атеросклероза с вирусной инфекцией была экспериментально обоснована в 70-е годы прошлого века. За последние 30 лет накопилось достаточно много экспериментальных и клинических данных, свидетельствующих об участии в патогенезе атеросклероза некоторых вирусов, среди которых вирус простого герпеса.
Тенденцию к ускорению процесса атеросклероза в последние годы связывают именно с огромным инфицированием ВПГ. Находит все большее подтверждение вирусная гипотеза происхождения атеросклероза, в основе которой лежит предположение об индуцирующей роли вирусов герпеса в развитии заболевания.
ВПГ, возможно, в ассоциации с цитомегаловирусом, играет значительную роль в индукции атеросклероза. Наиболее вероятной причиной изменений в атеросклеротической бляшке больных атеросклерозом является вирусное инфицирование, так как вирусы (в большинстве случаев ВПГ, ЦМВ) выявляются и в сосудистом эндотелии, и в гладкомышечных клетках сосудистой стенки. Данный факт также предполагает вероятность трансформации гладкомышечных клеток под действием ВПГ.
При аутопсии людей, погибших от случайных причин, в различных слоях артериальной стенки, в том числе эндотелии и гладкомышечных клетках, выявлены иммунологические маркёры цитомегаловируса (ЦМВ) и вируса простого герпеса (ВПГ). У больных атеросклерозом вирус простого герпеса в 90% случаях явился инфекционным агентом, причем, частота и патогенность ВПГ-1 несколько выше, чем ВПГ-2.
В атеросклеротических бляшках возможно присутствие сразу нескольких патогенов: например, ЦМВ, ВПГ-1 и других патогенных штаммов. Более того, в ряде исследований была продемонстрирована взаимосвязь между числом различных патогенов, которыми инфицирован индивидуум, и 1) распространенностью атеросклеротического процесса, 2) риском смерти вследствие сосудистых катастроф (в т.ч. и инсультов),
Вирус герпеса и болезни сердца.

Герпесвирусная инфекция повышает риск развития осложнений при сердечно-сосудистых заболеваниях, например влияет на особенности клинического течения ишемической болезни сердца (ИБС). Более тяжелое течение ИБС ассоциировано с инфицированием двумя типами вируса простого герпеса (более выраженные и продолжительные ангинозные боли, плохо купирующиеся приемом нитроглицерина или ингаляций нитроминта, одышка и чувство нехватки воздуха). При инфицировании только I типом вируса простого герпеса, в исследованиях отмечено более легкое течение ИБС.
Герпесвирусная инфекция в худшую сторону влияет и на клиническое течение инфаркта миокарда, вызывая осложнения. При инфаркте миокарда, у пациентов, имеющих высокие титры IgM и IgG к ВПГ-1 и ВПГ-2, на фоне активации хронической герпесвирусной инфекции, значительно повышается риск развитии острой сердечно-сосудистой недостаточности (в том числе отеков легких) и нарушений сердечного ритма в виде жизнеугрожающих аритмий.
Цитомегаловирус является представителем семейства герпесвирусов. Если этот вирус попадает в организм человека, то он остается там пожизненно. По различным исследованиям, инфицированность цитомегаловирусом составляет около 40% населения земного шара. При этом большая доля заражений приходится на младенческий и детский возраст.
ПУТИ ЗАРАЖЕНИЯ ЦИТОМЕГАЛОВИРУСОМ
Цитомегаловирус не является особо заразным, поэтому инфицирование происходит чаще всего в результате длительных и тесных контактов с вирусоносителем: через слюну (при поцелуях), через биологические жидкости при половом контакте, при переливании крови, от матери к ребенку во время беременности, родов и лактации.
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ ПРИ ЗАРАЖЕНИИ ЦИТОМЕГАЛОВИРУСОМ
Инкубационный период в 20-60 дней обычно завершается стартом острой фазы болезни, продолжающейся от 2 до 6 недель. Для цитомегаловируса характерны признаки общей интоксикации: повышение температуры, озноб, головные и мышечные боли, слабость. После окончания острой фазы в течение многих недель может развиваться состояние слабости с поражением внутренних органов.
Обычно активизация цитомегаловируса проявляется в трех основных формах:
ДИАГНОСТИКА ЦИТОМЕГАЛОВИРУСА
Диагностика цитомегаловируса основана, как правило, на предположениях о наличии вируса при трудности лечения клинических проявлений обычными способами, после чего делаются биохимические анализы: ПЦР или посев клеток на культуре. Обычно результаты этих исследований дают ответ на вопросы о том, есть ли цитомегаловирус в крови, насколько он активен и эффективна ли терапия.
ЛЕЧЕНИЕ ЦИТОМЕГАЛОВИРУСНОЙ ИНФЕКЦИИ
Лечение цитомегаловируса проводится в стандартной для большинства вирусных инфекций последовательности действий – иммуномодулирующее (укрепление защитных сил организма) воздействие, а также комплекс противовирусных терапевтических мероприятий.
Сам цитомегаловирус, попавший в кровь, излечить полностью невозможно, но отсутствие его в биологических жидкостях говорит о его переходе в безопасную латентную фазу, которая, при хорошем иммунном статусе, может всегда такой и оставаться.
ЦИТОМЕГАЛОВИРУС И БЕРЕМЕННОСТЬ
Первичное заражение матери цитомегаловирусом является достаточно опасным для плода, т.к. существует вероятность поражения ЦНС ребенка и различных отклонений в его развитии. По статистике, заражение плода происходит в 30% случаев, а отклонения в развитии наблюдаются только в 15% случаев, поэтому обычно прерывания беременности не рекомендуют.
При обострении уже имеющейся инфекции вред для ребенка гораздо меньший, т.к. у матери уже присутствуют антитела, ослабляющие вирус и препятствующие проникновению через плаценту.
Важным фактором также является и срок беременности: более опасны в плане инфицирования более ранние сроки – в этот период активизация цитомегаловируса может привести к выкидышу и серьезным нарушениям в развитии. А вот после 4 месяцев беременности вреда фактически не наблюдается, но инфицирование может произойти при родах, что, к счастью, не так опасно, как внутриутробное заражение.
ПРОФИЛАКТИКА ОСЛОЖНЕНИЙ БЕРЕМЕННОСТИ
Так что при планировании беременности всегда очень важно пройти полное обследование на наличие бактерий и вирусов и провести их своевременное лечение заранее. Вы всегда можете сделать это у нас – в Клинике Доктора Назимовой, где можете быть уверены в качестве диагностики и лечения.
Читайте также:

