Цитомегаловирусная инфекция у детей клинические рекомендации инфекционистов
Обновлено: 10.05.2024
Клиническая диагностика ЦМВИ представляет большие трудности и окончательный диагноз не может быть установлен без лабораторного подтверждения. Поиск маркеров ЦМВИ оправдан у новорожденных, если у них обнаруживаются признаки, которые возможны при врожденной ЦМВИ. К таким признакам можно отнести недоношенность, долго сохраняющуюся желтуху, кровоизлияния на коже, гепатолиенальный синдром, неврологические отклонения и др. Поводом для обследования женщин детородного возраста и беременных является отягощенный акушерский анамнез и осложнения беременности, в частности, выявленные с помощью ультразвукового исследования.
В настоящее время методов лабораторной диагностики ЦМВИ довольно много, но значимость их неодинакова. Наиболее клинически значимыми являются вирусологические методы, имеющие в виду выделение вируса или детекцию его белковых антигенов в культуре клеток, зараженных материалами от больных. Вирусологические методы сочетают с иммунологическими методами, целью которых является определение специфических антител различных классов.
Материалом для лабораторного анализа у новорожденных могут служить кровь из пуповины, венозная кровь, моча, слюна, спинномозговая жидкость; у беременных женщин — кровь, моча, соскоб с канала шейки матки; у родильниц дополнительно обследуется грудное молоко.
Для выделения вируса используется клеточная культура из фибробластов легких эмбриона человека. Однако определение вируса в клеточной культуре по цитопатическому эффекту — длительный процесс (в традиционном исполнении 2—3 недели). Поэтому в последние годы для определения присутствия вируса в клеточной культуре применяют методы, направленные на обнаружение ранних (или предранних) вирусных антигенов. Последние можно выявлять через 24—48 часов от начала культивирования методом непрямой иммунофлюоресценции или иммунопероксидазным методом.
В последнее время широкое распространение получают моле-кулярно-биологические методы, направленные на определение генома вируса. Особенно часто используется полимеразная цепная реакция (ПЦР), как высоко специфический и чувствительный метод, но и при применении этого метода возможны ложноположительные результаты. К тому же надо иметь в виду, что ПЦР, как метод высокочувствительный, выявляет не только ДНК активно реплицирующегося вируса, но и ДНК вируса, пребывающего в фазе латенции. Поэтому метод ПЦР следует, как правило, использовать в дополнение к другим методам лабораторной диагностики ЦМВИ.
С целью обнаружения антител к ЦМВ классов IgM и IgG используют иммуноферментный анализ (ИФА), метод флюоресцирующих антител (МИФ), иммуноблот (ИБ) и другие. Важное диагностическое значение может иметь исследование в динамике парных сывороток с нарастанием титра антител не менее чем в 4 раза.
Следует отметить, что существующие методы диагностики могут иметь разную ценность в зависимости от целей исследования. Например, обнаружение ДНК ЦМВ методом ПЦР в амниотической жидкости, где ее вообще не должно быть, означает инфицирование плода. В то время как выделение ДНК ЦМВ из секрета шейки матки не позволяет оценить активность инфекции.
Выделение вируса из мочи используют для диагностики врожденной и перинатальной инфекции и этот метод признается наиболее эффективным в этих целях.
В настоящее время еще нет четко установившихся взглядов относительно целесообразности широкого использования пренатальной диагностики врожденной ЦМВИ. Пренатальная диагностика ЦМВИ проводится в тех случаях, когда имеется серьезный риск развития врожденной ЦМВИ, особенно при первичной инфекции у матери. Сигналом к такому исследованию могут послужить и данные ультразвукового исследования при выявлении изменений в плаценте и плоде. Пренатальная диагностика проводится в различные сроки беременности, обычно во 2-ом триместре (16—30 недель).
Для получения материала для исследования проводят амниоцентез и кордоцентез. Исследование амниотической жидкости включает: 1) выделение вируса на клеточной культуре с детекцией вирусного антигена или цитопатического эффекта и; 2) выявление ДНК ЦМВ в ПЦР. Исследование крови направлено на: 1) выделение вируса на клеточной культуре и; 2) определение IgM анти-ЦМВ.
Наиболее эффективным для диагностики врожденной ЦМВ при исследовании амниотической жидкости являются прямые методы определения возбудителя — вирусологический и метод ферментной амплификации.
Исследование крови плода является менее результативным, чем исследование амниотической жидкости. Выделить вирус из крови пупочного канатика удается не всегда. Специфические иммуноглобулины IgM удается обнаружить не более чем в 50% случаев доказанной ЦМВИ. К тому же следует помнить, что образование специфических антител IgM анти-ЦМВ начинается с начала второй половины беременности. Определять IgM анти-ЦМВ в более ранние сроки не имеет смысла.
По-видимому, пренатальная диагностика ЦМВИ может найти ограниченное применение. Метод нельзя считать полностью безопасным, и он не позволяет диагностировать врожденную ЦМВИ во всех случаях (эффективность диагностики 75%). Не исключается возможность контаминации материалов, полученных у плода, материнской кровью. Занос инфекции в плод при проведении процедуры также возможен.
Большое значение следует придавать правильной интерпретации полученных результатов лабораторных исследований. Наиболее частым маркером, выявляемым при обследовании женщин, являются специфические иммуноглобулины класса IgG. Если они выявляются в качестве единственного маркера, то это свидетельствует, с одной стороны, об инфицированности цитомегаловирусом, или, иными словами, IgG анти-ЦМВ в этой ситуации становятся индикатором латентной инфекции. С другой стороны, присутствие IgG анти-ЦМВ указывает на наличие гуморального иммунитета к этой инфекции. Обнаружение IgG анти-ЦМВ у детей первого полугодия жизни при отсутствии других маркеров этой инфекции будет указывать на их материнское происхождение.
Нарастание титра специфических антител IgG в динамике в 4 и более раз может свидетельствовать о первичной ЦМВИ, ее реактивации или реинфекции. Труднее оценить значение высоты титра IgG анти-ЦМВ при его изолированном рассмотрении. Если имеется высокий титр специфических IgG при отсутствии других маркеров, то это может указывать на состоявшуюся антигенную стимуляцию, потому как в отсутствие антигенной стимуляции титр специфических антител класса IgG постепенно падает, иногда до столь низкого уровня, что при использовании недостаточно чувствительных тестов они вообще могут не выявляться. Одновременное выявление в сыворотке крови беременных специфических антител классов IgM и IgG указывает на реактивацию ЦМВИ.
Признается, что определение анти-ЦМВ класса IgM — это тест на продуктивную ЦМВИ. Многие исследователи рассматривают IgM анти-ЦМВ как фактор риска по развитию фетальной инфекции, что подтверждается и нашими данными.
Вместе с тем, определение анти-ЦМВ класса IgM, несмотря на широкое распространение, не является безупречным лабораторным методом диагностики продуктивной ЦМВИ. Тест на IgM анти-ЦМВ может давать ложноположительные результаты в силу перекрестных реакций с другими герпесвирусами, а также ложнонегативные результаты, связанные с недостаточной чувствительностью метода (чувствительность не более 75%).
Помимо специфических лабораторных тестов, направленных на верификацию ЦМВ, применяются и другие методы исследования, имеющие целью оценить состояние матери, плода, новорожденного. Эти методы включают:
- клинический анализ крови и мочи;
- биохимическое исследование крови;
- определение иммунного статуса;
- ультразвуковое исследование плода. Важное значение имеет ультразвуковая диагностика, с помощью которой выявляются осложнения беременности и патология плода. И при решении вопроса о сохранении беременности следует учитывать не только результаты лабораторных тестов на маркеры ЦМВИ, но и результаты, полученные другими методами исследования.
За беременными из группы риска проводится систематический вирусологический мониторинг на ЦМВИ с целью своевременного выявления ее активизации. Целесообразные сроки его проведения: 8—12 недель, 23—25 недель, 33—35 недель.
Ультразвуковое исследование плода и плаценты проводится в сроки беременности: до 15 недель, 20—24 недели, 33—35 недель.
Цитомегаловирусная инфекция (синонимы: цитомегалия, вирусная болезнь слюнных желез, инклюзионная цитомегалия, болезнь с включениями; salivarygland virus disease – англ.) хроническая антропонозная болезнь вирусной этиологии, характеризующаяся многообразием форм патологического процесса от латентной инфекции до клинически выраженного генерализованного заболевания [1,2].
Пользователи протокола: терапевты, врачи общей практики, инфекционисты, неврологи, дерматовенерологи, акушер-гинекологи, анестезиологи-реаниматологи, организаторы здравоохранения.
Класс I – польза и эффективность диагностического метода или лечебного воздействия доказана и и/или общепризнаны
Класс III – имеющиеся данные или общее мнение свидетельствует о том, что лечение неполезно/ неэффективно и в некоторых случаях может быть вредным
Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+).
Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию.
Классификация
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Минимальный перечень обследования, который необходимо провести при направлении на плановую госпитализацию: согласно внутреннему регламенту стационара с учетом действующего приказа уполномоченного органа в области здравоохранения.
• определение ДНК ЦМВ в ликворе, плевральной жидкости, отделяемого цервикального канала и уретры и т.д. в зависимости от органной патологии методом ПЦР;
• биохимическое исследование крови (билирубин и фракции, АЛТ, АСТ, тимоловая проба, амилаза, глюкоза);
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: не проводятся.
Жалобы: зависят от клинической формы инфекции, путей заражения и степени выраженности иммуносупрессии.
• отягощенный гинекологический анамнез (цервицит, эктопия шейки матки, хронический эндометрит и т.д.);
Физикальное обследование: зависит от клинической формы инфекции, путей заражения и степени выраженности иммуносупрессии.
У ВИЧ-инфицированных в 3 и 4 стадии: клиника манифестных форм с поражением легких, ЦНС, глаз (ретинит), ЖКТ, печени.
Иммунограмма: снижение CD4+, CD8+, снижение CD4\CD8.
• рентгенография органов грудной клетки (интерстициальная пневмония, фиброзирующий бронхиолит и альвеолит);
• спинномозговая пункция (лимфоцитарный плеоцитоз, повышение белка в ликворе при подозрении на менингит, энцефалит);
• офтальмоскопия (на сетчатке по периферии глазного дна очаги белого цвета с геморрагиями по ходу ретинальных сосудов, при прогрессировании инфильтрация с зонами атрофии и очагами кровоизлияний).
Дифференциальный диагноз
Алгоритм дифференциальной диагностики при цитомегаловирусной болезни


Лечение
• У иммунокомпроментированных – подавление репликации вируса, купирование клинических проявлений, профилактика осложнений.
Диета: стол № 15 с коррекцией в зависимости от клинической формы.
• интерферон рекомбинантный альфа 2 b 500 000 МЕ или 1 000 000 МЕ (виферон) по 1 свече 2 раза в сутки №10, далее 500 000 МЕ по 1 свече 2 раза в сутки через 12 часов 2-3 раза в неделю 1–12 месяцев в зависимости от клинической формы и течения болезни.
• меглюмина акридонацетат в таблетках: по 0,45 г (3 табл.) на прием 1 раз в сутки per os по схеме 1,2,4,6,8,11,14,17,21,23 дни., в инъекциях 12,5% - 2 мл в/м, 1 раз №10.
Латентная ЦМВИ: лечение не проводится.
• интерферон рекомбинантный альфа 2 b 500 000 МЕ или 1 000 000 МЕ по 1 свече 2 раза в сутки №10, далее 500 000 МЕ по 1 свече 2 раза 3 раза в неделю 1–12 месяцев;
• Панавир 0,004% раствор 5 мл в/в медленно №5 по схеме три инъекции с интервалом 48 часов, две последующие – с интервалом 72 часа и суппозитории ректальные Панавир 200 мкг, по 1 свече на ночь 3-х кратно в течении 1-ой недели с интервалом 48 часов и 2-х кратно в течении 2-ой недели с интервалом 72 часа. Курс лечения 11 дней.
• Валганцикловир 900 мг в сутки или Ганцикловир 5 мг/кг/сутки в течение месяца, перенёсшим ЦМВ – ретинит на фоне ВААРТ до повышения CD4 – лимфоцитов более 100 кл/мкл, сохраняющегося не менее 3 месяцев. Поддерживающий курс у этих больных при других манифестных формах ЦМВИ должен быть не менее одного месяца.
С целью дезинтоксикационной терапии: обильное питье из расчета 20-40 мл/кг массы тела, в тяжелых случаях – инфузионная терапия: кристаллоиды (физиологический раствор, ацесоль, лактосоль, ди- и трисоль и т.п.) и коллоиды (реополиглюкин) в соотношении 3:1 - 2:1;
С десенсибилизирующей, противотёчной, противовоспалительной целью при генерализованной ЦМВИ с поражением ЦНС: кортикостероидные препараты: преднизолон 2-5 мг\кг в сутки;
Антибактериальная терапия при наслоении бактериальной инфекции рекомендуется монотерапия одно нижеследующих препаратов:
С иммуномодулирующей и противовирусной целью рекомендуется монотерапия одно нижеследующих препаратов:
• интерферон рекомбинантный альфа 2b – суппозитории 150 000 МЕ, 500 000 МЕ, 1 000 000 МЕ, 3 000 000 МЕ;
• иммуноглобулин человека антицитомегаловирусный – раствор 500 ЕД (10мл), 1000 ЕД (20мл), 2500 ЕД (50мл);
• меглюмина акридонацетат в таблетках: по 0,45 г (3 табл.) на прием 1 раз в сутки per os по схеме 1,2,4,6,8,11,14,17,21,23 дни., в инъекциях 12,5% - 2 мл в/м, 1 раз №10.
• панавир – раствор для иньекций в ампулах по 5 мл с концентрацией 0,04 мг/м; суппозитории ректальные;
• Рингер раствор для инфузий, 200 мл и 400мл;
С профилактической целью – ганциклавир (реципиентам костного мозга, сердца, почек и печени; больным, получающим цитостатические препараты, беременным).
Препараты (действующие вещества), применяющиеся при лечении
| Валганцикловир (Valganciclovir) |
| Ганцикловир (Ganciclovir) |
| Декстран (Dextran) |
| Иммуноглобулин человека против цитомегаловируса (Immunoglobulin against human cytomegalovirus) |
| Интерферон альфа 2b (Interferon alfa-2b) |
| Калия хлорид (Potassium chloride) |
| Кальция хлорид (Calcium chloride) |
| Меглюмин (Meglumine) |
| Натрия хлорид (Sodium chloride) |
| Очищенный экстракт побегов растения Solanum tuberosum (The purified extract of plant shoots Solanum tuberosum) |
| Преднизолон (Prednisolone) |
| Цефепим (Cefepime) |
| Цефтриаксон (Ceftriaxone) |
| Ципрофлоксацин (Ciprofloxacin) |
Госпитализация
Показания для экстренной госпитализации: больные, в. т.ч. беременные с тяжелыми генерализованными формами цитомегаловирусной болезни.
Показания для плановой госпитализации: больные, в т.ч. беременные (в сроки до 30 недель беременности в инфекционный стационар, свыше 30 недель в родильные дома, перинатальный центр) с клинически выраженными формами ЦМВИ.
Информация
Источники и литература
Информация
Указание условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Цитомегаловирусная инфекция – инфекционное заболевание, обусловленное высокораспространенным вирусом герпеса 5-го типа, характеризующаяся политропностью поражений органов и систем, сложными иммунологическими реакциями со стороны макроорганизма, с формиров
Резюме. Цитомегаловирусная инфекция – инфекционное заболевание, обусловленное высокораспространенным вирусом герпеса 5-го типа, характеризующаяся политропностью поражений органов и систем, сложными иммунологическими реакциями со стороны макроорганизма, с формированием длительной, нередко пожизненной персистенции вируса в организме. В настоящее время отмечается рост заболеваемости цитомегаловирусной инфекцией во всех странах мира. Согласно эпидемиологическим данным, большинство людей в течение своей жизни инфицируются цитомегаловирусом. Так, в Европе и США серопозитивны по цитомегаловирусу 40-60% взрослого населения, в развивающихся странах распространенность цитомегаловирусой инфекции еще более высока – 80% детей и почти все взрослое население. Среди беременных специфические антитела к цитомегаловирусу определяются от 40% в развитых до 100% в развивающихся странах. Частота внутриутробной передачи цитомегаловируса колеблется в пределах 0,2-2,2%, в среднем составляя 1% в популяции. Многообразие клинических форм, от субклинического течения до развития тяжелых жизнеугрожающих форм у особых, иммунокомпроментированных групп пациентов, делает цитомегаловирусную инфекцию сложной и актуальной проблемой современной медицины. Одним из основных органов-мишеней для цитомегаловируса является гепатобилиарная система. Малое число наблюдений, ограниченные данные о патогенезе развития поражения печени при цитомегаловирусной инфекции у детей, а также отсутствие единых регламентирующих документов по диагностике и лечению указанных состояний в педиатрической практике послужили причиной для написания данной статьи. В работе приведены актуальные данные о патогенезе, клинической картине, диагностике, а также подходах к терапии цитомегаловирусного гепатита у детей.
Цитомегаловирусная инфекция (ЦМВИ) – инфекционное заболевание, вызванное герпесвирусом 5-го типа (Cytomegalovirus). Характеризуется полиморфной клинической симптоматикой и специфичной морфологической картиной с присутствием цитомегалических клеток на фоне лимфогистиоцитарных инфильтратов. В настоящее время ЦМВИ является одной из наиболее актуальных вирусных проблем инфекционной патологии, что обусловлено ее широким распространением, многообразием путей передачи, чрезвычайно большим спектром клинических проявлений, а также частым развитием тяжелых форм инфекции в определенных группах пациентов. Европейским регионарным бюро Всемирной организации здравоохранения (ВОЗ) ЦМВИ отнесена к числу болезней, которые определяют будущее инфекционной патологии. Многие эксперты считают необходимым принципиально изменить отношение к цитомегаловирусу (ЦМВ) и усилить борьбу с его распространением [2, 3].
Общие сведения
У людей с эффективным иммунитетом ЦМВИ в большинстве случаев характеризуется латентным течением. Клиническая манифестация заболевания с возможным развитием крайне тяжелых форм происходит относительно редко и зачастую у пациентов с приобретенными или врожденными иммунодефицитными состояниями (ИДС) [4]. В настоящее время, учитывая развитие биомедицинских технологий, в частности разработку и широкое использование цитостатических препаратов, а также высокоактивной биологической терапии, перманентный рост заболеваемости ВИЧ-инфекцией, рост онкопатологии и числа тяжелых аутоиммунных патологий, актуальность ЦМВИ не вызывает сомнений. Это одна из наиболее частых причин самопроизвольных выкидышей, преждевременных родов, врожденных пороков развития и фетопатий [4, 5].
Сегодня отмечается рост заболеваемости ЦМВИ во всех странах мира, что связано как с улучшением качества диагностики, так и с указанными выше причинами [5]. Согласно эпидемиологическим данным, большинство людей в течение жизни инфицируются ЦМВ. Так, в Европе и США 40-60% взрослого населения серопозитивны по ЦМВ, в развивающихся странах распространенность ЦМВИ еще выше – 80% детей и почти все взрослое население. Среди беременных специфические антитела к ЦМВ определяются от 40% в развитых до 100% в развивающихся странах. Частота внутриутробной передачи ЦМВ колеблется в пределах 0,2-2,2%, в среднем составляя 1% в популяции [2].
Учитывая, что ЦМВ характеризуется политропностью, клиническая картина может включать различные синдромы, однако одним из наиболее частых проявлений является синдром поражения печени. Наиболее распространенным заболеванием печени, связанным с ЦМВ, является острый гепатит, тяжесть которого варьирует от бессимптомного повышения аланиновой аминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ), а также самоограничивающегося гепатита до тяжелого поражения печени с развитием острой печеночной недостаточности (ОПчН). Кроме того, могут наблюдаться и нетипичные проявления, такие как холестатические формы острого гепатита, развитие хронического гепатита, а также вероятный дебют аутоиммунного гепатита [6, 7].
В зависимости от времени инфицирования ЦМВ выделяют врожденный и приобретенный гепатит. Поражение печени – характерный признак врожденной ЦМВ-инфекции – встречается у 40-63,3% больных [8, 9]. Врожденный ЦМВ-гепатит (ЦМВГ) всегда развивается как первично-хронический процесс. Поражение печени часто сочетается с другими пороками развития: атрезией желчевыводящих путей, поражением нервной системы, легких, почек и др. [10, 11]. В этиологической структуре неонатальных гепатитов ЦМВ-этиология составляет до 40% [12]. К концу первого года жизни поражение печени при врожденной ЦМВИ отмечается редко – примерно в 2% случаев [13]. Приобретенный ЦМВГ может протекать в форме острой инфекции в рамках мононуклеозоподобного синдрома, а также как самостоятельное заболевание, заканчиваясь выздоровлением с полным восстановлением функционального состояния печени или первично-хроническим процессом 12.
Эпидемиология
Патогенез
ЦМВИ может протекать в виде первичной инфекции у ранее неинфицированных (серонегативных) пациентов, реинфекции или реактивации у инфицированных (серопозитивных) людей; может вызывать острое, латентное и хроническое течение врожденных или приобретенных форм болезни. При острой ЦМВИ могут поражаться практически все типы клеток человеческого организма – эндотелиальные, эпителиальные, гладкомышечные, фибробласты, нейроны, гепатоциты, трофобласты, моноциты/макрофаги, дендритные клетки и многие другие, то есть вирус не имеет избирательной клеточной цели, что объясняет многообразие клинических форм поражения у различных групп пациентов [18].
Патогенез ЦМВГ до настоящего времени не до конца ясен. Традиционно считается, что ЦМВ поражает желчные протоки с развитием холестатического гепатита. Однако обнаружено, что вирус оказывает и прямое цитопатическое действие непосредственно на паренхиму печени, таким образом, ЦМВ является прямым гепатотропным агентом.
В формировании изолированного поражения гепатоцитов при ЦМВГ важную роль может играть непосредственное попадание возбудителя в кровь (парентеральный механизм инфицирования). Возбудитель сразу оказывается в системном кровотоке, откуда и попадает в паренхиму печени, где оказывает цитопатическое действие на клетки печени.
Образующиеся по ходу инфекции специфические антитела соединяются с вирусными антигенами и формируют иммунные комплексы, вовлекающие в патологический процесс другие органы и системы [21, 22].
Особое свойство ЦМВИ – способность вызывать депрессию практически всех звеньев иммунитета, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Внедрение ЦМВ приводит к иммунной перестройке в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью болезни), угнетением фагоцитарной активности и завершенности фагоцитоза [23]. Указанные изменения в иммунной системе приводят к формированию неэффективного иммунного ответа, что ухудшает течение основного патологического процесса, приводит к формированию предрасположенности к развитию вторичных вирусных и бактериальных инфекций.
Подходы к диагностике
Диагноз ЦМВГ устанавливают после тщательного анализа клинико-анамнестических данных, лабораторных и инструментальных методов обследования.
Ведущими методами этиологической диагностики являются определение антител (anti-CMV IgM, anti-CMV IgG + IEA IgG с определением авидности), а также качественная и количественная полимеразная цепная реакиця (ПЦР) для определения ДНК вируса в крови, слюне и моче и некоторых других средах [24].
Первым в сыворотке крови появляется IgM, сохраняющийся в среднем около 4 недель. В последующем возможно выявление IgG, для которых обязательно определение авидности. Данный показатель указывает на давность течения инфекционного процесса. Стоит отметить, что серодиагностика позволяет установить диагноз не во всех случаях [16]. При использовании серологических методик для диагностики острых ЦМВГ возможна перекрестная реакция с вирусом Эпштейна–Барр и гепатита Е [24].
У новорожденных серологические исследования редко информативны, особенно при манифестной клинике, так как врожденная иммунная система ко времени требуемого серологического ответа еще не эффективна. Отсутствие специфических фетальных IgM даже на фоне острой тяжелой ЦМВИ (серологическая ниша) – общая черта этого онтогенетического периода. Указанные маркеры начинают продуцироваться только через несколько месяцев [25].
Если лабораторная диагностика не дала результата, методом выбора, как и при любом неуточненном гепатите, является биопсия печени. Гистологически ЦМВГ характеризуется классическим цитопатическим действием вируса на гепатоциты, эпителий билиарного тракта, эндотелиальные клетки и клетки Купфера. Инфицированные клетки имеют как цитоплазматическое, так и ядерное увеличение с цитоплазматическими и внутриядерными включениями. Другие неспецифические изменения предполагают умеренный лобулярный гепатит, гепатоцеллюлярный некроз, портальную мононуклеарную инфильтрацию и микроабсцессы [26]. Также в некоторых случаях возможно использование иммуногистохимического исследования. Следует отметить, что биопсия печени, как перкутанная, так и трансъюгулярная, на настоящем этапе считается малоинвазивной процедурой и не несет высоких рисков, что позволяет считать ее решающим методом обследования, особенно при неуточненных поражениях печени.
Подходы к лечению
Учитывая, что в основе патогенеза ЦМВГ лежит прямое вирусное поражение, ведущее значение принадлежит этиотропной терапии. Несмотря на токсичность противовирусных анти-ЦМВ-препаратов при развитии у ребенка угрожающей жизни манифестной ЦМВИ, в частности острого ЦМВГ, применение ганцикловира и валганцикловира показано и необходимо после обязательного предварительного анализа риска и пользы. Ганцикловир впервые применен у новорожденных в конце 1980-х гг., в последующем было многократно показано, что он хорошо переносится в том числе и детьми, а также эффективен при лечении манифестных форм ЦМВИ. Препарат назначают в дозе 5-6 мг/кг два раза в сутки в среднем в течение 6 недель. Стоит отметить, что препарат обладает выраженными токсическими свойствами, поэтому применяется при наличии строгих показаний. Ограничения применения ганцикловира также связаны с необходимостью реализации для его инфузии венозного доступа с массивным кровотоком, у детей зачастую – центрального венозного катетера.
Альтернативой к инвазивному использованию ганцикловира стало введение валганцикловира, рандомизированное исследование эффективности которого завершено в 2015 г. Препарат обладает менее выраженными токсическими свойствами. Согласно международному Консенсусу 2017 г., лечение валганцикловиром показано детям со среднетяжелой врожденной ЦМВИ – 16 мг/кг 2 раза в сутки до 6 месяцев.
С патогенетической точки зрения важна гепатопротективная терапия. Наиболее доказанным в этом отношении препаратом является урсодезоксихолевая кислота, которая назначается в дозе 10 мг/кг 1 раз в сутки, курс зависит от динамики холестатического и цитолитического синдрома, а также от течения основного заболевания в целом.
Учитывая иммунные нарушения, реализующиеся при ЦМВИ и проявляющиеся депрессией различных звеньев иммунитета, а особенно интерферонопродукции, рационально применение иммуномодулирующей терапии препаратами интерферона альфа-2 бета.
При реализации тяжелых форм ЦМВГ с развитием ОПчНв терапии рационально применять стероиды (2 мг/кг по преднизолону) для купирования мезенхимально-воспалительного синдрома в паренхиме печени. При развитии печеночной энцефалопатии показаны препараты лактулозы. При отсутствии эффекта от проводимой терапии, прогрессировании ОПчН, а также при формировании хронического гепатита с признаками развития цирроза печени показано проведение трансплантации органа при соответствии характеристик кандидата на трансплантацию. В свою очередь при лечении легких или бессимптомных форм ЦМВГ используется симптоматическая терапия [16, 28].
Заключение
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
Сведения об авторах:
Information about the authors:
Цитомегаловирусный гепатит у детей: современное состояние проблемы/ Г. С. Карпович, А. Е. Шестаков, М. А. Михайленко, Ю. С. Серова
Для цитирования: Карпович Г. С., Шестаков А. Е., Михайленко М. А., Серова Ю. С. Цитомегаловирусный гепатит у детей: современное состояние проблемы // Лечащий Врач. 2022; 1 (25): 25-29. DOI: 10.51793/OS.2022.25.1.004
Теги: дети, инфекция, гепатобилиарная система, гепатит
Диагностика врожденной цитомегаловирусной инфекции головного мозга по КТ, МРТ, УЗИ
а) Терминология:
1. Сокращения:
• Врожденная цитомегаловирусная инфекция (ЦМВИ)
2. Определение:
• Врожденная инфекция, вызванная трансплацентарной передачей ЦМВ, представителя семейства герпесвирусов:
о Наиболее частый источник внутриутробной инфекции в США
б) Визуализация:
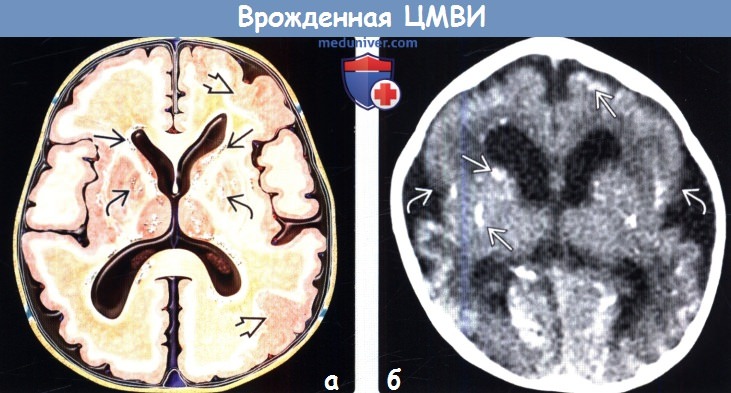
(а) На рисунке аксиального среза изображены многочисленные перивентрикулярные кальцификаты и отложения кальция в базальных ганглиях. Обратите внимание на участки кортикальной дисплазии (полимикрогирия). Расширение желудочков отражает потерю объема смежного белого вещества (БВ). Желтоватые зоны измененного БВ отражают зоны отека, демиелини-зации и/или глиоза.
(б) Бесконтрастная КТ, аксиальный срез: определяются распространенные перивентрикулярные и паренхиматозные кальцификаты. Обратите внимание на открытые сильвиевы щели и упрощенную архитектонику коры в пери-сил ьвиевых отделах. При МРТ была подтверждена полимикрогирия.
2. КТ признаки врожденной цитомегаловирусной инфекции (ЦМВИ):
• Бесконтрастная КТ:
о Внутричерепные кальцификаты (в 40-70% случаев): перивентрикулярные (субэпендимальные) (герминолитические)
о Потеря объема БВ, гиподенсные зоны в БВ, ± перивентрикулярные кисты, вентрикуломегалия
о Аномалии развития коры, извилин
о Гипоплазия мозжечка
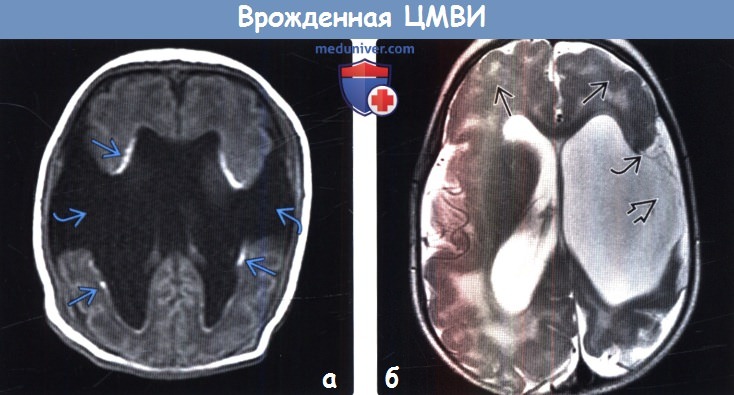
(а) МРТ, Т1 -ВИ: у младенца с врожденной ЦМВИ обнаруживается двусторонняя открытая шизэнцефалия. Обратите внимание на перивентрикулярное повышение интенсивности сигнала, что обусловлено кальцификацией.
(б) МРТ, Т2-ВИ, аксиальный срез: определяется открытая шизэнцефалия левого полушария головного мозга. Расщелина выстлана полимикрогирической корой. Обратите внимание на протяженную двустороннюю полимикрогирию лобных долей. Центральные зоны повышения сигнала от БВ отражают зоны демиелинизации или глиоза.
5. Рекомендации по визуализации:
• Лучший метод визуализации:
о УЗИ для пренатального или неонатального скрининга
о В проведении бесконтрастной КТ необходимость бывает редко
о МРТ головного мозга для комплексной оценки изменений
• Советы по протоколу исследования
о Неонатальная высокоразрешающая нейросонография:
о Бесконтрастная КТ или МРТ с использованием Т2* GRE для обнаружения слабо выраженных кальцификатов или кровоизлияний
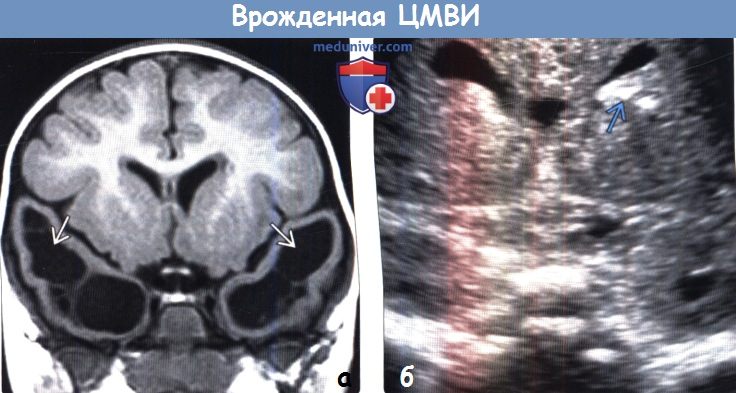
(а) МРТ, Т1-ВИ, корональный срез: у младенца с микроцералией определяются множественные перивентрикулярные полостные герминолитические кисты. Обнаружение этих кист при УЗИ, КТ или МРТ должно побуждать к рассмотрению возможности наличия врожденной ЦМВИ.
(б) Нейросонография, корональный срез: у младенца с врожденной ЦМВИ определяются перивентрикулярные гиперэхогенные очаги, соответствующие кальцификатам.
в) Дифференциальная диагностика врожденной цитомегаловирусной инфекции (ЦМВИ):
1. Врожденный лимфоцитарный хореоменингит:
• Ареновирус, переносимый грызунами: переносится дикими домовыми мышами и хомяками
• Некротизирующий эпендимит приводит к обструкции сильвиева водопровода (макроцефалия в 43% случаев, микроцефалия в 13% случаев)
• При бесконтрастной КТ может очень похоже имитировать ЦМВИ
2. Токсоплазмоз:
• Вызывается протозойными паразитами:
о факторы риска матери включают:
- Контакт с экскрементами кошек во время беременности
- Употребление в пищу сырого или неприготовленного мяса
• В 1/10 случаев частота схожа с ЦМВИ, макрокрания > микрокрания, дисплазия коры встречается реже, церебральные кальцификаты имеют стохастический характер
3. Псевдо-TORCH синдромы:
• Синдромы Берейтсера-Реардона, Айкарди-Гутьерес (плеоцитоз, ↑ α-интерферона в СМЖ)
о Аутосомно-рецессивный характер, прогрессирующая демиели-низация и дегенерация большого мозга и мозжечка
о Кальцификация базальных ганглиев и ствола мозга, перивентрикулярные кальцификаты встречаются менее часто
• Мутации гена OCLN, кодирующего окклюдин:
о Аутосомно-рецессивная микроцефалия
о Полимикрогирия с лентовидными участками субкортикальной кальцификации
г) Патология:
1. Общие характеристики врожденной цитомегаловирусной инфекции (ЦМВИ):
• Этиология:
о ЦМВИ - Повсеместно распространенный ДНК-содержащий вирус семейства герпесвирусов
о Нейротропный вирус, который реплицируется в эпендиме, герминальном матриксе, эндотелии капилляров
о Хроническая ишемия вследствие плацентита приводит к вторичной недостаточности перфузии
• Наиболее частая причина внутриутробной инфекции
• Механизмы инфекции:
о Внутриутробная инфекция:
- Первичное инфицирование матери во время беременности или повторная активация латентной инфекции у матери
о Неонатальная инфекция:
- Инфицирование при родах, передача вируса через грудное молоко или при переливании крови
3. Макроскопические и хирургические особенности:
• Микроцефалия
• Инфекция на ранних сроках гестации:
о Некроз герминальных зон, уменьшение количества глии и нейронов, потеря объема БВ
4. Микроскопия:
• Отличительный признак ЦМВИ: цитомегалия с вирусным поражением ядер и наличие цитоплазматических включений
• Фрагментарный и фокальный некроз клеток (в частности, клеток герминального матрикса)
• Воспаление сосудов и тромбоз, сосудистая и субэпендимальная дистрофическая кальцификация
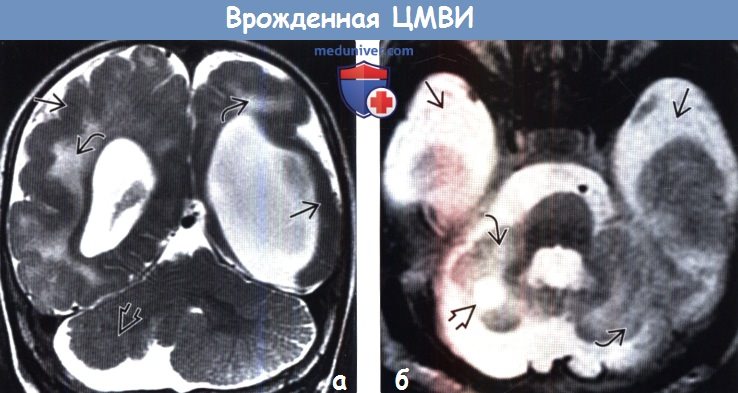
(а) МРТ, Т2-ВИ, корональный срез: определяется вентрикуломегалия, вызванная потерей объема центрального. Повышение сигнала от БВ отражает отек, глиоз или демиелинизацию. Кроме того, визуализируется полимикрогирия. Также обратите внимание на гипоплазию правого полушария мозжечка.
(б) МРТ, Т2-ВИ, аксиальный срез: у новорожденного определяется гипоплазия мозжечка и фокальное кистозное поражение мозжечка. Расширение субарахноидального пространства средней черепной ямки свидетельствует об атрофии височных долей.
д) Клиническая картина:
1. Проявления врожденной цитомегаловирусной инфекции (ЦМВИ):
• Наиболее частые признаки/симптомы:
о Клинические симптомы у большинства инфицированных новорожденных отсутствуют
о У 10% пациентов имеются системные признаки заболевания:
- Гепатоспленомегалия, петехии, хориоретинит, желтуха, задержка внутриутробного развития
о У 55% пациентов с системным заболеванием имеет место поражение ЦНС:
- Микроцефалия, судороги, гипотония или гипертония, ней-росенсорная тугоухость (НСТ)
• Клинический профиль:
о Более высокий риск вертикальной передачи вируса у женщин с серонегативной пробой
• Методы диагностики:
о Однослойная культура клеток для выявления ЦМВ (анализ мочи)
о Поздняя диагностика цитомегаловирусной ДНК методом ПЦР с использованием неонатальной карты Гатри
о Повышение в СМЖ уровня 3-2 микроглобулина, микроцефалия, нейровизуализационные признаки определяют исход
2. Демография:
• Эпидемиология:
о Поражает 1% всех новорожденных (10% из которых имеют признаки и симптомы поражения ЦНС или системного заболевания)
о 40% матерей, заразившихся инфекцией во время беременности, передают вирус плоду
3. Течение и прогноз:
• Три прогностические группы:
о Новорожденные с неврологическими проявлениями (микроцефалия, перивентрикулярное отложение Са++):
- До 95% детей имеют значительные нарушения со стороны неврологического развития
о У новорожденных только с системными проявлениями (гепатоспленомегалия, петехии, желтуха) прогноз более благоприятный, но клиническая картина при этом остается тяжелой
о Инфицированные новорожденные, не имеющие ни неврологических, ни системных проявлений, имеют наиболее благоприятный прогноз, но по-прежнему подвержены риску задержки развития, формирования моторного дефицита и НСТ
о Общая смертность - 5%
4. Лечение врожденной цитомегаловирусной инфекции (ЦМВИ):
• Терапия ганцикловиром инфицированных новорожденных может быть полезна
е) Диагностическая памятка:
1. Обратите внимание:
• Предполагайте врожденную ЦМВИ у отстающих в развитии младенцев с микроцефалией, НСТ
2. Советы по интерпретации изображений:
• Врожденный ЦМВ-энцефалит следует подозревать у ребенка при обнаружении методом МРТ следующих изменений:
о Микроцефалия, аномалии миграции, перивентрикулярные кисты, поражение БВ и гипоплазия мозжечка
• В случае, когда при бесконтрастной КТ обнаруживаются классические признаки ЦМВ-энцефалита, но результаты исследования на предмет (S)TORCH-инфекции отрицательные, следует предполагать:
о Лимфоцитарный хореоменингит (ЛХМ) и псевдо-TORCH синдромы
Читайте также:

