Цитомегаловирусные инфекции при спиде
Обновлено: 05.05.2024
Российский Федеральный НМЦ ПБ СПИД, г. Москва
НИИ эпидемиологии и микробиологии им. Н. Ф. Гамалеи РАМН
НИИ вирусологии им. Д. И. Ивановского РАМН, г. Москва
Клиническая инфекционная больница №2, г. Москва
В современной клинической медицине цитомегаловирусная инфекция, приобретает все большую актуальность. Помимо значения ЦМВ как этиологического фактора внутриутробной и перинатальной патологии, велика его роль в развитии тяжелых пневмоний у пациентов, перенесших пересадку органа, ожоговую травму, у онкогематологических больных. случаев посттрансфузионные гепатиты обусловлены С цитомегаловирусом связана разнообразная гинекологическая патология. Предполагается роль ЦМВ в развитии первичных и вторичных системных васкулитов, хронических диссеминированных заболеваний легких (в частности, фиброзирующего альвеолита), опухолевых процессов и даже атеросклероза. Данный вирус, возможно, причастен к развитию синдрома синдрома хронической усталости. Мы наблюдали клинически выраженную у взрослых пациентов, перенесших стрессовые ситуации.
Но особую значимость как патология взрослых приобрела после появления и широкого распространения в мире Клинически выраженная генерализованная занимает одно из первых мест в структуре вторичных заболеваний у больных нередко являясь непосредственной причиной их гибели. В тоже время, цитомегаловирусная инфекция остается одним их наименее изученных вторичных заболеваний больных.
Как нозологическая форма не имеет своих однозначных очертаний, отличаясь удивительным полиморфизмом. Клинический диагноз требует обязательного лабораторного подтверждения. В тоже время, используемые в настоящее время практическим здравоохранением серологические, вирусологические, методы выявления активной имеют различную диагностическую ценность при лабораторном подтверждении манифестной формы заболевания. На сегодняшний день отмечается большая противоречивость суждений при оценке различных методов диагностики активной и ее манифестной формы. Мало изучено значение специфических лабораторных маркеров для прогноза развития манифестной пациентов.
Как известно, ЦМВ в организме человека может находиться в латентном состоянии, в стадии активной репликации без развития органных поражений и быть причиной тяжелой клинически выраженной патологии. Как подчеркивал Н. А. Фарбер, далеко не всегда равнозначна цитомегаловирусному заболеванию. Следовательно, проблема лабораторного подтверждения манифестной ЦМВИ заключается не в установлении самого факта присутствия цитомегаловируса в организме пациента и даже не в выявлении косвенных признаков его активности, а в определении той высокой степени вирусной активности, которая обусловливает патологические изменения в органах и, соответственно, подтверждает цитомегаловирусную природу имеющихся у больного клинических проявлений.
В связи с выше изложенным, вопросы лабораторной диагностики сохраняют свою актуальность для практического здравоохранения и на сегодняшний день.
Материалы и методы
В течение 5 лет под нашим наблюдением находились 300 взрослых больных проходивших лечение в КИБ №2 г. Москвы и в поликлиническом отделении МГЦ СПИД.
Лабораторная диагностика активной цитомегаловирусной инфекции включала в себя молекулярно-биологические, вирусологические, серологические и морфологические методы исследования. Общее количество исследований составило 1359.
Качественное и количественное определение ДНК ЦМВ в крови, ликворе, тканях пораженных органов осуществляли с помощью метода полимеразной цепной реакции. Исследования по определению ДНК ЦМВ были выполнены по оригинальной методике (5). Разработанная методика позволила воспроизводимо идентифицировать 10 вирусных геномов при фоновой нагрузке не менее 1 мкг геномной ДНК человека. Для определения титра ДНК ЦМВ готовили четыре разведения исходного лизата, содержащего ДНК из 106 лейкоцитов в 100 мкл. Проводили реакцию амплификации с каждым разведением, включая исходный лизат. Наличие только в исходной пробе соответствовало минимальному титру ДНК ЦМВ (1:1), в исходной пробе и первом разведении низкому (1:10), в двух разведениях среднему (1:100), в трех высокому (1:1000).
Обнаружение цитомегаловируса в моче пациентов проводили путем изоляции ЦМВ на зараженной чувствительной клеточной культуре. Идентификация вируса была основана на характерном цитопатическом эффекте и на определении методом иммунофлюоресценции с использованием специфических поликлональных антител.
Выявление в сыворотке крови антител к ЦМВ класса IgМ (качественный анализ) и класса IgG (количественный анализ) осуществляли методом иммуноферментного анализа с использованием коммерческих диагностических наборов (ЗАО согласно инструкциям, прилагаемым к ним. Серологические исследования проводились с интервалом в 2 4 недели.
Подтверждением цитомегаловирусного поражения органов считали обнаружение в измененных тканях цитомегалоклеток характерных крупных клеток с внутриядерными и цитоплазматическими вирусными включениями. Цитомегаловирусную природу морфологических изменений подтверждали выявлением ДНК ЦМВ в исследуемых тканях.
Результаты и обсуждение
Мы наблюдали манифестную у 47 человек (39.2%) из 120 больных на стадии вторичных проявлений III B (СПИД). Больные находились в возрасте от 15 до 70 лет (37.7%). Мужчин было 39 (83%), женщин 8 (17.0%). Подавляющее большинство (93.6%) пациентов с манифестной имели количество ниже 0.05x109/л (0.018 + 0.002).
Для ЦМВИ был характерен необычайно широкий спектр клинических вариантов. Чаще всего имели место патология органов зрения некротический ретинит (51.1% от всех больных с манифестной ЦМВИ), поражение кишечника в виде колита или энтероколита (38.3%), эзофагит (17.0%), пневмония (29.8%) с быстрым развитием пневмофиброза, некротический энцефалит или энцефаловентрикулит (25.5%), приводившие к выраженным изменениям в психическом статусе больных, полирадикулопатия (21.3%). При постмортальных исследованиях у 56.4% пациентов была обнаружена тяжелая двусторонняя патология надпочечников в виде обширных некрозов коркового и мозгового слоев. Во всех случаях при в патологический процесс вовлекались несколько систем органов. Среди погибших больных с генерализованной цитомегаловирусной инфекцией, помимо описанного выше поражения внутренних органов, были выявлены некротический миелит, панкреатит с развитием фиброза поджелудочной железы, нефрит, миокардит, гепатит, склерозирующий холангит, холецистит, эрозивный цистит сиалоаденит, простатит, некротическое поражение аденогипофиза, селезенки, трахеальных и мезентериальных лимфатических узлов, глазных и блуждающего нервов. Цитомегаловирусное поражение внутренних органов явилось непосредственной причиной смерти у 17.5 % больных СПИДом.
С целью выявления наиболее чувствительных и специфических лабораторных маркеров манифестной у ВИЧ-инфицированных больных были проанализированы результаты комплексного обследования 250 пациентов на наличие специфических антител класса IgM и четырехкратного повышения антител класса IgG в сыворотке крови, цитомегаловируса в моче, различных титров ДНК ЦМВ в лейкоцитах периферической крови. 35 человек из данной группы имели манифестную Цитомегаловирусная этиология поражения органов была подтверждена гистологическими исследованиями.
Согласно полученным данным больные были распределены в одну из четырех возможных групп в зависимости от отрицательного или положительного значения лабораторного признака, а также наличия или отсутствия клинически выраженной Соответственно, по каждому лабораторному параметру было получено определенное число больных:
Специфичность диагностического признака определяли, согласно формуле 100% чувствительность согласно формуле:
Как видно из табл. 1, специфичность и чувствительность таких лабораторных маркеров активности ЦМВ, как увеличение наличие специфических антител класса IgМ в сыворотке крови, обнаружение цитомегаловируса в моче и даже наличие ДНК ЦМВ в лейкоцитах крови без учета ее концентрации в качестве подтверждающих лабораторных признаков манифестной оказались низки. Напротив, специфичность и чувствительность высокого титра ДНК ЦМВ в лейкоцитах периферической крови как маркера клинически выраженной явились наиболее высокими и были равны соответственно 97.1% и 97.7%.
Демонстрацией выше сказанного являются следующие данные. Четырехкратное повышение титров антител класса IgG к ЦМВ и обнаружение специфических антител класса IgM в сыворотке крови имели место у больных с манифестной лишь в 34.3% и 65.7% случаев, соответственно (табл. 2). У трети больных, несмотря на продолжающееся развитие заболевания, IgM перестали определяться. С другой стороны, в группе лиц, не имевших клинической симптоматики, связанной с действием ЦМВ, четырехкратное повышение титров специфических IgG антител и IgM антитела выявляли в сыворотке крови, соответственно, в 21.9% и 16.3% случаев. Помимо этого, среди пациентов, у которых не было выявлено не только заболевания но и активной (в их крови ДНК ЦМВ отсутствовала даже в минимальном титре), высокие титры IgG антител и IgM антитела обнаруживали у 16.1% и 13.2% лиц, соответственно. Данный факт вполне объясним, так как, из литературы известно, что тест на наличие IgM может быть положительным, в частности, присутствия в сыворотке крови больного ревматоидного фактора, при активной репликации других (вирусов у лиц, страдающих коллагенозами (8).
Низкие титры антител класса IgG к ЦМВ и отсутствие специфических антител класса IgМ в сыворотке крови больных СПИДом при наличии у них в крови цитомегаловируса в высокой концентрации можно объяснить (помимо существующих ограничений в чувствительности и специфичности используемых методов) характером иммунного ответа при длительно персистирующих в организме человека вирусных инфекциях и имеющимся нарушением продукции антител у больных на поздних стадиях вследствие существенного подавления у них не только звена иммунитета (3).
В тоже время нами отмечены случаи длительной (более 3 месяцев) персистенции в крови пациентов антител класса IgМ к ЦМВ в сочетании с низкими титрами IgG антител и низкой концентрацией ДНК ЦМВ в лейкоцитах крови. У ряда лиц срок обнаружения антител класса IgМ достигал 9 месяцев. Причины столь длительного определения специфических антител класса IgМ и отсутствие значительного повышения титров IgG после реинфекции или реактивации ЦМВ не вполне ясны. это связано с определенным дефектом в механизме переключения выработки на продукцию ими антител класса IgG. Возможно, играли роль постоянная антигенная стимуляция и дефицит значение которых в качестве стимулятора синтеза отличных от IgМ антител было уставлено (3). Интересен следующий факт: в группе пациентов, в крови которых IgM к ЦМВ определяли длительное время (более 3 месяцев), манифестная развивалась в течение 12 месяцев значительно чаще (в 52.3% случаев), чем у лиц, имевших специфические антитела данного класса кратковременно (35.0%) или не имевших их вообще (10.0%).
При проведении вирусологических исследований у 71.4% наблюдаемых нами пациентов с манифестной цитомегаловирус был выделен из мочи. В тоже время, в группе лиц, не имевших клинические проявления заболевания, ЦМВ в моче был обнаружен в 21.4% случаев (табл. 2). При одновременных исследованиях на наличие ДНК ЦМВ в лейкоцитах периферической крови и цитомегаловируса в моче выявлено совпадение результатов лишь в 65.8% случаев. У 21.6% пациентов ЦМВ был выделен из мочи при отсутствии ДНК ЦМВ в крови даже в минимальном титре, т. е. при отсутствии существенной активности цитомегаловируса. По данным ряда исследований, ЦМВ может выделяться из организма с мочой после имевшей место острой инфекции или ее реактивации в течение 3 5 лет (4). Таким образом, изоляция ЦМВ из мочи лиц не может быть единственным лабораторным критерием как при решении вопроса о наличии у них активной ЦМВ-инфекции, так и при постановке диагноза связанного с ЦМВ заболевания. Кроме того, использование данного метода требует строгого соблюдения временных рамок доставки материала в лабораторию, а сам метод является технически трудоемким, длительным в исполнении и дорогим.
В практике лабораторной диагностики активной все большее значение приобретает метод, основанный на полимеразной цепной реакции (1, 2, 7). Опыт нашей работы показал, что положительный результат при качественном варианте ПЦР (определение ДНК ЦМВ в лейкоцитах периферической крови без учета ее титра) свидетельствует об активности инфекционного процесса, но не позволяет судить о его степени, что необходимо для подтверждения манифестной Все пациенты с клинически выраженной цитомегаловирусной патологией имели ДНК ЦМВ в крови. При этом у 39.5% обследованных лиц, не имеющих заболевания также обнаружена ДНК ЦМВ (табл. 2). Ряд авторов обращают внимание на то, что при диагностике инфекций, вызываемых вирусами, длительно персистирующими в организме человека, диагностическая и прогностическая ценность положительных результатов ПЦР при выявлении вирусного генома в крови без учета его концентрации довольно низка (7, 11). Этот недостаток качественного варианта ПЦР проистекает из ее очень высокой чувствительности и состоит в способности выявлять возбудитель, находящийся в крайне незначительном количестве в биологических жидкостях.
Иное, высокое клиническое значение имеют данные, полученные при использовании количественного варианта ПЦР. В нашем исследовании 97.1% больных с манифестной имели высокий титр ДНК ЦМВ равный 1:1000 и более в 105 лейкоцитах периферической крови (табл. 2). Лишь у одного пациента титр ДНК ЦМВ был равен 1:100. Случаев клинически выраженной ЦМВИ при титре ДНК ЦМВ в лейкоцитах крови менее 1:100 выявлено не было. Лишь у 2.3% больных при отсутствии цитомегаловирусной органной патологии зафиксирован высокий титр ДНК ЦМВ в крови. Полученные данные убедительно свидетельствуют, что выявление ДНК ЦМВ в титре 1:1000 и более в лейкоцитах периферической крови больного, имеющего те или иные клинические симптомы, доказывает наличие у него манифестной Проведенные исследования в медицинских центрах США также демонстрируют возможность выделения определенного уровня цитомегаловирусной нагрузки в клетках крови или плазме, указывающего на имеющее место заболевание ЦМВ этиологии (7, 11). Диагностическое значение имеет факт обнаружения ДНК ЦМВ в спинномозговой жидкости при поражении цитомегаловирусом центральной нервной системы. Так, 80.0% обследованных больных с ЦМВ-энцефалитом имели ДНК ЦМВ в ликворе, в отличие от 3.8% пациентов с поражением ЦНС иной этиологии. Большую диагностическую ценность имеет наличие ДНК ЦМВ в биопсийных и аутопсийных материалах из пораженных органов. Мы считаем, и это находит подтверждение в ряде зарубежных работ (6, 9), что присутствие ДНК ЦМВ в патологически измененной ткани имеет такую же высокую диагностическую значимость, как и обнаружение в ней специфических ЦМК.
Помимо выше изложенного, факт обнаружения ДНК ЦМВ в крови больных является и неблагоприятным прогностическим признаком, свидетельствующим о вероятном развитии у них уже в течение последующего года манифестной В течение 12 месяцев наблюдения среди пациентов, изначально не имевших ДНК ЦМВ в крови, клинически выраженная ЦМВИ развилась лишь в 0.8% случаев, у больных с первоначально минимальным титром ДНК ЦМВ в 18.2%, низким в 31.3%, средним в 50.0% случаев. Во всех случаях появлению клинических симптомов предшествовало увеличение титра ДНК ЦМВ до высокого уровня. Среди пациентов, у которых первоначально ДНК ЦМВ была в высоком титре, заболевание, связанное с ЦМВ, диагностировано у 92.9% лиц. Эти данные свидетельствуют, что в течение года с момента первого обследования частота развития манифестной в группе больных, где ДНК ЦМВ в крови первоначально присутствовала хотя бы минимальном титре, достоверно выше по сравнению с больными, у которых ПЦР была отрицательной. Клинически выраженная ЦМВИ достоверно чаще развивалась у лиц с высокой вирусной нагрузкой, нежели у пациентов со средним, низким или минимальным титром ДНК ЦМВ. Более того, у больных, имеющих при первом обследовании титр ДНК ЦМВ 1:1000, манифестная ЦМВИ диагностирована не позднее 90 дня (53.0 + 3.8) от момента выявления высокого титра ДНК ЦМВ. Сходные результаты были получены и в работе S. Spector (1997), который показал, что наличие у больного ДНК ЦМВ в плазме повышает риск развития манифестной в 3.5 раза (11).
Безусловным достоинством использования количественного варианта ПЦР при выявлении ДНК ЦМВ является возможность оценки эффективности проводимого лечения. Этиотропное лечение препаратом цимевен (ганцикловир) было проведено нами у 29 пациентов с манифестной При завершении лечебного курса (5 мг/кг 2 раза в сутки в/в в течение 21 дня) параллельно с купированием клинических проявлений у 93.1% больных имело место снижение концентрации ДНК ЦМВ в лейкоцитах периферической крови в 1000 раз и более, в половины случаев до неопределяемого уровня. У двух больных (6.9%), несмотря на проводившееся лечение, существенного снижения концентрации ДНК цитомегаловируса не произошло, в дальнейшем отмечено прогрессирование заболевания с генерализацией патологического процесса.
Заключение
Определение в крови больного антител класса IgМ и/или существенного увеличения титров антител класса IgG к ЦМВ недостаточно ни для установления факта активной репликации цитомегаловируса, ни для подтверждения диагноза манифестной лиц. Изоляция ЦМВ из мочи на клеточной культуре обладает большей специфичностью и чувствительностью по сравнению с серологическими маркерами, однако также приносит малую диагностическую пользу. Положительный результат при определении ДНК ЦМВ в клетках крови без учета концентрации вируса свидетельствует об активной репликации ЦМВ, но не позволяет судить о ее степени, что необходимо для подтверждения клинически выраженной ЦМВИ. Достоверным критерием высокой активности цитомегаловируса, доказывающим его этиологическую роль в развитии тех или иных клинических синдромов, служит высокий титр ДНК ЦМВ в лейкоцитах периферической крови, обнаруживаемый почти у 100% лиц с клинически выраженной и отсутствующий у больных, имеющих другие оппортунистические заболевания. Наличие высокого титра ДНК ЦМВ в лейкоцитах крови является неблагоприятным прогностическим признаком развития манифестной ЦМВИ и его выявление требует безотлагательного начала этиотропной терапии.
Лечение цитомегаловирусной инфекции нервной системы. Вирус простого герпеса и нервная система.
В настоящее время используются два вирусостатических препарата для подавления активной ЦМВИ при СПИДе. Оба препарата относятся к вирусостатинам. Некоторые авторы предлагают комбинированную терапию больных с ЦМВ-поражением ЦНС.
Фоскарнет обладает лучшей способностью к проникновению в ЦСЖ, чем ганцикловир. Кроме действия на ЦМВ, он обладает умеренной антиретровирусной активностью. Начальная доза препарата составляет 90 мг/кг внутривенно и назначается пациентам с нормальной функцией почек в течение 14—21 дня. Затем рекомендован переход на поддерживающую терапию со снижением дозы до 90—120 мг/сут. Введение препарата облегчается при установке постоянного подключичного катетера. Больным, страдающим почечной недостаточностью, назначаются более низкие дозы. Кроме токсического поражения почек, выделяют следующие побочные эффекты фоскарнета: дисфункция желудочно-кишечного тракта, нарушения электролитного баланса, головные боли, парестезии, припадки и токсическая энцефалопатия. Иногда бывает трудно отличить побочные эффекты фоскарнета от проявлений собственно ЦМВ-инфекции.
Ганцикловир также эффективен для лечения ЦМВ-поражения нервной системы у больных СПИДом. Лучше всего лечению данным препаратом поддаются ЦМВ-ПРМ и мультифокальная нейропатия. Начальная доза препарата составляет 5 мг/кг внутривенно в течение 14—21 дня. Затем рекомендован переход на поддерживающую дозу 5 мг/кг/сут. Подавление кроветворной функции, в частности нейтропения, нередко отмечается при лечении ганцикловиром, особенно если одновременно больной получает антиретровирусные средства. Их дозу необходимо снизить. К другим побочным эффектам ганцикловира относятся токсическое поражение печени, желудочно-кишечные расстройства, головные боли, припадки, сонливость, парестезии, токсическая энцефалопатия и токсическое поражение почек. Так же, как и при лечении фоскарнетом, зачастую бывает трудно отличить побочные эффекты препарата от проявлений ЦМВ-инфекции. с. Вирусная резистентность может развиться при длительном лечении ганциковиром или фоскарнетом. При начальной ударной терапии ЦМВ-ретинита или энтерита могут появиться неврологические симптомы. Для их лечения рекомендуется назначение альтернативного средства.
Когда и ганцикловир, и фоскарнет утрачивают эффективность, можно попробовать их комбинацию.
Ожидаемый результат лечения цитомегаловирусной инфекции нервной системы. Проспективных исследований по определению эффективности лечения ЦМВ-поражениий нервной системы при СПИДе не проводилось. Известны только единичные описания улучшения на фоне лечения ЦМВ-ПРМ и мультифокальной нейропатии. Очень мало данных о реакции на лечение ЦМВЭ. Больные, получившие ударную терапию, должны быть переведены на поддерживающий режим, хотя до сих пор неясно, какие дозы препаратов целесообразны. Исследование ЦСЖ дает наиболее надежные критерии активности процесса, поэтому его следует проводить сразу после окончания ударной терапии, а также при прогрессировании неврологических симптомов на фоне поддерживающей терапии. Повторное воспаление и, возможно, неоднократное выявление вирусной ДНК в ЦСЖ методом ПЦР свидетельствует об активной репликации вируса и указывают на резистентность к выбранному режиму лечения.
Вирус простого герпеса и нервная система.
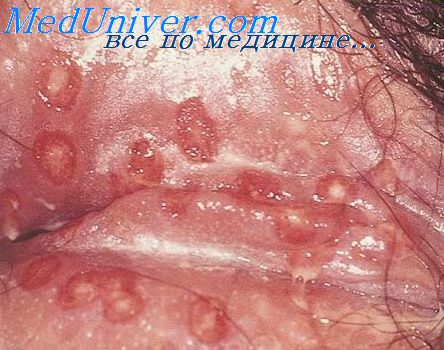
1. Течение инфекции вируса простого герпеса. ВПГ распространен повсеместно общей популяции, и у ВИЧ-инфицированных часто наблюдается инфекция, вызванная ВПГ-2 ректально-генитального типа. Многие случаи ВПГ-2-асептического менингита имеют самоограничивающийся характер, но менингорадикулит, энцефалит или миелит могут давать тяжелые проявления, требующие лечения. У ВИЧ-инфицированных описан также энцефалит, вызванный ВПГ-1, с подострым течением и атипичной клинической картиной, обусловленной глубоким иммунодефицитом.
2. Клиническая картина инфекции вируса простого герпеса. ВПГ-1 вызывает фокальный энцефалит с преимущественным поражением глубоких отделов лобных и височных долей. Клиническими признаками заболевания являются припадки, головные боли, изменения личности и нарушения речи. В течение нескольких дней может развиться спутанность сознания, ступор и кома. У некоторых больных СПИДом не наблюдается такого выраженного прогрессирования. ВПГ-2 вызывает асептический менингит с лихорадкой и головными болями; менингорадикулит с частым вовлечением крестцовых корешков, что служит причиной задержки мочи; менингоэнцефалит. У больных с менингомиелитом отмечается прогрессирующая слабость, спастичность, нарушения чувствительности и атаксия, преимущественно в нижних конечностях, а также нарушение тазовых функций. У больных с ВПГ-2-менингоэнцефалитом наблюдаются спутанность сознания, припадки, головные боли и двигательные нарушения различной степени тяжести. Признаки ВПГ-2-поражения нервной системы могут появиться непосредственно после высыпаний в анально-генитальной области или независимо от них.
3. Диагностика инфекции вируса простого герпеса. Диагноз ВПГ-энцефалита можно предположить при обнаружении ограниченных очагов в нижних отделах лобных или височных долей по данным МРТ-исследования с контрастом. На ЭЭГ регистрируются типичные периодические спайковые разряды. Характерных признаков ВПГ-1 энцефалита другой локализации не существует. В ЦСЖ обычно обнаруживается смешанный плеоцитоз, иногда — эритроциты, чуть сниженный или нормальный уровень глюкозы и повышенное содержание белка. Исследования в культуре редко выявляет наличие вируса. Разработан ПЦР-метод, позволяющий фиксировать вирусную ДНК в ЦСЖ.
4. Лечение инфекции вируса простого герпеса
Ацикловир — вирусостатический препарат, эффективный при герпетических инфекциях. Препарат активизирует тимидинкиназу, которая замедляет репликацию вируса. Ацикловир в дозе 10 мг/кг внутривенно назначают сразу же при подозрении на ВПГ-поражение ЦНС, не дожидаясь результатов диагностических исследований. В подтвержденных случаях лечение рекомендовано продолжать в течение 10—14 дней. После этого иногда назначается поддерживающая терапия повторной аногенитальной инфекции в дозе 200 мг внутрь 5 раз в сутки. К сожалению, появились резистентные штаммы вируса. Таким больным показано лечение фоскарнетом в дозе 60 мг/кг 2 раза в сутки в течение 14-21 дня.
К побочным эффектам ацикловира относятся токсическое поражение почек, печени, желудочно-кишечные расстройства и раздражение в области введения препарата. У больных, страдающих почечной недостаточностью, доза ацикловира должна быть снижена.
Если при лечении у пациента появились головные боли, головокружение и другие серьезные признаки токсического воздействия препарата, включая токсический делирий, спутанность сознания, припадки, необходимо определить уровень препарата в крови и при его высоких показателях откорректировать дозу. Описаны случаи подавления костномозгового кроветворения и артериальная гипотензия при лечении ацикловиром.
5. Ожидаемый результат лечения вируса простого герпеса. Клинические испытания, оценивающие течение ВПГ-энцефалита и других герпетических поражений нервной системы при СПИДе, немногочисленны. У многих пациентов лечение ацикловиром эффективно. У некоторых больных эффект отсутствует, что связано либо с вирусной резистентностью, либо с нарушением функции иммунной системы. Серийные исследования ЦСЖ считаются наиболее надежным методом подтверждения резистентности и должны проводиться после окончания антивирусной терапии, а также в случае прогрессирования неврологических симптомов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Приобретенная цитомегаловирусная инфекция ЦНС на МРТ
а) Терминология:
• Приобретенная цитомегаловирусная инфекция ЦНС: менингит, энцефалит, вентрикулит, поперечный миелит, радикуломиелит, хориоретинит
• Иммунокомпрометированные пациенты (СПИД, трансплантация органов) с повышенным риском → реактивация ранее латентной инфекции
б) Визуализация приобретенной цитомегаловирусной инфекции ЦНС:
• Лучший диагностический критерий: вентрикулит с уровнем жидкость-детрит и контрастированием эпендимы у иммунокомпрометированного пациента
• Энцефалит: зона гиперинтенсивного на Т2-ВИ сигнала с нечеткими контурами и вариабельным контрастным усилением
• Может имитировать ВИЧ-энцефалит с фрагментарными неспецифическими гиперинтенсивными на Т2-ВИ поражениями
• Введение контрастного препарата при диагностической визуализации следует проводить у всех иммунокомпрометированных пациентов
(а)МРТ, FLAIR, аксиальный срез: определяются легкая вентрикуломегалия и перивентрику-лярные очаги гиперинтенсивного сигнала, что обусловлено вентрикуло-энцефалитом.
(б) МРТ, постконтрастное Т1-ВИ, аксиальный срез: у этого же пациента определяется контрастирование эпендимы и перивентри-кулярных очагов. У данного пациента был иммунодефицит, вентрикулит в сочетании с энцефалитом. ЦМВ-энцефалит обычно представляет собой вентрикуло-энцефалит с вовлечением перивентрикулярного белого вещества. Однако ЦМВ также может вызывать появление геморрагических или некротических поражений. (а) МРТ, ДВИ, аксиальный срез: у 35- летнего ВИЧ-положительного пациента с очень низким числом CD4(+) клеток по ходу стенок боковых желудочков определяется тонкий гиперинтенсивный ободок. Кроме того, наблюдается легкое расширение желудочков и легкая атрофия коры.
(б) МРТ, постконтрастное Т1-ВИ, корональный срез: у того же пациента определяется слабовыраженное контрастирование эпендимы лобных рогов боковых желудочков. Данные изменения характерны для ЦМВ-вентрикулита.
в) Дифференциальный диагноз:
• ВИЧ-энцефалит
• ПМЛ
• Токсоплазмоз
• ОДЭМ
г) Клиническая картина приобретенной цитомегаловирусной инфекции ЦНС:
• Первичная цитомегаловирусная инфекция (ЦМВИ) обычно протекает бессимптомно
• Заражение может произойти вследствие реактивации латентной вирусной инфекции или инфекции, недавно приобретенной в результате трансплантации органа или костного мозга от серопозитивного донора:
о ЦМВ распространяется в ЦНС на поздних стадиях ВИЧ-инфекции, при низком количестве CD4(+) клеток
о Клинически может имитировать ВИЧ-энцефалит
• Проявления заболевания варьируют по степени тяжести в зависимости от степени иммуносупрессии пациента
• ВААРТ: выраженное ↓ заболеваемости ЦМВИ при СПИД; ↑ иммунокомпетентности против ЦМВ
Цитомегалия – это инфекционное заболевание вирусного генеза, передающееся половым, трансплацентарным, бытовым, гемотрансфузионным путем. Симптоматически протекает в форме упорной простуды. Отмечается слабость, недомогание, головные и суставные боли, насморк, увеличение и воспаление слюнных желез, обильное слюноотделение. Часто протекает бессимптомно. Опасна цитомегалия беременных: она может вызывать самопроизвольный выкидыш, врожденные пороки развития, внутриутробную гибель плода, врожденную цитомегалию. Диагностика осуществляется лабораторными методами (ИФА, ПЦР). Лечение включает противовирусную и симптоматическую терапию.
МКБ-10
Общие сведения
Другие названия цитомегалии, встречающиеся в медицинских источниках, - цитомегаловирусная инфекция (ЦМВ), инклюзионная цитомегалия, вирусная болезнь слюнных желез, болезнь с включениями. Цитомегалия является широко распространенной инфекцией, и многие люди, являясь носителями цитомегаловируса, даже не подозревают об этом. Наличие антител к цитомегаловирусу выявляется у 10—15% населения в подростковом возрасте и у 50% взрослых людей. По некоторым источникам, носительство цитомегаловируса определяется у 80% женщин детородного периода. В первую очередь это относится к бессимптомному и малосимптомному течению цитомегаловирусной инфекции.

Причины
- воздушно-капельным: при чихании, кашле, разговоре, поцелуях и т.д.;
- половым путем: при сексуальных контактах через сперму, влагалищную и шеечную слизь;
- гемотрансфузионным: при переливании крови, лейкоцитарной массы, иногда - при пересадке органов и тканей;
- трансплацентарным: во время беременности от матери плоду.
Нередко цитомегаловирус находится в организме многие годы и может ни разу не проявить себя и не нанести вреда человеку. Проявление скрытой инфекции происходит, как правило, при ослаблении иммунитета. Угрожающую по своим последствиям опасность цитомегаловирус представляет у лиц со сниженным иммунитетом (ВИЧ-инфицированных, перенесших трансплантацию костного мозга или внутренних органов, принимающих иммунодепрессанты), при врожденной форме цитомегалии, у беременных.
Патогенез
Попадая в кровь, цитомегаловирус вызывает выраженную иммунную реакцию, проявляющуюся в выработке защитных белковых антител – иммуноглобулинов М и G (IgM и IgG) и противовирусной клеточной реакцией - образованием лимфоцитов CD 4 и CD 8. Угнетение клеточного иммунитета при ВИЧ-инфекции приводит к активному развитию цитомегаловируса и вызываемой им инфекции.
Даже при бессимптомном течении инфекции носитель цитомегаловируса является потенциально заразным для неинфицированных лиц. Исключение составляет внутриутробный путь передачи цитомегаловируса от беременной женщины плоду, который происходит в основном при активном течении процесса, и лишь в 5% случаев вызывает врожденную цитомегалию, в остальных же носит бессимптомный характер.
Симптомы цитомегалии
Врожденная цитомегалия
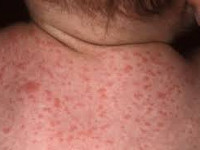
В 95% случаев внутриутробное инфицирование плода цитомегаловирусом не вызывает развития заболевания, а протекает бессимптомно. Врожденная цитомегаловирусная инфекция развивается у новорожденных, матери которых перенесли первичную цитомегалию. Врожденная цитомегалия может проявляться у новорожденных в различных формах:
- петехиальная сыпь – мелкие кожные кровоизлияния - встречается у 60-80% новорожденных;
- недоношенность и задержка внутриутробного развития плода - встречается у 30% новорожденных;
- желтуха;
- хориоретинит – острый воспалительный процесс в сетчатке глаза, часто вызывающий снижение и полную потерю зрения.
Летальность при внутриутробном инфицировании цитомегаловирусом достигает 20-30%. Из выживших детей большая часть имеет отставание в умственном развитии или инвалидность по слуху и зрению.
Приобретенная цитомегалия у новорожденных
При инфицировании цитомегаловирусом в процессе родов (при прохождении плода по родовым путям) или в послеродовом периоде (при бытовом контакте с инфицированной матерью или грудном вскармливании) в большинстве случаев развивается бессимптомное течение цитомегаловирусной инфекции. Однако у недоношенных младенцев цитомегаловирус может вызывать затяжную пневмонию, к которой часто присоединяется сопутствующая бактериальная инфекция. Часто при поражении цитомегаловирусом у детей отмечается замедление в физическом развитии, увеличение лимфоузлов, гепатит, сыпь.
Мононуклеозоподобный синдром
У лиц, вышедших из периода новорожденности и имеющих нормальный иммунитет, цитомегаловирус может вызывать развитие мононуклеозоподобного синдрома. Течение мононуклеазоподобного синдрома по клинике не отличается от инфекционного мононуклеоза, вызываемого другой разновидностью герпесвируса – вирусом Эбштейна-Барр. Течение мононуклеозоподобного синдрома напоминает упорную простудную инфекцию. При этом отмечается:
- длительная (до 1 месяца и более) лихорадка с высокой температурой тела и ознобами;
- ломота в суставах и мышцах, головная боль;
- выраженные слабость, недомогание, утомляемость;
- боли в горле;
- увеличение лимфоузлов и слюнных желез;
- кожные высыпания, напоминающие сыпь при краснухе (обычно встречается при лечении ампициллином).
В отдельных случаях мононуклеозоподобный синдром сопровождается развитием гепатита – желтухой и повышением в крови печеночных ферментов. Еще реже (до 6% случаев) осложнением мононуклеозоподобного синдрома служит пневмония. Однако у лиц с нормальной иммунной реактивностью она протекает без клинических проявлений, выявляясь лишь при проведении рентгенографии легких.
Длительность течения мононуклеозоподобного синдрома составляет от 9 до 60 дней. Затем обычно наступает полное выздоровление, хотя на протяжении нескольких месяцев могут сохраняться остаточные явления в виде недомогания, слабости, увеличенных лимфоузлов. В редких случаях активизация цитомегаловируса вызывает рецидивы инфекции с лихорадкой, потливостью, приливами и недомоганием.
Цитомегаловирусная инфекция у лиц с ослабленным иммунитетом
Ослабление иммунитета наблюдается у лиц, страдающих синдромом врожденного и приобретенного (СПИД) иммунодефицита, а также у пациентов, перенесших пересадку внутренних органов и тканей: сердца, легкого, почки, печени, костного мозга. После пересадки органов пациенты вынуждены постоянно принимать иммунодепрессанты, ведущие к выраженному подавлению иммунных реакций, что вызывает активность цитомегаловируса в организме.
У пациентов, перенесших трансплантацию органов, цитомегаловирус вызывает поражение донорских тканей и органов (гепатит – при пересадке печени, пневмонию при пересадке легкого и т. д.). После трансплантации костного мозга у 15-20% пациентов цитомегаловирус может привести к развитию пневмонии с высокой летальностью (84-88%). Наибольшую опасность представляет ситуация, когда инфицированный цитомегаловирусом донорский материал пересажен неинфицированному реципиенту.
Цитомегаловирус поражает практически всех ВИЧ-инфицированных. В начале заболевания отмечаются недомогание, суставные и мышечные боли, лихорадка, ночная потливость. В дальнейшем к этим признакам могут присоединяться поражения цитомегаловирусом легких (пневмония), печени (гепатит), мозга (энцефалит), сетчатки глаза (ретинит), язвенные поражения и желудочно-кишечные кровотечения.
У мужчин цитомегаловирусом могут поражаться яички, простата, у женщин – шейка матки, внутренний слой матки, влагалище, яичники. Осложнениями цитомегаловирусной инфекции у ВИЧ-инфицированных могут стать внутренние кровотечения из пораженных органов, потеря зрения. Множественное поражение органов цитомегаловирусом может привести к их дисфункции и гибели пациента.
Диагностика
С целью диагностики цитомегаловирусной инфекции проводится лабораторное обследование. Постановка диагноза цитомегаловирусной инфекции основана на выделении цитомегаловируса в клиническом материале или при четырехкратном повышении титра антител.
- ИФА-диагностика. Включает определение в крови специфических антител к цитомегаловирусу - иммуноглобулинов М и G. Наличие иммуноглобулинов М может свидетельствовать о первичном заражении цитомегаловирусом либо о реактивации хронической ЦМВИ. Определение высоких титров IgМ у беременных может угрожать инфицированию плода. Повышение IgМ выявляется в крови спустя 4-7 недель после заражения цитомегаловирусом и наблюдается на протяжении 16-20 недель. Повышение иммуноглобулинов G развивается в период затухания активности цитомегаловирусной инфекции. Их наличие в крови говорит о присутствии цитомегаловируса в организме, но не отражает активности инфекционного процесса.
- ПЦР-диагностика. Для определения ДНК цитомегаловируса в клетках крови и слизистых (в материалах соскобов из уретры и цервикального канала, в мокроте, слюне и т. д.) используется метод ПЦР-диагностики (полимеразной цепной реакции). Особенно информативно проведение количественной ПЦР, дающей представление об активности цитомегаловируса и вызываемого им инфекционного процесса.
В зависимости от того, какой орган поражен цитомегаловирусной инфекцией, пациент нуждается в консультации гинеколога, андролога, гастроэнтеролога или других специалистов. Дополнительно по показаниям проводится УЗИ органов брюшной полости, кольпоскопия, гастроскопия, МРТ головного мозга и другие обследования.
Лечение цитомегаловирусной инфекции
Неосложненные формы мононуклеазоподобного синдрома не требует специфической терапии. Обычно проводятся мероприятия, идентичные лечению обычного простудного заболевания. Для снятия симптомов интоксикации, вызываемой цитомегаловирусом, рекомендуется пить достаточное количество жидкости.
Лечение цитомегаловирусной инфекции у лиц, входящих в группу риска, проводится противовирусным препаратом ганцикловиром. В случаях тяжелого течения цитомегалии ганцикловир вводится внутривенно, т. к. таблетированные формы препарата обладают лишь профилактическим эффектом в отношении цитомегаловируса. Поскольку ганцикловир обладает выраженными побочными эффектами (вызывает угнетение кроветворения - анемию, нейтропению, тромбоцитопению, кожные реакции, желудочно-кишечные расстройства, повышение температуры и ознобы и др.), его применение ограничено у беременных, детей и у людей, страдающих почечной недостаточностью (только по жизненным показаниям), он не используется у пациентов без нарушения иммунитета.
Для лечения цитомегаловируса у ВИЧ-инфицированных наиболее эффективен препарат фоскарнет, также обладающий рядом побочных эффектов. Фоскарнет может вызывать нарушение электролитного обмена (снижение в плазме крови магния и калия), изъязвление половых органов, нарушение мочеиспускания, тошноту, поражение почек. Данные побочные реакции требуют осторожного применения и своевременной корректировки дозы препарата.
Прогноз
Особую опасность цитомегаловирус представляет при беременности, так как может провоцировать выкидыш, мертворождение или вызывать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с герпесом, токсоплазмозом и краснухой, относится к числу тех инфекций, обследоваться на которые женщины должны профилактически, еще на этапе планирования беременности.
Профилактика
Особенно остро вопрос профилактики цитомегаловирусной инфекции стоит у лиц, входящих в группу риска. Наиболее подвержены инфицированию цитомегаловирусом и развитию заболевания ВИЧ-инфицированные (особенно больные СПИДом), пациенты после трансплантации органов и лица с иммунодефицитом иного генеза.
Неспецифические методы профилактики (например, соблюдение личной гигиены) неэффективны в отношении цитомегаловируса, так как заражение им возможно даже воздушно-капельным путем. Специфическая профилактика цитомегаловирусной инфекции проводится ганцикловиром, ацикловиром, фоскарнетом среди пациентов, входящих в группы риска. Также для исключения возможности инфицирования цитомегаловирусом реципиентов при пересадке органов и тканей необходим тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Читайте также:

